ANALISIS SENYAWA KARSINOGENIK N-NITROSODIPROPILAMIN (NDPA) PADA DAGING OLAHAN DENGAN HEADSPACE-SINGLE
DROP MICROEXTRACTION-GAS CHROMATOGRAPHY-FLAME
IONIZATION DETECTOR (HS-SDME-GC-FID)
SKRIPSI
TEGUH HARI SUCIPTO
DEPARTEMEN KIMIA
FAKULTAS SAINS DAN TEKNOLOGI UNIVERSITAS AIRLANGGA
ANALISIS SENYAWA KARSINOGENIK N-NITROSODIPROPILAMIN (NDPA) PADA DAGING OLAHAN DENGAN HEADSPACE-SINGLE
DROP MICROEXTRACTION-GAS CHROMATOGRAPHY-FLAME
IONIZATION DETECTOR (HS-SDME-GC-FID)
SKRIPSI
Sebagai Salah Satu Syarat Untuk Memperoleh Gelar Sarjana Sains Bidang Kimia Pada Fakultas Sains dan Teknologi
Universitas Airlangga
Disetujui Oleh :
Dosen Pembimbing I, Dosen Pembimbing II,
LEMBAR PENGESAHAN NASKAH SKRIPSI
Judul : Analisis Senyawa Karsinogenik N-Nitrosodipropilamin (NDPA) Pada Daging Olahan Dengan Headspace-Single Drop Microextraction-Gas Chromatography-Flame Ionization Detector(HS-SDME-GC-FID)
Penyusun : Teguh Hari Sucipto
NIM : 080810645
Pembimbing I : Dr. rer. nat. Ganden Supriyanto, M.Sc Pembimbing II : Yanuardi Raharjo, S.Si., M.Sc
Tanggal Ujian : 18 Juli 2012
Disetujui oleh :
Pembimbing I, Pembimbing II,
Dr. rer. nat. Ganden Supriyanto, M.Sc Yanuardi Raharjo, S.Si., M.Sc NIP. 19681228 199303 1 001 NIK. 139090961
Mengetahui, Ketua Departemen Kimia Fakultas Sains dan Teknologi
Universitas Airlangga
PEDOMAN PENGGUNAAN SKRIPSI
Skripsi ini tidak dipublikasikan, namun tersedia di perpustakaan dalam lingkungan Universitas Airlangga, diperkenankan untuk dipakai sebagai referensi kepustakaan, tetapi pemgutipan harus seizin penyusun dan harus menyebutkan sumbernya sesuai kebiasaan ilmiah.
KATA PENGANTAR
Puji syukur ke hadirat Allah SWT yang telah melimpahkan rahmat dan hidayah-Nya segala petunjuk yang telah diberikan, sehingga penyusun dapat menyelesaikan penulisan skripsi yang berjudul “Analisis Senyawa Karsinogenik N-Nitrosodipropilamin (NDPA) Pada Daging Olahan Dengan Headspace-Single Drop Microextraction-Gas Chromatography-Flame Ionization Detector
(HS-SDME-GC-FID)” dengan lancar dan tepat pada waktunya. Penulis menyampaikan ucapan terima kasih kepada:
1. Bapak Dr. rer. nat. Ganden Supriyanto, M.Sc dan Bapak Yanuardi Raharjo, S.Si., M.Sc selaku dosen pembimbing I dan II yang telah memberikan bimbingan dan arahan kepada penulis hingga selesainya skripsi ini.
2. Ibu Dr. Pratiwi Pujiastuti, M.Si dan Bapak Drs. Handoko Darmokoesoemo, DEA selaku dosen penguji I dan II yang telah memberikan saran dan arahan kepada penulis hingga selesainya skripsi ini.
3. Bapak Drs. Joesoef Syah, MS selaku dosen dosen wali yang telah memberikan pengarahan dan nasehat kepada penulis.
4. Dr. Alfinda Novi Kristanti, DEA selaku Ketua Departemen Kimia yang telah memberikan fasilitas serta arahan selama penyusun belajar di Departemen Kimia.
5. Seluruh Staf Pengajar Program Studi S1 Kimia yang telah memberikan ilmu yang bermanfaat kepada penyusun.
6. Kedua Orang Tua, H. Slamet dan Hj. Munjiah yang telah memberikan motivasi dan nasehat kepada penulis.
7. Zarah Nur Intizzar, Kartika Laksmi Prasetyowati, dan Any Shofiyah yang selalu membantu dan memberi semangat dalam penyelesaian skripsi ini. 8. Teman-teman seperjuangan S1 Kimia angkatan 2008 yang tidak dapat
disebutkan satu persatu yang telah memberikan semangat, dukungan, dan bantuan selama penyusunan naskah skripsi.
10. Semua pihak yang telah membantu dalam penulisan naskah skripsi ini. Penulis menyadari bahwa masih terdapat banyak kekurangan dalam penyusunan skripsi ini, oleh karena itu penulis sangat mengharapkan kritik dan saran yang bersifat membangun untuk kesempurnaan penulisan skripsi ini agar bermanfaat bagi semua pihak.
Surabaya, 18 Juli 2012 Penyusun,
Sucipto, T.H., 2012, Analisis Senyawa Karsinogenik N-Nitrosodipropilamin (NDPA) Pada Daging Olahan Dengan Headspace-Single Drop Microextraction-Gas Chromatography-Flame Ionization Detector (HS-SDME-GC-FID). Skripsi Ini Dibawah Bimbingan Dr. rer. nat. Ganden Supriyanto, M.Sc dan Yanuardi Raharjo, S.Si., M.Sc. Departemen Kimia, Fakultas Sains dan Teknologi, Universitas Airlangga, Surabaya.
ABSTRAK
Analisis senyawa karsinogenik N-nitrosodipropilamin (NDPA) dalam daging olahan yaitu hamburger dan kebab telah dilakukan dengan HS-SDME-GC-FID. Hasil yang diperoleh penentuan pH optimum adalah 4, kecepatan pengadukan optimum adalah skala 6, dan suhu ekstraksi optimum adalah 30 °C. Pada penelitian ini diperoleh limit deteksi sebesar 78 ppb, persenrecoverysebesar 101,18%, presisi antara 0,089% sampai dengan 0,566%, dan true enrichment factorsebesar 3372,52 kali. Dari hasil penelitian disimpulkan teknik HS-SDME-GC-FID dapat digunakan untuk menganalisis senyawa karsinogenik N-nitrosodipropilamin (NDPA) yang terdapat pada daging olahan (hamburger dan kebab) dengan konsentrasi setiap sampel sebagai berikut, hamburger I sebesar 0,27 ppm, hamburger II sebesar 0,73 ppm, hamburger III sebesar 1,39 ppm, dan kebab I sebesar 3,13 ppm.
Sucipto, T.H., 2012, Analysis of N-nitrosodiprophylamines carcinogenic compound to meat-processing using Headspace-Single Drop Microextraction-Gas Chromatography-Flame Ionization Detector (HS-SDME-GC-FID). This script is under advisement of Dr. rer. nat. Ganden Supriyanto, M.Sc and Yanuardi Raharjo, S.Si., M.Sc. Chemistry Department, Science and Technology Faculty, Airlangga State University.
ABSTRACT
Analysis of N-nitrosodipropilamin carcinogenic compound in processed meat especially hamburger and kebab had occured by HS-SDME-GC-FID technique. The results were obtained determining the optimum pH was 4, the optimum stirring speed was 6 scale, and the temperature of extraction was 30 ºC. It was obtained in this study that the detection limit of 78 ppb, the percent recovery of 101,18%, precision between 0,089% to 0,566%, and the true enrichment factor was 3372,66 times. From the results of the study was concluded that HS-SDME-GC-FID technique can be used to analyze the carcinogenic compound N-nitrosodiprophylamines (NDPA) found in meat-processing (hamburger and kebab) by the concentration of each samples as follows, hamburger I of 0,27 ppm, hamburger II of 0,73 ppm, hamburger III of 1,39 ppm, and kebab I of 3,13 ppm.
DAFTAR ISI
1.1 Latar Belakang Masalah ... 1
1.2 Rumusan Masalah ... 6
1.3 Tujuan Penelitian... 6
1.4 Manfaat Penelitian... 7
BAB II TINJAUAN PUSTAKA... 8
2.1 Produk Daging Olahan... 8
2.1.1 Hamburger... 8
2.1.2 Kebab ... 8
2.2 Karsinogenik………... 9
2.2 N-Nitrosamin... ... 10
2.3 Headspace-Single Drop Microextraction... .... 12
2.4 Gas Chromatography (GC)... 13
BAB III METODE PENELITIAN... 15
3.1 Tempat dan Waktu Penelitian ... 15
3.2. Bahan Penelitian... 15
3.3 Alat-alat Penelitian ... 15
3.4 Prosedur Penelitian ... 16
3.4.1 Diagram alir penelitian... 16
3.4.2 Headspace-single drop microextraction(HS-SDME)... 17
3.4.3 Pembuatan larutan... 17
3.4.3.1 Pembuatan larutan induk NDPA 50 ppm ... 17
3.4.3.2 Pembuatan larutan standar NDPA 2 ppm; 4 ppm; 6 ppm; 8 ppm; dan 10 ppm... 18
3.4.3.3 Pembuatan larutan asam asetat 1 M ... 18
3.4.3.4 Pembuatan larutan natrium asetat 1 M ... 18
3.4.3.5 Pembuatan larutan natrium dihidrogen fosfat 1 M ... 18
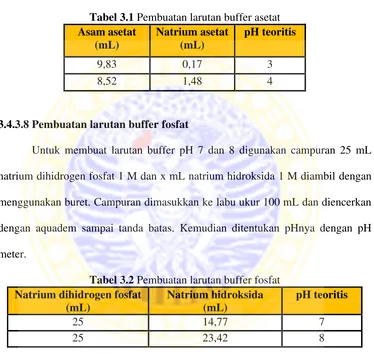
3.4.3.7 Pembuatan larutan buffer asetat... . 19
3.4.3.8 Pembuatan larutan buffer fosfat... ... 19
3.4.3.9 Pembuatan larutan buffer bikarbonat... . 19
3.4.4 Pembuatan kurva kalibrasi NDPA tanpa ekstraksi... 20
3.4.5 Optimasi parameter analitik ... 20
3.4.6.1 Optimasi pH... 20
3.4.6.2 Optimasi kecepatan pengadukan ... 20
3.4.6.3 Optimasi suhu ekstraksi... 21
3.4.6 Pembuatan kurva kalibrasi NDPA dengan ekstraksi HS-SDME...22
3.5 Validasi Parameter Analitik ... 22
3.5.1 Penentuan limit deteksi (sensitivitas)... 22
3.5.2 Penentuan persen recovery (R) ... 23
3.5.3 Uji koefisien variasi (presisi)... 23
3.5.4 Perhitungan enrichment factor... 24
3.6 Penyiapan Sampel ... 24
3.7 Analisis Sampel... 24
3.8 Spiking ... 25
BAB IV HASIL DAN PEMBAHASAN... 26
4.1 Optimasi Gas Chromatography(GC) ... 26
4.2 Pembuatan Kurva Kalibrasi NDPA Tanpa Ekstraksi ... 27
4.3 Headspace-Single Drop Microextraction(HS-SDME)... 29
4.3.1 Optimasi parameter analitik ... 31
4.3.1.1 Optimasi pH ... 31
4.3.1.2 Optimasi kecepatan pengadukan ... 33
4.3.1.3 Optimasi suhu ekstraksi ... 35
4.4 Pembuatan Kurva Kalibrasi NDPA dengan Ekstraksi HS-SDME 36 4.5 Validasi Parameter Analitik ... 38
4.5.1 Limit deteksi (sensitivitas) ... 38
4.5.2 Persen Recovery(R)... 39
4.5.3 Koefisien variasi (presisi)... 40
4.5.4 Enrichment factor... 40
4.6 Analisis Sampel... 41
4.7 Spiking ... 44
BAB V KESIMPULAN DAN SARAN... 47
5.1 Kesimpulan ... 47
5.2 Saran ... 47
DAFTAR GAMBAR
No. Judul Halaman
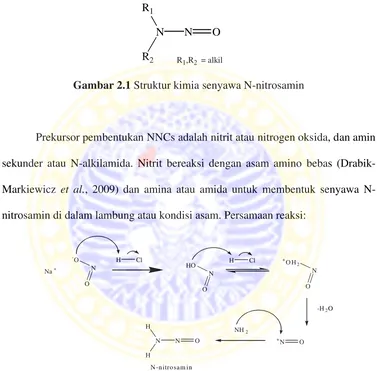
2.1 Struktur kimia senyawa N-nitrosamin... 10
2.2 Mekanisme reaksi pembuatan N-nitrosamin... 10
2.3 Persamaan reaksi nitrosating pembuatan N-nitrosodipropilamin... 11
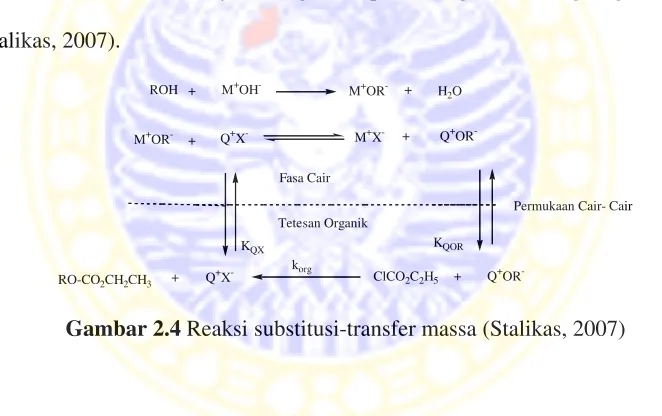
2.4 Reaksi substitusi-transfer massa... 12
2.5 2.6 Headspace-single drop microextraction(HS-SDME) Kromatografi gas... 13 14 3.1 Set-upHS-SDME... 17
3.2 Skema optimasi suhu ekstraksi... 21
4.1 Kurva optimasi GC... 27
4.2 Kromatogram N-nitrosodipropilamin... 27
4.3 Kurva kalibrasi NDPA tanpa ekstraksi... 28
4.4 Kurva optimasi pH... 32
4.5 Persamaan reaksi kondisi NDPA dalam suasana asam 32
4.6 Persamaan reaksi kondisi NDPA dalam suasana basa 33
4.7 Kurva optimasi kecepatan pengadukan... 34
4.8 Kurva optimasi suhu... 36
4.9 Kurva kalibrasi NDPA dengan ekstraksi HS-SDME... 37
DAFTAR LAMPIRAN
Pembuatan Kurva Kalibrasi NDPA Tanpa Ektraksi Pembuatan Kurva Optimasi pH
Pembuatan Kurva Optimasi Kecepatan Pengadukan Pembuatan Kurva Optimasi Suhu Ekstraksi
Pembuatan Kurva Kalibrasi NDPA dengan Ekstraksi HS-SDME Perhitungan Enrichment Factor
Perhitungan Konsentrasi Sampel
Perhitungan Spiking dan Recovery(%R) Spiking Kromatogram Nitrosodipropilamin (NDPA)
Kromatogram Sampel Hamburger I dan Spiking Sampel Hamburger I Kromatogram Sampel Hamburger II dan Spiking Sampel Hamburger II Kromatogram Sampel Hamburger III dan Spiking Sampel Hamburger III Kromatogram Sampel Kebab I dan Spiking Sampel Kebab I
BAB I PENDAHULUAN
1.1 Latar Belakang
Bahan pangan merupakan kebutuhan pokok bagi manusia disamping pendidikan, kesehatan, dan sandang. Kebutuhan bahan pangan ini akan terus meningkat sesuai dengan laju pertumbuhan penduduk. Secara garis besar masalah pangan dan sistem pangan umumnya dibagi atas sub sistem produksi, pengadaan, dan konsumsi. Bahan pangan tersebut akan mengalami perubahan-perubahan yang tidak diinginkan antara lain pembusukan. Proses pembusukan disebabkan oleh adanya reaksi kimia yang bersumber dari dalam dan dari luar bahan pangan tersebut (Barus, 2009). Pembusukan yang berasal dari luar bahan pangan disebabkan oleh mikroorganisme pembusuk.
Penggunaan bahan kimia sebagai bahan tambahan pada makanan (food addittive) saat ini sering ditemui pada makanan dan minuman. Pengawet bahan
Raharjo, 2005). Bahan kimia yang dapat digunakan untuk pengawet antara lain yaitu, NaCl, formalin, nitrit, dan lain sebagainya.
Penyakit kanker merupakan salah satu penyebab kematian terbesar di dunia. Di Indonesia penyakit kanker masuk dalam 6 urutan terbesar penyebab kematian (Sunaryanto, 2010). Menurut Tjindarbumi dan Mangunkusumo (2001), kasus penyakit kanker di Indosesia terus bertambah. Hasil penelitian menyebutkan bahwa setiap 100.000 orang terdapat kasus baru penyakit kanker sebanyak 170-190 kasus. Penyebab penyakit kanker salah satunya disebabkan oleh senyawa nitrosamin yang menyerang pada organ tubuh tertentu, misalnya perut dan kandung kemih (Domanska et al., 2005).
Pengawet nitrat dan nitrit merupakan salah satu zat pengawet yang sering ditemukan pada daging. Penggunaan pengawet ini bertujuan agar daging memperoleh warna yang baik dan tidak mudah rusak atau menghambat pertumbuhan mikroba (Husni dkk., 2007). Tingkat toleransi N-nitrosamin di
dalam tubuh manusia berkisar antara 5 sampai 10 μg/kg dari berat tubuh (Filho, et.
al., 2003). Negara Amerika Serikat (USA) telah mengatur tingkat toleransi untuk
N-nitrosamin sebesar 10.0 μg/kg sebagai batas maksimum peredaran produk di pasar (Ventanas dan Ruiz, 2006).
Berdasarkan uraian di atas, mengingat N-nitrosamin dalam hal ini NDPA bersifat karsinogen di dalam tubuh manusia dan menyebabkan kanker maka perlu adanya suatu teknik analisis yang sederhana dan mempunyai sifat sensitivitsas tinggi untuk mendeteksi adanya N-nitrosodipropilamin (NDPA) dalam makanan. Analisis mengenai N-nitrosamin dalam produk makanan (olahan daging), tembakau, dan air minum sudah banyak dikembangkan dengan berbagai macam teknik ekstraksi. Teknik ekstraksi yang digunakan oleh peneliti sebelumnya antara lain SPE-GC-MS (Solid-Phase Extraction Gas Chromatography Mass-Spectrometry) (Jurado-Sánchez et al., 2009), SPE-GC-MS-FID-NPD (Solid-phase
Extraction Gas Chromatography Mass Spectrometry Flame Ionization Detector
Nitrogen-phosphorus Detector) (Jurado-Sánchez et al., 2007), SPE-GC-MSD
(Solid-phase Extraction Gas Chromatography with Mass Selective Detector) (Yurchenko dan Mölder, 2007), SPME-DED-GC-MS (Solid Phase Microextraction Direct Extraction Device Gas Chromatography Mass
Phase Microextraction Gas Chromatography with Thermal Energy Analyzer
Detection) (Andrade et al., 2005), SPME-GC-NCD-NDP-CI-MS (Solid-phase
Microextraction Gas Chromatography Nitrogen Chemiluminesence Detection
Nitrogen-phosphorus Detection and Chemical Ionization Mass Spectrometry)
(Grebel et al., 2006), SFE-GC-TEA (Supercritical Fluid Extraction Gas Chromatography using Thermal Energy Analysis) (Recheet al., 2002), dan
TSE-GC-TEA (Traditional Solvent Extraction Gas Chromatography with Thermal Energy Analyzer Detection) (Incavo dan Schafer, 2006). Teknik ekstraksi di atas
mempunyai kelebihan, teknik SPE sangat kecil terjadinya kontaminasi yang bercampur pada analit, teknik SPME membuthkan jenis pelarut yang sedikit sehingga limbah pelarut organik yang banyak, teknik TSE mempunyai kapasitas sampel yang besar dan mempunyai pustaka yang banyak, teknik SFE dapat digunakan untuk mengektrak senyawa yang terdapat pada suatu fluida seperti karet. Akan tetapi, teknik-teknik ekstraksi tersebut masih kurang efisien dalam operasionalnya, teknik SPE membutuhkan pelarut organik dengan kemurnian yang tinggi dan waktu ekstraksi yang relatif lama karena mempunyai beberapa tahap ekstraksi, teknik SPME yang menggunakan absorben pelapis fiber dan teknik ekstraksi tradisional yang menghasilkan limbah pelarut organik. Sehingga masih belum efisien digunakan untuk analisis secara rutin karena akan membutuhkan biaya yang lebih mahal dan limbah pelarut organiknya tidak dapat didaur ulang.
peralatan khusus, mempunyai selektivitas tinggi, dan mempunyai batas deteksi rendah (Riccio et al., 2008). SDME mempunyai 2 model ekstraksi, yaitu SDME statis atau direct-SDME dan SDME dinamis atau Headspace-SDME (Stalikas, 2007).
1.2 Rumusan Masalah
Berdasarkan latar belakang yang telah diuraikan di atas, maka dapat diperoleh rumusan masalah sebagai berikut:
1. apakah teknik HS-SDME-GC-FID dapat digunakan untuk menganalisis senyawa nitrosodipropilamin (NDPA) yang terdapat pada daging olahan (hamburger dan kebab)?
2. bagaimana kondisi optimum yang meliputi pH, kecepatan pengadukan (skala), dan suhu (°C) pada analisis senyawa nitrosodipropilamin (NDPA) menggunakan teknik HS-SDME-GC-FID?
3. bagaimanakah validasi teknik HS-SDME-GC-FID meliputi limit deteksi, persen recovery, presisi, dan enrichment factor?
1.3 Tujuan Penelitian
Berdasarkan rumusan masalah di atas, maka dapat diperoleh tujuan penelitian sebagai berikut:
1. mengetahui kemampuan teknik HS-SDME-GC-FID untuk menganalisis senyawa nitrosodipropilamin (NDPA) yang terdapat pada daging olahan (hamburger dan kebab).
2. mengetahui kondisi optimum yang meliputi pH, kecepatan pengadukan (skala), dan suhu (°C) pada analisis senyawa nitrosodipropilamin (NDPA) menggunakan teknik HS-SDME-GC-FID.
1.4 Manfaat Penelitian
BAB II
TINJAUAN PUSTAKA
2.1 Produk Daging Olahan 2.1.1 Hamburger
Hamburger adalah suatu jenis makanan dari daging (Kamisa, 1997) yang berbentuk bulat, kemudian dipipihkan dan digoreng dengan mentega atau dipanggang di atas batu bara, biasanya dimakan sebagai isi roti bulat, diberi daun selada, saus tomat, dan bumbu lainnya.
Hamburger atau burger merupakan produk daging giling yang halus, dicampur dengan lemak hingga tercampur rata dengan proses kuring. Kuring adalah suatu proses pengolahan yang dapat menghambat pertumbuhan organisme melalui penggunaan garam nitrit dan berfungsi juga untuk memepertahankan warna daging. Manfaat melakukan kuring adalah untuk mendapatkan warna yang stabil, aroma, tekstur dan kelezatan yang baik, dan untuk mengurangi pengerutan daging selama proses pengolahan, serta memperpanjang masa simpan produk olahan daging (Cory, 2009).
2.1.2 Kebab
adalah nitrit, karena nitrit dapat berfungsi sebagai penghambat pertumbuhan organisme, sehingga kebab dapat lebih tahan lama.
2.2 Karsinogenik
2.3 N-Nitrosamin
N-Nitosamin adalah NNCs (N-nitroso compounds) senyawa yang terdapat pada makanan tertentu akibat dari reaksi zat nitrosating (Andrade et al., 2005).
Gambar 2.1Struktur kimia senyawa N-nitrosamin
Prekursor pembentukan NNCs adalah nitrit atau nitrogen oksida, dan amin sekunder atau N-alkilamida. Nitrit bereaksi dengan asam amino bebas (Drabik-Markiewicz et al., 2009) dan amina atau amida untuk membentuk senyawa N-nitrosamin di dalam lambung atau kondisi asam. Persamaan reaksi:
Na+ N
Gambar 2.2Mekanisme reaksi pembentukan N-nitrosamin
Nitrat dalam sayuran dapat direduksi menjadi nitrit oleh bakteri dari mulut. Sedangkan nitrit umumnya ditambahkan sebagai bahan tambahan pangan pada daging yang diawetkan, seperti sosis dan corned. Bahan pangan biasanya mengandung 10 ng/g, sedangkan daging dan ikan yang diasap mengandung
N N O
R1
R2 R
ratusan ng/g senyawa nitrit. Nitrit dengan mudah terdekomposisi dalam lingkungan asam membentuk nitrosating agents yang reaktif, yaitu NO+, N2O3dan
HNO2O3+. Nitrosating agents ini akan bereaksi dengan senyawa amina dan amida
yang terdapat dalam bahan pangan membentuk NNCs, yaitu N-nitrosodimetilamin (paling karsinogenik), N-nitrosodietilamin, dan N-nitrosodipropilamin (Pragdimurti, 2007). Permenkes RI No. 1168/Menkes/Per/X/1999 tentang Bahan Tambahan Makanan (BTM) yang membatasi penggunaan maksimum pengawet nitrit dalam produk daging olahan yaitu sebesar 125 mg/kg. Persamaan reaksi:
N N O
C3H7
C3H7
NO2- + 2H+ NO+ + H2O
N
C3H7 H C3H7
+ NO+ + H+
Gambar 2.3Persamaan reaksi nitrosating pembentukan N-nitrosodipropilamin (Belitz dan Grosh, 1999)
2.4. Headspace-Single Drop Microextraction(HS-SDME)
Headspace-Single Drop Microextraction (HS-SDME) merupakan salah satu model teknik ekstraksi dari Single Drop Microextraction (SDME). Headspace-Single Drop Microextraction (HS-SDME) merupakan suatu teknik ekstraksi cair-cair dengan menggunakan jumlah pelarut organik yang sangat sedikit, biasanya hanya 1 μL sampai 3 μL (Riccio et al., 2008). Posisi pelarut organik dibiarkan menggantung pada ujung microsyringe dan diletakkan di atas permukaan larutan sampel. Larutan sampel dihomogenkan agar terjadi transfer massa dan reaksi kimia senyawa target dan pelarut organik berlangsung sempurna (Stalikas, 2007).
ROH + M+OH- M+OR- + H2O
M+OR- + Q+X- M+X- + Q+OR
-Fasa Cair
Permukaan Cair- Cair
RO-CO2CH2CH3 + Q+X
-korg
ClCO2C2H5 + Q+OR -Tetesan Organik
KQX KQOR
Gambar 2.4Reaksi substitusi-transfer massa (Stalikas, 2007)
Gambar 2.5Headspace-single drop microextraction(HS-SDME)
Teknik Headspace-Single Drop Microextraction(HS-SDME) merupakan suatu teknik ekstraksi sederhana, cepat, dan murah. Selain itu, karena posisi pelarut organik berada di atas permukaan larutan sampel maka hasil ekstraksi bebas dari kontaminan yang dapat mengganggu analisis. Setelah proses ekstraksi selesai, tetesan (drop) yang berada di ujung microsyringe ditarik kembali ke dalam microsyringe dan dapat secara langsung dianalisis dengan GC (Gas Chromatography) (Riccioet al., 2008).
2.5 Gas Chromatography(GC)
INJECTION FLOW CONTROLLER REGULATOR
OVEN
COLUMN
RECORDER ELECTROMETER DETECTOR
MOL-SIEVE FIXED RESTRITORS
1 2 3
Keterangan: 1 . Air 2. Hydrogen 3. Carrier Gas
pada padatan pendukung yang inert berupa butiran halus dan fasa geraknya berupa gas yang bersifat inert (Handajani, 2005).
Gambar 2.6Kromatografi gas
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian dilaksanakan di Laboratorium Kimia Analitik dan Laboratorium Instrumentasi Departemen Kimia, Fakultas Sains dan Teknologi, Universitas Airlangga. Penelitian dilaksanakan pada bulan Januari 2012 sampai bulan Juni 2012.
3.2 Bahan Penelitian
Bahan-bahan yang digunakan pada penelitian ini antara lain metanol, larutan standar nitrosodipropilamin (NDPA) 99,9%, toluena, asam asetat glasial, natrium asetat, natrium dihidrogen fosfat, natrium hidroksida, aquadem, dan NaHCO3. Sampel daging hamburger dan daging kebab didapatkan dari Surabaya
Timur.
3.3 Alat-alat Penelitian
LMS-1003 Serial No. 2010051312, batang pengaduk (panjang 1,5 cm dan diameter 0,5 cm), termometer dan mortar.
3.4 Prosedur Penelitian 3.4.1 Diagram alir penelitian
Pembuatan Larutan Standar NDPA
Optimasi Parameter Analitik
Kecepatan Pengadukan (rpm)
Pembuatan kurva kalibrasi NDPA dengan Parameter Optimasi HS-SDME
Penentuan Parameter Validasi
Analisis Data Pembuatan Kurva
Kalibrasi NDPA
Analisis Sampel
Suhu (°C) pH
Limit Deteksi
Persen Recovery
Koefisien Variasi
Enrichment Factor
3.4.2 Headspace-single drop microextraction
Pada penelitian ini digunakan toluena untuk mengekstrak senyawa nitrosodipropilamin (NDPA). Sebanyak 10 mL larutan standar (misalnya, larutan standar NDPA 6 ppm) dimasukkan ke dalam botol yang berisi batang pengaduk magnetik. Kemudian ditutup dengan penutup karet. Microsyringe yang telah berisi pelarut organik (misalnya, toluena sebanyak 3 μL) dimasukkan ke dalam botol secara tegak lurus hingga tergantung di atas larutan standar. Kemudian ujungmicrosyringe ditekan sehingga pelarut organik menggantung di ujung jarum. Kemudian larutan standar NDPA diaduk dengan menggunakan pengaduk magnetik. Setelah proses ekstraksi selesai, pelarut organik ditarik kembali ke dalam microsyringe dan diinjeksikan langsung ke instrumen GC-FID, dan dihasilkan luas area untuk konsentrasi standar tersebut.
Gambar 3.1 Set-upHS-SDME
3.4.3 Pembuatan larutan
3.4.3.1 Pembuatan larutan induk NDPA 50 ppm
3.4.3.2 Pembuatan larutan standar NDPA 2 ppm; 4 ppm; 6 ppm; 8 ppm; dan 10 ppm
Sebanyak 1,2 mL larutan induk NDPA 50 ppm dimasukkan ke dalam labu ukur 10 mL, kemudian ditambahkan metanol sampai tanda batas. Kemudian dikocok sampai homogen. Sehingga diperoleh larutan standar 6 ppm. Untuk larutan standar 2 ppm; 4 ppm; 8 ppm; dan 10 ppm, masing-masing dibuat dari 0,4 mL; 0,8 mL; 1,6 mL; dan 2,0 mL larutan induk NDPA 50 ppm dimasukkan ke dalam labu ukur 10 mL, kemudian ditambahkan metanol sampai tanda batas. 3.4.3.3 Pembuatan larutan asam asetat 1 M
Diambil 5,75 mL asam asetat glasial dengan pipet skala, kemudian dimasukkan ke dalam labu ukur 100 mL dan diencerkan dengan aquadem sampai tanda batas.
3.4.3.4 Pembuatan larutan natrium asetat 1 M
Sebanyak 8,2 gram natrium asetat ditimbang dengan teliti, kemudian dilarutkan dengan aquadem dalam gelas beker. Larutan dipindahkan ke dalam labu ukur 100 mL dan diencerkan dengan aquadem sampai tanda batas.
3.4.3.5 Pembuatan larutan natrium dihidrogen fosfat 1 M
Ditimbang 12,0 gram natrium dihidrogen fosfat, kemudian dilarutkan dengan aquadem dalam gelas beker. Larutan dipindahkan ke dalam labu ukur 100 mL dan diencerkan dengan aquadem sampai tanda batas.
3.4.3.6 Pembuatan larutan natrium hidroksida 1M
3.4.3.7 Pembuatan buffer asetat
Untuk membuat larutan buffer pH 3 dan 4 digunakan campuran x mL asam asetat 1 M dan y mL natrium asetat 1 M. Kemudian ditentukan dengan pH meter.
Tabel 3.1Pembuatan larutan buffer asetat Asam asetat natrium dihidrogen fosfat 1 M dan x mL natrium hidroksida 1 M diambil dengan menggunakan buret. Campuran dimasukkan ke labu ukur 100 mL dan diencerkan dengan aquadem sampai tanda batas. Kemudian ditentukan pHnya dengan pH meter.
Tabel 3.2Pembuatan larutan buffer fosfat Natrium dihidrogen fosfat
Sebanyak 1,68 gram NaHCO3ditimbang, dimasukkan ke dalam labu ukur
Tabel 3.3Pembuatan larutan buffer bikarbonat NaHCO3
(mL)
NaOH (mL) Aquadem
(mL)
pH teoritis
50 10,7 39,3 10
50 22,7 27,3 11
3.4.4 Pembuatan kurva kalibrasi NDPA tanpa ekstraksi
Sebanyak 5 konsentrasi larutan standar NDPA masing-masing 2 ppm; 4 ppm; 6 ppm; 8 ppm; dan 10 ppm, dianalisis dengan menginjeksikan secara langsung ke GC-FID kemudian diplot grafik antara konsentrasi larutan standar dan luasan puncak.
3.4.5 Optimasi parameter analitik 3.4.5.1 Optimasi pH
Pada penelitian ini divariasi pH antara lain pH asam (pH 3 dan pH 4), pH netral (pH 7 dan pH 8), serta pH basa (pH 10 dan pH 11). Sementara variabel yang lain dibuat tetap (jenis pelarut organik yang digunakan adalah toluena, volume palarut organik 3 μL, kecepatan pengadukan skala 3, suhu 30 °C, waktu ekstraksi 30 menit, dan volume larutan standar NDPA 6 ppm sebanyak 10 mL ). Setiap variasi pH dilakukan pengulangan sebanyak 3 kali. Larutan hasil ekstraksi dianalisis dengan GC-FID, kemudian diplot suatu grafik antara pH dan luasan puncak. pH yang optimal akan digunakan dalam optimasi parameter selanjutnya. 3.4.5.2 Optimasi kecepatan pengadukan
µL, suhu 30 °C, waktu ekstraksi 30 menit, dan volume larutan standar 6 ppm sebanyak 10 mL), sedangkan pH sesuai dengan hasil optimasi pada prosedur 3.4.6.1. Prosedur ekstraksi seperti prosedur 3.4.3. Setiap variasi kecepatan pengadukan dilakukan pengulangan sebanyak 3 kali. Larutan hasil ekstraksi dianalisis dengan GC-FID, kemudian diplot suatu grafik antara kecepatan pengadukan dan luasan puncak. Kecepatan pengadukan yang optimal akan digunakan dalam optimasi parameter selanjutnya.
3.4.5.3 Optimasi suhu ekstraksi
Optimasi suhu ekstraksi digunakan suhu sebesar (30 °C, 35 °C, dan 40 °C). Sementara variabel yang lain dibuat tetap (jenis pelarut organik yang digunakan adalah toluena, volume pelarut organik 3 µL, waktu ekstraksi 30 menit dan volume larutan standar 6 ppm sebanyak 10 mL), sedangkan pH dan kecepatan pengadukan sesuai dengan hasil optimasi pada prosedur 3.4.6.1 dan 3.4.6.2. Prosedur ekstraksi seperti prosedur 3.4.3. Setiap variasi suhu dilakukan pengulangan sebanyak 3 kali. Larutan hasil ekstraksi dianalisis dengan GC-FID, kemudian diplot suatu grafik antara suhu ekstraksi dan luasan puncak.
3.4.6 Pembuatan kurva kalibrasi NDPA dengan ekstraksi HS-SDME
Sebanyak 5 konsentrasi larutan standar NDPA masing-masing 2 ppm; 4 ppm; 6 ppm; 8 ppm; dan 10 ppm, dengan menggunakan parameter-parameter analitik yang telah dioptimasi (prosedur 3.4.6.1, prosedur 3.4.6.2, dan prosedur 3.4.6.3), diekstraksi dan dianalisis dengan GC-FID kemudian diplot grafik antara konsentrasi larutan standar dan luasan puncak. Persamaan yang didapatkan digunakan untuk analisis sampel dan penentuan validasi parameter analitik.
3.5 Validasi Parameter Analitik
3.5.1 Penentuan limit deteksi (sensitivitas)
Limit deteksi (LOD) atau sensitivitas instrumen GC dan metode ekstraksi dengan HS-SDME dapat ditentukan dari persamaan regresi kurva kalibrasi NDPA. Pertama dilakukan adalah menghitung standar deviasi dari signal blanko (Sy/x),
dengan y merupakan luas area masing-masing pengukuran, ŷ dihitung dengan memasukkan x ke persamaan regreasi, dan n adalah jumlah standar. Kedua, hasil Sy/xdimasukkan ke dalam persamaan:
YLOD= a + 3 Sy/x ...(1.2)
dengan YLOD merupakan sinyal konsentrasi terkecil yang masih terdeteksi dan a
dimasukkan ke persamaan regrasi kurva kalibrasi NDPA. Sehingga didapatkan suatu konsentrasi NDPA terkecil dalam sampel yang masih dapat diukur atau terdeteksi dengan baik.
3.5.2 Penentuan persen recovery(R)
Persen recovery dapat ditentukan dari persamaan regresi kurva kalibrasi NDPA dengan ekstraksi HS-SDME. Pertama, masing-masing luas area setiap konsentrasi standar NDPA dimasukkan ke dalam persamaan regresi sebagai y, kemudian nilai x yang didapatkan dirata-rata, sehingga diperoleh nilai x yang merupakan nilai (konsentrasi) rata-rata hasil pengukuran. Kedua, nilai x untuk masing-masing konsentrasi standar NDPA dimasukkan ke dalam persamaan:
%
dengan μ merupakan nilai (konsentrasi) standar NDPA sebenarnya. Hasil pengukuran akurat nilai persen recoverysebesar 100%.
3.5.3 Uji koefisien variasi (presisi)
Koefisien variasi atau presisi dapat ditentukan dengan persamaan:
%
dengan x merupakan luas area kromatogram setiap pengukuran, nilai x merupakan rata-rata luas area kromatogram, dan n merupakan jumlah pengukuran (replication). Pengukuran memberikan presisi yang baik jika KV< 3%.
3.5.4 Perhitungan Enrichment Factor
Theoretical enrichment factor(EFth) dapat ditentukan dengan persamaan:
e s th
V V
EF ...(1.6)
dengan Vs merupakan volume larutan standar NDPA (larutan ekstrak) dan Ve
merupakan volume pelarut organik.
True enrichment factor(EFtr) dapat ditentukan dengan persamaan:
EFtr= EFthx R ...(1.7)
dengan EFth merupakan theoretical enrichment factor dan R merupakan persen
recovery.
3.6 Penyiapan sampel
Sampel (daging hamburger dan daging kebab) masing-masing dihaluskan dengan mortar. Limapuluh gram sampel yang telah halus direndam dalam metanol, didiamkan selama 3 jam, kemudian disaring filtratnya dengan menggunakan penyaring buchnerdan kertas saring. Larutan sampel yang diperoleh di masukkan dalam labu ukur 100 mL ditambah metanol sampai tanda batas.
3.7 Analisis Sampel
3.4.6.2, dan prosedur 3.4.6.3). Hasil ekstraksi dianalisis dengan menggunakan GC-FID. Konsentrasi senyawa nitrosodipropilamin (NDPA) dihitung menggunakan persamaan regresi kurva kalibrasi NDPA dengan ekstraksi HS-SDME.
3.8 Spiking
Sampel (daging hamburger dan daging kebab) masing-masing dihaluskan dengan mortar. Limapuluh gram sampel yang telah halus direndam dalam metanol serta ditambah larutan standar NDPA 50 ppm sebanyak 4 mL, didiamkan selama 3 jam, kemudian disaring filtratnya dengan menggunakan penyaring buchnerdan kertas saring.
BAB IV
HASIL DAN PEMBAHASAN
4.1 Optimasi Gas Chromatography(GC)
Gas Chromatography yang digunakan pada penelitian adalah tipe HP-Hewlett 5890 Packard Series II dengan kolom sebagai fasa diamnya digunakan HP-5 bersifat non polar (Reuessac dan Reuessac, 2007). Detektor yang digunakan adalah FID (Flame Ionization Detector) yang mempunyai kepekaan terhadap senyawa karbon organik (Hendayana, 2006). Fasa gerak berupa gas hidrogen dan gas nitrogen. Optimasi ini digunakan untuk mendapatkan hasil kromatogram yang optimum untuk pelarut organik (metanol dan toluena) maupun senyawa nitrosodipropilamin (NDPA).
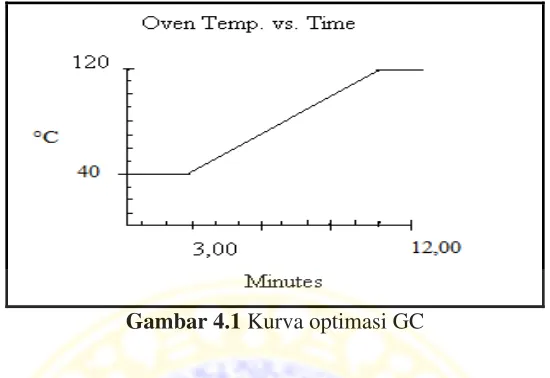
Pengaturan temperatur GC pada penelitian ini dapat dilihat pada Tabel 4.1, serta kurva temperatur GC-FID dapat dilihat pada Gambar 4.1. Berdasarkan pengaturan temperatur tersebut, waktu yang diperlukan pada setiap analisis menggunakan GC-FID selama 12 menit.
Tabel 4.1Kondisi Gas Chromatography(GC)
Pengaturan Kondisi
Injector A 250 °C
Detector A 300 °C
Initial Temperature 40 °C Initial Time 3 menit
Rate 10,0 C/min
Final Temperature 120 (C) Final Time 1,00 menit
Gambar 4.1Kurva optimasi GC
Berdasarkan pengaturan temperatur yang sudah dilakukan, peak metanol sebagai pelarut berada pada retention time 1,5 menit, sedangkan peak NDPA berada pada retention time sekitar 8 sampai dengan 9 menit. Kromatogram hasil optimasi GC dapat dilihat pada Gambar 4.2.
Gambar 4.2Kromatogram nitrosodipropilamin (NDPA)
4.2 Pembuatan Kurva Kalibrasi NDPA Tanpa Ekstraksi
selanjutnya diplotkan antara konsentasi larutan standar NDPA dengan luasan area kromatogram sehingga diperoleh kurva kalibrasi NDPA tanpa ekstraksi berupa garis linier. Pembuatan kurva kalibrasi ini bertujuan untuk mengetahui besarnya pemekatan yang terjadi pada proses ekstraksi dengan HS-SDME, membandingkan limit deteksi antara pengukuran larutan NDPA tanpa dan dengan menggunakan HS-SDME, dan untuk mengetahui linieritas dan reprodusibilitas alat.
Suatu kurva mempunyai linieritas tinggi apabila nilai koefisien korelasinya (R2) lebih besar dari 0,99. Sedangkan reprodusibilitas dapat dilihat dari nilai koefisien variasi, reprodusibilitas baik jika KV<3% (Miller dan Miller, 1988).
Data yang dihasilkan dapat dilihat pada Tabel 4.2 dan Gambar 4.3. Tabel 4.2 Data kurva kalibrasi NDPA tanpa ekstraksi Konsentrasi Standar NDPA
(ppm)
Luas Area Rata-rata (satuan)
2 1748,06
4 2823,44
6 3644,55
8 4501,88
10 5328,76
Dari data yang diperoleh pada pembuatan kurva kalibrasi tanpa ekstraksi dapat diketahui bahwa semakin besar konsentrasi larutan standar NDPA maka semakin besar luas area kromatogram yang dihasilkan. Kurva kalibrasi NDPA tanpa ekstraksi diperoleh regresi linier y = 454,37x + 858,4 dengan koefisien korelasi (R2) sebesar 0,9938. Ini menunjukkan ada korelasi antara konsentrasi NDPA dengan luasan area kromatogram. Sedangkan reprodusibilitas didapatkan dari rentang 0,15% sampai dengan 6,7%, empat dari lima data konsentarsi mempunyai KV<3%, hal ini dapat disimpulkan bahwa presisi yang dihasilkan oleh
instrumen GC baik digunakan untuk analisis senyawa NDPA.
4.3 Headspace-Single Drop Microextraction(HS-SDME)
Penelitian ini menggunakan Headspace-Single Drop Microextraction (HS-SDME), dengan berbagai parameter yang ditetapkan yaitu, toluena sebagai pelarut organik, waktu ekstraksi selama 30 menit, volume pelarut organik sebanyak 3 μL, dan sebanyak 10 mL larutan standar NDPA 6 ppm.
Tabel 4.3Sifat fisika pelarut organik dan senyawa NDPA
Sifat Fisika Metanol Toluena NDPA
Titik didih (°C) 64,7b 110.6c 206a Log Pow (25 °C) -0,82b 2,73c 1,36a
Massa Jenis pada 20 °C
(g/cm3) 0,7918b 0,87c 1,013d
Sumber: aReport on Carcinogens 2011, bMerck 2007, cMerck 2012, dDowdle 1989
mempunyai nilai tegangan permukaan yang tinggi sehingga gaya kohesif yang terjadi lebih tinggi, kelarutan dalam air lebih kecil, dan tetes pelarut organik lebih stabil (Battle dan Nerin, 2004). Alasan inilah yang menyebabkan toluena mempunyai kemampuan lebih besar dalam mengekstrak NDPA dari larutan ekstrak atau sampel.
Waktu ekstraksi yang digunakan adalah selama 30 menit, ini merupakan waktu optimum untuk mengekstraksi NDPA, karena semakin lama waktu ekstraksi larutan pengekstraknya semakin berkurang. Hal ini karena drop yang berisi pelarut organik secara perlahan menguap dengan peningkatan waktu ekstraksi (Sarkhosh et al., 2012), sehingga senyawa NDPA kurang terekstrak secara sempurna.
Volume toluena yang digunakan adalah sebanyak 3 μL, volume toluena ini merupakan volume optimum untuk ekstraksi dengan HS-SDME. Pelarut organik kurang dari 3 μL akan menguap terlebih dahulu sebelum waktu ekstraksi selesai, sedangkan pelarut organik lebih dari 3 μL menyebabkan drop tidak stabil dikarenakan mudah jatuh (Intissar, 2012). Hal ini disebabkan gaya tarik kebawah (Fg) lebih besar daripada gaya tarik keatas (Ff), sehingga drop pelarut organik
akan mudah jatuh.
4.3.1 Optimasi parameter analitik 4.3.1.1 Optimasi pH
Optimasi pH pada analisis NDPA dengan HS-SDME dilakukan menggunakan enam variasi pH yaitu, pH 3, pH 4, pH 7, pH 8, pH, 10, dan pH 11, dengan toluena sebagai pelarut organik, volume toluena 3 μL, kecepatan pengadukan skala 3, suhu ekstraksi 30 °C, waktu ekstraksi 30 menit, dan volume larutan standar NDPA 6 ppm sebanyak 10 mL sebagai variabel tetap. Optimasi pH ini digunakan untuk meningkatkan efisiensi ekstraksi pada analit (Grebel et al., 2006), dimana apabila suatu senyawa mengalami ionisasi menjadi ion-ionnya menyebabkan analit menjadi lebih polar atau mudah larut dalam fasa air sehingga akan menurunkan efisiensi ekstraksi. Dari hasil analisis dengan menggunakan GC-FID didapatkan luas area kromatogram pada masing-masing pH, seperti pada Tabel 4.4 dan Gambar 4.4.
Tabel 4.4Data optimasi pH
Variasi pH Luas Area Rata-rata (satuan)
3 379,38
4 853,90
7 255,84
8 238,29
10 227,36
Gambar 4.4Kurva optimasi pH
Kenaikan pH dalam fasa cair dapat meningkatkan jumlah analit yang tekstrak. Hal ini disebabkan karena adanya kesetimbangan disosiasi antara analit yang bersifat asam dengan analit yang bersifat basa. Analit yang bersifat asam dapat menyebabkan analit tidak dapat melepaskan ionnya sehingga di dalam larutan, analit berada dalam bentuk molekulnya dan hal ini dapat meningkatkan jumlah analit yang terekstrak.
N
C3H7
C3H7 N
O N
C3H7 C3H7 N+
O- H
+Cl
-N
C3H7
C3H7 N
Cl OH
Gambar 4.5Persamaan reaksi kondisi NDPA dalam suasana asam
N
Gambar 4.6Persamaan reaksi kondisi NDPA dalam suasana basa
Dari kurva di atas dapat dilihat bahwa pH lebih dari 4 menyebabkan penurunan luas area kromatogram, jumlah NDPA yang terekstrak semakin berkurang karena cenderung larut dalam air daripada fasa organiknya. Tetapi, menurut Report Carcinogens oleh National Toxicology Program, Department of Health and Human Services pada tahun 2011 mengatakan bahwa NDPA stabil dalam larutan netral atau basa dalam 14 hari, dan kurang stabil dalam larutan asam. Hal ini dapat dijelaskan bahwa stabilitas ini hanya digunakan untuk penyimpanan larutan NDPA dalam jangka waktu yang lama.
4.3.1.2 Optimasi kecepatan pengadukan
Data hasil analisis menggunakan GC didapatkan luas area kromatogram masing-masing kecepatan pengadukan seperti pada Tabel 4.5 dan Gambar 4.7.
Tabel. 4.5Data optimasi kecepatan pengadukan Variasi Kecepatan
Pengadukan (skala)
Luas Area Rata-rata (satuan)
3 853,904
4 3758,28
5 3970,91
6 8461,06
7 2165,26
Gambar 4.7Kurva optimasi kecepatan pengadukan
dengan bertambahnya kecepatan maka akan menyebabkan drop organik menjadi tidak stabil bahkan akan jatuh sebelum ekstraksi selesai sehingga dapat menurunkan efisiensi ekstraksi. Selain itu kecepatan pengadukan yang cepat mengakibatkan dislodgment drop organik dari jarum (Sarkhosh et al., 2012). 4.3.1.3 Optimasi suhu ekstraksi
Optimasi suhu pada analisis NDPA dengan HS-SDME dilakukan menggunakan tiga variasi suhu yaitu, 30 °C, 35 °C, dan 40 °C, dengan toluena sebagai pelarut organik, volume toluena 3 μL, pH 4, kecepatan pengadukan skala 6, waktu ekstraksi 30 menit, dan volume larutan standar NDPA 6 ppm sebanyak 10 mL sebagai variabel tetap. Optimasi ini bertujuan untuk meningkatkan penguapan dan transfer analit dari sampel sehingga menghasilkan efisiensi
ekstraksi yang baik (Valentinavičiūtė et al., 2008). Dari hasil analisis dengan
menggunakan GC didapatkan luas area kromatogram masing-masing suhu seperti Tabel 4.6 dan Gambar 4.8.
Tabel 4.6Data optimasi suhu
Variasi Suhu (°C) Luas Area Rata-rata(satuan)
30 8461,06
35 3833,14
Gambar 4.8Kurva optimasi suhu
Dari kurva di atas diperoleh suhu optimum untuk ekstraksi HS-SDME adalah 30 °C. Hal ini disebabkan karena dengan meningkatnya suhu dari larutan di atas 30 °C dapat menyebabkan kerusakan dropdan menguapnya drop. Hal ini dapat dibuktikan bahwa sebelum proses ekstraksi selesai, drop pelarut organik yaitu toluena hilang karena pemanasan. Suhu ekstraksi di bawah 30 °C akan menurunkan efisiensi ektraksi, karena suhu di bawah 30 °C transfer analit menuju pelarut organik akan berlangsung lebih lama (Hashemi et al, 2011). Oleh karena itu, suhu ekstraksi 30 °C dianggap sebagai suhu optimum pada penelitian ini.
dan 10 ppm sebanyak 10 mL. Kemudian didapatkan luas area kromatogram untuk larutan standar NDPA masing-masing konsentrasi dan selanjutnya diplotkan antara konsentasi larutan standar NDPA dengan luasan area kromatogram sehingga diperoleh kurva kalibrasi NDPA dengan ekstraksi HS-SDME berupa garis linier. Pembuatan kurva kalibrasi ini bertujuan untuk mengetahui besarnya pemekatan yang terjadi pada proses ekstraksi dengan HS-SDME, membandingkan limit deteksi antara pengukuran larutan NDPA tanpa dan dengan menggunakan HS-SDME, dan untuk mengetahui linieritas. Data yang dihasilkan dapat dilihat pada Tabel 4.7 dan Gambar 4.9.
Tabel 4.7Data kurva kalibrasi NDPA dengan ekstraksi HS-SDME Konsentrasi Standar NDPA
(ppm)
Luas Area Rata-rata (satuan)
2 5239,60
4 6840,90
6 8479,37
8 10040,85
10 11635,32
Kurva kalibrasi NDPA dengan HS-SDME pada kondisi parameter analitik optimum dibandingkan dengan data kurva kalibrasi NDPA tanpa ekstraksi. Besarnya pemekatan dalam proses ekstraksi menggunakan HS-SDME akan dibahas pada 4.5.4. Kurva kalibrasi NDPA dengan ekstraksi HS-SDME diperoleh regresi linier y = 799,57x + 3649,8 dengan koefisien korelasi (R2) sebesar 0,9999. Ini menunjukkan ada korelasi antara konsentrasi NDPA dengan luas area kromatogram.
4.5 Validasi Parameter Analitik
Validasi parameter analitik didasarkan pada persamaan regresi linier kurva kalibrasi NDPA dengan ekstraksi HS-SDME. Regresi linier tersebut digunakan untuk menentukan konsentrasi NDPA dalam sampel, menentukan % recovery, koefisien variasi dan limit deteksi (LOD) dari instrumen.
4.5.1 Limit deteksi (sensitivitas)
Limit deteksi merupakan konsentrasi atau jumlah terendah dari suatu zat yang dapat ditentukan dan secara statistik memiliki harga yang berbeda dengan blanko analinya. Semakin kecil nilai limit deteksi, maka semakin baik pula karakteristik instrumen tersebut (Miller dan Miller, 1988).
Dari hasil perhitungan limit deteksi (LOD) kurva kalibrasi NDPA dengan
ekstraksi HS-SDME, didapatkan nilai limit deteksi sebesar 78 ppb. Nilai tersebut merupakan batas terkecil konsentrasi yang masih dapat direspon oleh Gas Chromatography. Sedangkan limit deteksi untuk kurva kalibrasi tanpa ekstraksi
pengukuran NDPA tanpa ekstrakasi dan limit deteksi pengukuran NDPA dengan ekstraksi HS-SDME menunjukkan bahwa metode ekstraksi HS-SDME mampu meningkatkan sensitivitas GC-FID untuk memberikan respon terhadap NDPA. Dapat disimpulkan bahwa dengan adanya metode ekstraksi menggunakan HS-SDME sensitivitas GC-FID menjadi sangat tinggi (Sleiman et al., 2009).
4.5.2 Persen recovery(R)
Akurasi pada penelitian ini dinyatakan dalam % recovery. Persen recovery menyatakan ketepatan yang merupakan pendekatan setiap konsentrasi standar yang diperoleh kembali dengan konsentrasi larutan standar yang sebenarnya. Pengukuran nilai akurasi diperoleh dari persamaan regresi pada kurva kalibrasi dengan ekstraksi HS-SDME dengan lima konsentrasi larutan standar NDPA yaitu 2 ppm, 4 ppm, 6 ppm, 8 ppm, dan 10 ppm. Nilai %recovery penelitian ini dapat dilihat pada Tabel 4.8.
mendekati kedekatan konsentrasi NDPA sebenarnya. Nilai recovery ada yang menunjukkan 105,65% dikarenakan adanya senyawa lain yang memberikan sinyal yang sama pada retention timeNDPA.
4.5.3 Koefisien variasi (presisi)
Koefisien variasi atau presisi atau ketelitian ditentukan melalui perhitungan simpangan baku (SD) dan koefisien variasi. Koefisien variasi ini digunakan untuk melihat reprodubilitas instrumen, dalam penelitian ini adalah GC-FID. Nilai Koefisien variasi penelitian ini dapat dilihat pada Tabel 4.9.
Tabel 4.9 Data koefisien variasi larutan standar NDPA dengan ekstraksi HS-SDME
Konsentrasi NDPA (ppm) Simpangan Baku (SD)
Koefisien Variasi (%)
2 29,675 0,566
4 11,458 0,167
6 23,317 0,275
8 9,036 0,089
10 35,846 0,308
Metode dapat dikatakan mempunyai ketelitian atau presisi yang baik jika nilai koefisien variasi (KV<3%) (Miller dan Miller, 1988). Dapat disimpulkan
bahwa ketelitian atau presisi yang dihasilkan oleh GC-FID baik digunakan untuk analisis senyawa NDPA dalam sampel, yang dibuktikan dengan dihasilkan koefisien variasi dari 0,089 % sampai dengan 0,566 %.
4.5.4 Enrichment Factor
Gambar 4.10Kurva pemekatan NDPA menggunakan ekstraksi HS-SDME Setelah dilakukan perhitungan, maka didapatkan enrichmen faktor theoretical (EFth) sebesar 3333,33 kali. Menurut teoritis pemekatan yang terjadi
pada proses ekstraksi NDPA menggunakan HS-SDME sebesar 3333,33 kali. Sedangkan pemekatan sebenarnya atau true enrichment factor (EFtr) sebesar
3372,52 kali. Jadi dapat disimpulkan bahwa proses pemekatan yang terjadi pada ekstraksi menggunakan HS-SDME baik, karena hasil EFth tidak begitu
mempunyai selisih yang jauh dengan EFtr.
4.6 Analisis Sampel
mengekstrak senyawa nitrosodipropilamin yang terdapat pada sampel daging. Setelah 3 jam perendaman, filtrat disaring menggunakan buchner dan kertas saring sehingga diperoleh larutan sampel yang mengandung nitrosodipropilamin. Larutan sampel yang mengandung nitrosodipropilamin di masukkan dalam labu ukur 100 mL dan ditambahkan metanol sampai tanda batas.
Larutan sampel yang mengandung nitrosodipropilamin disimpan pada suhu dingin, gelap, dan analisis dilakukan paling lama 14 hari setelah pengambilan sampel. Hal ini dilakukan karena menurut Report Carsinogens National Toxicology Program Department of Health and Human Services tahun 2011, senyawa nitrosodipropilamin stabil sebelum 14 hari penyimpanan. Serta menghindari degradasi oleh mikroba dalam sampel. Setiap sebelum analisis, sampel terlebih dahulu disaring untuk menghilangkan kotoran yang dapat mengganggu proses analisis. Hasil analisis dari sampel Hamburger dan Kebab dapat dilihat pada Tabel 5.0.
Tabel 5.0Data analisis sampel
Sampel
Luas Area (satuan)
I II III
Hamburger 3864,19 4236,66 4763,75
Kebab 6148,55 0 1781,71
Tabel 5.1Data konsentrasi NDPA dalam sampel
Sampel
Konsentrasi (ppm)
I II III
Hamburger 0,27 0,73 1,39
Kebab 3,13 -
-Berdasarkan Tabel 5.1 di atas dapat teramati bahwa metode HS-SDME-GC-FID dapat mendeteksi sampel hamburger mengandung senyawa NDPA dari 0,27 ppm sampai dengan 1,39 ppm. Sedangkan sampel kebab hanya satu dari tiga sampel kebab yang terdeteksi yaitu sebesar 3,13 ppm. Dua sampel kebab yang lain tidak dapat terdeteksi, hal ini terdapat 2 kemungkinan yaitu senyawa NDPA dalam sampel tidak ada atau senyawa NDPA ada dalam sampel tetapi di bawah LOD.
Sedangkan berdasarkan uji yang dilakukan di Balai Besar Laboratorium Kesehatan Surabaya menyatakan bahwa senyawa nitrit yang merupakan senyawa pembentuk NDPA tidak terdeteksi. Hal ini disebabkan karena kandungan nitrit yang terdapat pada sampel hamburger dan kebab sangat kecil konsentrasinya, apabila digunakan metode konvensional (titrasi) untuk menentukan konsentrasinya tidak akan terdeteksi. Penyebab lainnya adalah nitrit sudah berubah menjadi senyawa NDPA.
4.7 Spiking
Sampel berupa daging hamburger dan kebab masing-masing dihaluskan dengan mortar untuk memperbesar luas permukaan daging, sehingga senyawa nitrosodipropilamin yang terkandung di dalam sampel daging dapat terekstraki dengan sempurna. Kemudian sebanyak 50 gram sampel daging yang halus ditimbang secara teliti, kemudian direndam dalam metanol dan 4 mL larutan standar NDPA 50 ppm selama 3 jam dalam keadaan tertutup agar senyawa nitrosodipropilamin tidak menguap dan larut sempurna pada metanol. Perendaman sampel daging bertujuan untuk mengekstrak senyawa nitrosodipropilamin yang terdapat pada sampel daging. Setelah 3 jam perendaman, filtrat disaring menggunakan buchnerdan kertas saring sehingga diperoleh larutan sampel yang mengandung nitrosodipropilamin. Larutan sampel yang mengandung nitrosodipropilamin di masukkan dalam labu ukur 100 mL dan ditambahkan metanol sampai tanda batas.
Tabel 5.2Data spiking sampel
Kemudian untuk mengetahui konsentrasi dalam spiking sampel maka luas area kromatogram tersebut dimasukkan kedalam persamaan regrasi linier dari kurva kalibrasi NDPA menggunakan ekstraksi HS-SDME yaitu, y= 799,57x + 3649,8 diperoleh konsentrasi NDPA dalam spiking sampel masing-masing dapat dilihat pada Tabel 5.3.
Tabel 5.3Data konsentrasi NDPA dalam spiking sampel Spiking
Dari setiap sampel spiking dihitung recovery-nya. Jika recovery sampel spiking mendekati 100% maka matrik dalam sampel tidak mempengaruhi proses analisis, begitu sebaliknya misalkan nilai recoverysampel spiking jauh dari 100% maka matrik dalam sampel mempengaruhi proses analisis. Hasil recovery sampel spiking dapat dilihat pada Tabel 5.4.
Dengan recovery yang jauh dari 100% dibandingkan dengan pada saat ekstraksi larutan standar maka dapat dikatakan bahwa matrik yang terdapat sampel mempengaruhi proses ekstraksi NDPA dengan metode HS-SDME.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan penelitian yang telah dilakukan dapat ditarik kesimpulan sebagai berikut :
1. Teknik HS-SDME-GC-FID dapat digunakan untuk menganalisis senyawa nitrosodipropilamin (NDPA) yang terdapat pada daging olahan (hamburger dan kebab) dengan konsentrasi setiap sampel sebagai berikut, hamburger I sebesar 0,27 ppm, hamburger II sebesar 0,73 ppm, hamburger III sebesar 1,39 ppm, dan kebab I sebesar 3,13 ppm.
2. Hasil optimasi dalam penentuan senyawa nitrosodipropilamin (NDPA) menggunakan teknik HS-SDME-GC-FID dapat dicapai pada kondisi yang optimum yakni dengan menggunakan pH 4, kecepatan pengadukan skala 6, dan suhu ekstraksi 30 °C.
3. Limit deteksi (LOD) dari teknik HS-SDME-GC-FID sebesar 78 ppb, persen recovery sebesar 101,18 %, presisi antara 0,089% sampai dengan 0,566%, dan true enrichment factor3372,66 kali.
5.2 Saran
DAFTAR PUSTAKA
Anonimus, 2011, N-Nitrosamines: 15 Listings Twelfth Edition, Report on Carcinogens, National Toxicology Program, Departemen of Health and Human Services
Adam, M., Dobiáš, P., Eisner, A., Ventura, K., 2008,Original Peper: Headspace Single-Drop Microextraction of Herbal Essential Oils, Original Paper, Departemen of Analytical Chemistry, Faculty of Chemical Technology, University of Pardubice
Andrade, R., Reyes, F.G.R., Rath S., 2005,A Method For The Determination of Volatile N-Nitrosamine in Food by HS-SPME-GC-TEA, J. Food Chem., 91: 173-179
Barus, P., 2009, Pemanfaatan Bahan Pengawet dan Antioksidan Alami pada Industri Bahan Makanan, Skripsi, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sumatera Utara, Medan
Battle, R., dan Nerin, C., 2004, Application of Single Drop Microextraction to The Determination of Dietil Phtalate Esters in Food Simultans, J. of Chrom. A, 1045, 29-35
Belitz, H.D., dan Grosch, W., 1999,Food Chemistry, Springer, Gerching
Cárdenes, L., Ayala, J.H., González, V., Afonso, A.M., 2002, Fast Microwave-Assisted Dansylation of N-Nitrosamines Analysis by High-Performance Liquid Chromatography with Fluorecence Detection, J. of Chrom. A, 946: 133-140
Cooper, M.T., dan Porter, T.D., 2000, Mutagenicity of Nitrosamines in Methyltranferase-Deficient Strains of Salmonella typhimurium Coexpressing Human Cytochrome P450 2E1 and Reductanse,Mutation Research, 454: 45-52
Cory S., M., 2009, Analisis Kandungan Nitrit dan Pewarna Merah pada Daging Burger yang Dijual Di Grosir Bahan Baku Burger Di Kota Medan Tahun 2009, Skripsi, Fakultas Kesehatan Masyarakat, Universitas Sumatera Utara, Medan
Domanska-Blicharz, K., Rachubik J., Kowalski, B., 2005, Occurrence of Volatile N-Nitrosamines in Polish Tinned Foods, Bull Vet Inst Pulawy, 49, 319-322
Dowdle, W., R., 1989, Toxicological Profile For N-Nitrosodi-n-Propylamine, Public Health Service US., US
Drabik-Markiewicz, G., Maagdenberg, K.V.D., Mey, E.D., Deprez, S., Kowalska, T., 2009, Role of Proline and Hydroxyproline in N-nitrosamines formation During Heating in Cured Meat, Meat Science, 81, 479-486 Filho, P.J.S., Rios, A., Valcárcel, M., Zanin, K.D., Caramão, E.B., 2003,
Development of a New Method for The Determination of Nitrosamines by Miceller Electrokinetic Capillary Chromatography,Water Research, 37: 3837-3842
Handajani, U., S., 2005, Kumpulan Materi Pelatihan Pengoperasian Instrumentasi Kimia, Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Airlangga, Surabaya
Hashemi, M., Habibi, A., Jahanshahi, N., 2011, Determination of Cyclamate in Artificial Sweeteners and Beverages Using Headspace Single-Drop Microextraction and Gas Chromatography Flame-Ionisation Detection, Food Chemistry, 124, 1258-1263
Hendayana, S., 2006, Kimia Pemisahan Metode Kromatografi dan Elektroforesis Modern, PT. Remaja Rosdakarya, Bandung
Hernani, dan Raharjo, M., 2005, Tanaman Berkhasiat Antioksidan, Penerbit Swadaya, Jakarta
Husni, E., Samah, A., Ariati, R., 2007, Analisa Zat Pengawet dan Protein dalam Makanan Siap Saji Sosis, Jurnal Sains dan Teknologi Farmasi, 12(2), 108-111
Grebel, J.E., Young, C.C., Suffet, I.H., 2006,Solid-Phase Microextraction of N-Nitrosamines,J. of Chrom. A, 1117, 11-18
Incavo, J.A., dan Schafer, M.A., 2006, Simplified Method for The Determination of N-Nitrosamines in Rubber Vulcanizates, Anal. Chim. Acta, 557, 256-261
Jurado-Sánchez, B., Ballesteros, E., Gallego, M., 2007, Comparison of The Sensitivities of Seven N-Nitrosamines in Pre-Screened Waters Using an Automated Preconcentration System and Gas Chromatography with Different Detectors, J. of Chrom. A, 1154, 66-73
Jurado-Sánchez, B., Ballesteros, E., Gallego, M., 2009, Comparison of Several Solid-Phase Extraction Sorbents for Continous Determination of Amines In Water by Gas Chromatography-Mass Spectrometry,Talanta, 1216, 1200-1205
Kamisa, 1997,Kamus Lengkap Bahasa Indonesia, Penerbit Kartika, Surabaya Lu, F., C., 1995, Toksikologi Dasar Edisi Kedua, Penerbit Universitas Indonesia,
Jakarta
Merck, 2007, Lembar Data Keselamatan Bahan Berdasarkan EC Directive 91/155/EEC, Katalog, Penerbit Merck
Merck, 2012, Lembar Data Keselamatan Bahan Menurut Peraturan (UE) No. 1907/2006, Katalog, Penerbit Merck
Miller, J.C., dan Miller, J.N., 1988, Statistics for Analytical Chemistry Second Edition, Elllis Horwood Limited, England
Pragdimurti, E., Zakaria, F.R., Palupi, N.S., 2007, Toksikan yang Terbentuk Karena Pengolahan Pangan,Modul e-learning ENBP topik 7, Departemen Ilmu dan Teknologi Pangan IPB, Bogor
Reche, F., Garrigós, M.C., Marín, M.L., Cantó, A., Jiménez, A., 2002, Optimization of Parameters for The Supercritical Fluid Extraction in The Determination of N-Nitrosamines in Rubbers, J. of Chrom. A, 963, 419-426
Riccio, D., Wood, D.C., Miller, J.M., 2008,Using Single Drop Microextraction for Headspace Analysis with Gas Chromatography, J. of Chem. Education, 85(7), 965-968
Rouessac, F., dan Rouessac, A., 2007, Chemical Analysis Modern Instrumentation Methods and Techniques 2ndEdition, Wiley, England
Sleiman, M., Maddalena, R.L., Gundel, L.A., and Destaillats, H., 2009, Rapid and Sensitive Gas Chromatography-Ion-Trap Tandem Mass Spectrometry Method for The Determination of Tobacco-Specific N-Nitrosamines in Secondhand Smoke, J. of Chrom. A, 1216, 7899-7905 Stalikas, C., 2007, Single-drop Microextraction Followed by In-drop
Derivatization for The Analysis of Organic Compounds by Gas Chromatography, ISSN-1996-918X, Pak. J. Anal. Environ. Chem. 8(1-2), 72-74
Sunaryanto, R., Marwoto, B., Matsuo, Y., 2010, Isolasi Actinomycetes Laut Penghasil Metabolit Sekunder yang Aktif Terhadap Sel Kanker A549, Jurnal Pascapanen dan Bioteknologi Kelautan dan Perikanan, 5(2), 111-116
Tjindarbumi, D., dan Mangunkusumo, R., 2001, Cancer in Indonesia, J. Clin. Oncol., 32(1), 17-21
Utomo, P., dan Priyanto, R., 2010, Pemurnian Etanol Teknis Menjadi Etanol Absolut Secara Batch dan Kontinyu dengan Adsorbent Tepung Jagung, Artikel Ilmiah, Jurusan Teknik Kimia, Fakultas Teknik, Universitas Diponegoro
Valentinavičiūtė, R., Prichodko, A., Vičkačkaitė, V., 2008, Single Drop Microextraction and Gas Chromatographic Determination of Volatile Halogenated Hydrocarbons, Chemija, 19, 38-42
Ventanas, S., dan Ruiz, J., 2006,On-Site Analysis of Volatile Nitrosamines in Food Model Systems by Solid-Phase Michroextraction Couples to a Dirct Extraction Device,Talanta, 70, 1017-1023
Lampiran 1 : Pembuatan Larutan NDPA 99,9 % dengan metanol hingga 100 mL.
b. Pembuatan Larutan Standar NDPA 2 ppm, 4 ppm, 6 ppm, 8 ppm, dan 10 ppm
1. Pembuatan larutan standar NDPA 2 ppm V1x N1 = V2x N2
V1x 50 ppm = 10 mL x 2 ppm