1 1.1 Latar Belakang
Kondisi suatu wilayah pesisir erat kaitannya dengan sistem suatu sungai
yang bermuara ke wilayah itu. Oleh karena itu, wilayah pesisir secara alami
merupakan bagian yang tidak terpisahkan dari suatu sistem aliran sungai
(Supriharyono, 2007). Sungai merupakan perairan yang memiliki peran penting
bagi makhluk hidup. Keberadaan ekosistem sungai dapat memberikan manfaat
bagi makhluk hidup, baik yang hidup didalam sungai maupun yang ada
disekitarnya. Kegiatan manusia sebagai bentuk kegiatan pembangunan akan
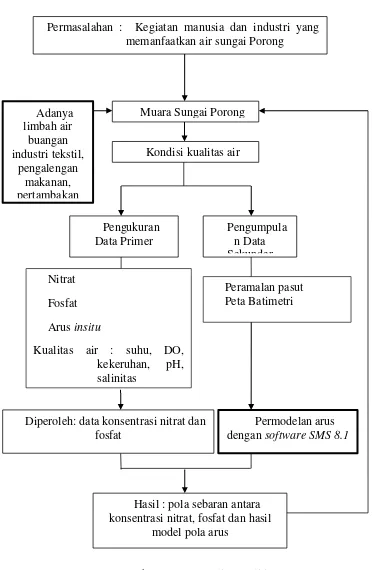
berdampak pada perairan sungai. Adanya kegiatan manusia dan industri yang
memanfaatkan air sungai sebagai tempat untuk membuang limbah akan
berdampak pada penurunan kualitas air, yaitu perubahan kondisi fisika, kimia dan
biologi (Sastrawijaya, 1991). Sungai akan memperoleh masukan bahan maupun
energi yang berasal dari wilayah sepanjang aliran sungai atau segala aktivitas
manusia yang berkaitan dengan produksi limbah dan kemudian dialirkan melalui
badan-badan sungai. Pembangunan industri di daerah permukiman sepanjang
aliran sungai memberikan masukan bahan-bahan pencemar bagi perairan sungai
yang pada akhirnya akan dialirkan ke muara (Santoso, 2007).
Pesisir Sidoarjo secara umum dialiri sejumlah sungai, salah satunya adalah
sungai Porong. Sungai Porong yang terletak di Kabupaten Sidoarjo Provinsi Jawa
Menurut Supriharyono (2007) muara sungai Porong merupakan perairan yang
sangat dipengaruhi oleh kegiatan manusia terutama dari daratan. Pemasukan air
dari darat cukup banyak karena adanya aliran sungai yang bermuara di Sungai.
Unsur-unsur hara yang berasal dari daratan dan aktivitas manusia yang masuk ke
dalam sungai akan terbawa oleh aliran sungai, sehingga mencapai ke muara
sungai. Aliran tersebut menyebabkan dampak terhadap lingkungan sekitarnya,
karena unsur-unsur hara akan mengendap di daerah muara. Masuknya limbah air
buangan dari indusri tekstil, industri pengalengan makanan, home industri, kegiatan pertambakan ikan dan pemukiman penduduk menyebabkan daerah
muara tersebut banyak mengandung unsur hara nitrat, fosfat dan zat organik lain.
Nitrat dan fosfat menyebar ke berbagai arah, dan pola sebaran ke dua unsur
tersebut sangat dipengaruhi oleh arah arus ke muara. Bagaimanakah pola atau
arah sebaran unsur nitrat dan fosfat di daerah muara, maka perlu dilakukan
penelitian tentang sebaran nitrat dan fosfat di perairan muara sungai Porong
Kabupaten Sidoarjo.
1.2 Pendekatan Masalah
Limbah atau buangan yang mengandung unsur hara (nitrat dan fosfat) akan
terbawa oleh aliran sungai Porong dan mencapai ke daerah muara. Nitrat dan
fosfat yang terdapat di muara sungai akan menyebar ke berbagai arah. Pola atau
arah sebaran akan sangat dipengaruhi oleh fenomena oseanografi terutama pola
fosfat perlu dilakukan pengolahan dengan software ArcGIS 10.1 dan permodelan arus dengan software SMS 8.1.
1.3 Tujuan Penelitian
Tujuan dari penelitian ini adalah untuk mengetahui konsentrasi dan arah
sebaran konsentrasi nitrat (N-NO3-) dan fosfat (P-PO4-) pada saat surut di perairan
muara Sungai Porong, Kabupaten Sidoarjo.
1.4 Manfaat Penelitian
Manfaat yang didapatkan dari penelitian ini adalah didapatkannya data
mengenai arah sebaran nitrat dan fosfat sebagai indikator produktivitas perairan
pesisir melalui parameter fisika kimia perairan yang diharapkan dapat menjadi
bagian penting dalam pengambilan keputusan dalam pengelolaan kawasan pesisir
dan muara Sungai Porong dengan mempertimbangkan seluruh aspek yang terlibat.
1.5 Waktu dan Tempat Penelitian
Waktu penelitian dilaksanakan pada 18-31 Desember 2013. Lokasi
penelitian berada di wilayah muara Sungai Porong, Kabupaten Sidoarjo, Provinsi
II.
TINJAUAN PUSTAKA
2.1. Unsur Hara dan Kesuburan Perairan
Senyawa kimia yang terdapat di laut sangat kompleks, baik zat-zat organik
maupun anorganik. Beberapa senyawa dari zat tersebut sangat dibutuhkan untuk
perkembangan populasi mahluk hidup dilaut yang selanjutnya disebut sebagai zat
hara (nutrien). Unsur hara adalah suatu unsur yang mempunyai peranan dalam
melestarikan kehidupan karena dimanfaatkan oleh fitoplankton dalam
peningkatan pertumbuhan yang mendukung produktivitas primer. Nitrat dan
fosfat merupakan unsur hara yang penting bagi pertumbuhan dan metabolisme
fitoplankton yang merupakan indikator untuk mengevaluasi kualitas dan tingkat
kesuburan perairan (Fachrul et al., 2005).
Kesuburan perairan adalah deskripsi kualitatif yang menyatakan
konsentrasi unsur hara yang terdapat dalam suatu badan air. Penelitian yang
dilakukan dari berbagai belahan bumi menemukan bahwa unsur hara anorganik
utama yang diperlukan fitoplankton untuk tumbuh dan berkembang biak adalah
fosfat dan nitrat sebagai komponen penyusun jaringan fitoplankton melalui
sintetis zat organik dalam aktivitas metabolisme. Menurut Chester (2003), proses
penguraian senyawa organik terjadi melalui aktivitas bakteri dan organisme
pengurai lainnya, mengalami dekomposisi menjadi senyawa anorganik dan
dimanfaatkan oleh organisme autotrof. Kandungan nutrien (nitrat dan fosfat) yang
diperoleh dari proses penguraian tersebut memacu pertumbuhan fitoplankton dan
2.2. Nitrat Dalam Perairan
Nitrat (NO3-) adalah bentuk utama nitrogen di perairan alami dan
merupakan nutrien utama bagi pertumbuhan tanaman dan alga. Nitrat sangat
mudah larut dalam air dan bersifat stabil. Senyawa ini dihasilkan dari proses
oksidasi sempurna senyawa nitrogen di perairan. Nitrifikasi yang merupakan
proses oksidasi ammonia menjadi nitrit dan nitrat adalah proses yang penting
dalam siklus nitrogen dan berlangsung pada kondisi aerob. Menurut Imas (1989),
nitrifikasi merupakan proses nitrit mengalami oksidasi menjadi nitrat. Sementara
Jenie (1993) menyebutkan, bahwa dalam sistem biologi, senyawa nitrogen
organik dapat ditransformasikan menjadi amonia dan dioksidasi menjadi nitrit dan
nitrat. Oksidasi amonia menjadi nitrit dan nitrat disebut nitrifikasi dan
berlangsung dalam kondisi aerobik. Konsentrasi nitrat di suatu perairan selain
berasal dari proses nitrifikasi nitrit, juga berasal dari masukan limbah rumah
tangga, limbah pertanian yang berupa sisa pemupukan, limbah peternakan sisa
dari pakan, pengikatan nitrogen bebas dari udara oleh mikroorganisme dan aliran
tanah yang masuk ke laut (Wardoyo, 1982).
Oksidasi ammonia menjadi nitrit dilakukan oleh bakteri Nitrosomonas
sedangkan oksidasi nitrit menjadi nitrat dilakukan oleh bakteri Nitrobacter. Kedua jenis bakteri tersebut merupakan bakteri kemotrofik, yaitu bakteri yang yang
mendapatkan energi dari proses kimiawi. Oksidasi nitrit menjadi ammonia
ditunjukkan oleh persamaan berikut : 2NH3 + 3O2 nitrosomonas 2NO2-+ 2H+ + 2H2O
sedangkan oksidasi nitrit menjadi nitrat ditujukkan oleh persamaan : 2NO2- + O2
nitrobakter
Nitrogen di air laut berada dalam bentuk nitrogen molekuler (N2) atau
sebagai garam-garam anorganik seperti nitrat (NO3-), nitrit (NO2-), amonium
(NH4+) dan beberapa senyawa nitrogen organik seperti urea dan asam-asam
amino. Nitrogen yang terdapat di laut selain berasal dari udara dan laut itu sendiri,
juga berasal dari limbah domestik dan industri, hujan serta dari bahan-bahan
organik yang dialirkan oleh sungai (Susana, 1987). Sementara menurut Sidjabat
(1973) menyatakan, bahwa senyawa-senyawa nitrogen dalam air laut terdapat
dalam bentuk gas nitrogen terlarut dan nitrogen yang terikat pada
senyawa-senyawa organik maupun anorganik.
Nitrat di alam didapatkan dari hasil siklus nitrogen, sehingga dalam
pembahasan tentang nitrat tidak terlepas dari unsur nitrogen. Pada umumnya
senyawa nitrogen organik terlarut dalam bentuk hasil metabolisme organisme
bahari dan hasil proses pembusukan. Nitrogen terdapat juga dalam bentuk
molekul-molekul protein pada organisme yang telah mati kemudian diuraikan
menjadi bentuk-bentuk anorganik oleh serangkaian organisme pengurai, terutama
bakteri pembusuk nitrat. Bentuk organik dapat berasal dari hasil metabolisme
organisme bahari dan hasil pembusukan, sedangkan yang berbentuk zarah
(particulate) dari reruntuhan sedimen, binatang dan tumbuhan laut (Koesoebiono,
1980).
Senyawa nitrat umumnya berada dalam kondisi terlarut sebagai hasil
metabolisme oragnisme laut dan hasil pembusukan. Bentuk nitrat yang berupa
molekul-molekul protein terdapat pada organisme mati kemudian diuraikan
di laut yang digunakan sebagai penyusun jaringan lunak plankton dan
pembentukan protoplasma. Menurut Millero dan Sohn (1992), proses biologi dan
fisika di laut mempengaruhi keberadaan nitrat dilaut.
Menurut Millero dan Sohn (1992), keberadaan nitrat di lapisan permukaan
laut juga diatur oleh proses biologi dan fisika. Pemanfaatan nitrat oleh
fitoplankton terjadi selama berlangsung proses fotosintesis dan tergantung pada
intensitas sinar matahari. Proses regenerasi NO3- sebagian oleh bakteri
pengoksidasi dari nitrogen organik, yang kemudian melepaskan NH4+dan PO42-
selanjutnya NH4+ akan mengalami oksidasi menjadi NO3-.
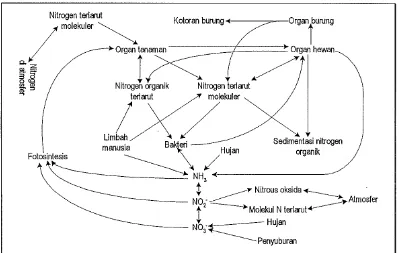
Pada siklus nitrogen (Gambar 1) terdapat dua bagian (Pescod, 1973),
yaitu:
a. Pemanfaatan nitrat oleh fitoplankton melalui proses fotosintesis yang
menghasilkan asam-asam amino.
b. Proses regenerasi, yaitu proses bakterial senyawa-senyawa organik yang
mengandung nitrogen dirombak menjadi amonia yang kemudian diubah
Gambar 1. Siklus nitrogen di laut (Millero dan Sohn, 1992)
2.3. Fosfat Dalam Perairan
Menurut Romimohtarto dan Juana (2003), fosfat merupakan unsur yang
sangat esensial sebagai bahan nutrien bagi berbagai organisme akuatik. Fosfat
merupakan salah satu zat hara yang diperlukan dan mempunyai pengaruh terhadap
pertumbuhan dan perkembangan hidup organisme di laut (Nybakken, 1992).
Sumber fosfat di perairan laut pada wilayah pesisir dan paparan benua
adalah sungai. Karena sungai membawa hanyutan sampah maupun sumber fosfat
daratan lainnya, sehingga sumber fosfat dimuara sungai lebih besar dari
sekitarnya. Keberadaan fosfat di dalam air akan terurai menjadi senyawa ionisasi
antara lain dalam bentuk ion H2PO4-, HPO42-, PO43-. Fosfat diabsorpsi oleh
antropogenik fosfor adalah dari limbah industri dan limbah domestik, yakni
berasal dari deterjen (Effendi, 2003).
Fosfat dalam air laut berbentuk ion fosfat. Ion fosfat dibutuhkan pada
proses fotosintesis dan proses lainnya dalam tumbuhan (bentuk ATP dan
nukleotid koenzim). Penyerapan dari fosfat dapat berlangsung terus walaupun
dalam keadaan gelap. Ortofosfat (H3PO4-) adalah bentuk fosfat anorganik yang
paling banyak terdapat dalam siklus fosfat. Distribusi bentuk yang beragam dari
fosfat di air laut dipengaruhi oleh proses biologi dan fisik. Di permukaan air,
fosfat di angkut oleh fitoplankton sejak proses fotosintesis. Di perairan unsur
fosfor tidak ditemukan dalam bentuk bebas sebagai elemen, melainkan dalam
bentuk senyawa anorganik yang terlarut (ortofosfat dan polifosfat) dan senyawa
organik yang berupa partikulat (Effendi, 2003).
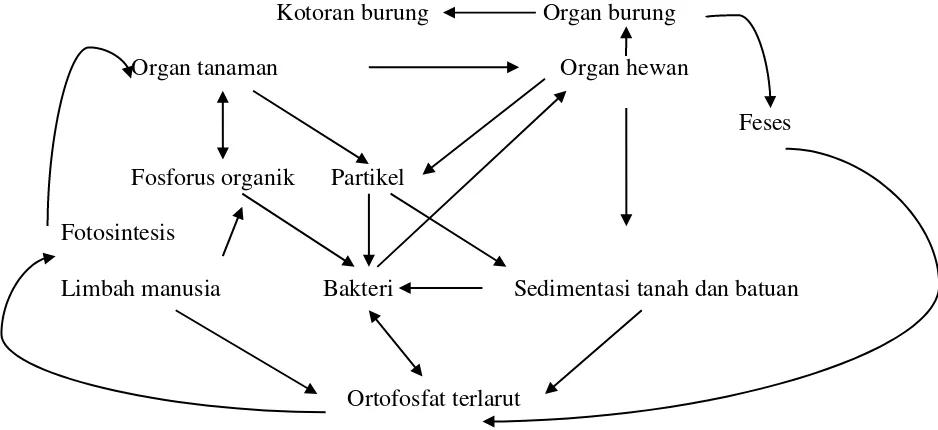
Kotoran burung Organ burung
Organ tanaman Organ hewan
Feses
Fosforus organik Partikel
Fotosintesis
Limbah manusia Bakteri Sedimentasi tanah dan batuan
Ortofosfat terlarut
Fosfor tidak bersifat toksik bagi manusia, hewan dan ikan. Keberadaan
fosfor secara berlebihan yang disertai dengan keberadaan nitrogen dapat
menstimulir ledakan pertumbuhan algae di perairan (algae bloom). Algae yang berlimpah ini dapat membentuk lapisan pada permukaan air yang selanjutnya
dapat menghambat penetrasi oksigen dan cahaya matahari sehingga kurang
menguntungkan bagi ekosistem perairan. Pada saat perairan cukup mengandung
fosfor, algae mengakumulasi fosfor di dalam sel melebihi kebutuhannya.
Fenomena ini dikenal istilah konsumsi berlebih (luxury consumption). Kelebihan fosfor yang diserap akan dimanfaatkan pada saat perairan mengalami defisiensi
fosfor sehingga algae masih dapat hidup untuk beberapa waktu selama periode
kekurangan pasokan fosfor (Effendi, 2003).
Damanhuri (1997) menyatakan, bahwa kadar fosfat akan semakin tinggi
dengan menurunnya kedalaman. Biasanya terjadi pengendapan sehingga nutrien
meningkat seiring dengan waktu karena proses oksidasi P dan bahan organik.
Adanya proses run off yang berasal dari daratan akan mensuplai kadar fosfat pada lapisan permukaan. Konsentrasi fosfat relatif konstan pada perairan dalam, tetapi
ini tidak terlalu besar. Penambahan terbesar dari lapisan dalam melalui proses
kenaikan massa.
2.4. Faktor Lingkungan Perairan
Faktor lingkungan perairan yang mempengaruhi konsentrasi nitrat dan
2.4.1. Salinitas
Salinitas adalah garam-garaman terlarut dalam satu kilogram air laut dan
dinyatakan dalam satuan perseribu (Nybakken, 1993). Salinitas merupakan
indikator utama untuk mengetahui penyebaran massa air laut sehingga
penyebaran nilai-nilai salinitas secara langsung menunjukkan penyebaran dan
peredaran massa air dari satu tempat ke tempat lainnya. Menurut Dahuri
(2001), secara umum salinitas permukaan perairan Indonesia rata-rata berkisar
antara 32-34 per mil. Nilai salinitas sangat dipengaruhi oleh suplai air tawar ke air
laut, curah hujan, musim, topografi, pasang surut dan evaporasi (Nybakken,
1993). Ditambahkan pula oleh Nontji (1987), bahwa sebaran salinitas dipengaruhi
oleh berbagai faktor seperti pola sirkulasi air, penguapan, dan aliran sungai.
Daerah yang mengalami penguapan cukup tinggi akan mengakibatkan
salinitas perairan yang tinggi. Salinitas air laut juga akan semakin tinggi dengan
bertambahnya kedalaman. Perbedaan terbesar terjadi pada kedalaman 100-1000
meter. Selain beberapa hal di atas perubahan salinitas juga dapat disebabkan oleh
pola sirkulasi massa air dan aliran sungai. Perubahan salinitas di perairan bebas
lebih kecil dibandingkan dengan perairan dangkal. Perubahan ini disebabkan
karena perairan pantai banyak dipengaruhi oleh massa air tawar terutama pada
musim hujan. Nilai kisaran salinitas di perairan laut terbuka secara umum
bervariasi antara 33 psu sampai 37 psu dengan nilai rata-rata 35 psu (Ross, 1970
dalam Rosmawati, 2004). Satuan psu dalam menuliskan nilai salinitas merupakan singkatan dari “practical salinity unit”. Karena salinitas praktis adalah rasio, maka
sebenarnya tidak mengandung makna apapun dan tidak diperlukan (Kalujnaia., et al 2007).
Tinggi rendahnya kadar garam (salinitas) sangat tergantung kepada banyak
sedikitnya sungai yang bermuara di laut tersebut, makin banyak sungai yang
bermuara ke laut tersebut maka salinitas laut tersebut semakin rendah dan
sebaliknya makin sedikit sungai yang bermuara ke laut tersebut maka salinitasnya
akan tinggi (Prasetyarto dan Suhendar, 2010 dalam Dewi, 2011).
2.4.2. Suhu
Suhu air laut merupakan salah satu faktor abiotik yang sangat berperan
dalam kehidupan dan pertumbuhan organimse perairan. Perubahan suhu pada
perairan alami terjadi karena adanya pemanasan oleh radiasi matahari yang
menembus lapisan air. Secara langsung suhu ini akan mempengaruhi organisme
fitoplankton dalam aktifitas fotosintesis dan kelarutan berbagai macam gas
(Boney, 1976). Hutabarat dan Evans (1985) menambahkan, bahwa suhu sebagai
salah satu faktor yang sangat penting bagi kehidupan organisme di laut karena
suhu mempengaruhi baik aktivitas metabolisme maupun perkembangbiakan dari
organisme-organisme tersebut.
Suhu di laut adalah faktor yang amat penting bagi kehidupan organisme
(Nybakken, 2000). Faktor-faktor yang mempengaruhi suhu air antara lain
komposisi substrat, kekeruhan, air hujan, luas permukaan perairan yang langsung
mendapat sinar matahari serta perairan yang menerima pasokan air (Nybakken,
1992). Selain itu suhu suatu badan air juga dipengaruhi oleh musim, lintang,
dan aliran serta kedalaman badan air.Suhu juga sangat berperan mengendalikan
kondisi ekosistem perairan.Perubahan suhu berpengaruh terhadap proses fisika,
kimia dan biologi badan air (Effendi,2003). Naiknya suhu air yang berubah lebih
hangat menyebabkan organisme perairan mengalami peningkatan laju respirasi
dan peningkatan konsumsi oksigen serta lebih mudah terkena penyakit, parasit
dan bahan kimia beracun (Haryono dan Badrus, 2004).
Secara alami suhu air permukaan merupakan lapisan hangat karena
mendapat radiasi matahari pada siang hari. Karena pengaruh angin, maka di
lapisan teratas sampai kedalaman kira-kira 50-70 m terjadi pengadukan, hingga di
lapisan tersebut terdapat suhu hangat (sekitar 28°C) yang homogen. Oleh sebab
itu lapisan teratas ini sering pula disebut lapisan homogen. Karena adanya
pengaruh arus dan pasang surut, lapisan ini bisa menjadi lebih tebal lagi. Di
perairan dangkal lapisan homogen ini sampai ke dasar (Nining, 2002).
Tingginya suhu memudahkan terjadinya penyerapan nutrien oleh
fitoplankton. Dalam kondisi konsentrasi fosfat sedang di dalam kolom perairan,
laju fotosintesis maksimum akan meningkat pada suhu yang lebih tinggi
(Brotowidjoyo dan Ruyitno, 1995).
2.4.3. Kekeruhan
Kekeruhan (turbiditas) adalah gambaran sifat optik air dari suatu perairan
yang ditentukan berdasarkan banyaknya cahaya yang dipancarkan dan diserap
Kekeruhan pada sungai lebih banyak disebabkan oleh bahan-bahan
tersuspensi yang berukuran lebih besar berupa lapisan permukaan tanah yang
terletak oleh aliran air pada saat hujan. Padatan tersuspensi mempengaruhi
kekeruhan dan kekeruhan sangat berpengaruh terhadap proses fotosintesis.
Menurut Davis dan Comwell (1991), kekeruhan menggambarkan sifat optik air
yang ditentukan berdasarkan banyaknya cahaya yang diserap dan dipancarkan
oleh bahan-bahan yang terdapat dalam air. Semakin banyak partikel atau bahan
organik terlarut maka kekeruhan akan meningkat. Perairan yang mempunyai
kekeruhan yang tinggi akan mengurangi penetrasi cahaya ke dalam kolom air
sehingga membatasi proses fotosintesis dan produktivitas perairan berkurang.
2.4.4. Derajat Keasaman (pH)
Nilai derajat keasaman (pH) suatu perairan mencirikan keseimbangan
antara asam dan basa dalam air dan merupakan pengukuran konsentrasi ion
hidrogen dalam larutan. Sebagian besar biota akuatik sensitif terhadap perubahan
pH dan menyukai nilai pH sekitar 7-8,5 (Effendi, 2003).
Air laut umumnya memiliki nilai pH diatas 7 yang berarti basa, namun
dalam kondisi tertentu nilainya dapat menjadi rendah sehingga menjadi bersifat
asam. pH merupakan variabel kualitas air yang dinamis dan berfluktuasi
sepanjang hari sehingga perubahan nilai pH yang demikian berpengaruh terhadap
kualitas perairan yang pada akhirnya berdampak terhadap kehidupan biota di
dalamnya. Banyaknya buangan yang berasal dari rumah tangga dan
Biasanya angka pH dalam suatu perairan dapat dijadikan indikator dari
adanya keseimbangan unsur-unsur kimia dan dapat mempengaruhi ketersediaan
unsur-unsur kimia dan unsur-unsur hara yang sangat bermanfaat bagi kehidupan
vegetasi akuatik. Tinggi rendahnya pH dipengaruhi oleh fluktuasi kandungan O2
dan CO2.
Perairan dengan pH < 4 merupakan perairan yang sangat asam dan dapat
menyebabkan kematian makhluk hidup. Adapun pH > 9,5 merupakan perairan
yang sangat basa yang dapat menyebabkan kematian dan mengurangi
produktivitas perairan. Perairan laut maupun pesisir memiliki pH relatif lebih
stabil dan berada dalam kisaran yang sempit, biasanya berkisar antara 7,7-8,4. pH
dipengaruhi oleh kapasitas penyangga (buffer), yaitu adanya garam-garam karbonat dan bikarbonat yang dikandungnya (Nybakken, 1993).
Satino (2010) menjelaskan bahwa air yang agak basa dapat mendorong
proses perombakan atau penguraian bahan organik yang ada dalam air menjadi
mineral-mineral yang dapat diasimilasi oleh tumbuhan dan fitoplankton sehingga
pH ikut berperan dalam menentukan produktivitas perairan. Perairan yang baik
untuk fitoplankton adalah pH normal, yaitu 7,0 atau mendekati basa, karena
perairan dengan pH tinggi (7-9) merupakan perairan yang produktif dan berperan
mendorong bahan organik dalam air menjadi mineral-mineral yang dapat
diasimilasikan oleh fitoplankton. Penggolongan nilai pH bila dihubungkan dengan
tipe kesuburan perairan maka perairan dengan pH 4-5 termasuk tipe perairan
oligotrofik, pH 5-7 termasuk tipe perairan mesotrofik dan pH 7-9 termasuk tipe
2.4.5. Oksigen Terlarut (DO)
DO atau Dissolved Oxygen atau oksigen terlarut adalah parameter kimia perairan yang menunjukkan banyaknya oksigen yang terlarut dalam ekosistem
perairan. Odum (1971) berpendapat, bahwa kadar oksigen dalam air laut akan
bertambah dengan semakin rendahnya suhu dan berkurang dengan semakin
tingginya salinitas dan dimanfaatkan untuk respirasi, dekomposisi kimia di dalam
air. Jumlah oksigen dalam air bervariasi sesuai dengan variasi parameter
lingkungan. Semakin besar ketinggian (latitude) serta semakin kecil tekanan
atmosfer, kadar oksigen terlarut juga semakin kecil (Effendi, 2003).
Oksigen terlarut dibutuhkan oleh semua jasad hidup untuk pernapasan,
proses metabolisme atau pertukaran zat yang kemudian menghasilkan energi
untuk pertumbuhan dan pembiakan. Sumber utama oksigen dalam suatu perairan
berasal dari suatu proses difusi dari udara bebas dan hasil fotosintesis organisme
yang hidup dalam perairan tersebut (Salmin, 2005).
Oksigen memegang peranan penting sebagai indikator kualitas perairan,
karena oksigen terlarut berperan dalam proses oksidasi dan reduksi bahan organik
dan anorganik. Selain itu, oksigen juga menentukan biologis yang dilakukan oleh
organisme aerobik atau anaerobik. Dalam kondisi aerobik, peranan oksigen adalah
untuk mengoksidasi bahan organik dan anorganik dengan hasil akhirnya adalah
nutrien yang pada akhirnya dapat meningkatkan kesuburan perairan (Salmin,
2.5. Faktor Hidro-Oseanografi
Arus adalah pergerakan massa air atau partikel air dari tempat yang satu ke
tempat yang lain di suatu perairan. Arus adalah gerakan massa air yang arah
gerakannya horizontal maupun vertikal. Arus sungai adalah gerakan massa air
sungai yang arahnya searus dengan aliran sungai menuju hilir atau muara. Faktor
yang mempengaruhi arus, yaitu tahanan dasar, gaya Coriolis, perbedaan densitas
(Wibisono, 2005).
Arus dapat dibedakan dalam 2 kategori, yaitu: arus permukaan (surface current) dan arus dalam (subsurface current). Arus permukaan dibangkitkan dari berbagai proses, termasuk di dalamnya adalah akibat gesekan angin dan
perbedaan densitas karena pemanasan matahari. Arus permukaan ini bergerak
secara horizontal sedangkan arus dalam yang dikenal dengan termohalin
merupakan pergerakan arus yang disebabkan oleh adanya perbedaan temperatur
dan salinitas. Arus ini dapat disebut juga arus densitas karena arus ini digerakkan
oleh gradien densitas air. Arus termohalin ini pergerakannya secara vertikal.
Menurut Hutabarat dan Evans (1985), faktor pembangkit arus permukaan
adalah:
1. Bentuk topografi pulau-pulau sekitarnya
Beberapa sistem lautan utama dunia dibatasi oleh massa daratan dari tiga
sisi dan juga oleh equatorial current disisi yang keempat. Batas-batas ini menghasilkan sistem aliran yang hampir tertutup dan cenderung membuat
2. Gaya Coriolis dan arus Ekman
Gaya Coriolis mempengaruhi aliran massa air, gaya ini akan membelokan arah arus dari arah yang lurus. Gaya ini timbul sebagai akibat dari
perputaran bumi pada porosnya. Pembelokan ini dibelahan bumi utara
mengarah kekanan dan dibelahan bumi selatan mengarah ke kiri.
Stress angin yang bekerja pada permukaan laut akan mendorong lapisan permukaan dan gerakan lapisan permukaan ini akan mendorong lapisan
dibawahnya dan begitu seterusnya, sehingga terbentuk arus permukaan sampai
kedalaman 100-300 m. Arus yang terjadi di perairan laut dapat dipisahkan
menjadi arus pasut dan arus residual, peran arus pasut di daerah estuari cenderung
lebih dominan dibandingkan dengan arus residu (Surbakti, 2012).
Arus pasut adalah pergerakan massa air laut secara horisontal yang
dihubungkan dengan naik turunnya permukaan air laut akibat gaya tarik
benda-benda angkasa terutama bulan dan matahari. Pada waktu pasang di suatu perairan
muara arus laut akan bergerak memasuki muara. Sebaliknya arus bergerak dalam
arah yang berlawanan (keluar muara) pada saat surut. Arus pasut memiliki sifat
bergerak dengan arah yang saling tolak belakang (bi-directional). Arah arus saat air meninggi biasanya bertolak belakang dengan arah arus saat air merendah.
Kecepatan arus pasut minimum atau efektif nol terjadi saat air tinggi atau air
rendah (slack waters), pada saat-saat tersebut pasut minimum terjadi saat-saat antara air tinggi dan air rendah. Dengan demikian, perioda kecepatan arus pasut
Pasang surut merupakan suatu fenomena pergerakan naik turunnya
permukaanair laut secara berkala yang diakibatkan oleh kombinasi gaya gravitasi
dan gaya tarik benda-benda astronomi terutama oleh bumi, bulan dan matahari.
Pengaruh benda angkasa lainnya dapat diabaikan karena jaraknya lebih jauh dan
ukurannya lebih kecil. Faktor non astronomi yang mempengaruhi pasang surut
terutama di perairan semi tertutup seperti teluk adalah bentuk garis pantai dan
topografi dasar perairan (Musrifin, 2011).
Pada tipe pasut harian tunggal arus pasut yang terjadi adalah harian
tunggal sedangkan untuk tipe pasut harian ganda maka arus pasutnya akan
mengalami dua kali perubahan arah arus dalam satu hari. Pasut campuran arahnya
akan mengalami perubahan dalam interval sekali sampai dua kali sehari. Pada saat
elevasi pasut mencapai titik tertinggi (maksimum) dan terendah (minimum) maka
laju arus akan sama dengan nol. Laju arus maksimum terjadi pada saat elevasinya
sama dengan nol. Arus pasut akan mengalami perubahan arah setelah elevasi
pasut mencapai minimum atau maksimum (Wyrtki, 1961).
Energi pasang dari laut akan berkurang sebanding dengan berkurangnya
kedalaman. Ketika memasuki estuari air sungai didesak ke atas sehingga alirannya
menjadi relatif terhenti saat puncak pasang tertinggi selama beberapa saat. Ini
berarti permukaan air sungai sama tinggi dengan permukaan air laut dimana
kecepatan aliran dari kedua belah pihak menjadi nol. Sebaliknya kecepatan air
sama dengan nol juga terjadi pada saat air rendah. Suatu titik yang berada di
tengah antara air tinggi dan air rendah mempunyai kecepatan alir terbesar (Danial,
Kecepatan arus saat kondisi perbani tidak sebesar saat kondisi purnama,
hal ini disebabkan karena saat kondisi purnama gaya tarik bulan dan matahari
mencapai maksimum sehingga selain menyebabkan muka air laut mengalami
kenaikan tertinggi juga menyakibatkan pergerakan arus yang disebabkan oleh
pasang surut menjadi maksimal maka kecepatan arus yang terjadi menjadi besar,
sedangkan saat kondisi perbani gaya tarik bulan dan matahari menjadi minimum
sehingga muka air laut mengalami kenaikan terendah hal ini menyakibatkan
pergerakan arus pasut menjadi minimal maka kecepatan arus yang terjadi menjadi
kecil (Atmodjo, 2011).
2.6. Pemodelan Pergerakan Arus Dengan Program SMS
Program SMS ini dirancang untuk mensimulasikan kondisi oseanografi
yang terjadi di alam ke dalam sebuah model satu dimensi, dua dimensi, atau tiga
dimensi dengan finite element method (metode elemen hingga). Model yang dipakai untuk membuat simulasi pola arus yang terjadi pada lokasi studi adalah
ADCIRC. Pemodelan dengan ADCIRC berdasarkan finite element methode
(metode elemen hingga) untuk memperoleh simulasi pola arus dan pasang surut.
Parameter yang mempengaruhi pola arus dan pasang surut adalah kedalaman
nodal, periode gelombang, bentuk garis pantai, garis boundary dan posisi matahari dan bulan.
Menggunakan peta batimetri dapat diketahui kedalaman nodal, bentuk
cepat-rambat gelombang, sedangkan panjang gelombang di laut dangkal dapat
diketahui dari data periode gelombang.
Data yang dibutuhkan untuk menjalakan model ADCIRC yaitu:
1. Peta batimetri lokasi studi
III.
MATERI DAN METODE
3.1. Keadaan Umum Muara Sungai Porong Sidoarjo
Kabupaten Sidoarjo memiliki luas wilayah sebesar 714.243 km2 yang
terbagi dalam 353 Kelurahan/Desa dan 18 Kecamatan. Secara administratif
Kabupaten Sidoarjo dibatasi oleh:
Sebelah Utara berbatasan dengan Kota Surabaya dan Kabupaten
Gresik
Sebelah Selatan berbatasan dengan Kabupaten Pasuruan
Sebelah Barat berbatasan dengan Kabupaten Mojokerto
Sebelah Timur berbatasan dengan Selat Madura
Geomorfologi daerah Sidoarjo dapat dibedakan menjadi dua macam, yaitu
daerah pegunungan yang menempati bagian selatan, dan daerah dataran yang
menempati bagian utara. Daerah dataran terdapat di bagian utara dengan
ketinggian mencapai 15-18 m dpl merupakan delta dikenal sebagai delta Brantas
yang terbentuk oleh sungai Surabaya yang mengalir di bagian utara ke Kota
Surabaya dan sungai Porong yang mengalir di bagian selatan. Ke dua sungai ini
merupakan anak dari sungai Brantas. Sungai Porong merupakan anak dari sungai
Brantas yang termasuk sungai terbesar di Jawa Timur, sungai-sungai tersebut
memasok sejumlah besar angkutan sedimen yang terbawa dari daratan, sehingga
mempengaruhi banyak hal di perairan muara sungai Porong, seperti
3.2. Waktu dan Lokasi Penelitian
Penelitian ini dilakukan di perairan muara sungai Porong Kabupaten
Sidoarjo. Lokasi penelitian terletak di perairan Selat Madura dan secara geografis
terletak pada 112°53'10.98" BT dan 7°34'40.50" LS. Pelaksanaan survei lapangan
dilakukan pada tanggal 4-6 November 2013 dan pelaksanaan penelitian dilakukan
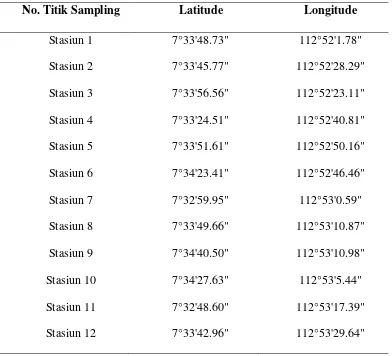
pada tanggal 18 Desember 2013. Lokasi pengamatan dan koordinat titik sampling
tersaji dalam Tabel 1:
Tabel 1. Lokasi pengambilan sampel
No. Titik Sampling Latitude Longitude
Stasiun 1 7°33'48.73" 112°52'1.78"
Stasiun 2 7°33'45.77" 112°52'28.29"
Stasiun 3 7°33'56.56" 112°52'23.11"
Stasiun 4 7°33'24.51" 112°52'40.81"
Stasiun 5 7°33'51.61" 112°52'50.16"
Stasiun 6 7°34'23.41" 112°52'46.46"
Stasiun 7 7°32'59.95" 112°53'0.59"
Stasiun 8 7°33'49.66" 112°53'10.87"
Stasiun 9 7°34'40.50" 112°53'10.98"
Stasiun 10 7°34'27.63" 112°53'5.44"
Stasiun 11 7°32'48.60" 112°53'17.39"
3.3. Materi Penelitian
Materi yang digunakan dalam penelitian ini adalah data primer dan data
sekunder. Data primer yang digunakan adalah data hasil pengukuran selama
pengambilan sampel. Data primer berupa data nutrien (nitrat dan fosfat) data
kualitas perairan (suhu, DO, kekeruhan, salinitas dan pH) dan data arus lapangan,
sedangkan data sekunder atau data pendukung yang digunakan dalam penelitian
ini adalah data peramalan pasut dan peta batimetri.
3.3.1. Bahan Penelitian
Bahan-bahan yang digunakan dalam penelitian adalah bahan kimia untuk
analisa nitrat dan fosfat (Tabel 2).
Tabel 2. Bahan-bahan kimia yang digunakan untuk analisis kadar nitrat dan fosfat
No. Nama Bahan
1. Bahan kimia untuk analisis nitrat
- Aquabides
2. Bahan kimia untuk analisis fosfat - H2SO4
- Aquabides
- Asam Askorbat (AA)
1
Tabel 3 . Alat-alat yang digunakan di perairan muara Sungai Porong
No. Nama alat Kegunaan
1. GPS Menentukan posisi sampling
2. Perahu Alat transportasi
3. Botol sampel Menyimpan sampel air
4. Kertas label Memberi label pada sampel
5. Coolbox Menyimpan botol sampel
6. Bola duga Mengambil data arus
7. Spektrofotometer Untuk mengukur kandungan nitrat dan fosfat dari sampel air laut, panjang gelombang 880 nm untuk fosfat dan 454 nm untuk nitrat
8. Termometer (digital)
Mengukur temperatur di lokasi penelitian
9 pH meter Digunakan untuk mengukur pH sampel
10. DO meter Untuk mengetahui kandungan oksigen terlarut di lokasi penelitian
11. Salinometer Untuk mengukur salinitas
12. Software SMS 8.1 Membuat permodelan arus
13. Software ArcGIS
10.1
3.4. Bagan Alir Penelitian
3.5. Metode Penelitian
Penelitian ini menggunakan metode deskriptif dan bersifat eksploratif.
Menurut Whitney (1960) dalam Dianingrum (2007), metode deskriptif adalah pencarian fakta dengan interpretasi yang tepat. Tujuan dari penelitian deskriptif
ini adalah untuk membuat deskripsi, gambaran atau lukisan secara sistematis,
faktual dan akurat mengenai fakta-fakta, sifat-sifat serta hubungan antar fenomena
yang diselidiki (Nasir, 1983 dalam Dianingrum, 2007). Menurut Husein (1999) metode eksploratif adalah jenis penelitian yang berusaha mencari ide-ide atau
hubungan-hubungan yang baru. Dalam hal ini adalah kandungan unsur hara yang
menyebar akibat adanya pengaruh arus.
Posisi stasiun pengambilan sampel air ditetapkan dengan menggunakan
GPS (Global Positioning System) secara purposive. Hadi (2004) menerangkan bahwa, metode purposive merupakan metode pengambilan sampel yang merepresentasikan keadaan keseluruhan. Penentuan lokasi stasiun penelitian
dilakukan berdasarkan kondisi yang dapat mewakili kondisi secara keseluruhan
daerah dan memperhatikan kemudahan pencapaian.
3.6. Metode Pengambilan Data dan Analisis Data
Dalam penelitian ini, pengambilan data dilakukan di beberapa stasiun
dengan menggunakan alat GPS (Global Positioning system). Data yang di ambil meliputi data nutrien (nitrat dan fosfat), data kualitas air dan data arus. Parameter
agar dapat diketahui distribusinya. Adapun metode pengumpulan data tersebut
diuraikan sebagai berikut:
3.6.1. Data Kualitas Air
Pengambilan sampel air laut dilakukan dengan menggunakan botol sampel
dan analisis sampel air laut yang meliputi konsentrasi nitrat dan fosfat yang
dilakukan di Laboratorium Balai Besar Teknik Kesehatan Lingkungan (BBTKL)
Surabaya. Parameter lingkungan perairan yang diukur selama penelitian seperti
suhu, DO, kekeruhan, salinitas, dan pH, merupakan data pendukung dari
penelitian Tim Porong.
Pengujian sampel air untuk menentukan konsentrasi nitrat dan konsentrasi
fosfat dilakukan di Laboratorium Balai Besar Teknik Kesehatan Lingkungan
(BBTKL) Surabaya, dimana metode yang dilakukan adalah sebagai berikut :
1. Nitrat
Butiran Cd (Cadmium) dalam kolom pereduksi yang akan mereduksi
semua kandungan nitrat untuk diubah menjadi nitrit. Selanjutnya nitrit dari
hasil reduksi tersebut dalam suasana asam kuat di determinasi dengan
sulphanilamide dalam senyawa diazonium. Senyawa tersebut dengan
N-1-Napthtylene diamin dihidrocloride dapat bereaksi menjadi larutan
berwarna pink kemudian diukur absorbansinya pada spektrofotometer
2. Fosfat
10 ml larutan sampel ditambah dengan 1 ml mix reagen. Kemudian
diamkan selama 10 menit. Selanjutnya dibaca absorbansinya pada
spektrofotometer dengan panjang gelombang 880 nm (Prosedur fosfat
pada lampiran 1).
3.6.2. Data Arus
Pengambilan data arus dilakukan dengan teknik pengukuran Lagrangian.
Dalam proses perekaman data arus didapat juga koordinat titik pengukuran. Data
kecepatan arus dalam cm/det diubah kesatuan m/det. Data kecepatan arus yang
dikelompokkan dan diubah kesatuan m/det tersebut digunakan untuk verifikasi
dengan kecepatan arus hasil model. Dalam pembuatan model ini menggunakan
modul RMA2 untuk pola sirkulasi arus. Simulasi dilakukan untuk 15 hari untuk
simulasi pola arus dengan RMA2.
Verifikasi model adalah proses membandingkan data lapangan dan hasil
simulasi menggunakan cara statistik. Dalam proses verifikasi ini, hanya dilihat
sejauh mana kemiripan hasil simulasi terhadap data lapangan. Metode statistik
yang dapat digunakan pada proses verifikasi model adalah rata-rata kesalahan
relatif (Mean Relative Error/MRE) (Thomann. et al., 1987)
RE = [
] x 100%
Keterangan :
hc = besar nilai hasil model
ho = besar nilai pengukuran lapangan
n = jumlah lapangan
Jika MRE < 10 %, maka model diterima
Jika MRE > 10 %, maka model ditolak
3.7. Metode Pengolahan Data
Data yang diperoleh melalui pengukuran lapangan kemudian dianalisa di
laboratorium. Berikut teknis pengolahan datanya.:
3.7.1. Data Kualitas Air
Hasil pengujian laboratorium untuk data kandungan nitrat, fosfat dan
parameter lingkungan perairan yang lain seperti suhu, DO, kekeruhan, salinitas,
dan pH yang merupakan data sekunder dilakukan pemetaan sebaran
konsentrasinya diolah dengan menggunakan software ArcGIS 10.1.
3.7.2. Data Arus
Pengambilan data arus dilakukan dengan teknik pengukuran Lagrangian
dengan menggunakan Bola Duga untuk memperoleh data kecepatan arus (jarak
tempuh bola, waktu tempuh bola). Berdasarkan pengukuran data lapangan, maka
didapatkan besar dan arah arus total serta titik koordinat tempuh bola). Peneliti
tidak menggunakan ADCP disebabkan karena ketidaktersediaan alat tersebut
dahulu sebelum di dapatkan data arus yang dibutuhkan, sehingga peneliti hanya
melakukan pengukuran arah dan kecepatan arus secara insitu di lapangan. Hasil vektor plot yang berupa vektor arah arus yang diperoleh dari penelitian ini berasal
dari pengolahan data batimetri. Untuk mendapatkan vektor arah arus
IV.
HASIL DAN PEMBAHASAN
4.1. Hasil
Hasil analisis sampel air untuk menentukan konsentrasi nitrat, fosfat dan
pengolahan data hidro-oseanografi disajikan sebagai berikut :
4.1.1. Konsentrasi Nitrat
Hasil analisis laboratorium untuk nilai konsentrasi nitrat (N-NO3-) yang
terukur di perairan muara Sungai Porong, Kabupaten Sidoarjo berkisar antara
1,3043-3,1079 mg/l (Tabel 4). Konsentrasi nitrat tertinggi terdapat di stasiun 3,
dan terendah terdapat di stasiun 5. Secara ilustratif arah sebaran konsentrasi nitrat
dapat dilihat pada Gambar 5.
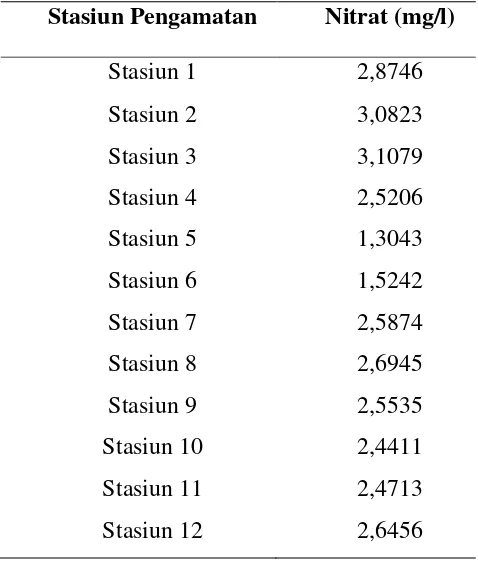
Tabel 4. Konsentrasi nitrat (mg/l) di muara Sungai Porong
Stasiun Pengamatan Nitrat (mg/l)
Stasiun 1 2,8746
Stasiun 2 3,0823
Stasiun 3 3,1079
Stasiun 4 2,5206
Stasiun 5 1,3043
Stasiun 6 1,5242
Stasiun 7 2,5874
Stasiun 8 2,6945
Stasiun 9 2,5535
Stasiun 10 2,4411
Stasiun 11 2,4713
4.1.2. Konsentrasi Fosfat
Hasil analisis laboratorium untuk nilai konsentrasi fosfat(P-PO4-) yang
terukur di perairan muara Sungai Porong, Kabupaten Sidoarjo berkisar antara
0,084-0,128 mg/l (Tabel 5). Konsentrasi fosfat tertinggi terdapat di stasiun 9, dan
terendah terdapat di stasiun 2.Secara ilustratif arah sebaran konsentrasi fosfat
dapat dilihat pada Gambar 6.
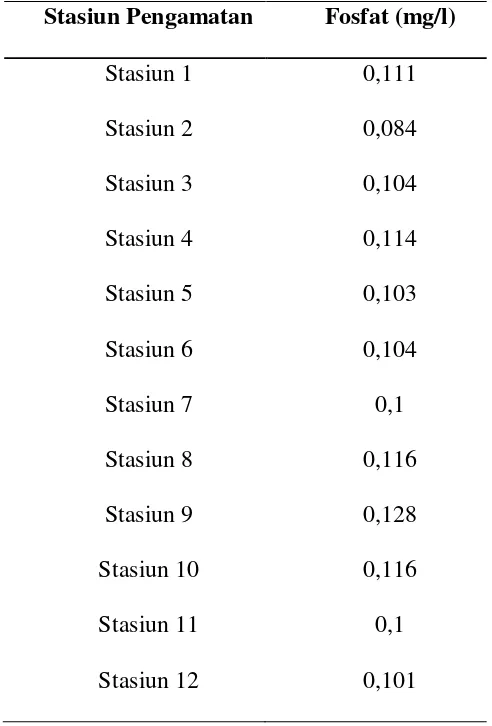
Tabel 5. Konsentrasi fosfat (mg/l) di muara Sungai Porong
Stasiun Pengamatan Fosfat (mg/l)
Stasiun 1 0,111
Stasiun 2 0,084
Stasiun 3 0,104
Stasiun 4 0,114
Stasiun 5 0,103
Stasiun 6 0,104
Stasiun 7 0,1
Stasiun 8 0,116
Stasiun 9 0,128
Stasiun 10
Stasiun 11
Stasiun 12
0,116
0,1
4.1.3. Parameter Pendukung Kualitas Perairan
Hasil pengukuran kualitas perairan yang menjadi faktor pendukung dalam
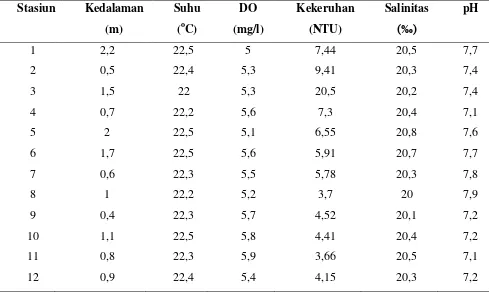
penelitian meliputi kedalaman, suhu, DO, kekeruhan, salinitas dan pH. Hasil
pengukuran kualitas air tersebut masih baik. Nilai kedalaman pada masing-masing
stasiun berkisar antara 0,4-2,2 m. Stasiun 1 memiliki kedalaman paling besar yaitu
2,2 m dibandingkan stasiun lainnya. Suhu berkisar antara 22-22,5oC. Oksigen
terlarut (DO) perairan ini berkisar antara 5-5,9 mg/l dan nilai kekeruhan berkisar
antara 3,6-20,5 NTU. Nilai salinitas berkisar antara 20-20,8 ‰, dan nilai pH
berkisar antara 7,1-7,9 (Tabel 6).
Tabel 6. Hasil parameter pendukung kualitas perairan
4.1.4. Arus Permukaan
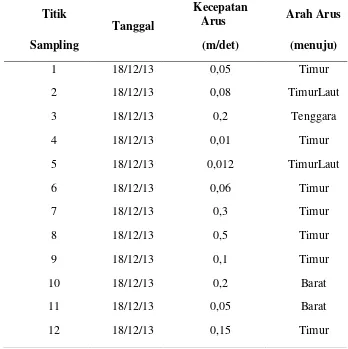
Dari hasil pengukuran kecepatan dan arah arus yang dilakukan pada saat
penelitian menunjukkan arah arus permukaan dominan mengalir dari Barat ke
Timur. Kecepatan arus maksimal di permukaan mencapai 0,5 m/det dan kecepatan
arus minimal adalah 0,01 m/det. Data sampling kecepatan dan arah arus disajikan
pada Tabel 7.
Tabel 7. Data sampling arah dan kecepatan arus di permukaan perairan muara Sungai Porong
4.1.4.1. Verifikasi Hasil Permodelan
Berdasarkan hasil permodelan pola arus di muara sungai Porong yang
telah di dapat, selanjutnya dilakukan verifikasi data hasil model dengan data arus
lapangan agar diketahui hasil permodelan tersebut dapat diterima atau tidak.
Perbandingan data lapangan dan data hasil permodelan disajikan pada Tabel 8.
Tabel 8. Verifikasi hasil permodelan dan nilai MRE
Data arus lapangan (m/det)
Data arus hasil model (m/det)
RE (%)
0,05 0,0146345 0,70731
0,08 0,108266 0,864668
0,2 0,0011223 0,994389
0,01 0,00271026 0,728974
0,012 0,002833 0,763917
0,06 0,00402554 0,932908
0,3 0,128085 0,57305
0,5 0,242849 0,514302
0,1 0,0508789 0,491211
0,2 0,0286698 0,856651
0,05 0,0440658 0,118684
0,15 0,0421037 0,719309
4.1.5. Pasang Surut
Data pasang surut digunakan sebagai data sekunder berasal dari data
pengamatan pasang surut yang dilakukan oleh Lembaga Ilmu Pengetahuan
Indonesia (LIPI) untuk wilayah perairan sekitar Surabaya tahun 2011, kemudian
diolah dengan menggunakan metode admiralty untuk menentukan nilai MSL, HHWL dan LLWL serta tipe pasang surut.
Pengamatan pasang surut dilakukan untuk memperoleh data tinggi muka
air laut di lokasi penelitian. Berdasarkan hasil pengamatan tersebut dapat
ditetapkan datum vertikal penelitian yang sesuai untuk keperluan-keperluan
tertentu pula.
Berdasarkan perhitungan dengan metode Admiralty didapatkan
perhitungan bilangan Formzahl untuk komponen pasang surut menghasilkan nilai
0,9607 yang berarti pasut bertipe campuran cenderung ganda. Tinggi muka air
laut (MSL) 180 cm, pasang tertinggi (HHWL) 337 cm dan surut terendah
(LLWL) 24 cm seperti terlihat pada Gambar 7. Dari data yang diperoleh
selanjutnya dianalisis dengan menggunakan metode Admiralty sehingga diperoleh
Tabel 9. Konstanta harmonik hasil pengolahan data dengan menggunakan metode
Admiralty
Konstanta Harmonik
A (cm) g 0
S0 180 -
M2 60 224
S2 11 345
N2 18 269
K1 43 175
O1 25 44
M4 0 447
MS4 0 207
K2 3 345
P1 14 175
Keterangan :
A = tinggi/nilai komponen pasut (cm) ; g = besar gaya pembangkit
Gambar 9. Waktu pengambilan sampel pada saat pasang menuju surut
4.2. Pembahasan 4.2.1. Sebaran Nitrat
Berdasarkan Tabel 4, terlihat bahwa pada masing-masing sampel air laut
yang diambil di perairan muara Sungai Porong, Kabupaten Sidoarjo, memiliki
konsentrasi antara 1,3043-3,1079 mg/l. Konsentrasi nitrat semakin jauh dari
pantai semakin besar. Menurut Hutagalung dan Rozak (1997), distribusi
horizontal kadar nitrat semakin tinggi menjauhi pantai dan kadar tinggi biasanya
ditemukan di perairan muara. Dilihat dari Gambar 5 sebaran konsentrasi nitrat
tertinggi pada lapisan permukaan ditunjukkan oleh stasiun 3 dengan nilai 3,1079
mg/l. Hal ini disebabkan karena stasiun 3 berada di sekitar Pulau Tujuh. Pulau
Tujuh tersebut terbentuk karena adanya proses sedimentasi lumpur Lapindo yang
membentuk suatu daratan kecil dan di pulau Tujuh tersebut ditumbuhi hutan
mangrove. Dekomposisi sedimen maupun senyawa-senyawa organik yang berasal
dari jasad flora dan fauna yang mati dapat mempengaruhi tingginya kandungan
nitrat di perairan. Hutan mangrove yang serasahnya membusuk oleh bakteri,
diuraikan menjadi zat hara nitrat. Nitrat merupakan zat yang diperlukan dan
organisme di perairan. Adanya masukan nitrat baru (new nitrate) dari ligkungan sekitarnya. Hal ini sangat mungkin terjadi mengingat di hulu muara Sungai
Porong terdapat banyak tambak. Menurut Yoo dan Boyd (1994) adanya aktivitas
pertambakan dapat memberikan kontribusi bahan organik yang banyak
mengandung senyawa nitrat.
Sebaran konsentrasi nitrat semakin tinggi menjauhi pantai, hal ini
dikarenakan adanya pengaruh arus pasut. Arus yang dominan di perairan ini
adalah arus pasang surut karena berada di wilayah muara sungai. Hal ini sesuai
dengan hasil penelitian Atmodjo (2011) yang menyatakan bahwa pasang surut
yang terjadi di muara Sungai Porong sangat berpengaruh terhadap pola arus yang
terjadi. Arus pada saat surut dari sungai menuju laut sehingga kecepatan arus
menjadi relatif besar menjauhi pantai. Karakteristik pola arus di perairan Sungai
Porong cenderung bergerak ke arah Timur (Gambar 7). Menurut Mann dan Lazier
(1991) pasang surut dapat menyebabkan arus pasut. Arus pasut ini dapat
menyebabkan terjadinya turbulensi dalam air. Jika kedalaman suatu perairan tidak
terlalu besar maka kekuatan arus pasut semakin besar dan berpengaruh terhadap
proses percampuran (mixing) (Tabel 6). Proses mixing yang besar pada stasiun yang agak jauh dari pantai tersebut (stasiun 7-12) berdampak meningkatkan kadar
nitrat. Proses percampuran ini akan terjadi ke semua arah dan lapisan. Davis
(1992) mengatakan bahwa peranan pasang surut terhadap proses-proses di estuari
yaitu adanya interaksi antara lautan dan sungai secara horizontal.
Seperti halnya dengan proses fisik perairan, proses kimia dan hayati
semakin tinggi menjauhi pantai. Jadi semakin meningkat suhu perairan, maka
konsentrasi nitrat pada perairan tersebut cenderung menurun. Menurut Stum dan
Morgan (1981), suhu dapat mempengaruhi proses dan keseimbangan reaksi kimia
yang terjadi dalam air. Rata-rata suhu jauh dari pantai lebih rendah dibandingkan
rata-rata suhu di pantai (Tabel 6). Semakin rendah nilai suhu di perairan maka
nilai salinitas rendah dan nilai salinitas yang rendah mengakibatkan kandungan
nutrien tinggi. Oksigen terlarut (DO) dan kekeruhan memiliki peranan dalam
mempengaruhi kandungan nitrat di perairan. Semakin tinggi DO, konsentrasi
nitrat juga akan tinggi dan semakin tinggi kekeruhan, konsentrasi nitrat rendah.
Rata-rata nilai DO semakin tinggi menjauhi pantai dan nilai kekeruhan semakin
rendah menjauhi pantai (Tabel 6).
4.2.2. Sebaran Fosfat
Berdasarkan Tabel 5, terlihat bahwa pada masing-masing sampel air laut
yang diambil di perairan muara Sungai Porong Kabupaten Sidoarjo, memiliki
konsentrasi antara 0,0804-0,128 mg/l. Kadar fosfat tertinggi pada lapisan
permukaan diperoleh dari stasiun 9 yaitu sebesar 0,128 mg/l. Dilihat dari posisi
stasiun 9 berada jauh dari pantai. Kondisi perairan sangat menentukan konsentrasi
dan sebaran fosfat. Sistem penyebaran fosfat di perairan dipengaruhi oleh proses
fisik, kimia dan hayati perairan. Arus dan pengadukan massa air merupakan faktor
fisik yang mempengaruhi penyebaran fosfat diperairan.
Seperti halnya dengan pola sebaran nitrat, pola sebaran konsentrasi fosfat
pengaruh arus pasut. Arus pasang surut sangat berpengaruh terhadap sebaran
fosfat, sehingga semakin menjauhi dari pantai maka konsentrasi fosfat semakin
besar karena arus bergerak ke arah Timur dan menjauhi pantai (Gambar 7). Arus
pada saat surut dari sungai menuju laut, sehingga kecepatan arus menjadi relatif
besar menjauhi pantai.
Proses kimia dapat mempengaruhi sebaran konsentrasi fosfat di perairan
yaitu parameter kualitas perairan. Sebaran konsentrasi fosfat semakin tinggi
menjauhi pantai. Hal ini dibuktikan dengan rata-rata suhu jauh dari pantai (stasiun
7-12) lebih rendah dibandingkan rata-rata suhu di pantai (stasiun 1-6) (Tabel 6).
Levinton (1982) menyatakan, bahwa pengaruh suhu dalam perairan sangat
penting dalam hal produktivitas perairan. Perairan dengan suhu rendah lebih kaya
akan nutrien dibandingkan dengan perairan yang memiliki suhu tinggi. Semakin
tinggi suhu, semakin rendah kandungan nutrien (nitrat dan fosfat).
Oksigen terlarut (DO) dan kekeruhan memiliki peranan dalam
mempengaruhi kandungan fosfat di perairan. Semakin tinggi DO, konsentrasi
fosfat juga akan tinggi dan semakin tinggi kekeruhan, konsentrasi fosfat rendah.
Rata-rata nilai DO semakin tinggi menjauhi pantai dan nilai kekeruhan semakin
rendah menjauhi pantai (Tabel 6). pH memiliki peranan dalam mempengaruhi
kandungan fosfat di perairan. Menurut Santoso (2007) organisme akuatik dapat
hidup dalam suatu perairan yang mempunyai nilai pH yang netral dengan kisaran
antara 7 sampai 8,5 yang ideal bagi kehidupan organisme akuatik. (Tabel 6).
perairan. Nilai pH akan mempengaruhi proses-proses biokimia perairan, misalnya
proses nitrifikasi akan berakhir jika pH rendah (Effendi,2003).
4.2.3. Verifikasi Hasil Permodelan
Berdasarkan hasil perhitungan MRE (Mean Relative Error), diperoleh hasil bahwa nilai error antara hasil di lapangan dengan simulasi model untuk data
arus sebesar 0,68 % (Tabel 8). Berdasarkan nilai tersebut, maka hasil permodelan
masih dapat diterima. Hal ini sesuai dengan pernyataan Thomann et al., (1987) yang menyatakan bahwa jika nilai MRE <10 % maka model diterima, sebaliknya jika
V. KESIMPULAN DAN SARAN
5.1. Kesimpulan
Berdasarkan hasil penelitian ini, maka dapat disimpulkan sebagai berikut :
1. Konsentrasi nitrat di perairan muara Sungai Porong, Kabupaten Sidoarjo
memiliki kisaran sebesar 1,3043-3,1079 mg/l, dan konsentrasi fosfat
berkisar antara 0,084-0,128 mg/l.
2. Arah sebaran konsentrasi nitrat dan fosfat di daerah penelitian
menunjukkan bahwa lokasi stasiun penelitian yang berada jauh dari pantai
adalah semakin tinggi ke arah Tmur, hal ini dikarenakan adanya pengaruh
arus pasut, dimana kecepatan arus menjadi meningkat karena
meningkatkan proses mixing yaitu percampuran antara lautan dan sungai secara horizontal.
5.2. Saran
1. Mengingat penelitian ini hanya menggunakan 12 stasiun penelitian, maka
untuk penelitian selanjutnya disarankan untuk memperbanyak stasiun
penelitian agar data yang didapatkan lebih representif.
2. Mengingat penelitian ini hanya menggunakan kondisi perairan pada bulan
Desember 2013, maka perlu dilakukan penelitian lebih lanjut tentang
pengaruh musim terhadap kondisi hidrodinamika dan sebaran kualitas
DAFTAR PUSTAKA
[APHA] American Public Health Association. 1989. Standard Methods for the Examination of Water and Wastewater. 20th Ed. Washington DC.
Bennekom,A. J. Van. 1998. Deep Water Transit Times in the Eastern Indonesian Basins, Calculated from Dissolved Silica in Deep and Interstitial Waters. Neth. J. Sea Res. 22 : 341-354.
Boney, A.D. 1976. Phytoplankton. The Institut of Biologys Studies in Biology, No.52. Edward Arnold. 109 pp.
Brotowidjoyo, M. D dan A. S. Ruyitno. 1995. Pengantar Lingkungan Perairan dan Budidaya Air. Liberty. Yogyakarta.
Chester, R. 2003. Marine Geochemistry. London:Academic Division of Unwin Hyman.
Dahuri, R., Jacub, R., Sapta P. G dan M.J. Sitepu. 1996. Pengelolaan Sumber Daya Wilayah Pesisir dan Lautan Secara Terpadu. Pradnya Paramitha, Jakarta.
Dahuri R., Rais Y., Putra S.,G., Sitepu, M. J., 2001. Pengelolaan Sumber Daya Wilayah Pesisir dan Lautan Secara Terpadu. PT. Pradnya Paramitha, Jakarta.
Damanhuri, T.P., N. Halim, dan S. Nurtiono. 1997. The Role of Effluen Recirculation in Increasing Efficiency of Anaerobic and Aerobic Wastewatertreatment of Tofu Industry. ITB. Bandung.
Davis, M.L. and D.A, Cornwell. 1991. Introduction to Environmental Engiineering. Second edition, Mc-Graw-Hill, Inc., New York.
Davis, R.A.Jr. 1992. Depotinal System. An Introduction to Sedimentlogy and Stratigraphy. Second Edition. PrenticeHall. Englewood Cliffs. New Jersey.
Effendi, H. 2003. Telaah Kualitas Air bagi Pengelolaan Sumberdaya dan Lingkungan Perairan. Penerbit Kanisius.
Fachrul, M.F, H. Haeruman dan L.C. Sitepu. 2005. Komunitas Fitoplankton Sebagai Bio-Indikator Kualitas Perairan Teluk Jakarta, Proceeding Seminar Nasional MIPA UI, Fakultas MIPA Universitas Indonesia, Depok 25-26 November 2005.
Haryono H.S. dan B. Zaman. 2004. Analisis Sebaran Temperatur dan Salinitas Air Limbah PLTU-PLTGU Berdasarkan Sistem Pemetaan Spasial (Studi Kasus : PLTU-PLTGU Tambak Lorok Semarang). UNDIP, Semarang.
Haslam, S.M. 1995. River Pollution, an Ecological Perspective. Belhaven Press. London UK.
Hutabarat. S dan S.M Evans., 1985. Pengantar Oseanografi. Cetakan Kedua. Universitas Indonesia Press. Jakarta.
Husein, U. 1999. Metode Penelitian : Aplikasi Dalam Pemasaran, Jakarta. PT Gramedia Pustaka Utama.
Hutagalung, H.P. dan Rozak. 1997. Metode Analisis Air Laut, Sedimen dan Biota. Buku 2. P3O-LIPI. Jakarta.
Kalujnaia, S., et al. 2007. Salinity Adaption and Gen Profiling Analysis in the European Eel Using Microaary Technology. General and Comparative Endocrinology 9 Vol. 152) : Page 274-280.
Koesoebiono. 1980. Dasar Ekologi Umum, bagian IV. Ekologi Perairan. Sekolah Pasca Sarjana. Jurusan Pengelolaan Sumber Daya Alam dan Lingkungan. Institusi Pertanian Bogor.
Levinton, J.F. 1982. Marine Ecology. New Jersey Prentice-Hall Inc. Englewood Cliff.
Lihan, T., S.-I. Saitoh. 2008. Satellite Measured Temporal And Spatial Variability Of The Tokachi River plume Estuarine, Coastal and Shelf Science. 78(2):
237-249.
Mann, K.H. and J.R,N Lazier.1991. Dynamic of Marine Ecosystem. Biological-Physical Interaction in The Oceans. Blackwell Scientific Publications.
Masduqi, A. 2004. Penurunan Senyawa Fosfat dalam Air Limbah Buatan dengan Proses Adsorpsi menggunakan Tanah Haloisit. [tesis]. Bandung: Program Studi Teknik Lingkungan, Program Pascasarjana, Institut Teknologi Bandung.
Nontji, A. 1986. Biomassa dan Produktivitas Fitoplankton di Perairan Teluk Jakarta serta Kaitannya dengan Faktor-Faktor Lingkungan. Disertasi Bogor:Program Pascasarjana IPB.
Nontji, A. 1987. Variasi Musiman Beberapa Faktor Ekologi di Perairan Teluk Jakarta. Oseanologi di Indonesia 11:27-36.
Nontji, A. 2002. Laut Nusantara. Jakarta: Djambatan.
Nontji, A. 2008. Plankton Laut. Jakarta: LIPI Press.
Nybakken, J. W. 1988. Biologi Laut, Suatu Pendekatan Ekologi. PT. Gramedia Pustaka Utama, Jakarta, 459 hlm. (diterjemahkan oleh Eidman, M. dan Koesoebiono).
Nybakken, J. W. 1992. Biologi Laut Suatu Pendekatan Ekologis. Gramedia Pustaka Utama. Jakarta.
Nybakken, J.W. 1998. Marine Biology: An Ecological Approach. 3rd Ed. Harper Collins College Publishers.
Odum, H.T.1971. Fundamental of Ecology. 3 rd Edition. Toppan Co.Ltd,Tokyo.
Perzelin B.B., 1981. Light Reactions in Photosynthesis Dalam: Physiological Bases of Phytoplankton Ecology (T.Piatt ed.) Canadian Bulletin of Fish and Aquatic Sciince210:1-43.
Parsons, TR,. M. Takahashi and B. Hargrave. 1984. Biological Oceanographic Processes. 3rd Ed. Oxford:Pergamon Press.
Pescod, N. B. 1973. Investigation of Rational Effluent and Stream for Tropical Countries. AIT. Bangkok.
Riley, JP and G. Skirrow. 1975. Chemical Oceanography. New York:Academic Press.
Rockford. 1962. A Biology of The Algae. USA:Wim. C. Brown Publisher.
Romimohtarto. K dan S. Juwana. 1991. Kualitas Air dalam Budidaya Laut, Faeming Workshop Report. Bandar Lampung.
Rosmawati. 2004. Kondisi Oseanografis Perairan Selat Tiworo Pada Bulan Juli-Agustus 2002. Skripsi. Program Studi Ilmu Kelautan. Fakultas Perikanan dan Ilmu Kelautan. Institut Pertanian Bogor. Bogor.
Santoso, A. D. 2007. Kandungan Zat Hara Fosfat pada Musim Barat dan Musim Timur di Teluk Hurun Lampung. Jurnal Teknologi Lingkungan. Jakarta. Vol. No. 14. Halaman 43-47.
Sastrawijaya, A. T. 1991. Pencemaran Lingkungan. Penerbit PT. Rineka Cipta Jakarta.
Stum, W. and Morgan. 1981. Aquatic Chemistry : an Introduction Emphasizing Chemical Equalibra in Natural Water. John Wiley & Sons, Inc. Canada.
Siagian, M. 2000. Diktat Ekologi Perairan. Universitas Riau Press, Pekanbaru.
Sidjabat. 1973. Distribusi Spasial Klorofil-a dan Struktur Komunitas Fitoplankton di Perairan Teluk Ambon. Jakarta:Program Pascasarjana UI.
Vink, S and M. Atkinson. 1983. Chemical Analysed Used at Waterman Marine Laboratory. University of Westren Australia.
Susana. 1987. Oseanografi Kimia. Workshop: Basic Science Bidang Kimia. Kerjasama Univ. Udayana-Indonesia Australia Eastern Universities Project (IAEUP).
Strickland J.D.H. and T.R. Parsons. 1960. A Practical Hand Book of Sea Water Analysis. Bull. Fish. Res. Bd. Of Canada 167 : 65-70.
Supriharyono. 2007. Konservasi Ekosistem Sumberdaya Hayati di Wilayah Pesisir dan Laut Tropis. Pustaka Pelajar. Yogyakarta.
Thomann et al., 1987. Principles of Surface Water Quality Modelling and Control. New York: Harper & Row, Publisher, Inc.
Triatmodjo, B. 1999. Teknik Pantai: Edisi kedua, Beta Offset,Yogayakarta.
Wibisono, M. S. 2005. Pengantar Ilmu Kelautan. PT Gramedia. Jakarta.
Wyrtki, K. 1961. Physical Oceanography of the South East Asian Waters. Published by the Scripps Institution of Oceanography, Univ. Of California. San Diego, C.A.
Lampiran 1.
A. Analisis Konsentrasi Nitrat
Dalam analisa terhadap nitrat, digunakan butiran Cd (Cadmium) sebagai
kolom pereduksi yang akan mereduksi semua kandungan nitrat untuk diubah
menjadi nirit. Selanjutnya nitrit dari hasil reduksi tersebut dalam suasana asam
kuat dapat di determinasi dengan sulphanilamide dalam senyawa diazonium,
dimana senyawa tersebut dengan N-1-Napthtylene diamin dihidrocloride dapat
bereaksi menjadi larutan berwarna pink yang bisa diukur dengan
spektrofotometer (Parson et al., 1984 ; Macintosh, 1984).
Menurut Sue Vink dan Marlin Atkinson (1983), tahapan metoda reduksi
dalam analisa konsentrasi nitrat adalah sebagai berikut:
1. Membuat Reagen
a. Larutan buffer ammonium clorida : 10 gram NH4CL dilarutkan dalam 1
liter aquabides.
b. Reagen pewarna : ke dalam 1500 cc aquabides ditambahkan 200 cc
asam fosforat, 20 gram sulphanilamide, 1 gram N-1-Napthtylene
diamin dihidrocloride, kemudian ditambah aquabides sampai menjadi 2
liter.
c. Merakit kolom reduksi : Cuci butiran Cadmium dengan 1 N HCL,
kemudian dicuci 20 kali dengan aquabides, dengan catatan selama
pencucian dijaga agar butiran Cadmium tadi tidak berhubungan
dengan 50 cc karutan Cupri Sulfat (CUSO4), sampai warna biru dari
larutan tersebut hilang semua. Kemudian dicuci lagi dengan aquabides
sebanyak 20 kali.
Langkah berikutnya segera diisikan ke kolom (pipa plastik) dengan
menggunakan syringe dan aquabides untuk melindungi terjadinya
gelembung udara selama pengisian. Dalam pengisian butiran Cadmium
ke kolom tersebut, terlebih dulu bagian bawah disumbat dengan glass
wool, selanjutnya setelah terisi cukup bagian atasnya juga disumbat
dengan glass wool. Langkah berikutnya kolom reduksi tersebut dirakit
sedemikan rupa.
d. Larutan standart nitrat
- Larutan A : larutkan 0,101 gram kalium nitrat dalam aquabides
sebanyak 1 liter, simpan dalam botol gelap dan tambahkan
chloroform sebagai pengawet.
- Larutan B : larutkan 5 ml larutan A dengan gelas ukur menjadi 50
ml dengan aquabides untuk membuat standart 100 nm simpan
dalam botol gelap.
2. Menganalisa Sampel
a. Mempersiapkan larutan blank : 5 ml aquabides ditambah 5 ml NH4CL
buffer ditambah 1 ml reagen warna.
b. Kolom pereduksi dicuci dengan 10 ml NH4CL buffer, diulangi lagi dengan
c. Diambil 5 ml sampel ditambah dengan 5 ml NH4CL buffer, kemudian
dilewatkan melalui kolom reduksi dan air hasilnya ditampung dalam
tabung reaksi.
d. Larutan tertampung ditambah dengan 1 ml reagen pewarna, didiamkan 15
menit selanjutnya dibaca absorbansinya pada spektrofotometer dengan
panjang gelombang 454 nm.
Menurut Sue Vink dan Marlin Atkinson (1983), analisa konsentrasi nitrat
dengan metoda kolom reduksi ini m maka akan terdeterminasi juga nitrit dari
sampel ke dalam hasil yang diperoleh. Untuk itu makan perlu dianalisa
konsentrasi nitrit. Selanjutnya konsentrasi nitrat yang sesungguhnya yaitu hasil
B. Analisis Konsentrasi Fosfat 1. Pembuatan Pereaksi
- Larutan Ammonium Molybdate
Larutkan 15 gr ammonium molybdate (NH4)6Mo7O244H2O dalam
500 ml aquabides. Simpan dalam botol plastik dan d9 simpan dalam
tempat gelap.
- Larutan Asam Sulfat
Encerkan 70 ml asam pekat, H2SO4 dengan 450 ml aquabides dalam
labu ukur 1000 ml. Dalam mencampurkan larutan, maka asam dulu
yang dituang, kemudian aquabides. Biarkan larutan tersebut dingin.
- Larutan Asam Askorbat
Larutkan 27 gr asam askorbat (C6H8O6) dalam 500 ml aquabides.
Simpan dalam botol dan lemari pendingin, jika berubah warna
jangan digunakan sebagai pereaksi.
- Larutan Antimonyl-Tartrate
Timbang 0,34 gr antimonil tartrate K(SbO)C6H4O6) dan larutkan ke
dalam 250 ml aquabides. Stabil dalam beberapa bulan dan jika
keruh jangan digunakan.
- Larutan Standar
Larutkan 0,0816 gr KH2PO4 anhydrous dengan beberapa ml
aquabides dalam labu ukur 100 ml hingga batas tera labu (1 ml = 6
- Larutan Mix Reagen
Larutan ini tidak dapat disimpan dalam waktu lama, oleh karena itu
dibuat pada waktu akan menganilsa sampel. Jumlahnya supaya
disesuaikan dengan kebutuhan. Cara membuatnya dengan
mencampurkan larutan ammonium molibdate (2 ml), larutan asam
sulfat (5 ml) dan larutan asam askorbat (2 ml) serta larutan
antimonyl-tatrate (1 ml). Perbandingan larutan ini adalah 2:5:2:1.
Tahapan dalam analisis Fosfat pada sampel air di laboratorium adalah :
1. 10 ml larutan sampel ditambah dengan 1 ml mix reagen , kemudian
diamkan selama 10 menit.
2. Selanjutnya dibaca absorbansinya pada spektrofotometer dengan