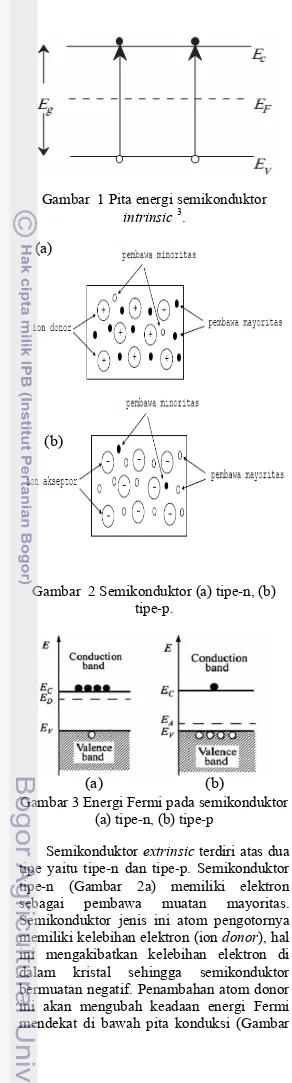
Gambar 1 Pita energi semikonduktor intrinsic 3.
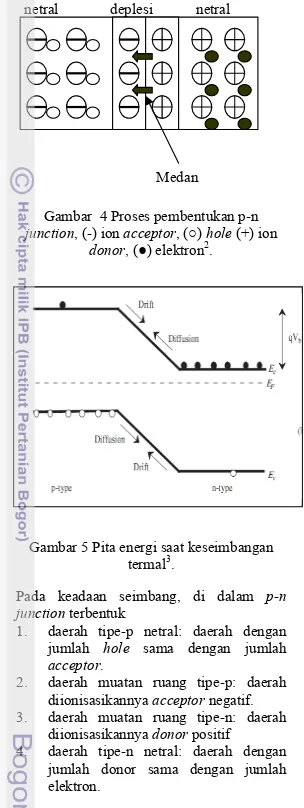
Gambar 2 Semikonduktor (a) tipe-n, (b) tipe-p.
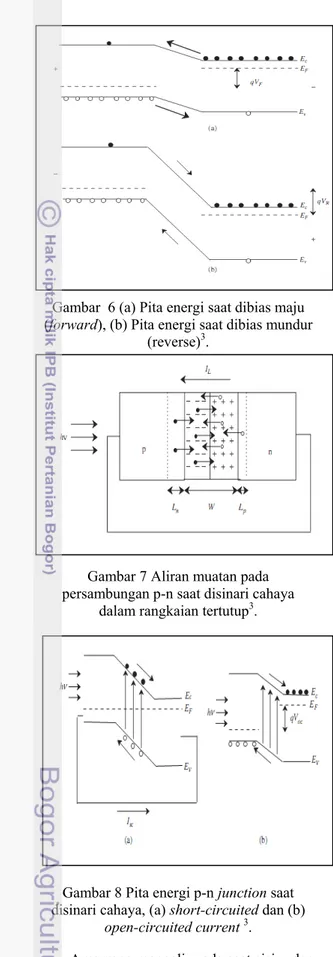
Gambar 3 Energi Fermi pada semikonduktor (a) tipe-n, (b) tipe-p
Semikonduktor extrinsic terdiri atas dua tipe yaitu tipe-n dan tipe-p. Semikonduktor tipe-n (Gambar 2a) memiliki elektron sebagai pembawa muatan mayoritas. Semikonduktor jenis ini atom pengotornya memiliki kelebihan elektron (ion donor), hal ini mengakibatkan kelebihan elektron di dalam kristal sehingga semikonduktor bermuatan negatif. Penambahan atom donor ini akan mengubah keadaan energi Fermi mendekat di bawah pita konduksi (Gambar
2a). Semikonduktor tipe-p (Gambar 2b)memiliki lubang (hole) sebagai pembawa muatan mayoritas. Semikonduktor jenis ini atom pengotornya kekurangan elektron (ion acceptor), hal ini mengakibatkan kekosongan di dalam kristal sehingga semikonduktor bermuatan positif. Gambar 3b menunjukkan energi Fermi pada semikonduktor tipe-p mendekat ke atas pita valensi.
Sel Surya p-n Junction
Sel surya adalah suatu piranti yang mengkonversi energi cahaya menjadi energi listrik. Pada umumnya sel surya dibuat dari bahan semikonduktor anorganik, seperti silikon mono kristal dan multi kristal. Sel surya konvensional seperti ini dapat menyerap cahaya matahari lebih dari 24%. Efisiensi yang telah dicapai oleh sel surya berbahan dasar material anorganik sekitar 10-20%. Sel surya konvensional pada umumnya tersusun dari persambungan semikonduktor tipe-p dan tipe-n (p-n junction).
(a)
(b)
Hal terpenting pada sel surya p-n adalah adanya pemisahan muatan, yaitu hole dan elektron akibat penyinaran oleh cahaya. Adanya persambungan antara kedua tipe semikonduktor ini mengakibatkan terbentuknya potensial pada persambungan dan difusi muatan. Difusi muatan terjadi karena adanya gradient konsentrasi muatan pembawa antara semikonduktor tipe-p dan n. Difusi hole dari semikonduktor tipe-p menuju titipe-pe-n, sedangkan elektron dari semikonduktor tipe-n menuju tipe-p.
Difusi hole dan elektron tidak terjadi terus menerus, karena ketika hole meninggalkan tipe-p dan hilang di dalam tipe-n akibat rekombinasi, maka sebuah akseptor diionisasikan menjadi negatif di daerah tipe-p yang membentuk muatan ruang negatif. Hal yang sama terjadi pada elektron yang meninggalkan muatan ruang positif pada daerah tipe-n, sehingga membangkitkan medan listrik yang berasal dari ruang muatan postif menuju ruang muatan negatif (Gambar 4). Medan listrik ini menghambat difusi hole dan elektron. Medan listrik menjadi bertambah kuat dengan semakin banyaknya difusi dan rekombinasi. Aliran-aliran muatan pembawa ini segera berhenti setelah terdapat keseimbangan antara aliran difusi dan aliran drift. Keseimbangan ini ditandai oleh adanya kesamaan antara tingkat energi Fermi tipe-p dan tipe-n (Gambar 5).
(a) (b)
Gambar 4 Proses pembentukan p-n junction, (-) ion acceptor, (○) hole (+) ion
donor, (●) elektron2.
Gambar 5 Pita energi saat keseimbangan termal3.
Pada keadaan seimbang, di dalam p-n junction terbentuk
1. daerah tipe-p netral: daerah dengan jumlah hole sama dengan jumlah acceptor.
2. daerah muatan ruang tipe-p: daerah diionisasikannya acceptor negatif. 3. daerah muatan ruang tipe-n: daerah
diionisasikannya donor positif
4. daerah tipe-n netral: daerah dengan jumlah donor sama dengan jumlah elektron.
Besarnya potensial internal pada daerah deplesi dapat dipengaruhi oleh tegangan external yang dipasang pada p dan sisi-n. Pemasangan tegangan bias positif pada sisi tipe-p dan negatif pada sisi tipe-n akan menurunkan potensial internal pada daerah deplesi (Gambar 6a). Keadaan ini disebut bias maju (forward) (VF). Pemasangan bias maju akan menurunkan arus drift, tetapi dapat menaikkan disfusi elektron dari tipe-n
ke p dan difusi hole dari p ke tipe-n. Rapat arus total (J) yang mengalir pada saat persambungan p-n di bias maju adalah pertambahan rapat arus difusi pada sisi-n (Jn) dengan rapat arus difusi pada sisi-p (Jp). netral deplesi netral
⎟
⎟
⎠
⎞
⎜
⎜
⎝
⎛
−
=
+
=
0 kT1
qV n p Fe
J
J
J
J
(1) Keterangan : J0 adalah rapat arus saturasi (A/cm), k adalah konstanta Boltzmann (1.381 × 10−23 J/K), q adalah muatan (C) dan T adalah suhu mutlak (K).Medan
Pemasangan bias negatif pada sisi-p dan positif pada sisi-n akan menaikkan potensial internal pada daerah deplesi (Gambar 6b). Keadaan ini disebut bias mundur (reverse) (VR). Rapat arus yang mengalir pada saat bias mundur adalah
Besarnya arus pembawa pada p-n junction dipengaruhi oleh penyinaran cahaya. Penyinaran cahaya pada persambungan p-n akan membentuk pasangan elektron-hole yang memiliki energi lebih besar dari pada celah energi. Pembentukan pasangan elektron-hole terjadi di daerah difusi dengan panjang Lp untuk difusi hole dan Ln untuk difusi elektron. Pasangan elektron-hole ini akan berkontribusi terhadap arus foto. Jumlah pasangan elektron-hole dipengaruhi intensitas cahaya yang datang. Pasangan elektron-hole akan berpisah karena medan listrik yang ada pada daerah deplesi. Adanya pemisahan muatan pada daerah deplesi, akan menghasilkan aliran arus dari sisi-n ke sisi-p ketika sisi-p dan sisi-n dihubungkan dengan kawat luar (Gambar 7).
Penyinaran p-n junction dengan cahaya pada rangkaian terbuka mengakibatkan pemisahan muatan pembawa. Pemisahan muatan pembawa ini menghasilkan beda potensial. Diagram pita energi p-n junction pada saat dihubung singkat (short-circuited) dan arus rangkaian terbuka (open-circuited current) ditunjukkan pada Gambar 8a dan 8b.
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
−
=
0 −kT1
qVR (2)e
J
J
3Gambar 6 (a) Pita energi saat dibias maju (forward), (b) Pita energi saat dibias mundur
(reverse)3.
Gambar 7 Aliran muatan pada persambungan p-n saat disinari cahaya
dalam rangkaian tertutup3.
Gambar 8 Pita energi p-n junction saat disinari cahaya, (a) short-circuited dan (b)
open-circuited current 3.
Arus yang mengalir pada saat sisi-p dan sisi-n dihubungkan seperti rangkaian tertutup disebut arus short-circuit (Isc) yang nilainya sama dengan arus foto (IL) jika
hambatan seri (series resistance) sama dengan nol. Ketika sisi-p dan sisi-n diisolasi, elektron bergerak menuju sisi-n dan hole menuju sisi-p. Elektron dan hole akan berkumpul pada kedua sisi, sehingga menghasilkan tegangan. Tegangan tersebut dianamakan tegangan open-circuit (Voc). Kurva karakteristik arus-tegangan p-n junction saat disinari cahaya dan saat dalam keadaan gelap (tidak menerima cahaya) ditunjukkan oleh Gambar 9.
Gambar 9 Kurva karakteristik arus-tegangan(I-V) saat gelap dan disinari
cahaya3.
Arus yang mengalir pada persambungan p-n ketika disinari cahaya adalah:
sc nkT qV
I
e
I
I
⎟
⎟
−
⎠
⎞
⎜
⎜
⎝
⎛
−
=
01
(3) Ketika rangkaian terbuka (I = 0), tegangannya adalah:⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
+
=
ln
1
0I
I
q
nkT
V
sc oc (4) Keterangan : Voc adalah tegangan open-circuit (volt), Isc adalah arus short-open-circuit (A), Io adalah arus yang mengaliar pada rangkaian (A), N adalah jumlah paertikel, k adalah konstanta Boltzmann (1.381 × 10−23 J/K), q adalah muatan (C) dan T adalah suhu mutlak (K)Fill factor merupakan parameter fotovoltaik sel surya yang dapat dijadikan penentu baik dan buruknya sel. Fill factor
(FF) dapat dicari dengan menggunakan persamaan: sc oc m m
I
V
I
V
FF
=
(5) VmIm adalah daya maksimum sel.Efisiensi konversi pada sel surya (η) didefinisikan sebagai perbandingan daya output maksimum yang dihasilkan terhadap daya total intensitas cahaya yang diterima (PIn).
(6) Efisiensi % = Pmax/Pin x 100 (7) Arus sirkuit singkat (Isc) dicapai jika sel surya dihubung singkat, pada kondisi ini tidak ada potensial yang melintasi sel. Lebih jelasnya arus sirkuit singkat sama dengan jumlah foton absolute yang terkonversi menjadi pasangan electron – hole4. Sedangkan potensial sirkuit terbuka (Voc) adalah potensial yang dicapai saat tidak ada arus yang mengalir dari sel surya.
Sel Surya Hybrid
Pengangkutan muatan pada semikonduktor organik bergantung pada kemampuan pembawa muatan untuk melintas dari satu molekul ke molekul lain. Loncatan muatan pembawa dari satu molekul ke molekul lain ditentukan oleh celah energi antara tingkat energi HOMO (high occupied molecule orbital) dan LUMO (lowest unoccupied molecule orbital). Bahan semikonduktor organik yang digunakan sebagai lapisan aktif sel surya dapat berbentuk molekul atau polimer conjugate.
Untuk menemukan sel surya organik dengan efisiensi tinggi adalah dengan menciptakan sel surya heterojunction, material organik menerima elektron dan hole yang lebih banyak jika dibandingkan piranti tunggal saja yang menunjukkkan nilai efisiensi yang lebih baik. Dengan menggunakan heterojunction, excitons (ikatan pasangan electron-hole) yang mengalami fotogenerasi pada polimer dapat secara efisien dipisahkan menjadi pembawa muatan pada interface, sedangkan pada piranti tunggal banyak elektron yang mengalami rekombinasi dalam waktu singkat. Pemisahan muatan terjadi pada interface antara molekul donor dan acceptor, yang dimediasi oleh penurunan potensial yang besar. Setelah terjadi
foto-eksitasi elektron dari HOMO ke LUMO, elektron dapat melompat dari LUMO donor (bahan dengan LUMO yang tinggi) ke LUMO acceptor jika terdapat perbedaan potensial ΔΦ antara potensial ionisasi donor dan afinitas elektron acceptor yang lebih besar dari energi ikat excitons. Proses ini disebut sebagai pemindahan muatan terfotoinduksi, dapat mempermudah mobilitas muatan bebas jika hole tertinggal pada donor karena tingkat HOMOnya yang lebih besar. Sebaliknya, jika HOMO acceptor lebih besar, pemindahan excitons sepenuhnya terjadi pada bahan dengan bandgap kecil yang disertai dengan kehilangan energi.
Pemisahan excitons yang efisien pada heterojunction, bahan donor dan acceptor sangat berhubungan. Skala jarak optimum berhubungan dengan panjang difusi excitons. Selain itu, ketebalan lapisan aktif harus sebanding dengan panjang penetrasi cahaya yang pada semikonduktor organik, nilainya berkisar antara 80–200 nm19.
Bahan organik yang dikonjugasikan dengan polimer menujukkan suatu sifat fotoelektronik semikonduktor seperti sifat mekanik dan manfaat yang diharapkan pada bahan polimer. Kajian tentang sel surya
hybrid organik-inorganik heterojunction
diawali dengan fotovoltaik organik berbasis molekul-molekul kecil, kemudian diikuti oleh sel fotovoltaik berbasis polimer. Pada penelitian sebelumnya cara membuat sel surya hybrid yaitu dengan menyambungkan CdS dengan polimer poly(3-octylthiophene) (P3OT) yang merupakan turunan dari polythiophene dan diperoleh efisiensi konversi sebesar 0,015 % dengan intensitas penyinaran 100 mW/cm2. Dari penelitian ini diperoleh rapat arus short-circuit yang kecil yang diakibatkan oleh P3OT yang tebal dan mobilitas pembawa muatannya yang rendah. Ketebalan lapisan P3OT ternyata sangat mempengaruhi besarnya ISC dan VOC.
Cadmium Sulfide (CdS)
Cadmium Sulfide (CdS) merupakan semikonduktor dalam kelompok senyawa golongan II-IV dengan struktur kristal zinc blended dan wurtzite. Seperti pada bahan semikonduktor dalam kelompok senyawa-senyawa yang lain, maka senyawa-senyawa II-IV yakni CdS memiliki sifat optik dan listrik yang cocok untuk aplikasi sel surya.
CdS memiliki koefisien absorpsi yang tinggi sehingga sebagian besar cahaya dapat diabsorpsi pada CdS dalam bentuk lapisan
tipis sehingga sangat efektif untuk sel surya lapisan tipis. CdS memiliki lebar celah pita (bandgap) antara 2 sampai 3 eV serta memiliki jenis celah pita semikonduktor direct bandgap pada n=½ (untuk indirect, n=2). CdS juga memiliki fotokonduktivitas yang tinggi sehingga sangat cocok untuk bahan piranti fotodetektor.
Secara umum, CdS memiliki dua fase kristal yaitu fase kubik yang merupakan fase metastabil dan fase heksagonal yang merupakan fase yang stabil pada suhu ruang. Selain itu dalam beberapa literatur menunjukkan struktur CdS yang lainnya yaitu orthorombik10. Proses annealing secara khusus dapat mengubah fase CdS dari kubik menjadi heksagonal. Jika film dipanasi pada suhu di atas 300 oC, maka fase CdS akan mengalami transisi fase dari fase kubik menjadi fase heksagonal. Tidak semua fase kubik berubah menjadi fase heksagonal tetapi hanya sebagian saja11.
Lapisan tipis CdS memiliki struktur polikristal yang dideposisi dengan menggunakan cadmium chloride (CdCl2 . ½ H2O), thiourea, triethanolamine (TEA) yang dipanaskan pada suhur 70oC5. Lapisan tipis CdS berwarna jingga kekuning-kuningan. Reaksi kimia untuk menghasilkan lapisan tipis CdS yaitu dengan menggunakan TEA kompleks seperti persamaan kimia sebagai berikut :
[Cd(TEA)+2] + (NH
2)2CS + 2 O CdS + TEA + (NH2)2CO + H2O
Senyawa yang menghasilkan ion Cd2+ berasal dari Cd(TEA)+2 dan ion S2- berasal dari senyawa (NH2)CS. Hasil reaksi tersebut menghasilkan senyawa CdS sebagai hasil utama. TEA dan H2O sebagai senyawa tambahan.
Polythiophene
Polimer thiophene relatif stabil di udara bebas maupun di lingkungan air dan memiliki mobilitas hole yang tinggi6. Polythiophene dapat dibuat dari monomer 3-methylthiophene secara klasik maupun elektrokimia. Thiophene merupakan salah satu polimer konduktif jenis aromatik heterocylic yang hampir mirip dengan pyrrole. Rumus kimianya adalah C4H4S. Sulfur disini merupakan heteroatom. Polimer poly(3-hexylthiophene) merupakan turunan dari polythiophene. Struktur polimer
poly(3- hexylthiophene) ditunjukkan pada Gambar 10.
P3HT
Gambar 10 Struktur polimer poly3-heksilthiophene7
Poly(3-hexylthiophene) (P3HT) memiliki berat molekul 65,5 gram/mol merupakan semikonduktor organik tipe-p yang mendapat perhatian sangat besar saat ini karena polimer ini memiliki mobilitas hole yang tinggi jika digunakan sebagai material semikonduktor. Mobilitas hole P3HT sebesar 3.8 3.9 x 10-4 cm2/Vs8. Penggunaan material ini juga sangat sederhana, mudah dilarutkan dan konduktif. Oleh karena itu, P3HT dapat digunakan pada banyak aplikasi. Selain itu polimer ini relatif stabil terhadap perubahan suhu dan kondisi lingkungan. Penggunaan polimer juga dapat mengatasi masalah pada semikonduktor inorganik yang efektibilitas dan stabilitasnya yang rendah. Polimer organik memiliki gap yang lebih lebar dibandingkan dengan semikonduktor. Hal ini merupakan hal yang sangat mendukung untuk digunakan sebagai aplikasi sel surya.
Kitosan
Kitosan merupakan bahan dasar polielektrolit yang mengandung gugus amina dan gugus hidroksil, yang banyak digunakan sebagai bahan molekul transport aktif suatu anion dalam larutan. Kitosan memiliki sifat mudah terdegradasi, biocompatible dan tidak beracun. Sifat-sifat kitosan dihubungkan dengan adanya gugus amina dan karboksil yang terikat. Adanya gugus tersebut mengakibatkan kitosan mempunyai reaktivitas kimia yang baik dan penyumbang sifat elektrolit kation sehingga dapat berperan sebagai amino exchange. Gambar 11 menunjukkan struktur kitosan.
Gambar 11 Struktur kitosan9.
BAHAN DAN METODE
Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan Agustus 2010 - September 2011 di Laboratorium Biofisika dan Laboratorium Fisika Lanjut, Departemen Fisika IPB. Karakterisasi XRD dilakukan di Litbang Hasil Hutan, Departemen Kehutanan, Bogor. Alat dan Bahan
Alat yang digunakan dalam penelitian ini adalah hot plate, magnetic stirrer, pengaduk, pipet, tabung reaksi, gelas kimia, furnace, spektrofotometer UV-Vis, Interface scientific workshop 750 (PASCO), Radiometer, gelas ukur dan neraca analitik sedangkan bahan yang digunakan adalah kaca ITO (indium tin oxide), cadmium klorida (CdCl2), thiourea (H2NCSNH2), TEA(triethanolamine), polietilenglikol (PEG), asam borat (H3BO3), kitosan, poly3-heksiltiophene (P3HT), amonium hidroksida (NH4OH), asam asetat, dan akuades.
Metode Pembuatan dan Karakterisasi Pembuatan lapisan CdS
Lapisan CdS dibuat dengan metode CBD (chemical bath deposition) pada substrat kaca ITO. Dengan metode ini, film terdeposisi pada substrat dengan mencelupkan substrat ke dalam larutan yang mengandung ion-ion Cd2+ dan ion-ion sulfida S2- sambil dipanaskan serta diaduk.
Bahan-bahan yang digunakan adalah CdCl2 sebagai sumber ion kadmuim (Cd2+), thiourea sebagai sumber ion sulfur (S2-), larutan amonia sebagai agen pengkompleks (complexing agent), air destilasi dan TEA sebagai stabilizer agar larutan tidak cepat mengendap.
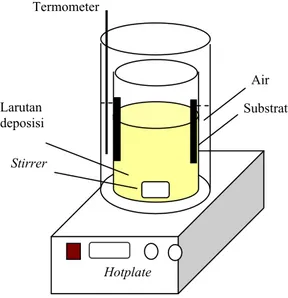
Skema metode CBD ditunjukkan pada Gambar 12, terdiri dari dua gelas piala dengan ukuran berbeda. Salah satunya berukuran kecil sehingga dapat dimasukkan ke dalam gelas yang lebih besar. Gelas yang kecil diisi larutan deposisi, kemudian
dimasukkan ke dalam gelas lebih besar yang diisi air. Sebelumnya, pada dinding sebelah dalam gelas kecil ditempel beberapa substrat kaca dengan ukuran yang telah ditentukan. Selanjutnya, kedua gelas diletakkan di atas pemanas (hot plate) yang dilengkapi pengaduk magnetik (magnetic stirrer).
Termometer
Gambar 12 Skema deposisi CBD Mula-mula dibuat larutan campuran 20 ml CdCl2 (0,1 M) dengan 20 ml Thiourea (1 M) di dalam gelas piala 100 ml. Larutan tersebut diletakkan di atas hot plate dipanaskan pada suhu 30o C dan diputar pada kelajuan 300 rpm selama 30 menit. Sebanyak 10 mL NH4OH (0.1 M) dan 5 ml TEA ditambahkan ke dalam larutan campuran tersebut. Larutan campuran tersebut dipanaskan pada suhu 70 oC dan diputar pada kelajuan 300 rpm selama 2 jam. Optimasi suhu dan waktu perlu dilakukan untuk mengatur morfologi, struktur, sifat dan ketebalan lapisan yang dihasilkan. Selanjutnya dilakukan annealing terhadap beberapa sampel film tipis CdS pada suhu 200 oC selama 1 jam.
Karakterisasi lapisan CdS
Sampel-sampel lapisan CdS yang berhasil ditumbuhkan dengan metode CBD selanjutnya dikarakterisasi dengan XRD dan spektroskopi UV-Vis. Karakterisasi XRD dilakukan untuk mengetahui struktur kristal CdS dan memastikan CdS telah tumbuh pada substrat. Pola-pola difraksi berupa puncak-puncak karakteristik orientasi kristal
Hotplate Substrat Stirrer Air Larutan deposisi 7