46
DAFTAR PUSTAKA
Agnes, 2006, Aplikasi Manajemen Database Pendidikan Berbasis Web dengan PHP dan MySQL, Yogyakarta : Andi Offset
Bundjali, B., Surdia N.M., Liang, O.B., Ariwahjoedi, B., 2004, JMS: Konstruksi Diagram Potensial-pH untuk Baja Karbon dalam Buffer Asetat secara Potensiodinamik Eksperimental, 9, 307-312
Bundjali, B., Surdia N.M., Liang, O.B., Ariwahjoedi, B., 2006, PROC. ITB Sains & Tek.: Pelarutan Besi Selektif pada Korosi Baja Karbon dalam Larutan Buffer Asetat, Natrium Bikarbonat - CO
2 Jenuh, 38, 149-161
CRC Handbook of Chemistry and Physics, 84th Edition (online version), CRC Press. Boca Raton, Florida, 2003; Section 4, Properties of the Elements and Inorganic Compounds; Physical Properties of the Rare Earth Metals Dalimunthe, I.S., 2004, e-USU: Kimia Dari Inhibitor Korosi, Universitas
Sumatera Utara
Hagerman, A.E., 2002, Tanin Chemistry, Miami University
J. Mabrour, M. Akssira, M. Azzi, M. Zertoubi, N. Saib, A. Messaoudi, A. Albizane, S. Tahiri, 2004, Corrosion Science: Effect of vegetal tanin on anodic copper dissolution in chloride solutions, 46, 1833-1847
Lower, S., 2007, Chem1 virtual textbook: Electrochemistry, Simon Fraser univ., Canada
Melfachrozi, Penggunaan Aplikasi E-learning (Moodle), 2006, http://e-learning.stsi-bdg.
Nestor Perez, 2004, Electrochemistry and Corrosion Science, Kluwer academic publishers.
Singh, N.P., Gupta, S.C., Sood, B.R., 1995, JCE: Resistance Measurement as a Tool for Corrosion Studies, 72, 465-466
Sinly Evan Putra, Sudrajat, Beni Hermawan, 2008, Ekstrak Bahan Alam sebagai Alternatif Inhibitor Korosi, Jurusan Kimia FMIPA Universitas Lampung Takeuchi Y., Buku Teks Pengantar Kimia (terjemahan), 2006, Tokyo, Iwanami
Shoten, Publishers, Tokyo
47
Trethewey, K.R., Chamberlain, J., 1991, Korosi untuk Mahasiswa Sains dan Rekayasa, Jakarta, Gramedia Pustaka Utama
Wibisono Y., 2006, Petunjuk Singkat Penggunaan Moodle bagi Pengajar, Universitas Pendidikan Indonesia
www.corrosiondoctor.com, 2003, The Theory for Aqueous Corrosion www.knovel.com, 2000, Thermodynamics Data and E-pH Diagrams www.metallographic.com, 2006, Data Storage GMR Copper Corrosion www.voltalab.com., 2005., Voltalab catalogue equipment
48
DAFTAR LAMPIRAN
Lampiran 1. Modul Praktikum Penentuan Laju Korosi Tembaga dengan Metode Pengurangan Berat Bahan (untuk siswa)
JUDUL: Pengukuran Laju Korosi Tembaga TUJUAN
1. Menentukan laju korosi logam tembaga melalui pengukuran berkurangnya berat tembaga pada beberapa pH larutan aqua regia
2. Mempelajari pengaruh penambahan inhibitor tanin terhadap laju korosi logam tembaga
TEORI
Korosi atau perkaratan merupakan fenomena kimia pada bahan-bahan logam. Pada dasarnya, korosi merupakan reaksi logam menjadi ion pada permukaan logam yang kontak langsung dengan lingkungan berair dan oksigen. Dalam kehidupan sehari-hari, korosi dapat dijumpai pada bangunan dan peralatan yang menggunakan komponen logam seperti: seng, tembaga, besi baja dan sebagainya. Tembaga adalah logam yang tidak bereaksi dengan air (H2O), tetapi oksigen di
udara akan bereaksi dengan tembaga secara perlahan pada suhu ruang membentuk lapisan tembaga oksida. Tembaga dalam air murni mempunyai sifat lebih mulia daripada hidrogen, akibatnya tidak akan terkorosi dalam air bebas oksigen dan laju korosinya pun lambat dalam air beroksigen. Lapisan yang terbentuk dari reaksi udara dengan tembaga mempunyai efek proteksi untuk korosi selanjutnya.
Proses yang terjadi pada korosi dimulai dari oskidasi bagian logam yang berfungsi sebagai anoda dan dipercepat dengan adanya oksigen, asam dan unsur yang lebih mulia, proses tersebut diilustrasikan sebagai berikut:
49
Pengujian laju korosi secara tradisional adalah dengan cara menimbang hilangnya berat bahan (weight loss) pada selang waktu kontak tertentu dengan lingkungan tetapi hal ini memerlukan waktu yang lama. Metode yang biasa dilakukan di laboratorium untuk pengurangan berat adalah menggunakan alat Corrosion Wheel test, di mana sampel dalam bentuk kupon diputar dalam selang waktu dan suhu tertentu sehingga proses korosi dapat lebih cepat berlangsung.
Berdasarkan pengamatan langsung, terlihat adanya perbedaan antara logam tembaga sebelum dan sesudah mengalami korosi. Demikian juga tampak adanya perbedaan warna pada beberapa pH. Secara kualitatif ini dapat digunakan untuk menunjukkan adanya proses korosi. Sedangkan untuk pengukuran secara kuantitatif sederhana, digunakan penimbangan berat bahan sebelum dan sesudah terjadi korosi. Selanjutnya data pengurangan berat (gram) tersebut dikonversikan ke dalam satuan laju korosi yaitu μm.tahun-1.
ALAT dan BAHAN Alat:
1. 1 set alat corrosion wheel test
2. Lempeng tembaga (ketebalan 0,5 mm) 3. Neraca analitis
4. Botol reaksi bervolume 250 mL Bahan:
1. Larutan aqua regia pH 1, 2 dan 4 2. Aquadest (ukur juga pH nya)
50 3. Etanol
4. Larutan tanin 10 ppm, 25ppm dan 40 ppm
PROSEDUR
Persiapan awal praktikum:
1. Buat sampel logam dalam bentuk kupon. Potong logam yang sebelumnya telah diampelas dengan dimensi sekitar 2 cm x 1 cm x 0,05 cm (diukur dengan jangka sorong) lalu dicuci dengan aquadest dan etanol. Catat dimensi kupon. 2. Timbang berat kupon kering menggunakan neraca analitis sebelum dimasukkan
ke dalam botol reaksi (gunakan pinset untuk memindahkan kupon logam). Catat berat kupon awal (m1).
3. Isi botol reaksi bervolume 250 mL dengan 200 mL larutan aqua regia pH 1 masukkan kupon ke dalamnya dan tutup rapat.
4. Simpan di rak botol alat wheel test. Botol dijepit dengan pemegang botol
5. Lakukan hal yang sama untuk tiga botol reaksi yang lainnya, dengan menggunakan pH aqua regia 2, 4 dan aquadest (blanko)
6. Putar alat corrosion wheel test dengan menghubungkan dinamo ke sumber arus listrik AC selama 18 jam pada suhu kamar.
Prosedur saat praktikum
1. Hentikan putaran alat lalu keluarkan kupon dengan menggunakan pinset
2. Cuci kupon menggunakan aquadest dan lap dengan kertas tissue yang telah dibasahi etanol
3. Timbang berat kupon. Catat sebagai berat kupon akhir (m2)
4. Hitung selisih berat kupon (∆m) untuk setiap pH aqua regia dan blanko aquadest
5. Hitung laju korosi pada setiap pH tembaga dari setiap kondisi percobaan
6. Bandingkan warna tembaga sebelum terkorosi dan sesudah terkorosi. Catat warna tembaga dari setiap kondisi percobaan.
Lakukan prosedur yang sama, dengan menggunakan pH 2 dan membuat variasi penambahan inhibitor tanin, yaitu:
51
200 mL larutan + 0 ppm tanin, 200 mL larutan + 10 ppm tanin, 200 mL + 25 ppm tanin dan 200 mL tanin + 40 ppm
PERTANYAAN
Berdasarkan percobaan di atas,
1. Bagaimana pengaruh pH terhadap laju korosi tembaga ?
2. Bagaimana perubahan warna pH tinggi dan rendah dibandingkan dengan aquadest ?
3. Jelaskan pengaruh penambahan inhibitor tanin terhadap laju korosi tembaga ? 4. Adakah perubahan warna yang terlihat sebelum dan sesudah penambahan
inhibitor ?
5. Tuliskan reaksi redoks yang terjadi pada korosi logam tembaga ?
6. Sebutkan metode lain yang dapat digunakan untuk mengukur laju korosi suatu logam?
52
Lampiran 2. Modul Praktikum Penentuan Laju Korosi dengan Metode Pengurangan Berat Bahan (Panduan Guru)
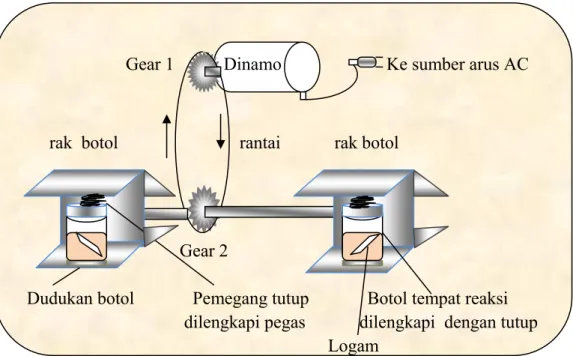
Sebelumnya rancanglah 2 buah alat seperti skema Gambar 1. Rancangan alat dapat disesuaikan dengan ketersediaan bahan yang dimiliki sekolah, seperti rancangan yang terlihat pada Gambar 2. Untuk mengatur kecepatan putaran tempat botol dapat digunakan variabel condensator (varco) yang dihubungkan ke dynamo. Buat agar alat ini berputar dengan kecepatan putaran di bawah 20 rpm dalam keadaan kosong tanpa beban botol. Dalam skema rancangan, alat tersebut dapat menampung 4 botol reaksi dengan posisi botol saling berlawanan sehingga diharapkan putarannya seimbang.
Alat yang pertama, digunakan untuk melihat percobaan pengaruh pH terhadap tingkat korosifitas tembaga. Sedangkan alat yang kedua untuk melihat pengaruh jumlah inhibitor terhadap tingkat korosifitas tembaga pada satu pH tertentu saja.
Pada praktikum ini siswa dibagi menjadii 2 kelompok besar. Persiapan praktikum dilakukan sehari sebelum praktikum atau sekitar 18 jam sebelum praktikum (dapat dilakukan di luar jam pelajaran) sehingga praktikan dapat melihat hasilnya pada saat hari praktikum.
JUDUL: Pengukuran Laju Korosi Tembaga TUJUAN
1. Menentukan laju korosi logam tembaga melalui pengukuran berkurangnya berat tembaga pada beberapa pH aqua regia
2. Mempelajari pengaruh penambahan inhibitor tanin terhadap laju korosi logam tembaga
TEORI
Korosi atau perkaratan merupakan fenomena kimia pada bahan-bahan logam. Pada dasarnya, korosi merupakan reaksi logam menjadi ion pada permukaan
53
logam yang kontak langsung dengan lingkungan berair dan oksigen. Dalam kehidupan sehari-hari, korosi dapat dijumpai pada bangunan dan peralatan yang menggunakan komponen logam seperti: seng, tembaga, besi baja dan sebagainya. Tembaga adalah logam yang tidak bereaksi dengan air (H2O), tetapi oksigen di
udara akan bereaksi dengan tembaga secara perlahan pada suhu ruang membentuk lapisan tembaga oksida. Tembaga dalam air murni mempunyai sifat lebih mulia daripada hidrogen, akibatnya tidak akan terkorosi dalam air bebas oksigen dan laju korosinya pun lambat dalam air beroksigen. Lapisan yang terbentuk dari reaksi udara dengan tembaga mempunyai efek proteksi untuk korosi selanjutnya.
Proses yang terjadi pada korosi dimulai dari oskidasi bagian logam yang berfungsi sebagai anoda dan dipercepat dengan adanya oksigen, asam dan unsur yang lebih mulia, proses tersebut diilustrasikan seperti pada korosi tembaga berikut:
Pengujian laju korosi secara tradisional adalah dengan cara menimbang hilangnya berat bahan (weight loss) pada selang waktu kontak tertentu dengan lingkungan tetapi hal ini memerlukan waktu yang lama. Metode yang biasa dilakukan di laboratorium untuk pengurangan berat adalah menggunakan alat Corrosion Wheel test, di mana sampel dalam bentuk kupon diputar dalam selang waktu dan suhu tertentu sehingga proses korosi dapat lebih cepat berlangsung.
Berdasarkan pengamatan langsung, terlihat adanya perbedaan antara logam tembaga sebelum dan sesudah mengalami korosi. Demikian juga tampak adanya
54
perbedaan warna pada beberapa pH. Secara kualitatif ini dapat digunakan untuk menunjukkan adanya proses korosi. Sedangkan untuk pengukuran secara kuantitatif sederhana, digunakan penimbangan berat bahan sebelum dan sesudah terjadi korosi. Selanjutnya data pengurangan berat (gram) tersebut dikonversikan ke dalam satuan laju korosi yaitu μm.tahun-1.
ALAT dan BAHAN Alat:
1. Set alat corrosion wheel test
2. Lempeng tembaga, ketebalan 0,5 mm 3. Neraca analitis
4. Botol reaksi bervolume 250 mL Bahan:
1. Larutan aqua regia pH 1, 2 dan 4 2. Aquadest (ukur juga pHnya) 3. Etanol
4. Larutan tanin 10 ppm, 25 ppm dan 40 ppm
PROSEDUR
Gear 1 Dinamo Ke sumber arus AC
rak botol rantai rak botol
Gear 2
Dudukan botol Pemegang tutup Botol tempat reaksi dilengkapi pegas dilengkapi dengan tutup
Logam
55
Gambar 2. Salah satu rancangan alat Corrosion Wheel Test yang dimodifikasi Persiapan awal praktikum:
1. Buat sampel logam dalam bentuk kupon. Potong logam yang sebelumnya telah diampelas dengan dimensi sekitar 2 cm x 1 cm x 0,05 cm (diukur dengan jangka sorong) lalu dicuci dengan aquadest dan etanol. Catat dimensi kupon.
2. Timbang berat kupon kering menggunakan neraca analitis sebelum dimasukkan ke dalam botol reaksi (gunakan pinset untuk memindahkan kupon logam). Catat berat kupon awal (m1).
3. Isi botol reaksi bervolume 250 mL dengan 200 mL larutan aqua regia pH 1 masukkan kupon ke dalamnya dan tutup rapat.
4. Simpan di rak botol alat wheel test. Botol dijepit dengan pemegang botol. 5. Lakukan hal yang sama untuk tiga botol reaksi yang lainnya, dengan
menggunakan pH aqua regia 2, 4 dan aquadest (blanko)
6. Putar alat corrosion wheel test dengan menghubungkan dinamo ke sumber arus listrik AC selama 18 jam pada suhu kamar.
Prosedur saat praktikum
1. Hentikan putaran alat lalu keluarkan kupon dengan menggunakan pinset
2. Cuci kupon menggunakan aquadest dan lap dengan kertas tissue menggunakan etanol
56
4. Hitung selisih berat kupon (∆m) untuk setiap pH aqua regia dan blanko aquadest
5. Hitung laju korosi pada setiap pH percobaan, dengan melihat contoh perhitungan berikut:
misal
Pada pH aqua regia 2,89 terjadi pengurangan berat (∆m) sebesar 0,0126 gram Massa jenis logam Cu = 8,96 gram.cm-3 (dari Handbook CRC)
Lama pengkorosian = 18 jam atau 0,75 hari atau 0,0021 tahun (1 thn = 365 hari)
Dimensi kupon Cu adalah 2 cm x 1,05 cm x 0,04 cm maka
Luas selimut kupon (L):
L = 2.(2 cm x 1,05 cm) + 2.(1,05 cm x 0,04 cm) + 2.(2 cm x 0,04 cm) = 4,444 cm2
Volume kupon yang hilang: ∆V = ∆m /ρ
= (0,0126 gram) / (8,96 gram.cm-3 ) = 0,00141 cm3
Ketebalan kupon yang hilang ∆t = ∆V / L
= 0,00141 cm3 / 4,444 cm2 = 0,000316 cm
Laju korosi (CR) dalam μm.tahun-1 adalah : CR = 0,000316.104 / 0,0021 = 1540,00 μm.tahun-1
Lakukan prosedur yang sama, dengan menggunakan pH 2 dan membuat variasi penambahan inhibitor tanin, yaitu:
200 mL larutan + 0 ppm tanin, 200 mL larutan + 10 ppm tanin, 200 mL + 25 ppm tanin dan 200 mL tanin + 40 ppm
57 PERTANYAAN
Berdasarkan percobaan di atas,
1. Bagaimana pengaruh pH terhadap laju korosi tembaga ?
2. Bagaimana perubahan warna pH tinggi dan rendah dibandingkan dengan aquadest ?
3. Jelaskan pengaruh penambahan inhibitor tanin terhadap laju korosi tembaga ? 4. Adakah perubahan warna yang terlihat sebelum dan sesudah penambahan
inhibitor ?
5. Tuliskan reaksi redoks yang terjadi pada korosi logam tembaga ?
6. Sebutkan metode lain yang dapat digunakan untuk mengukur laju korosi suatu logam?
58 Lampiran 3 Lembar Pengamatan Siswa
Nama siswa: ... Kelas: ... Tanggal Percobaan: ...
Judul Percobaan: ... ... ...
Hasil Pengamatan:
A. Pengaruh peningkatan pH terhadap laju korosi
pH larutan Berat awal m1, gram Berat akhir m2, gram Selisih berat gram Luas kupon, cm2 Volume kupon cm3 Ketebalan yg hilang, cm Laju korosi μm.th-1 1 2 4 Aquades
B. Pengaruh peningkatan konsentrasi tanin terhadap laju korosi Konsent. tanin, ppm Berat awal m1, gram Berat akhir m2, gram Selisih berat gram Luas kupon, cm2 Volume kupon cm3 Ketebalan yg hilang, cm Laju korosi μm.th-1 0 10 25 40
59 C. Perhitungan-perhitungan ... ... ... ...
D. Diskusi dan pembahasan
... ... ... ... ... E. Kesimpulan ... ... ... F. Jawaban pertanyaan ... ... ... ... ... ... ...
Paraf orang tua siswa Paraf guru