PEMERIKSAAN INHIBITOR FAKTOR VIII DENGAN MENGGUNAKAN SYSMEX CS2100i
Departemen Ilmu Patologi Klinik FK UH-RSUP dr.WAHIDIN SUDIROHUSODO Makassar
I . PENDAHULUAN
Inhibitor faktor VIII adalah suatu poliklonal antibodi imunoglobulin (Ig) G dengan afinitas tinggi, yang dapat menetralisasi aktivitas faktor VIII dan berfungsi menghancurkan substansi yang tidak dikenali. Penderita hemofilia A lebih sering membentuk inhibitor dibandingkan hemofilia B dengan prevalensi sekitar 20-40% pada penderita dengan hemofilia A dan 1-6% pada penderita hemofilia B. Pada hemofilia B, inhibitor lebih jarang terjadi, kira-kira 1 diantara 100 penderita. Prevalensi pasien hemofilia A yang mengalami inhibitor dua kali lebih banyak pada pasien kulit hitam dibanding kulit putih. Insiden terbentuknya inhibitor pada hemofilia berkisar 20-40% pada penderita hemofilia berat, jarang terjadi pada penderita hemofilia ringan dan sedang.1,2
314 kasus.1,4. Salah satu komplikasi berat pada penderita hemofilia adalah terbentuknya neutralizing alloantibody atau inhibitor.1,3,4
Penderita hemofilia A, B, atau C, inhibitor langsung melawan faktor VIII, IX, atau XI selama diberikan terapi pengganti. Inhibitor dapat mengenai 1 diantara 5 penderita hemofilia A berat pada suatu ketika dalam hidupnya.1,3,4
Rerata insiden terbentuknya faktor inhibitor adalah usia 12 tahun, namun sebagian besar inhibitor timbul ketika anak masih sangat muda yaitu setelah ±10 kali menerima infus rekombinan faktor VIII, dengan rerata usia 1 – 2 tahun. Inhibitor dapat timbul antara 10-20 hari pengobatan terhadap faktor VIII, dan menghilang sendiri dalam rerata kurun waktu 9 bulan pada sekitar 60 % penderita, sedangkan sisanya (40%) menetap.1,3
Koagulasi dimulai dengan dua mekanisme yang berbeda, yaitu proses aktifasi kontak dan kerja dari tissue factor. Rangkaian dimulai dari tempat terjadinya kerusakan endotel dengan aktivasi kontak FXII menjadi FXIIa. (aktivasi endogen). F XIIa kemudian mengaktivasi PKK menjadi kalikrein yang meningkatkan aktivasi F.XII fase kontak dengan umpan balik positif untuk menguatkan). FXIIa mengaktivasi FXI menjadi FXIa. Selanjutnya faktor XIa mengaktivasi FIX menjadi FIXa, dan seterusnya sampai akhirnya terbentuk monomer fibrin dari fibrinogen . Monomer ini secara bersama-sama akan diikat secara kovalen oleh F XIII (transamidase) menjadi benang fibrin . Jika lukanya luas, trombokinase jaringan (faktor III) akan ikut mengadakan kontak dengan darah dan mengaktivasi faktor VII yang ada dalam kompleks bersama Ca+2 dan fosfolipid mengaktivasi faktor X seperti pada gambar 1 kaskade koagulasi.5,6
Gambar 1. Kaskade Koagulasi.5
proses hemostatis dan merupakan jalur bersama antara jalur intrinsik dan jalur ekstrinsik. Kekurangan salah satu dari FVIIIa atau FIXa menyebabkan penurunan aktifitas platelet tenase, pada keadaan ini maka format klot akan melambat oleh karena pembentukan thrombin sangat menurun, sumbat trombosit yang terjadi akan rapuh yang menyebabkan mudah terjadi perdarahan.5,6
mengandung inhibitor, dan yang lain hanya plasma normal; kemudian diinkubasi selama 2 jam pada suhu 37oC. 2,4,7
Tutorial ini membahas Metoda kuantitatif, umumnya dilakukan untuk mencari inhibitor yang time dependent, yaitu jika sampel yang mengandung inhibitor faktor VIII dicampur dengan plasma normal maka sejumlah faktor VIII akan dinetralisasi. Jika faktor VIII yang ditambahkan dan waktu inkubasi dapat distandardisasi maka kekuatan faktor inhibitor dapat diukur berdasarkan jumlah aktivitas faktor VIII yang tersisa, dan hasilnya dilaporkan dalam satuan Bethesda Unit (BU).2,4,7
II. TUJUAN
Tutorial ini bertujuan untuk mengetahui kadar inhibitor faktor VIII pada penderita hemofilia.2,4 Natrium sitrat (0,109 M ) yang dicampur dengan darah vena 1: 9. Gunakan tabung sitrat berlapis silicon, ambil darah sesuai volume yang tercantum pada tabung. Segera sentrifugasi sedikitnya 3000 rpm selama 10 menit.4,7
Preparasi material untuk kalibrasi inhibitor F VIII:
Material Volume Preparasi
Coagulation Factor VIII Deficient Plasma
Preparasi Sampel untuk pemeriksaan inhibitor faktor VIII:
200 µl 200 µl 200 µl Campurkan, lalu
homogenisasikan dengan baik Tabung 2
(pengenceran ½)
Ambil 200 µl dari campuran tabung 1
200 µl 200 µl Campurkan, lalu homogenisasikan dengan baik Tabung 3
(pengenceran ½)
Ambil 200 µl dari campuran tabung 2
200 µl 200 µl Campurkan, lalu homogenisasikan dengan baik Lakukan inkubasi untuk tabung 1,2,3, dalam waterbath suhu 37 OC selama 2 jam
3. Alat dan Bahan
a) Alat yang digunakan Sysmex CS2100i b) Sentrifus
c) Waterbath d) Tabung reaksi e) Mikropipet 200 µl
Sysmex CS2100i Unit komputer Sentrifus
Dalam alat Sysmex 2100i Waterbath
Mikropipet
Coag. FVIII Pathrombin CaCl2 OVB Buffer Ca Clean
Kontrol N Kontrol P SHP Sampel
Gambar 2. Alat dan bahan Tes Inhibitor Faktor VIII menggunakan CS2100i (Sumber: Pribadi dan Package insert kit Sysmex CS2100i
B. Analitik
1. Prinsip Tes :
VIII ditambah ke plasma yang mengandung inhibitor dan diinkubasi maka faktor VIII tersebut akan dinetralisasi. Sisa faktor VIII yang tidak dinetralisasi merupakan residu faktor VIII yang diukur. Hasil tersebut kemudian dikonfirmasi menggunakan kurva Bethesda untuk mendapat nilai Bethesda Unit (BU). Bethesda Unit dikenal juga sebagai inhibitor unit, dimana 1 BU menyatakan terdapat sejumlah inhibitor faktor VIII yang menyebabkan berkurangnya aktivitas faktor VIII sebesar 50%. 2,4
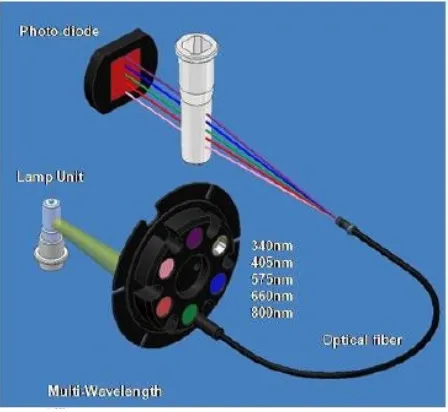
Gambar 3 : Multi-Wavelength Detection System2
F VIII sampel + (FIXa-PL-Ca++) FVIIIa-FIXa-PL- Ca++complex
FVIIIa-FIXa-PL- Ca++complex
F X F Xa
2. Cara Kerja :
(1) Periksalah ketersediaan aquadest, reaction tube, kertas printer, isi kembali bila kurang.
(2) Periksalah keadaan botol limbah, kosongkan bila perlu.
(3) Siapkan reagent secukupnya.
(4) Periksalah saluran selang, power connection, pastikan kabel power menempel pada stop kontak dengan benar.2
b) Prosedur menghidupkan alat
(1) Hidupkan komputer, printer dan power pada Main Unit.
(2) Selama melakukan self check, splash screen akan menutup otomatis
(3) Klik Lab, ketik lab lalu Enter
(5) Masukkan reaction tube ke dalam tempatnya2
c) Preparasi Reagen
(2) Letakkan semua reagen yang diperlukan dan Ca clean di dalam rack reagen
(7) Klik OK untuk scannning barcode reagent.
(8) Bila scanning barcode gagal, akan muncul tampilan seperti dibawah ini.
(9) Setelah seluruh reagen terbaca pada reagen scan, klik pad tiap icon reagent lalu klik Lot Group Setting, lalu isi cecklist pada kotak yang tersedia.
d) Cara kalibrasi / mencari kurva standar F VIII residual
(1) Campurkan Coagulation factor VIII Deficient Plasma 200 ul dengan Kontrol Plasma Normal 200 ul, lalu homogenisasikan dengan baik. Kemudian inkubasi dalam waterbath suhu 37 0C selama 2 jam.
(2) Setelah inkubasi selama 2 jam, letakkan material untuk kalibrasi inhibitor faktor VIII di posisi reagen.
(3) Jika reagen yang dibutuhkan sudah terscan dengan benar , tekan [Order].
(4) Tekan [Switch Order], lalu pilih [Holder Calib Curve]. (5) Pilih pemeriksaan INH8.
(6) Tekan No. lot reagen dan material yang akan digunakan dan isi assay value dengan konsentrasi 100 %.
(7) Tekan [Ok] lalu tekan [Regist].
(8) Tekan [Job List] , pastikan order sudah ada pada Job List, jika sudah, Tekan START.
(9) Setelah proses kalibrasi selesai, tekan menu [Calibration curve].
(10) Tekan [Change], pilih parameter INH8, dan pilih no lot reagen yang digunakan, lalu tekan [Validate] untuk melakukan validasi kurva.
(11) Kalibrasi / kurva standar baru harus dilakukan setiap kali sebelum pengerjaan sampel F VIII residual. Kurva bisa digunakan untuk sampel yang lain dalam hari pengerjaan yang sama.2,7
e). Quality Control
(3) Tekan [Order] lalu tekan [Order Entry] lalu pilih QC
(6) Hasil QC akan secara otomatis disimpan pada alat . Hasil di dapat dari alat : sec dan % aktivitas.
f) Pengerjaan Sampel
(1) Setelah pengerjaan kalibrasi residual faktor VIII, letakkan 3 tabung pengeceran sampel pemeriksaan inhibitor F VIII di rak.
(5) Tekan [Job List], pastikan order sampel sudah ada pada job list, lalu tekan START.
(6) Hasil sampel akan secara otomatis disimpan pada alat . Hasil didapat dari alat : sec dan % aktivitas F VIII residual.
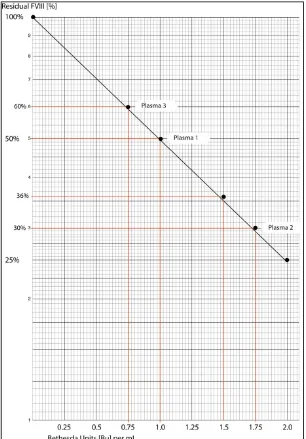
(8) Plotkan hasil % aktivitas FVIII residual yang paling mendekati 50 % tersebut ke grafik Bethesda Curve.
(9) Hasil Bethesda Unit yang didapat dikalikan dengan pengenceran sampel tersebut .
(10) Jika kandungan inhibitor di dalam sampel terlalu tinggi, maka pengenceran awal harus diperbesar (>1/8 )2,
(11) Manual dalam alat :
10 l sampel + 40 l OVB + 50 l Deficient Factor VIII
+ 50 l Prathrombin SL + 50 l CaCl2.
a. Reagen I (40 l OVB): ditambahkan pada detik ke 30”, kemudian diinkubasi
b. Reagen II(50l Deficient Factor VIII): ditambahkan pada detik ke 60”, kemudian diinkubasi
c. Reagen III(50l Prathrombin): ditambahkan pada detik ke
60”, kemudian diinkubasi
d. Reagen IV(50l CaCl2) ditambahkan pada detik ke 60”, kemudian di inkubasi , hasil dapat di baca setelah 240 detik kemudian.
C. PASCA ANALITIK
Interpretasi hasil pemeriksaan berdasarkan aktivitas residual faktor VIII adalah sebagai berikut :
Residu F VIII 80-100% : sampel tidak mengandung inhibitor
Residu F VIII 60-80 % : borderline, artinya perlu dilakukan pengulangan dengan sampel baru sebelum menentukan diagnosis
DAFTAR PUSTAKA
1. Yantie VK, Ariawati K, Inhibitor in Hemophilia ; Jurnal MEDICINA 2012, vol.43, 31-6
2. Wirawan R, Shaping Hematology & Pleural Body Fluid Analysis: Automation vs Conventional Method, PT Sysmex Indonesia: XN-Series – The Next Generation in Hematology, Symposium in PIT IX 2012, www.sysmex.co.id
3. Kempton CL and White GC, How we treat a hemophilia A patient with a factor VIII inhibitor, Blood , Jan 2009 , Volume 113, No.1 : 11-17
4. Kasper CK, Diagnosis and Management of inhibitors to factors VIII and IX, Treatment of Hemophilia, Canada, WFH, 2004 No 34 : 1-12, www.wfh.org
5. Setiabudy Rd. Fisiologi Hemostasis dan Fibrinolisis. Dalam: Hemostasis dan Trombosis. Edisi ke-4. Jakarta. Balai penerbit FKUI.2007:1-10
6. Silbernagl S, Lang F, Hemostatis dan gangguannya dalam Teks & Atlas berwrna Patofisiologi, Jakarta , EGC 2003 : 60-63
7. Kit Siemens, Coagulation Factors VIII, IX, XI and XII Deficient Plasma in Hemostatis products Reference , Guide,3rd Edition, 2004
8. Hoffbrand AV, Pettit JE. Kapita Selekta Hematologi. Edisi ke-4. Jakarta.EGC 2005: 225-229