BAB II
KAJIAN TEORI
2.1. Pendekatan Belajar
Menurut teori belajar kontekstual, belajar terjadi hanya ketika
siswa memproses informasi maupun pengetahuan baru sedemikian rupa
sehingga informasi tersebut beradaptasi dengan kerangka acuan mereka.
Pendekatan ini menganggap bahwa pikiran manusia secara alamiah
mencari makna dalam suatu konteks, yaitu berkaitan dengan
lingkungan seseorang.
Dari pemahaman pendekatan teori belajar di atas, belajar
hendaknya memfokuskan pada banyak aspek dari lingkungan belajar,
sekolah, laboratorium, maupun lingkungan sekitar siswa. Dengan
demikian, siswa akan menemukan hubungan yang bermakna antara ide
abstrak dan aplikasi praktis dikonteks dunia nyata, dan konsep
diinternalisasi melalui proses penemuan, penguatan, dan pengaitan.
Menurut David Kolb, (dalam Ekohariadi, 2002) Siswa belajar
cenderung menerima informasi secara abstrak (thinking) maupun
kongkrit (feeling) dan lalu memproses informasi secara aktif (doing)
maupun reflektif (watching). Namun masih menurut Kolb, kebanyakan
siswa mempunyai kecenderungan belajar dengan cara kongkrit
cenderung mengajar dengan cara abstrak (penekanan pada thinking dan
watching).
Dalam penelitian ini, peneliti berusaha melakukan pendekatan
belajar dengan membiasakan siswa menerima dan memproses informasi
melalui pengalaman dan eksperimen kongkrit.
Dalam menggunakan metode eksperimen, menurut Winarno
Surakhmad (1986) ada beberapa kelemahan, seperti keterbatasan alat
yang mengakibatkan tidak semua siswa dapat memperoleh kesempatan
untuk melakukan eksperimen dan jika dalam pelaksanaannya
membutuhkan waktu yang cukup lama dapat menghambat pelajaran
selanjutnya, juga kurangnya persiapan dan pengalaman siswa dapat
menimbulkan kesulitan dalam pelaksanaan eksperimen tersebut.
Namun menurut Aripin (1995), keuntungan dalam menggunakan metode
eksperimen lebih banyak manfaatnya, antara lain dapat memberikan
pengalaman praktis serta ketrampilan dalam menggunakan alatalat
praktikum, memberikan gambaran yang konkrit tentang suatu peristiwa
sehingga siswa tidak mudah percaya pada sesuatu yang belum pasti
kebenarannya sebelum mereka mengamati secara langsung, serta
melatih siswa lebih aktif dan mengembangkan cara berpikir ilmiah.
Eksperimen tidak harus dilakukan dengan menggunakan peralatan dan
bahan kimia yang mahal, tetapi dapat dilaksanakan dengan
menggunakan peralatan sederhana yang didesain sendiri oleh guru.
Alat peraga adalah segala sesuatu yang digunakan untuk
menjelaskan konsep pembelajaran dari materi yang bersifat abstrak
menjadi nyata sehingga dapat merangsang pikiran, perasaan, perhatian
dan minat siswa yang menjurus ke arah terjadinya proses belajar
mengajar. Penggunaan alat peraga dalam pembelajaran sangat
dianjurkan, karena dengan memanfaatkan alat peraga yang sesuai
dengan materi, pembelajaran kimia akan lebih efektif dengan langsung
1. Alat untuk memperjelas bahan pembelajaran pada saat guru
menyampaikan pelajaran.
2. Alat untuk mengangkat atau menimbulkan persoalan untuk dikaji
lebih lanjut dan dipecahkan oleh para peserta didik dalam proses
belajarnya.
3. Sumber belajar bagi siswa baik secara individu ataupun kelompok.
4. Melalui alat peraga siswa terbantu dalam memahami konsep kimia
Dalam penelitian ini, alat peraga yang digunakan adalah
molarimeter optik yang didesain sendiri oleh guru. Molarimeter optik
adalah alat yang dapat digunakan untuk mengukur konsentrasi larutan.
Dengan alat ini pula siswa dapat mengamati perubahan konsentrasi
larutan setelah pengenceran. Prinsip kerja alat ini adalah interaksi
antara cahaya dengan materi.
Besar penyerapan cahaya (absorbansi) dari suatu kumpulan
atom/molekul dinyatakan oleh Hukum BeerLambert.
1. Hukum Lambert menyatakan bahwa proporsi berkas cahaya datang
yang diserap oleh suatu bahan/medium tidak bergantung pada
intensitas berkas cahaya yang datang. Hukum Lambert ini tentunya
hanya berlaku jika di dalam bahan/medium tersebut tidak ada
reaksi kimia ataupun proses fisis yang dapat dipicu atau diimbas
oleh berkas cahaya datang tersebut. Dalam hal demikian, intensitas
cahaya yang keluar setelah melewati bahan/medium tersebut dapat
dituliskan dalam bentuk sederhana sbb.:
I = T x I0,
dimana I adalah intensitas berkas cahaya keluar, I0 adalah intensitas
berkas cahaya masuk/datang, dan T adalah transmitansi. Jika
transmisi dinyatakan dalam prosentase, maka
%T = (I/I0) x 100 (dalam satuan %)
2. Hukum Beer menyatakan bahwa absorbansi cahaya berbanding
lurus dengan konsentrasi dan ketebalan bahan/medium, yakni
dimana ε adalah molar absorbsitivitas untuk panjang gelombang
tertentu, atau disebut juga sebagai koefisien ekstinsif (dalam l mol1
cm1)),
c adalah konsentrasi molar (mol l1),
l adalah panjang/ketebalan dari bahan/medium yang dilintasi
oleh cahaya (cm).
Kombinasi dari kedua hukum tersebut (Hukum BeerLambert) dapat
dituliskan sebagai berikut:
%T = (I/I0) x 100 = exp(− ε c l)
atau
A = log (I0/I) = c l.ε
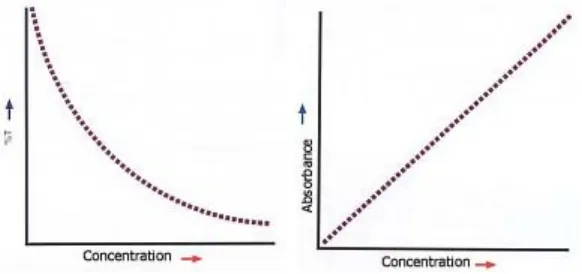
Gambar di bawah menunjukkan plot %T vs. c dan A vs. c. Bentuk
persamaan terakhir menyatakan sebuah hubungan penting, yakni
absorbansi A memiliki hubungan linier dengan konsentrasi c (A µ c) dan
dapat ditentukan dengan mengukur ratio antara intensitas cahaya
setelah melewati bahan/medium dan intensitas sebelum melewati
bahan/medium.
Karena sifat hubungan linieralitas antara A dan c, penentuan
konsentrasi bahan/sampel dapat dilakukan dengan lebih mudah jika
bekerja dengan absorbansi A daripada bekerja dengan transimisi %T.
Konsentrasi dapat ditentukan lewat perkalian atau pembagian
sederhana dari nilai koefisien molar ekstinsi yang telah diketahui.
2.3. Molaritas
Konsentrasi adalah istilah umum untuk menyatakan banyaknya
bagian zat terlarut dan pelarut yang terdapat dalam larutan. Konsentrasi
dapat dinyatakan secara kuantitatif maupun secara kualitatif. Untuk
ukuran secara kualitatif, konsentrasi larutan dinyatakan dengan istilah
larutan pekat (concentrated) dan encer (dilute). Kedua istilah ini
menyatakan bagian relatif zat terlarut dan pelarut dalam larutan.
Larutan pekat berarti jumlah zat terlarut relatif besar, sedangkan
Molaritas atau kemolaran menyatakan jumlah mol zat terlarut (n)
Titrasi biasanya dibedakan berdasarkan jenis reaksi yang terlibat di
dalam proses titrasi, sebagai contoh bila melibatkan reaksi asam basa
maka disebut sebagai titrasi asam basa, titrasi redox untuk titrasi yang
melibatkan reaksi reduksi oksidasi, titrasi kompleksometri untuk titrasi
yang melibatkan pembentukan reaksi kompleks dan lain sebagainya.
(disini hanya dibahas tentang titrasi asam basa).
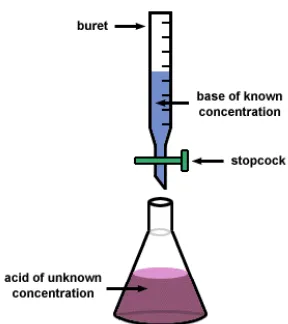
Zat yang akan ditentukan kadarnya disebut sebagai “titrant” dan
biasanya diletakan di dalam Erlenmeyer, sedangkan zat yang telah
diketahui konsentrasinya disebut sebagai “titer” dan biasanya diletakkan
Gambar 2.1. Proses Titrasi
Prinsip Titrasi Asam Basa
Titrasi asam basa melibatkan asam maupun basa sebagai titer
ataupun titrant. Titrasi asam basa berdasarkan reaksi penetralan. Kadar
larutan asam ditentukan dengan menggunakan larutan basa dan
sebaliknya.
Titrant ditambahkan titer sedikit demi sedikit sampai mencapai
keadaan ekuivalen (artinya secara stoikiometri titrant dan titer tepat
habis bereaksi). Keadaan ini disebut sebagai “titik ekuivalen”.
Pada saat titik ekuivalen, proses titrasi dihentikan, kemudian kita
mencatat volume titer yang diperlukan untuk mencapai keadaan
tersebut. Dengan menggunakan data volume titrant, volume dan
konsentrasi titer kita bisa menghitung kadar titrant.
Cara Mengetahui Titik Ekuivalen
Ada dua cara umum untuk menentukan titik ekuivalen pada
1. Memakai pH meter untuk memonitor perubahan pH selama titrasi
dilakukan, kemudian membuat plot antara pH dengan volume titrant
untuk memperoleh kurva titrasi. Titik tengah dari kurva titrasi
tersebut adalah “titik ekuivalent”.
indikator yang berbahan warna dipengaruhi oleh pH. Penambahan
indikator diusahakan sesedikit mungkin dan umumnya adalah dua
hingga tiga tetes.
Untuk memperoleh ketepatan hasil titrasi maka titik akhir titrasi
dipilih sedekat mungkin dengan titik equivalen, hal ini dapat dilakukan
dengan memilih indikator yang tepat dan sesuai dengan titrasi yang
Molekuivalen diperoleh dari hasil perkalian antara Normalitas dengan
Bahan-bahan yang diperlukan dalam pembuatan molarimeter optik:
Transistor 2N3906 4 biji LED superbright biru, merah, kuning, hijau 1 biji
Volt meter 4
Aluminium 50 x 50 cm
Cuvet (tempat larutan/sampel) 4
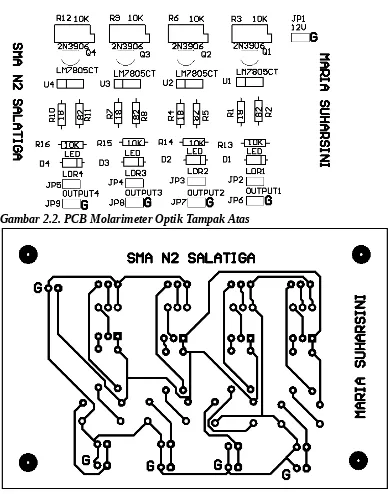
a. Rancangan alat seperti gambar berikut :
Gambar 2.2. PCB Molarimeter Optik Tampak Atas
Gambar 2.4. Skema Molarimeter Optik