Aplikasi Prinsip Kinetika
t k
untuk
Penentuan Masa Simpan
Produk Pangan
•• Penelitian &
Penelitian &
pengujian
pengujian
UMUR SIMPAN
UMUR SIMPAN
PENENTUAN UMUR SIMPAN
PENENTUAN UMUR SIMPAN
•• pengalaman
pengalaman
empiris
empiris
Informasi yang diperlukan:
Informasi yang diperlukan:
Purwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011
y g p
y g p
•• Identifikasi faktor kritis
Identifikasi faktor kritis
•• batasan mutu dan batas mutu minimum yang
batasan mutu dan batas mutu minimum yang
diharapkan/dijanjikan (masih layak dijual?)
diharapkan/dijanjikan (masih layak dijual?)
•• parameter kinetika penurunan mutu (E
parameter kinetika penurunan mutu (E
aa, Q
, Q
1010, dll)
, dll)
•• kondisi mutu awal
kondisi mutu awal
KINETIKA PENURUNAN MUTU
KINETIKA PENURUNAN MUTU
--dQ/dt = kQ
dQ/dt = kQ
n
n
Q = kualitas (mutu)
Q = kualitas (mutu)
t = waktu
t = waktu
k = konstanta laju penurunan mutu
k = konstanta laju penurunan mutu
k konstanta laju penurunan mutu
k konstanta laju penurunan mutu
n = ordo reaksi penurunan mutu
n = ordo reaksi penurunan mutu
100
100
Penurunan Mutu Ordo Nol (n=0)
Penurunan Mutu Ordo Nol (n=0)
--dQ/dt = k
dQ/dt = k
atau
atau
Q
Q
tt
= Q
= Q
0
0
-- kt
kt
100
100
80
80
60
60
40
40
20
20
alitas (mutu)
relatif
alitas (mutu)
relatif
Purwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011
20
20
00
0 2 4 6 8 10
0 2 4 6 8 10
Waktu penyimpanan (bulan)
Waktu penyimpanan (bulan)
Ku
a
Ku
a
Penurunan Mutu Ordo Nol (n=0)
Penurunan Mutu Ordo Nol (n=0)
--dQ/dt = k
dQ/dt = k
atau
atau
Q
Q
tt
= Q
= Q
0
0
-- kt
kt
Jika ditentukan bahwa Q
Jika ditentukan bahwa Q
ss
adalah mutu akhir (mutu
adalah mutu akhir (mutu
produk saat harus ditarik dari pasaran), maka
produk saat harus ditarik dari pasaran), maka
Q
Q
ss
= Q
= Q
00
-- kt
kt
ss
atau
atau
atau
atau
tt
ss
= (Q
= (Q
00
--Q
Q
ss
)/k
)/k
dimana t
100
100
Penurunan Mutu Ordo Satu (n=1)
Penurunan Mutu Ordo Satu (n=1)
--dQ/dt = kQ
dQ/dt = kQ
atau
atau
ln (Q
ln (Q
tt
/Q
/Q
0
0
) =
) = -- kt
kt
100
100
80
80
60
60
40
40
20
20
alitas (mutu)
relatif
alitas (mutu)
relatif
Purwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011
20
20
00
0 2 4 6 8 10
0 2 4 6 8 10
Waktu penyimpanan (bulan)
Waktu penyimpanan (bulan)
Ku
a
Ku
a
Penurunan Mutu Ordo Satu (n=1)
Penurunan Mutu Ordo Satu (n=1)
--dQ/dt = kQ
dQ/dt = kQ
atau
atau
ln (Q
ln (Q
tt
/Q
/Q
0
0
) =
) = -- kt
kt
Jika Q
Jika Q
ss
adalah mutu akhir, maka
adalah mutu akhir, maka
ln (Q
ln (Q
ss
/Q
/Q
00
) =
) = -- kt
kt
ss
atau
atau
tt
ss
= [ln(Q
= [ln(Q
00
/Q
/Q
ss
)]/k
)]/k
atau
atau
atau
atau
tt
1/2
1/2
= 0,693/k
= 0,693/k
dimana t
BEBERAPA PENURUNAN MUTU PRODUK
PANGAN SELAMA PENYIMPANAN
Orde Nol
Orde Nol
• Mutu (overall quality) pangan beku
• Pencoklatan Non-enzimatis
Orde Pertama
• Kehilangan/kerusakan vitamin
Purwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011
• Inaktivasi/pertumbuhan mikroba
• Kerusakan warna oksidatif
• Kerusakan tekstur karena panas
Orde Nol
Atau
Orde
Pertama??
Penurunan mutu selama
penyimpanan : Perbedaan
antara model kinetika orde
nol dan orde pertama.
Orde Nol
Atau
Orde
Pertama??
Purwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011
Penurunan mutu selama
penyimpanan : Perbedaan
antara model kinetika orde
nol dan orde pertama.
Orde Nol
Atau
Orde
Pertama??
Penurunan mutu selama
penyimpanan : Perbedaan
antara model kinetika orde
nol dan orde pertama.
Orde Nol
Atau
Orde
Pertama??
Purwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011
Penurunan mutu selama
penyimpanan : Perbedaan
antara model kinetika orde
nol dan orde pertama.
Orde Nol
Atau
Orde
Pertama??
Penurunan mutu selama
penyimpanan : Perbedaan
antara model kinetika orde
nol dan orde pertama.
Orde Nol
Atau
Orde
Pertama??
x
Daerah yang
Memungkinkan
pembedaan antara
Purwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011
Penurunan mutu selama
penyimpanan : Perbedaan
antara model kinetika orde
nol dan orde pertama.
x
x
p
ordo 0 dan ordo 1
Uji Umur Simpan Yang Dipercepat
(
Accelerated Shelf Life Test
)
(
Accelerated Shelf Life Test
)
Berdasarkan Suhu (Metode Arrhenius)
MODEL ARRHENIUS
: mempercepat umur simpan dengan
i k tk
h
t
k
meningkatkan suhu secara terukur
Rumus umum penurunan mutu:
-dQ/dt = kQ
nNilai k dipengaruhi oleh suhu :
k = k
0.exp
-Ea/RTPurwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011
dimana:
k = konsntanta laju penurunan mutu
k
0= konstanta (faktor frekuensi, tidak tgt suhu)
Ea = energi aktivasi
T = suhu mutlak (K)
R = konstanta gas; 1,986 kal/mol (8.314 J/mol.K)
Uji Umur Simpan Yang Dipercepat
(
Accelerated Shelf Life Test
)
Berdasarkan Suhu (Metode Arrhenius)
k
R
T
a
E
e
o
k
k
=
-Perubahan nilai k terhadap perubahan suhu (T) yang
dinyatakan sebagai hubungan Arrhenius
Uji Umur Simpan Yang Dipercepat
(
Accelerated Shelf Life Test
)
Berdasarkan Suhu (Metode Arrhenius)
Ln k
oLnk = Ln k
o- (Ea/R)(1/T)
Ln k
Kemiringan
- Ea/R
Purwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011
(1/T)
Hubungan Arrhenius
Uji Umur Simpan Yang Dipercepat
(
Accelerated Shelf Life Test
)
Berdasarkan Suhu (Metode Arrhenius)
Kenali produk Anda!
Karbohidrat pd kondisi amorphous dapat mengalami
kristalisasi pada suhu rendah
.
Retrogradasi
• tekstur keras
• tekstur keras
• membebaskan air
(
Accelerated Shelf Life Test
)
Berdasarkan Suhu (Metode Arrhenius)
Kenali produk Anda!
Karbohidrat pd kondisi amorphous dapat mengalami
kristalisasi pada suhu rendah
Laju “staling”
Purwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011
meningkat dengan
menurunnya suhu
(4°C - 40°C)
Laju “staling”
maksimum : 4°C.
Kenali produk Anda!
Uji Umur Simpan Yang Dipercepat
(
Accelerated Shelf Life Test
)
Berdasarkan Suhu (Metode Arrhenius)
Anomali Arrhenius
Ln (staling
rate)
Anomali Arrhenius.
Pengaruh suhu pada laju
“bread staling” : typical
negative
Ea" = - 9 kcal/mol..
3.2
3.3
3.4
3.5
3.6
100
100
80
80
elatifelatif
T1 > T2 > T3
Ilustrasi Penggunaan Model Arrhenius
Ilustrasi Penggunaan Model Arrhenius
80
80
60
60
40
40
20
20
Kualitas (mutu) r
e
Kualitas (mutu) r
e
T1Jumlah &
frekuensi
sampling
!
Purwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011
00
0 2 4 6 8 10
0 2 4 6 8 10
Waktu penyimpanan (bulan)
Waktu penyimpanan (bulan)
KK
T3 T2Dengan melakukan pengujian laju kerusakan mutu pada
-paling tidak-
3 suhu yang berbeda; yaitu :
• Suhu yg lbh tinggi daripada suhu penyimpanan normal
Ilustrasi Penggunaan Model Arrhenius .. 1
Ilustrasi Penggunaan Model Arrhenius .. 1
• Suhu yg tidak menyebabkan perubahan mekanisme
kerusakan/penurunan mutu produk
• Kenali produk Anda
Æ
hub Arrhenius:
ln k
Kisaran suhu penyimp normal Kisaran Suhu ASLT A B1/T
Maksimum suhu untuk ASLTTiga (3) suhu berbeda yang mana?
Tiga (3) suhu berbeda yang mana?
Ilustrasi Penggunaan Model Arrhenius .. 2
Ilustrasi Penggunaan Model Arrhenius .. 2
Jenis/Tipe
Jenis/Tipe
Produk
Produk
Suhu Pengujian
Suhu Pengujian
((
°°
C)
C)
Suhu Kontrol
Suhu Kontrol
((
°°
C)
C)
Makanan dalam
Makanan dalam
Kaleng
Kaleng
30, 35, 40, 45
30, 35, 40, 45
44
Pangan kering
Pangan kering
30, 35, 40, 45
30, 35, 40, 45
--18
18
Purwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011
Chilled Products
Chilled Products
5, 10, 15, 20
5, 10, 15, 20
00
Pangan beku
Pangan beku
--5,
5, --10,
10, --15
15
<
< --40
40
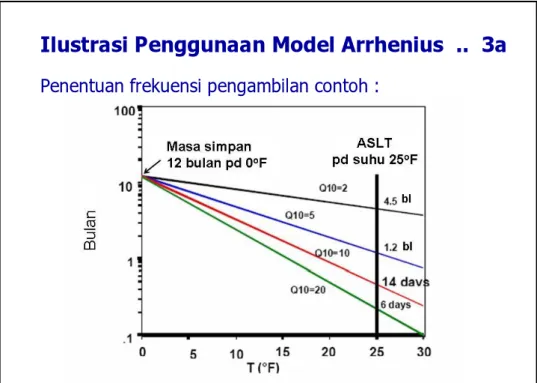
Ilustrasi Penggunaan Model Arrhenius .. 3a
Ilustrasi Penggunaan Model Arrhenius .. 3b
Penentuan frekuensi pengambilan contoh :
Masa simpan pada suhu 5
oC= 12 bulan
Jika Q
10=2
Æ
ASLT (pada suhu 25
oC) : 3 bulan
Jika Q
10=3
Æ
ASLT (pada suhu 25
oC) : 1.3 bulan
Jika Q
10=4
Æ
ASLT (pada suhu 25
oC) : 23 hari
Purwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011
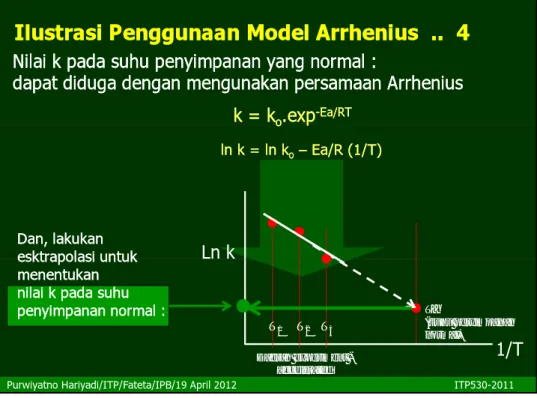
Nilai k pada suhu penyimpanan yang normal :
Nilai k pada suhu penyimpanan yang normal :
dapat diduga dengan mengunakan persamaan Arrhenius
dapat diduga dengan mengunakan persamaan Arrhenius
k = k
k = k
oo.exp
.exp
--Ea/RTEa/RTIlustrasi Penggunaan Model Arrhenius .. 4
Ilustrasi Penggunaan Model Arrhenius .. 4
oo
pp
ln k = ln k
ln k = ln k
oo–– Ea/R (1/T)
Ea/R (1/T)
Ln k
Dan, lakukan
Dan, lakukan
esktrapolasi untuk
esktrapolasi untuk
Ta (suhu peryimpanan normal)Ln k
1/T
Daerah experiment -acceleratedT
1T
2T
3esktrapolasi untuk
esktrapolasi untuk
menentukan
menentukan
nilai k pada suhu
nilai k pada suhu
penyimpanan normal :
penyimpanan normal :
Tentukan Qs.
Tentukan Qs.
•• Standard of identity, SNI, dll
Standard of identity, SNI, dll
Ilustrasi Penggunaan Model Arrhenius .. 5
Ilustrasi Penggunaan Model Arrhenius .. 5
•• Sensory
Sensory
•• Rule 80/80
Rule 80/80
Waktu kadaluwarsa dapat diduga dengan :
Waktu kadaluwarsa dapat diduga dengan :
tt
ss= (Q
= (Q
00--Q
Q
ss)/k, untuk laju reaksi ordo nol
)/k, untuk laju reaksi ordo nol
Purwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011 ss
(Q
(Q
00Q
Q
ss)/ ,
)/ ,
j
j
tt
ss= [ln(Q
= [ln(Q
00/Q
/Q
ss)]/k : untuk laju reaksi ordo I
)]/k : untuk laju reaksi ordo I
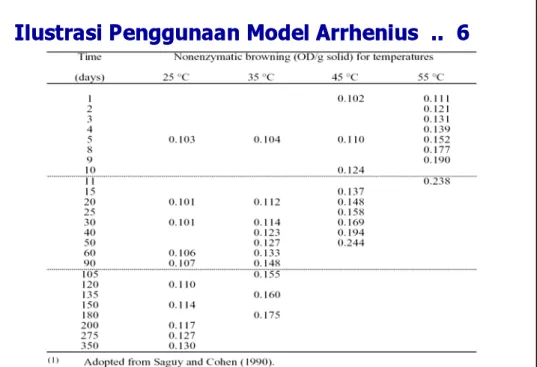
Ilustrasi Penggunaan Model Arrhenius .. 6
Ilustrasi Penggunaan Model Arrhenius .. 6
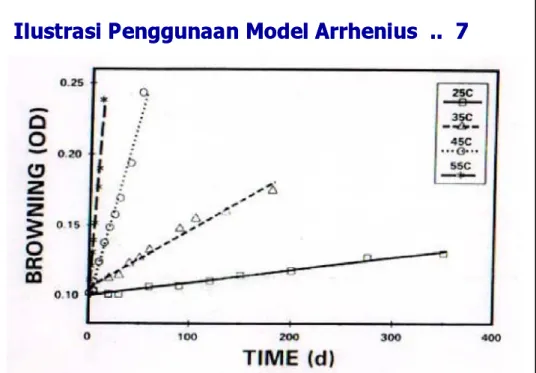
Ilustrasi Penggunaan Model Arrhenius .. 7
Ilustrasi Penggunaan Model Arrhenius .. 7
Purwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011
Ilustrasi
Penggunaan
Model
Arrhenius
8
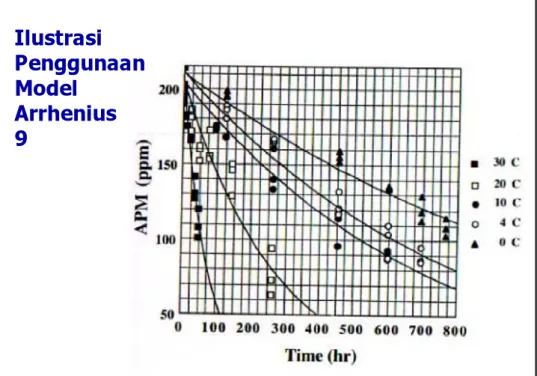
Ilustrasi
Penggunaan
Model
Arrhenius
9
Purwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011
Ilustrasi
Penggunaan
Model
Arrhenius
10
Ilustrasi
Penggunaan
Model
Arrhenius
11
Purwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011
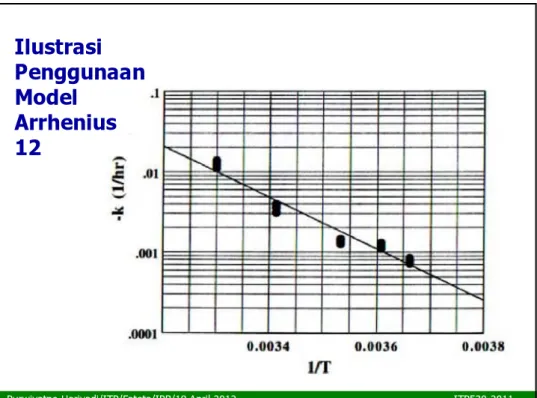
Ilustrasi
Penggunaan
Model
Arrhenius
12
menggunakan model Arrhenius dan jumlah aktualnya
menggunakan model Arrhenius dan jumlah aktualnya
Jumlah kehilangan (%) setelah
Jumlah kehilangan (%) setelah
Jenis
Jenis
6 bulan, pd 20
6 bulan, pd 20
ooC, RH 75%
C, RH 75%
Jenis
Jenis
6 bulan, pd 20
6 bulan, pd 20 C, RH 75%
C, RH 75%
Vitamin
Vitamin
Diduga dengan
Diduga dengan
Hasil
Hasil
model Arrhenius
model Arrhenius
Analisis
Analisis
Vitamin C
Vitamin C
(asam askorbat)
(asam askorbat)
24,0
24,0
23,0
23,0
Purwiyatno Hariyadi/ITP/Fateta/IPB/19 April 2012 ITP530-2011