OPTIMASI PRETREATMENT
ASAM SULFAT ENCER DARI BONGGOL JAGUNG UNTUK
PRODUKSI BIOETHANOL
NAMA: JAMES WIJAYA SALIM
NPM: 2009620128
PEMBIMBING: H.Maria Inggrid, Dra.,M.Sc.
UNIVERSITAS KATOLIK PARAHYANGAN
FAKULTAS TEKNIK INDUSTRI
JURUSAN TEKNIK KIMIA
BANDUNG
1
OPTIMASI STATISTIK PRETREATMENT
ASAM SULFAT ENCER DARI BONGGOL JAGUNG UNTUK
PRODUKSI BIOETHANOL
James Wijaya 1), H.Maria Inggrid, Dra., M.Sc.2)
1) Mahasiswa S1 Jurusan Teknik Kimia, Program Sarjana, Universitas Katolik Parahyangan, Bandung, Indonesia 2) Dosen Pembimbing, Jurusan Teknik Kimia, Universitas Katolik Parahyangan, Bandung, Indonesia
ABSTRAK
Penggunaan lignoselulosa sebagai bahan dasar untuk meproduksi bahan kimia atau bahan bakar minyak semakin meningkat karena material tersebut murah, dapat diperbarui, dan mempunyai kandungan gula yang tinggi. Bonggol jagung adalah bahan biomassa yang menarik untuk memproduksi bioethanol dan xylosa karena kandungan xylan dan glucan nya yang tinggi. Penelitian ini menggunakan central composite design dari metoda respon permukaan untuk mengoptimalkan pretreatment asam sulfat encer. Variabel yang digunakan dalam penelitian ini ialah lama reaksi (0.5-1.5 jam), konsentrasi asam sulfat (0.5-2.5%), dan temperatur (110oC-130 oC). Proses pretreatment kemudian dilanjutkan dengan hidrolisis enzim untuk memaksimalkan produksi glukosa. Hasil menunjukan bahwa kondisi terbaik untuk produksi glukosa adalah 1.5 % asam sulfat selama 1.84 jam pada 120 oC. Sedangkan perolehan xylosa terbanyak didapatkan pada konsentrasi asam 2.5 % selama 0.5 jam dan 130
oC. Hasil dengan perolehan glukosa terbanyak kemudian difermentasi menggunakan
Saccharomyces Cerevisae untuk mendapatkan bioethanol sekitar 1.9%. Kata-kata kunci:
ABSTRACT
The interest on use of lignocellulose for producing fuels and chemicals is increasing as these materials are low cost, renewable and widespread sources of sugars. Corncob is an attractive raw material for xylose and fuel ethanol production due to its high content of xylan and glucan. This study used the central composite design of response surface method to optimize dilute H2SO4 pretreatment. The variables in this study are treatment time (0.5-1.5 h), acid concentration (0.5-2.5%), and temperature (110-130 oC). Enzymatic hydrolisis of the remaining solid was carried out further to evaluate the acid pretreatment conditions for maximizing glucose production. The results showed that pretreatment conditions for the highest glucose production was 1.5 % sulfuric acid for 1.84 h at 120 oC and that for the highest xylose recovery was 2.5% sulfuric acid for 0.5 h at 130 oC. The best results with highest glucose production then fermented(using Saccharomyces Cerevisae) to produce 1% - 2% ethanol yield.
2
Latar Belakang
Indonesia sekarang adalah salah satu negara dengan pertumbuhan ekonomi yang sangat cepat, terutama di Asia. Dengan pendapatan domestik bruto (PDB) sebesar US$ 0,8 triliun, Indonesia merupakan kekuatan ekonomi yang penting di Asia bersama dengan India, Cina, Jepang, dan Korea Selatan. Pertumbuhan ekonomi yang luar biasa ini tentu disertai dengan konsumsi energi yang semakin meningkat tiap tahunnya. Dengan jumlah penduduk Indonesia yang mencapai 240 juta orang saat ini, kebutuhan akan energi terutama bahan bakar minyak sangat tinggi.
Gambar 1. Konsumsi minyak Indonesia
(barrel per hari) [1]
Konsumsi bahan bakar minyak yang terus bertambah ini akan menimbulkan efek negatif dalam jangka panjang. Selain karena cadangan minyak yang semakin menurun (dapat dilihat pada gambar 1.2), bahan bakar minyak juga memilki kekurangan lain yaitu efek samping yang ditimbulkan terhadap lingkungan, seperti besarnya gas CO2 yang dilepaskan, minyak yang tumpah
di lautan, atau bahaya yang mungkin paling besar dampaknya, yaitu global warming.
Gambar 2. Cadangan minyak bumi
Dalam mengantisipasi berbagai macam hal tersebut, negara-negara di dunia sekarang berlomba untuk mengembangkan energi terbarukan yang dapat memenuhi kebutuhan energi dunia secara keseluruhan untuk berpuluh-puluh tahun ke depan. Berbagai macam energi terbarukan sudah mulai dikembangkan dan diterapkan seperti sel surya, energi angin, energi geotermal,
mikrohidro, dan biomassa. Dalam
penelitian ini, penulis memfokuskan untuk meneliti mengenai energi dari biomassa, khususnya untuk memproduksi bioetanol.
Lignoselulosa banyak ditemui pada residu tanaman pangan seperti sekam padi, berangkas jagung, bonggol jagung, bagas tebu, bonggol pisang, dan sebagainya. Kendala dalam penggunaan teknologi ini ialah efisiensi konversi bahan lignoselulosa menjadi bioetanol yang masih rendah, karena struktur kimia mengandung lignin sehingga sulit dijangkau oleh enzim.[3]
Konversi Lignoselulosa menjadi bioetanol umunya dibagi menjadi 4 tahap, yaitu pretreatment untuk memisahkan lignin, hidrolisis enzimatik, fermentasi, dan purifikasi[1]. Dari pustaka yang telah
dipelajari, pretreatment merupakan proses penting dalam produksi bioetanol. Tujuan utama dari pretreatment ialah untuk mengubah struktur selulosa dari biomassa untuk membuat selulosa lebih mudah diakses oleh enzim yang mengkonversi polimer karbohidrat menjadi gula yang siap difermentasi menghasilkan bioetanol. Ada beberapa macam pretreatment yang telah dilaporkan dari pustaka, yang didasarkan pada eksperimen. Pretreatment asam sulfat adalah metoda yang paling banyak diteliti dewasa ini, karena prosesnya yang cukup
sederhana dan kemampuannya untuk
memecah struktur lignoselulosa yang baik sehingga hasil yang diperoleh (konversi menjadi glukosa yang siap difermentasi) cukup tinggi bila dibandingkan dengan metoda lainnya.
Bonggol jagung adalah produk sampingan dari tanaman jagung, umumnya
3
digunakan sebagai makanan ternak atau disebarkan kembali di ladang sebagai pupuk kompos. Sebagai produk sampingan yang kurang memiliki nilai guna lagi, ditambah dengan kandungan karbohidrat yang tinggi (≈70%) dan kandungan lignin yang rendah (≈10%), maka bonggol jagung merupakan biomassa yang potensial untuk diteliti lebih lanjut.
Rumusan Masalah
1) Berapa konsentrasi optimum H2SO4
untuk pretreatment dilute acid pada bonggol jagung untuk perolehan glukosa dan xylosa?
2) Berapa temperatur optimum
pretreatment dilute acid pada bonggol jagung untuk perolehan glukosa dan xylosa?
3) Berapa lama reaksi optimum
pretreatment dilute acid pada bonggol jagung untuk perolehan glukosa dan xylosa?
4) Berapa ethanol yang dihasilkan dari proses fermentasi hasil pretreatment dengan perolehan gukosa terbanyak?
Tujuan Penelitan
1) Mengidentifikasi signifikansi variabel temperatur pada perolehan xylosa dan glukosa
2) Mengidentifikasi signifikansi variabel lama reaksi pada perolehan xylosa dan glukosa
3) Mengidentifikasi signifikansi variabel konsentrasi asam sulfat pada perolehan xylosa dan glukosa.
4) Mengetahui banyaknya ethanol yang dapat dihasilkan dari proses fermentasi menggunakan Saccharomyces cerevisae.
Landasan Teori
Komposisi utama dari lignoselulosa ialah selulosa, hemiselulosa, dan lignin. Selulosa dan hemiselulosa adalah material
pendukung dari dinding sel. Kadar lignin tinggi di bagian tengah lamella dari sel. Namun karena perbedaan volume yang cukup besar antara dinding sel dan lamella tengah, kebanyakan lignin terletak pada dinding sel. Lignin dan hemiselulosa dapat membentuk ikatan lignin-karbohidrat, yang menghasilkan molekul kompleks yang bersifat sebagai lapisan (di sekitar selulosa) yang resistan terhadap hidrolisis.
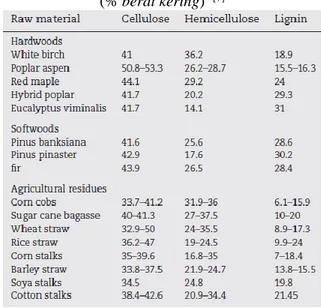
Tabel 1 menunjukkan klasifikasi dari bahan lignoselulosa dan komposisi yang dikandungnya. Komposisi ini dihitung berdasarkan berat kering dari biomassa. Bagaimana pun, material ini pasti mengandung uap air, yang berbeda antar tiap material, yang menyebabkan adanya variasi hasil pada perhitungan.
Tabel 1. Komposi Selulosa, Lignin,
dan Hemiselulosa dari Lignoselulosa (% berat kering) [7]
Selulosa
Selulosa merupakan senyawa
organik dengan jumlah terbanyak di bumi, yang memiliki formula (C6H10O5)n.
Selulosa merupakan homopolimer dengan berat molekul yang tinggi yang terdiri dari ratusan hingga ribuan rantai D-glukosa yang saling terhubung oleh ikatan β(1,4) glikosidik. Struktur kimia dari selulosa dapat dilihat pada gambar 2.3. Ikatan glikosidik tersebut yang memungkinkan
selulosa untuk membentuk struktur
4
selulosa memiliki luas permukaan yang kecil. Struktur kristalin ini merupakan suatu fitur yang penting pada selulosa, yang tidak biasa ditemukan pada polisakarida lainnya. Kristalinitas pada selulosa ini juga
bervariasi bergantung pada jenis
sumbernya.
Gambar 3. Struktur Kimia senyawa Selulosa
Properti dari selulosa ditentukan oleh derajat polimerisasinya (DP), yaitu jumlah unit glukosa yang menyusun satu molekul polimer. DP dari selulosa dapat mencapai angka 17000, di mana umumnya berkisar pada 800-10000 unit (Kirk-Otmer, 2001).
Ikatan alami antar molekul glukosa (β 1,4 glikosidik) memungkinkan polimer untuk tersusun dalam bentuk rantai lurus panjang. Gugus hidroksil yang tersebar merata pada kedua sisi monomer juga
memungkinkan terbentuknya ikatan
hidrogen antar molekul selulosa. Ikatan
hidrogen ini juga nantinya akan
menghasilkan rantai paralel yang saling terhubung antar molekul. Ilustrasi dari susunan molekul glukosa dalam rantai paralel dan ikatan hidrogen.
Gambar 4. Susunan paralel dari polimer selulosa
Selulosa ditemukan dalam bentuk kristalin dan non-kristalin. Gabungan dari
beberapa rantai polimer membentuk
mikrofibril, yang pada akhirnya membentuk
makrofibril (fiber). Proses inilah yang akhirnya menghasilkan struktur kristalin pada selulosa. Gambar 2.4 mengilustrasikan struktur dan juga letak selulosa pada dinding sel.
Gambar 5. Pembentukan mikro dan makrofibril
pada selulosa di dinding sel Hemiselulosa
Hemiselulosa diklasifikasikan
sebagai polisakarida heterogen.
Hemiselulosa merupakan polymer amorf yang mengandung 5 jenis gugus gula yang berbeda (Sjostorm, 1981), yaitu: heksosa (glukosa, manosa, dan galaktosa) dan pentosa (xylosa, arabinosa). Struktur dari gugus primer gula ini dapat dilihat pada gambar 2.3. Hemiselulosa memiliki ikatan acak, bercabang-cabang, struktur amorf, dan kurang kuat, sehingga lebih mudah dihidrolisis oleh asam encer atau basa encer. Hemiselulosa bergabung dengan selulosa dalam jaringan lignin untuk membangun dinding sel tanaman yang keras dan kuat. Penampang membujur hemiselulosa dalam jaringan tanaman dapat dilihat pada gambar berikut.
Gambar 6. Penampang membujur hemiselulosa
5
Struktur molekul monosakarida sebagai monomer penyusun hemiselulosa diperlihatkan pada gambar berikut:
Gambar 7. Gugus primer dalam hemiselulosa
Rantai hemiselulosa lebih pendek dari rantai pada selulosa yang lebih sederhana, dapat dicabangkan, dan umunya
memiliki gugus sampingan, seperti
monosakarida dan gugus asetil (Mai et al 2004). Komposisi secara umum dari hemiselulosa berbeda antara hardwood dan softwood, di mana hemiselulosa pada hardwood terutama terdiri dari pentosa, sedangkan hemiselulosa pada softwood mencakup juga heksosa (Phaiboonsilpa et al, 2010). Hemiselulosa berfungsi lebih sebagai sel pendukung pada dinding sel dan lebih mudah untuk dihidrolisis jika dibandingkan dengan selulosa.
Lignin
Lignin merupakan biopolimer
aromatik yang kaku dengan berat molekul sekitar 10,000 Da (1 Da = 1,667 x10-27kg), terhubung dengan ikatan kovalen ke xylan (bagian hemiselulosa) yang menyebabkan dinding sel memiliki tingkat kekompakan yang tinggi. Lignin tersusun dari 3 monomer fenolik (fenil propionik alkohol), yaitu: coumaryl, coniferyl, dan sinapyl alcohol. Lignin terbentuk dengan hilangnya air dari gula hingga terbentuk struktur aromatik. Reaksi tersebut merupakan reaksi irreversible. Monomer yang menyusun lignin dapat dilihat pada gambar berikut:
Gambar 8. Monomer pada lignin
Gugus OH (dalam ikatan rantai atau dalam cincin aromatik) dapat saling bereaksi satu sama lain ataupun dengan aldehid atau keton. Ketika OH bereaksi, maka akan terbentuk eter. Reaksi OH dengan aldehid membentuk hemiasetal, reaksi OH dengan keton membentuk ketal[37]. Kondensasi tahap awal berbagai
monomer untuk membentuk lignin
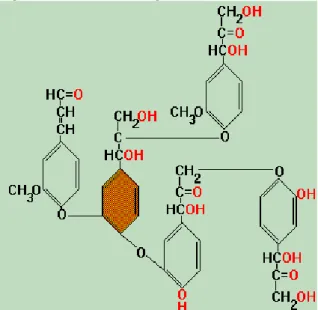
digambarkan melalui gambar berikut:
Gambar 9. Tahap awal proses kondensasi
monomer membentuk lignin
Dari gambar di atas dapat dilihat bahwa beberapa gugus yang berwarna merah dapat bereaksi lebih lanjut. Ada yang memanjang dalam bentuk polimer dan ada pula yang membentuk ikatan silang. Sebagai contoh monomer yang berwarna jingga memiliki 3 gugus fungsional yang terhubung dengan monomer lainnya melalui percabangan atau ikatan silang.
Metode Penelitian
Berangkas dan bonggol jagung disiapkan
Pretreatmen dilute acid
Hidrolisis Fermentasi
6
Analisa Bonggol Jagung dan Berangkas Jagung Mula-mula
Percobaan dilakukan untuk
mengetahui kadar selulosa dan lignin sebelum bonggol jagung melewati tahap pretreatment, hidrolisis, dan fermentasi. Analisis kadar selulosa dilakukan dengan metoda Norman-Jenkins.
Penentuan Pengaruh Temperatur dan
Konsentrasi pada Dilute Acid
Pretreatment
Percobaan dilakukan dengan variasi: Konsentrasi H2SO4: 0,5%; 1.5%; 2.5%
Temperatur :110oC; 120oC; 130oC
Proses pretreatment dilakukan dengan merendam 10 gram bonggol jagung yang sudah digiling menggunakan dry mill dalam larutan 100 mL H2SO4 pada suasana
asam selama (0.5;1;1.5 jam) menggunakan oil bath. Sampel yang telah di-pretreatment kemudian dinetralisasi dengan penambahan NaOH hingga pH sekitar 4,8 – 5. Padatan dan cairan sampel dipisahkan dengan filtrasi. Padatan yang diperoleh dibilas dengan akuades. Sampel dikeringkan dalam oven pada suhu 55 ± 5 oC selama 24 jam (hingga massa konstan). Padatan bonggol jagung yang telah kering ditimbang. Sampel yang telah kering diambil untuk analisa kadar selulosa dan lignin. Dari analisa tersebut diketahui kondisi optimal konsentrasi H2SO4 dan temperatur operasi.
Hidrolisis enzimatik dilakukan dengan menginkubasi sampel padatan bonggol jagung di dalam larutan yang mengandung 0,1M buffer asam sitrat. Hidrolisis menggunakan 1 mL enzim/gram substrat dengan pH 4,8 pada temperatur 50oC. Enzim yang digunakan adalah enzim selulase industrial grade. Fermentasi dilakukan untuk sampel tertentu, dipilih
menggunakan mikroba Saccharomyces
cereviseae. Fermentasi dikondisikan dalam keadaan anaerob selama 3 hari pada suhu 33oC. Kadar etanol hasil fermentasi dapat
dianalisa menggunakan metoda
spektrofotometri.
Bagan Tahap Pretreatment dengan H2SO4
PEMBAHASAN
Penelitian ini terdiri dari 3 tahap, yaitu pretreatment asam sulfat encer, hidrolisis enzimatik, dan fermentasi. Tahap pretreatment asam sulfat terdiri dari 3 variasi perlakuan yaitu : lama reaksi, temperatur, dan konsentrasi asam sulfat.
Variasi perlakuan pada tahap pretreatment ini dapat dilihat pada tabel di bawah ini:
Bonggol jagung dipotong dengan ketebalan 2 cm lalu dimasukan dalam dry
mill
Pretreatment dengan H2SO4 0,5 %,
1.5%, dan 2.5 %
Perbandingan Feed : Solven = 1 :10 10
Larutan didiamkan selama 20 menit pada temperatur 110, 120, 130 oC
menggunakan oil bath (silicon oil)
Filtrasi Filtrat Padatan Uji kadar selulosa Hidrolisis menggunakan Enzim Selulase
Fermentasi menggunakan ragi Saccharomyces cereviseae
Etanol
Uji kadar glukosa
7 Tabel 2. Variasi perlakuan pada percobaan
Pretreatment dilakukan dengan menggunakan Oil Bath yang diisi dengan Silicon Oil sehingga mampu mencapai suhu 130 oC. Bonggol jagung pertama-tama
dikeringkan dan di-blender hingga
mencapai ukuran sekitar 40 mesh.
Perlakuan ini dimaksudkan agar penetrasi asam sulfat dan enzim selulase pada biomassa dapat maksimal.
Analisis Statistik
Data respons pada tabel 3 dilakukan uji analysis of variance (ANOVA) yang bertujuan untuk mengetahui apakah setiap
variabel perlakuan mempengaruhi
perolehan glukosa dan xylosa yang didapat. Uji ANOVA dihitung dengan menggunakan program Design Expert 7.0.0. Berikut tabel
ANOVA dari hasil pretreatment
menggunakan H2SO4 :
Tabel 3. Rancangan percobaan pretreatment
H2SO4 per 10 g bonggol jagung
Tabel 4. ANOVA untuk perolehan Glukosa
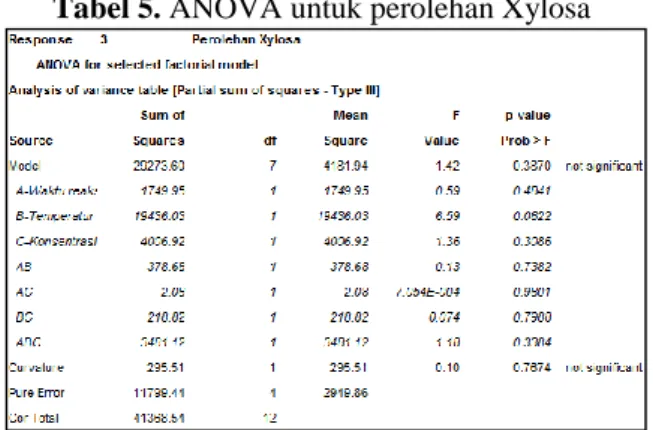
Tabel 5. ANOVA untuk perolehan Xylosa
Efek dari pretreatment pada perolehan Glukosa
Setelah pretreatment asam sulfat, slurry dipisahkan menjadi 2 fasa: fasa liquid dan fasa solid. Perolehan glukosa dan xylosa yang didapat ditampilkan pada tabel 4.2. Hasil dari model respon permukaan orde-dua dalam bentuk Analysis of Variance (ANOVA) ditampilkan Pada tabel 4.3 dan 4.4 dapat dilihat
variabel yang berpengaruh adalah variabel dengan nilai P-value di bawah 5%. Variabel lama reaksi, temperatur, dan konsentrasi pada tabel 4.3 dan tabel 4.4 memiliki nilai P-value > 0.05 yang berarti ketiga variabel tersebut tidak mempunyai pengaruh yang signifikan pada perolehan glukosa dan xylosa. Hal berarti hasil percobaan pada variasi awal dan variasi akhir tidak memiliki perbedaan yang signifikan. Tetapi bukan berarti ketiga variabel tersebut tidak berpengaruh sama sekali sehingga perlu meninjau grafik model pada variabel lama reaksi, temperatur, dan konsentrasi untuk melihat apakah interaksi antar ketiga variabel tersebut memiliki pengaruh pada hasil percobaan.
8
Gambar 9. Interaksi Variabel
Waktu-Konsentrasi (a) dan Temperatur-Waktu-Konsentrasi (b) pada Glukosa
Gambar 9(a) menunjukkan perolehan
glukosa rata–rata dengan variasi lama reaksi. Dari grafik dapat dilihat pada lama reaksi 0.5 jam dengan rata–rata 1500 ppm lalu mengalami kenaikan pada center point (1 jam) dan turun kembali ke 2150 ppm pada lama reaksi 1.5 jam. Hal ini berarti perolehan glukosa akan naik pada lama reaksi 0.5 jam dan mencapai puncaknya pada waktu 1 jam. Setelah lewat 1 jam
maka perolehan pun akan menurun
kembali. Berdasarkan teori, semakin lama reaksi berlangsung maka semakin banyak ikatan glikosidik pada selulosa yang terpecah dan menghasilkan glukosa [12].
Semakin lama waktu proses, maka
kesempatan selulosa melakukan
dekomposisi lebih panjang, sehingga kadar glukosa naik. Garis merah menandakan
perolehan glukosa pada perubahan
konsentrasi larutan. Dari grafik interaksi waktu-konsentrasi diatas dapat dilihat bahwa kenaikan konsentrasi H2SO4 malah
menurunkan perolehan glukosa. Hal ini disebabkan kareana pada konsentrasi yang tinggi akan terbentuk Furfural, yang dapat menghambat kinerja enzim selulase yang pada akhirnya akan menurunkan perolehan glukosa.
Gambar 9(b) menunjukkan perolehan
glukosa rata-rata dengan variasi interaksi antara temperatur dan konsentrasi. Dari grafik dapat dilihat pada temperatur dengan rata-rata 110oC diperoleh glukosa sebesar
1500 ppm lalu mengalami puncaknya (2500 ppm) pada 120oC jam dan turun kembali ke 2150 ppm pada temperatur 120oC.
Berdasarkan teori, semakin tinggi
temperatur reaksi maka semakin mudah ikatan glikosidik pada selulosa dan xilan untuk terpecah dan menghasilkan glukosa dan xylosa [12]. Hal ini dikarenakan reaksi
hidrolisa merupakan reaksi endotermis sehingga memerlukan panas untuk dapat bereaksi. Tetapi, jika suhu terlalu tinggi, maka katalis (H2SO4) akan menguap yang
mengakibatkan melambatnya reaksi
hidrolisa tersebut yang juga akan berakibat pada konsentrasi glukosa dan xylosa yang diperoleh. Pada suhu yang terlalu tinggi juga akan terbentuk selulosa yang pecah menjadi arang (warna larutan hasil semakin tua). Kondisi ini juga akan menurunkan konversi selulosa menjadi glukosa.
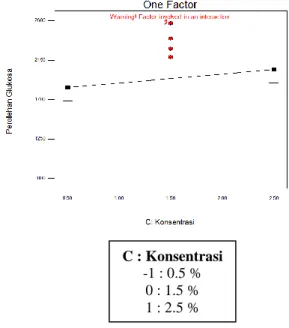
Gambar 10. Pengaruh konsentrasi terhadap
perolehan Glukosa
Gambar 10 menunjukkan perolehan glukosa rata- rata dengan variasi konsentrasi. Dari grafik dapat dilihat pada
konsentrasi dengan rata-rata 0.5%
diperoleh glukosa sebesar 1800 ppm lalu mengalami puncaknya sebesar 2500 ppm pada 1.5% dan turun kembali ke 2150 ppm pada konsentrasi 2.5%. Berdasarkan teori, semakin tinggi konsentrasi asam maka
C : Konsentrasi
-1 : 0.5 % 0 : 1.5 % 1 : 2.5 %
9
semakin mudah ikatan glikosidik pada selulosa untuk terpecah dan menghasilkan glukosa [12]. Penambahan katalisator asam bertujuan memperbesar kecepatan reaksi, sesuai dengan persamaan Arhenius. Jadi makin banyak asam yang dipakai makin cepat reaksi hidrolisis, dan dalam waktu tertentu selulosa dan xylan yang berubah
menjadi glukosa dan xylosa juga
meningkat. Tetapi penggunaan asam
sebagai katalisator sedapat mungkin terbatas pada konsentrasi yang tidak terlalu tinggi karena dapat menghasilkan produk sampingan seperti furfural, yang dapat menghambat kinerja enzim selulase.
.
Efek dari pretreatment pada perolehan Xylosa
Pada tabel 5 dapat dilihat variabel yang berpengaruh adalah variabel dengan nilai P-value di bawah 5%. Variabel lama reaksi, temperatur, dan konsentrasi pada tabel 4.4 memiliki nilai P-value > 0.05 yang berarti ketiga variabel tersebut tidak mempunyai pengaruh yang signifikan pada perolehan xylosa. Selain itu, interaksi antar variabel pada perolehan xylosa (AB, BC, AC, dan ABC) juga memiliki nilai yang lebih besar dari 0.05. Hal ini berarti hasil percobaan pretreatment tidak memiliki pengaruh signifikan pada perolehan xylosa akhir. Hal ini disebabkan karena ketiadaan enzim xylanase pada percobaan, yang mampu mendekomposisi xylan menjadi xylosa. Proses pretreatment saja tidak cukup kuat untuk memecah ikatan hidrogen yang terdapat dalam xylan, sehingga hasil akhir (xylosa) yang didapat sangat minim.
Fermentasi
Hasil pretreatment dengan perolehan glukosa terbanyak yaitu run 10 (2619.43 ppm) dan run 11 (2577.29 ppm) kemudian difermentasi menjadi bioethanol. Proses pembuatan berhasil dilakukan pada kondisi temperatur 30oC dan agitasi 100 rpm di dalam laboratory shaker dan dibiarkan selama 3 hari. Kondisi operasi ini
ditentukan berdasarkan pertimbangan kondisi yang dapat ditoleransi oleh mikroba fermentasi dimana mikroba Saccharomyces
cerevisiae tumbuh optimum pada
temperatur 25-30oC dan mampu bertahan
pada temperatur 35-47oC dengan pH 4-5.[9]. Pada penelitian ini, pH operasi tidak divariasikan, pH operasi awal sekitar 5 diperoleh tanpa penambahan asam maupun basa. Sampel dianalisa menggunakan instrumen HPLC dan spektrofotometer untuk menentukan kadar etanol dan sisa glukosa, sedangkan jumlah sel mikroba dihitung langsung menggunakan mikroskop
perbesaran 400 dengan bantuan
haemocytometer. Konsentrasi
Saccharomyces Cerevisiae yang digunakan didapat sebesar 1.2 x 107 sel/ml untuk sampel 10 (perolehan glukosa 2619.43 ppm) dan 1.44 x 107 sel/ml untuk sampel 11 (perolehan glukosa 2577.29 ppm). Dari analisa glukosa akhir menggunakan HPLC dapat dilihat bahwa hampir seluruh glukosa terkonversi menjadi ethanol, sehingga tidak terdapat sisa pada sampel.
Kesimpulan
Kesimpulan yang diperoleh dari percobaan adalah:
1) Kondisi percobaan yang dapat
menghasilkan perolehan glukosa
maksimum sebanyak 2577.29 ppm
ialah lama perendaman 1 jam,
temperatur 120 oC, dan konsentrasi H2SO4 1.50 %
2) Kondisi optimum yang dapat
menghasilkan perolehan glukos
maksimum berdasarkan perhitungan menggunakan Design Expert ialah lama perendaman 0.7 jam, temperatur 118.05 oC, dan konsentrasi H
2SO4 1.91
%
3) Kondisi percobaan yang dapat
menghasilkan perolehan xylosa
maksimum sebanyak 311.08 ppm ialah lama perendaman 0.5 jam, temperatur 130 oC, dan konsentrasi H2SO4 2.50 %
10
4) Kondisi optimum yang dapat
menghasilkan perolehan glukos
maksimum berdasarkan perhitungan menggunakan Design Expert ialah lama perendaman 0.64 jam, temperatur 111.11 oC, dan konsentrasi H2SO4 0.82
%
5) Etanol yang didapat dari hasil perolehan glukosa terbaik (2577.29 ppm) memiliki yield 1.899 %
Saran
Saran untuk penelitian selanjutnya adalah: 1) Menggunakan reaktor khusus yang
dapat mempertahankan suhu di atas 130 oC secara konstan
2) Menggunakan rentang variasi pada perlakuan yang cukup besar sehingga perbedaan hasil yang diperoleh dapat jelas terlihat
3) Menggunakan enzim selulase murni sehingga perolehan glukosa yang didapat bisa maksimal
4) Menggunakan enzim xylanase agar perolehan xylosa dapat lebih maksimal
DAFTAR PUSTAKA
[1] Qu YB, Zhu MT, Liu K, Bao XM, Lin JQ. Studies on cellulosic ethanol production for sustainable supply of liquid fuel in China. Biotechnol J 2006;1:1235e40. [2] Rodriguez CA, Ramirez JA, Garrote G, Vazquez M. Hydrolysis of sugarcane bagasse using nitric acid: a kinetic assessment J Food Eng 2004;61:143e52. [3] Lavarack BP, Griffin GJ, Rodman D. The acid hydrolysis of sugarcane bagasse hemicellulose to produce xylose, arabinose, glucose and other products. Biomass Bioenerg 2002;23:367e80.
[4] Herrera A, Te´ llez-Luis SJ, Ramı´rez JA, Va´zquez M. Production of xylose from sorghum straw Using Hydrochloric Acid. J Cereal Sci 2003;37:267e74.
[5] Rahman SHA, Choudhury JP, Ahmad AL. Production of xylose from oil palm
empty fruit bunch fiber using sulfuric acid.Biochem Eng J 2006;30:97e103. [6] Garrote G, Dominguez H, Parajo JC. Generation of xylose solutions from
eucalyptus wood by
autohydrolysiseposthydrolysis processes: posthydrolysis
kinetics. Bioresour Technol; 2001:155e64. [7] Eva P, Ba¨rbel H. Fermentation of
lignocellulosic hydrolysates. I.
Inhibitionanddetoxification. BioresourTechnol 2000;74:17e24.
[8] Washuttle J, Riederer P, Banchen E. Qualitative and quantitative study of sugarealcohols in several foods. J Food Sci 1973;38:1262e3.
[9] Emodi A. Xylitol: its properties and
food applications. Food Technol
1978;32:28e32.
[10] Carvalho W, Santos JC, Canilha L, Silva SS, Perego P, Converti A. Xylitol
production from sugarcane bagasse
hydrolysate: metabolic behaviour of Candida guilliermondii cells entrapped in
Ca-alginate. Biochem Eng J
2005;25:25e31.
[11] Liaw WC, Chen CS, Chang WS, Chen KP. Xylitol production from rice straw hemicellulose hydrolyzate by polyacrylic hydrogel thin films with immobilized Candida subtropicalis WF79. J Biosci Bioeng 2008;105:97e105.
[12] Mancilha IM, Karim MN. Evaluation of ion exchange resins for removal of inhibitory compounds from corn stover hydrolyzate for xylitol fermentation. Biotechnol Prog 2003; 19:1837e41.
[13] Solange IM, Giuliano D, Ineˆs CR. Influence of the toxic compounds present in brewer’s spent grain hemicellulosic
hydrolysate on xylose-to-xylitol
bioconversion by Candida guilliermondii. Process Biochem 2005;40:3801e6.
[14] Villarreal MLM, Prata AMR, Felipe MGA, Almeida JBES. Detoxification procedures of eucalyptus hemicellulose hydrolysate for xylitol production by
11
Candida guilliermondii.Enzyme Microb Technol 2006;40:17e24.
[15] Canilha L, Almeida SJB, Solenzal AIN. Eucalyptus hydrolysate detoxification with activated charcoal adsorption or ionexchanger resins for xylitol production. Process Biochem 2004;39:1909e12.
[16] Cheng KK, Zhang JA, Ling HZ, Ping WX, Huang W, Ge JP, et al. Optimization of pH and acetic acid concentration for bioconversion of hemicellulose from corncobs to xylitol by Candida tropicalis. Biochem Eng J 2009;43:203e7.
[17] Cheng KK, Zhang JA, Erik C, Li JP. Integrated production of xylitol and ethanol using corncob. Appl Microbiol Biotechnol 2010;87:411e7.
![Gambar 1. Konsumsi minyak Indonesia (barrel per hari) [1]](https://thumb-ap.123doks.com/thumbv2/123dok/4256397.2880938/3.892.131.455.456.674/gambar-konsumsi-minyak-indonesia-barrel-hari.webp)