91
Isolasi Senyawa dari Fraksi Etil Asetat Daun Pedada (
Sonneratia
caseolaris
L.) dan Uji Aktifitas Antioksidan
(
Isolation of Ethyl acetate Fraction Coumpound from Leaves of Pedada (Sonneratia
caseolaris L.) and Its Antioxidant Activities
)
Yulianis
1*; Madyawati Latief
2; & M. Redho
1 1Program Studi Farmasi STIKES Harapan Ibu Jambi
2Fakultas Sains dan Teknologi Universitas Jambi
Corresponding email: yulianisaljazila@yahoo.com
ABSTRAK
Telah dilakukan penelitian tentang isolasi senyawa dari fraksi etil asetat daun pedada (Sonneratia
caseolaris L.) dan aktifitas antioksidannya. Fraksi diperoleh dengan maserasi bertingkat menggunakan
n-heksan, etil asetat dan metanol. Fraksi etil asetat diisolasi dengan kromatografi kolom sehingga diperoleh Fraksi 1, 2, 3 dan 4. Fraksi 1 diisolasi kembali dengan kromatografi kolom sehingga diperoleh fraksi 1.1, 1.2, 1.3 dan 1.4. kemudian fraksi 1.2 dilakukan pemurnian dengan KLT preparatif dihasilkan Isolat A dan B, keduanya berbentuk serbuk, berwarna putih dan tidak berbau. Hasil identifikasi dengan spektrofotometer Uv. dan IR terhadap isolat tersebut diduga terpenoid. Uji Aktivitas antioksidan fraksi 1.2 dilakukan dengan metode DPPH diperoleh nilai IC50 Sebesar 39,89 ppm.
Kata Kunci: isolasi, DPPH, pedada (Sonneratia caseolaris L.), antioksidan PENDAHULUAN
Indonesia kaya akan berbagai
keanekaragaman hayati yang berpotensi untuk dikembangkan sebagai obat atau bahan baku obat. Survei tentang obat di Amerika Serikat yang diakui oleh Food and Drug Administration AS pada periode 1983-1994 menunjukkan bahwa 157 dari 520 (30%) jenis obat berasal dari bahan alam atau turunannya, dimana 61% senyawa antikanker yang diakui juga berasal dari bahan alam atau turunannya (Fajriah dkk, 2007).
Di dunia terdapat 119 senyawa yang digunakan sebagai bahan obat yang berasal dari 90 spesies tumbuhan, dimana 77% ditemukan sebagai hasil penelitian tumbuhan yang
didasarkan pemakaiannya secara tradisional (Fajriah dkk, 2007). Beberapa tumbuhan yang berkhasiat mengandung senyawa antioksidan misalnya senyawa golongan fenolik, flavonoid, dan xanton. Senyawa ini dapat digolongkan sebagai antioksidan alami (Efendi, 2007).
Antioksidan adalah senyawa yang mampu menghambat laju oksida molekul lain atau menetralisir radikal bebas (Fajriah dkk, 2007). Tubuh kita memerlukan senyawa antioksidan yang dapat membantu melindungi tubuh dari serangan radikal bebas mengingat begitu banyaknya radikal bebas yang berasal dari luar
tubuh berupa makanan yang banyak
mengandung bahan pengawet, pewarna,
92 Emisi kendaraan bermotor dan industri, asap
rokok serta pelepasan senyawa kimia reaktif ke alam merupakan penyumbang radikal bebas yang cukup besar (Zuhra, Taringan, Sihotang, 2008). Tubuh tidak mempunyai system pertahanan antioksidan eksogen (Sunarni, Pramono, & Asmah, 2007).
Antioksidan dapat diperoleh dalam bentuk sintetik dan alami. Akan tetapi
kekhawatiran terhadap efek samping
antioksidan sintetik menjadikan antioksidan
alami menjadi alternatif yang terpilih.
Antioksidan alami mampu melindungi tubuh terhadap kerusakan oksigen reaktif, mampu
menghambat penyakit degeneratif, serta
menghambat peroksidasi lipid pada makanan. Tumbuhan merupakan sumber antioksidan alami dan umumnya merupakan senyawa fenolik yang tersebar pada bagian tumbuhan baik pada kayu, biji, daun, buah, akar, bunga maupun serbuk sari (Sunarni, Pramono, & Asmah, 2007).
Salah satu tumbuhan yang berpotensi sebagai antioksidan adalah tumbuhan pedada merah. Tumbuhan ini mengandung senyawa alkaloid, flavonoid, glikosida, saponin dan fenol (Avenido, P. and Serrano,A.E. 2012). Secara tradisional tumbuhan ini digunakan sebagai ramuan bedak dingin. Berdasarkan hasil penelitian Sariful et al, (2012) yang menguji ekstrak etanol dari daun tumbuhan pedada
dengan menggunakan
1,1-difenil-2-picrylhydrazyl (DPPH), ternyata ekstrak
tersebut memiliki aktifitas antioksidan, dengan perolehan nilai IC50 68µg/ml. Selanjutnya penelitian Madyawati (2014) yang menguji aktifitas antioksidan terhadap berbagai ekstrak daun pedada diperoleh nilai persen inhibisi yang tertinggi terdapat pada fraksi etil asetat yaitu pada konsentrasi 500 ppm sebesar
68,97% dan konsentrasi 1000 ppm sebesar 70,39%. Berdasarkan penelitian terdahulu tersebut, kesempatan untuk mendapatkan senyawa aktif antioksidan cukup besar, oleh karena itu peneliti tertarik untuk melakukan isolasi senyawa aktif antioksidan dari fraksi etil asetat daun pedada.
METODE PENELITIAN
Alat dan Bahan
Alat yang digunakan pada penelitian ini meliputi: Rotary evaporator, spektrofotometer UV-Vis, timbangan digital, gelas ukur, tabung reaksi, pipet ukur, kertas saring, kolom kromatografi, gelas ukur, labu ukur, corong, batang pengaduk, cawan penguap, pipa kapiler, vial, lampu UV dengan panjang gelombang 254 nm, chamber.
Bahan yang digunakan : daun tumbuhan pedada (Sonneratia caseolaris L.) diidentifikasi di Herbarium Universitas Andalas, n-heksan, etil asetat, metanol, silika gel, plat KLT, DPPH.
Prosedur Penelitian Ekstraksi
Tumbuhan pedada diperoleh dari pesisir sungai Kabupaten Tanjung Jabung Barat, Kecamatan Tungkal Ilir. Bagian Tumbuhan yang digunakan adalah daun pedada. Daun pedada sebanyak 10 kg di kering-anginkan hingga didapat berat konstan 3,5 Kg kemudian dirajang halus. Daun yang sudah dirajang halus kemudian dimaserasi bertingkat dengan n-heksan, etil asetat, dan metanol dengan 3 kali pengulangan. Masing-masing hasil maserasi disaring dengan menggunakan kertas saring Whatman no.1, Filtrat dipekatkan dengan menggunakan rotary evaporator, sehingga
93 diperoleh ekstrak kental n-heksan, etil asetat
dan metanol daun pedada.
Isolasi Fraksi Etil Asetat
Ekstrak kental etil asetat diisolasi dengan kromatografi kolom. Kolom kromatografi disiapkan dengan membuat bubur silika yang dimasukkan ke dalam kolom kromatografi secara perlahan-lahan. Ekstrak kental etil asetat dilarutkan dengan aseton lalu dihomogenkan dengan silika gel untuk preadsorbsi kemudian dimasukkan ke dalam kolom.
Kemudian dibuat sistem fase gerak dengan komposisi n-heksan, etil asetat dan metanol dengan berbagai perbandingan secara bergradien. Langkah pertama dilakukan dengan mengaliri kolom dengan fase gerak n-heksan 100%. Pelarut yang menetes dari kolom ditampung dalam vial yang sebelumnya telah ditimbang dan diberi nomor. Penggantian gradient fase gerak dilakukan ketika fase gerak gradien sebelumnya telah habis digunakan untuk mengaliri kolom. Jumlah perbandingan pelarut n-heksan dan etil asetat yang digunakan selanjutnya adalah (9:1, 8:2, 7:3, 5:5, 2:8), Etil asetat 100% dan Etil asetat : Metanol (4:6, 2:8). Pada tahap akhir kromatografi kolom, kolom dicuci dengan mengaliri pelarut methanol 100% untuk membersihkan silika gel dari sisa ekstrak yang menempel.
Fraksi-fraksi hasil pengoloman
ditampung dan kemudian diuapkan
menggunakan rotary evaporator. Seluruh fraksi
yang diperoleh diidentifikasi dengan
kromatografi lapis tipis (KLT) dengan eluen
n-heksan:etil asetat dengan berbagai
perbandingan. Kemiripan bercak yang timbul pada lempeng amati baik secara langsung maupun dibawah sinar UV 254 nm. Fraksi yang mempunyai kemiripan bercak dijadikan satu.
Fraksinasi dilakukan kembali hingga diperoleh isolat murni.
Uji Aktifitas Antioksidan
Penentuan Panjang Gelombang DPPH: Dipipet sebanyak 3,8 ml larutan DPPH 400 ppm dan ditambahkan 0,2 ml metanol. Setelah dibiarkan selama 30 menit ditempat gelap
serapan larutan diukur dengan
spektrofotometer UV-Vis pada panjang
gelombang 400 - 800 nm.
Uji Aktifitas Antioksidan Senyawa Hasil
Isolasi: Pengujian aktivitas antioksidan
dilakukan dengan metoda DPPH (Selvi et al, 2003). Sampel ditimbang sebanyak 10 mg, dilarutkan dalam 25 ml metanol dalam labu ukur 25 ml. untuk penentuan aktivitas antioksidan, 0,2 ml larutan sampel dipipet dengan pipet mikro kedalam vial, kemudian ditambahkan 3,8 ml larutan DPPH 400 ppm. Campuran larutan dihomogenkan dan dibiarkan selama 30 menit ditempat gelap. Serapan diukur dengan spektrofotometer UV-Vis pada panjang gelombang 517 nm. Untuk Kontrol positif digunakan asam askorbat perlakuan yang sama dengan sampel.
Identifikasi Senyawa Hasil Isolasi
Identifikasi senyawa hasil isolasi
menggunakan kromatografi lapis tipis,
Spektrofotometri UV-Vis dan FTIR. HASIL DAN DISKUSI
Pada penelitian ini sampel yang digunakan adalah daun pedada kering dengan berat 3,5 kg. Proses ekstraksi dan fraksinasi menggunakan metode maserasi bertingkat yang dimulai dari n-heksan, etil asetat dan metanol. Hal ini bertujuan untuk menyederhanakan komponen kimia berdasarkan kepolarannya
94 sehingga diperoleh kelompok senyawa non
polar, semi polar dan polar. Kemudian hasil maserasi dipekatkan menggunakan rotary evaporator sehingga diperoleh ekstrak kental dari masing-masing ekstrak. Dari 3,5 kg daun pedada diperoleh randemen fraksi kental n-heksan, etil asetat dan metanol berturut-turut yaitu 0,642;2,564 dan 3,008%.
Gambar 1. Hasil Uji KLT terhadap hasil isolasi fraksi etil asetat
Isolasi fraksi etil asetat dilakukan dengan menggunakan kromatografi kolom. Kolom dielusi menggunakan fase gerak mulai dari pelarut nonpolar n-heksan 100%, kemudian ditingatkan kepolaran secara bergradien dengan n-heksan : etil asetat (9:1, 8:2, 7:3, 5:5, 2:8) , Etil asetat 100% dan Etil asetat : Metanol ( 4:6, 2:8), masing-masing hasil elusi ditampung dalam vial-vial secara berurut, sehingga diperoleh 39 vial. setiap vial dilakukan uji kromatografi lapis tipis (KLT) dan dilihat pola noda yang dihasilkan di bawah lampu UV dengan panjang gelombang 254 nm. Fraksi yang memperlihatkan pola noda yang sama digabungkan diperoleh 4 fraksi yaitu F1(Vial 1-6), F2 (vial 7-8), F3(vial 9-16) dan F4 (vial 17-39) (gambar 1). Dari F1 diisolasi
dengan kromatografi kolom lagi dan diperoleh 4 subfraksi yaitu F1.1, F1.2, F1.3 dan F1.4.
Gambar 2. Hasil Uji KLT terhadap F1.2 dengan fase gerak yang berbeda {kiri: n-heksan : etil asetat (7:3); kanan: diklorometana : etil asetat (1:1)}
Tabel 1. Hasil identifikasi isolate A dan B dengan FTIR
Pada subfraksi F1.2 terdapat Kristal putih dengan berat 10 mg yang diuji aktifitas antioksidannya. Pengujian aktifitas antioksidan dengan menggunakan metode DPPH, dibuat seri konsentrasi 8, 16 dan 24 ppm diperoleh nilai IC50 sebesar 39,89 ppm.
95 Pada subfraksi F1.2 dilakukan pemisahan
dan melihat kemurnian senyawa dengan KLT menggunakan fase gerak Heksan:Etil asetat (7:3) memperlihatkan 1 noda, kemudian dielusi
kembali menggunakan fase gerak lain
diklorometana, ternyata memperlihatkan 2 noda (gambar 2). Untuk pemisahan dilakukan kromatografi Lapis tipis preparatif sehingga diperoleh 2 isolat , Isolat A dengan Rf 0,92 dan Isolat B dengan Rf 0,64. Pada Kromatografi lapis tipis disemprotkan dengan reagen Liebermann Burchard memberikan noda berwarna merah muda reaksi ini positif untuk senyawa golongan terpenoid. Isolat A dan isolat B yang dihasilkan berbentuk serbuk, berwarna putih dan tidak berbau.
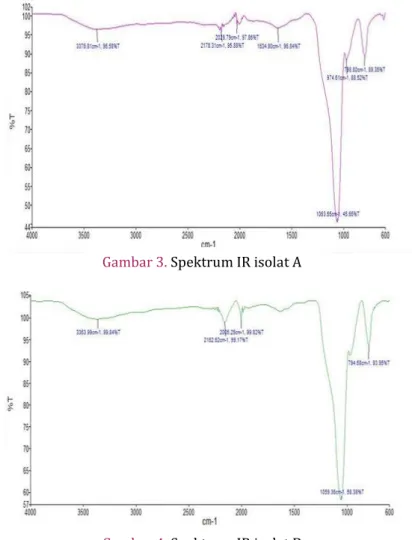
Hasil identifikasi dengan
spektrofotometri Uv-Vis diperoleh panjang
gelombang maksimal isolat A 417 nm dan Isolat B 528 nm, hal ini kemungkinan dikarenakan kadar isolat yang terlalu sedikit sehingga mempengaruhi intensitas absorban. Hasil identifikasi terhadap Isolat A dan B dengan FTIR terlihat pada tabel 1.
KESIMPULAN
Berdasarkan hasil penelitian F1.2 aktif sebagai antioksidan dengan nilai IC50 sebesar 39,89 ppm. Dari hasil isolasi F1.2 diperoleh 2 isolat yaitu isolat A dan isolat B diidentifikasi senyawa ini merupakan golongan terpenoid. UCAPAN TERIMA KASIH
1. Bapak Aguspairi, S.Kp, M.Kep. sebagai Ketua STIKES Harapan Ibu.
Gambar 3. Spektrum IR isolat A
96 2. Ibu Dr. Madyawati Latief, S.P, M.Si. atas
kerjasama dan sumbangsihnya dalam penelitian ini.
3. M. Redho Okta Kurniawan atas semangat dan kerjanya dalam penelitian ini.
DAFTAR PUSTAKA
Efendi Hastrian. 2007. Isolasi Senyawa Antioksidan dari Fraki Butanol Akar Tapak Liman (Elephanthopus scabeer L). Padang.
Fajriah, dkk. 2007. Isolasi Senyawa Antioksidan dari Ekstrak Etil Asetat Daun Benalu Dendrophtoe pentandra L yang Tumbuh pada Inang Lobo-lobi. Jurnal Kimia Indonesia.
Madyawati, Nazaradin, Nelson. 2014. Skrining Bioaktivitas Beberapa Tumbuhan Mangrove Asal Kabupaten Tanjung Jabung Timur Provinsi Jambi. Laporan Penelitan Fundamental Pedada.
Avenido, P. and Serrano,A.E. 2012. Effects of the apple
mangrove (Sonneratia caseolaris) on growth,
nutrient utilization and digestive enzyme activities of theblack tiger shrimp Penaeus monodon postlarvae. European Journal of Experimental Biology.
Sariful et al. 2012. Evaluation of antinociceptive and antioxidant properties of the ethanolic extract of
Sonneratia caseolaris leaves. Pelagia Research
Library.
Selvi, A.T., Joseph, G.S., and Jayaprakarsa, G.K., 2003. Inhibition of growth and flatoxin production in Aspergillus flavus by Garcinia indica extract and its antioxidant activity. J. Food Microbiology 20 : 455-460
Sunarni, T., Pramono, S. & Asmah, R. 2007. Flavonoid antioksidan penangkap radikal dari daun Kepel (Stelechocarpus burahol (Bl.) Hook f. & Th.). Majalah Farmasi Indonesia. 18(3): 111-116. Zuhra, C.F, Tarigan, J. & Sihotang, H. 2008. Aktivitas
Antioksidan Senyawa Flavonoid dari Daun Katuk (Sauropus androgunus(L) Merr.). Jurnal Biologi Sumatera. ISSN : 1907-5537-3(1) : 7-10