EKSTRAKSI XILAN JERAMI PADI SEBAGAI BAHAN BAKU PREBIOTIK XILOOLIGOSAKARIDA
Oleh
Nurtika Kurniati
Jerami padi merupakan salah satu limbah berlignoselulosa yang mengandung hemiselulosa sekitar 24,5% dan belum banyak dimanfaatkan. Hemiselulosa pada jerami padi mengandung xilan yang dapat digunakan untuk produksi xilooligosakarida. Penelitian ini bertujuan untuk melakukan ekstraksi xilan dari jerami padi dan mempelajari hidrolisis xilan menggunakan enzim xilanase untuk menghasilkan xilooligosakarida. Ekstraksi xilan dari jerami padi dilakukan dengan menggunakan metode netralisasi dan diperoleh endapan sebesar 1,61-3,19%. Selanjutnya pada tahap pemurnian xilan, endapan xilan diperoleh sebesar 1,39-2,27%. Enzim xilanase diperlukan untuk menghidrolisis xilan menghasilkan xilooligosakarida. Aktivitas enzim xilanase yang diperoleh sebesar 0,330 U/mL. Pemurnian enzim xilanase dengan menggunakan pelarut organik berdasarkan variasi konsentrasi terhadap aseton. Pada konsentrasi aseton 60% menunjukkan aktivitas enzim xilanase tertinggi sebesar 0,881 U/mL. Analisis kuantitatif xilooligosakarida dilakukan dengan Kromatografi Cair Kinerja Tinggi (KCKT) dan metode DNS. Hasil penelitian menujukkan hidrolisis xilan diperoleh kadar xilosa terbesar pada waktu inkubasi 12 jam dengan menggunakan metode DNS sebesar 0,170 mg/mL.
EXTRACTION OF XYLAN FROM RICE STRAW AS RAW MATERIAL PREBIOTIC XYLOOLIGOSACCHARIDES
By
Nurtika Kurniati
Rice straw is one of lignocellulosic waste which contain about 24.5% hemicellulose which has not been utilized. Hemicellulose of rice straw contain xylan which can be used for xylooligosaccharides production. The objectives of this research was to do xylan ekstraction from rice straw and study xylan hydrolysis use xylanolytic enzyme to get xylooligosaccharides. Xylan ekstraction of rice straw has been done with neutralise method and get sediment about 1.61-3.19%. And than, xylan purification get sediment about 1.39-2.27%. Xylanolytic enzyme is needed to xylan hydrolysis. Xylanolytic enzyme activity from enzymes crude extract about 0.330 U/mL. Xylanolytic enzyme purification use organic solvent according concentration variation to aceton. Acetonic concentration 60% show xylanolytic enzyme activity supreme about 0.881 U/mL. Quantitative analysis of xylooligosaccharides were done using High Performance Liquid Chromatography and DNS method. The research result show that the highest xylose at the time of incubation 12 hours by using DNS method about 0.170 mg/mL.
I. PENDAHULUAN
A. Latar Belakang
Indonesia merupakan negara agraris dengan beberapa komoditas pertanian
unggulan, salah satunya adalah padi. Produksi padi mengalami peningkatan yang cukup signifikan. Menurut data BPS pada tahun 2009, produksi padi di Indonesia mengalami peningkatan sebesar 64.398.890 ton per tahun. Salah satu provinsi yang produksi padinya selalu mengalami peningkatan adalah provinsi Lampung. Berdasarkan data BPS pada tahun 2007–2008 produksi padi di provinsi
Lampung meningkat sebesar 0,77 %, pada tahun 2008–2009 meningkat sebesar 0,85 %. Meningkatnya produksi padi tersebut, secara tidak langsung
menyebabkan peningkatan volume jerami padi sebagai hasil samping produksi padi.
Pemanfaatan jerami padi selama ini masih belum dirasakan optimal, karena petani masih banyak membakarnya untuk menghindari penumpukan. Secara kimia, jerami padi masih memiliki nilai ekonomis yang tinggi karena jerami merupakan polimer lignoselulosa yang dapat dimanfaatkan untuk berbagai keperluan.
sebagian besar merupakan polimer xilan dengan konsentrasi sebesar 15-30 % berat kering jerami (Wenzl, 2003).
Xilan merupakan polimer dari xilosa yang berikatanβ-1,4-glikosidik dengan jumlah monomer 150-200 unit. Secara umum, xilan dapat ditempatkan ke dalam tiga kelas polisakarida yaitu pentosa, glikan dan hemiselulosa. Xilan dimasukkan ke dalam kelas pentosa karena pada prinsipnya xilan adalah polimer dari pentosa (xilosa). Jerami padi mengandung sekitar 35 % pentosa. Xilan dimasukkan ke dalam kelas glikan karena jumlahnya yang cukup besar dan merupakan polimer dari gula yang tak termodifikasi. Kebanyakan xilan diklasifikasikan atau disebut sebagai hemiselulosa karena dapat diperoleh melalui prosedur ekstraksi
hemiselulosa dan xilan adalah komponen pokok dari hemiselulosa. Menurut Whistler (1950) hemiselulosa murni identik dengan xilan.
Xilan dapat diekstraksi dari beberapa bahan berlignoselulosa dengan berbagai proses meliputi ekstraksi fisik secara proses hidrotermal (Garroteet al., 2001),
metodenya masih rumit dan belum dipelajari lebih lanjut. Sedangkan ekstraksi xilan secara kimia dengan metode netralisasi mudah dikerjakan dan lebih efisien dibandingkan dengan ekstraksi secara fisik dan enzimatis (Widyani, 2002).
Widyani (2002) melakukan ekstraksi xilan dari tongkol jagung dengan rendemen produk xilan sebesar 0,52 sampai 0,63 % setelah dimurnikan dengan berat awal tongkol jagung sebesar 50 gram dalam bentuk tepung menggunakan metode netralisasi. Kandungan tongkol jagung adalah 40 % selulosa, 36 % hemiselulosa dan 16 % lignin serta zat-zat lainnya 8 %.
Xilan dapat dihidrolisis menjadi xilooligosakarida melalui dua cara yaitu
hidrolisis menggunakan asam dan hidrolisis secara enzimatik. Cara yang pertama memiliki kelemahan karena produk akhir hidrolisis lebih banyak mengandung xilosa sebagai monomer penyusun xilan dibandingkan dengan xilooligosakarida. Sedangkan hidrolisis secara enzimatis menggunakan enzim xilanase yaitu enzim ekstraseluler yang dapat menghidrolisis polisakarida β-1,4-xilan yang merupakan komponen utama hemiselulosa menjadi xilooligosakarida dan xilosa (Richana, 2002). Xilosa hanya dihasilkan dalam jumlah yang terbatas pada akhir hidrolisis karena xilosa dapat menghambat aktivitas enzim xilanase untuk menghidrolisis xilan (Akpinaret al., 2010).
Hidrolisis xilan secara enzimatis dapat menghasilkan xilooligosakarida (XOS). XOS dapat berfungsi sebagai prebiotik yaitu senyawa yang dapat memperbaiki mikroflora pada usus dengan menstimulasi pertumbuhanBifidobacteriadan
2009). Upaya biokonversi xilan dari jerami padi menghasilkan XOS secara ekonomi dapat menguntungkan. Menurut Chenet al.,(2009), harga jual xilooliogosakarida mencapai $22 per-kg sehingga sangat potensial untuk meningkatkan nilai ekonomis limbah jerami padi.
Pada penelitian ini dilakukan proses ekstraksi xilan dari jerami padi menggunakan metode netralisasi. Untuk selanjutnya dipelajari proses hidrolisis xilan secara enzimatis menggunakan enzim xilanase yang dihasilkan dariActinomycetes.
B. Tujuan Penelitian
Penelitian ini memiliki beberapa tujuan, yaitu:
1. Melakukan ekstraksi xilan dari jerami padi menggunakan metode netralisasi. 2. Mempelajari hidrolisis xilan secara enzimatis menggunakan enzim xilanase
untuk menghasilkan xilooligosakarida.
C. Manfaat Penelitian
III. METODELOGI PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini dilakukan pada bulan Juni sampai Oktober 2011, bertempat di Laboratorium Instrumentasi Jurusan Kimia Fakultas MIPA Universitas Lampung. Analisis HPLC dilakukan di Laboratorium Penelitian dan Pengujian Terpadu Universitas Gajah Mada Yogyakarta.
B. Alat dan Bahan
1. Alat-alat yang digunakan
Alat-alat yang digunakan dalam penelitian ini meliputi alat-alat gelas, KNAUER HPLC FLD & RID (Complete Sys), sentrifugasi,waterbath, autoklaf merk Speed Clave Model S-90 N,Laminar air flowCRUMA model 9005-FL,
spektrofotometer UV-vis merek Hitachi 150-280, oven, lemari pendingin,
2. Bahan-bahan yang digunakan
Bahan yang digunakan adalah jerami padi yang telah dikeringkan dan dihaluskan, diperoleh dari Desa Gondang Rejo Kecamatan Pekalongan Kabupaten Lampung Timur Provinsi Lampung varietas Siherang. Bahan kimia yang dipakai meliputi medium YM (Yeast Malt), natrium klorida, reagen DNS, 0,02 M buffer sitrat fosfat pH 4, aseton, 0,02 M buffer fosfat pH 7, natrium hipoklorit, natrium
hidroksida, metanol, etanol, asetonitril,bircwood xylan(Sigma Chemical Co.) dan enzim xilanase yang dihasilkan dari isolatActinomycetesAcP-7.
C. Prosedur Penelitian
1. Pembuatan MediaYM (Yeast Malt)
Medium YM terdiri dari 4 g ekstrak khamir, 10 g ekstrak malt, 15 g glukosa per 1 Liter media, diautoklaf selama 15 menit pada suhu 121ºC dan tekanan 2 atm, kemudian ditambahkan dengan 50 µg/L Nistatine dan 25 µg/L
Streptomycine.
2. Pembuatan Pereaksi
a. Pembuatan Buffer Fosfat
1) Larutan Stok A (NaH2PO4·H2O 0,2 M)
Sebanyak 27,8 g NaH2PO4·H2O dilarutkan dengan air suling hingga volume 1000 mL.
Sebanyak 35,6 g Na2HPO4·2H2O dilarutkan dengan air suling hingga volume 1000 mL.
b. Pembuatan Pereaksi DNS
Larutan A : 3 g NaOH; 0,6 g fenol; 3 g DNS dalam 240 mL air suling. Larutan B : 0,25 g Na-sulfit; 2 g Na-K-tartarat dan 5 mL air suling. Sebanyak 3 mL larutan B ditambahkan pada 240 mL larutan A dan ditambahkan air suling hingga volume 300 mL.
3. Ekstraksi Xilan
Sebanyak 100 gram sampel jerami padi dalam bentuk tepung dimasukkan ke dalam wadah plastik dan direndam dalam 1 liter NaOCl 1 % selama 5 jam pada suhu ruang. Setelah 5 jam, sampel dibilas dengan air dan disaring (penghilangan lignin). Sampel kemudian dikeringkan dibawah sinar matahari atau pada suhu 50oC selama 48 jam dan selanjutnya diekstraksi.
Setelah netralisasi, dilakukan sentrifugasi untuk memisahkan cairan (supernatan) dengan padatan (endapan). Sentrifugasi berlangsung selama 30 menit dengan kecepatan putar 4000 rpm. Xilan terkandung dalam supernatan. Etanol ditambahkan ke dalam supernatan untuk memisahkan xilan yang larut di
dalamnya. Perbandingan supernatan dengan etanol yang ditambahkan adalah 1:2 (Yoshidaet al., 1994). Sebagai tahap akhir, dilakukan pemisahan antara xilan yang diperoleh dengan cairan campuran supernatan-etanol yang tidak ikut mengendap sebagai xilan.
4. Purifikasi Xilan
Hemiselulosa A (endapan yang diperoleh dari ekstraksi xilan) dilarutkan dalam aquades (1:12,5 b/v), disentrifuga dengan kecepatan putaran 6000 rpm selama 30 menit. Endapan yang diperoleh dilarutkan dalam NaOH 4 %. Larutan alkali yang mengandung xilan tersebut kemudian disaring untuk memisahkan kotoran-kotoran yang terdapat di dalamnya. Filtrat yang diperoleh diasamkan dengan HCl 6 N hingga pH 4,5-5,0, kemudian dilakukan sentrifuga 4000 rpm selama 30 menit untuk memperoleh endapan (xilan murni) selanjutnya disaring. Xilan dapat didispersikan kembali dalam etanol.
5. Produksi Enzim Xilanase
xilanase dilakukan dengan mengikuti prosedur fermentasi fase padat dengan menggunakan kondisi optimum pada penetapan waktu optimum hidrolisis jerami padi. Enzim xilanase diproduksi pada media YM cair dengan komposisi : 4,0 g ekstrak khamir, 10 g ekstrak malt, 15 g glukosa, dan 0,5% xilan birchwood diinkubasi pada suhu ruang selama 15 hari. Sebanyak 7 ose isolatActinomycetes
dimasukkan ke dalam media inokulum. Selanjutnya 100 mL inokulum
ditambahkan pada 100 g jerami padi ukuran 1-2 cm. Pemanenan dilakukan pada waktu optimum selama 15 hari dengan menambahkan 1000 mL 0,2 M buffer fosfat pH 7 kemudian diaduk dan disaring dengan menggunakan kertas saring. Filtrat yang diperoleh digunakan sebagai ekstrak kasar enzim xilanase yang akan diukur aktivitasnya.
6. Pengukuran Aktivitas Enzim Xilanase
Aktivitas xilanase diujikan dengan substratbirchwoodxilan menggunakan reagen DNS (Miller, 1959). Sebanyak 1000μL substrat 0,5% xilan birchwood
ditambahkan 900μL 0,02 M bufer fosfat pH 7. Kemudian larutan ini
pada suhu ruang. Pengukuran absorbansi masing-masing larutan dilakukan padaλ 540 nm. Satu unit aktivitas xilanase didefinisikan sebagai jumlahμmol xilosa yang dihasilkan permenit untuk setiap mL enzim pada kondisi optimumnya.
7. Pengendapan Xilanase Menggunakan Aseton
Ekstrak kasar xilanase dimurnikan dengan diendapkan menggunakan aseton secara bertahap pada konsentrasi 60, 70, 80 dan 90%. Sebanyak 10 mL ekstrak kasar xilanase ditambahkan aseton dingin (disimpan pada suhu -200C) sedikit demi sedikit sampai tercapai konsentrasi yang diinginkan sambil diaduk perlahan menggunakan pengaduk magnetik (Scopes, 1987). Campuran tersebut disimpan dalam lemari pendingin selama 2 jam, kemudian disentrifuga pada kecepatan 4500 rpm pada suhu 40C selama 15 menit. Endapan protein yang terbentuk diambil dan dilarutkan dalam 0,02 M bufer fosfat pH 7 dengan volume seminimal mungkin (1 mL). Aktivitas yang tinggi menunjukkan persentase konsentrasi aseton yang optimum.
8. Hidrolisis Xilan
9. Analisis Produk Akhir Xilooligosakarida dengan KCKT
II. TINJAUAN PUSTAKA
A. Jerami Padi
Jerami adalah tanaman padi yang telah diambil buahnya (gabahnya), sehingga tinggal batang dan daunnya yang merupakan limbah pertanian terbesar serta belum sepenuhnya dimanfaatkan karena adanya faktor teknis dan ekonomis. Pada sebagian petani, jerami sering digunakan sebagai mulsa pada saat menanam palawija. Hanya sebagian kecil petani menggunakan jerami sebagai pakan ternak alternatif di kala musim kering karena sulitnya mendapatkan hijauan. Di lain pihak jerami sebagai limbah pertanian, sering menjadi permasalahan bagi petani, sehingga sering di bakar untuk mengatasi masalah tersebut (Ikhsanet al., 2009). Sementara itu, pembakaran limbah pertanian meningkatkan kadar CO2di udara yang berdampak terjadinya pemanasan global (Puspaningsih, 2007)
limbah kayu tergantung pada spesies tanaman, umur tanaman, kondisi lingkungan tempat tumbuh dan langkah pemprosesan (Erikssonet al., 1990).
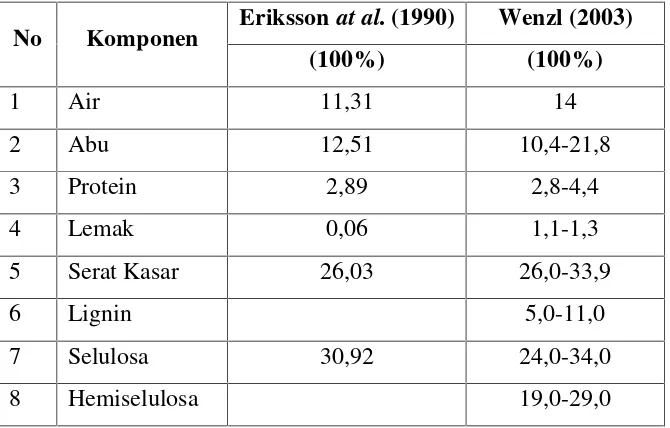
Tabel 1. Komposisi kimiawi jerami padi
No Komponen Erikssonat al. (1990) Wenzl (2003)
(100%) (100%)
1 Air 11,31 14
2 Abu 12,51 10,4-21,8
3 Protein 2,89 2,8-4,4
4 Lemak 0,06 1,1-1,3
5 Serat Kasar 26,03 26,0-33,9
6 Lignin 5,0-11,0
7 Selulosa 30,92 24,0-34,0
8 Hemiselulosa 19,0-29,0
B. Hemiselulosa
Hemiselulosa merupakan salah satu komponen lignoselulosa yang sering diartikan sebagai selulosa dengan bobot molekul rendah. Hemiselulosa terdiri dari dua sampai tujuh residu gula yang berbeda. Sifat–sifat hemiselulosa di antaranya adalah tidak tahan terhadap perlakuan panas, struktur amorf dan mudah dimasuki pelarut (Sjostrom, 1995), dapat diekstraksi menggunakan alkali dan ikatannya lemah sehingga mudah dihidrolisis (Winarno, 1984). Menurut Judoamidjojoet al.,(1989) molekul hemiselulosa lebih mudah menyerap air, bersifat plastis dan mempunyai permukaan kontrol antar molekul yang lebih luas dibandingkan selulosa. Berbeda dengan selulosa yang merupakan homopolisakarida, hemiselulosa merupakan heteropolisakarida.
Hemiselulosa terdiri dari monomer gula penyusun yang dapat dikelompokkan pada heksosa, pentosa, asam heksuronat dan deoksi heksosa. Rantai utama hemiselulosa dapat hanya terdiri dari satu macam monomer saja (homopolimer), misalnya xilan, atau dapat terdiri dari dua atau lebih monomer (heteropolimer) misalnya glukomanan.
C. Xilan
Xilan terdapat pada tanaman berlignoselulosa, kebanyakan dijumpai pada tanaman-tanaman tahunan dan khususnya pada limbah-limbah pertanian seperti tongkol jagung, bagas tebu, jerami padi, dedak gandum dan biji kapas.
bahan-bahan yang kaya akan xilan, kayu keras mengandung 20-25% xilan sedangkan kayu lunak mengandung 7-12% (Saha, 2003).
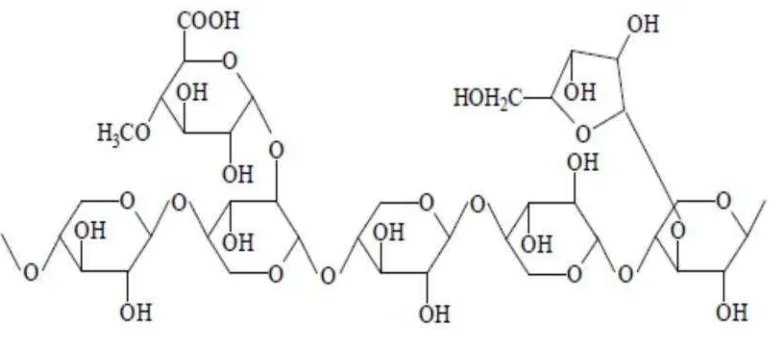
Xilan merupakan komponen utama dari hemiselulosa. Xilan atau polimer xilosa adalah komponen yang paling banyak terdapat dalam hemiselulosa tanaman. Xilan terikat pada selulosa, pektin, lignin, dan polisakarida lainnya untuk membentuk sel tanaman (Howardet al., 2003). Xilan merupakan polimer dari xilosa yang berikatan β -1, 4-glikosidik dengan jumlah monomer 150–200 unit.
Rantai utama penyusun polimer xilan terdapat rantai samping berupa arabinosa, galaktosa, asam glukoronat, asam asetat, asam ferulat dan asam p-kumarat. Setiap sepuluh residu xilosa terikat asam 4-O-metil glukoronat pada posisi atom C nomor 2 di xilosa kedua. Pada kayu keras asetilasi xilan lebih banyak ditemui pada posisi atom C nomor 3 dibandingkan dengan atom C nomor 2. Adanya asetil menyebabkan xilan dapat larut di air. Gugus asetil dapat dihilangkan dengan perlakuan basa (Beget al., 2001). Pada kayu lunak, xilan tersusun atas arabinosa-metilglukuroxilan dan dengan kandungan asam
4-O-metilglukoronat yang lebih tinggi dibanding xilan pada kayu keras. Xilan pada kayu lunak tidak terasetilasi karena atom C nomor 3 telah mengikatα -L-arabinofuranosa dengan membentuk ikatan α-1,3 glikosida. Struktur asli xilan sangat kompleks dan dapat disubstitusi dengan grup asetil, L-arabinofuranosil, glukuronosil pada rantai sampingnya (Saha, 2000).
persen pentosa. Xilan dimasukkan ke dalam kelas glikan karena jumlahnya yang cukup besar dan merupakan polimer dari gula yang tak termodifikasi.
Kebanyakan xilan diklasifikasikan atau disebut sebagai hemiselulosa karena dapat diperoleh melalui prosedur ekstraksi hemiselulosa dan xilan adalah komponen pokok dari hemiselulosa.
Gambar 1 : Struktur hipotetikal xilan dari tumbuhan (Beget al., 2001)
Xilan mempunyai sifat-sifat dapat larut dalam larutan alkali (NaOH atau KOH 2-15 %), larut dalam air dan penyulingan dengan menggunakan larutan HCL xilan dapat berubah menjadi furfural. Xilan mudah dihidrolisis oleh asam dan
mempunyai putaran optik negatif (Howardet al., 2003).
Ditinjau dari segi industri, xilan memiliki banyak kegunaan, diantaranya adalah 1. Xilan dapat diubah menjadi xilosa, melalui proses hidrolisis dengan bantuan
asam maupun enzim.
3. Xilosa sangat baik untuk penderita diabetes (Irawadi, 1999). Selain itu, dapat digunakan sebagai pemanis pada permen karet karena di samping tidak menyebabkan kegemukan juga tidak merusak gigi. Kegunaan lainnya dari xilosa adalah sebagai campuran pasta gigi karena memperkuat gusi (Saha, 2003).
4. Xilan dapat dikonversi menjadi xilooligosakarida sebagai bahan prebiotik dengan menggunakan enzim xilanase (Ramirezet al., 2002).
D. Ekstraksi Xilan
Xilan dapat diperoleh dengan cara mengekstraksi bahan berlignoselulosa.
Beberapa pelarut dapat dipergunakan untuk mengekstrak xilan, diantaranya adalah natrium hidroksida (NaOH), amonium hidroksida (NH4OH) dan kalium
hidroksida (KOH). Di antara ketiga pelarut tersebut, Natrium Hidroksida adalah yang terbaik karena dapat menghasilkan xilan yang relatif bersih dari pengotor, warnanya lebih putih, serta mudah larut dalam air. Adapun pelarut lain yang dapat digunakan untuk mengekstraksi adalah dimetilsufoxida, akan tetapi
Xilan dapat diekstraksi dari beberapa bahan berlignoselulosa dengan berbagai proses meliputi ekstraksi secara alkali dengan menggunakan NaOH, KOH (Pulset al.,2006), proses hidrotermal,pretreatmentdengan asam sulfat dan ultrasonikasi.
1. Ekstraksi Xilan secara Netralisasi
Menurut Widyani (2002), jerami padi direndam dalam NaOCl 1 % pada suhu ruang. Kemudian sampel dibilas dengan air dan disaring (penghilangan lignin). Sampel kemudian dikeringkan di bawah sinar matahari atau pada suhu 50oC selama 48 jam dan selanjutnya diekstraksi. Padatan yang dihasilkan pada tahap sebelumnya direndam dalam larutan NaOH 15 % selama 24 jam pada suhu 28oC. Perendaman ini bertujuan untuk mengekstraksi xilan dan disaring untuk
memperoleh filtrat. Filtrat yang dihasilkan ditampung untuk diukur pH-nya dan selanjutnya dinetralkan dengan HCl 6 N hingga pH 7. Ampas yang sudah tidak terpakai dibuang.
Setelah netralisasi, dilakukan sentrifugasi untuk memisahkan cairan (supernatan) dengan padatan (endapan). Xilan terkandung dalam supernatan. Etanol
ditambahkan ke dalam supernatan untuk memisahkan xilan yang larut di
dalamnya. Perbandingan supernatan dengan etanol yang ditambahkan adalah 1:2 (Yoshidaet al., 1994). Sebagai tahap akhir, dilakukan pemisahan antara xilan yang diperoleh dengan cairan campuran supernatan-etanol yang tidak ikut mengendap sebagai xilan.
2. Ekstraksi Xilan dengan proses Hidrotermal
Jerami padi yang telah kering diblender dan dipanaskan pada suhu 60oC selama 16 jam. Xilan diekstraksi selama 3 jam pada suhu 35oC dengan penambahan 24 persen KOH (w/v) yang mengandung 1 persen NaBH4, dengan volume KOH 17 mL per 2 gram jerami. Ekstrak disentrifugasi pada 10000 rpm selama 2 menit lalu difiltrasi menggunakan kertas Wattman No. 1. Xilan diendapkan dengan menambahkan 2 kali volum etanol dingin dan 0,2 kali volume asam asetat. Endapan disaring dan dikeringkan dalam oven bersuhu 60oC.
3. Ekstraksi Xilan secara Ultrasonikasi
Ultrasonikasi dengan intensitas yang tinggi merupakan cara untuk mengisolasi fibril yang digunakan untuk perlakukan material yang mengandung selulose untuk menghasilkan fibril yang kecil pada skala nano dan mikro (Chenget al., 2009). Ultrasonikasi dapat menghasilkan kekuatan mekanis yang sangat kuat, sehingga pemisahan mikrofibril selulosa dari selulosa kemungkinan dilakukan oleh kekuatan hidrodinamik dari ultrasonikasi. Metode ini secara luas terpakai pada beberapa proses, terutama diemulsifikasi, katalisis, homogenisasi dan disperse. Efisiensi proses sonifikasi dari tanaman telah dibuktikan, dari pemecahan serabut yang meningkatkan hasil ekstraksi dan waktu ekstraksi cepat. Waktu yang diperlukan untuk proses ultrasonikasi dapat dikurangi ketika kekuatan iradiasi meningkat (Kimet al., 1999)
E. Hidrolisis Xilan
penyusunnya (glukosa & xilosa). Hidrolisis sempurna selulosa menghasilkan glukosa, sedangkan hemiselulosa menghasilkan beberapa monomer gula pentosa (C5) dan heksosa (C6). Secara umum teknik hidrolisis dibagi menjadi dua, yaitu: hidrolisis dengan enzim dan hidrolisis dengan asam.
1. Hidrolisis Enzim
Hidrolisis enzim merupakan proses penguraian suatu polimer yang kompleks menjadi monomer penyusunnya dengan menggunakan enzim (Perezet al., 2002). Hidrolisis enzimatis memiliki beberapa keuntungan dibandingkan hidrolisis asam, antara lain: tidak terjadi degradasi gula hasil hidrolisis, kondisi proses yang lebih lunak (suhu rendah, pH netral), berpotensi memberikan hasil yang tinggi, dan biaya pemeliharaan peralatan relatif rendah karena tidak ada bahan yang korosif (Taherzadeh and Karimi, 2007). Beberapa kelemahan dari hidrolisis enzimatis antara lain adalah membutuhkan waktu yang lebih lama, dan kerja enzim dihambat oleh produk. Di sisi lain harga enzim saat ini lebih mahal daripada asam sulfat, namun demikian pengembangan terus dilakukan untuk menurunkan biaya dan meningkatkan efisiensi hidrolisis maupun fermentasi (Sanchez and Cardona, 2007).
2. Hidrolisis asam
Di dalam metode hidrolisis asam, biomassa lignoselulosa dipaparkan dengan asam pada suhu dan tekanan tertentu selama waktu tertentu, dan menghasilkan
diteliti dan dimanfaatkan untuk hidrolisis asam (Taherzadeh and Karimi, 2007). Hidrolisis asam dapat dikategorikan melalui dua pendekatan umum, yaitu hidrolisis asam konsentrasi tinggi pada suhu rendah dan hidrolisis asam konsenrasi rendah pada suhu tinggi. Pemilihan antara dua cara tersebut pada umumnya didasarkan pada beberapa hal yaitu laju hidrolisis, hasil total hidrolisis, tingkat degradasi produk dan biaya total proses produksi (Kosaricet al., 1983).
F. Enzim Xilanase
Enzim merupakan produk protein sel hidup yang berperan sebagai biokatalisator dalam proses biokimia, baik yang terjadi di dalam sel maupun di luar sel
(Poedjiadi, 1994). Enzim merupakan katalisator sejati yang meningkatkan kecepatan reaksi kimia spesifik dengan nyata. Tanpa enzim, suatu reaksi kimia akan berlangsung lambat. Enzim tidak dapat mengubah titik kesetimbangan reaksi yang dikatalisisnya, enzim juga tidak akan habis dipakai atau diubah secara permanen oleh reaksi-reaksi tersebut. Fungsi terpenting dari enzim adalah
kemampuannya menurunkan energi aktivasi suatu reaksi kimia. Kemampuan enzim dalam mendegradasi substrat dipengaruhi oleh beberapa faktor antara lain konsentrasi enzim, konsentrasi substrat, pH serta temperatur (Lehninger, 1982).
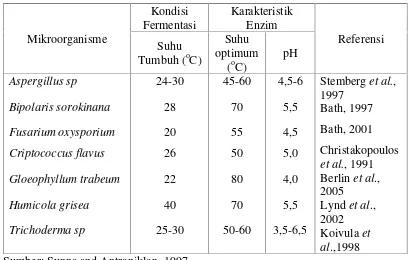
Bacillus, Cryptococcus, Penicillium, Aureo-basidium, Fusarium, Rhizomucor,
Humicola(Haltrichet al., 1996).
Tabel 2: Beberapa mikroorganisme penghasil xilanase
Mikroorganisme Sumber: Sunna and Antraniklan, 1997
Xilanase merupakan enzim ekstraseluler yang dapat menghidrolisis polisakarida β-1,4-xilan yang merupakan komponen utama hemiselulosa menjadi
xilooligosakarida dan xilosa (Richana, 2002). Struktur xilan yang sangat bervariasi mulai dari rantai linier 1,4-β-polixilosa sampai heteropolisakarida bercabang banyak. Xilanase dapat diklasifikasi berdasarkan substrat yang dihidrolisis yaituβ-1,4-D-xilosidase (EC 3.2.1.37) eksoxilanase dan endo-β -1,4-xilanase (EC3.2.1.8) atau biasa disebut endo-1,4-xilanase (Yarema, 2005). β -1,4-xilosidase yaitu xilanase yang mampu menghidrolisis xilooligosakarida yang berantai pendek menjadi xilosa. Aktivitas enzim akan menurun dengan
juga merupakan inhibitor bagi enzim β-1,4-D-xilosidase. Eksoxilanase mampu memutus rantai polimer xilan pada ujung reduksi, sehingga menghasilkan xilosa sebagai produk utama dan sejumlah oligosakarida rantai pendek. Endoxilanase mampu memutus ikatan β-1,4 pada bagian dalam xilan secara teratur. Ikatan yang diputus ditentukan berdasarkan panjang rantai substrat, derajat percabangan, ada atau tidaknya gugus substitusi, dan pola pemutusan dari enzim hidrolase (Richana, 2002; Jefries, 1996).
Xilanase (endo-beta-1,4-xilanase, E.C 3.2.1.8) adalah enzim yang mampu memutuskan ikatan pada rantai utama xilan yang akan membentuk molekul oligosakarida. Enzim inilah yang memegang peranan kunci dalam mendegradasi polimer xilan yang banyak ditemukan pada dinding sel tanaman berkayu (Saha, 2003).
Mekanisme kerja enzim xilanase mampu mendegradasi polimer xilan dengan cara memutus ikatan antargugus pada bagian tengah secara acak yang akan
menghasilkan xilooligosakarida,(Collinset al., 2005).
G. Prebiotik
merugikan dalam tubuh, sehingga ASI pun dikatakan sebagai prebiotik. Sebenarnya prebiotik sudah terdapat dalam tanaman seperti pada umbi dahlia, bawang merah, bawang putih, asparagus, kedelai, ubi jalar, dan juga pada susu. Namun itu bukan berarti dengan hanya mengkonsumsi bahan-bahan tersebut maka kita akan dapat memperoleh prebiotik yang diharapkan. Alasannya kadar prebiotiknya biasanya sangat rendah dan bervariasi tergantung varietasnya. Alasan lainnya adalah karena jumlahnya sangat kecil, maka glukosa dan fruktosa dari bahan-bahan tadi sangat mudah diserap usus sehingga prebiotiknya ikutan habis sebelum mencapai usus besar. Padahal di usus besar itu terjadi penyerapan nutrisi yang dibantu mikroba, tidak seperti pemahaman masa lalu yang mengira usus besar hanya berisi sampah yang siap dibuang. Contoh prebiotik adalah fruktooligosakarida (Gibson, 1995) dan xilooligosakarida (Vazquezet al., 2000).
Bentuk yang paling umum dari probiotik adalah produk peternakan dan makanan probiotik. Bagaimanapun juga, tablet dan kapsul berisikan bakteri dalam kondisi dibekukan juga dapat ditemukan.
Beberapa probiotik umum meliputi berbagai spesies dari generaBifidobacterium
Prebiotik yang banyak dikenal dan digunakan adalah oligosakarida kedelai (yang terdiri atas rafinosa dan stakiosa), frukto-oligosakarida (oligofruktosa), Inulin, Laktulosa, Laktosukrosa dan xilooligosakarida. Prebiotik XOS yang disebutkan dapat meningkatkan pertumbuhanbifidobacterium. Bakteri bermanfaat yang terdapat dalam minuman yoghurt atau susu fermentasi komersial. Apabila dikonsumsi dengan dosis yang tepat dan cara yang benar, maka prebiotik dapat mengobati atau mendukung pengendalian penyakit seperti kanker usus, liver, sembelit, diabetes melitus dan kanker (Hidayat dkk., 2008).
Sifat oligosakarida yang tidak dicerna ataupun diserap oleh saluran pencernaan akan mencapai usus besar dalam keadaan utuh dan digunakan sebagai makanan oleh bakteri non patogen di dalam usus besar yaituBifidobacteriadan
Lactobacilli(Muchtadi, 2009).
H. Kromatografi Cair Kinerja Tinggi (KCKT)
Kromatografi cair kinerja tinggi ideal untuk memisahkan molekul yang mempunyai bobot molekul tinggi. Proses kromatografi cair kinerja tinggi dilakukan di dalam kolom dengan tekanan tinggi. Sistem fase gerak pada kromatografi kinerja cair tinggi berupa larutan yang mempunyai perbedaan polaritas di mana larutan tersebut harus murni dan tidak mengandun gas. Sistem injeksi sangat efisien karena di dalam mikroliter. Pada kromatografi kinerja cair tinggi juga terdapat kolom yang juga berfungsi sebagai tempat larutan fase gerak yang dialirkan ke detektor (Jonhson, 1991).
Menurut Safitri (2007), produk hidrolisis xilooligosakarida oleh enzim xilosidase termofilik rekombinan ini dianalisis dengan HPLC untuk memperoleh hasil yang maksimal. Analisis HPLC menggunakan kolom karbohidrat (Waters), detektor indeks bias pelarut asetonitril 60% dalam air, kecepatan alir 1 mL/menit, konsentrasi senyawa standar 1%, volume injek 20 mikroliter dan suhu 40oC.
I. Spektrofotometer Ultraviolet-Visibel (UV-vis)
Spektrosfotokopi merupakan studi mengenai interaksi cahaya dengan atom atau molekul. Bila cahaya jatuh pada senyawa, maka sebagai cahaya tersebut akan terserap oleh molekul tersebut. Banyaknya sinar yang diabsorbsi adalah sebanding dengan konsentrasi senyawa yang dianalisis (Sudjadi, 1983).
karakteristik dari molekul. Spektrum tampak (visibel) terentang dari sekitar 400 nm (ungu) sampai 750 nm (merah), sedangkan spektrum ultraviolet terentang dari 100 nm sampai dengan 400 nm (Fessenden and Fessenden, 1986).
Serapan cahaya oleh molekul dalam daerah spektrum UV-vis tergantung pada struktur elektronik dari molekul. Spektrum UV-vis dari senyawa organik berkaitan erat dengan transisi-transisi elektron di antara tingkatan-tingkatan tenaga elektronik. Transisi-transisi tersebut biasanya antara orbital ikatan dan orbital anti ikatan. Tetapi dalam praktek, UV-vis digunakan terbatas pada sistem-sistem terkonjugasi (Sudjadi, 1983). Menurut Septiyana (2010), pengukuran aktivitas enzim xilanase dapat dilakukan dengan menggunakan spektrofotometer
UV-Vis. Pengukuran absorbansi masing-masing larutan dilakukan padaλ540
A. Simpulan
Berdasarkan hasil penelitian yang telah dilakukan, dapat disimpulkan bahwa: 1. Hasil ekstraksi xilan dari jerami dengan metode netralisasi sebesar
1,61-3,19% sedangkan setelah dilakukan purifikasi xilan sebesar 1,39-2,27%. 2. Aktivitas enzim xilanase terbesar adalah 0,967 U/mL setelah dilakukan
pengendapan dengan aseton 60%.
3. Kadar xilosa terbesar adalah 0,170 mg/mL dengan waktu inkubasi 12 jam.
B. Saran
(Skripsi)
Oleh
NURTIKA KURNIATI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
Oleh
nurtika kurniati
SKRIPSI
Sebagai Salah Satu Syarat untuk Mencapai Gelar SARJANA SAINS
Pada Jurusan Kimia
Fakultas Matematika dan Ilmu Pengetahuan Alam
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
Nama Mahasiswa : Nurtika Kurniati Nomor Pokok Mahasiswa : 0717011013
Jurusan : Kimia
Fakultas : Matematika dan Ilmu Pengetahuan Alam
MENYETUJUI 1. Komisi pembimbing
Heri Satria, M.Si. Dian Herasari, M.Si.
NIP.197110012005011002 NIP. 197108062000032001
2. Ketua Jurusan Kimia
1. Tim Penguji
Ketua :Heri Satria, M.Si. ………
Sekretaris/Anggota :Dian Herasari, M.Si. ………
Penguji Utama :Prof. Dr. Tati Suhartati, M.S. ………
2. Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Prof. Dr. Suharso, M.S. NIP 195704241987031001
Dengan segenap rasa syukur dan cintaku
kepada Allah SWT
Ku persembahkan karya kecil ini
Teruntuk
Rasullullah SAW , suri tauladan segala umat
Orang-orang yang sangat ku sayangi
(Bapak dan Ibu)
Kasih sayang, cinta, kesabaran, keikhlasan,
Dan do a yang terpernah putus di setiap hela napasmu..
Adikku yang selalu memberikan semangat..
(Dek Angga Nurhadiansyah)
Seseorang yang akan menjadi pendampingku kelak
Biarkan Masa Depan Datang Sendiri
Telah pasti datangnya ketetapan Allah, maka janganlah kamu meminta agar
disegerakan (datang)nya.
(QS. An-Nahl: 1)
Jadikan Buah Lemon Itu Minuman yang Manis
Boleh jadi kamu membenci sesuatu, padahal ia amat baik bagimu.
(QS. Al-Baqarah: 216)
Jangan Meletakkan Bola Dunia di Atas Kepala
Mereka mengira bahwa tiap-tiap teriakan yang keras ditujukan kepada mereka
(QS. Al-Munafiqun: 4)
Kesuksesan, bukan semata-mata karena betapa keras otot dan betapa tajam otak Namun Juga dari betapa lembut hati dalam
menjalani sesuatu
Penulis dilahirkan di Pekalongan pada tanggal 11 Juni 1989, anak pertama dari dua bersaudara, yang merupakan buah hati dari pasangan Bapak Mario dan Ibu Karsiti.
Penulis menyelesaikan pendidikan di Yayasan Taman Kanak-kanak Pertiwi Pekalongan pada tahun 1995, SD Negeri 2 Bratasena Mandiri pada tahun 2001, SLTP Negeri 1 Gedung Meneng pada tahun 2004 dan SMA Kartikatam Metro pada tahun 2007. Pada tahun yang sama, penulis diterima sebagai mahasiswa Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung melalui Penelusuran Kemampuan Akademik dan Bakat (PKAB).
tahun 2007-2008, Anggota Muda ROIS (AMAR) FMIPA Unila tahun 2007-2008, anggota Bidang Sains dan Penalaran Ilmu Kimia Himaki FMIPA Unila tahun 2008-2009, anggota Biro Akademik ROIS FMIPA Unila tahun 2008-2009. Sekretaris Umum Himaki FMIPA tahun 2009-2010 dan Sekretaris Eksekutif Badan Eksekutif Mahasiswa (BEM) FMIPA Unila tahun 2010-2011.
Assalamu’alaikum Wr. Wb.
Segala puji syukur selalu terpanjatkan kepada Allah SWT yang telah memberikan limpahan rahmat, nikmat dan karunia-Nya sehingga penulis dapat menyelesaikan skripsi ini dengan baik. Shalawat serta salam selalu tercurah kepada suri tauladan dan pemimpin umat, baginda Rasulullah Muhammad SAW, keluarga, sahabat dan semoga kita mendapat syafaatnya di Yaumil Akhir Kelak. Amin ya Rabbal alamin.
Skripsi dengan judul “Ekstraksi Xilan Jerami Padi sebagai Bahan Baku Prebiotik Xilooligosakarida” adalah salah satu syarat untuk memperoleh gelar Sarjana Sains pada Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung.
Dalam menyelesaikan skripsi ini, penulis banyak mendapat masukan, bantuan, bimbingan, dorongan, saran serta kritik dari berbagai pihak. Pada kesempatan ini, penulis mengucapkan terima kasih yang sebesar-besarnya kepada:
Abi dan dek Riska untuk dukungan dan doanya selama ini.
2. Bapak Heri Satria, M.Si., selaku Pembimbing Utama, yang telah bersedia meluangkan waktu dan dengan penuh kesabaran memberikan banyak ilmu pengetahuan, saran, arahan, motivasi, dukungan serta nasihat sehingga penulis dapat menyelesaikan penelitian dan skripsi ini dengan baik.
3. Ibu Dian Herasari, M.Si., selaku Pembimbing Kedua yang telah meluangkan waktu, memberikan banyak ilmu, arahan, saran, dan motivasi selama penyusun skripsi ini.
4. Ibu Prof. Dr. Tati Suhartati, M.S., selaku Pembahas yang telah meluangkan waktu, memberikan saran dan kritik demi terselesainya skripsi ini.
5. Ibu Dra. Ilim, M.S., selaku pembimbing akademik yang telah memberikan saran, semangat dan dukungan selama menyelesaikan studi.
6. Bapak Dr. Eng. Suripto Dwi Yuwono, M.T., selaku Sekretaris Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung atas saran, dukungan dan bantuan selama menyelesaikan studi.
7. Bapak Andi Setiawan, Ph.D., selaku Ketua Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam.Universitas Lampung atas saran dan dukungan selama menyelesaikan studi.
8. Bapak Prof. Dr. Suharso, M.S., selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung.
ini.
11. Seluruh dosen dan karyawan Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam.
12. Pak Wifik, Pak Kholid, Pak Bustomi, Pak Ocy, Pak Irwansyah, Pak Adit, Pak Anas, Bu Nidar, Bu Mar, Bu Mely, Bu Endah, Bu Eva, Bu Amy dan seluruh dewan guru SMA Plus Muhammadiyah Natar terima kasih atas semangat, motivasi dan nasehat selama ini. Serta siswa-siswa SMA Plus Muhammadiyah Natar kelas X–XII terima kasih atas keceriaan dan semangat kalian.
13. Untuk mb ku, Apri Triana, S.Pd (UNY) terima kasih selama di Yogya, Zaenal Irawan S.Pd (UNY) terima kasih telah membantuku selama analisis di Yogya, Tri Putra (IPB) terima kasih banyak sudah membantuku mencari informasi HPLC di Bogor dan sekitarnya dan Vera Khoirunisa, S.Si (Unair) terima kasih foto skripsi XOSnya sangat membantu untuk penyelesaian skripsi ini. 14. Sahabat-sahabatku: Andi Yuli Fitriani, S.Si., Clara Citra Resmie, S.Si., Dwi
Puji Astuti, S.Si., Eka Eprianti, S.Si., Eka Sulis Sundari, S.Si., Gia Yustika Asmoro, S.Si., Hade Sastra Wiyana, S.Si., Halimah, S.Si., Mega Dewi Fusfita Sari, S.Si dan Tristian Martika, S.Si., terima kasih untuk semua cerita, canda, tawa, sedih dan doa yang telah kalian berikan. Kalian adalah kebahagianku. 15. Temen-temen angkatan 2007: Afriyorawan N, Astri Rahayu, Dewi
Mitra Septanto, Riri Napitupulu, Sari Handayani, S.Si., Sunardi Sutrisna, S.Si (Physic Crew’s), Feby Indri S. S.Si., Lisa Eka Wahyuni, S.Si., Putri Amalia, S.Si., Ratna Maulina Dewi, S.Si., Sartika Putri Fauziana dan Winda Rahmawati (Biochemistry Crew’s), Yulistiawan, Adi Firman Shafa, Murdiyah, Muhlisun, Renius H dan Fajar Elin terima kasih teman-teman atas kebersamaan dan semua dukungannya.
16. Teman-teman seperjuangan di Laboratorium Instrumentasi: Yuniarti, S.Si. dan Hady Novadianto, S.Si. terima kasih atas motivasi, doa, saran dan kritiknya.
17. Untuk mbak-mbak ku : Karlina Widiyanti, Amd., Septiyana, S.Si, Eka Eva Krisna, S.Si dan Lince Dameria, S.Si selalu memberikan keceriaan, semangat dan motivasi dalam kebersamaan kita di Lab. Instrumentasi tercinta dan tersayang. Majid Rimbani dan M. Ruzki terima kasih untuk kebersamaannya selama ini
18. Teman-teman angkatan 2005, 2007, 2008, 2009, 2010 dan 2011 atas dukungan dan doa yang telah diberikan.
19. Himaki Crew’s 2009-2010 dan BEM FMIPA Crew’s Unila 2010-2011 atas doa, dukungan, semangat, dan saran selama masa perjuangan kita. Keceriaan kalian tidak akan pernah aku lupakan.
22. Teman-teman kost Salsabila: Ariska, Ayi, Ayu, Emil, Eli, Iin, Maya, Nita, Nory, Oci, Ria, Tika, Yuli, Mb Yayai, Mb Desti terima kasih keceriaan dan semangat kalian.
23. Semua pihak yang telah membantu dan dukungan dalam penyusunan skripsi ini yang tidak bisa disebutkan satu persatu.
Akhir kata, penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan. Akan tetapi, dengan segala kerendahan dan keikhlasan hati, penulis berharap semoga skripsi yang sederhana ini dapat berguna dan bermanfaat bagi semua pihak. Amin ya Rabb.
Wassalamu’alaikum Wr. Wb
Bandar Lampung, Februari 2012 Penulis,