APLIKASI SELULOSA
WHISKERS
BAGAS TEBU SEBAGAI
PENGUAT DALAM FILM KOMPOSIT BERBASIS PVA/MMT
ZAHRATUL AINI
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa tesis berjudul Aplikasi Selulosa
Whiskers Bagas Tebu sebagai Penguat dalam Film Komposit Berbasis PVA/MMT
adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Februari 2016
Zahratul Aini
RINGKASAN
ZAHRATUL AINI. Aplikasi Selulosa Whiskers Bagas Tebu sebagai Penguat
dalam Film Komposit Berbasis PVA/MMT. Dibimbing oleh TUN TEDJA IRAWADI, HENNY PURWANINGSIH dan LISMAN SURYANEGARA.
Di Indonesia, bagas tebu berpotensi sebagai sumber alternatif selulosa. Bagas tebu merupakan hasil samping dari proses ekstraksi cairan tebu di pabrik gula. Serat dari bagas tebu tidak dapat larut dalam air dan komposisi lignoselulosa bagas tebu terdiri atas 52.7% selulosa, 20% hemiselulosa, dan 24.2% lignin berdasarkan bobot kering. Hidrolisis asam dapat membuat mikroserat selulosa mengalami pemutusan pada bagian amorfus dan meninggalkan bagian kristalin yang disebut dengan selulosa whiskers. Kristal murni dari selulosa whiskers
memiliki tingkat kekakuan, luas permukaan, dan derajat kristalinitas yang tinggi sehingga sangat baik diaplikasikan dalam matriks polimer dan dapat berperan sebagai elemen penguat material.
Penambahan whiskers yang berukuran nanometer dalam komposit saat ini
sedang berkembang di dunia penelitian karena whiskers memiliki luas permukaan
yang sangat besar. Penelitian ini bertujuan menghasilkan selulosa whiskers dari
bagas tebu yang dapat diaplikasikan sebagai penguat dalam pembuatan film komposit.
Isolat selulosa diisolasi menggunakan basa dan pemucatan peroksida dilanjutkan hidrolisis asam pada suhu 45 °C. Selulosa whiskers dianalisis dengan
mikroskop elektron pemayaran (SEM), difraksi sinar-X (XRD), dan analisis thermogravimetrik (TGA) pada atmosfer udara. Kemudian film komposit poli (vinil alkohol) (PVA) dan mineral liat montmorilonit (MMT) dibuat dengan metode cetak. Film komposit dianalisis kuat tarik, persen perpanjangan, kristalinitas, dan degradasi termal. Hasil penelitian menunjukkan bahwa isolat selulosa bagas tebu bisa digunakan sebagai sumber untuk mendapatkan selulosa
whiskers dan memiliki struktur dengan panjang (L) 100 nm-10 µm dan diameter
(D) 10-100 nm Film komposit berhasil diperkuat dengan selulosa whiskers
ditunjukkan dengan meningkatnya kuat tarik, kristalinitas, dan suhu degradasi termal.
Kata kunci: selulosa whiskers, bagas tebu, film komposit, PVA, monmorilonit,
SUMMARY
ZAHRATUL AINI. Application of Cellulose Whiskers from Sugarcane Bagasse as Reinforcement in Nanokomposit Film Based on PVA/MMT. Supervised by TUN TEDJA IRAWADI, HENNY PURWANINGSIH and LISMAN SURYANEGARA.
Sugarcane bagasse is abundant in Indonesia, that can be used as an alternative source of cellulose. Sugarcane bagasse is a waste of the extraction process liquid cane sugar. Fiber from sugarcane bagasse can not be dissolved in water and the consist of lignocellulosic sugarcane bagasse is composed of 52.7% cellulose, 20% hemicellulose, and lignin 24.2% based on dry weight. Acid hydrolysis removed the amorphous and left parts of crystallinity, its called cellulose whiskers. Pure crystals of cellulose whiskers have high levels of rigidity, surface area and high crystallinity so it is the best way to apply in the polymer matrix and may serve as elements of reinforcement material.
The addition of whiskers in nanometer-sized in the composite is currently being developed in research because the whiskers have a very large surface area. Cellulose whiskers are suitable for reinforcement the matrix of polymers. This research aims to produce cellulose whiskers from sugarcane bagasse that could be applied as reinforcement in the composite film.
Cellulose were isolated using alkaline and peroxide bleaching followed by acid hydrolysis at 45 °C to produce cellulose whiskers. Cellulose whiskers were analyzed using scanning electron microscopy (SEM), X-ray diffraction (XRD), and Thermo gravimetric analysis (TGA) in air atmosphere. Futhermore, composite film of poly(vinyl alcohol) (PVA) and clay of montmorillonite (MMT) were made by casting method. Composites film were analyzed based on tensile strength, elongation to breaks, crystallinity, and thermal degradation. The result showed that sugarcane bagasse could be use as a source to obtain cellulose whiskers with length (L) 0.1-10 µm and diameter (D) 10-100 nm. The hybrid film were successfully reinforced by cellulose whiskers, indicated by increasing tensile strength, crystallinity and thermal degradation.
© Hak Cipta Milik IPB, Tahun 2016
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Kimia
APLIKASI SELULOSA
WHISKERS
BAGAS TEBU SEBAGAI
PENGUAT DALAM FILM KOMPOSIT BERBASIS PVA/MMT
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2016
Judul Tesis : Aplikasi Selulosa Whiskers Bagas Tebu sebagai Penguat dalam
Film Komposit Berbasis PVA/MMT Nama : Zahratul Aini
NIM : G451130061
Disetujui oleh Komisi Pembimbing
Prof Dr Tun Tedja Irawadi, MS Ketua
Dr Henny Purwaningsih, MS Anggota
Dr Lisman Suryanegara, M.Agr Anggota
Diketahui oleh
Ketua Program Studi Kimia
Prof Dr Dyah Iswantini P, MscAgr
Dekan Sekolah Pascasarjana
Dr Ir Dahrul Syah, MScAgr
PRAKATA
Bismillahirrahmanirrahimi
Alhamdulillah puji dan syukur penulis panjatkan kepada Allah subhanahu
wa ta’ala atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Shalawat serta salam tak lupa selalu tercurah kepada junjungan Nabi besar Muhammad SAW, sahabat, keluarga dan pengikutnya hingga akhir zaman. Ucapan terimakasih yang tak ternilai kepada Ayahanda dan Ibunda tercinta, Asnawi Hasan dan Nurmala M.Ali, serta saudara saudari tercinta Raudhatul Idami dan Asnawi Harun yang dengan kesabaran dan keikhlasan telah memberikan dorongan moral, material dan doa yang tulus. Selain itu, penulis juga menyampaikan rasa terimakasih yang dalam kepada suami tercinta Muhammad Ridho Afifi, M.Si.
Penulis mengucapkan terima kasih yang tulus kepada Prof Dr Tun Tedja Irawadi, MS selaku Ketua Komisi Pembimbing, Dr Henny Purwaningsih, MS dan Dr. Lisman Suryanegara, M.Agr selaku Anggota Komisi Pembimbing, atas segala curahan waktu, bimbingan, arahan, serta dorongan moral kepada penulis. Tidak lupa ucapan terima kasih kepada staf Laboratorium Kimia Terpadu IPB, dan teman-teman di Departemen Kimia IPB atas bantuan dan dukungan yang diberikan kepada penulis dalam menyelesaikan tesis ini
Semoga karya ilmiah ini bermanfaat.
Bogor, Februari 2016
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
1 PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 2
Tujuan Penelitian 2
Manfaat Penelitian 2
Ruang Lingkup Penelitian 2
2 METODE 3
Bahan 3
Alat 3
Prosedur Analisis Data 3
3 HASIL DAN PEMBAHASAN 5
Isolat Selulosa dari Bagas Tebu 5
Selulosa Terhidrolisisdari Isolat Selulosa 7
Sifat Mekanik Film Komposit 11
Morfologi Film Komposit 13
Kristalinitas Film Komposit 14
Kurva TG/DTA Film Komposit 15
4 SIMPULAN DAN SARAN 15
Simpulan 15
Saran 16
DAFTAR PUSTAKA 16
DAFTAR TABEL
1 Variasi perlakuan pembuatan film komposit (%) 5
2 Analisis komponen kimia (%) 6
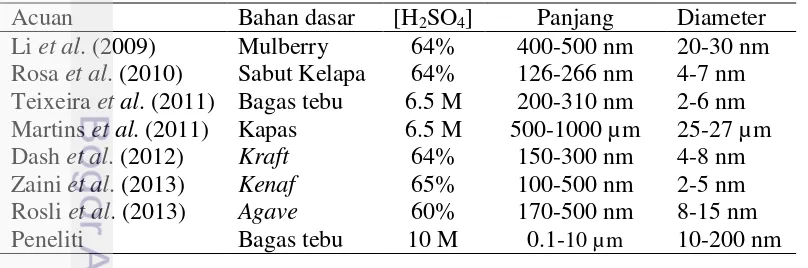
3 Hasil hidrolisis selulosa dari berbagai laporan penelitian 8 4 Ukuran panjang dan diameter serat selulosa whiskers 9
5 Pengaruh variasi konsentrasi selulosa whiskers dalam PVA 20% 12
6 Pengaruh variasi konsentrasi montmorilonit terhadap PVA 20% 12 7 Pengaruh konsentrasi selulosa whiskers pada film komposit dengan
montmorilonit 1.5% 13
DAFTAR GAMBAR
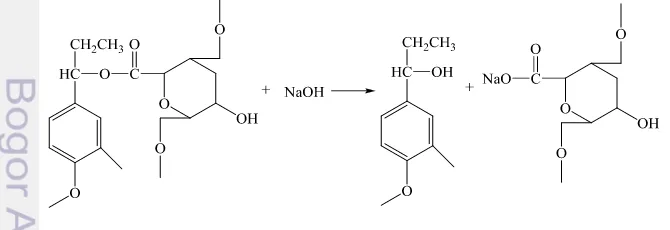
1 Skema reaksi kompleks karbohidrat lignin dengan NaOH 5
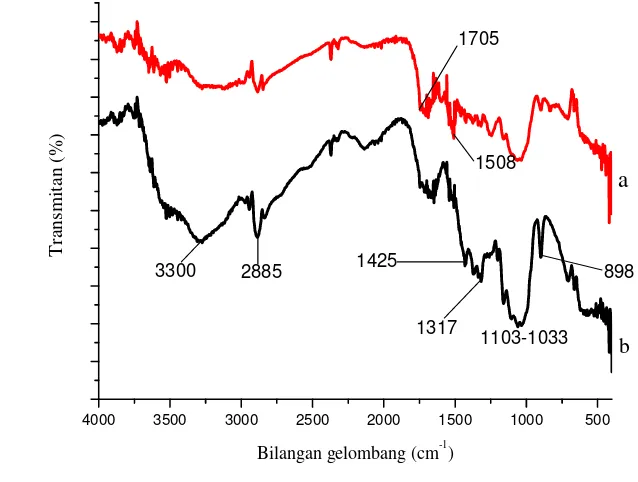
2 Spektrum FTIR (a) bagas tebu dan (b) isolat selulosa 7
3 Skema reaksi pemutusan ikatan eter pada selulosa dengan asam 8
4 Morfologi selulosa whisker 9
5 Difraktogram XRD (―) selulosa whiskers dan (―) isolat selulosa 10 6 Kurva TGA (―) Isolat selulosa dan (---) selulosa whiskers 11 7 Morfologi film PVA-MMT-SW (a) samping dan (b) permukaan film 14
8 Difraktogram XRD film (a) PVA-MMT-SW dan (b) PVA-MMT 14
9 Kurva TG/DTG film komposit (a) PVA-MMT dan (b) PVA-MMT-SW 15
DAFTAR LAMPIRAN
1 Diagram Alir Penelitian 21
2 Spektrum FTIR Bagas Tebu dan Isolat Selulosa 22
3 Difraktogram XRD Isolat Selulosa 23
4 Morfologi serat selulosa 24
5 Proses hidrolisis selulosa menggunakan varian konsentrasi H2SO4 25
6 Difraktogram XRD selulosa whiskers 26
7 Kurva TG/DTG Film Komposit 27
8 Ketebalan Film 28
9 Film komposit 28
10Analisis kuat tarik 29
1
PENDAHULUAN
Latar Belakang
Di Indonesia, bagas tebu berpotensi sebagai sumber alternatif selulosa. Bagas tebu merupakan hasil samping dari proses ekstraksi (pemerahan) cairan tebu di pabrik gula. Serat dari bagas tebu tidak dapat larut dalam air dan komposisi lignoselulosa bagas tebu terdiri atas 52.7% selulosa, 20% hemiselulosa, dan 24.2% lignin berdasarkan bobot kering (Samsuri et al. 2007). Ranby (1952)
mengatakan hidrolisis dengan menggunakan asam dapat membuat mikroserat selulosa mengalami pemutusan pada bagian amorfus dan meninggalkan bagian kristalin yang disebut dengan selulosa whiskers.
Samir et al. (2005) mengatakan whiskers sebagai bentuk kristal tunggal
dengan tingkat kemurnian yang tinggi dapat dibentuk dari mikrofibril. Kristal murni ini memiliki tingkat kekakuan, luas permukaan, dan kristalinitas yang tinggi sehingga sangat baik diaplikasikan dalam matriks polimer dan dapat berperan sebagai elemen penguat material. Proses utama untuk menghasilkan selulosa whiskers dari serat selulosa adalah dengan hidrolisis asam. Bagian
amorfus akan lebih mudah dihidrolisis, menyisakan bagian kristal (Habibi et al.
2010).
Ukuran dan morfologi whiskers bergantung pada sumber bahan baku
selulosa. Beberapa sumber selulosa whiskers telah diteliti di antaranya, mulberry
(Li et al. 2009), sabut kelapa (Rosa et al. 2010), bagas tebu (Teixeira et al. 2011;
Mandal & Chakrabarty 2011), kapas (Martins et al. 2011), kraft (Dash et al. 2012), kenaf (Zaini et al. 2013), Agave (Rosli et al 2013). Karakteristik geometris dari
selulosa whiskers bergantung pada kondisi proses hidrolisis asam, seperti waktu,
suhu, konsentrasi, dan kemurnian material. Jenis asam yang digunakan dalam tahap hidrolisis berpengaruh pada sifat permukaan whiskers. Kristal yang
dihasilkan dengan menggunakan HCl menunjukkan stabilitas koloid yang rendah, sedangkan hidrolisis menggunakan H2SO4 akan mengalami sulfatasi pada
beberapa permukaan (Laopaiboon et al. 2010; Klemm et al. 2011).
Penambahan whiskers yang berukuran nanometer dalam komposit saat ini
sedang berkembang di dunia penelitian karena whiskers memiliki luas permukaan
yang sangat besar dan kristalinitas yang baik. Apabila whiskers dikompositkan
dan terdistribusi merata akan mengubah mobilitas molekuler dan sifat mekanik film sehingga menghasilkan komposit dengan fleksibilitas, kekakuan, dan ketahanan panas yang baik (Kvien & Oksman 2007).
Banyak peneliti sebelumnya menggunakan selulosa sebagai penguat dalam film komposit. Sifat penguat (reinforcement) dari selulosa whiskers berbahan
dasar kapas terhadap PVA 30% menunjukkan bahwa penambahan selulosa
whiskers sebesar 5% meningkatkan kuat tarik selulosa whiskers yang lebih baik
sebesar 1.89 GPa dibandingkan dengan PVA murni sebesar 1.48 GPa (Jalaluddin
et al. 2011). Khan et al. (2012) meneliti sifat penguat selulosa nanokristal
berbahan baku karft dalam film berbasis kitosan. Selulosa nanokristal dengan
2
Kefektifan selulosa whiskers sebagai penguat diujikan menggunakan matrik
poli vinil alkohol (PVA). PVA merupakan polimer sintetis yang mudah larut dalam air, tidak berbau, tidak memiliki rasa, tidak beracun dan mudah terdegradasi secara alami (Tang & Alavi 2011). Hal yang menyebabkan PVA banyak digunakan sebagai bahan kemasan alternatif yang menjanjikan karena sifatnya sangat baik dalam pembentukan kemasan, tahan terhadap minyak dan lemak, memiliki kekuatan tarik, dan fleksibilitas tinggi.
Metode alternatif lain untuk meningkatkan barrier oksigen/air dan sifat mekanik selulosa whiskers diperlukan penambahan senyawa anorganik ke dalam
matriks, sehingga menciptakan material campuran organik-anorganik. Di antara material yang digunakan adalah mineral liat berupa Na-montmorilonit (MMT) yang telah banyak digunakan sebagai pengisi berbagai matriks polimer. Penambahan MMT dalam komposit diketahui dapat meningkatkan stabilitas termal dan laju degradasi pada matriks (Azeredo 2009).
Pada penelitian ini selulosa diisolasi dari bagas tebu menggunakan metode alkali dan pemucatan peroksida dilanjutkan dengan proses hidrolisis asam untuk menghasilkan selulosa whiskers. Selanjutnya selulosa whiskers diaplikasikan
sebagai penguat dalam film. Pencirian dilakukan terhadap sifat mekanik (kuat tarik dan persen perpanjangan), kristalinitas, dan degradasi termal.
Perumusan Masalah
Secara spesifik permasalahan yang akan diteliti adalah sebagai berikut: 1. Kesesuaian hasil isolat selulosa bagas tebu dengan referensi. 2. Karakteristik dan pencirian selulosa whiskers dari bagas tebu.
3. Kemampuan selulosa whiskers berperan sebagai penguat dalam pembuatan
film komposit.
Tujuan Penelitian
Penelitian ini bertujuan menghasilkan selulosa whiskers dari bagas tebu
yang dapat diaplikasikan sebagai penguat dalam pembuatan film komposit.
Manfaat Penelitian
Manfaat yang ingin dicapai adalah tersedianya informasi penggunaan selulosa whiskers yang diperoleh dari bagas tebu untuk diaplikasikan sebagai
penguat dalam pembuatan film komposit.
Ruang Lingkup Penelitian
3 komposit berbasis PVA/MMT dengan selulosa whiskers sebagai penguat matriks.
Pencirian film komposit berupa sifat mekanik (kuat tarik dan perpanjangan hingga putus), kristalinitas, analisis termal, dan morfologi film.
2
METODE
Penelitian ini dilaksanakan pada bulan Maret 2015 hingga Desember 2015 bertempat di Laboratorium Kimia Terpadu Kampus Institut Pertanian Bogor (IPB). Metode penelitian terdiri atas beberapa tahap yaitu isolasi selulosa bagas tebu, hidrolisis isolat selulosa menjadi selulosa whiskers, Pencirian selulosa whiskers
menggunakan SEM, XRD, DTA. Selanjutnya diaplikasikan pada pembuatan film nanokomposit dan pencirian film berupa sifat mekanik film (kuat tarik dan perpanjangan), morfologi film, analisis kristalinitas, dan degradasi termal.
Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah bagas tebu yang diperoleh dari pabrik gula Bungamayang Lampung utara, NaOH (pellet, Merck), H2O2 30% (Merck), H2SO4 98% (PT SMART Lab Indonesia), Akuades, kertas pH,
Polivinil Alkohol (PVA) (bratachem, Indonesia) dengan berat molekul 20 000, Na-montmorilonit.
Alat
Alat-alat yang digunakan adalah seperangkat alat gelas (pyrex), magnetic stirrrer (IKAMAG), differential thermogravimetric (Shimadzu DTG-60,
BATAN), sentrifugator (Suprema 21, Biomaterial LIPI Cibinong), spektrofotometer FTIR (IR Prestige-21 Shimadzu), SEM (EVO MA 10, LabFOR MABES Polri), XRD (Shimadzu XRD-7000, Indocement).
Prosedur Analisis Data
Isolasi Selulosa Bagas Tebu
4
larutan H2O2 5% dan dipanaskan dalam penangas air bersuhu 70 °C yang dijaga
konstan selama 3 jam kemudian campuran disaring dan endapan dicuci dengan aquades hingga pH netral. Perlakuan dengan larutan peroksida di ulang kembali 2 kali dengan penambahan waktu berturut-turut 3 jam dan 2 jam. Setelah itu, campuran disaring dan endapan dicuci hingga pH netral dan dikeringkan dalam oven bersuhu 60 °C.
Pencirian Selulosa
Pencirian selulosa meliputi penetapan kadar hemiselulosa, α-selulosa, lignin, dan analisis gugus fungsi dari spektrum FTIR.
Hidrolisis Selulosa (Dash et al. 2013)
Sebanyak 5 g selulosa bagas tebu yg telah dimurnikan dilarutkan dalam 100 mL H2SO4 dengan variasi konsentrasi 4 M, 6 M, 8 M, 10 M dan 12 M pada 45 °C,
diaduk selama 40 menit. Selanjutnya ditambahkan 500 mL akuades dingin untuk menghentikan reaksi. Sebagian dari asam sulfat akan hilang dari suspensi dengan disentrifugasi pada 12 000 rpm selama 10 menit. Hasil sentrifugasi dilanjutkan dengan dialisis menggunakan membran dialisis hingga mencapai pH 6-7. Hasil suspensi disonikasi selama 5 menit. Suspensi dimasukkan dalam lemari pendingin.
Pencirian Selulosa Whiskers
Analisis termal dilakukan untuk melihat suhu degradasi sampel dengan TG/DTA, kristalinitas whiskers dianalisis dengan XRD, dan morfologi dari
selulosa whiskers yang terbentuk dilihat dengan SEM.
Pembuatan Film Komposit (Spoljaric et al. 2014)
Pembuatan komposit dilakukan dengan metode cetak. Sejumlah larutan montmorilonit 1% dan larutan PVA 20% di aduk dengan kecepatan tinggi selama 40 menit, disonikasi selama 10 menit untuk memaksimalkan pendispersian molekul montmorilonit. Sejumlah selulosa whiskers 5% ditambahkan ke dalam
5 Tabel 1 Variasi perlakuan pembuatan film komposit (%)
Sampel PVA SW MMT
Film komposit dicirikan sifat mekaniknya berupa kuat tarik dan persen perpanjangan hingga putus, ketebalan film menggunakan mikrometer sekrup, pengaruh termal dengan TG/GTA, analisis kristalinitas selulosa whiskers dalam
film komposit menggunakan XRD, dan morfologi permukaan film dengan SEM.
3
HASIL DAN PEMBAHASAN
Isolat Selulosa dari Bagas Tebu
Berbagai metode isolasi selulosa yang telah dipublikasikan mengatakan adanya kesulitan yang cukup tinggi untuk mendapatkan selulosa murni (Sun et al.
2004), sehingga yang diperoleh adalah selulosa dalam bahan kasar berupa α -selulosa. α-selulosa merupakan selulosa yang tidak larut dalam larutan NaOH. Perlakuan dengan basa (NaOH) dapat memutuskan ikatan ester antara lignin dan selulosa melalui reaksi hidrolisis. Pada tahap awal isolasi selulosa menggunakan larutan NaOH untuk memutuskan ikatan antara lignin dengan selulosa dan menghilangkan hemiselulosa. Purwaningsih (2012) melaporkan larutan NaOH dapat menghilangkan lignin sebesar 60%. Gambar 1 menyajikan skema reaksi kompleks karbohidrat lignin dengan basa. Pada Gambar 1 dapat dilihat bahwa NaOH mampu memutuskan ikatan ester anatara selulosa dengan lignin.
6
Pada umumnya proses delignifikasi menggunakan natrium klorit (NaClO2)
dalam suasana asam. Penggunaan natrium klorit tidak ramah lingkungan karena penggunaan klorin dan senyawa turunannya dapat menghasilkan beberapa senyawa lain yang terklorinasi sehingga menyebabkan masalah yang serius terhadap lingkungan. H2O2 merupakan senyawa oksidator kuat sehingga dapat
digunakan pada proses pemucatan (bleaching) dan delignifikasi. H2O2 lebih
mudah terurai jika dilarutkan dalam media basa menghasilkan anion peroksida dan air, seperti reaksi dibawah ini.
H2O2 + HO-→ HOO- +H2O
Anion peroksida (HOO-) merupakan spesiaktif yang berperan penting dalam penghilangan gugus kromofor lignin. Anion peroksida bersifat nukleofilik kuat yang akan menyerang gugus etilena dan karbonil pada molekul lignin dan mengubahnya menjadi spesi yang tidak mengandung kromofor. Perlakuan dengan H2O2 dalam media basa juga dapat meningkatkan pH reaksi sehingga dapat
digunakan untuk melarutkan sebagian besar hemiselulosa, selain berfungsi sebagai pereaksi pada proses delignifikasi dan pemucatan (Sun et al. 2000).
Analisis komponen kimia pada isolat selulosa dari bagas tebu adalah salah satu indikator keberhasilan tahap isolasi. Evaluasi keberhasilan isolasi ditandai
dengan meningkatnya kandungan α-selulosa, dan adanya penurunan terhadap kandungan lignin dan hemiselulosa secara signifikan. Hasil isolasi dapat dilihat pada Tabel 2.
Tabel 2 Analisis komponen kimia (%)
Kandungan Bagas Tebu Isolat Selulosa Purwaningsih (2012) Sun (2004) et al.
Air 8.05 4.15
Hemiselulosa 23.72 5.38
α-selulosa 46.68 88.37 77.47 92.8
Lignin 22.59 0.19 0.96 3.86
Keberhasilan tahap delignifikasi pada proses isolasi selulosa dievaluasi berdasarkan penurunan kandungan lignin pada isolat selulosa dari 22.59% menjadi 0.19%. Hal ini disebabkan lignin yang terdapat dalam sampel telah hilang saat proses delignifikasi, sehingga menaikkan kadar α-selulosa sebesar 88%.
Selain itu, keberhasilan tahap ini juga dapat dipantau dari hasil spektroskopi inframerah ditunjukkan pada Gambar 2. Spektrum FTIR bahan baku bagas tebu menunjukkan adanya serapan pada 1508 cm-1mengindentifikasi vibrasi karboksil lignin dan cincin lignin dan serapan untuk vibrasi gugus asetil ester pada bilangan gelombang 1705 cm-1, hal ini didukung dengan tingginya kandungan lignin sebesar 22.59% (Liu et al. 2006). Setelah perlakuan alkali pada bagas tebu,
serapan khas untuk senyawa lignin semakin berkurang dan semakin besar pita pada bilangan gelombang pada 1103-1033 cm-1 yang menunjukkan gugus C-O-C yang terdapat pada cincin piranosa selulosa dan munculnya serapan khas untuk selulosa pada 898 cm-1 yang cukup tajam. Serapan ini menandakan telah
7 serapan pada bilangan gelombang 1425-1317 cm-1 menunjukkan vibrasi tekuk
gugus C-H2 dan serapan 2885 cm-1 mengidentifikasi vibrasi ulur gugus C-H (Khan et al. 2012), vibrasi gugus O-H ulur berada pada serapan 3300 cm-1 dan pada
bilangan gelombang 1201 cm-1 diprediksikan vibrasi gugus O-H tekuk pada
bidang selulosa, serapan 1161 cm-1 menunjukkan vibrasi ulur gugus C-O (Sun et al. 2004).
4000 3500 3000 2500 2000 1500 1000 500
Tr
Gambar 2 Spektrum FTIR (a)bagas tebu dan (b) isolat selulosa
Selulosa Terhidrolisisdari Isolat Selulosa
Morfologi Permukaan
Hasil isolat selulosa telah dihidrolisis menggunakan H2SO4 dengan
beberapa variasi konsentrasi, sehingga dapat memutuskan ikatan eter pada rantai selulosa. Mekanisme yang dapat dijelaskan pada proses hidrolisis dengan protonasi dari asam menyerang gugus eter pada selulosa, sehingga memutuskan rantai molekul menjadi bagian kecil selulosa. Gambar 3 menjelaskan skema reaksi pemutusan ikatan eter pada selulosa.
Hidrolisis selulosa dilakukan pada suhu 45 °C selama 40 menit. Penambahan selulosa dilakukan sedikit demi sedikit kedalam larutan H2SO4, hal
ini menyebabkan tidak homogen atau seragam ukuran serat yang terbentuk dalam satu perlakuan. Produk selulosa whiskers yang dihasilkan dari penambahan serbuk
8
Gambar 3 Skema reaksi pemutusan ikatan eter pada selulosa dengan asam Perlakuan hidrolisis dengan konsentrasi asam rendah tidak mengubah morfologi serat selulosa, hal ini menandakan bahwa penggunaan konsentrasi asam rendah (4, 6, dan 8 M) pada isolat selulosa tidak mampu memutuskan rantai selulosa hingga berukuran nano (Lampiran 4). Penggunaan konsentrasi asam yang terlalu pekat (12 M) memutuskan seluruh rantai karbon pada selulosa sehingga meninggalkan residu karbon berwarna hitam (Lampiran 5).
Pengukuran morfologi suspensi selulosa terhidrolisis menggunakan mikroskop biasa. Selulosa terhidrolisisyang dihasilkan dengan konsentrasi H2SO4
10 M tidak terlihat pada mikroskop biasa, sehingga menggunakan SEM. Morfologi serat selulosa terhidrolisis dengan konsentrasi H2SO4 10 M
menunjukkan sebagian serat telah berukuran nanometer (lingkar kuning), disebabkan konsentrasi H2SO4 10 M mampu memotong bagian amorfus pada
selulosa. Pada hakikatnya penggunaan konsentrasi H2SO4 10 M belum sempurna
memutuskan rantai selulosa hingga berukuran nano, sehingga masih ada serat yang berukuran panjang mencapai ± 9 µm. Gambar morfologi serat selulosa terhidrolisis H2SO4 10 M disajikan pada Gambar 4. Perbandingan ukuran panjang
dan diameter serat yang diperoleh dengan acuan penelitian yang lain menggunakan bahan baku berbeda ditunjukkan pada Tabel 3.
9
Gambar 4 Morfologi selulosa whisker
Tabel 4 menjelaskan bahwa semakin besar konsentrasi asam yang digunakan maka semakin kecil ukuran serat selulosa. Hasil yang diperoleh peneliti menunjukkan bahwa hidrolisis menggunakan konsentrasi H2SO4 10 M dapat
menghilangkan bagian amorfus pada serat selulosa sehingga bentuk yang diperoleh layak disebut sebagai whiskers. Akan tetapi diameter selulosa
terhidrolisis masih lebih besar dari standar. Standar ukuran whiskers adalah
panjang berkisar 100-600 nm dan diameter 2-20 nm (Siro & Plackett 2010). Ukuran selulosa whiskers berbeda dengan nanoserat selulosa yang memiliki
panjang >1000 dan diameter 10-40 nm.
Tabel 4 Ukuran panjang dan diameter serat selulosa whiskers
Konsentrasi H2SO4 Panjang Diameter
4 Ma > 100 µm > 20 µm
6 Ma 45-200 µm 5-18 µm
8 Ma 30-80 µm 4-10 µm
10 Mb 0.1-10 µm 10-200 nm
a pengukuran dengan mikroskop biasa/konvensional b pengukuran dengan SEM
Kristalinitas
Selulosa terdiri atas dua bagian yaitu amorfus dan kristal. Bagian amorfus akan lebih mudah dihidrolisis, menyisakan bagian kristal. Proses kimia dimulai dengan penghilangan ikatan antar polisakarida pada permukaan serat selulosa diikuti dengan pecah dan rusaknya bagian amorfus sehingga melepaskan bagian kristal selulosa (Habibi et al. 2010). Penentuan derajat kristalinitas dilakukan
10
kristal dalam suatu material dengann membandingkan luasan kurva kristal dengan total luasan amorfus dan kristal (Purnama 2006). Derajat kristalinitas dapat dihitung dengan metode Segal et al. (1959), yaitu
% kristalinitas = Ikristalin
Ikristalin Iamorfus
× 100
Evaluasi keberhasilan hidrolisis selulosa whiskers dapat dilihat dari pola
difraksi sinar-X pada Gambar 5. Difraktogram selulosa whiskers memperlihatkan
dua puncak utama pada 2θ =12.2°, d = 7.15 Ǻ dengan hkl = 100, dan 2θ = 22.04°, d = 4.427 diperoleh struktur kristal dengan hkl = 020. Menurut Klemm et al.
(2005) karakteristik selulosa memperlihatkan dua puncak utama, yaitu 2θ = 12.5°, dan 2θ =22.5°. Derajat kristalinitas selulosa whiskers yang diperoleh pada
penelitian ini sebesar 86.7% meningkat 15% dari kristalinitas isolat selulosa bagas tebu. Hal ini serupa dengan penelitian yang telah dilakukan Teixeira et al. (2011)
menggunakan bahan baku berupa bagas tebu, difraktogram selulosa whiskers
menunjukkan dua puncak pada 2θ =12.3° dan 2θ = 22.6°, dengan derajat
kristalinitas 87.5%.
Perubahan pada intensitas puncak difraksi menunjukkan terjadi perubahan struktur kristal atau keteraturan rantai molekul selulosa. Bagian kristal meningkat dengan menurunnya puncak pada bagian amorfus sehingga perubahan struktur kristal dari isolat selulosa membentuk kristal baru. Pada kasus difraktogram selulosa whiskers menunjukkan puncak doublet pada intensitas puncak utama
hampir pada intensitas yang sama (I22.04/I19.95~0.99). Hasil serupa juga dilaporkan
oleh Mandal dan Chakrabarty (2011) yang menggunakan isolat selulosa bagas tebu sebagai bahan baku pembuatan nanoselulosa menghasilkan tingkat intensitas mendekati 0.93.
11
Kurva TGA
Thermogravimetric Analysis (TGA) merupakan teknik analisis untuk
menentukan stabilitas termal suatu material dan fraksi komponen volatil dengan menghitung perubahan berat yang dihubungkan dengan perubahan suhu.
Gambar 6 menunjukkan kurva TGA isolat selulosa bagas tebu dan selulosa
whiskers. Isolat selulosa mengalami penurunan bobot tahap awal pada suhu
27-305 °C sebanyak 10% sesuai dengan suhu dekomposisi residu hemiselulosa, tahap kedua menurun dratis hingga suhu 374 °C menunjukkan suhu depolimerisasi selulosa, dan kehilangan massa sebesar 80%. Tahap terakhir massa berkurang 6% hingga suhu 500 °C diduga kerusakan lebih lanjut dari selulosa membentuk residu karbon. Isolat selulosa terdegradasi pada suhu 344 °C. Suhu degradasi ini tidak jauh berbeda dengan hasil penelitian yang telah dilaporkan, yaitu 340 °C (Liu et al.
2006), 343 °C (Mandal & Chakrabarty 2011), 270 °C (Teixeira et al. 2011).
Pada tahap ini, degradasi termal pada selulosa whiskers berjalan lebih
rendah dari suhu isolat selulosa, diduga adanya gugus sulfat dapat mengurangi stabilitas termal pada kristal selulosa (Roman & Winter 2004). Suhu degradasi selulosa whiskers mulai pada suhu 200.4 °C dan maksimum 324.6 °C. Suhu
degradasi pada penelitian lain yang menggunakan bagas tebu sebagai baku menunjukkan bahwa nanoselulosa mulai terdegradasi pada suhu 249 °C dan 345 °C menandakan telah rusaknya struktus kristal (Mandal & Chakrabarty 2011).
Gambar 6 Kurva TGA (―) Isolat selulosa dan (---) selulosa whiskers
Sifat Mekanik Film Komposit
Kekuatan tarik adalah gaya tarik atau tarikan maksimum yang dapat dicapai sampai film dapat tetap bertahan sebelum putus. Pengukuran kuat tarik dilakukan untuk mengetahui besarnya gaya yang diperoleh untuk mencapai tarikan maksimum pada setiap satuan luas area film untuk meregang dan memanjang.
0 100 200 300 400 500
12
Panjang putus atau proses perpanjangan merupakan perubahan panjang maksimum pada saat terjadi peregangan hingga sampel film terputus.
Selulosa whiskers memiliki kristalilnitas yang tinggi. Banyaknya jumlah
konsentrasi selulosa whiskers yang ditambahkan dalam pembuatan film, dapat
mengakibatkan film menjadi regas sehingga menurunkan nilai kuat tarik yang diberikan (Jalaluddin et al. 2011). Hal serupa dapat dilihat pada Tabel 5 yang
menunjukkan pengaruh penambahan konsentrasi selulosa whiskers dalam PVA
20%. Kemudian, kemampuan film untuk meregang semakin meningkat dengan penambahan konsentrasi selulosa whisker. Cheng et al. (2009) menggunakan
PVA 10% dan 1% suspensi berbagai jenis serat selulosa diantaranya, serat selulosa murni dan mikrokristalin selulosa. Hasil yang diperoleh bahwa film yang dibuat dengan menggunakan mikrokristalin mampu menaikkan kuat tarik sebesar 110 MPa dari PVA murni 95 MPa.
Tabel 5 Pengaruh variasi konsentrasi selulosa whiskers dalam PVA 20%
Sampel Perpanjangan (%) Kuat tarik (MPa)
PVA 99.89 7.87
PVA + SW 7.5% 126.21 6.21
PVA + SW 15% 137.40 5.38
Oleh karena rendahnya kuat tarik yang diberikan dengan penambahan selulosa whiskers, dilakukan penambahan pengisi dalam film. Secara umum
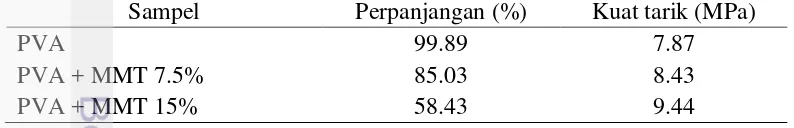
kegunaan montmorilonit sebagai barrier oksiden dan air serta meningkatkan stabilitas panas film komposit. Untuk melihat efek penambahan montmorilonit secara mekanik dilakukan uji kuat tarik dan daya regang film. Tabel 6 menyajikan pengaruh penambahan montmorilonit terhadap PVA 20%. Hasil penelitian menunjukkan terjadinya peningkatan nilai kuat tarik yang signifikan seiring bertambahnya jumlah konsentrasi yang diberikan. Kemampuan film meregang semakin kecil seiring bertambahnya konsentrasi montmorilonit yang digunakan. Arjmandi et al. (2015) meneliti pengaruh montmorilonit dalam PLA. Hasil yang
diperoleh bahwa dengan konsentrasi montmorilonit 5% mampu meningkatkan kuat tarik, namun seiring bertambahnya konsentrasi montmorilonit yang ditambahkan dalam film kembali menurunkan nilai perpanjangan film.
Tabel 6 Pengaruh variasi konsentrasi montmorilonit terhadap PVA 20% Sampel Perpanjangan (%) Kuat tarik (MPa)
PVA 99.89 7.87
PVA + MMT 7.5% 85.03 8.43
PVA + MMT 15% 58.43 9.44
Penggunaan montmorilonit 7.5% mampu meningkatkan kuat tarik film seiring dengan meningkatnya konsentrasi selulosa whiskers yang ditambahkan
pada film dapat dilihat pada Tabel 7. Hal ini diduga selulosa whiskers mampu
13 selulosa nanofiber (SNF) 1.1%, dan variasi penambahan konsentrasi mineral liat monmorilonit (MMT). Hasil yang diperoleh dari penelitian tersebut bahwa banyaknya jumlah konsentrasi montmorilonit yang ditambahkan dalam film komposit mampu meningkatkan kuat tarik, namun menurunkan daya regang film.
Film komposit yang memiliki kuat tarik dan daya regang yang bagus adalah pada komposisi 7.5% montmorilonit dan 15% selulosa whiskers. Kuat tarik yang
dihasilkan dari penelitian ini masih rendah dibandingkan penelitian yang telah dilaporkan. Perbedaan komposisi dan konsentrasi bahan-bahan yang digunakan dalam pembentukan film komposit serta metode yang digunakan diduga sebagai salah satu penyebab rendahnya kuat tarik yang dihasilkan.
Tabel 7 Pengaruh konsentrasi selulosa whiskers pada film komposit dengan
montmorilonit 1.5%
Sampel Perpanjangan (%) Kuat tarik (MPa)
PVA + MMT 7.5% 85.03 8.43
PVA + MMT 7.5% + SW 7.5% 69.39 16.25
PVA + MMT 7.5% + SW 15% 93.02 17.51
Morfologi Film Komposit
Permukaan film komposit yang telah dibuat dapat dilihat morfologi permukaan dengan menggunakan SEM. Hasil analisis morfologi permukaan komposit PVA-MMT-SW. ditunjukkan pada Gambar 7. Pada Gambar 7a dilihat dari samping permukaan film, panah merah menunjukkan adanya selulosa
whiskers dan 7b permukaan film dari atas. Montmorilonit dengan konsentrasi
selulosa whiskers yang lebih banyak akan membentuk interaksi antara matriks
dalam film komposit (Arjmandi et al. 2015).
Montmorilonit merupakan mineral liat yang memiliki interaksi-interaksi intermolekul sehingga sangat mudah teraglomerasi. Adanya selulosa whiskers
yang tersebar dalam permukaan film dapat menjadi pembatas montmorilonit tidak teraglomerasi lebih besar, sehingga dapat tersebar secara merata. Hal ini terbukti dari pengukuran kuat tarik saat PVA-MMT tanpa selulosa whiskers, nilai kuat
tariknya lebih kecil daripada dengan adanya selulosa whiskers. Penambahan
14
(a) (b)
Gambar 7 Morfologi film PVA-MMT-SW (a) samping dan (b) permukaan film
Kristalinitas Film Komposit
Kristalinitas pada film komposit ini dipengaruhi penambahan selulosa
whiskers. Kristalinitas film dapat dilihat pada pola difraktogram yang tersedia
pada Gambar 8 menunjukkan selulosa whiskers membuat film memiliki puncak
kritalinitas pada 2θ = 19.08° dengan d-spacing (d) = 4.65 Å diperoleh bentuk
kristal dengan hkl = 220. Jika dibandingkan dengan pola difraksi film dengan hanya PVA-MMT. Informasi pendukung untuk puncak kristalinitas dari
montmorilonit berada pada 2θ = 7.64° (Spoljaric et al. 2014).
Fasa kristalin pada selulosa whiskers memberikan kekuatan, kekakuan dan
kekerasan. Disisi lain fasa kristalin juga dapat menyebabkan polimer komposit menjadi lebih regas. Penggunaan PVA berguna untuk mengurangi kekakuan pada film komposit, sehingga adanya pergeseran puncak pada difraktogram film PVA-MMT-SW. Tingginya puncak pada kurva film komposit PVA-MMT-SW menandakan besarnya kristalinitas. Oleh karena itu film ini memiliki daya tahan panas yang baik. Hal ini didukung dengan hasil analisis pengukuran daya termal film.
5 10 15 20 25 30
In
te
n
si
ta
s
2derajat)
a b
15
Kurva TG/DTA Film Komposit
Analisis termal dilakukan untuk mengetahui intensitas tahanan termal sampai pada suhu berapa panas berpengaruh terhadap bahan film komposit. Sifat termal dilakukan karena memiliki peran yang penting untuk menentukan sifat mekanik bahan yang digunakan dalam film komposit pada sistem kemasan. Suatu film komposit layak disebut tahan panas atau stabil terhadap panas, harus tidak terurai di bawah suhu 400 °C dan dapat mempertahankan sifat-sifatnya yang bermanfaat pada suhu terdekat dengan suhu dekomposisi. Stabilitas panas merupakan fungsi dari energi ikatan. Ketika suhu meningkat ke titik yang membuat energi getaran menimbulkan putusnya ikatan, maka film komposit akan terurai (Feng et al. 2001)
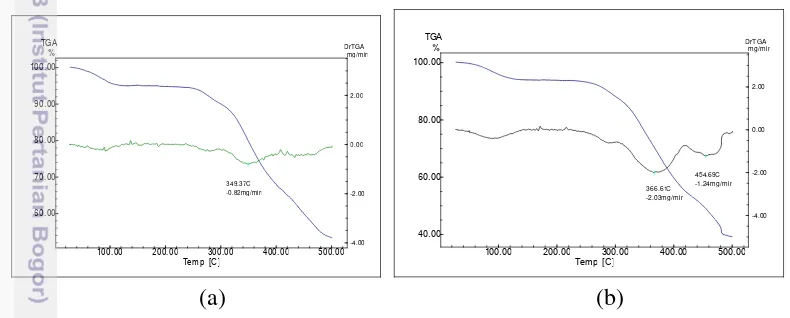
Film PVA-MMT mulai terdekomposisi pada suhu 349 °C disajikan pada Gambar 9a. Gambar 9b menunjukkan film PVA-MMT-SW akan mulai terdekomposisi pada suhu 366.6 °C dan terdekomposisi maksimal pada suhu 454.7 °C. Hal ini menunjukkan selulosa whiskers mampu meningkatkan suhu
dekomposisi dan montmorilonit mampu menjaga stabilitas termal pada film komposit.
Gambar 9 Kurva TG/DTG film komposit (a) PVA-MMT dan (b) PVA-MMT-SW
4
SIMPULAN DAN SARAN
Simpulan
Selulosa dari bagas tebu telah berhasil diisolasi dengan perlakuan alkali dan pemucat peroksida. Kadar α-selulosa pada isolat sebesar 88% dan sisa kadar lignin sebesar 0.19%. Hasil hidrolisis selulosa menggunakan H2SO4 10 M
memiliki bentuk whiskers dengan ukuran panjang 0.1-10 µm dan diameter 10-100
nm. Film komposit mampu diperkuat oleh selulosa whiskers dibuktikan dengan
16
selanjutnya meningkatnya daya tahan film terhadap panas sebesar 366 °C, dibandingkan dengan film tanpa selulosa whiskers sebesar 349 °C.
Saran
Saran yang diberikan pada penelitian selanjutnya, yaitu pembuatan selulosa
whiskers dilakukan dengan konsentrasi H2SO4 11 M atau 11.5 M, dan optimasi
waktu pengadukan serta suhu yang digunakan. Dalam proses pembuatan film komposit, perlu ditambahkan perbandingan antara selulosa whiskers dengan
montmorilonit lebih banyak, sehingga lebih mudah memastikan pengaruh yang diberikan. Film komposit untuk kemasan perlu di lakukan uji permeabilitas uap air.
DAFTAR PUSTAKA
Aguilar R, Ramized J, Garrote G, Vazquez M. 2002. Kinetic study of acid hydrolysis of sugarcane bagasse. Journal Food Engineer. 55:309-318
Arjmandi R, Hassan A, Eichhorn SJ, Haafiz MKM, Zakaria Z, Tanjung FA. 2015. Enhanced ductility and tensile properties of hybrid montmorillonite/cellulose nanowhiskers reinforced polylactic acid nanocomposites. Journal of Materials Science 50:3118–3130.
Doi:10.1007/s10853-015-8873-8
Azeredo HMC. 2009. Review: Nanocomposites for food packaging applications.
Food Research International 42:1240–1253.
Doi:10.1016/j.foodres.2009.03.019
Cheng Q, Wang S, Rials TG. 2009. Poly(vinyl alcohol) nanocomposites reinforced with cellulose fibril isolated by high intensity ultrasonication.
Composites: Part A 40:218-224. Doi:10.1016/j.compositesa.2008.11.009
Dash R, Foston M, Ragauskas AJ. 2013. Improving the mechanical and thermal properties of gelatin hydrogels cross-linked by cellulose whiskers.
Carbohydrate Polymers 91:638– 645. Doi: 10.1016/j.carbpol.2012.08.080
Eichhorn SJ, Dufresne A, Aranguren M, Marcovich NE, Capadona JR, Rowan SJ, Weder C, Thielemans W, Roman M, Renneckar S et al. 2010. Review:
current international research into cellulose nanofibres and nanocomposites.
Journal of Materials Science 45:1–33. Doi:10.1007/s10853-009-3874-0
Feng D, Caulfield DF, Sanadi AR. 2001. Effect of compatibilizer on the structure property relationships of kenaf-fiber/polypropylene composites. Polymer Composites 22(4):506-517. Doi:10.1002/pc.10555
Folarin, O.M., Sadiku E.R., and Mayti, A. 2011. Polymer-noble metal nanocomposites: Review. International Journal of the Physical Sciences.
6(21) : 4869-4882
Habibi Y, Lucia LA, Rojas OJ. 2010. Cellulose Nanocrystals: Chemistry, Self-Assembly, and Applications. Chemical review 6:3479-3500.
17
Jalaluddin A, Araki J, Gotoh Y. 2011. Toward “strong” green nanocomposites:
polyvinyl alcohol reinforced with extremely oriented cellulose whiskers.
Biomacromolecules 12:617–624. Doi:10.1021/bm101280f .
Kanmani, P and Rhim J.W. 2014. Physicochemical properties of gelatin/silver nanoparticle antimicrobial composite films. Food Chemistry. 148:162-169
Kargarzadeh H, Sheltami RM, Ahmad I, Abdullah I, Dufresne A. 2014. Cellulose nanocrystal: A promising toughening agent for unsaturated polyester nanocomposite. Polymer. Doi:10.1016/j.polymer.2014.11.054
Khan A, Khan RA, Salmieri S, Tien CL, Riedl B, Bouchard J, Chauve G, Tan V, Kamal MR, Lacroix M. 2012. Mechanical and barrier properties of nanocrystalline cellulose reinforced chitosan based nanocomposite films.
Carbohydrate Polymers 90:1601– 1608. Doi:10.1016/j.carbpol.2012.07.037
Klemm D, Heublein B, Fink HP, Bohn A. 2005. Cellulose: Fascinating biopolymer and sustainable raw material. Polymer Science 44:3358-3393
Doi: 10.1002/anie.200460587
Kvien I dan Oksman K. 2007. Orientation of cellulose nanowhiskers in polyvinyl alcohol. Applied Physics A: Materials Science and Processing 87:641-643.
Doi: 10.1007/s00339-007-3882-3
Laopaiboon P, Thani A, Leelavatcharamas V, Laopaiboon L. 2010. Acid hydrolysis of sugarcane bagasse for lactic acid production. Bioresource Technology 101(3):1036-1043. Doi:10.1016/j.biortech.2009.08.091
Li R, Fei J, Cai Y, Li Y, Feng J, Yao J. 2009. Cellulose whiskers extracted from mulberry: A novel biomass production. Carbohidrate polymers 76:94-99.
Doi:10.1016/j.polymer.2007.03.062
Liu CF, Ren JL, Xu F, Liu JJ, Sun JX, Sun RC. 2006. Isolation and characterization of cellulose obtain from ultrasonic irradiated sugarcane bagasse. Journal of Agriculture Food Chemistry 54(16):5742-8.
Mandal A dan Chakrabarty D. 2011. Isolation of nanocellulose from waste sugarcane bagasse (SCB) and its characterization. Carbohydrate Polymers.
86:1291– 1299. Doi:10.1016/j.carbpol.2011.06.030
Martin MA, Teixera EM, Correa AC, Ferreira M, Mattoso LHc. 2011. Characterization of cellulose whisker from commercial cotton fiber. Journal of Materials Science 46: 7858 – 7864. Doi: 10.1007/s10853-011-5767-2
Paul DR dan Robeson LM. 2008. Polymer nanotechnology: Nanocomposites.
Polymer, 49:3187–3204.
Peresin MS, Vesterinen AH, Habibi Y, Johansson LS, Pawlak JJ,Nevzorov AA, Rojas OJ. 2014. Crosslinked pva nanofibers reinforced with cellulose nanocrystals: water interactions and thermomechanical properties. Applied Polymer Science 1-12.DOI: 10.1002/APP.40334
Purnama EF. 2006. Pengaruh suhu reaksi terhadap derajat kristalinitas dan komposisi hidroksiapatit dibuat dengan media air dan cairan tubuh buatan (synthetic body fluid) [Skripsi]. Bogor (ID): Institut Pertanian Bogor
Purwaningsih H. 2012. Rekayasa biopolimer dari limbah pertanian berbasis selulosa dan aplikasinya sebagai material separator [disertasi]. Bogor (ID): Institut Pertanian Bogor
18
behavior. Carbohydrate Polymers 81:83-92. Doi:
10.1016/j.carbpol.2010.01.059
Ranby BG. 1952. The Mercerization of Cellulose: II. A phase transition study with X-ray diffraction. Acta Chemical Scandinavica 119-127.
Roman M dan Winter WT. 2004. Effect of sulfate groups from sulfuric acid hydrolysis on the thermal degradation behavior of bacterial cellulose.
Biomacromolecules 5:1671-1677. Doi:10.1021/bm034519
Rosli NA, Ahmad I, Aggbdullah I, 2013. Isolation and characterization of cellulose nanocrystals from agave angustifolia fibre. BioResources 8(2):
1893-1908.
Rowell RM. 2005. Handbook of wood chemistry and wood composites. Florida: CRC Pr
Samir MAS, Alloin F, Dufresne A. 2005. Review of recent research into celluloic
whiskers, their properties and their application in nanocomposite field. Biomacromolecules 6:612-626. Doi:10.1021/bm0493685
Samsuri M, Gozan M, Mardias R, Baiquni M, Hermansyah H, Wijanarko A, prasetya B, Nasikin M. 2007. Pemanfaatan selulosa bagas untuk produksi etanol melalui sakarifikasi dan fermentasi serentak dengan enzim xylase.
Makara Teknologi 11:17-24
Segal L, Creely JJ, Martin AE, Conrad CM. 1959. An empirical method for estimating the degree of crystallinity of native cellulose using the x-ray diffractometer. Textile Research Journal 29 (10):786-794.
Doi:10.1177/004051755902901003
Siro I, Plackett D. 2010. Microfibrillated cellulose and new nanocomposite materials: a review. Springer science 17:459-494.
Doi:10.1007/s10570-010-9405-y
Spoljaric S, Salminen A, Luong ND, Lathinen P, Vartiainen J, Tammelin T, Seppala J. 2014. Nanofibrillated cellulose, poly(vinyl alcohol), montmorillonite clay hybrid nanocomposites with superior barrier and thermomechanical properties. Polymer Composites. Doi: 10.1002/pc.2259
Sun JX, Sun XF, Zhao H, Sun RC. 2004. Isolation and characterization of cellulose from sugarcane bagasse. Polymers Degradation and Stability
84:331-339. Doi:10.1016/j.polymdegradstab.2004.02.008
Sun RC, Tomkinson J, MaPL, Liang SF. 2000. Comparative study of hemicelluloses from rice straw by alkali and hydrogen peroxide treatment.
Carbohydrate polymers 42:111-122.
Tang X dan Alavi S. 2011. Recent advances in starch, polyvinyl alcohol based polymer blends, nanocomposites and their biodegradability. Carbohydrate polymers 85: 7-16. Doi:10.1016/j.carbopol.2011.01.030
Teixeira EM, Bondancia TJ, Teodoro KBR, Correa AC, Marconcini JM, Mattoso LHC. 2011. Sugarcane bagasse whiskers: extraction and characterizations.
Industrial Crops and Products 33:63–66. Doi:10.1016/j.indcrop.2010.08.009
Wang N, Ding E, Rongshi C. 2007. Thermal degradation behaviors of spherical cellulose nanocrystals with sulfate groups. Polymers 48:3486-3493.
Doi:10.1016/j.polymer.2007.03.062
19 Zaini LH, Jonoobi M, Tahir PMd, Karimi S. 2013. Isolation and characterization of cellulose whiskers from kenaf (Hibiscus cannabinus L) bast fibers.
20
21 Lampiran 1 Diagram Alir Penelitian
Bagas tebu
Isolat selulosa
bagas tebu Pencirian dengan FTIR Delignifikasi
dan pemucatan
Hidrolisis selulosa dengan berbagai varian H2SO4
Selulosa
Whiskers (SW)
Pencirian dengan SEM, XRD dan DTA
Aplikasi sebagai penguat dalam film komposit berbasis PVA/MMT
Film Komposit
22
Lampiran 2 Spektrum FTIR Bagas Tebu dan Isolat Selulosa
a. Spektrum FTIR Bagas Tebu
24
Lampiran 4 Morfologi serat selulosa
a. H2SO4 4 M
b. H2SO4 6 M
25 Lampiran 5 Proses hidrolisis selulosa menggunakan varian konsentrasi H2SO4
(a) H2SO4 4 M (b) H2SO4 6 M (c) H2SO4 8 M
26
27 Lampiran 7 Kurva TG/DTG Film Komposit
a. Kurva TG/DTG film PVA-MMT
100.00 200.00 300.00 400.00 500.00
b. Kurva TG/DTG film PVA-MMT-SW
28
Lampiran 8 Ketebalan Film
Ulangan A B C D E F G H I
I 0.067 0.064 0.051 0.028 0.068 0.03 0.052 0.065 0.038
II 0.044 0.06 0.068 0.037 0.036 0.04 0.048 0.08 0.034
III 0.048 0.055 0.065 0.037 0.064 0.035 0.045 0.078 0.034
IV 0.038 0.035 0.029 0.025 0.041 0.033 0.048 0.068 0.028
V 0.038 0.046 0.039 0.038 0.003 0.041 0.055 0.077 0.068
29 Lampiran 10 Analisis kuat tarik
Kode
Sampel Ulangan Load Max (kgf) A (cm^2) thickness (mm) σ (Mpa) Rerata
30
I
1 1.2507 0.0076 0.038 16.12744737
13.40549
2 0.8101 0.0068 0.034 11.67497059
3 1.03576 0.0068 0.034 14.92712941
4 0.90249 0.0056 0.028 15.793575
5 1.18019 0.0136 0.068 8.504310294
Perhitungan
σ = A = 0.87905 kgf
31 Lampiran 11 Analisis persen perpanjangan
32
I
1 100 173.01147 73.01147
71.3989
2 100 182.42659 82.42659
3 100 179.52828 79.52828
4 100 150.62904 50.62904
Perhitungan
Perpanjangan = Lakhir- Lawal
Lawal
=
1 5.9558 -100
100 = 0.459558
33
RIWAYAT HIDUP
Penulis dilahirkan di Aceh Besar pada tanggal 10 Januari 1989 dari pasangan Asnawi Hasan dan Nurmala M.Ali. Penulis merupakan anak pertama dari dua bersaudara dan istri dari Muhammad Ridho Afifi, M.Si