ANALISIS KANDUNGAN MINERAL ESENSIAL
PADA DAUN EKOR NAGA (Rhaphidophora pinnata
(L.f.) Schott) SECARA SPEKTROFOTOMETRI
SERAPAN ATOM
SKRIPSI
OLEH:
SYAFRIDAH
NIM 071501030
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
ANALISIS KANDUNGAN MINERAL ESENSIAL
PADA DAUN EKOR NAGA (Rhaphidophora pinnata
(L.f.) Schott) SECARA SPEKTROFOTOMETRI
SERAPAN ATOM
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk mencapai gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
SYAFRIDAH
NIM 071501030
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
ANALISIS KANDUNGAN MINERAL ESENSIAL
PADA DAUN EKOR NAGA (Rhaphidophora pinnata
(L.f.) Schott) SECARA SPEKTROFOTOMETRI
SERAPAN ATOM
OLEH:
SYAFRIDAH
NIM 071501030
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: Maret 2011
Disetujui Oleh:
Pembimbing I, Panitia Penguji,
Dra. Masfria, M.S., Apt. Drs. Muchlisyam, M.Si., Apt. NIP 195707231986012001 NIP 195006221980021001
Dra. Masfria, M.S., Apt. Pembimbing II, NIP 195707231986012001
Drs. Chairul Azhar Dalimunthe,M.Sc.,Apt. Dra. Aswita Hafni Lubis, M.Si., Apt. NIP 194907061980021001 NIP 195304031983032001
Dra. Sudarmi, M.Si., Apt. NIP 195409101983032001
Medan, Maret 2011
Fakultas Farmasi Universitas Sumatera Utara
Dekan,
KATA PENGANTAR
Puji syukur penulis panjatkan kehadirat Allah SWT yang telah
memberikan berkah, rahmat dan hidayah-Nya, sehingga penulis dapat
menyelesaikan penelitian dan penyusunan skripsi ini. Skripsi ini disusun untuk
melengkapi salah satu syarat mencapai gelar Sarjana Farmasi pada Fakultas
Farmasi Universitas Sumatera Utara, dengan judul: “Analisis Kandungan
Mineral Esensial pada Daun Ekor Naga (Rhaphidophora pinnata (L.f.)
Schott) Secara Spektrofotometri Serapan Atom”.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan
terima kasih yang sebesar-besarnya kepada:
1. Ibunda Siti Fatimah dan Ayahanda Syarifuddin yang telah memberikan cinta
kasih yang tidak ternilai dengan apapun, doa yang tulus serta pengorbanan baik
materi maupun non-materi, serta kakak-kakak tercinta, Siti Hajar, S.E. dan
dr. Siti Zuhroh yang selalu mendoakan dan memberikan semangat.
2. Ibu Dra. Masfria, M.S., Apt. dan Bapak Drs. Chairul Azhar Dalimunthe, M.Sc.,
Apt., atas waktu dan kesabarannya membimbing penulis selama penelitian
hingga selesainya skripsi ini.
3. Bapak Dekan, staf pengajar dan staf administrasi Fakultas Farmasi yang telah
mendidik penulis selama masa perkuliahan dan membantu kemudahan
administrasi.
4. Ibu Dra. Masria, M.Si., Apt., selaku penasehat akademik yang telah
memberikan bimbingan kepada penulis selama masa perkuliahan.
Penelitian Kelapa Sawit (PPKS) Medan dan Bang Hambali selaku Operator
Laboratorium Pusat Penelitian Kelapa Sawit (PPKS) Medan yang telah
memberikan fasilitas kepada penulis selama melaksanakan penelitian.
6. Sahabat-sahabat tersayang, Yuyun, Icha, Meiva, Damay, Ade, Ecy, serta
seluruh teman-teman Sains dan Teknologi Farmasi USU stambuk 2007 atas
bantuan, motivasi, inspirasi yang diberikan selama masa perkuliahan sampai
penulisan skripsi ini.
7. Seluruh staf dosen Laboratorium Kimia Farmasi Kualitatif Farmasi USU dan
Laboratorium Statistik Farmasi USU, rekan-rekan asisten Rio, Vintha,
Rachmad, Bang Aulia, Bang Yogi, Rima, Uti, Fia, Mayang, Dheo, Bang Surya,
yang telah membantu penulis selama penelitian hingga penyusunan skripsi ini.
8. Kakak dan abang senior Farmasi, adik-adik junior Farmasi, terutama Kak Yani,
Kak Syebi, Kak Andien, Bang Rico, serta seluruh pihak yang telah banyak
membantu hingga selesainya penulisan skripsi ini yang tidak dapat disebutkan
satu persatu.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih
jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis
menerima kritik dan saran demi kesempurnaan skripsi ini.
Akhirnya, penulis berharap semoga skripsi ini dapat bermanfaat bagi kita
semua.
Medan, Maret 2011
Penulis,
ANALISIS KANDUNGAN MINERAL ESENSIAL PADA DAUN EKOR NAGA (Rhaphidophora pinnata (L.f.) Schott) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Daun ekor naga (Rhaphidophora pinnata (L.f.) Schott) merupakan salah satu tanaman yang telah dikenal masyarakat sebagai tanaman obat. Diperoleh informasi bahwa, masyarakat yang mengkonsumsi air rebusan daun ekor naga memiliki efek polyuri (banyak buang air kecil). Kalium dan natrium berhubungan erat dengan efek ini. Tujuan penelitian ini adalah untuk mengetahui kadar kalium (K), natrium (Na), kalsium (Ca), besi (Fe) dan magnesium (Mg) pada daun ekor naga.
Penetapan kadar dilakukan dengan menggunakan spektrofotometer serapan atom nyala udara-asetilen. Analisis kuantitatif kalium (K), natrium (Na), kalsium (Ca), besi (Fe) dan magnesium (Mg) dilakukan pada panjang gelombang berturut-turut 769,9 nm, 589,6 nm, 422,7 nm, 248,3 nm dan 202,6 nm.
Hasil penelitian menunjukkan bahwa daun ekor naga mengandung kalium (K), natrium (Na), kalsium (Ca), besi (Fe) dan magnesium (Mg). Hasil penetapan kadar yang diperoleh untuk K adalah 847,9111 ± 3,3573 mg/100g, Na adalah 8,2117 ± 0,1442 mg/100g , Ca adalah 474,6638 ± 4,5448 mg/100g, Fe adalah 1,7975 ± 0,0357 mg/100g dan Mg adalah 69,5370 ± 4,0158 mg/100g. Uji validasi metode memberikan hasil akurasi, batas deteksi dan batas kuantitasi yang dapat diterima dengan persen perolehan kembali untuk K adalah 103,3123% dengan nilai LOD 0,0835 mcg/ml dan LOQ 0,2783 mcg/ml , Na 82,3034% dengan LOD 0,0452 mcg/ml dan LOQ 0,1501 mcg/ml, Ca 105,5125% dengan LOD 0,0052 mcg/ml dan LOQ 0,0173 mcg/ml, Fe 97% dengan LOD 0,1145 dan LOQ 0,3815 dan Mg 102,3854% dengan LOD 0,3705 mcg/ml dan LOQ 1,2351 mcg/ml.
Kata kunci : Mineral esensial, daun ekor naga (Rhaphidophora pinnata (L.f.)
Schott), kalium (K),knatrium (Na), kalsium (Ca), besi (Fe),
ANALYSIS OF ESSENTIAL MINERAL IN DAUN EKOR NAGA (Rhaphidophora pinnata (L.f.) Schott) WITH ATOMIC
ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Daun ekor naga (Rhaphidophora pinnata (L.f.) Schott) is one of plant that is known as herbal medicine. Obtained information that, drinking boiling water of daun ekor naga causes polyuri effect. Potassium and sodium have a closed related with this effect. The aim of this study is to determine the levels of potassium (K), sodium (Na), calcium (Ca), iron (Fe) and magnesium (Mg) in daun ekor naga.
The determination is conducted by using atomic absorption spectrophotometer with air-acetylene flame. Quantitative analysis of potassium (K), sodium (Na), calcium (Ca), iron (Fe) and magnesium (Mg) is performed at the 769,9 nm, 589,6 nm, 422,7 nm, 248,3 nm and 202,6 nm wave length.
The results showed that daun ekor naga (Rhaphidophora pinnata (L.f.) Schott) contain potassium (K), sodium (Na), calcium (Ca), iron (Fe) and magnesium (Mg). The results indicate that the average K content is 847,9111 ± 3,3573 mg/100g, Na is 8,2117 ± 0,1442 mg/100g , Ca is 474,6638 ± 4,5448 mg/100g, Fe is 1,7975 ± 0,0357 mg/100g and Mg is 69,5370 ± 4,0158 mg/100g. Method validity test exhibited accuracy, limit of detection (LOD), and limit of quantitation (LOQ) that can be accepted with percent recovery for K is 103,3123% with LOD is 0,0835 mcg/ml and LOQ is 0,2783 mcg/ml , Na is 82,3034% with LOD is 0,0452 mcg/ml and LOQ is 0,1501 mcg/ml, Ca is 105,5125% with LOD is 0,0052 mcg/ml and LOQ is 0,0173 mcg/ml, Fe is 97% with LOD is 0,1145 and LOQ is 0,3815 and Mg is 102,3854% with LOD is 0,3705 mcg/ml and LOQ is 1,2351 mcg/ml.
Keywords : Essential mineral, daun ekor naga (Rhaphidophora pinnata (L.f.)
DAFTAR ISI
Halaman
JUDUL…. ... i
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT... vi
DAFTAR ISI ... vii
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... x
DAFTAR LAMPIRAN ... xi
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Daun Ekor Naga ... 5
2.2 Mineral ... 6
2.3 Spektrofotometri SerapanAtom ... 9
2.4 Validasi Metode Analisis ...13
3.1 Tempat dan Waktu Penelitian ...17
3.2 Bahan-bahan ...17
3.2.1 Sampel ...17
3.2.2 Pereaksi ...17
3.3 Alat-alat ...17
3.4 Pembuatan Pereaksi ...18
3.4.1 Larutan HNO3 (1:1) ...18
3.4.2 Larutan HCl (1:1) ...18
3.4.3 Asam pikrat 1% b/v...18
3.4.4 Larutan H2SO4 1 N ...18
3.4.5 Larutan NH4SCN 1,5 N ...18
3.4.6 Larutan K4[Fe(CN)6] 2 N ...18
3.4.7 Kuning titan 0,1% b/v ...18
2.4.8 Larutan NaOH 2 N ...19
3.5 Prosedur Penelitian ...19
3.5.1 Pengambilan Sampel ...19
3.5.2 Identifikasi Tumbuhan ...19
3.5.3 Penyiapan Sampel ...19
3.5.4 Proses Destruksi...19
3.5.5 Pembuatan Larutan Sampel ...20
3.5.6 Pemeriksaan Kualitatif ...20
3.5.6.1 Kalium ...20
3.5.6.1.1 Uji Kristal Kalium dengan Asam Pikrat ...20
3.5.6.2.1 Uji Kristal Natrium dengan Asam Pikrat ...20
3.5.6.3 Kalsium ...21
3.5.6.3.1 Uji Kristal Kalsium dengan Asam Sulfat ...21
3.5.6.4 Besi ...21
3.5.6.4.1 Reaksi Kualitatif dengan Larutan K4[Fe(CN)6] 2 N ....21
3.5.6.4.2 Reaksi Kullitatif dengan Larutan NH4SCN 1,5 N ...21
3.5.6.5 Magnesium ...21
3.5.6.5.1 Reaksi Kualitatif dengan Larutan Titan 0,1% ...21
3.5.7 Pemeriksaan Kuantitatif ...21
3.5.7.1 Pembuatan Kurva Kalibrasi Logam Kalium ...21
3.5.7.2 Pembuatan Kurva Kalibrasi Logam Natrium ...22
3.5.7.3 Pembuatan Kurva Kalibrasi Logam Kalsium ...22
3.5.7.4 Pembuatan Kurva Kalibrasi Logam Besi ...23
3.5.7.5 Pembuatan Kurva Kalibrasi Logam Magnesium ...23
2.5.7.6 Penetapan Kadar Logam dalam Sampel...24
3.5.7.6.1 Penetapan Kadar Logam Kalium ...24
3.5.7.6.2 Penetapan Kadar Logam Natrium ...24
3.5.7.6.3 Penetapan Kadar Logam Kalsium ...24
3.5.7.6.4 Penetapan Kadar Logam Besi ...25
3.5.7.6.5 Penetapan Kadar Logam Magnesium ...25
3.5.8 Penentuan Batas Deteksi (Limit of Detection) dan Kuantitasi (Limit of Quantitation) ...25
3.5.9 Uji Perolehan Kembali (Recovery) ...26
3.5.11 Simpangan Baku Relatif ...28
BAB IV HASIL DAN PEMBAHASAN ...29
4.1 Hasil Identifikasi Tumbuhan ...29
4.2 Analisis Kualitatif ...29
4.3 Analisis Kuantitatif ...30
4.3.1 Kurva Kalibrasi Logam Kalium, Natrium, Kalsium, Besi dan Magnesium ...30
4.3.2 Analisis Kadar Logam Kalibrasi Logam Kalium, Natrium, Kalsium, Besi dan Magnesium dalam Daun Ekor Naga ....33
4.3.3 Batas Deteksi dan Batas Kuantitasi ...34
4.3.4 Uji Perolehan Kembali (Recovery) ...35
4.3.5 Simpangan Baku Relatif ...36
BAB V KESIMPULAN DAN SARAN ...37
5.1 Kesimpulan.. ...37
5.2 Saran……… ...37
DAFTAR PUSTAKA… ...38
DAFTAR TABEL
Halaman
Tabel 1. Hasil Analisis Kualitatif... 17
Tabel 2. Kadar Logam Kalium, Natrium, Kalsium, Besi dan Magnesium ... 22
Tabel 3. Persen Uji Perolehan Kembali (recovery) Kalium, Natrium,
DAFTAR GAMBAR
Halaman
Gambar 1. Kurva Kalibrasi Logam Kalium ... 19
Gambar 2. Kurva Kalibrasi Logam Natrium... 19
Gambar 3. Kurva Kalibrasi Logam Kalsium ... 20
Gambar 4. Kurva Kalibrasi Logam Besi ... 20
Gambar 5. Kurva Kalibrasi Logam Magnesium ... 21
Gambar 6. Gambar Tanaman Daun Ekor Naga (Rhaphidophora pinnata (L.f.) Schott.) ... 28
Gambar 7. Daun Ekor Naga (Rhaphidophora pinnata (L.f.) Schott.)... 28
Gambar 8. Gambar Kristal Kalium pikrat dan Natrium pikrat (Perbesaran 10x10) ... 32
Gambar 9. Gambar Kristal Kalsium Sulfat (Perbesaran 10x10)... 32
Gambar 10. Hasil Analisis Kualitatif dengan Kalium heksasianoferat (II) 2 N ... 33
Gambar 11. Hasil Analisis Kualitatif dengan Amonium tiosianat 1,5 N ... 33
Gambar 12. Hasil Analisis Kualitatif dengan Kuning Titan 0,1% ... 34
Gambar 13. Alat Spektrofotometer Serapan Atom... 70
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Gambar Tanaman Daun Ekor Naga (Rhaphidophora
pinnata (L.f.) Schott.)...40
Lampiran 2. Hasil Identifikasi/ Determinasi Tumbuhan ...41
Lampiran 3. Bagan Alir Proses Destruksi Kering ...42
Lampiran 4. Bagan Alir Pembuatan Larutan Sampel ...43
Lampiran 5. Hasil Analisis Kualitatif Logam Kalium, Natrium, Kalsium, Besi dan Magnesium ...44
Lampiran 6. Data Kalibrasi Kalium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r). ...47
Lampiran 7. Data Kalibrasi Natrium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r). ...48
Lampiran 8. Data Kalibrasi Kalsium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r). ...49
Lampiran 9. Data Kalibrasi Besi dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r). ...50
Lampiran 10. Data Kalibrasi Magnesium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r). ...51
Lampiran 11. Hasil Analisis Kadar Logam Kalium, Natrium, Kalsium, Besi dan Magnesium dalam Sampel ...52
Lampiran 12. Contoh Perhitungan Kadar Logam Kalium, Natrium, Kalsium, Besi dan Magnesium dalam Sampel ...54
Lampiran 13. Perhitungan Statistik Kadar Logam Kalium, Natrium, Kalsium, Besi dan Magnesium dalam Sampel ...57
Lampiran 15. Hasil Uji Perolehan Kembali Logam Kalium, Natrium,
Kalsium, Besi dan Magnesium Setelah Penambahan
Masing-masing Larutan Standar. ...77
Lampiran 16. Perhitungan Uji Perolehan Kembali Logam Kalium, Natrium, Kalsium, Besi dan Magnesium dalam Sampel ...79
Lampiran 17. Alat Spektrofotometer Serapan Atom ...82
Lampiran 18. Alat Tanur ...83
Lampiran 19. Tabel Distribusi t ...84
ANALISIS KANDUNGAN MINERAL ESENSIAL PADA DAUN EKOR NAGA (Rhaphidophora pinnata (L.f.) Schott) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Daun ekor naga (Rhaphidophora pinnata (L.f.) Schott) merupakan salah satu tanaman yang telah dikenal masyarakat sebagai tanaman obat. Diperoleh informasi bahwa, masyarakat yang mengkonsumsi air rebusan daun ekor naga memiliki efek polyuri (banyak buang air kecil). Kalium dan natrium berhubungan erat dengan efek ini. Tujuan penelitian ini adalah untuk mengetahui kadar kalium (K), natrium (Na), kalsium (Ca), besi (Fe) dan magnesium (Mg) pada daun ekor naga.
Penetapan kadar dilakukan dengan menggunakan spektrofotometer serapan atom nyala udara-asetilen. Analisis kuantitatif kalium (K), natrium (Na), kalsium (Ca), besi (Fe) dan magnesium (Mg) dilakukan pada panjang gelombang berturut-turut 769,9 nm, 589,6 nm, 422,7 nm, 248,3 nm dan 202,6 nm.
Hasil penelitian menunjukkan bahwa daun ekor naga mengandung kalium (K), natrium (Na), kalsium (Ca), besi (Fe) dan magnesium (Mg). Hasil penetapan kadar yang diperoleh untuk K adalah 847,9111 ± 3,3573 mg/100g, Na adalah 8,2117 ± 0,1442 mg/100g , Ca adalah 474,6638 ± 4,5448 mg/100g, Fe adalah 1,7975 ± 0,0357 mg/100g dan Mg adalah 69,5370 ± 4,0158 mg/100g. Uji validasi metode memberikan hasil akurasi, batas deteksi dan batas kuantitasi yang dapat diterima dengan persen perolehan kembali untuk K adalah 103,3123% dengan nilai LOD 0,0835 mcg/ml dan LOQ 0,2783 mcg/ml , Na 82,3034% dengan LOD 0,0452 mcg/ml dan LOQ 0,1501 mcg/ml, Ca 105,5125% dengan LOD 0,0052 mcg/ml dan LOQ 0,0173 mcg/ml, Fe 97% dengan LOD 0,1145 dan LOQ 0,3815 dan Mg 102,3854% dengan LOD 0,3705 mcg/ml dan LOQ 1,2351 mcg/ml.
Kata kunci : Mineral esensial, daun ekor naga (Rhaphidophora pinnata (L.f.)
Schott), kalium (K),knatrium (Na), kalsium (Ca), besi (Fe),
ANALYSIS OF ESSENTIAL MINERAL IN DAUN EKOR NAGA (Rhaphidophora pinnata (L.f.) Schott) WITH ATOMIC
ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Daun ekor naga (Rhaphidophora pinnata (L.f.) Schott) is one of plant that is known as herbal medicine. Obtained information that, drinking boiling water of daun ekor naga causes polyuri effect. Potassium and sodium have a closed related with this effect. The aim of this study is to determine the levels of potassium (K), sodium (Na), calcium (Ca), iron (Fe) and magnesium (Mg) in daun ekor naga.
The determination is conducted by using atomic absorption spectrophotometer with air-acetylene flame. Quantitative analysis of potassium (K), sodium (Na), calcium (Ca), iron (Fe) and magnesium (Mg) is performed at the 769,9 nm, 589,6 nm, 422,7 nm, 248,3 nm and 202,6 nm wave length.
The results showed that daun ekor naga (Rhaphidophora pinnata (L.f.) Schott) contain potassium (K), sodium (Na), calcium (Ca), iron (Fe) and magnesium (Mg). The results indicate that the average K content is 847,9111 ± 3,3573 mg/100g, Na is 8,2117 ± 0,1442 mg/100g , Ca is 474,6638 ± 4,5448 mg/100g, Fe is 1,7975 ± 0,0357 mg/100g and Mg is 69,5370 ± 4,0158 mg/100g. Method validity test exhibited accuracy, limit of detection (LOD), and limit of quantitation (LOQ) that can be accepted with percent recovery for K is 103,3123% with LOD is 0,0835 mcg/ml and LOQ is 0,2783 mcg/ml , Na is 82,3034% with LOD is 0,0452 mcg/ml and LOQ is 0,1501 mcg/ml, Ca is 105,5125% with LOD is 0,0052 mcg/ml and LOQ is 0,0173 mcg/ml, Fe is 97% with LOD is 0,1145 and LOQ is 0,3815 and Mg is 102,3854% with LOD is 0,3705 mcg/ml and LOQ is 1,2351 mcg/ml.
Keywords : Essential mineral, daun ekor naga (Rhaphidophora pinnata (L.f.)
BAB I
PENDAHULUAN
1.1 Latar Belakang
Mineral merupakan unsur esensial untuk pemeliharaan fungsi tubuh,
seperti pengaturan kerja enzim-enzim, pemeliharaan keseimbangan asam-basa dan
membantu pembentukan ikatan misalnya pembentukan haemoglobin. Tubuh tidak
mampu mensintesa unsur-unsur tersebut sehingga harus disediakan lewat
makanan (Budiyanto, 2001). Unsur ini digolongkan ke dalam mineral makro dan
mineral mikro. Mineral makro adalah mineral yang dibutuhkan tubuh dalam
jumlah lebih dari 100 mg sehari, sedangkan mineral mikro dibutuhkan kurang dari
100 mg sehari. Unsur yang termasuk mineral makro, seperti natrium, kalium,
kalsium dan magnesium, sedangkan yang termasuk mineral mikro, seperti besi.
Kelima mineral tersebut sangat diperlukan oleh tubuh (Almatsier, 2004).
Sumber mineral yang paling banyak adalah makanan hewani, kecuali
magnesium yang lebih banyak terdapat di dalam makanan nabati terutama sayuran
hijau. Sayuran hijau yang merupakan sumber unsur kalsium, seperti bayam, sawi,
daun melinjo, daun katuk, selada air dan daun singkong. Natrium dijumpai pada
daun selada, pisang, kacang merah, jambu biji dan teh. Kalium terutama terdapat
dalam buah, sayuran dan kacang-kacangan seperti selada, bayam, tomat, alpukat,
kacang merah dan kacang hijau. Mineral mikro seperti besi dapat ditemukan
dalam telur, kacang-kacangan, bayam, sawi, kangkung, daun katuk dan daun
singkong (Almatsier, 2004).
dianggap cukup manjur untuk mengobati berbagai macam penyakit (Mangan,
2003). Salah satu tanaman obat yang digunakan secara tradisional oleh
masyarakat Indonesia adalah “daun ekor naga” (Rhaphidophora pinnata (L.f)
Schott). Belum ditemukan unsur kimia pada daun ekor naga di beberapa literatur.
Tanaman ini merupakan tanaman merambat, batang bulat, mempunyai
akar pelekat dan akar gantung (Heyne, 1987). Diperoleh informasi bahwa,
masyarakat yang mengkonsumsi air rebusan daun ekor naga memiliki efek polyuri
(banyak buang air kecil). Pada umumnya masyarakat awam tidak mengetahui
kandungan dalam daun ekor naga yang dapat memberikan efek tersebut.
Natrium berperan menjaga keseimbangan cairan ekstraseluler agar cairan
tidak keluar dari darah dan masuk ke dalam sel-sel sedangkan di dalam sel kalium
yang menjaga agar cairan ini tidak keluar dari sel. Konsumsi kalium yang banyak
akan meningkatkan konsentrasinya di dalam cairan intraseluler, sehingga
cenderung menarik cairan dari bagian ekstraseluler dan menyebabkan polyuri.
Kalium dan kalsium berperan dalam transmisi saraf dan relaksasi otot. Kalsium
juga penting dalam pembentukan tulang dan gigi. Dengan menahan kalsium di
dalam email gigi, magnesium dapat mencegah kerusakan gigi. Selain itu,
magnesium bertindak sebagai katalisator dalam reaksi biologik termasuk
reaksi-reaksi yang berkaitan dengan metabolisme energi. Besi berada di dalam
haemoglobin berperan sebagai alat angkut oksigen dari paru-paru ke jaringan
tubuh yang penting untuk reaksi biologik (Almatsier, 2004).
Berdasarkan keterkaitan fungsi dari kelima mineral di atas, maka penulis
meneliti kandungan kalium, natrium, kalsium, besi dan magnesium yang terdapat
tersebut adalah spektrofotometri serapan atom karena pelaksanaannya relatif
sederhana, interferensinya sedikit (Rohman, 2009). Disamping itu, kecepatan
analisisnya yang tidak memerlukan pemisahan pendahuluan (Khopkar, 2003).
1.2 Perumusan Masalah
Berdasarkan uraian di atas, maka permasalahan dalam penelitian ini dapat
dirumuskan sebagai berikut:
a. Apakah daun ekor naga mengandung unsur kalium, natrium, kalsium, besi
dan magnesium?
b. Berapa kadar kalium, natrium, kalsium, besi dan magnesium di dalam
daun ekor naga?
1.3 Hipotesis
Hipotesis dalam penelitian ini adalah:
a. Daun ekor naga mengandung unsur kalium, natrium, kalsium, besi dan
magnesium.
b. Daun ekor naga mengandung unsur kalium, natrium, kalsium, besi dan
magnesium dalam jumlah tertentu.
1.4 Tujuan Penelitian
Tujuan penelitian ini adalah:
a. Untuk mengetahui apakah daun ekor naga mengandung unsur kalium,
natrium, kalsium, besi dan magnesium.
b. Untuk mengetahui kadar kalium, natrium, kalsium, besi dan magnesium
1.5 Manfaat Penelitian
Dari hasil penelitian ini, masyarakat dapat mengetahui kadar mineral
BAB II
TINJAUAN PUSTAKA
2.1 Daun Ekor Naga
Daun ekor naga sejenis tanaman merambat yang besar, memanjat,
tingginya mencapai 5 – 15 m, dengan batang yang bulat, dan mempunyai akar
pelekat dan akar gantung yang panjang bergantungan seperti ular yang meliliti
pohon. Daun bentuk bulat memanjang, berbagi-bagi, mempunyai toreh dalamnya
melebihi setengah panjang tulang daun yang berjumlah 7-12 pasang, ujung daun
meruncing. Tanaman ini berasal dari Himalaya sampai Australia dan Pasifik
(Burkill, 1935, Heyne, 1987).
2.1.1 Sinonim (Lemmens and N. Bunyapraphatsara, 2003)
Epipremnum pinnatum (L.) Engl., Scindapsus pinnatus (L.) Schott, Rhaphidophora merrillii Engl.
2.1.2 Nama Daerah (Heyne, 1987)
Indonesia : Tapanawa tairis
Sunda : Lolo munding, Lolo tali
Jawa : Jalu mampang, Sulang
Bali : Samblung
Sumatera Utara : Daun ekor naga
2.1.3 Sistematika Tanaman Daun Ekor Naga (Arthur, 1981)
Divisi : Spermatophyta
Kelas : Monocotyledoneae
Famili : Araceae
Genus : Rhaphidophora
Spesies : Rhaphidophora pinnata (L.f.) Schott
2.1.4 Kegunaan Daun Ekor Naga
Di Singapura, daunnya digunakan sebagai herbal tea untuk mengobati
reumatik dan kanker. Di Philiphina, getah dari batang tanaman digunakan untuk
mengobati gigitan ular beracun. Di Indonesia, bagian dalam dari batang
digunakan sebagai minyak gosok untuk keseleo. Di Vietnam, tanaman ini berguna
untuk mengobati batuk, paralisis, antidotum dan konjugtivitis. Ekstrak daun ekor
naga menunjukkan aktivitas sitotoksis melawan sel kanker secara in vitro.
Alkaloid polihidroksi ada pada daun ini (Lemmens and N. Bunyapraphatsara,
2003).
2.2 Mineral
Yang dimaksud dengan mineral di sini adalah unsur-unsur yang berada
dalam bentuk sederhana. Dalam ilmu gizi biasanya disebut unsur-unsur mineral
atau nutrien/zat gizi anorganik (Poedjiadi, 1994). Unsur ini memegang peranan
penting dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ
maupun fungsi tubuh secara keseluruhan (Almatsier, 2004).
Mineral digolongkan ke dalam mineral makro dan mineral mikro. Mineral
makro adalah mineral yang dibutuhkan tubuh dalam jumah lebih dari 100 mg
sehari, sedangkan mineral mikro dibutuhkan kurang dari 100 mg sehari. Jumlah
mineral mikro dalam tubuh kurang dari 15 mg. Unsur yang termasuk mineral
makro, seperti natrium, kalium, kalsium, fosfor, dan magnesium, sedangkan yang
2.2.1 Kalium
Kalium merupakan ion bermuatan positif, terdapat di dalam sel.
Perbandingan natrium dan kalium di dalam cairan intraseluler adalah 1:10,
sedangkan di dalam cairan ekstraseluler 28:1. Sebanyak 95% kalium tubuh berada
di dalam cairan intraseluler. Taraf kalium normal darah dipelihara oleh ginjal
melalui kemampuannya menyaring, mengabsorbsi kembali dan mengeluarkan
kalium di bawah pengaruh aldosteron. Kalium dikeluarkan dalam bentuk ion
dengan menggantikan ion natrium melalui mekanisme pertukaran di dalam tubula
ginjal (Almatsier, 2004).
Bersama natrium, kalium memegang peranan dalam pemeliharaan
keseimbangan cairan dan elektrolit. Bersama kalsium, kalium berperan dalam
transmisi saraf dan relaksasi otot. Di dalam sel, kalium berfungsi sebagai
katalisator dalam banyak reaksi biologik, terutama dalam metabolisme energi dan
sintesis glikogen dan protein. Kalium berperan dalam pertumbuhan sel. Tekanan
darah normal memerlukan perbandingan antara natrium dan kalium yang sesuai di
dalam tubuh (Almatsier, 2004).
2.2.2 Natrium
Natrium adalah kation utama dalam cairan ekstraseluler. 35-40% natrium
ada di dalam kerangka tubuh. Cairan saluran cerna, sama seperti cairan empedu
dan penkreas, mengandung banyak natrium. Sebagai kation utama dalam cairan
ekstraseluler, natrium menjaga keseimbangan cairan dalam kompartemen tersebut.
Natriumlah yang sebagian besar mengatur tekanan osmosis yang menjaga cairan
tidak keluar dari darah dan masuk ke dalam sel-sel. Di dalam sel tekanan osmosis
dapat menjaga keseimbangan antara natrium di luar sel dan natrium di dalam sel
(Almatsier, 2004).
2.2.3 Kalsium
Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh
yaitu 1,5-2% dari berat badan orang dewasa atau kurang lebih sebanyak 1 kg. Dari
jumlah ini, 99% berada di dalam jaringan keras, yaitu tulang dan gigi terutama
dalam bentuk hidroksiapatit. Selebihnya kalsium tersebar luas di dalam tubuh. Di
dalam cairan ekstraseluler dan intraseluler kalsium memegang peranan penting
dalam mengatur fungsi sel, seperti transmisi saraf, kontraksi otot, penggumpalan
darah dan menjaga permeabilitas membran sel. Kalsium mengatur pekerjaan
hormon-hormon dan faktor pertumbuhan (Almatsier, 2004).
2.2.4 Besi
Zat besi merupakan mineral mikro yang esensial bagi tubuh. Zat ini
terutama diperlukan dalam hemopobesis (pembentukan darah), yaitu dalam
sintesa hemoglobin (Hb). Di samping itu berbagai jenis enzim memerlukan Fe
sebagai faktor penggiat. Di dalam tubuh sebagian besar Fe dapat terkonjugasi
dengan protein, dan terdapat dalam bentuk ferro atau ferri. Bentuk aktif zat besi
biasanya terdapat sebagai ferro, sedangkan bentuk inaktif adalah sebagai ferri
(Sediaoetama, 2008).
2.2.5 Magnesium
Magnesium adalah kation nomor dua paling banyak setelah natrium di
dalam cairan interseluler. Magnesium di dalam alam merupakan bagian dari
klorofil daun. Magnesium memegang peranan penting dalam lebih dari tiga ratus
sebagai katalisator dalam reaksi-reaksi biologik termasuk reaksi yang berkaitan
dengan metabolisme energi, karbohidrat, lipid, protein dan asam nukleat. Di
dalam cairan ekstraseluler magnesium berperan dalam transmisi saraf, kontraksi
otot dan pembekuan darah. Magnesium mencegah kerusakan gigi dengan cara
menahan kalsium di dalam email gigi (Almatsier, 2004).
2.3 Spektrofotometeri Serapan Atom
Spektrofotometri serapan atom adalah suatu metode yang digunakan untuk
mendeteksi atom-atom logam dalam fase gas. Metode ini seringkali
mengandalkan nyala untuk mengubah logam dalam larutan sampel menjadi
atom-atom logam berbentuk gas. Metode ini secara luas digunakan untuk analisis
kuantitatif logam dalam matriks yang kompleks (Bender, 1987).
Teknik SSA menjadi alat yang canggih dalam analisis. Ini disebabkan di
antaranya oleh kecepatan analisisnya, ketelitiannya sampai tingkat runut, tidak
memerlukan pemisahan pendahuluan. Kelebihan kedua adalah kemungkinannya
untuk menentukan konsentrasi semua unsur pada konsentrasi runut. Ketiga,
sebelum pengukuran tidak selalu perlu memisahkan unsur yang ditentukan karena
kemungkinan penentuan satu unsur dengan kehadiran unsur lain dapat dilakukan
asalkan katoda berongga yang diperlukan tersedia (Khopkar,2003).
Spektrofotometri serapan atom digunakan untuk analisis kuantitatif
unsur-unsur logam dalam jumlah sekelumit (trace) dan sangat sekelumit (ultratrace).
Cara analisis ini memberikan kadar total unsur logam dalam suatu sampel dan
tidak tergantung pada bentuk molekul logam dalam sampel tersebut. Cara ini
cocok untuk analisis sekelumit logam karena mempunyai kepekaan yang tinggi
interferensinya sedikit. Spektrofotometri serapan atom didasarkan pada
penyerapan energi sinar oleh atom-atom netral dalam bentuk gas (Rohman, 2007).
Proses yang terjadi ketika dilakukan analisis dengan menggunakan
spektrofotometri atom dengan cara absorbsi yaitu penyerapan energi radiasi oleh
atom-atom yang berada pada tingkat dasar. Atom-atom tersebut menyerap radiasi
pada panjang gelombang tertentu, tergantung pada sifat atom tersebut. Sebagai
contoh natrium menyerap pada panjang gelombang 589 nm, kalium menyerap
pada panjang gelombang 766,5 nm. Dengan menyerap energi, maka atom akan
memperoleh energi sehingga suatu atom pada keadaan dasar dapat ditingkatkan
menjadi ke tingkat eksitasi (Rohman, 2007).
Secara eksperimental akan diperoleh puncak-puncak serapan sinar oleh
atom-atom yang dianalisis. Garis-garis spektrum serapan atom yang timbul karena
serapan sinar yang menyebabkan eksitasi atom dari keadaan azas ke salah satu
tingkat energi yang lebih tinggi disebut garis-garis resonansi (Resonance line).
Garis-garis resonansi ini akan dibaca dalam bentuk angka oleh Readout (Rohman,
2007).
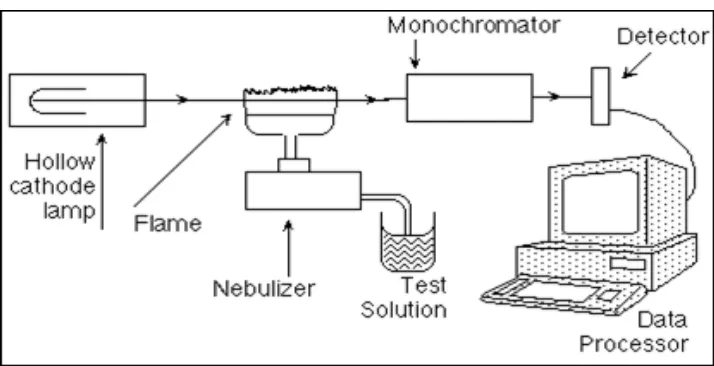
Adapun instrumentasi spektrofotometer serapan atom adalah sebagai
berikut:
a. Sumber Radiasi
Sumber radiasi yang digunakan adalah lampu katoda berongga (hollow
cathoda lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung
suatu katoda dan anoda. Katoda berbentuk silinder berongga yang dilapisi dengan
b. Tempat sampel
Dalam analisis dengan spektrofotometer serapan atom, sampel yang akan
dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam keadaan
azas. Ada berbagai macam alat yang digunakan untuk mengubah sampel menjadi
uap atom-atomnya, yaitu:
1. Dengan nyala (Flame)
Nyala digunakan untuk mengubah sampel yang berupa cairan menjadi
bentuk uap atomnya dan untuk proses atomisasi. Suhu yang dapat dicapai oleh
nyala tergantung pada gas yang digunakan, misalnya untuk gas asetilen-udara
suhunya sebesar 2200ºC. Sumber nyala asetilen-udara ini merupakan sumber
nyala yang paling banyak digunakan. Pada sumber nyala ini asetilen sebagai
bahan pembakar, sedangkan udara sebagai bahan pengoksidasi (Rohman, 2007).
2. Tanpa nyala (Flameless)
Pengatoman dilakukan dalam tungku dari grafit. Sejumlah sampel diambil
sedikit (hanya beberapa μL), lalu diletakkan dalam tabung grafit, kemudian
tabung tersebut dipanaskan dengan sistem elektris dengan cara melewatkan arus
listrik pada grafit. Akibat pemanasan ini, maka zat yang akan dianalisis berubah
menjadi atom-atom netral dan pada fraksi atom ini dilewatkan suatu sinar yang
berasal dari lampu katoda berongga sehingga terjadilah proses penyerapan energi
sinar yang memenuhi kaidah analisis kuantitatif (Rohman, 2007).
c. Monokromator
Monokromator merupakan alat untuk memisahkan dan memilih spektrum
sesuai dengan panjang gelombang yang digunakan dalam analisis dari sekian
d. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui
tempat pengatoman (Rohman, 2007).
e. Amplifier
Amplifier merupakan suatu alat untuk memperkuat signal yang diterima
dari detektor sehingga dapat dibaca alat pencatat hasil (Readout) (Rohman, 2007).
e. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai
pencatat hasil. Hasil pembacaan dapat berupa angka atau berupa kurva yang
menggambarkan absorbansi atau intensitas emisi (Rohman, 2007).
Gambar 1. Komponen Spektrofotometer Serapan Atom
Gangguan-gangguan dapat terjadi pada saat dilakukan analisis dengan alat
spektrofotometer serapan atom, gangguan itu antara lain adalah:
a. Gangguan oleh penyerapan non-atomik.
Gangguan ini terjadi akibat penyerapan cahaya dari sumber sinar yang
bukan berasal dari atom-atom yang akan dianalisis. Penyerapan non-atomik dapat
berada di dalam nyala. Cara mengatasi penyerapan non-atomik ini adalah bekerja
pada panjang gelombang yang lebih besar (Rohman, 2007).
b. Gangguan spektrum.
Gangguan spektrum dalam spektrofotometer serapan atom timbul akibat
terjadinya tumpang tindih antara frekuensi-frekuensi garis resonansi unsur yang
dianalisis dengan garis-garis yang dipancarkan oleh unsur lain. Hal ini disebabkan
karena rendahnya resolusi monokromator (Mulja, 1995).
c. Gangguan kimia yang dapat mempengaruhi jumlah atau banyaknya atom di
dalam nyala.
Pembentukkan atom-atom netral dalam keadaan azas di dalam nyala sering
terganggu oleh dua peristiwa kimia, yaitu:
• Disosiasi senyawa-senyawa yang tidak sempurna disebabkan terbentuknya
senyawa refraktorik (sukar diuraikan dalam api), sehingga akan
mengurangi jumlah atom netral yang ada di dalam nyala.
• Ionisasi atom-atom di dalam nyala akibat suhu yang digunakan terlalu
tinggi. Prinsip analisis dengan spektrofotometer serapan atom adalah
mengukur absorbansi atom-atom netral yang berada dalam keadaan azas.
Jika terbentuk ion maka akan mengganggu pengukuran absorbansi atom
netral karena spektrum absorbansi atom-atom yang mengalami ionisasi
tidak sama dengan spektrum atom dalam keadaan netral (Rohman,2007).
2.4 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap
parameter tertentu berdasarkan percobaan laboratorium untuk membuktikan
parameter analisis yang harus dipertimbangkan dalam validasi metode analisis
adalah sebagai berikut:
a. Kecermatan (accuracy)
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil
analisis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai
persen perolehan kembali (recovery) analit yang ditambahkan. Kecermatan
ditentukan dengan dua cara, yaitu:
1. Metode simulasi
Metode simulasi (Spiked-placebo recovery) merupakan metode yang
dilakukan dengan cara menambahkan sejumlah analit bahan murni ke dalam suatu
bahan pembawa sediaan farmasi (plasebo), lalu campuran tersebut dianalisis dan
hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang
sebenarnya) (Harmita, 2004).
2. Metode penambahan baku
Metode penambahan baku (standard addition method) merupakan metode
yang dilakukan dengan cara menambahkan sejumlah analit dengan konsentrasi
tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode yang akan
divalidasi. Hasilnya dibandingkan dengan sampel yang dianalisis tanpa
penambahan sejumlah analit. Persen perolehan kembali ditentukan dengan
menentukan berapa persen analit yang ditambahkan ke dalam sampel dapat
ditemukan kembali (Harmita, 2004).
Rentang persen perolehan kembali yang diizinkan pada setiap konsentrasi
Tabel 1. Rentang persen perolehan kembali yang diizinkan.
Jumlah analit pada sampel Persen perolehan kembali yang diizinkan (%)
1 ppm
100 ppb
10 ppb
1 ppb
80-110
80-110
60-115
40-120
(Harmita, 2004)
b. Keseksamaan (precision)
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau
koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan
derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara
berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang
memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan
(Harmita, 2004).
Dari penelitian yang telah dilakukan, ditemukan bahwa simpangan baku
relatif atau RSD meningkat seiring dengan menurunnya kadar analit yang
dianalisis. Nilai simpangan baku relatif untuk analit dengan kadar kurang dari 1
ppm yang diizinkan yaitu tidak lebih dari 32% (Harmita, 2004).
c. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuannya yang
hanya mengukur zat tertentu secara cermat dan seksama dengan adanya
komponen lain yang ada di dalam sampel (Harmita, 2004).
d. Linearitas dan rentang
Linearitas adalah kemampuan metode analisis yang memberikan respon
baik secara langsung maupun dengan bantuan transformasi matematika,
dalam sampel. Rentang merupakan batas terendah dan batas tertinggi analit yang
dapat ditetapkan secara cermat, seksama dan dalam linearitas yang dapat diterima
(Harmita, 2004).
e. Batas deteksi dan batas kuantitasi
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan, sedangkan batas kuantitasi
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Farmasi Kualitatif
Fakultas Farmasi USU dan di Laboratorium Pusat Penelitian Kelapa Sawit
(PPKS) Medan pada bulan Desember 2010 – Februari 2011.
3.2 Bahan – bahan
3.2.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah daun ekor naga
(Rhaphidophora pinnata (L.f.) Schott) yang berasal dari daerah Medan Timur
(Gambar dapat dilihat pada Lampiran 1 Halaman 42).
3.2.2 Pereaksi
Semua bahan yang digunakan dalam penelitian ini berkualitas pro analisis
keluaran E. Merck kecuali disebutkan lain yaitu asam nitrat, asam klorida, asam
pikrat, asam sulfat, etanol 96%, kalium heksasianoferat (II), ammonium tiosianat,
natrium hidroksida, kuning titan, larutan standar kalium, larutan standar natrium,
larutan standar kalsium, larutan standar besi, larutan standar magnesium,
akuabides (IKA).
3.3 Alat – alat
Spektrofotometer Serapan Atom (GBC Avanta Σ, Australia) lengkap
dengan dengan lampu katoda K, Na, Ca, Fe, dan Mg, neraca analitik (BOECO,
Germany), hot plate (FISONS), alat tanur NEY M-525, blender, kertas saring
3.4 Pembuatan Pereaksi
3.4.1 Larutan HNO3 (1:1)
Larutan HNO3 65% v/v sebanyak 500 ml diencerkan dengan 500 ml air
suling (Helrich, 1990).
3.4.2 Larutan HCl(1:1)
Larutan HCl 37% v/v sebanyak 500 ml diencerkan dengan 500 ml air
suling (Helrich, 1990).
3.4.3 Asam Pikrat 1% b/v
Sebanyak 1 gram asam pikrat dilarutkan dalam air suling hingga 100 ml
(Manan, 2009).
3.4.4 Larutan H2SO4 1 N
Dipipet 3 ml H2SO4 96% v/v, dimasukkan perlahan-lahan melalui dinding
labu tentukur 100 ml yang telah berisi air suling setengahnya. Dicukupkan
volumenya dengan air suling hingga garis tanda (Walinga, 1989).
3.4.5 Larutan NH4SCN 1,5 N
Sebanyak 57,09 gram ammonium tiosianat dilarutkan dalam 100 ml air
suling, diencerkan hingga 500 ml (Manan, 2009).
3.4.6 Larutan K4[Fe(CN)6] 2 N
Sebanyak 105,5 gram K4[Fe(CN)6] dilarutkan dalam air suling hingga 500
ml (Manan, 2009).
3.4.7 Kuning Titan 0,1% b/v
Larutan Kuning Titan 0,1% b/v dibuat dengan cara melarutkan 0,1 g titan
3.4.8 Larutan NaOH 2 N
Sebanyak 80,02 gram NaOH dilarutkan dengan air suling hingga 1000 ml
(Ditjen POM, 1979).
3.5 Prosedur Penelitian
3.5.1 Pengambilan sampel
Sampel yang digunakan adalah daun ekor naga (Rhaphidophora pinnata
(L.f.) Schott) segar yang diperoleh dari Jl. Umar No.17 Glugur Darat I Kecamatan
Medan Timur, Kota Medan, Provinsi Sumatera Utara. Metode pengambilan
sampel dilakukan dengan cara sampling purposif atau sampling pertimbangan
(Sudjana, 2005).
3.5.2 Identifikasi Tumbuhan
Identifikasi tumbuhan dilakuka n di Lembaga Ilmu Pengetahuan
Indonesia-Pusat Penelitian Biologi, Bogor.
3.5.3 Penyiapan Sampel
Sebanyak 1 kg daun ekor naga (Rhaphidophora pinnata (L.f.) Schott)
yang segar dibersihkan dari pengotoran, dicuci bersih, ditiriskan. Selanjutnya
dikeringkan dengan cara diangin-anginkan di udara terbuka terhindar dari sinar
matahari langsung, setelah kering, dihaluskan dengan blender.
3.5.4 Proses Destruksi
Sampel ditimbang seksama sebanyak 10 gram dalam krus porselen,
diarangkan di atas hot plate, lalu diabukan dalam tanur dengan temperatur awal
100oC dan perlahan – lahan temperatur dinaikkan hingga suhu 500oC dengan
interval 25oC setiap 5 menit. Pengabuan dilakukan selama 6 jam dan dibiarkan
ditambahkan 10 ml HNO3 (1:1), kemudian diuapkan pada hot plate sampai kering.
Krus porselen dimasukkan kembali ke dalam tanur dengan temperatur awal 100oC
dan perlahan – lahan temperatur dinaikkan hingga suhu 500oC dengan interval
25oC setiap 5 menit. Pengabuan dilakukan selama 1 jam dan dibiarkan hingga
dingin pada desikator (Helrich, 1990). Bagan alir penyiapan sampel dan proses
destruksi dapat dilihat pada gambar 2.
Gambar 2. Bagan alir penyiapan sampel dan proses destruksi.
Daun ekor naga
Ditimbang 10 gram di atas krus porselen
Diabukan dalam tanur dengan temperatur awal 100oC dan perlahan – lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit
Dibasahi dengan 10 tetes akuabides
Diuapkan pada hot plate sampai kering
Dilakukan selama 6 jam dan dibiarkan hingga dingin pada desikator
Abu
Dilakukan selama 1 jam dan dibiarkan hingga dingin pada desikator
Dibersihkan dari pengotoran
Dimasukkan kembali ke dalam tanur dengan temperatur awal 100oC dan perlahan – lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit. Dicuci bersih
Ditiriskan
Dikeringkan dengan cara diangin-anginkan di udara terbuka terhindar dari sinar matahari langsung
Dihaluskan dengan blender
Sampel yang telah dihaluskan
Hasil
3.5.5 Pembuatan Larutan Sampel
Sampel hasil destruksi dilarutkan dalam 20 ml HCl (1:1), lalu dituangkan
ke dalam labu tentukur 100 ml dan diencerkan dengan akuabides hingga garis
tanda (Helrich, 1990). Kemudian disaring dengan kertas saring Whatman No. 42,
5 ml filtrat pertama dibuang untuk menjenuhkan kertas saring kemudian filtrat
selanjutnya ditampung ke dalam botol. Larutan ini digunakan untuk analisis
kualitatif dan kuantitatif. Bagan alir pembuatan larutan sampel dapat dilihat pada
gambar 3.
Gambar 3. Bagan alir pembuatan larutan sampel
Sampel yang telah didestruksi
Dilarutkan dalam 20 ml HCl (1:1)
Dituangkan ke dalam labu tentukur 100 ml Diencerkan dengan akuabides hingga garis tanda
Dimasukkan ke dalam botol
Larutan sampel
Disaring dengan kertas saring Whatman No.42
Dibuang 5 ml untuk menjenuhkan kertas saring
Dilakukan analisis kualitatif
Dilakukan analisis kuantitatif dengan Spektrofotometer Serapan atom pada λ 769,9 nm untuk kalium, λ 589,6 nm untuk natrium, λ 422,7 nm untuk kalsium, λ 248,3 nm untuk besi dan λ 202,6 nm untuk magnesium
3.5.6 Pemeriksaan Kualitatif
3.5.6.1 Kalium
3.5.6.1.1 Uji Kristal Kalium dengan Asam Pikrat
Larutan zat diteteskan 1-2 tetes pada object glass kemudian ditetesi
dengan larutan asam pikrat, dibiarkan ± 5 menit lalu diamati di bawah mikroskop.
Jika terdapat kalium, akan terlihat kristal berbentuk jarum besar.
3.5.6.2 Natrium
3.5.6.2.1 Uji Kristal Natrium dengan Asam Pikrat
Larutan zat diteteskan 1-2 tetes pada object glass kemudian ditetesi
dengan larutan asam pikrat, dibiarkan ± 5 menit lalu diamati di bawah mikroskop.
Jika terdapat natrium, akan terlihat kristal berbentuk jarum halus.
3.5.6.3 Kalsium
3.5.6.3.1 Uji Kristal Kalsium dengan Asam Sulfat 1 N
Larutan zat diteteskan 1-2 tetes pada object glass kemudian ditetesi
dengan larutan asam sulfat dan etanol 96% akan terbentuk endapan putih lalu
diamati di bawah mikroskop. Jika terdapat kalsium akan terlihat kristal berbentuk
jarum (Vogel, 1990).
3.5.6.4 Besi
3.5.6.4.1 Reaksi Kualitatif dengan Larutan K4[Fe(CN)6] 2 N
Kedalam tabung reaksi dimasukkan 2 ml larutan sampel, ditambahkan 10
tetes kalium heksasianoferat (II). Dihasilkan larutan berwarna biru tua (Vogel,
3.5.6.4.2 Reaksi Kualitatif dengan Larutan NH4SCN 1,5 N
Kedalam tabung reaksi dimasukkan 2 ml larutan sampel, ditambahkan 3
tetes amonium tiosianat. Dihasilkan warna merah (Vogel, 1990).
3.5.6.5 Magnesium
3.5.6.5.1 Reaksi Kualitatif dengan Larutan Kuning Titan 0,1% b/v
Kedalam tabung reaksi dimasukkan 2 ml larutan sampel, ditambah 5-6
tetes NaOH 2 N dan 3 tetes pereaksi kuning titan. Dihasilkan endapan merah
terang (Vogel, 1990).
3.5.7 Pemeriksaan Kuantitatif
3.5.7.1 Pembuatan Kurva Kalibrasi Kalium
Larutan baku kalium (1000 mcg/ml) dipipet sebanyak 10 ml, dimasukkan
ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan
akuabides (konsentrasi 100 mcg/ml). Larutan baku kalium (100 mcg/ml) dipipet
sebanyak 10 ml, dimasukkan ke dalam labu ukur 100 ml kemudian dicukupkan
sampai garis tanda dengan akuabides (konsentrasi 10 mcg/ml).
Larutan untuk kurva kalibrasi kalium dibuat dengan memipet 5; 10; 20; 30
dan 40 ml larutan baku 10 mcg/ml, masing-masing dimasukkan ke dalam labu
tentukur 100 ml dan dicukupkan hingga garis tanda dengan akuabides (larutan ini
mengandung 0,5; 1,0; 2,0; 3,0 dan 4,0 mcg/ml) dan diukur pada panjang
gelombang 769,9 nm dengan tipe nyala udara-asetilen.
3.5.7.2 Pembuatan Kurva Kalibrasi Natrium
Larutan baku natrium (1000 mcg/ml) dipipet sebanyak 10 ml, dimasukkan
ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan
sebanyak 10 ml, dimasukkan ke dalam labu ukur 100 ml dicukupkan sampai garis
tanda dengan akuabides (konsentrasi 10 mcg/ml).
Larutan untuk kurva kalibrasi natrium dibuat dengan memipet 2; 4; 6; 12
dan 14 ml larutan baku 10 mcg/ml, masing-masing dimasukkan ke dalam labu
tentukur 100 ml dan dicukupkan hingga garis tanda dengan akuabides (larutan ini
mengandung 0,2; 0,4; 0,6; 1,2 dan 1,4 mcg/ml) dan diukur pada panjang
gelombang 589,6 nm dengan tipe nyala udara-asetilen.
3.5.7.3 Pembuatan Kurva Kalibrasi Kalsium
Larutan baku kalsium (1000 mcg/ml) dipipet sebanyak 10 ml, dimasukkan
ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan
akuabides (konsentrasi 100 mcg/ml). Larutan baku kalsium (100 mcg/ml) dipipet
sebanyak 10 ml, dimasukkan ke dalam labu ukur 100 ml kemudian dicukupkan
sampai garis tanda dengan akuabides (konsentrasi 10 mcg/ml).
Larutan untuk kurva kalibrasi kalsium dibuat dengan memipet 5; 10; 20;
30 dan 40 ml larutan baku 10 mcg/ml, masing-masing dimasukkan ke dalam labu
tentukur 100 ml dan dicukupkan hingga garis tanda dengan akuabides (larutan ini
mengandung 0,5; 1,0; 2,0; 3,0 dan 4,0 mcg/ml) dan diukur pada panjang
gelombang 422,7 nm dengan tipe nyala udara-asetilen.
3.5.7.4 Pembuatan Kurva Kalibrasi Besi
Larutan baku besi (1000 mcg/ml) dipipet sebanyak 10 ml, dimasukkan ke
dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan akuabides
(konsentrasi 100 mcg/ml). Larutan baku besi (100 mcg/ml) dipipet sebanyak 10
ml, dimasukkan ke dalam labu ukur 100 ml, kemudian dicukupkan sampai garis
Larutan untuk kurva kalibrasi besi dibuat dengan memipet 5; 10; 20; 30
dan 40 ml larutan baku 10 mcg/ml, masing-masing dimasukkan ke dalam labu
tentukur 100 ml dan dicukupkan hingga garis tanda dengan akuabides (larutan ini
mengandung 0,5; 1,0; 2,0; 3,0 dan 4,0 mcg/ml) dan diukur pada panjang
gelombang 248,3 nm dengan tipe nyala udara-asetilen.
3.5.7.5 Pembuatan Kurva Kalibrasi Magnesium
Larutan baku magnesium (1000 mcg/ml) dipipet sebanyak 10 ml,
dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda
dengan akuabides (konsentrasi 100 mcg/ml). Larutan baku magnesium (100
mcg/ml) dipipet sebanyak 10 ml, dimasukkan ke dalam labu ukur 100 ml,
kemudian dicukupkan sampai garis tanda dengan akuabides (konsentrasi 10
mcg/ml).
Larutan untuk kurva kalibrasi magnesium dibuat dengan memipet 5; 10;
20; 30 dan 40 ml larutan baku 10 mcg/ml, masing-masing dimasukkan ke dalam
labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan akuabides
(larutan ini mengandung 0,5; 1,0; 2,0; 3,0 dan 4,0 mcg/ml) dan diukur pada
panjang gelombang 202,6 nm dengan tipe nyala udara-asetilen.
3.5.7.6 Penetapan Kadar Kalium, Natrium, Kalsium, Besi dan Magnesium dalam Sampel
3.5.7.6.1 Penetapan Kadar Kalium
Larutan sampel hasil destruksi dipipet sebanyak 1 ml, dimasukkan ke
dalam labu tentukur 500 ml dan dicukupkan hingga garis tanda dengan akuabides.
Kemudian diukur absorbansinya dengan menggunakan spektrofotometer serapan
berada dalam rentang kurva kalibrasi larutan baku kalium. Konsentrasi kalium
dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.5.7.6.2 Penetapan Kadar Natrium
Larutan sampel hasil destruksi dipipet sebanyak 10 ml, dimasukkan ke
dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan akuabides.
Kemudian diukur absorbansinya dengan menggunakan spektrofotometer serapan
atom pada panjang gelombang 589,6 nm. Nilai absorbansi yang diperoleh harus
berada dalam rentang kurva kalibrasi larutan baku natrium. Konsentrasi natrium
dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.5.7.6.3 Penetapan Kadar Kalsium
Larutan sampel hasil destruksi dipipet sebanyak 1 ml, dimasukkan ke da-
lam labu tentukur 250 ml dan dicukupkan hingga garis tanda dengan akuabides.
Kemudian diukur absorbansinya dengan menggunakan spektrofotometer serapan
atom pada panjang gelombang 422,7 nm. Nilai absorbansi yang diperoleh harus
berada dalam rentang kurva kalibrasi larutan baku kalsium. Konsentrasi kalsium
dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.5.7.6.4 Penetapan Kadar Besi
Larutan sampel hasil destruksi diukur absorbansinya dengan menggunakan
spektrofotometer serapan atom pada panjang gelombang 248,3 nm. Nilai
absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan
baku besi. Konsentrasi besi dalam sampel ditentukan berdasarkan persamaan garis
3.5.7.6.5 Penetapan Kadar Magnesium
Larutan sampel hasil destruksi dipipet sebanyak 2 ml, dimasukkan ke
dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan akuabides.
Kemudian diukur absorbansinya dengan menggunakan spektrofotometer serapan
atom pada panjang gelombang 202,6 nm. Nilai absorbansi yang diperoleh harus
berada dalam rentang kurva kalibrasi larutan baku magnesium. Konsentrasi
magnesium dalam sampel ditentukan berdasarkan persamaan garis regresi dari
kurva kalibrasi.
Kadar kalium, natrium, kalsium, besi dan magnesium dalam sampel dapat
dihitung dengan cara sebagai berikut:
(g) Sampel Berat
n pengencera Faktor
x (ml) Volume x
(mcg/ml) i
Konsentras (mcg/g)
Kadar =
3.5.8 Penentuan Batas Deteksi (Limit of Detection) dan Batas Kuantitasi (Limit of Quantitation)
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan. Sedangkan batas kuantitasi
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
kriteria cermat dan seksama.
Batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai
berikut (Harmita, 2004):
Simpangan Baku =
(
)
2
2
− −
∑
n Yi Y
Batas deteksi (LOD) =
slope SB x
3
Batas kuantitasi (LOQ) =
slope SB x
3.5.9 Uji Perolehan Kembali (Recovery)
Uji perolehan kembali atau recovery dilakukan dengan metode
penambahan larutan baku (standard addition method). Dalam metode ini, kadar
logam dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan
kadar logam dalam sampel setelah penambahan larutan baku dengan konsentrasi
tertentu (Ermer, 2005). Larutan baku yang ditambahkan yaitu, 10 ml larutan baku
kalium (konsentrasi 3 mcg/ml), 10 ml larutan baku natrium (konsentrasi 1,2
mcg/ml), 15 ml larutan baku kalsium (konsentrasi 4 mcg/ml), 6 ml larutan baku
besi (konsentrasi 3 mcg/ml) dan 11 ml larutan baku magnesium (konsentrasi 4
mcg/ml).
Daun ekor naga yang telah dihaluskan ditimbang secara seksama sebanyak
10 gram, lalu ditambahkan 10 ml larutan baku kalium (konsentrasi 3 mcg/ml),
kemudian dilanjutkan dengan prosedur destruksi kering seperti yang telah
dilakukan sebelumnya. Lakukan langkah kerja yang sama untuk uji perolehan
kembali natrium, kalsium, besi dan magnesium dengan penambahan larutan baku
masing-masing.
Persen perolehan kembali dapat dihitung dengan rumus di bawah ini
(Harmita, 2004):
= 100%
an ditambahak yang
baku larutan kadar
awal sampel dalam
logam kadar sampel
dalam logam total kadar
× −
3.5.10 Analisis Data Secara Statistik
Kadar kalium, natrium, kalsium, besi dan magnesium yang diperoleh dari
hasil pengukuran masing-masing larutan sampel dianalisis dengan metode standar
SD =
( )
1 -nX
-Xi 2
∑
Keterangan : Xi = Kadar sampel
X− = Kadar rata-rata sampel
n = jumlah perulangan
Untuk mencari thitung digunakan rumus:
t hitung =
dan untuk menentukan kadar logam di dalam sampel dengan interval kepercayaan
95%, α = 0.05, dk = n-1, dapat digunakan rumus:
Kadar Logam : µ = X ± (t(α/2, dk) x SD / √n )
Keterangan : X− = Kadar rata-rata sampel
SD = Standar Deviasi
dk = Derajat kebebasan (dk = n-1)
α = interval kepercayaan
n = jumlah perulangan
3.5.11 Simpangan Baku Relatif
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau
koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan
derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara
berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang
memenuhi persyaratan menunjukkan adanya keseksamaan metode yang
Adapun rumus untuk menghitung simpangan baku relatif adalah (Harmita,
2004) :
RSD = ×100%
X SD
Keterangan : X− = Kadar rata-rata sampel
SD = Standar Deviasi
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan di Pusat Penelitian dan Pengembangan
Biologi, LIPI, Bogor, disebutkan bahwa tumbuhan yang digunakan adalah daun
ekor naga (Rhaphidophora pinnata (L.f.) Schott) suku Araceae (Jambak, 2008).
Tumbuhan yang digunakan pada penelitian ini diambil pada tempat yang sama
sehingga tidak dilakukan identifikasi kembali. Hasil identifikasi tumbuhan dapat
dilihat pada Lampiran 2 Halaman 43.
4.2 Analisis Kualitatif
Analisis kualitatif dilakukan sebagai analisis pendahuluan untuk
mengetahui ada atau tidaknya kalium, natrium, kalsium, besi dan magnesium
dalam sampel. Data dapat dilihat pada tabel 2 dan Lampiran 3 Halaman 44 s/d
[image:48.596.104.521.509.695.2]46.
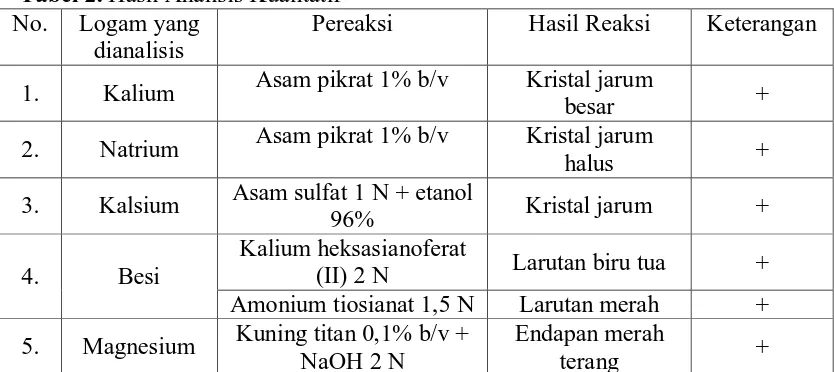
Tabel 2. Hasil Analisis Kualitatif
No. Logam yang dianalisis
Pereaksi Hasil Reaksi Keterangan
1. Kalium Asam pikrat 1% b/v Kristal jarum
besar +
2. Natrium Asam pikrat 1% b/v Kristal jarum
halus +
3. Kalsium Asam sulfat 1 N + etanol
96% Kristal jarum +
4. Besi
Kalium heksasianoferat
(II) 2 N Larutan biru tua +
Amonium tiosianat 1,5 N Larutan merah +
5. Magnesium Kuning titan 0,1% b/v + NaOH 2 N
Endapan merah
terang +
Keterangan :
Tabel di atas menunjukkan bahwa daun ekor naga mengandung kalium,
natrium, kalsium, besi dan magnesium. Sampel dikatakan positif mengandung
kalium jika menghasilkan kristal jarum besar dengan penambahan asam pikrat dan
mengandung natrium jika menghasilkan kristal jarum halus. Dikatakan positif
mengandung kalsium jika menghasilkan endapan putih berbentuk kristal jarum
dengan penambahan asam sulfat dan etanol, mengandung besi jika menghasilkan
larutan biru dengan penambahan larutan kalium heksasianoferat (II) dan larutan
merah dengan penambahan amonium tiosianat dan mengandung magnesium jika
menghasilkan endapan merah terang dengan penambahan larutan kuni ng titan dan
natrium hidroksida (Vogel, 1979).
4.3 Analisis Kuantitatif
4.3.1 Kurva kalibrasi Kalium, Natrium, Kalsium, Besi dan Magnesium
Kurva kalibrasi kalium, natrium, kalsium, besi dan magnesium diperoleh
dengan cara mengukur absorbansi dari larutan baku kalium, natrium, kalsium, besi
dan magnesium pada panjang gelombang masing-masing. Dari pengukuran kurva
kalibrasi untuk kalium, natrium, kalsium, besi dan magnesium diperoleh
persamaan garis regresi yaitu Y = 0,1801X - 0,0048 untuk kalium, Y = 0,1752X
+ 0,0026 untuk natrium, Y = 0,0446 + 0,0058 untuk kalsium, Y = 0,0219X -
0,0008 untuk besi dan Y = 0,0408X + 0,0060 untuk magnesium.
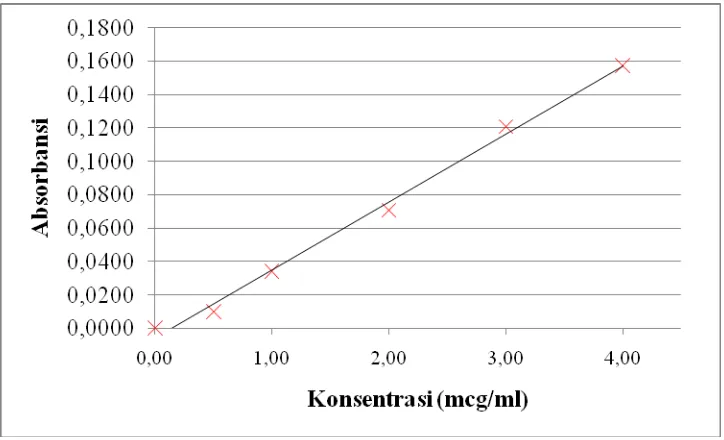
Kurva kalibrasi larutan baku kalium, natrium, kalsium, besi dan
Gambar 4. Kurva Kalibrasi Kalium
[image:50.596.131.494.393.616.2]Gambar 6. Kurva Kalibrasi Kalsium
[image:51.596.132.495.394.615.2]Gambar 8. Kurva Kalibrasi Magnesium
Berdasarkan kurva di atas diperoleh hubungan yang linear antara
konsentrasi dengan absorbansi, dengan koefisien korelasi (r) untuk kalium sebesar
0,9999, natrium sebesar 0,9997, kalsium sebesar 0,9995, besi sebesar 0,9998 dan
magnesium sebesar 0,9974. Nilai r ≥ 0,95 menunjukkan adanya korelasi linier
yang menyatakan adanya hubungan antara X dan Y (Shargel dan Andrew, 1999).
Data hasil pengukur an absorbansi larutan baku kalium, natrium, kalsium, besi
dan magnesium dan perhitungan persamaan garis regresi dapat dilihat pada
Lampiran 4 s/d 8 Halaman 47 s/d 51.
4.3.2 Analisis Kadar Kalium, Natrium, Kalsium, Besi dan Magnesium dalam
Daun Ekor Naga
Penentuan kadar kalium, natrium, kalsium, besi dan magnesium dilakukan
secara spektrofotometri serapan atom. Konsentrasi kalium, natrium, kalsium, besi
dan magnesium dalam sampel ditentukan berdasarkan persamaan garis regresi
dapat dilihat pada Lampiran 9 Halaman 52 s/d 53 dan Lampiran 10 Halaman
54 s/d 56.
Analisis dilanjutkan dengan perhitungan statistik (Perhitungan dapat
dilihat pada Lampiran 11 Halaman 57 s/d 71). Hasil analisis kuantitatif kalium,
[image:53.596.152.474.247.379.2]natrium, kalsium, besi dan magnesium pada sampel dapat dilihat pada Tabel 3.
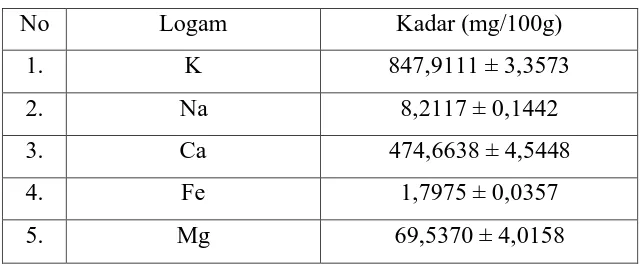
Tabel 3. Kadar Kalium, Natrium, Kalsium, Besi dan Magnesium
No Logam Kadar (mg/100g)
1. K 847,9111 ± 3,3573
2. Na 8,2117 ± 0,1442
3. Ca 474,6638 ± 4,5448
4. Fe 1,7975 ± 0,0357
5. Mg 69,5370 ± 4,0158
Dari Tabel 3. di atas dapat diketahui bahwa kadar kalium jauh lebih besar
dibandingkan dengan natrium. Selanjutnya diikuti dengan kalsium, magnesium
dan yang paling kecil adalah besi. Konsumsi kalium yang banyak akan
meningkatkan konsentrasinya di dalam cairan intraseluler, sehingga cenderung
menarik cairan dari bagian ekstraseluler dan menyebabkan polyuri (Almatsier,
2004). Ketidakseimbangan jumlah kalium dan natrium inilah yang menyebabkan
orang yang meminum air rebusan daun ekor naga memiliki efek polyuri.
4.3.3 Batas Deteksi dan Batas Kuantitasi
Berdasarkan data kurva kalibrasi kalium, natrium, kalsium, besi dan
magnesium, diperoleh batas deteksi dan batas kuantitasi untuk kelima logam
tersebut. Dari hasil perhitungan diperoleh batas deteksi untuk kalium, natrium,
kalsium, besi dan magnesium masing-masing sebesar 0,0835 mcg/ml, 0,0452
kuantitasinya sebesar 0,2783 mcg/ml, 0,1501 mcg/ml, 0,0173 mcg/ml, 0,3815
mcg/ml dan 1,2351 mcg/ml.
Dari hasil perhitungan dapat dilihat bahwa semua hasil yang diperoleh
pada pengukuran sampel berada diatas batas deteksi dan batas kuantitasi.
Perhitungan batas deteksi dan batas kuantitasi dapat dilihat pada Lampiran 12
Halaman 72 s/d 76.
4.3.4 Uji Perolehan Kembali (Recovery)
Hasil uji perolehan kembali (recovery) kalium, natrium, kalsium, besi dan
magnesium setelah penambahan masing-masing larutan baku logam dalam sampel
dapat dilihat pada Lampiran 13 Halaman 77 s/d 78. Perhitungan persen recovery
kalium, natrium, kalsium, besi dan magnesium dalam sampel dapat dilihat pada
Lampiran 14 Halaman 79 s/d 81. Persen recovery kalium, natrium, kalsium,
[image:54.596.125.498.470.619.2]besi dan magnesium dalam sampel dapat dilihat pada Tabel 4.
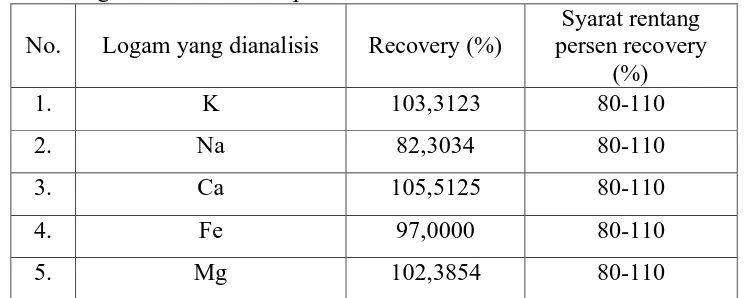
Tabel 4. Persen Uji Perolehan Kembali (recovery) Kalium, Natrium, Kalsium,
Besi dan Magnesium dalam Sampel
No. Logam yang dianalisis Recovery (%)
Syarat rentang persen recovery
(%)
1. K 103,3123 80-110
2. Na 82,3034 80-110
3. Ca 105,5125 80-110
4. Fe 97,0000 80-110
5. Mg 102,3854 80-110
Berdasarkan tabel di atas, dapat dilihat bahwa rata-rata hasil uji perolehan
kembali (recovery) untuk kalium adalah 103,3123%, untuk natrium adalah
82,3034%, untuk kalsium adalah 105,5125%, untuk besi adalah 97,0000%, dan
untuk magnesium adalah 102,3854%,. Persen recovery tersebut menunjukkan
kalsium, besi dan magnesium dalam sampel. Hasil uji perolehan kembali
(recovery) ini memenuhi syarat akurasi yang telah ditetapkan, yaitu rata-rata hasil
perolehan kembali (recovery) untuk analit yang jumlahnya antara 0,1 ppm - 10
ppm berada pada rentang 80-110% (Harmita, 2004).
4.3.5 Simpangan Baku Relatif
Dari perhitungan yang dilakukan terhadap data hasil pengukuran kadar
logam kalium, natrium, kalsium, besi dan magnesium pada daun ekor naga,
diperoleh nilai simpangan baku yaitu 2,7039; 0,0905; 2,8562; 0,0224; 2,5223 dan
nilai simpangan baku relatif yaitu 0,3189%; 1,1021%; 0,6017%; 1,2462%;
3,6273% . Menurut Harmita (2004), nilai simpangan baku relatif untuk analit
dengan kadar part per million (ppm) RSDnya adalah tidak lebih dari 16% dan
untuk analit dengan kadar part per billion (ppb) RSDnya adalah tidak lebih dari
32%. Dari hasil yang diperoleh menunjukkan bahwa metode yang dilakukan
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Hasil analisis secara kualitatif dari daun ekor naga (Rhaphidophora
pinnata (L.f.) Schott) mengandung kalium, natrium, kalsium, besi dan
magnesium.
Hasil penetapan kadar dengan menggunakan spektrofotometer serapan
atom menunjukkan bahwa kadar kalium, natrium, kalsium, besi dan magnesium
dari daun ekor naga masing-masing adalah 847,9111 ± 3,3573 mg/100g kalium
(K), 8,2117 ± 0,1442 mg/100g natrium (Na), 474,6638 ± 4,5448 mg/100g kalsium
(Ca), 1,7975 ± 0,0357 mg/100g besi (Fe) dan 69,5370 ± 4,0158 mg/100g
magnesium (Mg).
5.2 Saran
Disarankan kepada masyarakat untuk tidak ragu menggunakan daun ekor
naga sebagai alternatif pengobatan (pencegahan beberapa penyakit), seperti:
antipireutik (penurun panas), antihipertensi (penurun tekanan darah) dengan efek
samping polyuri (banyak buang air kecil), dan sebagai sumber untuk mencukupi
kebutuhan mineral. Dan kepada peneliti selanjutnya, disarankan untuk
menetapkan kadar mineral tersebut, khususnya kalium dan natrium pada air
DAFTAR PUSTAKA
Almatsier, S. (2004). Prinsip Dasar Ilmu Gizi. Jakarta: PT. Gramedia Pustaka Utama. Hal. 228, 229-231, 233, 234-236, 242, 246, 247, 249, 253, 255.
Arthur, C. (1981). An Intergrated System Of Classifacation Of Flowering Plants. Columbia University Press: Hal. 477.
Bender, G.T. (1987). Principal of Chemical Instrumentation. Philadelphia: W.B.Sounders Company. Hal. 98.
Budiyanto, M. A. K. (2001). Dasar-dasar Ilmu Gizi. Edisi Kedua. Cetakan I. Malang: UMM-Press. Hal. 59.
Burkill, I. H. (1935). A Dictionary Of The Economic Products Of The Malay
Peninsula. Volume II. London. Hal. 889.
Ditjen POM. (1979). Farmakope Indonesia Edisi III. Jakarta: Departemen Kesehatan RI. Hal. 744, 748.
Ermer, J. (2005). Method Validation in Pharmaceutical Analysis. Weinheim: Wiley-Vch Verlag GmbH & Co. KGaA. Hal. 171.
Garfield, F.M. (1991). Quality Assurance Principles for Analytical Laboratories. USA: AOAC international. Hal. 71.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara
Perhitungannya. Review Artikel. Majalah Ilmu Kefarmasian. Vol.1 No.3.
Hal. 117-119, 121, 122, 127, 128, 130.
Helrich, K. (1990). Official Methods of the Association of Official Analytical
Chemist. Edisi kelimabelas. USA: AOAC international. Hal. 42.
Heyne, K. (1987). Tumbuhan Berguna Indonesia. Jilid I. Cetakan I. Penerjemah : Badan Litbang Kehutanan. Jakarta: Penerbit Yayasan Sarana Wanajaya. Hal. 493.
Khopkar, S.M. (1990). Konsep Dasar Kimia Analitik. Penerjemah: Saptorahardjo, A. Jakarta: UI-Press. Hal. 283.
Lemmens and N. Bunyapraphatsara. (2003). Plant Resources Of Sou