STUDI TAHAP PERKEMBANGAN KUNCUP BUNGA,
MIKROSPORA DAN OVUL
Dianthus chinensis
L.
Abstrak
Stadia perkembangan mikrospora dan ovul yang tepat sangat menentukan keberhasilan mendapat tanaman haploid melalui androgenesis dan ginogenesis. Tujuan penelitian ialah mendapatkan penanda morfologi bunga dan stadia yang tepat dari perkembangan mikrospora dan ovu. Studi biologi bunga meliputi studi tahap perkembangan bunga, penghitungan jumlah dan ukuran mikrospora, rasio tahap perkembangan mikrospora, viabilitas mikrospora dan seleksi stadia mikrospora dan ovul yang tepat untuk inisiasi kultur mikrospora dan ovul.. Hasil penelitian menunjukkan bahwa ukuran kuncup bunga dan warna antera merupakan indikator waktu dilakukan pengambilan donor eksplan. D. chinensis “Dchi-11” memiliki jumlah dan viabilitas mikrospora tertinggi (60,36%). Tahap perkembangan mikrospora dengan persentaselate-uninucleate tertinggi (44,64%) pada saat ukuran kuncup bunga T2 (ukuran kuncup antara 1,31 – 1,50 cm, warna antera putih, umur 5 hari, pencoklatan antera paling rendah). Tahap perkembangan ovul T7 (ukuran kuncup antara 1,81 – 2.00 cm, panjang petal 30% lebih panjang dari panjang sepal, umur 10 hari) merupakan tahap yang tepat untuk induksi kultur ovul berdasarkan persentase pembentukan kalus (59,375%) dengan tipe kalus remah dan agak remah dan berwarna hijau.
Kata kunci: indikator morfologi, viabilitas mikrospora, tahap perkembangan, mikrospora, ovul.
STUDY OF FLOWER BUD DEVELOPMENT, MICROSPORE
AND OVULE OF
Dianthus chinensis
L.
Abstract
The study of anther or microspore and ovule critical development were important to determine the successfull of obtaining haploid plants through androgenesis and gynogenesis. The aim of the research was to determine mophological indicator of bud, dominan uninucleate microspore and the right ovule development stage for. Flower biological study comprised study of flower development, the number and size of microspore, ratio of microspore development stage, microspore viability and selection of the right microspore and ovule stage for culture initiation of microspore and ovul. The research showed that bud size and anther color are indicators for isolating donor explants. D. chinensis “Dchi-11” has the highest microspore number and viability (60.36%). Bud size of T2 stage (44,64%, 1.31 – 1.50 cm, white anther color, 5 days old, and the lowest browning anther) produce the highest late uninucleate microspore. Ovule development of T7 (1.81 – 2,00 cm, the length of petals are 30% longer than sepals length, 10 days old) was the right stage for ovule culture based on percentage of callus formation ((59,375%) and friable green callus.
Key words: morphology indicator, microspore viability, flower bud development, microspore, ovule.
Pendahuluan
Aplikasi teknologi kultur antera dan ovul pada tanaman anyelir masih jarang, oleh karena itu pengembangan penelitian ini dimulai dari studi tanaman donor, kajian khusus mengenai biologi bunga dan perkembangannya (morfologi maupun mikroskopi), studi perkembangan mikrospora, metode kultur; pemilihan pra-perlakuan yang optimal; pengembangan media inisiasi, regenerasi dan pemasakan embrio; analisis ploidi; penggandaan kromosom yang menjadi bagian penting dalam pengembangan teknologi haploid pada anyelir. Dari berbagai kajian mendasar tersebut pada akhir studi diharapkan dapat ditemukan teknologi haploid anyelir yang efektif, efisien, mudah diproduksi (reproducible) dan mudah diulang (repeatable).
Induksi tanaman haploid melalui kultur in vitro antera, ovul dan ovari yang tidak diserbuki menjadi pendekatan yang biasa dilakukan untuk mendapatkan tanaman haploid pada beberapa tanaman. Pada beberapa spesies tanaman, efisiensi induksi haploid sangat bervariasi dan terdapat banyak kendala yang dapat mengurangi keberhasilan protokol yang telah dihasilkan (Musialet al. 2005). Tahap perkembangan eksplan merupakan salah satu faktor penting yang mempengaruhi induksi haploid (Yang & Zhou 1982). Namun studi yang berkaitan dengan tahap perkembangan eksplan sedikit dipublikasi. Pada androgenesis tahap perkembangan serbuk sarinya mudah diamati, sedangkan pada ginogenik tahap perkembangan dalam kantong embrio lebih sulit diamati. Hasil-hasil penelitian yang telah dilakukan pada umumnya tahap perkembangan megagametofit yang digunakan untuk induksi ginogenik ialah pada tahap kantong embrio masak (Musial et al.2005). Namun menurut Bhojwani dan Thomas (2001) pada tahap kantong embrio muda lebih sesuai untuk diinduksi karena sel gamet betina melanjutkan perkembangannya sampai sel-sel yang ada dalam kantong embrio telah berdiferensiasi.
Pada tahap awal studi ini diarahkan untuk mengungkap perkembangan kuncup bunga secara morfologi terkait dengan penampilan morfologi bunga (ukuran panjang, lebar diameter bunga, dan waktu bunga mekar), jumlah serbuk sari, ukuran dan viabilitas serbuk sari, rasio tahap perkembangan serbuk sari serta anatomi ovul. Aktivitas tahap ini memiliki tujuan utama untuk menyediakan data dasar terkait dengan pemanfaatannya dalam pengembangan kultur antera dan ovul anyelir.
Tahap perkembangan polen merupakan faktor yang penting untuk androgenesis in vitro, maka pemilihan tanaman donor untuk studi ini sangat penting. Berkenaan dengan hal tersebut korelasi antara tahap perkembangan polen dan morfologi kuncup (panjang petal, munculnya petal dari kelopak dan lain-lain), bervariasi antara spesies dan umur tanaman donor. Antera yang paling responsif biasanya pada tahap perkembangan serbuk sari uninukleat yaitu pada tahap antara tetrad dan mitosis polen pertama (Heberle-Bors 1985). Sementara pada ginogenesis meskipun gametofit betina melanjutkan perkembangannya selama kultur in vitro, perkembangan tahap awal kantong embrio sampai tahap masak perlu diuji untuk melihat potensi perkembangan masing-masing tahap perkembangannya. Tujuan penelitian adalah menentukan indikator morfologi dari tahap perkembangan kuncup, stadia perkembangan serbuk sari uninukleat dominan serta stadia ovul yang tepat untuk digunakan dalam kultur antera, ovul dan pseudofertilisasi
Bahan dan Metode
Penelitian dilakukan di Laboratorium Kultur Jaringan dan Rumah Sere Anyelir, Balai Penelitian Tanaman Hias Segunung, Laboratorium Mikroteknik, Departemen Agronomi dan Hortikultura, Institut Pertanian Bogor, dan Laboratorium Anatomi dan Sitologi Puslitbang Biologi LIPI, Cibonong mulai April 2009 – Maret 2010. Bahan tanaman yang digunakan ialah kuncup dari lima genotipe Dianthus chinensis Dchi-11, Dchi-12, Dchi-13, Dchi-14 dan Dchi-15 (Gambar 2).
Gambar 2. Morfologi bunga lima genotype Dianthus chinensis (A) Dchi-11, (B) Dchi-12, (C) Dchi-13, (D) Dchi-14 dan (E) Dchi-15
Perkembangan kuncup bunga
Studi biologi ini difokuskan untuk melihat perkembangan bunga sejak kuncup bunga terlihat hingga bunga mekar sempurna. Berbagai peubah yang menyangkut ukuran kuncup bunga: panjang, lebar, diameter dan pengamatan
antera, serbuk sari dan ovul dari tanaman donor, diamati dan diukur. Studi biologi ini melibatkan aplikasi anatomi sederhana (baik irisan lintang maupun membujur) dan pewarnaan (haematoxilin, fuchsin, Metilen-blue, orcein dan aceto-carmin) untuk membantu memperjelas pengamatan. Studi ini akan dibandingkan langsung dengan studi tahap perkembangan serbuk sari dan ovul untuk menentukan tahap yang tepat untuk pengambilan tanaman donor.
Perkembangan antera dan serbuk sari
Penghitungan jumlah dan ukuran serbuk sari
Untuk penghitungan jumlah serbuk sari, 2-3 antera dipanen, seluruh serbuk sarinya dikeluarkan dari kotak spora, kemudian dilarutkan dalam 1 ml media cair embriogenesis. Suspensi serbuk sari dibuat sehomogen mungkin melalui pengocokan menggunakan vortex. Setelah dirasa cukup homogen, sampel dipipet dan diletakkan di atas haemacytometer, dan ditutup dengan gelas penutup, diamati di bawah mikroskop. Serbuk sari dihitung menggunakan rumus A = (n x B)/N (Godini 1979), n : jumlah serbuk sari dalam setiap kotak, B = 10.000/jumlah kotak yang dihitung dan N = jumlah antera yang digunakan. Ukuran serbuk sari diukur menggunakan mikrometer okuler yang telah dikalibrasi. Pengukuran dilakukan sebanyak mungkin mewakili jumlah serbuk sari secara keseluruhan. Hasil penghitungan dan pengukuran selanjutnya ditampilkan dalam bentuk data rata-rata dan standar deviasinya untuk setiap tanaman donor.
Studi rasio tahap perkembangan serbuk sari
Tahap perkembangan serbuk sari diamati melalui pewarnaan inti sel menggunakan 4,6-diamidino-2-phenylindole (DAPI) (Custers et al, 2001) yang dilakukan pada Dianthus chinensis. Sebanyak 25 µl larutan serbuk sari dimasukkan dalam Eppendorf kecil kemudian disentrifugasi pada 4000 rpm selama 2-4 menit. Supernatan dipipet hingga hanya tersisa pelet dan sesedikit mungkin supernatan ditambah larutan kerja DAPI dengan konsentrasi 1 µg/ml, dan diaduk merata menggunakan ujung pipet. Campuran serbuk sari dan larutan DAPI dipipet dan letakkan di atas kaca obyek ditutup dengan gelas penutup, dan dibiarkan minimal 4 jam (1 malam) pada suhu 4ºC. Setelah inkubasi, serbuk sari diamati di bawah mikroskop UV pada perbesaran 200 dan 400x. Tahap-tahap perkembangan serbuk sari dihitung jumlahnya dan dibagi dengan jumlah seluruh
sel yang diamati dikalikan 100 untuk mengetahui persentasenya. Rasio perkembangan dihitung dengan membandingkan frekuensi perkembangan serbuk sari early uninucleate,mid uninucleate, late uninucleate, early binucleate dan binucleate yang ada dalam satu bidang pandang pengamatan. Frekuensi setiap tahap perkembangan serbuk sari dihitung dan dibagi total serbuk sari yang diamati pada tahap kuncup yang sama. Pengamatan dilakukan minimal pada 5 bidang pandang dan diulang minimal 5 kali untuk mendapatkan data yang valid.
Uji viabilitas serbuk sari
Pengujian viabilitas atau vitalitas sel serbuk sari atau polen menggunakan larutan kerja 10 µM fluorescein diacetate (FDA) (Custers et al. 2001). Larutan serbuk sari (90 µl) ditempatkan dalam Eppendorf yang telah dibungkus dengan aluminium ditambah 10 µl larutan stok FDA ke dalam larutan kultur serbuk sari dan diaduk rata, ditempatkan dalam gelap 10 menit. Sebanyak 50-100µl kultur serbuk sari yang telah diberi perlakuan FDA dipipet dan ditetes di atas kaca obyek dan ditutup dengan kaca penutup, dan segera dilakukan pengamatan di bawah mikroskop fluoresen. Jumlah serbuk sari yang memendarkan warna hijau diamati dan dihitung. Pengamatan diulang minimal pada 5 bidang pandang pengamatan. Viabilitas atau vitalitas sel (%) dihitung dengan membagi jumlah total sel yang fluoresen dengan jumlah total sel yang diamati pada satu bidang pandang dikalikan dengan 100%.
Seleksi tahap perkembangan kuncup bunga pada berbagai media inisiasi double layer untuk kultur antera
Percobaan faktorial terdiri atas dua faktor, disusun dalam Rancangan Acak Kelompok. Faktor pertama ialah tahap perkembangan kuncup bunga dan faktor ke dua ialah media induksi. Empat tahap perkembangan kuncup bunga yang diuji dalam kegiatan ini yaitu (1) kuncup 1 (T2), dominan mikrospora berada dalam kondisi tetrad, (2) kuncup 2 (T3), dominan mikrospora berada dalam tahap early dan middle uninucleate, (3) kuncup 3 (T4), dominan mikrospora berada pada tahap late uninucleate, dan (4) kuncup 4 (T5), dominan mikrospora berada pada tahap early binucleate. Masing-masing tahap ditanam dalam lima media yang diuji responnya dalam induksi pembentukan kalus dan/atau embrio adalah (1) M1 (Winartoet al. 2011), (2) M2 (Nontaswatsriet al. 2007), (3) M3 (Mosqueraet al.
1999), (4) M4 (Satoet al,2000) dan (5) M5 (Fuet al. 2008). Setiap unit perlakuan diulang 10 kali. Setiap ulangan terdiri atas 1 cawan petri yang berisi 10 antera.
Isolasi antera dilakukan dengan cara membersihkan kuncup bunga dengan kapas yang dibasahi alkohol 70%, kemudian dilewatkan di atas api sekilas. Antera diisolasi dengan cara membuka kuncup bunga, kemudian antera dan filament dipisahkan, dan ditanam dalam media induksi. Metode kultur sebar mikrospora antera (anther shed microspore culture) pada media double layer digunakan dalam penelitian ini. Prosedur penelitian menggunakan prosedur standard dari Dolcet-Sanjuanet al. 1997.Media embriogenesis yang digunakan disusun dengan sistem double layer yang tersusun atas dua lapisan yaitu lapisan padat di bawah dan cair di atas. Media padat ditambahkan 0,5% arang aktif , dengan pH 5,8. Pengamatan dilakukan terhadap persentase pencoklatan dan kontaminasi.
Perkembangan ovari atau ovul
Pembuatan sayatan kuncup bunga D. chinensis
Bahan difiksasi di dalam larutan FAA (formali : asam asetat glasial : alkohol 70% (v/v) = 5 :5 :90) selama 24 jam. Selanjutnya didehidrasi secara bertahap menggunakan alkohol 50% – 100% masing-masing selama 30 menit. Kemudian dilakukan dealkoholisasi secara bertahap menggunakan campuran alkohol-xylol, dilanjutkan dengan xylol murni 1 dan 2 masing-masing 30 menit. Parafin diinfiltrasi sedikit demi sedikit sampai jenuh dan disimpan dalam oven dengan suhu 60oC selama 3 jam. Parafin diganti dengan parafin baru dan disimpan dalam oven dengan suhu 50-60oC selama 3 hari. Sampel dimasukkan dalam parafin, kemudian blok sampel disayat dengan ketebalan 15-17 µm menggunakan mikrotom putan (Yamato RV-240). Sayatan parafin yang berrbentuk pita di rekatkan pada gelas objek yang telah diolesi dengan larutan albumin-gliserin dan dikeringkan di atas hot plate dengan suhu 40oC selama 3-5 jam. Sampel diwarnai dengan safranin 2% (b/v) dan fastgreen 0,5% (b/v).
Seleksi tahap perkembangan kuncup bunga untuk kultur ovula tau ovari
Percobaan merupakan faktor tunggal yang disusun dengan Rancangan Acak Kelompok. Tiga tahap perkembangan kuncup bunga yang diuji dalam kegiatan ini yaitu (1) kuncup bunga tahap T5, (2) kuncup bunga tahap T7, (3) kuncup bunga tahap T9. Kuncup bunga disimpan pada suhu 4 oC selama 1 hari
sebelum diisolasi. Masing-masing tahap tersebut ditanam dalam media MS + 4,52 µM 2,4-D+ 4.44 µM BAP + 20 g L-1sukrosa (Mosquera et al. 1999), yang diuji responnya dalam induksi pembentukan kalus. Setiap unit perlakuan diulang 8 kali. Setiap ulangan terdiri atas 1 cawan petri yang berisi 4 potongan ovul. Semua kultur diinkubasi pada kondisi gelap ± selama 7 hari pada suhu 4 oC dilanjutkan dengan inkubasi terang pada suhu 25oC dengan lama penyinaran 16 jam di bawah lampu fluoresen (13 µmol.m-2.s-1) hingga kalus terbentuk. Peubah yang diamati dalam percobaan ini ialah persentase eksplan membentuk kalus (%), dan pengamatan kalus secara visual. Pengamatan dilakukan 1 bulan setelah inisiasi kultur.
Analisis statistik
Data pengamatan yang diperoleh dari hasil seleksi tahap perkembangan kuncup bunga untuk kultur ovul atau ovari, dianalisis menggunakan analisis ragam (ANOVA) dengan program SAS Release window 9.1. Data dalam bentuk persen ditransformasi ke dalam Arcsin. Untuk nilai 0% sebelum ditransformasi diganti dengan 1/4n, di mana n adalah jumlah satuan percobaan dari data persentase yang diperoleh. Jika terdapat perbedaan nilai rata-rata perlakuan maka dilakukan uji lanjutan menggunakan uji jarak berganda Duncan pada taraf kepercayaan 5%.
Hasil
Perkembangan kuncup bunga
Inisiasi bunga ditandai dengan munculnya daun-daun kecil pada ujung tunas. Hari ke empat setelah inisiasi bunga ditentukan sebagai tahap perkembangan kuncup bunga T1. Pada tahap tersebut mikrospora didominasi oleh pollen mother cell (PMC) dan tetrad. Hari ke lima setelah inisiasi bunga ditentukan sebagai tahap perkembangan kuncup bunga T2 yang didominasi oleh mikrospora mid uninukleat. Tahap T3 yang didominasi oleh mikrospora late uninukleat pada hari ke enam setelah inisiasi bunga dan seterusnya sampai bunga mekar sebagai tahap T10 pada hari ke 13 setelah inisiasi kuncup bunga.
Hasil studi ini diketahui bahwa dari lima genotipe Dianthus chinensisyang digunakan memiliki kecepatan antesis yang. Pada tahap T3 bagian pucuk kuncup sedikit terbuka, dan pada tahap T4 ujung petal yang berwarna putih mulai
kelihatan, dan tahap T5 ujung petal berubah warna menjadi pink. Tahap selanjutnya warna petal berubah menjadi kemerahan (Gambar 3). Ukuran panjang kuncup bunga setiap genotipe berbeda-beda. Panjang kuncup D. chinensis merupakan ukuran panjang kelopak, dan tidak berubah sampai bunga mekar. Pada tahap T2 berkisar 1,295 cm pada Dchi-13 sampai 1,535 cm pada Dchi-15 (Lampiran 1).
Gambar 3. Perkembangan kuncup bunga, ovari dan antera Dianthus chinensis Dchi-11. T1 sampai T10 adalah 4 sampai 13 hari setelah inisiasi bunga. Bar = 0,5 cm
Perkembangan antera dan serbuk Sari
Pengamatan antera dan serbuk sari
Masa reseptif putik dan kemasakan polen D. chinenesis tidak terjadi secara bersamaan. Serbuk sari D. chinenesis masak lebih dahulu dibandingkan putik. Antera terbuka dan mengeluarkan polen pada umur 14 – 16 hari setelah inisiasi bunga. Pengamatan antera dilakukan dari T1 sampai T7. Pengamatan tahap terakhir pada tahap T7 karena pada tahap tersebut 100% antera dalam satu kuncup sudah berwarna ungu tua.
Dari hasil pengamatan pada jumlah antera diketahui bahwa lima genotipe dari kultivar yang berbeda memiliki jumlah antera yang sama yaitu 10. Jumlah antera 12 ditemukan pada genotipe Dchi-14, tetapi jumlah antera 12 ini sangat jarang ditemukan. Pada tahap perkembangan bunga T1-T2 antera berwarna putih. Kemudian pada tahap pertumbuhan lanjut warna antera berubah sesuai dengan warna petal. Perubahan warna antera dimulai pada tahap T3, 6 hari setelah munculnya kuncup bunga (Gambar 3 dan Tabel 1).
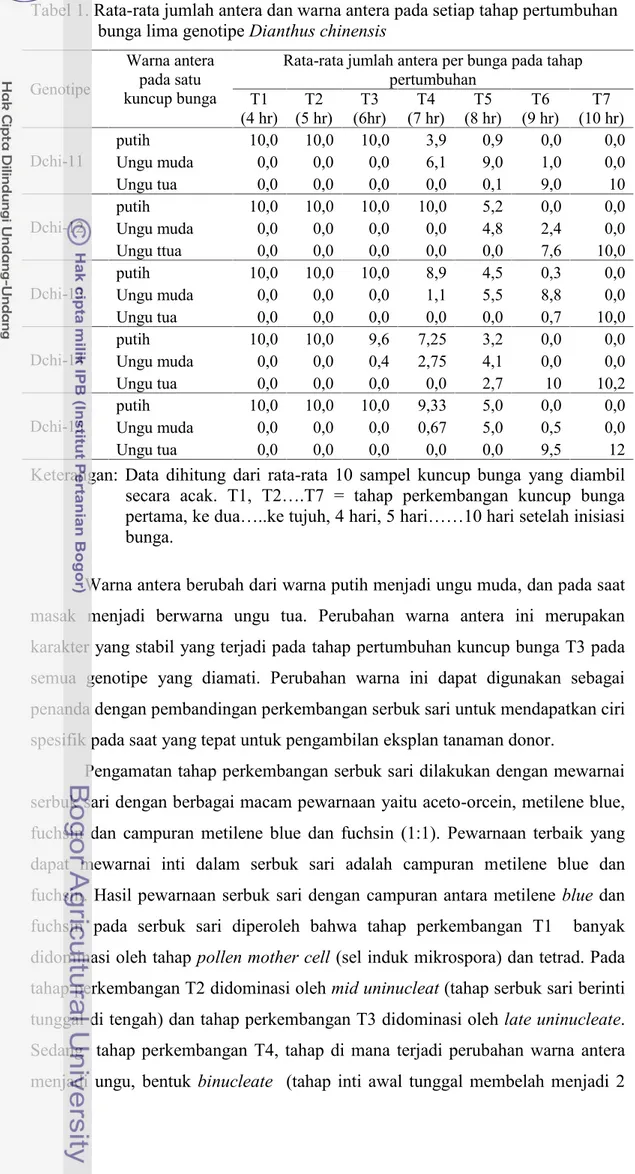
Tabel 1. Rata-rata jumlah antera dan warna antera pada setiap tahap pertumbuhan bunga lima genotipeDianthus chinensis
Genotipe
Warna antera pada satu kuncup bunga
Rata-rata jumlah antera per bunga pada tahap pertumbuhan
T1
(4 hr) (5 hr)T2 (6hr)T3 (7 hr)T4 (8 hr)T5 (9 hr)T6 (10 hr)T7 Dchi-11 putihUngu muda 10,00,0 10,00,0 10,00,0 3,96,1 0,99,0 1,00,0 0,00,0
Ungu tua 0,0 0,0 0,0 0,0 0,1 9,0 10
Dchi-12 putihUngu muda 10,00,0 10,00,0 10,00,0 10,00,0 5,24,8 2,40,0 0,00,0
Ungu ttua 0,0 0,0 0,0 0,0 0,0 7,6 10,0
Dchi-13 putihUngu muda 10,00,0 10,00,0 10,00,0 8,91,1 4,55,5 8,80,3 0,00,0
Ungu tua 0,0 0,0 0,0 0,0 0,0 0,7 10,0
Dchi-14 putihUngu muda 10,00,0 10,00,0 9,60,4 7,252,75 3,24,1 0,00,0 0,00,0
Ungu tua 0,0 0,0 0,0 0,0 2,7 10 10,2
Dchi-15 putihUngu muda 10,00,0 10,00,0 10,00,0 9,330,67 5,05,0 0,50,0 0,00,0
Ungu tua 0,0 0,0 0,0 0,0 0,0 9,5 12
Keterangan: Data dihitung dari rata-rata 10 sampel kuncup bunga yang diambil secara acak. T1, T2….T7 = tahap perkembangan kuncup bunga pertama, ke dua…..ke tujuh, 4 hari, 5 hari……10 hari setelah inisiasi bunga.
Warna antera berubah dari warna putih menjadi ungu muda, dan pada saat masak menjadi berwarna ungu tua. Perubahan warna antera ini merupakan karakter yang stabil yang terjadi pada tahap pertumbuhan kuncup bunga T3 pada semua genotipe yang diamati. Perubahan warna ini dapat digunakan sebagai penanda dengan pembandingan perkembangan serbuk sari untuk mendapatkan ciri spesifik pada saat yang tepat untuk pengambilan eksplan tanaman donor.
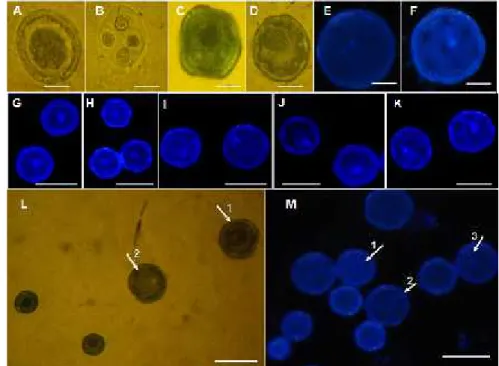
Pengamatan tahap perkembangan serbuk sari dilakukan dengan mewarnai serbuk sari dengan berbagai macam pewarnaan yaitu aceto-orcein, metilene blue, fuchsin dan campuran metilene blue dan fuchsin (1:1). Pewarnaan terbaik yang dapat mewarnai inti dalam serbuk sari adalah campuran metilene blue dan fuchsin. Hasil pewarnaan serbuk sari dengan campuran antara metilene blue dan fuchsin pada serbuk sari diperoleh bahwa tahap perkembangan T1 banyak didominasi oleh tahap pollen mother cell (sel induk mikrospora) dan tetrad. Pada tahap perkembangan T2 didominasi oleh mid uninucleat(tahap serbuk sari berinti tunggal di tengah) dan tahap perkembangan T3 didominasi oleh late uninucleate. Sedang tahap perkembangan T4, tahap di mana terjadi perubahan warna antera menjadi ungu, bentuk binucleate (tahap inti awal tunggal membelah menjadi 2
yaitu inti generatif dan vegetatif) mulai muncul (Gambar 4A-D). Tahap inti binucleateini hanya dapat dilihat dengan pewarnaan DAPI (Gambar 4F) dan tidak dapat dilihat dengan pewarnaan campuran metilene blue dan fuchsin (Gambar 4L1).
Gambar 4. Tahap perkembangan serbuk sari. Pewarnaan mikrospora dengan Fuchsin + Metilen-blue (A-D dan L) dan DAPI (E-K, M). (A) PMC (pollen mother cell); (B) tetrad; (C, G) early uninucleate; (H) mid uninucleate; (D, I) late uninucleate; (E) serbuk sari dengan dua inti identik (F) serbuk sari tahap binucleate dengan inti vegetatif (warna pudar) dan inti generatif (warna terang). (L, M) Serbuk sari dengan ukuran yang berbeda: (1) serbuk sari berinti 1, (2) serbuk sari tanpa inti, (3) serbuk sari berinti 2, (A – D) bar = 10 µm; (G-K) bar = 15 µm (L-M) bar = 25 µm
Jumlah serbuk sari dan ukurannya
Hasil pengamatan yang dilakukan pada lima genotipe menunjukkan bahwa rata-rata jumlah serbuk sari per antera berkisar 4000 – 64000 (Tabel 2). Jumlah serbuk sari yang terkandung dalam antera akan berpengaruh terhadap jumlah antera yang harus diisolasi, dan terkait dengan kepadatan antera dalam kultur. Kepadatan antera memiliki pengaruh fisik dan biokimia pada pembentukan embrio. Pada kepadatan yang rendah antera akan memisah pada media, sedangkan pada kepadatan yang tinggi akan cenderung mengelompok.
Hasil pengamatan pada dua sampel genotipe (Dchi-11 dan Dchi-14) diketahui terdapat tiga macam kisaran ukuran serbuk sari yaitu besar dengan
ukuran >20 µm, sedang dengan ukuran 15 – 20 µm, dan ukuran kecil <15 µm. Semua genotipe yang diamati memiliki ukuran serbuk sari yang bervariasi.
Tabel 2. Jumlah serbuk sari per antera lima genotipeDianthus chinensis Genotipe Jumlah serbuk sari per antera
kisaran Rata-rata* Dchi-11 10000 - 64000 30400 ± 16297 Dchi-12 4000 - 30000 21400 ± 9143 Dchi-13 4000 - 40000 21200 ± 10840 Dchi-14 4000 - 32000 23200 ± 10799 Dchi-15 6000 - 30000 20400 ± 8044
Keterangan: Data dihitung dari rata-rata 10 kali isolasi pada 5 bidang pengamatan. *Rata-rata ± standard deviasi
Rasio tahap perkembangan serbuk sari
Seleksi tahap perkembangan serbuk sari didasarkan penanda morfologi dan antera. Panjang sepal, dan petal kuncup bunga serta morfologi kuncup sangat berguna untuk menentukan tahap awal sebagai indikator seleksi kuncup bunga yang tepat. Hasil pengamatan pada serbuk sari tahap T2 merupakan tahap dengan serbuk sari late uninukleat tertinggi (44,64%), dan tidak terjadi perubahan warna antera dari putih menjadi ungu (Tabel 3). Tahap T2 ini bentuk kuncup masih tertutup rapat, dan akan mulai terbuka pada tahap T3 (Gambar 5A). Tahap T3 mulai terjadi perubahan warna antera yang didominasi serbuk sari pada tahap early binukleat (Gambar 3, Tabel 3). Penggunaan kriteria warna pada antera merupakan kriteria yang paling efektif sebagai indikator seleksi bahan dasar yang lebih sesuai dibandingkan dengan ukuran kuncup, karena adanya keragaman yang disebabkan oleh pengaruh lingkungan.
Gambar 5. Karakteristik kuncup bunga dan antera pada 5 tahap perkembangan bungaDianthus chinensis. (A) ujung kuncup tahap T1-T2 belum terbuka, tahap T3 mulai terbuka, tahap T4 petal terlihat 30% dan T5 terjadi perubahan warna petal (B)Kuncup tahap T1-T2 warna petal putih, T3 petal sedikit ungu (C)Warna antera dalam satu bunga putih tahap T1-T2, warna antera dalam satu bunga 30% putih, 30% ungu muda dan 40% ungu tua pada T3, warna antera dalam satu bunga > 50% ungu tua pada tahap T4, dan semua antera berwarna ungu tua pada tahap T5.
A B C
ukuran >20 µm, sedang dengan ukuran 15 – 20 µm, dan ukuran kecil <15 µm. Semua genotipe yang diamati memiliki ukuran serbuk sari yang bervariasi.
Tabel 2. Jumlah serbuk sari per antera lima genotipeDianthus chinensis Genotipe Jumlah serbuk sari per antera
kisaran Rata-rata* Dchi-11 10000 - 64000 30400 ± 16297 Dchi-12 4000 - 30000 21400 ± 9143 Dchi-13 4000 - 40000 21200 ± 10840 Dchi-14 4000 - 32000 23200 ± 10799 Dchi-15 6000 - 30000 20400 ± 8044
Keterangan: Data dihitung dari rata-rata 10 kali isolasi pada 5 bidang pengamatan. *Rata-rata ± standard deviasi
Rasio tahap perkembangan serbuk sari
Seleksi tahap perkembangan serbuk sari didasarkan penanda morfologi dan antera. Panjang sepal, dan petal kuncup bunga serta morfologi kuncup sangat berguna untuk menentukan tahap awal sebagai indikator seleksi kuncup bunga yang tepat. Hasil pengamatan pada serbuk sari tahap T2 merupakan tahap dengan serbuk sarilate uninukleat tertinggi (44,64%), dan tidak terjadi perubahan warna antera dari putih menjadi ungu (Tabel 3). Tahap T2 ini bentuk kuncup masih tertutup rapat, dan akan mulai terbuka pada tahap T3 (Gambar 5A). Tahap T3 mulai terjadi perubahan warna antera yang didominasi serbuk sari pada tahap early binukleat (Gambar 3, Tabel 3). Penggunaan kriteria warna pada antera merupakan kriteria yang paling efektif sebagai indikator seleksi bahan dasar yang lebih sesuai dibandingkan dengan ukuran kuncup, karena adanya keragaman yang disebabkan oleh pengaruh lingkungan.
Gambar 5. Karakteristik kuncup bunga dan antera pada 5 tahap perkembangan bungaDianthus chinensis. (A) ujung kuncup tahap T1-T2 belum terbuka, tahap T3 mulai terbuka, tahap T4 petal terlihat 30% dan T5 terjadi perubahan warna petal (B)Kuncup tahap T1-T2 warna petal putih, T3 petal sedikit ungu (C)Warna antera dalam satu bunga putih tahap T1-T2, warna antera dalam satu bunga 30% putih, 30% ungu muda dan 40% ungu tua pada T3, warna antera dalam satu bunga > 50% ungu tua pada tahap T4, dan semua antera berwarna ungu tua pada tahap T5.
A B C
ukuran >20 µm, sedang dengan ukuran 15 – 20 µm, dan ukuran kecil <15 µm. Semua genotipe yang diamati memiliki ukuran serbuk sari yang bervariasi.
Tabel 2. Jumlah serbuk sari per antera lima genotipeDianthus chinensis Genotipe Jumlah serbuk sari per antera
kisaran Rata-rata* Dchi-11 10000 - 64000 30400 ± 16297 Dchi-12 4000 - 30000 21400 ± 9143 Dchi-13 4000 - 40000 21200 ± 10840 Dchi-14 4000 - 32000 23200 ± 10799 Dchi-15 6000 - 30000 20400 ± 8044
Keterangan: Data dihitung dari rata-rata 10 kali isolasi pada 5 bidang pengamatan. *Rata-rata ± standard deviasi
Rasio tahap perkembangan serbuk sari
Seleksi tahap perkembangan serbuk sari didasarkan penanda morfologi dan antera. Panjang sepal, dan petal kuncup bunga serta morfologi kuncup sangat berguna untuk menentukan tahap awal sebagai indikator seleksi kuncup bunga yang tepat. Hasil pengamatan pada serbuk sari tahap T2 merupakan tahap dengan serbuk sarilate uninukleat tertinggi (44,64%), dan tidak terjadi perubahan warna antera dari putih menjadi ungu (Tabel 3). Tahap T2 ini bentuk kuncup masih tertutup rapat, dan akan mulai terbuka pada tahap T3 (Gambar 5A). Tahap T3 mulai terjadi perubahan warna antera yang didominasi serbuk sari pada tahap early binukleat (Gambar 3, Tabel 3). Penggunaan kriteria warna pada antera merupakan kriteria yang paling efektif sebagai indikator seleksi bahan dasar yang lebih sesuai dibandingkan dengan ukuran kuncup, karena adanya keragaman yang disebabkan oleh pengaruh lingkungan.
Gambar 5. Karakteristik kuncup bunga dan antera pada 5 tahap perkembangan bungaDianthus chinensis. (A) ujung kuncup tahap T1-T2 belum terbuka, tahap T3 mulai terbuka, tahap T4 petal terlihat 30% dan T5 terjadi perubahan warna petal (B)Kuncup tahap T1-T2 warna petal putih, T3 petal sedikit ungu (C)Warna antera dalam satu bunga putih tahap T1-T2, warna antera dalam satu bunga 30% putih, 30% ungu muda dan 40% ungu tua pada T3, warna antera dalam satu bunga > 50% ungu tua pada tahap T4, dan semua antera berwarna ungu tua pada tahap T5.
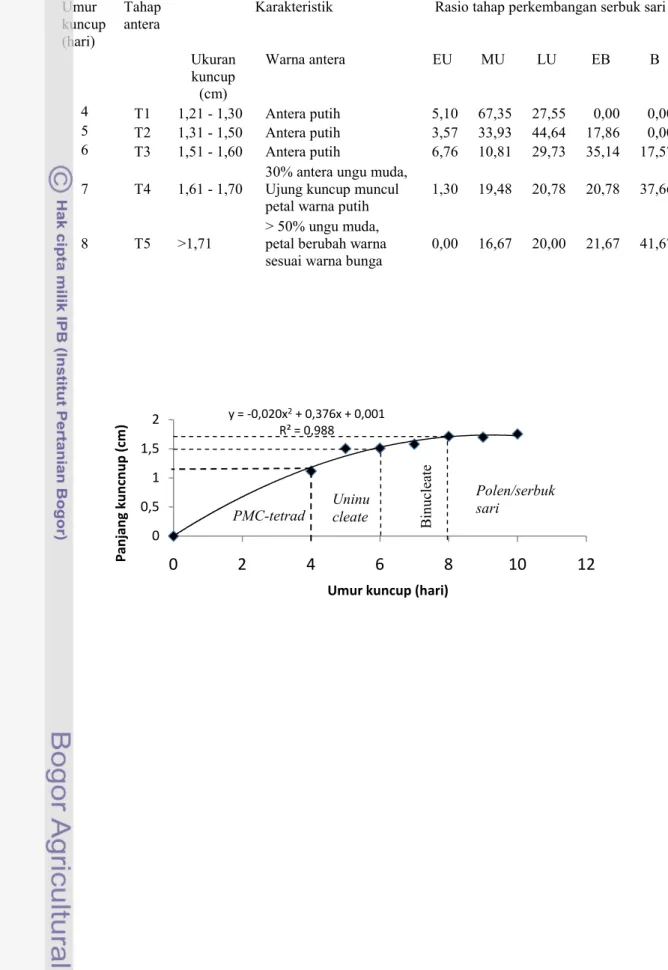
Tabel 3. Rasio tahap perkembangan serbuk sariD. chinensis Dchi-11 berdasarkan ukuran kuncup bunga dan warna antera
Umur kuncup (hari)
Tahap
antera Karakteristik Rasio tahap perkembangan serbuk sari Ukuran kuncup (cm) Warna antera EU MU LU EB B 4 T1 1,21 - 1,30 Antera putih 5,10 67,35 27,55 0,00 0,00 5 T2 1,31 - 1,50 Antera putih 3,57 33,93 44,64 17,86 0,00 6 T3 1,51 - 1,60 Antera putih 6,76 10,81 29,73 35,14 17,57 7 T4 1,61 - 1,70 30% antera ungu muda,Ujung kuncup muncul
petal warna putih 1,30 19,48 20,78 20,78 37,66 8 T5 >1,71 > 50% ungu muda,petal berubah warna
sesuai warna bunga 0,00 16,67 20,00 21,67 41,67
Keterangan: Data diambil dari rata-rata minimal 3 x isolasi pada 5 bidang pengamatan. T1= 4 hari setelah inisiasi bunga, T2 = bunga mekar 5 hari setelah inisiasi bunga, dst.T= tahap perkembangan. EU=early uninucleate, MU=mid uninucleate, LU=late uninucleate, EB=early binucleate,B =binucleate
Gambar 6. Hubungan antara panjang kuncup dengan umur kuncup dan tahap perkembangan serbuk sari Dianthus chinensis Dchi-11. Setiap titik adalah rata-rata dari 10 pengamatan
Pada tahap T2 walaupun mengandung late uninucleate tertinggi, tetapi frekuensinya termasuk rendah (< 50%). Setiap genotipe memiliki potensi yang berbeda, sehingga hasil ini perlu diuji lebih lanjut. Dari Tabel 3 didapatkan grafik hubungan antara panjang kuncup bunga dengan tahap perkembangan serbuk sari. Gambar 6 memperlihatkan bahwa serbuk sari pada tahap meiosis merupakan proses tahap pembentukan dari sel induk mikrospora sampai tetrad. Tahap meiosis ini kuncup berukuran kurang dari 1,2 cm berumur kurang dari 4 hari setelah inisiasi bunga. Tahapuninucleatepanjang kuncup 1,21- 1,5 cm berumur 4 – 6 hari setelah insiasi bunga merupakan tahap T1 – T2. Tahap mitosis dimulai pada umur 6 hari (T3 – T4) dengan panjang kuncup antara 1,51 – 1,70 cm merupakan tahap pembelahan intiuninucleate menjadi dua inti yaitu generatif dan vegetatif. Tahap
y = -0,020x2+ 0,376x + 0,001 R² = 0,988 0 0,5 1 1,5 2 0 2 4 6 8 10 12 Pan jan g ku nc nu p (c m )
Umur kuncup (hari) PMC-tetrad Uninucleate Binuc
le
ate
Polen/serbuk sari
binucleate (T5) panjang kuncup berukuran > 1,71 cm berumur 8 hari setelah inisiasi bunga. Dari Gambar 6 diketahui bahwa terdapat hubungan yang erat antara umur kuncup dengan ukuran kuncup dengan koefisien determinasi R2= 98.8% pada genotipe Dchi-11.
Viabilitas serbuk sari
Serbuk sari yang viabel ditunjukkan oleh tingkat fluorescen yang tinggi setelah pewarnaan dengan FDA, sementara serbuk sari yang non viabel ditunjukkan oleh tingkat fluorescen yang rendah. Yang menarik di sini, serbuk sari yang memiliki ukuran yang besar tidak seperti serbuk sari pada umumnya yang memancarkan warna hijau terang, tetapi terdapat serbuk sari berwarna coklat kehitaman (anak panah kuning) (Gambar 7) walaupun tidak banyak. Namun tidak semua serbuk sari berukuran besar berwarna coklat kehitaman, serbuk sari berwarna terang (anak panah putih) juga ada. Warna coklat kehitaman ini diduga merupakan polen yang tidak memiliki inti. Hasil uji viabilitas pada tanaman uji sangat rendah (Tabel 4). Serbuk sari berwarna coklat kehitaman tidak ditemukan pada dua genotipe yaitu Dchi-12 dan Dchi-14, namun jumlah serbuk sari per antera kedua genotipe ini lebih rendah dibandingkan dengan genotipe lain.
Gambar 7. Hasil pewarnaan serbuk sari dengan FDA Dchi-15. Serbuk sari besar dengan warna terang atau viabel (anak panah putih); serbuk sari dengan warna pudar atau non viabel (anak panah hitam); serbuk sari tanpa inti (warna kuning). Bar = 50 µm
Tabel 4. Viabilitas serbuk sari pada lima genotipe dari spesiesDianthus chinensis.
Genotipe Viabilitas serbuk sari (%)
Viabel Non viabel
Dchi-11 60,36 ± 10,73 39,64 ± 10,73
Dchi-12 56,72 ± 36,15 43,28 ± 36,15
Dchi-13 57,85 ± 7,93 42,15 ± 7,93
Dchi-14 44,91 ± 21,51 55,09 ± 21,51
Dchi-15 55,02 ± 22,26 44,98 ± 22,26
Keterangan : Data dihitung dari rata-rata 4 kali isolasi pada minial 5 bidang pengamatan pada masing-masing genotipe
Hasil uji viabilitas serbuk sari terlihat bahwa rata-rata serbuk sari viabel berkisar 44 – 60% (Tabel 4). Persentase viabilitas tertinggi ditunjukkan oleh genotipe Dchi-11 dan Dchi-13. Uji viabilitas ini terkait dengan jumlah antera yang harus ditanam.
Seleksi tahap perkembangan kuncup bunga pada berbagai media inisiasi double layer untuk kultur antera
Hasil seleksi tahap perkembangan kuncup bunga tidak dapat dianalisis secara statistik, karena hasil pengamatan tidak diperoleh embrio. Hasil yang disajikan bersifat observatif dengan mengamati pencoklatan dan kontaminasi. Hasil observasi peroleh bahwa pada tahap T2 yang memiliki antera dengan pencoklatan terkecil (Tabel 5) dan pencoklatan tertinggi yaitu tahap T4. Makin lanjut tahap kuncup bunga, makin tinggi pencoklatan.
Tabel 5. Respon empat tahap perkembangan mikrospora genotipe Dchi-11 pada berbagai media induksi embrio/kalus.
Tahap kuncup
bunga M1 M2 MediaM3 M4 M5 Pencoklatan (%)Rata-rata
T2 10 0 20 20 0 10 T3 50 30 20 50 30 36 T4 70 70 70 70 50 66 T5 60 50 40 70 50 54 rata-rata 47.5 37.5 37.5 52.5 32.5 Tahap kuncup
bunga M1 M2 MediaM3 M4 M5 Kontaminasi (%)Rata-rata
T2 10 40 20 10 40 24
T3 90 70 60 60 60 68
T4 70 70 60 60 40 60
T5 50 50 40 70 50 52
rata-rata 55 57.5 45 50 47.5
Keterangan: data merupakan rata-rata dari 10 ulangan. T1= 4 hari setelah inisiasi bunga, T2 = bunga mekar 5 hari setelah inisiasi bunga, dst. T= tahap perkembangan. Komposisi media di lampiran 3.
Kontaminasi disebabkan oleh munculnya bakteri pada minggu ke dua setelah tanam. Pencoklatan terjadi mulai minggu ke dua terutama pada tahap T4 dan T5. Tahap T4 dan T5 mengandung antera dengan warna ungu, yang pada umumnya paling cepat mengalami degenerasi. Dari 5 macam media yang diuji, tidak ada satu media yang sesuai. Pada media yang mengalami kontaminasi, menyebabkan pencoklatan pada eksplan (Gambar 8A), sehingga kondisi ini dapat mengaburkan hasil, apakah pencoklatan terjadi karena media yang tidak sesuai atau karena pengaruh kontaminasi.
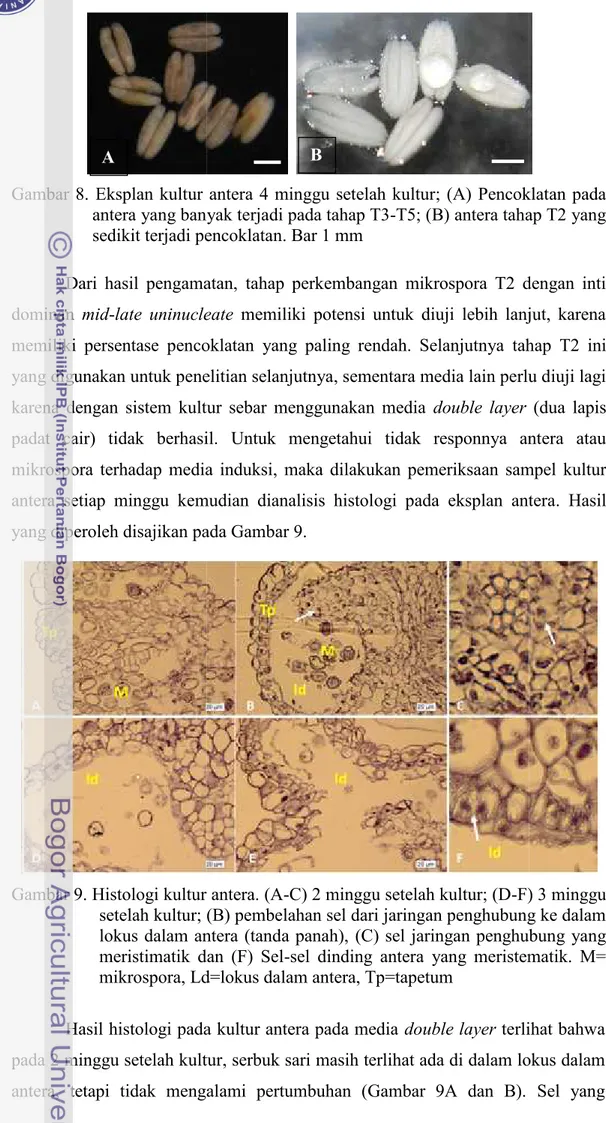
Gambar 8. Eksplan kultur antera 4 minggu setelah kultur; (A) Pencoklatan pada antera yang banyak terjadi pada tahap T3-T5; (B) antera tahap T2 yang sedikit terjadi pencoklatan. Bar 1 mm
Dari hasil pengamatan, tahap perkembangan mikrospora T2 dengan inti dominan mid-late uninucleate memiliki potensi untuk diuji lebih lanjut, karena memiliki persentase pencoklatan yang paling rendah. Selanjutnya tahap T2 ini yang digunakan untuk penelitian selanjutnya, sementara media lain perlu diuji lagi karena dengan sistem kultur sebar menggunakan media double layer (dua lapis padat cair) tidak berhasil. Untuk mengetahui tidak responnya antera atau mikrospora terhadap media induksi, maka dilakukan pemeriksaan sampel kultur antera setiap minggu kemudian dianalisis histologi pada eksplan antera. Hasil yang diperoleh disajikan pada Gambar 9.
Gambar 9. Histologi kultur antera. (A-C) 2 minggu setelah kultur; (D-F) 3 minggu setelah kultur; (B) pembelahan sel dari jaringan penghubung ke dalam lokus dalam antera (tanda panah), (C) sel jaringan penghubung yang meristimatik dan (F) Sel-sel dinding antera yang meristematik. M= mikrospora, Ld=lokus dalam antera, Tp=tapetum
Hasil histologi pada kultur antera pada media double layerterlihat bahwa pada 2 minggu setelah kultur, serbuk sari masih terlihat ada di dalam lokus dalam antera, tetapi tidak mengalami pertumbuhan (Gambar 9A dan B). Sel yang
A B
Gambar 8. Eksplan kultur antera 4 minggu setelah kultur; (A) Pencoklatan pada antera yang banyak terjadi pada tahap T3-T5; (B) antera tahap T2 yang sedikit terjadi pencoklatan. Bar 1 mm
Dari hasil pengamatan, tahap perkembangan mikrospora T2 dengan inti dominan mid-late uninucleate memiliki potensi untuk diuji lebih lanjut, karena memiliki persentase pencoklatan yang paling rendah. Selanjutnya tahap T2 ini yang digunakan untuk penelitian selanjutnya, sementara media lain perlu diuji lagi karena dengan sistem kultur sebar menggunakan media double layer (dua lapis padat cair) tidak berhasil. Untuk mengetahui tidak responnya antera atau mikrospora terhadap media induksi, maka dilakukan pemeriksaan sampel kultur antera setiap minggu kemudian dianalisis histologi pada eksplan antera. Hasil yang diperoleh disajikan pada Gambar 9.
Gambar 9. Histologi kultur antera. (A-C) 2 minggu setelah kultur; (D-F) 3 minggu setelah kultur; (B) pembelahan sel dari jaringan penghubung ke dalam lokus dalam antera (tanda panah), (C) sel jaringan penghubung yang meristimatik dan (F) Sel-sel dinding antera yang meristematik. M= mikrospora, Ld=lokus dalam antera, Tp=tapetum
Hasil histologi pada kultur antera pada media double layerterlihat bahwa pada 2 minggu setelah kultur, serbuk sari masih terlihat ada di dalam lokus dalam antera, tetapi tidak mengalami pertumbuhan (Gambar 9A dan B). Sel yang
A B
Gambar 8. Eksplan kultur antera 4 minggu setelah kultur; (A) Pencoklatan pada antera yang banyak terjadi pada tahap T3-T5; (B) antera tahap T2 yang sedikit terjadi pencoklatan. Bar 1 mm
Dari hasil pengamatan, tahap perkembangan mikrospora T2 dengan inti dominan mid-late uninucleate memiliki potensi untuk diuji lebih lanjut, karena memiliki persentase pencoklatan yang paling rendah. Selanjutnya tahap T2 ini yang digunakan untuk penelitian selanjutnya, sementara media lain perlu diuji lagi karena dengan sistem kultur sebar menggunakan media double layer (dua lapis padat cair) tidak berhasil. Untuk mengetahui tidak responnya antera atau mikrospora terhadap media induksi, maka dilakukan pemeriksaan sampel kultur antera setiap minggu kemudian dianalisis histologi pada eksplan antera. Hasil yang diperoleh disajikan pada Gambar 9.
Gambar 9. Histologi kultur antera. (A-C) 2 minggu setelah kultur; (D-F) 3 minggu setelah kultur; (B) pembelahan sel dari jaringan penghubung ke dalam lokus dalam antera (tanda panah), (C) sel jaringan penghubung yang meristimatik dan (F) Sel-sel dinding antera yang meristematik. M= mikrospora, Ld=lokus dalam antera, Tp=tapetum
Hasil histologi pada kultur antera pada media double layerterlihat bahwa pada 2 minggu setelah kultur, serbuk sari masih terlihat ada di dalam lokus dalam antera, tetapi tidak mengalami pertumbuhan (Gambar 9A dan B). Sel yang
tumbuh dan berkembang adalah jaringan penghubung (Gambar 9B dan C, anak panah putih). Hasil ini memberikan indikasi bahwa pertumbuhan lanjut pada kultur antera tidak melalui embriogenesis, tetapi melalui pendekatan kalus. Srbuk sari cepat mengalami degenerasi pada minggu ke 3 (Gambar 9D dan E).
Perkembangan ovari atau ovul
Anatomi kuncup bunga, ovari dan ovul D. chinensis
Setelah periode viabilitas polen berakhir, diikuti dengan masa reseptif putik 18-20 hari setelah inisiasi bunga yang ditandai dengan keluarnya bulu-bulu pada tangkai putik. Hasil pengamatan anatomi kuncup bunga, ovul dan ovari menunjukkan bahwa pada tahap T5 ovari dan ovul belum terbentuk secara maksimal (Gambar 10A, B dan C), sedangkan pada tahap T7 ovul telah membentuk dua inti di dalam kantong embrio (Gambar 10F).
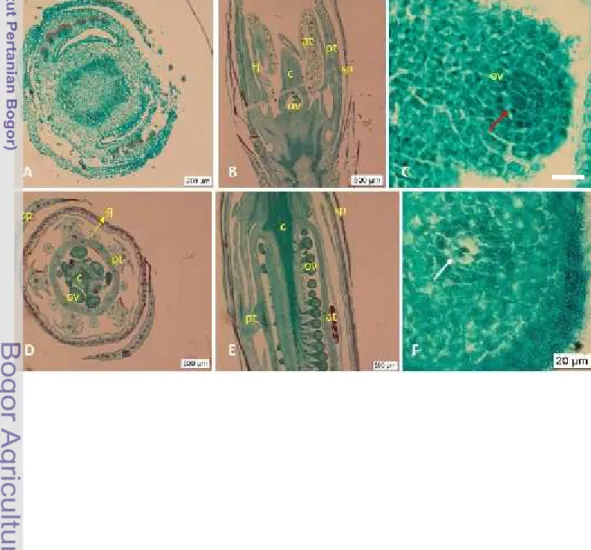
Gambar 10. Irisan melintang dan membujur kuncup bunga dan ovul (A) irisan melintang kuncup bunga pada tahap T5, (B) irisan membujur kucup bunga pada tahap T5, (C) irisan membujur ovul pada tahap T5(Bar = 20 µm), (D) irisan melintang kuncup bunga pada tahap T7, (E) irisan membujur ovari pada tahap T7 dan (F) irisan membujur ovul pada tahap T7. at=antera, c=poros bunga, pt=petal, sp=sepal, fl=filamen, ov=ovul, panah merah=megaspore mother cell (sel induk megaspora), panah putih=2 inti hasil pembelahan mitosis.
Penentuan tahap pembentukan inti dalam kantong embrio ini penting, karena dalam kantong embrio yang diinginkan ialah kantong embrio yang berisi
sel tunggal yang merupakan hasil pembelahan mitosis sel induk megaspora pada tahap T7. Sel induk megaspora yang lengkap ada delapan inti yang terdiri atas dua inti polar, tiga inti sel antipodal, satu inti sel telur dan dua inti sel sinergid. Jaringan-jaringan lain selain 8 inti tersebut merupakan jaringan dengan level ploidi 2n yaitu jaringan nuselus, integumen, dan funikulus. Pada tahap T5 didominasi oleh sel nuselus (Gambar 9C). Pada tahap T7 di dalam ovul telah terbentuk dua inti (Gambar 9F).
Seleksi tahap perkembangan kuncup bunga untuk kultur ovul/ovari
Hasil penelitian menunjukkan bahwa tahap perkembangan kuncup bunga mempengaruhi terbentuknya kalus pada eksplan. Tahap kuncup T5 memiliki rata-rata persentase terbentuknya kalus terendah dan lebih rendah dari pada tahap kuncup T7 dan T9 (Tabel 6). Tahap kuncup T7 merupakan tahap kuncup yang paling banyak membentuk kalus, tetapi tidak berbeda dengan tahap kuncup T9. Tabel 6. Pengaruh tahap kuncup terhadap terbentuknya kalus pada ovula atau
ovari Dchi-11, 8 minggu setelah tanam.
Perlakuan Umur kuncup
bunga (hari sejak inisiasi bunga) Rata-rata persentase terbentuknya kalus* (%)
Warna dan tipe kalus
Tahap kuncup T5 8 9,375 b kalus hijau agak remah
Tahap kuncup T7 10 59,375 a kalus hijau remah dan
kalus hijau agak remah
Tahap kuncup T9 12 46,875 ab kalus hijau agak remah
Keterangan : * rata-rata persentase terbentuknya kalus dihitung dari rata-rata setiap unit perlakuan. Angka rataan yang diikuti oleh huruf yang sama pada kolom yang sama menunjukkan tidak berbeda nyata berdasarkan uji wilayah berganda Duncan pada taraf kepercayaan 5%. T5= 8 hari setelah inisiasi bunga, T7 = 10 hari setelah inisiasi bunga, T9 = bunga mekar 12 hari setelah inisiasi bunga.
Pembahasan
Perkembangan kuncup bunga
Hasi penelitian menunjukkan bahwa setiap tahap perkembangan bunga terdapat variasi ukuran kuncup bunga antar genotipe yang kemungkinan disebabkan oleh faktor internal (genotipe) tanaman dan faktor eksternal (lingkungan). Variasi ukuran kuncup bunga ini akan menyulitkan penetapan
stándar untuk seleksi tanaman donor. Panjang kuncup bunga Dianthus chinensis untuk donor antera menurut Fu et al. (2008) adalah antara 7,5 - 8 mm. Pada ukuran kuncup bunga tersebut, tahap serbuk sari adalah uninukleat. Hasil penelitian ini berbeda dengan hasil penelitian Fu et al. (2008). Apabila dikaitkan dengan pengamatan serbuk sari setiap tahap pada penelitian ini, tahap uninukleat dominan dicapai pada ukuran kuncup bunga 1,31-1,5 cm. Hasil ini menunjukkan bahwa ukuran kuncup bunga kemungkinan dipengaruhi oleh perbedaan genotipe, umur kuncup, lingkungan tempat tumbuh dan iklim, serta budidaya tanaman, sehingga ukuran kuncup bunga pada penelitian ini hanya berlaku untuk genotipe yang sedang diamati.
Perkembangan antera dan serbuk sari
Pengamatan antera dan serbuk sari
Penanda lain yang dapat diamati dan dijadikan sebagai standar adalah mulai sedikit terbukanya kelopak di bagian ujung kuncup (tahap T3), di mana pada kondisi itu mulai terjadi perubahan warna antera dari putih menjadi ungu, dan pada tahap ini, kuncup bunga tidak dapat dijadikan sebagai donor antera, karena pada tahap ini serbuk sari berada pada tahap dominan binukleat. Pengamatan ini tidak dilakukan Fuet al.(2000), sehingga hasil penelitian Fuet al. (2000) berdasarkan ukuran bunga tidak dapat dijadikan acuan. Seleksi tanaman donor didasarkan pada perubahan warna antera juga dilakukan pada tanaman cabe yang merupakan penanda morfologi yang penting (Supena 2004).
Penghitungan jumlah serbuk sari dan ukurannya
Penghitungan jumlah serbuk sari dilakukan untuk menentukan kepadatan antera atau serbuk sari yang harus dikultur. Kepadatan antera dalam kultur akan menentukan keberhasilan. Antera cenderung untuk melekat satu sama lain sehingga kepadatan tertentu akan melindungi antera menempel pada dinding cawan petri pada kultur media cair (Keller 1984; Hoekstraet al. 1993 dan Arnison et al. 1990). Setiap tanaman akan memiliki kepadatan antera atau serbuk sari yang berbeda-beda. Pada tanaman Brassica jumlah 6 antera per ml media merupakan kepadatan yang optimal (Keller 1984), sedang pada tanaman padi kepadatan antera yang diperlukan adalah 3 antera per ml media. Menurut Huang et al. (1990) kepadatan kultur serbuk sari pada Brassica napus adalah 3-4 x 104
mikrospora per ml dan pada jagung 6-8 x 104 mikrospora per ml (Gaillard et al. 1991). Kepadatan antera yang sesuai untuk kultur juga tergantung pada kualitas materi yaitu persentase serbuk sari yang viabel.
Rasio tahap perkembangan serbuk sari
Tahap uninucleate sampai tahap early binucleate pada banyak kasus merupakan tahap paling responsif untuk menginduksi perubahan serbuk sari dari perkembangan gametofit (membentuk polen) ke perkembangan sporofit (membentuk embrio atau kalus) akibat stres lingkungan pada beberapa perlakuan yang diberikan (Palmer & Keller 2005). Penelitian androgénesis pada tanaman Dianthus sp sebagian besar regeneran yang diperoleh melalui tahap kalus yang diaplikasikan pada tahap late uninucleate sampai tahap early binucleate (Mosquera et al. 1999; Nontaswatsri et al. 2008; Fu et al. 2008). Tahap ini dikatakan merupakan tahap yang kompeten di mana sel-sel serbuk sari memiliki respon yang tinggi terhadap induksi stres yang diberikan. Karena pada tahap uninucleate ini sel serbuk sari mengalami peningkatan síntesis protein dan berkurangnya laju síntesis DNA serta RNA (Cordeweneret al.1995; Saunders & Saunders 1988) yang berkorelasi dengan perkembangan embriogenik. Pada tahap uninucleate akhir sampai tahap awal binucleate perkembangan embriogenik dimulai dengan pembelahan asimetris pertama yang dengan adanya sinyal yang berasal dari induksi stres yang diberikan, dirubah menjadi pembelahan simetris. Jika tahap induksi awal menggunakan tahap biselular sebagai donor awal perkembangan embriogenik dimulai dengan masuknya kembali ke siklus sel G1 dari vegetatif sel. Pembelahan sporofitik berlanjut untuk membentuk embrio (Binarovaet al.1997).
Hasil pengamatan antara morfologi kuncup bunga dan tahap perkembangan serbuk sari dapat digambarkan dalam bentuk grafik hubungan antara panjang kuncup bunga dengan tahap perkembangan serbuk sari (Sunderland & Wick 1971). Studi mengenai hubungan antara panjang kuncup dengan tahap perkembangan serbuk sari sangat penting untuk menentukan tahap perkembangan polen pada saat akan dilakukan isolasi, karena tidak mungkin semua antera satu persatu dianalisis sitologis (Sopory & Maheswari 1976). Walaupun penentuan morfologi kuncup bunga ini bukan merupakan kriteria utama penentuan materi donor, tetapi kuncup bunga mewakili tahap seleksi awal tanaman donor.
Uji viabilitas serbuk sari
Viabilitas serbuk sari Dianthus sp pada umumnya rendah. Menurut Galbally & Galbally (1997) anyelir memiliki viabilitas yang sangat rendah dengan persentase perkecambahan kurang dari 10%. Pengamatan viabilitas serbuk sari diperlukan untuk menentukan kepadatan antera dalam kultur. Kepadatan suatu kultur tergantung dari kualitas materi yaitu persentase serbuk sari yang embriogenik (Sopory & Munshi 1996). Apabila rata-rata viabilitas 50%, maka jumlah antera yang harus di tanam dua kali jumlah prediksi optimalnya. Mengacu pada kepadatan serbuk sariBrassicaoptimal yaitu 30000 – 40000 per ml (Sopory & Munshi 1996), maka dengan jumlah serbuk sari per antera rata-rata Dchi-11 ± 30000 (Tabel 2), viabilitas serbuk sari Dchi-11 50%, maka dengan cawan petri berdiameter 6 cm berisi 5 ml media, jumlah anteraDianthus yang harus ditanam adalah 10 – 13 antera. Selain itu dengan melihat morfologi atau ciri unik dari Dianthus chinensis yang memiliki dua inti identik yang diduga merupakan gamet 2n menurut Fuet al.(2008), maka penentuan donor polen untuk kultur antera atau serbuk sari sangat menentukan karena apabila serbuk sari ini yang berkembang maka dipastikan tanaman tersebut adalah heterosigot. Hasil pengamatan menunjukkan bahwa genotipe Dchi-11, Dchi-13 dan Dchi-15 memiliki serbuk sari berukuran besar, sehingga apabila genotipe ini disertakan, kemungkinan-kemungkinan di atas harus diantisipasi.
Seleksi tahap perkembangan kuncup bunga pada berbagai media inisiasi padat cair untuk kultur antera
Tahap perkembangan mikrospora sejalan dengan perubahan warna antera. Pada tahap perkembangan T3 (30% antera ungu muda) pencoklatan mulai meningkat sejalan dengan makin lanjutnya tahap perkembangan mikrospora. Pencoklatan kemungkinan terjadi karena adanya akumulasi komponen fenolik pada eksplan dimana terjadi proses perubahan adaptif bagian tanaman akibat adanya pengaruh fisik dan biokimia (memar, pengupasan, pemotongan, serangan penyakit, atau kondisi yang tidak normal), bisa juga merupakan gejala alamiah dari proses penuaan yang terjadi pada antera.
Menurut Sheeler dan Bianchi (1987), bagian sel tanaman yaitu vakuola sebagai tempat untuk penyimpanan air dan produk-produk sel khususnya metabolit sekunder termasuk fenol. Didalam pemotongan jaringan, vakuola
terpotong dan mengeluarkan fenol yang akan bereaksi dengan enzim fenol oksidase di dalam sitosol sehingga terbentuk kuinon yang menyebabkan warna coklat dan beracun. Eksplan pada penelitian ini tidak dilakukan pemotongan, sehingga apabila terjadi pencoklatan kemungkinan berkaitan dengan penggunaan eksplan tahap perkembangan kuncup yang makin lanjut. Makin lanjut tahap perkembangan kuncup bunga, pencoklatan makin tinggi. Apabila pencoklatan bersumber dari hasil pemotongan eksplan, kemungkinan bersumber dari pemotongan fillamen dari antera.
Perkembangan ovari atau ovul
Anatomi kuncup bunga, ovari dan ovul D. chinensis
TanamanD. chinensis memiliki ovul yang terbentuk dari satu poros bunga. Poros bunga menyatu membentuk satu ruangan (loculus) (Gambar 10E). Ovul melekat pada plasenta yang dihubungkan oleh funikulus. Sel induk mikrospora dalam ovul akan membelah secara meiosis menghasilkan empat megaspora yang masing-masing mempunyai set kromosom haploid. Hanya satu megaspora yang bertahan dan berkembang menjadi kantong embrio, sedangkan tiga yang lain gugur. Inti dalam kantong embrio mengalami pembelahan tiga kali membentuk satu inti sel telur, dua inti sel sinergid, tiga inti antipodal dan dua inti polar. Pola perkembangan megasporogenesis D. chinensis termasuk tipe polygonum (Sniezko 2006). Dua inti pada tahap perkembangan T7 pada Gambar 10F diduga merupakan hasil pembelahan pertama yang berasal dari satu inti hasil meiosis yang masih bertahan.
Seleksi tahap perkembangan kuncup bunga untuk kultur ovul atau ovari
Biasanya tahap serbuk sari late-uninucleate merupakan target yang responsif untuk mengubah gametofitik menjadi sporofitik. Pada ginogenesis kisaran tahap perkembangan ovul untuk diinduksi sangat lebar. Gametofit jantan dan betina tanaman Dianthus chinensis tidak masak bersamaan. Pada tanaman bit gula kuncup bunga diisolasi pada umur 1-3 hari sebelum antesis (Ferrant & Bouharmont 1994), tanaman bawang merah 3-5 hari sebelum antesis (Martinez et al. 2000). Pada penelitian ini donor ovul terbaik berasal dari kuncup bunga pada tahap T7 (umur 10 hari setelah munculnya bunga).
Simpulan
1. Ukuran, bentuk kuncup bunga dan warna antera merupakan indikator waktu dilakukan pengambilaan donor eksplan.
2. Tahap perkembangan kuncup T2 (LU tertinggi (44,64%), ukuran kuncup antara 1,31 – 1,50 cm, warna antera putih, umur 5 hari, pencoklatan terendah) merupakan tahap yang tepat untuk kultur antera.
3. Tahap perkembangan kuncup T7 (ukuran kuncup antara 1,81 – 2.00 cm, panjang petal 30% lebih panjang dari panjang sepal, umur 10 hari) merupakan tahap yang tepat untuk kultur ovul dan ovari berdasarkan persentase terbentuknya kalus dan tipe kalus.