Menulis Proposal Penelitian – Penjelasan disertai
Contoh
Oleh: S.Muryanto, Ketua Lembaga Penelitian UNTAG Semarang Disampaikan dalam acara Sosialisasi Penulisan Proposal yang diselenggarakan oleh Fakultas Teknik UNTAG Semarang, Selasa, 19
Maret 2013
Pendahuluan
Kami berpendapat bahwa proposal penelitian yang baik tidaklah mungkin dihasilkan dari kerja yang asal-asalan. Tidaklah berlebihan jika dikatakan bahwa untuk menghasilkan proposal seperti itu diperlukan latihan, secara sungguh-sungguh dan teratur. Oleh sebab itu diperlukan pula adanya panduan atau petunjuk penulisan proposal penelitian. Memang sudah banyak panduan yang ditulis oleh berbagai kalangan, akan tetapi umumnya tidak disertai dengan contoh-contoh. Hal demikian ini sering dirasakan sebagai salah satu kekurangan oleh mereka yang belajar menulis proposal penelitian. Contohnya seperti apa? Bentuk konkritnya seperti apa? Demikianlah, dalam makalah ini kami mencoba menjelaskan satu per satu komponen dari sebuah proposal penelitian, dilengkapi dengan contoh. Contoh tersebut diambil dari sebuah proposal SKIM Hibah Fundamental yang telah disetujui dan dilaksanakan pada tahun 2011. Harapan kami, dengan disertakannya contoh-contoh seperti itu, menjadi makin mudahlah usaha menulis proposal penelitian.
JUDUL
Berikut ini adalah daftar/checklist, tentang apa saja yang perlu diperhatikan dalam menulis judul. Ini adalah semacam rambu-rambu.
Checklist
1. Apakah dengan membaca judul, maka topik yang diusulkan/akan diteliti sudah nampak jelas bagi pembaca, terutama pembaca yang tidak se-bidang ilmu dengan pengusul?
2. Apakah judul sudah cukup menggambarkan apa yang nanti akan dikerjakan/diteliti?
3. Apakah terlalu panjang?
5. Apakah terlalu rinci?
Contoh judul
a. Kristalisasi Mineral Struvite (MgNH4PO4.6H2O)
b. Studi Kristalisasi Mineral Struvite dalam Kristaliser Batch:
c. Kristalisasi Mineral Struvite (MgNH4PO4.6H2O) dalam Kristaliser Batch:
d. Kristalisasi Mineral Struvite (MgNH4PO4.6H2O) dalam Kristaliser Batch: Efek
Tingkat Supersaturasi dan Penambahan Additif
e. Kristalisasi Mineral Struvite (MgNH4PO4.6H2O) dalam Kristaliser Batch: Efek
Tingkat Supersaturasi dan Penambahan Additif (Ca2+ , Cu , dan Zn2+ 2+ )
f. Kristalisasi Mineral Struvite (MgNH4PO4.6H2O) dalam Kristaliser Batch:
Efek Tingkat Supersaturasi dan Penambahan Additif (Ca2+ , Cu2+ , dan Zn2+ )
terhadap Kinetika Reaksi dan Morphologi Kristal
Catatan:
ABSTRAK
Checklist
1. Apakah sudah nampak, penelitian yg diusulkan ini akan meneliti bidang ilmu apa, berkaitan dengan apa? Apakah sudah sesuai dengan skim yang dituju?
2. Apakah sudah diuraikan metode yg nanti akan digunakan? Apakah kelihatan jelas bahwa metode/langkah-langkah penelitian dapat dilakukan oleh orang lain yg se-bidang ilmu? Apakah urut-urutan langkah penelitian masuk akal?
3. Apakah sudah dijelaskan, hasil penelitian yg diharapkan seperti apa?
4. Apakah sudah diuraikan originalitas penelitian: bahwa belum pernah diteliti, atau sudah pernah diteliti tetapi perlu diulang untuk mengetahui validitas temuan yang terdahulu, atau perlu dikembangkan?
Contoh Abstrak (tulisan aslinya dalam satu paragraph):
Tujuan penelitian ini adalah mempelajari kinetika reaksi kristalisasi, morphologi serta kemurnian struvite dalam proses kristalisasi yang berlangsung dalam kristaliser batch dengan penambahan additif yaitu ion-ion asing (foreign ions): Ca2+, Cu2+, dan Zn2+.
Kristalisasi struvite dilakukan dengan mereaksikan kedua larutan ion pembentuknya, yaitu dari larutan sediaan (stock solutions) MgCl2 dan NH4H2PO4 masing-masingdengan
konsentrasi tertentu sehingga diperoleh perbandingan molaritas Mg2+, NH
4+ dan PO4-3 1:1:1,
dalam sebuah kristaliser batch berpengaduk pada tiga temperatur yang berbeda: 25, 35 dan 400C.
Additif yang berupa ion-ion: Ca2+, Cu2+, Zn2+ disiapkan dari larutan garam-garam
khloridanya (CaCl2, CuCl2, dan ZnCl2) dan ditambahkan ke dalam larutan MgCl2 dalam skala
ppm.
struvite selama reaksi kristalisasi, yaitu ion-ion yang tertinggal di dalam larutan, dilakukan dengan atomic absorption spectrometry (AAS) dan atau wet analysis.
Data dari analisa AAS ini dipergunakan untuk menghitung konstanta kecepatan reaksi dan energi aktivasi (lihat uraian dalam sub-bab V. Design dan Metode Penelitian).
Kristal struvite yang diperoleh diamati morphologi dan komposisi/kemurniannya dengan scanning electron microscopy (SEM) dan X-Ray Diffraction Energy Dispersive Spectrometry (XRD-EDS).
Penelitian pada tahun pertama dilakukan untuk kristalisasi dengan tingkat supersaturasi tinggi, karena juga penting untuk mengetahui batas atas zona metastabil.
Kemudian tahun kedua dilakukan kristalisasi dengan tingkat supersaturasi rendah, antara lain untuk mengetahui batas bawah zona metastabil atau solubility curve-nya.
Catatan:
Abstrak adalah bentuk mini dari keseluruhan proposal, oleh sebab itu juga ditulis paling akhir, yaitu setelah semua bagian proposal ditulis.
KAJIAN PUSTAKA
Checklist
1. Apakah sudah membahas penelitian-penelitian serupa dari pihak lain?
2. Apakah sudah memaparkan kesesuaian, kontradiksi, korelasi, dan kekurangan-kekurangan dari hasil-hasil penelitian yg dibahas dalam no 1?
3. Apakah sudah dijelaskan apa yang dapat disumbangkan/kontribusi hasil penelitian yang diusulkan? Apakah sudah dijelaskan temuan baru yang diharapkan?
Contoh Kajian Pustaka
Kajian pustaka meliputi pokok-pokok berikut, yang telah mencakup semua aspek dari penelitian yang akan dikerjakan. Di samping itu, juga merupakan penjabaran dari seluruh kata yang tercantum dalam Judul.
1. Pendahuluan
2. Nukleasi
a. Nukleasi primer
b. Nukleasi sekunder
3. Pertumbuhan Kristal
4. Pengaruh ion asing
a. Pengaruh ion kalsium (Ca2+)
b. Pengaruh ion tembaga (Cu2+) dan seng (Zn2+)
1. Pendahuluan
Di dalam fasilitas pengolahan air limbah (wastewater treatment facilities), terutama bila limbah mengandung Mg+, NH4+, dan PO42- dalam jumlah yang cukup secara
stoikiometri, dapat terjadi pengkristalan struvite secara spontan apabila terdapat faktor-faktor yang mendukung.
Faktor-faktor ini misalnya: suhu [Le Corre 2006], pH [Pastor dkk 2008; Stratful dkk 2001; Bouropoulos dan Koutsoukos 2000], konsentrasi [Yoshino dkk 2003] dan turbulensi [Yoshino dkk 2003; Mohajit dkk 1989].
Faktor-faktor ini sulit dikendalikan sehingga terjadinya kerak struvite, misalnya pada pipa-pipa dan pompa sirkulasi juga tidak dapat diprediksi. Kristalisasi struvite dan proses pembentukan kerak pada alat-alat serta sistim pemipaan dalam berbagai industri
Di sisi lain struvite dapat dijadikan pupuk alternatif [Britton dkk 2005; Shu dkk 2006], karena mempunyai kandungan Mg2+, N (dari NH
4+) dan P (dari PO4-3) [Le Corre dkk
2005; Ali 2007; Kofina dan Koutsoukos 2005] setara pupuk. Struvite sebagai pupuk
mempunyai karakteristik lebih baik, sebab kelarutannya dalam air kecil [Rahaman dkk 2006; Anon 2006; Barak dan Stafford 2006], sehingga dapat merupakan pupuk slow release [Shu dkk 2006; Wang dkk 2005]. Oleh sebab itu studi tentang struvite telah banyak dilakukan [de-Bashan dan [de-Bashan 2004].
Struvite mengkristal dalam bentuk orthorhombik berwarna putih menurut persamaan reaksi berikut [Rahaman dkk 2008]:
Mg2+ + NH+ + H
nPO4n-3 + 6 H2O MgNH4PO4.6H2O + nH+ (1)
Tergantung pada pH larutannya, harga n adalah antara 0, 1 atau 2. Dalam ranah industri, kerak terjadi pada lingkungan yang praktis tidak bisa terbebas dari keberadaan additif atau impuritas.
Efek additif terhadap kinetika kristalisasi dan morphologi kristal, jadi juga efek terhadap pembentukan kerak, dapat sangat signifikan meski pun additif jumlahnya sangat sedikit [Hoang dkk 2009]. Walau pun penelitian tentang pengaruh additif terhadap proses kristalisasi sudah banyak dilakukan, pengaruh atau efek itu pada umumnya spesifik (case by case) tergantung dari jenis dan konsentrasi additif serta karakteristik dari tiap jenis kristal [Muryanto dkk 2002].
Di lain pihak, penelitian tentang pengaruh ion asing terhadap nukleasi dan pertumbuhan kristal struvite relatif masih sedikit [Le Corre 2006].
Penelitian yang diusulkan ini akan mempelajari pengaruh ion-ion asing yang umum terdapat dalam air limbah [Muryanto dan Ang 2005] terhadap kinetika reaksi kristalisasi struvite serta morphologinya.
2.Nukleasi
Nukleasi atau peristiwa terbentuknya nukleus/inti kristal dapat diamati secara
makroskopis mau pun mikroskopis. Inti kristal dapat terbentuk dari hasil attrisi antara sesama kristal, terutama bila kristal-kristal berukuran besar[Jancic dan Grootscholten 1984; Larson 1984]. Sebaliknya, pembentukan inti kadang hanya dapat diikuti secara mikroskopis, yaitu hanya dapat dideteksi dengan bantuan mikroskop, terutama scanning electron microscope atau sejenisnya yang mempunyai magnifikasi tinggi. Nukleasi homogen (homogeneous nucleation) biasanya menghasilkan inti ukuran mikroskopis ini.
Karena kristalisasi adalah proses yang didorong oleh konsentrasi (a concentration-driven process), maka kenaikan konsentrasi larutan, yang umumnya dinyatakan dengan tingkat kejenuhan atau tingkat supersaturasi, mengakibatkan kenaikan laju pembentukan inti kristal. Laju pembentukan ini menjadi sangat cepat dan tidak terkendali apabila tingkat supersaturasi amat tinggi. Proses kristalisasi, terutama skala industri, harus dikendalikan agar laju pembentukan inti dapat diatur, sehingga jumlah mau pun distribusi ukuran kristal sesuai dengan yang diinginkan. Idealnya, distribusi ukuran kristal harus sempit sehingga mudah dalam penanganannya, misal dalam pengayakan atau filtrasi. Secara garis besar,
pembentukan inti dapat diklasifikasi menjadi dua: nukleasi primer dan nukleasi sekunder.
a.Nukleasi primer
Nukleasi primer berlangsung dalam larutan yang bebas dari kristal dan biasanya untuk larutan dengan konsentrasi tinggi. Sebagaimana diketahui, suatu larutan yang lewat jenuh (supersaturated) berada dalam keadaan tidak setimbang, dan di dalamnya terjadi fluktuasi konsentrasi yaitu konsentrasi di suatu titik dalam larutan tersebut dapat berbeda dari titik-titik lain di seluruh larutan (local concentrations). Hal ini mengakibatkan tarik menarik di antara molekul-molekul sehingga terjadi aggregat molekul yang dapat menjadi inti kristal. Apabila konsentrasi larutan cukup tinggi maka aggregat molekul-molekul tersebut dapat mencapai ukuran kritis, sehingga inti kristal dapat bertahan dan tumbuh. Semakin tinggi konsentrasi larutan maka ukuran kritis inti semakin kecil, sehingga kemungkinan terjadinya inti semakin besar [Myerson 1993].
b.Nukleasi sekunder
Nukleasi sekunder lebih banyak terjadi karena tidak membutuhkan tingkat supersaturasi atau kejenuhan larutan yang tinggi. Di samping itu, larutan yang akan dikristalkan pada umumnya tidak dapat terbebas sama sekali dari kontaminasi benda asing, seperti debu atau partikel-partikel yang terdapat di dalam bejana tempat proses kristalisasi berlangsung. Mekanisme pembentukan kristal/nukleasi secara ringkas adalah sebagai berikut:
Komponen-komponen pembentuk inti, yaitu molekul atau ion-ion dalam larutan berinteraksi satu sama lain secara acak membentuk aggregat yang makin lama makin besar sehingga mencapai ukuran kritis dan menjadi inti kristal. Molekul atau ion-ion ini selain berinteraksi satu sama lain, juga berinteraksi dengan benda asing yang kemungkinan besar ada di dalam larutan. Interaksi dengan benda asing ini juga menghasilkan inti kristal. Inti kristal yang telah terbentuk selanjutnya akan tumbuh menjadi kristal dan dapat dideteksi secara visual. Pertumbuhan kristal itu diuraikan dalam sub-bab berikut ini.
3.Pertumbuhan Kristal
Tahap awal dari proses kristalisasi adalah terbentuknya inti kristal atau nukleus. Setelah inti kristal terbentuk, inti ini akan tumbuh karena bergabungnya molekul-molekul atau ion-ion dalam larutan di sekelilingnya. Semakin tinggi konsentrasi larutan maka laju pertumbuhan akan semakin tinggi karena jarak antara molekul-molekul dan ion-ion satu sama lain semakin pendek. Seiring tumbuhnya kristal maka konsentrasi larutan menurun. Bentuk akhir kristal ditentukan oleh muka kristal yang tumbuh paling lambat.
Seperti terlihat dalam Gambar 1, bentuk kristal awal (a) tidak sama dengan bentuk akhir (c), disebabkan laju pertumbuhan permukaan samping kiri dan kanan kristal tidak sama dengan pertumbuhan permukaan atas dan bawah kristal. Pertumbuhan muka atas dan bawah lebih cepat sehingga akhirnya bentuk akhir kristal ditentukan oleh pertumbuhan permukaan samping kiri dan kanan.
Gambar 1 Skema efek perbedaan kecepatan tumbuh permukaan kristal: (a)bentuk awal kristal, (c) bentuk akhir kristal. (a) berbeda dengan (c)
Gambar 2 Skema Model Difusi Permukaan atau Model BCF(ref: Myerson 1993)
Pertumbuhan kristal sangat ditentukan oleh struktur permukaannya, yang biasanya dibedakan menjadi tiga zona: terrace, step, dan kink (Gambar 2). Komponen atau satuan pertumbuhan, yaitu atom, molekul atau partikel, dapat teradsorpsi baik pada terrace, step atau kink. Energi yang diperlukan komponen pertumbuhan untuk teradsorpsi pada terrace lebih besar, daripada yang diperlukan untuk step atau lebih-lebih untuk kink. Kink adalah daerah dengan energi ikat (bonding energy) paling tinggi karena memiliki tiga sisi untuk mengadsorpsi komponen pertumbuhan. Dengan demikian kink mempunyai probabilitas paling tinggi untuk tumbuh.
4.Pengaruh ion asing
Walau pun ion asing terdapat dalam jumlah kecil (ppm) tetapi pengaruhnya terhadap nukleasi dan pertumbuhan kristal dapat sangat besar[Muryanto 2002, Hoang dkk 2009].Hal ini
disebabkan ion-ion asing dapat menutup “active sites” yaitu tempat-tempat pertumbuhan aktif [Ohara dan Reid 1973], sehingga ukuran kristal tidak dapat bertambah dan morfologinya berubah [Myerson 1993]. Dalam hal pengkristalan struvite, ion-ion asing itu banyak jenis dan jumlahnya, yaitu tergantung dari lingkungan atau larutan tempat kristal tumbuh (Nelson dkk, 2003). Dalam penelitian yang diusulkan ini, ion asing yang akan diteliti pengaruhnya
terhadap nukleasi dan pertumbuhan kristal, berturut-turut adalah Ca2+, Cu2+, dan Zn2+.
a.Pengaruh ion kalsium (Ca2+)
Adanya ion kalsium (Ca2+) dalam larutan yang mengandung phosphat memungkinkan
terjadinya kompetisi antara pembentukan struvite (MgNH4PO4.6H2O) dan pembentukan
kalsium phosphat: Ca3(PO4)2 [Pastor dkk 2008]. Ion kalsium mungkin berkompetisi dengan
ion magnesium dalam “memperebutkan” phosphat, tetapi hal itu baru akan terjadi bila
konsentrasi ion kalsium dalam larutan tinggi, yaitu di atas 300 ppm [Yi dkk 2005]. Penelitian Pastor dan rekan-rekan baru-baru ini [Pastor dkk 2010] menunjukkan bahwa adanya ion kalsium juga memungkinkan terjadinya kalsite (CaCO3) dan dolomite: CaMg(CO3)2 bila
konsentrasi ion magnesium dalam larutan cukup tinggi. Penelitian Le Corre dan kawan-kawan [Le Corre dkk 2005] memperlihatkan bahwa ion kalsium mempengaruhi bentuk serta kemurnian kristal struvite. Karena pada umumnya air limbah mengandung ion kalsium cukup tinggi [Parsons dkk 2001], maka pengaruh ion kalsium terhadap proses pengkristalan struvite dari limbah tersebut juga akan diteliti dalam penelitian yang diusulkan ini.
b.Pengaruh ion tembaga (Cu2+) dan seng (Zn2+)
Limbah peternakan, misal dari peternakan babi, dapat mengandung Cu2+ serta Zn2+ cukup
tinggi[Marcato dkk 2008, Suzuki dkk 2001], yaitu berasal dari suplemen makanan yang diberikan di peternakan itu. Kedua jenis kation tersebut dianggap tidak ramah lingkungan, sehingga keberadaannya dalam limbah sudah lama menjadi perhatian para peneliti [Lake dkk 1985]. Namun penelitian yang lebih akhir [Lisitsin dkk 2005] menunjukkan bahwa
keberadaan Zn2+ dalam air minum tidak membahayakan, dan sampai dengan lima ppm
diperbolehkan. Penelitian yang sama [Lisitsin dkk 2005] juga memperlihatkan bahwa Zn2+
yang tumbuh dalam larutan (bulk crystallization) mau pun kristal CaCO3 yang tumbuh dan
membentuk kerak (scale) pada membran untuk desalinasi RO. Sebagai zat penghambat kerak (antiscalant), Zn2+ mempunyai kemampuan sama dengan antiscalant organik, namun lebih
mudah dalam pemakaiannya karena sumber Zn2+ (dan juga Cu2+) dapat menggunakan unggun
butiran paduan Cu-Zn (granular bed of KDF© Cu-Zn alloys) [Stenger dan Dobbs 1995;
Al-Kharusy 1996]. Dalam penelitian yang diusulkan ini Cu2+ dan Zn2+ diharapkan dapat
memberikan efek terhadap kinetika kristalisasi mau pun morphologi struvite [Kabdasli dkk 2006, Lisitsin dkk 2005].
MASALAH PENELITIAN
Checklist
1. Jelaskan masalahnya dengan singkat, berikan faktanya.
2. Jelaskan apa yang salah, apa yang masih kurang.
3. Jelaskan penyebab kesalahan atau kekurangan itu.
4. Jelaskan pentingnya masalah sekarang dan di masa yad.
Contoh Masalah Penelitian dan Perumusan Masalahnya
Timbulnya kerak (scale) pada pipa-pipa dan alat-alat, misalnya pada fasilitas pengolahan air limbah, merupakan masalah yang hingga kini belum dapat diatasi sepenuhnya.
Salah satu komponen utama pada kerak seperti itu adalah struvite atau magnesium ammonium phosphate heksahidrat: MgNH4PO4.6H2O [Nelson dkk 2003; Kofina dan
Koutsoukos 2005; Kabdasli dkk 2006; Le Corre dkk 2007].
Banyak penelitian yang telah dilakukan terhadap struvite ini, tetapi sebagian besar mengenai proses pembersihan kerak, bukan penelitian terhadap terbentuknya kristal penyusun kerak itu sendiri [Wang dkk 2005].
Oleh karena itu, penelitian yang diusulkan ini bermaksud meneliti fenomena pembentukan kristal struvite, terutama di dalam larutan yang dibuat menyerupai air limbah.
Proses terbentuknya kristal, sebagai awal dari proses terbentuknya kerak, sangat penting untuk diteliti, karena bentuk akhir kristal/morphologinya ikut menentukan cepat lambatnya proses pembentukan kerak[Muryanto 2002].
Penelitian yang diusulkan ini menekankan segi teoritis yaitu kinetika reaksi kristalisasi pembentukan kristal struvite, dan morfologi serta kemurnian kristal tersebut.
Secara spesifik penelitian akan dijalankan untuk mengetahui:(1) konstanta kecepatan reaksi, (2) energy aktivasi, (3) waktu induksi, dan (4) morfologi dan kemurnian kristal struvite yang tumbuh dalam kristaliser batch dalam lingkungan yang menyerupai air limbah sesungguhnya, yaitu adanya ion-ion asing: Ca2+, Cu2+, dan Zn2+.
Pengetahuan teoritis tentang ke empat hal tersebut, sangat penting sebagai landasan teori dalam penanganan kerak dalam air limbah.
Catatan:
TUJUAN PENELITIAN
Tujuan penelitian ini adalah mempelajari kinetika reaksi kristalisasi, morphologi serta kemurnian struvite dalam proses kristalisasi yang berlangsung dalam kristaliser batch dengan penambahan additif yaitu ion-ion asing (foreign ions): Ca2+, Cu2+, dan Zn2+.
Kristalisasi struvite dilakukan dengan mereaksikan kedua larutan ion pembentuknya, yaitu dari larutan sediaan (stock solutions) MgCl2 dan NH4H2PO4 masing-masingdengan
konsentrasi tertentu sehingga diperoleh perbandingan molaritas Mg2+, NH
4+ dan PO4-3 1:1:1,
dalam sebuah kristaliser batch berpengaduk pada tiga temperatur yang berbeda: 25, 35 dan 400C.
Penelitian pada tahun pertama dilakukan untuk kristalisasi dengan tingkat supersaturasi tinggi, karena juga penting untuk mengetahui batas atas zona metastabil.
Kemudian tahun kedua dilakukan kristalisasi dengan tingkat supersaturasi rendah, antara lain untuk mengetahui batas bawah zona metastabil atau solubility curve-nya.
METODE PENELITIAN
Checklist
1. Apa yang akan saya teliti?
2. Di mana penelitian ini akan dilakukan?
3. Bagaimana rancangan percobaannya? Apakah ada asumsi-asumsi?
4. Variabel apa saja yang akan diukur? Dan mengapa variabel itu yg diteliti?
5. Alat-alat apa saja yang diperlukan? Di mana alat-alat itu berada? Apakah alat perlu dimodifikasi?
6. Bagaimana saya akan menganalisa data yang didapat? Apakah ada prosedur statistik tertentu? Apakah ada persamaan-persamaan matematik? Apakah perlu software khusus?
7. Kesulitan-kesulitan apa yang mungkin dijumpai dalam percobaan?
8. Apakah metode ini sudah dipakai dalam penelitian-penelitian terdahulu? Apakah saya memodifikasi metode tersebut?
Contoh Penulisan Metode Penelitian
Penelitian kristalisasi struvite ini akan menggunakan kristaliser jenis batch yang
berpengaduk. Kristaliser tersebut berupa beaker atau gelas piala ukuran satu (1) liter. Dinding bagian dalam gelas piala harus benar-benar licin, tak ada goresan agar tidak terjadi nukleasi sekunder [Muryanto 2002].
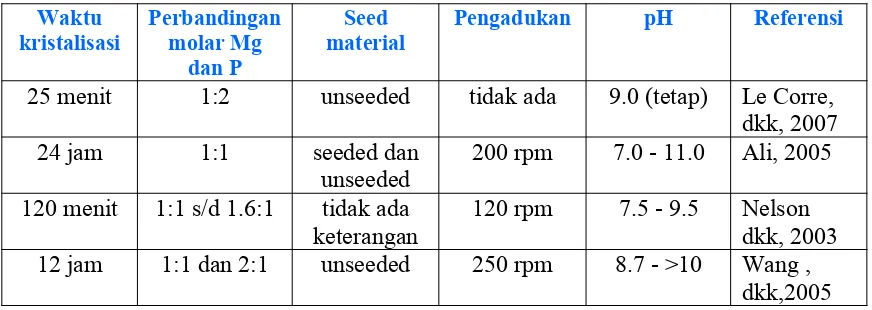
Desain penelitian untuk kristalisasi batch ini adalah “One-factor-at-a-time” method menurut Davies [1978]. Desain ini dipilih karena tidak diketemukan keseragaman yang dapat dijadikan acuan dalam menentukan variable-variabel percobaan kristalisasi sejenis. Studi pustaka menunjukkan bahwa kondisi operasi untuk kristalisasi struvite dengan sistim batch bervariasi seperti terlihat dalam Tabel1 berikut.
Tabel 1 Kondisi operasi kristalisasi struvite sistim batch dari beberapa peneliti
Waktu
25 menit 1:2 unseeded tidak ada 9.0 (tetap) Le Corre, dkk, 2007
24 jam 1:1 seeded dan
unseeded 200 rpm 7.0 - 11.0 Ali, 2005 120 menit 1:1 s/d 1.6:1 tidak ada
selanjutnya (tahun ke II). Variabel-variabel yang dipilih adalah jenis dan konsentrasi additif, temperatur dan waktu kristalisasi.
Perbandingan molar ion pembentuk: Mg2+, NH
4+ dan PO4-3 merupakan variabel tetap, yaitu
1:2:1[Kofina dan Koutsoukos, 2005]. Additif yang digunakan adalah Ca2+, Cu2+, dan Zn2+
dalam garam khloridanya. Temperatur kristalisasi ditetapkan 250C, 300C dan 400C. Tabel 2
memuat variabel-variabel berubah yang dipakai. Dalam Tabel2 diperlihatkan pemakaian ion kalsium (Ca2+) dan ion tembaga (Cu2+), baik sendiri mau pun campuran antara keduanya.
Dengan mengikuti pola ini (Tabel 2), maka dalam perlakuan berikutnya akan dipasangkan Ca2+ dengan Zn2+, dan akhirnya Cu2+ dengan Zn2+.
Tabel 2 Variabel-variabel berubah yang dipakai dalam penelitian ini
Langkah percobaan penelitian kristalisasi struvite dengan variabel-variabel yang diuraikan sebelumnya, adalah sebagai berikut ini.
Sebagai larutan yang akan dikristalkan digunakan kristal MgCl2.6H2O dan NH4H2PO4,
masing-masing dilarutkan dalam aquadest (double-distilled water) sehingga mencapai konsentrasi 0.1 M dan 0.20 M. Larutan induk (stock solutions) 0.10 M dan 0.20 M ini kemudian akan diencerkan dengan aquadest menurut keperluan percobaan sehingga perbandingan molar Mg2+, NH
4+ dan PO4-3 = 1:1:1 dan 2:1:1 [Le Corre dkk, 2007, Kofina dan
Koutsoukos 2005].
Untuk menghilangkan CO2 terlarut yang kemungkinan dapat mengganggu kestabilan pH
larutan, maka aquadest yang akan digunakan dididihkan dahulu, kemudian disimpan dalam wadah plastik yang tertutup rapat (jerry can). Demikian pula larutan yang siap dicampurkan, sebelum pencampuran selalu ditutup dengan plastik (plastic film) agar terhindar dari masuknya partikel-partikel misalnya debu, yang dapat menimbulkan nukleasi yang tidak dikehendaki.
Kecepatan pengadukan ditetapkan 100 rpm [Chan,1997] karena hanya berfungsi untuk membuat larutan homogen dan tercampur sempurna. Di samping itu kecepatan pengadukan yang tinggi dapat menyebabkan atrisi dan pecahnya kristal-kristal yang terbentuk sehingga menyulitkan interpretasi terhadap morfologi kristal yang diperoleh.
Larutan MgCl2 dan NH4H2PO4 masing-masing sebanyak 300 mL dimasukkan kedalam
kristaliser, pengaduk dijalankan dan seluruh sistim itu dibiarkan mencapai temperatur yang diinginkan: 25°C, 30°C dan 40°C. Segera setelah temperatur yang dikehendaki tercapai, 20 mL larutan sampel (yang menandakan t = 0 menit atau waktu nol) diambil dengan syringe untuk analisa AAS (Atomic Absorption Spectrometry). Syringe pada ujungnya dilengkapi kertas saring ukuran lubang 0,22 µm untuk menyaring kristal yang diperoleh. Selanjutnya kertas saring bersama kristal didalamnya dikeringkan dalam oven bertemperatur 600C selama
24 jam. Kemudian kertas saring bersama kristal yang kering ditimbang untuk mengetahui massa kristal yang terbentuk. Untuk menyelidiki morfologi, kristal yang terbentuk dipindahkan dari kertas saring dengan hati-hati dan kemudian disimpan dalam vial tertutup.
1.Penentuan konstanta kecepatan reaksi
Penentuan konstanta kecepatan reaksi kristalisasi dalam larutan dapat dilakukan dengan menggunakan model difusi Chernov [Myerson 1993]. Model tersebut menunjukkan bahwa difusi zat terlarut kedalam unit pertumbuhan kristal dalam boundary layer (lapisan batas) dan tebalnya lapisan itu merupakan faktor penting yang mengendalikan pertumbuhan. Ketika unit pertumbuhan meninggalkan lapisan difusi menuju permukaan kristal, maka pertambahan masa kristal dapat dihitung dengan hukum Fick [Nyvlt dkk 1985] sebagai berikut:
dx
dm/dt = laju pertambahan massa, (g/detik)
D = koefisien difusi, cm2/detik
A = luas permukaan kristal, cm2
dc/dx = gradient konsentrasi unit pertumbuhan dalam lapisan difusi g/(cm3.cm)
Selanjutnya hukum Fick di atas oleh Myerson [1993] diubah menjadi
gKG = konstanta integrasi
C = konsentrasi ion-ion pembentuk kristal, gr.cm-3
Ceq = konsentrasi ion-ion pembentuk kristal pada kesetimbangan, gr.cm-3
dm/dt = gradient konsentrasi unit pertumbuhan dalam lapisan difusi g/(cm3.cm)
g = eksponen dengan nilai 1 atau 2.
Secara umum KG dan A dapat diganti dengan k, yaitu konstanta kecepatan reaksi,
sehingga persamaan menjadi:
Cat CaeqN
- dCa/dt = kecepatan penurunan konsentrasi ion pembentuk, karena terjadinya kristal, ppm. menit-1 (jika orde reaksi adalah satu)
Ca = konsentrasi ion-ion pembentuk kristal, ppm (dalam penelitian ini adalah Mg2+, NH
4+ atau PO4-3)
Caeq = konsentrasi Ca pada saat kesetimbangan, ppm
(dalam penelitian ini diasumsi t saat kesetimbangan = 90 menit) k = konstanta kecepatan reaksi
N = orde reaksi, bernilai 1 atau 2.
Kristalisasi struvite menunjukkan bahwa reaksinya adalah orde satu (1) [Ohlinger dkk1999; Nelson, dkk 2003; Quintana dkk 2005; Le Corre 2006; Rahaman dkk 2008] atau orde dua (2) [Kofina dkk 2007; Kofina dan Koutsoukos 2005; Britton dkk 2005; Boropoulos and Koutsoukos 2000). Oleh karena itu dari analisa AAS untuk penentuan Mg2+ dapat dicari orde
yang ada dalam penelitian ini yaitu dengan memberi N dalam persamaan di atas harga 1 atau 2.
Untuk orde satu:
Cat CaeqN
k dt dCa
(5)
dengan N = 1, persamaan dapat diselesaikan menjadi :
Ca CaeqlnCatCaeqkt
ln 0 (6)
Maka plotting dari ruas kiri pers. (6) di atas terhadap waktu kristalisasi t akan menghasilkan garis lurus dengan angka arah k, yaitu konstanta kecepatan kristalisasi yang dicari. Untuk menentukan persamaan mana yang lebih sesuai, maka ditentukan dengan harga koefisien korelasi R2. Persamaan dengan harga R2 yang lebih besar, yaitu > 95% dan mendekati 1,
itulah yang dipilih.
2.Penentuan energi aktivasi
Hubungan antara kecepatan reaksi dengan temperatur biasanya dinyatakan dengan Hukum Arrhenius. Hukum Arrhenius berlaku untuk proses-proses seperti difusi, pelarutan (dissolution) mau pun kristalisasi. Dalam proses kristalisasi, energy aktivasi pertumbuhan kristal tergantung driving force untuk pertumbuhan [Mullin 1979]. Energi aktivasi yang rendah (10 s/d 20 kJ.mol-1) menunjukkan bahwa pertumbuhan kristal dikendalikan oleh
Hukum Arrhenius dinyatakan sebagai:
atau dalam bentuk logaritma,
RT
k = konstanta kecepatan reaksi
A = parameter Arrhenius
= jumlah tumbukan efektif molekul-molekul persatuan waktu
Ea = energy aktivasi, kJ. mol-1
R = tetapan gas umum, 8.31 kJ.mol-1K-1
T = suhu mutlak, 0K.
Dalam penelitian kristalisasi ini digunakan tiga temperatur yang berbeda: 250C, 300C, dan
400C, sehingga plotting harga k yang diperoleh terhadap 1/T (lih.pers. 8) akan menghasilkan
garis lurus dengan angka arah –Ea/R dan intercept A. Oleh karena A dan R diketahui, maka Ea dapat dihitung.
3.Penentuan morfologi dan kemurnian struvite
PENDANAAN
Usulan biaya:
Tahun pertama: Rp 37.105.000 (tigapuluhtujuh juta seratuslima ribu rupiah).
Tahun kedua: Rp 37.310.000 (tigapuluhtujuh juta tigaratus sepuluh ribu rupiah).
VII.Pembiayaan
Jenis Pengeluaran Jumlah Anggaran Yang Diusulkan (Rp) Tahun ke 1 Tahun ke 2 Gaji & upah (30% total anggaran) 11.100.000 11.190.000
Biaya peralatan 9.400.000 10.300.000
Bahan habis pakai – material
penelitian 6.510.000 5.525.000
Biaya perjalanan 1.600.000 1.800.000
Bahan habis pakai – alat tulis kantor 695.000 695.000 Dokumentasi, pembuatan laporan dan
publikasi 7.800.000 7.800.000
Total anggaran per tahun 37.105.000 37.310.000 Total anggaran untuk dua tahun 74.415.000
VIII. Rincian Biaya Penelitian
1.Rekapitulasi Rincian Biaya Tahun ke 1 (Rp 37.105.000,-)
1. Gaji dan upah (30% dari total anggaran) = Rp
11.100.000,-2. Biaya peralatan = Rp 9.400.000,-
3. Bahan habis pakai – material penelitian = Rp 6.510.000,-
4. Biaya perjalanan = Rp 1.600.000,-
5. Bahan habis pakai – alat tulis kantor = Rp 695.000,- 6. Dokumentasi, pembuatan laporan dan publikasi = Rp
7.800.000,--- + Jumlah biaya tahun ke 1 = Rp 37.105.000,-(tigapuluhtujuh juta seratuslima ribu rupiah)
a.Gaji dan Upah (30% maksimum dari anggaran)
No Tim Peneliti Jumlah Jumlah minggu/bulan
1 Peneliti Utama 1 4 10 15 6.500 3.900.00
0
2 Anggota 2 4 10 12 5.000 4.800.00
0
3 Teknisi/laboran 1 4 10 15 4.000 2400000
000
(sebelas juta seratus ribu rupiah)
b.Biaya peralatan
No Jenis Jumlah Biaya satuan (Rp.) Jumlah (Rp)
1 XRD (sewa) 6 400.000 2.400.000
2 SEM (sewa) 6 500.000 3.000.000
3 Sewa alat lain: pH meter, * sewa lab per bulan Rp.500.000,-.
(sembilan juta empatratus ribu rupiah)
c.Biaya bahan habis pakai (material penelitian)
No Jenis Jumlah Harga satuan (Rp) Jumlah (Rp.)
1 Filter paper 0.2 micron 4 pack 500.000 2.000.000 2 NH4H2PO4 - AR 500 gram 670.000/500 gram 670.000
3 CaCl2.2H2O – AR 500 gram 610.000/500 gram 610.000
4 CuCl2 – AR 250 gram 930.000/250 gram 930.000
5 ZnCl2 – AR 250 gram 725.000/250 gram 725.000
6 HCl 25% - AR 1 liter 625.000/liter 625.000
7 KOH – AR 500 gram 675.000/500 gram 675.000
8 Kertas label utk sampel 5 set 15.000/set 75.000
9 Vial/botol sampel 20 10.000 200.000
Jumlah biaya material
penelitian 6.510.000 (enam juta limaratus sepuluh ribu rupiah)
d.Biaya perjalanan
No Jenis Jumlah Biaya Satuan (Rp) Biaya (Rp)
1 Luar kota (Smg – Jogja)* 4 350.000 1.400.000
2 Dalam kota 4 50.000 200.000
Jumlah biaya perjalanan 1.600.000 * analisa XRD dan SEM. (satu juta enamratus ribu rupiah)
e.Bahan habis pakai - ATK
No Jenis Jumlah Harga satuan (Rp)
1 Kertas HVS 3 rim 50.000 150.000
3 Whiteboard marker 3 15.000 45.000 Jumlah biaya ATK 695.000
f.Dokumentasi, Pembuatan Laporan, Seminar dan Publikasi N
o Uraian Kegiatan
Volum
e Biaya satuan (Rp) Biaya (Rp)
1 Laporan akhir 7 copy 100.000,00 700.000,00
2 Laporan Kemajuan 7 copy 100.000,00 700.000,00
3 Dokumentasi 1 400.000 400.000
4 Seminar 2 2.500.000 5.000.000
5 Publikasi Jurnal 1 1.000.000 1.000.000
Jumlah biaya dokumentasi dll
7.800.000,0 0 (tujuh juta delapanratus ribu rupiah)
2.Rekapitulasi Rincian Biaya Tahun ke 2 (Rp 37.310.000,-)
1. Gaji dan upah (30% dari total anggaran) = Rp
11.190.000,-2. Biaya Peralatan = Rp 10.300.000,-
3. Bahan habis pakai – material penelitian = Rp 5.525.000,-
4. Biaya perjalanan = Rp 1.800.000,-
5. Bahan habis pakai – alat tulis kantor = Rp 695.000,- 6. Dokumentasi, pembuatan laporan dan publikasi = Rp
7.800.000,--- + Jumlah biaya tahun ke 1 = Rp 37.310.000,-(tigapuluh tujuh juta tigaratus sepuluh ribu rupiah)
a.Gaji dan Upah (30% maksimum dari anggaran)
No Tim Peneliti Jumlah Jumlah minggu/bulan
1 Peneliti Utama 1 4 10 12 7.000 3.360.00
0
2 Anggota 2 4 10 12 5.500 5.280.00
0
3 Teknisi/laboran 1 4 10 15 4.250 2.550.00
0
Jumlah gaji dan upah 11.190. 000
(sebelas juta seratus sembilanpuluh ribu rupiah)
b.Biaya peralatan
No Jenis Jumlah Biaya satuan (Rp.) Jumlah (Rp)
2 SEM (sewa) 6 600.000 3.600.000 * sewa lab per bulan Rp.500.000,-.
(sepuluh juta tigaratus ribu rupiah)
c.Biaya bahan habis pakai (material penelitian)
No Jenis Jumlah Harga satuan (Rp) Jumlah (Rp.)
1 Filter paper 0.2 micron 4 pack 500.000 2.000.000 2 NH4H2PO4 - AR 250 gram 600.000/250 gram 600.000
3 CaCl2.2H2O – AR 250 gram 500.000/250 gram 500.000
4 CuCl2 – AR 100 gram 700.000/100 gram 700.000
5 ZnCl2 – AR 100 gram 600.000/100 gram 600.000
6 HCl 25% - AR 1/2 liter 525.000/0,5 liter 525.000
7 KOH – AR 250 gram 400.000/250 gram 400.000
8 Kertas label utk sampel
9 Vial/botol sampel 20 10.000 200.000
Jumlah biaya material
penelitian 5.525.000 (lima juta limaratus duapuluhlima ribu rupiah)
d.Biaya perjalanan
No Jenis Jumlah Biaya Satuan (Rp) Biaya (Rp)
1 Luar kota (Smg – Jogja)* 4 400.000 1.600.000
2 Dalam kota 4 50.000 200.000
Jumlah biaya perjalanan 1.800.000 * analisa XRD dan SEM. (satu juta delapanratus ribu rupiah)
e.Bahan habis pakai - ATK
No Jenis Jumlah Harga satuan (Rp)
1 Kertas HVS 3 rim 50.000 150.000
2 Cartridge/tinta printer 1 500.000 500.000
3 Whiteboard marker 3 15.000 45.000
Jumlah biaya ATK 695.000 (enamratus sembilanpuluhlima ribu rupiah)
f.Dokumentasi, Pembuatan Laporan, Seminar dan Publikasi N
o Uraian Kegiatan Volume Biaya satuan (Rp) Biaya (Rp)
2 Laporan Kemajuan 7 copy 100.000,00 700.000,00
3 Dokumentasi 1 400.000 400.000
4 Seminar 2 2.500.000 5.000.000
5 Publikasi Jurnal 1 1.000.000 1.000.000
Jumlah biaya dokumentasi dll