18 DETEKSI RESISTENSI INH (gen inhA) PADA PENDERITA TUBERCULOSIS KASUS BARU DENGAN MENGGUNAKAN KULTUR CAIR MGIT (Mycobacteria Growth Indicator
Tube) DAN METODE PCR (Polymerase Chain Reaction)
Sitti Romlah (1), Rina Heryawan (2), Siti Rezki (1)
1)Prodi Analis Kesehatan, Stikes Jenderal Achmad Yani, Jalan Terusan Jenderal Sudirman Cimahi
2)RSP dr. H.A Rotinsulu , Jl. Bukit Jarian N0 40 Ciumbuleuit Bandung
Email : [email protected]
ABSTRAK
Tuberculosis (TB) adalah suatu penyakit menular yang disebabkan bakteri Mycobacterium tuberculosis yang sebagian besar menyerang paru tetapi dapat juga mengenai organ tubuh lain. Terjadinya resistensi kuman M. tuberculosis terhadap obat anti tuberculosis (OAT) menimbulkan masalah untuk penatalaksanaan TB karena resiko penularan yang tinggi sehingga menyebabkan M. tuberculosis menjadi semakin virulen.Terjadinya mutasi pada gen inhA yang berperan dalam mengkode enzim ACP reductase akan menyebabkan terjadinya resistensi terhadap INH. Penelitian ini bertujuan untuk mengetahui adanya pita DNA gen inhA penyebab resistensi terhadap INH dengan metode PCR dan elektroforesis dari sampel kultur cair MGIT sehingga didapatkan tingkat sensitivitas dan spesifisitas metode PCR. Sampel penelitian diambil dari semua pasien suspek tuberculosis kasus baru yang ada di Laboratorium Mikrobiologi Rumah sakit Paru Rotinsulu Bandung dengan hasil kultur MGIT positif. Jumlah sampel yang digunakan sebanyak 15 sampel. Kemudian dilakukan isolasi DNA. Setelah didapat isolat DNA dilakukan PCR dan elektroforesis.Hasil penelitian dapat disimpulkan bahwa terdapat kesesuaian dari 5 sampel yang dinyatakan resisten INH pada tes DST dengan teknik PCR dengan tingkat sensitivitas dan spesifisitas 100%.
19 Pendahuluan
Penyakit Tuberculosis (TB) sampai saat ini masih menjadi masalah kesehatan masyarakat di dunia, dimana diperkirakan terdapat 9 juta penduduk dunia terserang penyakit TB dengan kematian 3 juta jiwa. Penyakit TB ini menjadi masalah terutama di negara – negara berkembang termasuk Indonesia. Menurut World Health Organization (WHO), Indonesia merupakan negara dengan kasus TB terbesar ketiga di dunia, setelah Cina dan India. WHO memperkirakan di Indonesia setiap tahunnya terjadi 539.000 kasus baru TB sedangkan TB paru sebesar 236.029 kasus dengan kematian karena TB sekitar 250 orang per hari ( I Made, 2013).
Menurut Rattan (1998 dalam Paul, 1999) angka kematian tiap minggu 52.000 orang atau tiap hari lebih dari 7000 orang yang meninggal. Pengobatan dan kontrol terhadap penyakit TB telah dilakukan, tetapi akhir – akhir ini dilaporkan timbulnya resistensi kuman TB terhadap Isoniazid (INH) dan Rifampicin di Amerika serikat dan negara lainnya di dunia. Terdapatnya resistensi multiple obat terhadap Mycobacterium tuberculosis, tercermin pada meningkatnya angka kasus baru dan angka kematian serta kurang berhasilnya pengobatan terhadap penyakit TB. Pengobatan terhadap penyakit TB memerlukan waktu yang lama, hal ini merupakan problem kesehatan masyarakat di seluruh dunia. Hasil penelitian Aditama dkk, menunjukkan bahwa resistensi primer terhadap INH sebesar 2,16%, rifampisin 0,50%, resistensi sekunder terhadap INH 5,05 %, rifampisin 2,03 % ( Paul, 1999 ).
Pada tahun 1991, Rumah Sakit Persahabatan Jakarta sebagai rumah sakit rujukan nasional penyakit paru dan memiliki laboratorium mikrobiologi yang diakui sebagai “WHO Collaborating Centre”, melaporkan terjadinya 26,5 % kasus resisten terhadap INH. Sedangkan pada tahun 1995 sebanyak 23,97 % kasus resistensi terhadap INH dan sebesar 14,26 % dengan resistensi multi obat (Multi Drug Resistance). MDR-TB adalah
Mycobacterium tuberculosis yang resisten setidaknya terhadap Isoniazid dan Rifampicin yang merupakan Obat AntiTuberkulosis primer atau lini pertama yang paling efektif (Soewarta, 1997).
Terjadinya resistensi kuman M.
tuberculosis terhadap obat anti tuberculosis
biasanya meliputi beberapa jenis obat yang termasuk dalam “first line drugs” yaitu Isoniazid (INH), Rifampicin, Ethambutol, dan
Pyrazinamid. Penyebab utama terjadinya
resistensi terhadap obat anti tuberculosis adalah
pengobatan yang tidak adekuat dimana
pemakaian obat anti tuberculosis yang tidak
sesuai dengan aturan baik dari segi dosis, cara
pemakaian maupun lamanya penggunaan obat
yang akan meyebabkan berkembangnya kuman
yang resisten. Namun resistensi terhadap
kuman M. tuberculosis juga dapat terjadi secara
langsung yaitu jika penderita tertular oleh
kuman M. tuberculosis yang telah resisten dari
penderita TB yang lain ( Nofriyanda, 2010).
Resistensi kuman M. tuberculosis
terhadap obat anti tuberculosis terjadi pada
umumnya karena mutasi sel kuman pada
tingkat gen. Gen yang mengalami mutasi ini
berperan untuk mengkode enzim yang menjadi
target obat anti tuberculosis. Mekanisme
terjadinya resistensi kuman M. tuberculosis
terhadap INH secara biomolekuler dipengaruhi
oleh mutasi pada beberapa gen, tapi mutasi ini
20 carrier protein (ACP) reductase ini menjadi
target utama dari obat INH bekerja dalam
sintesis asam mikolat pada kuman M.
tuberculosis (Nofriyanda, 2010).
Resistensi primer adalah keadaan
resistensi terhadap Obat AntiTuberculosis
(OAT) pada penderita yang belum pernah
mendapat pengobatan dengan OAT
sebelumnya. Sedangkan resistensi sekunder
adalah resistensi yang terjadi pada penderita
yang pernah mendapat OAT sebelumnya ( Paul,
1999 ). Upaya penanggulangan penyakit TB
sudah dilakukan melalui berbagai program
kesehatan di tingkat Puskesmas, berupa
pengembangan strategi penanggulangan TB
yang dikenal sebagai strategi DOTS ( Directly
Observed Treatment Short course =
pengawasan langsung menelan obat jangka
pendek ), yang telah terbukti menekan
penularan, juga mencegah perkembangan multi
drugs resistance (MDR), tetapi hasilnya masih
dirasakan belum sesuai dengan yang
diharapkan ( Helper, 2010 ). Diperlukan
pemeriksaan yang cepat dan mempunyai
sensitivitas yang tinggi sehingga dapat
mempercepat pengobatan tanpa menunggu
konfirmasi hasil kultur yang relatif lama.
Pemeriksaan gold standar untuk TB terdapat 2 jenis pemeriksaan yaitu Pemeriksaan preparat BTA secara langsung dan pemeriksaan kultur padat dan cair, dimana kultur padat yang direkomendasikan oleh WHO adalah menggunakan medium Ogawa dan Low Jensen yang kedua kultur tersebut merupakan kultur padat yang berbasis telur.Tetapi kultur TB tersebut masih memililki kelemahan seperti memerlukan waktu yang cukup lama dan fasilitas metode ini tidak selalu tersedia disetiap laboratorium walaupun memiliki sensitifitas
dan spesifisitas yang cukup tinggi. Selain dengan kultur padat, kultur cair MGIT ( Mycobacteria Growth Indicator Tube ) bisa juga digunakan untuk mendeteksi terhadap pertumbuhan dan uji resistensi terhadap adanya Mycobacterium tuberculosis. Cara ini berdasarkan flouresensi pada pertumbuhan kuman. Tabung gelas berisi media Middlebrook 7H9 yang telah dimodifikasi bersama dengan flouresence quenching – based oxygen sensor yang ditanam didasar tabung. Pertumbuhan kuman dengan cara ini dapat di deteksi dalam waktu 7 – 12 hari dan dibaca secara otomatis dengan Bactec MGIT 960 system (Sari, 2007). Jenis spesies yang dapat di deteksi oleh tabung MGIT ini adalah M. africanum, M. avium complex, M. chelone, M. flafecens, M. fortulinum, M. gastri, M. gordone, M. hemophilum, M. kansasii, M. smegmatis, M. tuberculosis dan lain sebagainya (Kusdarmadji, 2000).
Seiring bertambah pesatnya kemajuan
teknologi saat ini, yakni teknik atau metode
PCR ( Polymerase Chain Reaction ) adalah
suatu teknik atau metode pemeriksaan yang
prinsip kerjanya memperbanyak (amplifikasi)
DNA in vitro secara enzimatis. Pemeriksaan
sputum penderita dapat dilakukan dengan tiga
teknik pemeriksaan, yaitu dengan teknik PCR,
teknik kultur bakteri, dan pemeriksaan BTA
secara mikroskopik. Menurut penelitian Diana
Krisanti dkk pada tahun 2004, deteksi M.
tuberculosis dengan teknik PCR dibandingkan
dengan teknik kultur memiliki sensitivitas 65%,
spesifisitas 40% serta akurasi 57% yang berarti
tidak ada perbedaan yang bermakna, hal ini
dapat diartikan bahwa deteksi M. tuberculosis
dengan teknik PCR sama baiknya dengan
teknik kultur bakteri M. tuberculosis, namun
waktu pemeriksaan dengan teknik PCR lebih
singkat dibandingkan dengan kultur kuman M.
21 Metode Penelitian
Metode penelitian yang digunakan adalah metode deskriptif Penelitian ini dilakukan dalam 3 tahapan. Pertama dilakukan isolasi DNA dari kultur MGIT, kemudian dilakukan amplifikasi dengan metode PCR dan terakhir dilakukan visualisasi menggunakan metode elektroforesis. Isolasi DNA menggunakan metode boilling water pada suhu 95 º C. Amplifikasi dilakukan menggunakan Automated Thermal Cycle dengan siklus meliputi denaturasi awal 95º C selama 5 menit diikuti 40 siklus terdiri dari denaturasi pada 95º C selama 30 detik, annealing pada 50° C selama 30 detik dan ekstensi primer pada 72º C selama 45 detik dan ekstensi akhir pada 72º C selama 5 menit. Elektroforesis menggunakan konsentrasi agarose 1,8%, voltase 50 dalam waktu 60 menit.
Hasil Penelitian
Penelitian diawali dengan melakukan
optimasi kondisi amplifikasi gen inhA dari
kontrol positif. Optimasi dilakukan dengan
melakukan variasi pengenceran sampel :
75%,50%, dan 25%. Didapatkan kondisi
amplifikasi yang optimum adalah dengan
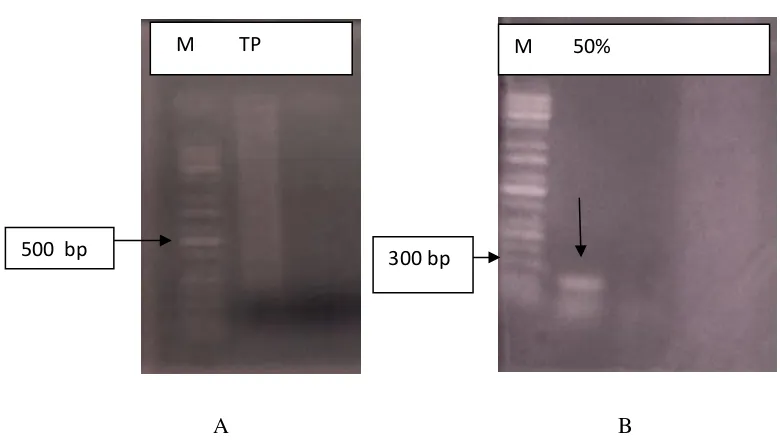
variasi pengenceran 50%.Hasil optimasi dapat
dilihat pada gambar 1 dibawah ini :
A B
Gambar 1 . Hasil optimasi variasi pengenceran sampel. A : Kontrol positif yang tanpa pengenceran, B:
Kontrol positif dengan variasi pengenceran yang optimum di 50%.
Berdasarkan hasil optimasi tersebut, maka dilakukan pemeriksaan terhadap 15 sampel isolat
DNA. Hasil nya dapat dilihat pada gambar 2 berikut :
M TP M 50%
22
Keterangan : Well 4 : 161; well 5 :163; well 6 : sampel 167; well 7: sampel 172; well 8 : 190;
well 9 : sampel 181; well 10 : sampel 171. Well 11 :173; well 12 :196; well 13 : sampel 183,
well 14 : sampel 185; well 15 : sampel 186; well 16 : sampel 200; well 17 : sampel 197; well
18: sampel 212.
Pembahasan
Isolasi DNA merupakan pemisahan
molekul DNA dari molekul atau komponen lain
seperti dinding sel (Shabarni, 2007). Proses
isolasi yang digunakan metode isolasi DNA
sederhana dengan menggunakan prinsip
mekanik / fisika yaitu metode boiling yang
memiliki beberapa kelebihan, diantaranya
mudah dilakukan, biaya murah, waktu yang
dibutuhkan singkat dan lebih ramah
lingkungan. Kekurangan dari metode boiling
ini adalah kualitas DNA yang dihasilkan relatif
lebih rendah dibandingkan dengan metode lain,
hal ini terjadi karena proses pengeluaran DNA
tidak sempurna sehingga masih dimungkinkan
adanya DNA terperangkap dalam sel (Sunarno,
dkk, 2014) dan hal tersebut bisa dilihat pada
hasil optimasi dan PCR pada penelitian ini.
Adanya smear pada hasil PCR menandakan
adanya kontaminan pada hasil isolasi DNA.
Kualitas DNA diukur berdasarkan
kemurniannya pada absorbansi panjang
gelombang 260 / 280 dalam kisaran 1,8 - 2,0
(Sambrook,1989). Kemurnian DNA
merupakan faktor yang penting karena
kontaminasi pada fragmen DNA menyebabkan
produk amplifikasi yang tidak diinginkan ikut
dilipat gandakan (Fatchiyah, 2011). Produk
isolasi DNA yang berkualitas baik ditunjukkan
dengan pita DNA yang terlihat tebal dan bersih,
DNA yang berkualitas baik ditandai dengan
tidak adanya smear pada DNA yang
dielektroforesis (Syafaruddin, 2011).
Dari total 15 sampel yang ada, 5 sampel
hasil yang menandakan adanya pita terdapat
pada hasil elektroforesis adalah no sampel 181,
183,185,186, dan 200, dengan ukuran produk
PCR 207 bp. Ketebalan pita dari hasil sampel
yang positif tidak sama , hal ini tergantung pada
konsentrasi sampel dari hasil isolasi.
Konsentrasi DNA yang diperlukan untuk 500 bp
23 amplifikasi berkisar antara 100-200 pg/µL
(Yuniar, 2003).
Adanya pita yang terbentuk ini
menandakan terjadinya resistensi terhadap
Isoniazid (INH). Isoniazid (INH) termasuk obat
yang bersifat bakterisida dimana INH
membunuh dengan cepat kuman yang sedang
aktif bermultiplikasi. INH aktif bekerja dalam
sintesis asam mikolat yang merupakan salah
satu komponen pembentukkan dinding sel.
Target utama mekanisme ini yaitu mengganggu
enzim enoyl – acyl carrier protein (ACP)
reductase melalui adanya ikatan kovalen INH –
NAD, dengan adanya ikatan ini maka akan
menghambat aktivitas enzimatik inhA sehingga
menganggu sintesis asam mikolat. Terjadinya
mutasi pada gen inhA yang berperan dalam
mengkode enzim enoyl – acyl carrier protein
(ACP) reductase akan menyebabkan terjadinya
resistensi terhadap INH (Nofriyanda, 2010).
Dari hasil PCR yang positif
menunjukkan adanya pita dengan ukuran 207
pb adalah pada nomor sampel 181, 183, 185,
186 dan 200. Kemudian dibandingkan dengan
hasil DST untuk mengetahui tingkat sensitivitas
serta spesifisitas dari PCR yang dilakukan.
Berikut tabel hasil perbandingan antara DST
dengan teknik PCR seperti yang terlihat pada
tabel 4.1 dibawah ini.
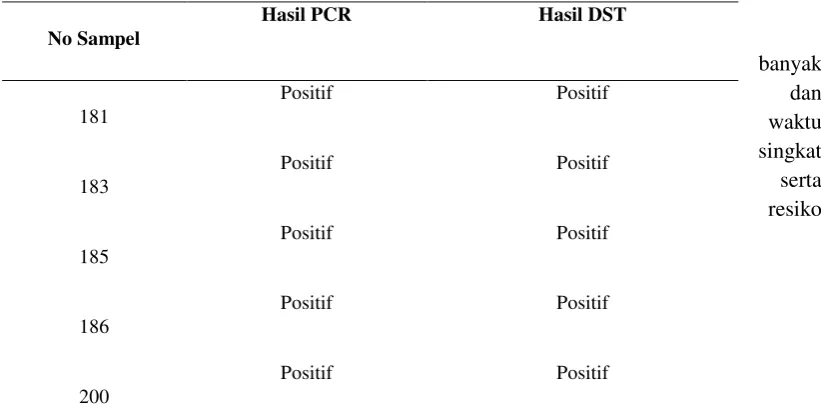
Tabel 1.1 Hasil Perbandingan PCR positif dan DST dari kultur cair MGIT
Dari 15 sampel terdapat 5 sampel positif menggunakan PCR . Dari tabel 1.1 diatas, menunjukkan adanya kesesuaian antara DST serta teknik PCR pada 5 sampel hasil positif. Berdasarkan hasil pemeriksaan tersebut dapat dinyatakan tingkat sensitivitas dan spesifisitas pada metode PCR tersebut sebesar 100%, karena adanya kesesuaian hasil tadi serta mampu mendeteksi sampel dalam jumlah
banyak kelebihan sehingga sangat menentukan tingkat sensitivitas dan spesifisitas yaitu salah satunya dapat mendeteksi keberadaan kuman walau jumlahnya hanya 1–10 buah kuman. Prinsip PCR sendiri terdiri atas beberapa siklus dimana pada setiap siklus terjadi penggandaan materi genetik dan jika siklus ini dilakukan berulang-ulang, maka materi genetik yang diperoleh akan
24 menjadi banyak sehingga mempermudah
deteksi keberadaannya (Chandra, 2007).
Optimasi PCR dilakukan untuk
mendapatkan kondisi PCR yang optimal
sehingga dihasilkan produk PCR spesifik, yaitu
terbentuk pita DNA tebal dengan ukuran sesuai
yang diharapkan. Pada penelitian ini digunakan
sepasang primer forward dan reverse dengan
panjang primer 18 pasang basa, komposisi
jumlah Guanin dan Cytosin sebesar 50%
hampir sama dengan DNA target yang akan
diamplifikasi, hal ini berkaitan dan dapat
menentukan kandungan G dan C yang baik
untuk primet adalah sekitar 40-60%.
Konsentrasi MgCl2 yang digunakan pada optimasi terhadap kontrol positif serta sampel pada penelitian ini yaitu 1,5 mM, konsentrasi yang digunakan tersebut optimum atau ideal karena konsentrasi ion Mg2+ dalam reaksi PCR bisa berkisar antara 0,5 - 5,0 mM. Ion Mg2+ berperan dalam membentuk kompleks dengan dNTP sehingga dNTP menjadi semakin larut, meningkatkan aktivitas enzim DNA polymerase. Konsentrasi MgCl2 juga
spesifisitas metode PCR dengan adanya primer yang spesifik. Primer yang memiliki ukuran panjang 18-24 pasang basa akan menghasilkan produk PCR spesifik karena akan mempermudah proses penempelan primer dengan cetakanDNA pada saat annealing. Primer dengan panjang kurang dari 18 pasang basa akan menjadikan spesifisitas primer rendah (Darmo, 2001).
Primer memegang peranan penting untuk spesifisitas maksimal efisiensi PCR. Sensitivitas PCR dipengaruhi oleh persentase kandungan G dan C. Persentase berpengaruh besar terhadap spesifitas dan jumlah produk PCR (Mukhammad Asy’ari, 2005)
Konsentrasi DNA yang digunakan pada optimasi terhadap kontrol positif serta sampel pada penelitian ini tidak diketahui karena tidak dilakukan pengukuran konsentrasi DNA terlebih dahulu sebelum dilakukan PCR, akan tetapi pada penelitian ini dilakukan pengenceran dari larutan stok kontrol DNA dan diperoleh pengenceran yang optimal yaitu pada pengenceran 50% karena pada pengenceran tersebut didapatkan pita DNA pada ukuran 207 pb.
DAFTAR PUSTAKA
Handoyo Darmo, Rudiretna Ari. (2000 – 2001). Prinsip Umum Dan Pelaksanaan Polymerase Chain Reaction (PCR), 9(1), 18 – 24.
Hewajuli, D.A. (2013). Perkembangan Teknologi Reverse Transcriptase – Polymerase Chain Reaction dalam Mengidentifikasi Genom Avian Influenza dan Newcastle Diseases, (27).
Kusdarmadji, (2000), Uji Diagnostik Mycobacteria Growth Indicator Tube (MGIT) Pada Penderita Tuberkulosis Paru Tersangka Di Rumah Sakit Umum Pusat Dr. Kariadi Dan BP4 Semarang, Tesis, Semarang, Universitas Diponegoro.
25 Nofriyanda. (2010). Analisis Molekuler Pada
Proses Resistensi Mikobakterium Tuberkulosis Terhadap Obat – Obat Anti Tuberkulosis. Padang: Fakultas Kedokteran Unand
Nur F., (2011), Polimorfisme ikan Kerapu Macan ( Ephinephelus fuscoguttatus) yang Tahan Bakteri Vibrio alginolitycus Dan Toleran Salinitas Rendah Serta Salinitas Tinggi, Skripsi, Makassar, Universitas Hasanudin.
Nuraida, D. (2010). Pemilihan Bagian Tanaman Kapas Gossypium hirsutum Sebagai Bahan Untuk Isolasi DNA. Tuban, 580.
Nurruhwati, Isni. Mulyani, Yuniar., Purwanto, Agus. (2003). Perbandingan Beberapa Metode Isolasi DNA Untuk Deteksi Dini Koi Herpes virus (KHV) Pada Ikan Mas (Cyprinus carpio. L.). Jatinangor: Fakultas Perikanan dan Ilmu Kelautan Universitas Padjajaran.
Onggowidjaja, P., Jasaputra, D.K., Soeng, S. (2005). Akurasi Deteksi Mycobacterium tuberculoisis Dengan Teknik PCR Menggunakan “Primer X” Dibandingkan Dengan Pemeriksaan Mikroskopik (BTA) Dan Kultur Sputum Penderita Dengan Gejala Tuberkulosis Paru, 5(1), 7.
Pranawaty, R.N., Buwono, I.D., Liviawaty, E. (2012). Aplikasi Polymerase Chain Reaction (PCR) Konvensional Dan Real Time PCR Untuk Deteksi White Spot Syndrome Virus Pada Kepiting. Jurnal Perikanan Dan Kelautan, 3(4), 62.
Sambrook, J., Fritsch, E.F, dan Maniatis, T. 1989. Molecular Cloning. Cold Spring Harbor Press. University of Texas South Western Medical Centre, Texas.
Sonia Z., (2014), Amplifikasi DNA Leptospira dengan Menggunakan Metode Isulated Isothermal Polymerase Chain Reaction (ii-PCR), Skripsi, Jakarta, UIN Syarif Hidayatullah.
Sunarno., Muna Fauzul., Fitri Nyoman. (2014). Metode Cepat Ekstraksi DNA Corynebacterium diphtheria Untuk Pemeriksaan PCR, 42(2), 88 – 90.
Syafaruddin dan T.J. Santoso. 2011. Optimasi Metode Isolasi dan Purifikasi DNA yang Efisien dan Efektif pada Kemiri Sunan (Reutalis trisperma (Blanco) Airy Shaw). J. Littri. 17(1).
Syahrini, H. (2008), Tuberkulosis Paru Resisten Ganda, Medan, Universitas Sumatera Utara.
Wahyudi, T. Danang. (2006). Sensitivitas dan Spesifisitas Pendekatan Sindrom dan Jumlah Sel Polimorfonuklear (PMN) Pada Infeksi Chlamydia trachomatis Genital Wanita Dibandingkan dengan Hasil Pemeriksaan Polymerase Chain Reaction (PCR), Makalah, Jakarta, Universitas Indonesia.