BAB III
METODE PENELITIAN
A. Rancangan Penelitian
Penelitian ini adalah penelitian deskriptif eksploratif, yaitu penelitian yang menjajaki sesuatu informasi sementara atau kasus yang belum dikenal atau hanya sedikit diketahui yang berkaitan dengan pengumpulan data untuk memberikan gambaran atau penegasan suatu konsep atau gejala, juga menjawab.1 Penelitian ini bertujuan untuk mendeskripsikan dan menggali informasi tentang kualitas mikrobiologi dan kelayakan konsumsi minuman olahan “Teh Poci” di Kecamatan Jekan Raya Palangka Raya.
B. Populasi dan Sampel Penelitian
1. Populasi
Populasi dalam penelitian ini adalah seluruh minuman olahan “Teh poci” yang dijual di Kecamatan Jekan Raya.
2. Sampel
Sampel dalam penelitian ini adalah sebagian dari minuman olahan “Teh poci” yang
diambil dari masing-masing penjual minuman olahan yang terpilih. Tahapan pengambilan sampel dilakukan dengan dua kali tahapan, yakni pengambilan sampel
kelurahan dan pengambilan sampel minuman olahan “Teh poci”.
1
a) Teknik pencuplikan sampel
Teknik dalam pencuplikan sampel depot “Teh poci” menggunakan teknik
Purposive sampling. Purposive sampling merupakan teknik pengambilan sampel
dengan memperhatikan pertimbangan-pertimbangan yang dibuat oleh peneliti.2
b)Pemilihan sampel kelurahan
Pengambilan sampel dilakukan dengan menghitung seluruh penjual
minuman olahan “Teh poci” yang ada di Kecamatan Jekan Raya kota Palangka Raya. Pemilihan sampel penjual minuman olahan “Teh poci” merujuk pada masing-masing Kelurahan yang ada di Kecamatan Jekan Raya. Berdasarkan hasil
observasi ditemukan bahwa jumlah penjual “Teh poci” di Kecamatan Jekan Raya
adalah sebanyak 24 unit, yang tersebar pada masing-masing Kelurahan sebagai
berikut:
Kelurahan Menteng = 8 Depot Teh poci
Kelurahan Palangka = 10 Depot Teh poci
Kelurahan Bukit Tunggal = 6 Depot Teh poci
Kelurahan Petuk Ketimpun = 0 Depot Teh poci
Total = 24 Depot Teh poci3
2
Hadi. S. 2004. Metodologi Penelitian. Andi offset. Yogyakarta. Hal: 91 3
c) Pengambilan Sampel Minuman Olahan
Teknik pengambilan sampel yang diperlukan dapat dibatasi pada 10-20%
dari jumlah sampel keseluruhan, karena dianggap sudah mampu mewakili data
yang diinginkan.4 Berdasarkan teknik pengambilan sampel tersebut, maka
diperoleh 7 depot “Teh Poci” yang diambil sebagai lokasi pencuplikan sampel
jajanan minuman olahan “Teh poci”. Banyaknya pengulangan penelitian untuk
menambah keakuratan data yang diperoleh dengan ini ditentukan dengan
menghitung banyaknya sampel dengan rumus federer:
t = banyak depot terpilih
Hujjatusnaini, Noor. Kelayakan Konsumsi Minuman Ringan Di Lingkungan Kampus STAIN Palangkaraya Berdasarkan Kualitas Mikrobiologi, Kimia,Dan Fisik Air, Laporan Hasil Penelitian Individu Dosen STAIN Palangka Raya. November 2012. Hal: 27
5
C. Tempat dan Waktu Penelitian
Penelitian dilaksanakan selama 2 (dua) bulan dari tanggal 3 April sampai dengan 20 Mei, di Laboratorium Mikrobiologi Program Studi Tadris Biologi Jurusan Tarbiyah Sekolah Tinggi Agama Islam Negeri Palangka Raya.
D. Instrumen Penelitian
Alat dan bahan yang digunakan dalam penelitian ini adalah: 1. Alat
Alat yang digunakan dalam penelitian ini adalah alat untuk analisa yang meliputi: Tabung reaksi, Neraca analitik, Labu erlenmeyer, Spatula, Rak tabung reaksi, Ose, Tabung Durham, Pipet volume, Lampu spritus, Alumunium foil, Autoclave, Laminar Air Flow (LAF), Inkubator, Kapas, Hot plate,dan Oven.6
2. Bahan
Untuk uji kualitasnya digunakan bahan seperti: Sampel Teh Poci, Aquades steril, Alcohol 70%, Vaseline, Media Kaldu Laktosa (Beef Extract, Pepton dan
lactose), Briliant Green Lactose Bile Broth (Pepton, Lactose dan Oxgall Brilliant Green) dan Mac Conkey Agar (Pepton, Proteose Pepton, Lactose dan Agar Powder).7
6
Hujjatusnaini, Noor. Penuntun Praktikum Mikrobiologi. Palangka Raya. 2013 7
E. Prosedur Penelitian
Penelitian ini dilakukan sebanyak 4 kali pengulangan dengan dilakukan dalam skala laboratorium dengan tahapan penelitian sebagai berikut:
1. Pembuatan media
a. Menyiapkan medium KL (Kaldu Laktosa)
Pembuatan medium kaldu laktosa (KL) dengan ketentuan perbandingan sebagai berikut:
1) Beef (3 gram)
2) Pepton (5 gram)
3) Lactose (5 gram)
4) 1000 ml
a) Menimbang media yang
dibutuhkan kemudian memasukkan dalam labu erlenmeyer 250 ml, kemudian memanaskan dengan hot plate sampai media homogen.
b) Memasukkan media sebanyak 4 ml
medium KL ke dalam 9 tabung rekasi yang sudah ada tabung Durham.
c) Kemudian menyumbat seluruh
steril. Mensterilisasikan pada autoclave dengan suhu 121 °C dengan tekanan 15 lbs selama 15-20 menit.8
b. Pembuatan Media BGLBB
(Briliant Green Laktose Bile Broth)
Pembuatan medium Brilliant Green Lactose Bile Broth (BGLBB) dengan ketentuan perbandingan sebagai berikut:
1. Serbuk BGLBB (40 gram)
2. Aquades 1000 ml
a) Menimbang media yang dibutuhkan kemudian memasukkan dalam labu erlenmeyer 250 ml, kemudian memanaskan dengan hot plate sampai media homogen.
b) Memasukkan media sebanyak 4 ml medium BGLBB ke dalam 9 tabung rekasi yang sudah ada tabung Durham.
c)
Kemudian menyumbat seluruh tabung reaksi yang berisi tabung Durham dan medium BGLBB dengan kapas steril. Mensterilisasikan pada
autoclave dengan suhu 121 °C dengan tekanan 151 lbs selama 15-20 menit.9
8
Hujjatusnaini, Noor. Petunjuk Praktikum Mikrobiologi. Palangkaraya. Sekolah Tinggi Agama Islam Negeri Palangka Raya. 2013. Hal.2-3
9
c. Pembuatan Media MCA (Mac Conkey Agar)
Pembuatan medium Mac Conkey Agar (MCA) dengan ketentuan sebagai berikut: 1.Serbuk MCA (50 gram)
2.Aquades 1000 ml
a) Menimbang media yang dibutuhkan kemudian memasukkan dalam labu erlenmeyer 250 ml, kemudian memanaskan dengan hot plate sampai media homogen.
b) Memasukkan media sebanyak 10 ml medium MCA ke dalam 9 cawan petri tanpa ada gelembung udara pada medium MCA.
c) Kemudian membungkus seluruh cawan petri dan medium MCA kemudian dengan kertas sampul. Mensterilsasikan pada autoclave dengan suhu 121 °C dengan tekanan 151 lbs selama 15-20 menit.10
d. Sterilisasi Alat dan Bahan Medium
Sterilisasi alat dan bahan medium sebagai berikut : 1.Mengisi autoclave dengan air sebatas sarangan.
2.Mengoleskan vaselin dengan tipis dan merata pada tepi autoclave pada bagian tempat dan tutupnya.
3.Memasukkan semua alat dan bahan yang akan disterilisasikan ke dalam
autoclave, memasukkan selang uap autoclave pada bagian lubang,
memposisikan tanda panah pada tutup dan wadah autoclave sebelum diratakan
10
kedudukan tutupnya, meratakan bagian tutup autoclave sampai benar-benar seimbang, kemudian mengunci dengan sempurna.
4.Mengatur posisi katup autoclave dengan posisi tegak, kemudian melipat katup sampai pada posisi mendatar.
5.Menunggu sampai pada keluar uap air pada lubang katup, kemudian melipat katup sampai pada posisi mendatar.
6.Menunggu sampai jarum manometer menunjukkan angka 15, berarti tekanan di dalam autoclave telah mencapai 15 lbs, mengatur panas sampai tekanan tetap bertahan pada posisi 15 lbs selama 15 menit.
7.Setelah 15 menit, mematikan arus listrik. Kemudian menunggu sampai tekanan pada jarum manometer kembali normal, yaitu pada posisi 0 kembali.
8.Menegakkan posisi katup uap autoclave, kemudian membuka autoclave dan mengeluarkan dengan perlahan semua alat dan bahan yang ada di dalam
autoclave.
9.Meletakkan semua alat dan bahan yang dari dalam autoclave ke atas nampan, meletakkan pada posisi mendatar untuk memperoleh medium lempeng.
10.Menunggu 1-3 hari. Jika medium tetap bersih dan tidak ditumbuhi jamur atau bakteri, maka medium dapat digunakan. Jika medium belum dipakai dalam waktu dekat, medium dapat disimpan di dalam lemari es, dengan membungkusnya menggunakan kertas sampul.11
11
Pengujian Kualitas Mikrobiologi Sampel
a. Tes pendugaan
1) Menyediakan tabung 100 ml sampeles teh pociyang akan diperiksa. Menyiapkan 3 tabung rekasi berisi 9 ml aquades dan 9 tabung reaksi berisi Durham yang telah diisi 4 ml kaldu laktosa.
2) Secara aseptic menginokulasi 1ml sampel es teh poci ke dalam tabung reaksi berisi 3 ml aquades steril lalu mengocok tabung reaksi tersebut.
3) Melakukan pengenceran dengan cara yang sama, sehingga diperoleh pengenceran 1:100 dan 1:1000.
4) Menyiapkan 9 tabung reaksi berisi medium KL, beri kode A1, A2, A3, B1, B2, B3, C1, C2, C3.Memasukkan 1 ml sampel dengan pengenceran 1:10 pada medium KL berkode A1, A2, A3. Memasukkan 1 ml sampel dengan pengenceran 1:100 pada medium KL berkode B1, B2, B3. Memasukkan sebanyak 1 ml sampel dengan pengenceran 1:1000 pada medium KL berkode C1, C2, C3.
5) Menginkubasi semua tabung reaksi selama 1-2 X 24 jam dengan suhu 370C. Jika terdapat gas pada tabung Durham, maka akan dilanjutkan pada tes penegasan. Jika tidak terdapat gas pada dasar tabung Durham, maka tidak dilanjutkan pada tes penegasan.12
12
b. Tes penegasan
1) Melakukan inokulasi Teh Poci yang menghasilkan gas pada tes pendugaan. Melakukan seperti pada tes pendugaan, tetapi medium yang digunakan adalah medium BGLBB sebanyak 9 tabung reaksi 4 ml.
2) Memasukkan semua tabung reaksi ini dalam incubator pada suhu 450C selama 1-2 X 24 jam. Jika terdapat gas pada bagian dasar tabung Durham maka dalam sampel tersebut terdapat bakteri Coliform. Untuk menghitung angka MPN bakteri Coliform yang terkandung dalam sampel teh poci dilihat dengan menggunakan tabel MPN.
3) Meinokulasi satu ose sampel es teh poci pada medium MCA dengan arah zig-zag. Kemudian menginkubasikan pada suhu 370C selama 1-2 X 24 jam. Mengamati koloni bakteri yang memfermentasikan lactose yang ditandai dengan koloni berwarna merah, sedangkan koloni yang tidak berwarna merupakan koloni yang tidak dapat memfermentasikan laktose.
4) Menghitung jumlah koloni bakteri tersebut.13
c. Tes Kepastian
Untuk uji kepastian medium yang digunakan adalah Mac Concey Agar
(MCA), medium ini digunakan untuk memastikan dan melihat nilai MPN bakteri
Coliform, Coliform fecal dan Escherichia coli pada medium buatan yang
13
selanjutnya hasil dari pengamatan tersebut dibandingkan dengan standar baku mutu keamanan pangan dan minuman dari PERMENKES No. 492 Tahun 2010. Adapun cara kerja uji kepastian, antara lain:
1)Melakukan inokulasi sampel air yang menghasilkan gas pada uji pendugaan. Perlakuan seperti tes pendugaan tetapi yang digunakan ialah medium Brilliant Green Lactose Bile Broth (BGLBB) sebanyak 9 tabung reaksi 3 ml.
2)Memasukkan semua tabung reaksi ini dalam inkubator pada suhu 45oC selama 1 x 24 jam, jika terdapat gas pada bagian dasar tabung Durham berarti dalam sampel air terdapat bakteri Coliform. Jika tidak ada gas maka menunggu sampai 2x24 jam. Jika ada gas berarti sampel air ini mengandung bakteri
Coliform. Untuk mengetahui angka MPN bakteri Coliform yang terkandung dalam sampel air ini melihat tabel MPN.
3)Menginkulasi satu ose sampel air tanah pada medium Mac Conkey Agar dengan arah zig-zag. Kemudian mengikubasikan pada suhu 37oC selama 1x24 jam atau 2x24 jam. Lalu mengamati koloni bakteri yang menfermentasikan laktosa, sedangkan koloni yang tidak berwarna merupakan koloni yang tidak memfermentasikan laktosa, menghitung jumlah koloni kedua kelompok bakteri ini.14
F. Teknik Pengumpulan Data
14
Teknik pengumpulan data pada penelitian ini adalah teknik observasi langsung terhadap objek penelitian, melalui kegiatan pengukuran terhadap kekeruhan dan gas yang terdapat pada dasar tabung Durham. Pengukuran data dilakukan berjumlah 252 tabung reaksi berumur 2x24 jam setelah pelaksanaan penelitian.
Data diambil pada semua unit penelitian, yaitu berupa hasil perhitungan gas dan kekeruhan yang terdapat pada setiap dasar tabung Durham baik yang terdapat pada media KL (Kaldu Laktosa) dan BGLBB (Briliant Green Laktose Bile Broth) dan koloni bakteri yang berwarna merah pada media MCA (Mac Conkey Agar). Hasil pada pemeriksaan baik yang positif dan negatif disajikan dalam bentuk tabel. Pemeriksaan sampel dinyatakan positif apabila terbentuk gas dan kekeruhan dalam tabung yang berisi media KL (Kaldu Laktosa) dan media media BGLBB (Brilliant Green Laktose Bile Broth). Hasil disajikan dalam bentuk persentase dan hasil yang positif dicatat dan dicocokkan berdasarkan angka yang tertera dalam MPN/100 ml.
G. Teknik Analisis Data
PERMENKES/RI/No492/MENKES/Per/IV/2010, maka dapat disimpulkan bahwa air tanah tersebut tidak layak untuk dikonsumsi.15
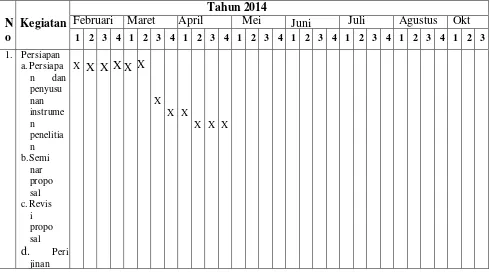
H. Jadwal Penelitian
Penelitian ini dilaksanakan pada bulan Februari sampai Oktober 2014. Jadwal kegiatan penelitian disusun dalam Tabel 3.5 sebagai berikut:
Tabel 3.1 Jadwal Kegiatan Penelitian