Abstrak
UJI KUALITAS BIODIESEL DENGAN PEMBANDING BIODIESEL STANDAR PRODUKSI BPPT BERDASAR PARAMETER KANDUNGAN
SENYAWA, TURBIDITAS, DAN VISKOSITAS KINEMATIK
Pada penelitian ini telah dibuat biodiesel dari jelantah dan metanol dengan variasi konsentrasi NaOH dalam metanol berturut-turut 3 g/60 ml, 3 g/70 ml, 3 g/80 ml, 3 g/90 ml, dan 3 g/100 ml. Untuk mengetahui senyawa yang terkandung pada biodiesel digunakan UV /Vis Spektrofotometer SP8-400 dan Gas Chromatography (GC). Selain itu dilakukan pula pengukuran turbiditas dan viskositas kinematik. Hasil
yang diperoleh dibandingkan terhadap senyawa yang terkandung, turbiditas, dan viskositas kinematik biodiesel standar produksi Badan Pengkajian dan Penerapan Teknologi (BPPT). Dari hasil pengukuran sampel biodiesel diketahui bahwa senyawa penyusun pada sampel biodiesel mirip dengan senyawa biodiesel standar. Nilai turbiditas sampel biodiesel antara 0,69-1,72 NTU dan nilai viskositas kinematik sampel biodiesel 4,19 - 6,49 mm2/s.
Abstract
BIODIESEL QUALITY TEST BY COMPARING ITS COMPOUNDS CONTAIN, TURBIDITY, AND KINEMATIC VISCOSITY TO THE BPPT
STANDARD BIODIESEL PRODUCT
In this research, biodiesel is made from jelantah and methanol using NaOH as catalyst. The mount of jelantah is 500 ml with variation of NaOH concentration in metanol are 3 g/60 ml, 3 g/70 ml, 3 g/80 ml, 3 g/90 ml, and 3 g/100 ml respectively. The UV/Vis Spectrophotometer SP8-400 and Gas Chromatography (GC) are used to analize the compounds contain in biodiesel. Inspite of UV/Vis Spectrophotometer SP8-400 and GC analysis, the measurement of turbidity and kinematic viscosity are also perfomed. The obtained results compare to the compounds contain, turbidity, and kinematic viscosity of Agency for the Assessment and Application of Technology (BPPT) standard biodiesel. From the biodiesel samples results, it is known that the compound of biodiesel samples similar with the standard biodiesel. The biodiesel samples turbidity values are in the range 0.69-1.72 NTU and kinematic viscosity in the range 4.19-6.49 mm2/s.
UJI KUALITAS BIODIESEL DENGAN PEMBANDING BIODIESEL STANDAR PRODUKSI BPPT BERDASAR PARAMETER KANDUNGAN
SENYAWA, TURBIDITAS, DAN VISKOSITAS KINEMATIK
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Sains
Program Studi Fisika
Disusun oleh : B. ADE DIRGANTARA
NIM : 043214006
JURUSAN FISIKA
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
2010
BIODIESEL QUALITY TEST BY COMPARING ITS COMPOUNDS CONTAIN, TURBIDITY, AND KINEMATIC VISCOSITY TO THE BPPT
STANDARD BIODIESEL PRODUCT
A THESIS
Presented as a Partial Fullfillment of the Requirements To Obtain The Sarjana Sains
In Phisycs Department
by :
B. ADE DIRGANTARA NIM : 043214006
PHYSICS STUDY PROGRAM
PHYSICS DEPARTMENT
FACULTY OF SCIENCE AND TECHNOLOGY
SANATA DHARMA UNIVERSITY
YOGYAKARTA
2010
KUPERSEMBAHKAN KEPADA
Seluruh mahluk di bumi, guna kehidupan yang lebih beradab, dan bermartabat,
Bangsa Indonesia sebagai bentuk pengabdianku,
Masyarakat Desa Rengas yang kucintai.
“Tak ada kata lain selain berjuang untuk menang. Karena sejatinya hidup
adalah perjuangan. Manusia dilahirkan dengan segala potensinya, maka manusia
yang mencapai kesempurnaan dan pencerahan adalah manusia
yang berjuang dan terus berjuang”
“Sebelumnya aku hanya mendengar hal-hal ini, sekarang aku hidup dengan
mengalaminya sendiri. Kini dengan pengetahuan yang dalam aku menembusnya
dan membuktikan secara jelas”
(Samyutta Nikaya . V, 226)
Persembahan yang sangat berarti ini pula kuberikan kepada :
Orangtuaku,
Y. Widodo & Martina
Desta Gunara
Dionisius W.
Fransisca E.S.P.
Gregorius V.K.
Sahabat, Kekasih, Temanku yang menyertai perjuangan ini....
Manasikara
Bahwa
Diri Kita Harus berarti Bagi Sesama.
Mari wujudkan dunia menjadi indah dengan kasih dan cinta
Abstrak
UJI KUALITAS BIODIESEL DENGAN PEMBANDING BIODIESEL STANDAR PRODUKSI BPPT BERDASAR PARAMETER KANDUNGAN
SENYAWA, TURBIDITAS, DAN VISKOSITAS KINEMATIK
Pada penelitian ini telah dibuat biodiesel dari jelantah dan metanol dengan variasi konsentrasi NaOH dalam metanol berturut-turut 3 g/60 ml, 3 g/70 ml, 3 g/80 ml, 3 g/90 ml, dan 3 g/100 ml. Untuk mengetahui senyawa yang terkandung pada biodiesel digunakan UV /Vis Spektrofotometer SP8-400 dan Gas Chromatography (GC). Selain itu dilakukan pula pengukuran turbiditas dan viskositas kinematik. Hasil
yang diperoleh dibandingkan terhadap senyawa yang terkandung, turbiditas, dan viskositas kinematik biodiesel standar produksi Badan Pengkajian dan Penerapan Teknologi (BPPT). Dari hasil pengukuran sampel biodiesel diketahui bahwa senyawa penyusun pada sampel biodiesel mirip dengan senyawa biodiesel standar. Nilai turbiditas sampel biodiesel antara 0,69-1,72 NTU dan nilai viskositas kinematik sampel biodiesel 4,19 - 6,49 mm2/s.
Abstract
BIODIESEL QUALITY TEST BY COMPARING ITS COMPOUNDS CONTAIN, TURBIDITY, AND KINEMATIC VISCOSITY TO THE BPPT
STANDARD BIODIESEL PRODUCT
In this research, biodiesel is made from jelantah and methanol using NaOH as catalyst. The mount of jelantah is 500 ml with variation of NaOH concentration in metanol are 3 g/60 ml, 3 g/70 ml, 3 g/80 ml, 3 g/90 ml, and 3 g/100 ml respectively. The UV/Vis Spectrophotometer SP8-400 and Gas Chromatography (GC) are used to analize the compounds contain in biodiesel. Inspite of UV/Vis Spectrophotometer SP8-400 and GC analysis, the measurement of turbidity and kinematic viscosity are also perfomed. The obtained results compare to the compounds contain, turbidity, and kinematic viscosity of Agency for the Assessment and Application of Technology (BPPT) standard biodiesel. From the biodiesel samples results, it is known that the compound of biodiesel samples similar with the standard biodiesel. The biodiesel samples turbidity values are in the range 0.69-1.72 NTU and kinematic viscosity in the range 4.19-6.49 mm2/s.
KATA PENGANTAR
Puji dan Syukur penulis panjatkan kehadirat Tuhan Yang Maha Esa, karena segala rahmat dan kasih karunia-Nya, penulis dapat menyelesaikan skripsi yang berjudul “UJI KUALITAS BIODIESEL DENGAN PEMBANDING BIODIESEL STANDAR PRODUKSI BPPT BERDASAR PARAMETER KANDUNGAN SENYAWA, TURBIDITAS, DAN VISKOSITAS KINEMATIK” sebagai salah satu syarat untuk memperoleh gelar sarjana sains pada Program Studi Fisika Fakultas Sains dan Teknologi Universitas Sanata Dharma Yogyakarta.
Penulis menyadari tanpa adanya bantuan dan dukungan dari berbagai pihak, skripsi ini tidak dapat terselesaikan dengan baik. Oleh karena itu, secara khusus penulis ingin mengucapkan terima kasih kepada :
1. Bapak Dr. Ign. Edi Santosa, M.S selaku dosen pembimbing yang dengan sabar telah membimbing, membantu dan menyemangati selama proses penulisan skripsi ini.
2. Ir. Sri Agustini Sulandari, M.Si selaku Ketua Jurusan Fisika.
3. Dr. Drs. (Vet). Asan Damanik, M.Si selaku dosen pembimbing akademik dan dosen penguji.
4. Dwi Nugraheni Rositawati, M.Si selaku dosen penguji. 5. Seluruh Dosen Prodi Fisika yang telah membagikan ilmunya.
6. Aryo Wicaksono, S.Sc dan Aditya, S.T yang telah bekerja sama dalam pembuatan biodiesel.
7. Ibu Yuliana, S.Psi dan Pihak Hotel Quality yang telah bekerja sama dalam penyediaan minyak jelantah sebagai bahan baku biodiesel.
8. BPPT yang telah bersedia membantu dalam pengadaan standar biodiesel.
9. Kedua orang tua saya (Bapak Y. Widodo dan Ibu Martina), yang telah memberikan dukungan baik materi maupun doa.
10. Kakak saya Desta, adik-adik saya Dion, Putri dan Vizar yang telah memberikan dorongan dalam menyelesaikan studi ini.
11. Dhani Manasikara, S.Psi, M. Psi kekasih dan sahabatku yang selalu mendukung, memotivasi selama penelitian ini. Terima kasih juga buat Tri Ratana Satya Paramitha, SE yang telah membantu fasilitas komputer.
12. Bapak Daryono beserta keluarga dan Bapak Y. Supama, M.Hum beserta keluarga. Terima kasih atas bantuan materi, bimbingan dan nasehatnya.
13. Teman seangkatan Sujadmoko, S.Si, Erlina Ekawati, dan Fransiska Endang Kinasih, S.Si yang senantiasa saling menyemangati dan mewarnai angkatan 2004. 14. Seluruh karyawan Universitas Sanata Dharma khususnya Mas Bimo, Mas Sis,
Pak Gito dan Mas Ngadiyo.
15. Semua pihak yang sudah membantu penulis dalam menyelesaikan skripsi ini.
DAFTAR ISI
HALAMAN JUDUL………... HALAMAN PERSETUJUAN PEMBIMBING………. HALAMAN PENGESAHAN………. HALAMAN PERSEMBAHAN………. PERNYATAAN KEASLIAN KARYA………. ABSTRAK...……… ABSTRACT ………. KATA PENGANTAR...……….. DAFTAR ISI………... DAFTAR TABEL………... DAFTAR GAMBAR……….. BAB I. PENDAHULUAN……….. I. 1 Latar Belakang………...
II.2.1 Pengukuran Kandungan Senyawa... II.2.1.1. UV/Vis Spektrofotometer... II.2.1.2 Gas Chromatography... II.2.2 Pengukuran Turbiditas... II.2.3 Pengukuran Viskositas... BAB III. METODE PENELITIAN………... III.1 Tempat Penelitian………... III.2 Alat dan Bahan……… III.3 Pembuatan ...………... III.4 Pengukuran………... BAB IV. HASIL DAN PEMBAHASAN………....
IV.1 Hasil……… IV.2 Pembahasan……….... BAB V. KESIMPULAN DAN SARAN………. V.1 Kesimpulan………... V.2 Saran……….... DAFTAR PUSTAKA……….. LAMPIRAN A. Hasil Pengukuran Kandungan Senyawa.………... LAMPIRAN B. Hasil Pengukuran Turbiditas...………. LAMPIRAN C. Hasil Pengukuran Waktu Alir Biodiesel...………... LAMPIRAN D. Hasil Perhitungan Viskositas Kinematik...
DAFTAR TABEL
Halaman
Tabel 1.1 Intensitas pemakaian energi di Indonesia... 1 Tabel 4.1 Turbiditas awal dan akhir dan viskositas kinematik biodiesel
dengan komposisi NaOH 3 gram dan jelantah 500 ml pada
suhu 28 0C... 42
Tabel A.1.Penyerapan biodiesel terhadap radiasi gelombang
elektromagnetik pada panjang gelombang 200–250 nm... 53 Tabel B.1 Turbiditas awal dan akhir biodiesel ... 64
Tabel D.1 Waktu alir biodiesel... 69
DAFTAR GAMBAR
Gambar 2.1 Perpindahan elektron pada kulit atom …... Gambar 2.2 Diagram tingkat energi yang menunjukkan perubahan energi saat penyerapan radiasi infra merah (IR), visible (Vis), dan ultraviolet (UV)... Gambar 2.3 Prinsip transmitasi cahaya berdasar hukum spektroskopi ... Gambar 2.4 Peristiwa hamburan yang terjadi pada pengukuran turbiditas ... Gambar 2.5. Perubahan yang terjadi pada penampung satu saat pengukuran
Gambar 4.4 Grafik tegangan terhadap waktu tanggap detektor pada biodiesel sampel 2... Gambar 4.5 Grafik tegangan terhadap waktu tanggap detektor pada biodiesel sampel 3….……….……….……….………. Gambar 4.6 Grafik tegangan terhadap waktu tanggap detektor pada biodiesel sampel 4….……….……….……….………. Gambar 4.7 Grafik tegangan terhadap waktu tanggap detektor pada biodiesel sampel 5……….……….……... Gambar 4.8 Grafik tegangan terhadap waktu tanggap detektor pada
biodiesel sampel 6... Gambar 4.9 Grafik tegangan terhadap waktu tanggap detektor pada biodiesel sampel 7….……….……….……….………... Gambar 4.10 Grafik tegangan terhadap waktu tanggap detektor pada
Gambar B.1 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 1…….……….……….……….………... Gambar B.2 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 2……….……….……….………... Gambar B.3 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 3…….……….……….……….………... Gambar B.4 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 4…….……….……….……….………... Gambar B.5 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 5……….……….……….………... Gambar B.6 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 6…….……….……….……….………... Gambar B.7 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 7……... Gambar B.8 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 1…….……….……….……….………. Gambar B.9 Grafik turbiditas terhadap waktu pengendapan pada biodiesel
Gambar B.11 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 4…..……….……….……….………. Gambar B.12 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 5…...……….……….……….………. Gambar B.13 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 6…...……….……….……….………. Gambar B.14 Grafik turbiditas terhadap waktu pengendapan pada biodiesel
sampel 7…...……….……….……….………. Gambar B.15 Grafik turbiditas terhadap waktu pengendapan pada biodiesel standar……..……….……….……….………. Gambar C.1 Grafik pertambahan massa terhadap waktu pada biodiesel
sampel 1 dengan menggunakan neraca ohause…... Gambar C.2 Grafik pertambahan massa terhadap waktu pada biodiesel sampel 2 dengan menggunakan neraca ohause……….... Gambar C.3 Grafik pertambahan massa terhadap waktu pada biodiesel sampel 3 dengan menggunakan neraca ohause……….... Gambar C.4 Grafik pertambahan massa terhadap waktu pada biodiesel sampel 4 dengan menggunakan neraca ohause…………... Gambar C.5 Grafik pertambahan massa terhadap waktu pada biodiesel sampel 5 dengan menggunakan neraca ohause…………...…
Gambar C. 6 Grafik pertambahan massa terhadap waktu pada biodiesel sampel 6 dengan menggunakan neraca ohause……... Gambar C. 7 Grafik pertambahan massa terhadap waktu pada biodiesel
sampel 7 dengan menggunakan neraca ohause………
68
68
BAB I PENDAHULUAN I.1 Latar Belakang
Akhir-akhir ini tingkat kebutuhan akan energi di indonesia makin meningkat. Seperti terlihat pada tabel 1.1 di bawah ini, tentang peningkatan konsumsi energi dari tahun 1996–2006. Energi yang digunakan di Indonesia umumnya berasal dari bahan bakar minyak bumi. Minyak bumi berasal dari fosil yang jumlahnya terbatas atau tidak terbarukan. Keterbatasan ini menjadi permasalahan yang harus diselesaikan. Oleh karena itu, dibutuhkan solusi mengenai ketersediaan energi untuk jangka panjang berupa energi yang terbarukan.
Tabel 1.1 Intensitas pemakaian energi di Indonesia Jumlah
penduduk
Pemakaian energi final (tanpa
biomassa)
Intensitas energi final Tahun
Ribu Ribu SBM SBM/Kapita SBM/Juta Rp
1996 194.34 337.485 1,74 0,23
1997 199.837 361.514 1,81 0,24
1998 202.873 355.988 1,75 0,27
1999 203.047 401.654 1,98 0,30
2000 205.843 440.403 2,14 0,32
2001 208.647 467.239 2,23 0,32
2002 212.003 477.853 2,25 0,32
2003 215.276 481.064 2,23 0,30
2004 217.854 530.286 2,43 0,32
2005 219.893 546.641 2,49 0,31
2006 220.854 565.745 2,75 0,39
Sumber : Data Statistik Ekonomi Energi Indonesia 2006
Salah satu energi alternatif yang terbarukan adalah biodiesel. Biodiesel dapat dibuat dari bahan baku minyak nabati, lemak hewani, atau minyak goreng bekas (jelantah) melalui reaksi transesterifikasi [Prihandana et all, 2006]. Diantara beberapa bahan baku tersebut, jelantah merupakan bahan baku yang paling mudah didapatkan dalam kehidupan sehari-hari. Jelantah juga merupakan minyak sisa penggorengan yang tidak dapat digunakan lagi karena hanya menjadi limbah dan dapat menimbulkan penyakit bagi manusia.
Berdasarkan latar permasalahan terjadinya peningkatan kebutuhan akan energi dan adanya informasi bahwa jelantah dapat digunakan sebagai energi alternatif (biodiesel), maka dilakukan penelitian mengenai pembuatan biodiesel berbahan baku jelantah dan metanol menggunakan katalisator NaOH.
berdiri di Afrika Selatan pada tahun 1981. Setelah itu perkembangan biodiesel amat pesat menyebar ke Eropa, Amerika, bahkan Asia termasuk Indonesia. Di Indonesia, biodiesel mulai dikembangkan oleh Lemigas dan Pertamina, Perguruan Tinggi baik swasta maupun negeri, dan juga Balai Rekayasa dan Desain pada Badan Pengkajian dan Penerapan Teknologi (BPPT) sejak tahun 2000 [Rahmadi, 2008].
Biodiesel yang berkualitas adalah biodiesel yang sesuai dengan spesifikasi Badan Standarisasi Nasional melalui Standar Nasional Indonesia (SNI). Parameter berdasar SNI harus memenuhi 18 parameter. Analisa terhadap 18 parameter ini akan efektif jika yang dihasilkan memang benar-benar biodiesel. Analisa 18 parameter ini membutuhkan biaya yang besar, oleh karena itu perlu langkah awal uji analisa kualitas untuk memastikan bahwa produk olahan jelantah yang dihasilkan adalah biodiesel.
Langkah awal ini meliputi analisa dengan pengukuran kandungan senyawa menggunakan UV/Vis spektrofotometer SP8-400 dan Gas Chromatography (GC). Analisa selanjutnya adalah dengan menggunakan
I.2 Perumusan Masalah
Berdasarkan latar belakang tersebut dapat dirumuskan beberapa masalah yaitu :
1. Bagaimana membuat biodiesel dari bahan baku jelantah dan metanol menggunakan katalisator NaOH ?
2. Bagaimana menganalisa kandungan senyawa, turbiditas, dan viskositas kinematik pada biodiesel?
3. Bagaimana kualitas kandungan senyawa, turbiditas, dan viskositas kinematik pada biodiesel sampel bila dibandingkan dengan biodiesel standar?
1.3 Batasan Masalah
Adapun batasan masalah untuk penelitian ini adalah
1. Penelitian ini hanya terbatas pada proses pembuatan biodiesel pada skala laboratorium berkapasitas 500 ml.
2. Metode analisa yang digunakan untuk mengetahui kualitas biodiesel sampel adalah dengan cara membandingkan parameter parameter biodiesel sampel dengan biodiesel standar.
1.4 Tujuan Penelitian
Sesuai dengan rumusan di atas, maka tujuan dari penelitian ini adalah 1. Mengetahui bagaimana cara membuat biodiesel berbahan baku
jelantah dan metanol menggunakan katalisator NaOH.
2. Mengetahui proses analisa kandungan senyawa, turbiditas, dan viskositas kinematik biodiesel.
3. Mengetahui kualitas biodiesel dilihat dari kandungan senyawa, turbiditas, dan viskositas kinematik biodiesel bila dibandingkan dengan biodiesel standar.
I.5 Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan manfaat. Beberapa manfaatnya adalah
1. Memberi informasi mengenai cara membuat dan menganalisa kualitas biodiesel pada skala laboratorium.
2. Memberi informasi mengenai kualitas biodiesel, sehingga dapat diketahui metode yang paling baik dalam membuat biodiesel.
I.6 Sistematika Penulisan
Penelitian ini akan dituliskan dengan sistematika sebagai berikut : BAB I. Pendahuluan
Pada Bab I diuraikan tentang latar belakang masalah yang diangkat, perumusan masalah, batasan masalah, tujuan penelitian, manfaat penelitian, dan sistematika penulisan.
BAB II. Dasar Teori
Pada Bab II diuraikan tetang dasar teori pendukung dalam pembuatan biodiesel dan menganalisanya.
BAB III. Metode Penelitian
Dalam Bab III diuraikan tentang susunan alat dan bahan yang akan digunakan saat penelitian serta langkah-langkah yang dilakukan saat penelitian.
BAB IV. Hasil dan Pembahasan
Pada Bab IV diuraikan tentang hasil penelitian dan pembahasan hasil penelitian.
BAB V. Penutup
BAB II DASAR TEORI
II.1 Biodiesel
Jelantah adalah minyak nabati sisa penggorengan yang berwujud cair pada
suhu kamar. Jelantah ini dapat dibuat menjadi biodiesel. Pada proses pembuatan
biodiesel, terjadi pemecahan molekul trigliserida. Pemecahan ini dilakukan
dengan metanol dan dibantu dengan NaOH.
Biodiesel merupakan bahan bakar terbarukan, dan tidak beracun. Biodiesel
adalah minyak nabati (kedelai, kanola, kelapa, dan bunga matahari), lemak
hewan, atau minyak goreng bekas (jelantah) yang diubah melalui proses
transesterifikasi. Proses ini pada dasarnya mereaksikan minyak-minyak tersebut
dengan alkohol (metanol) menggunakan katalisator NaOH atau KOH
[Prihandana et all, 2006].
II.2 Pengukuran
Pengukuran dilakukan secara analisa eksperimen. Analisa eksperimen
adalah dengan membandingkan parameter pada biodiesel sampel terhadap
parameter biodiesel standar. Analisa eksperimen dalam penelitian ini dilakukan
untuk mengukur kandungan senyawa, turbiditas, dan viskositas kinematik
biodiesel.
II.2.1 Pengukuran Kandungan Senyawa
Pengukuran kandungan senyawa dilakukan secara bertahap dengan
menggunakan dua alat ukur. Alat ukur tersebut adalah UV/Vis spektrofotometer
SP8-400 dan GC.
II.2.1.1 UV/Vis spektrofotometer SP8-400
Landasan dari pengukuran kandungan senyawa menggunakan UV/Vis
spektrofotometer SP8-400 adalah serapan molekul. Setiap molekul dianalisa
dengan melihat karakteristik serapannya pada radiasi gelombang elektromagnetik
pada panjang gelombang tertentu [Skoog et all, 1965]. Pada proses ini energi
radiasi diserap oleh molekul dan akibatnya intensitas radiasi berkurang.
Sebuah molekul adalah gabungan mantap dari dua atau lebih atom.
Pengertian dari gabungan mantap adalah bahwa dibutuhkan energi untuk
melepaskan ikatan antar atom tersebut. Molekul menyerap radiasi berkas
elektromagnetik karena adanya elektron valensi, yang akan tereksitasi ke tingkat
energi yang lebih tinggi [Khopkar, 1990].
Berkas radiasi elektromagnetik yang dipancarkan akan berinteraksi dengan
elektron pada atom. Penyerapan energi ini terkait dengan sifat elektron untuk
menempati tingkat energi yang lebih tinggi. Seperti terlihat pada gambar 2.1
dibawah ini, elektron akan berpindah ke kulit yang tingkat energinya lebih tinggi
ketika mendapatkan energi dan berpindah ke kulit yang tingkat energinya lebih
rendah dengan melepaskan energi. Elektron dapat berpindah dari satu tingkat
akan menyerap energi, dan bila berpindah dari n=2 ke n=1 maka elektron akan
melepaskan energi, energi yang dilepaskan ini berupa emisi cahaya dengan
panjang gelombang tertentu.
Inti atom n=1 n=2
[image:32.595.92.510.194.623.2]energi energi
Gambar 2.1 Perpindahan elektron pada kulit atom
dengan besarnya energi adalah energi awal dikurangi energi akhir.
λ
υ hc
h E E
E = − = =
Δ 2 1 (2.1)
denganΔEadalah energi yang dibutuhkan untuk berpindah ke tingkatan energi
yang lebih tinggi atau energi yang dilepaskan ketika elektron berpindah dari
tingkat energi tinggi ke tingkat yang lebih rendah, υ adalah frekuensi radiasi
foton yang dipancarkan, h adalah konstanta planck ( 6,63 x 10-34 J.s), c adalah
kecepatan cahaya (3 x 108m/s), λ adalah panjang gelombang (m).
Suatu atom atau molekul akan menyerap radiasi elektromagnetik bila
frekuensi gelombang elektromagnetik sama dengan salah satu frekuensi spektrum
radiasi berkas elektromagnetik sama dengan energi yang dibutuhkan oleh atom
untuk bertransisi ke energi yang lebih tinggi.
Sesuai dengan teori kuantum, setiap molekul berada pada keadaan energi
tertentu, dan yang terendah dalam keadaan dasar. Ketika sebuah foton pada
radiasi melewati dekat molekul, energi pada foton akan diserap oleh elektron pada
molekul jika energi pada foton sama dengan perbedaan energi antara keadaan
dasar dengan keadaan energi diatasnya [Skoog et all, 1965].
Molekul yang menyerap energi akan mengalami transisi. Ketika terjadi
penyerapan ultraviolet, cahaya tampak, dan radiasi infra merah, molekul dapat
mengalami tiga transisi. Transisi ini meliputi transisi elektronik, transisi vibrasi,
dan transisi rotasi. Transisi ini terjadi pada energi hv, pada foton harus sama
dengan perbedaan antara dua tingkat energi. Radiasi inframerah akan
menstimulasi molekul bervibrasi, sedangkan cahaya tampak dan ultraviolet akan
menyebabkan elektron terdorong ke tingkat energi yang lebih tinggi [Harris,
4 3 2 1 0 4 3 2 1 0 4 3 2 1 0
IR VIS UV
E
2E
1E
0E
n
er
g
i
1λ
λ
4 ' [image:34.595.85.513.98.623.2]1
λ
' 5λ
'' 1λ
'' 5λ
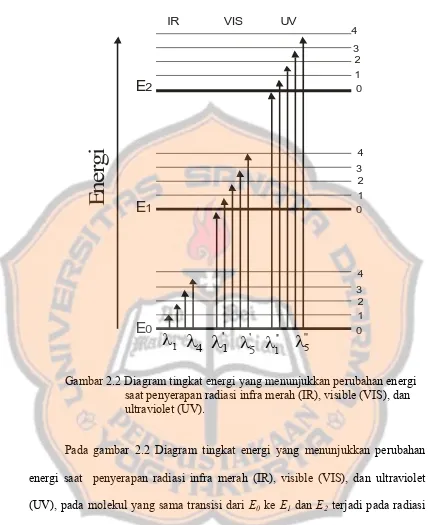
Gambar 2.2 Diagram tingkat energi yang menunjukkan perubahan energi saat penyerapan radiasi infra merah (IR), visible (VIS), dan ultraviolet (UV).
Pada gambar 2.2 Diagram tingkat energi yang menunjukkan perubahan
energi saat penyerapan radiasi infra merah (IR), visible (VIS), dan ultraviolet
(UV), pada molekul yang sama transisi dari E0 ke E1 dan E2 terjadi pada radiasi
ultraviolet yang memilki panjang gelombang berbeda.
Besarnya energi radiasi berkas elektromagnetik yang tertentu memiliki
panjang gelombang tertentu pula. Pada spektroskopi ultraviolet dengan panjang
gelombang 190-380 nm dan daerah tampak dengan panjang gelombang 380-780
Pada pengukuran kandungan senyawa mengunakan UV/Vis
Spektrofotometer SP8-400 terjadi penyerapan dan transmitasi. Seperti terlihat
pada gambar 2.3 mengenai prinsip transmitasi cahaya berdasar hukum
spektroskopi.
[image:35.595.94.512.187.621.2]P 0 Pt
Gambar 2.3 Prinsip transmitasi cahaya berdasar hukum spektroskopi
Suatu berkas radiasi elektromagnetik dengan panjang gelombang (λ )
200-450 nm dan intensitas cahaya mula-mula P0 melewati suatu medium. Berkas
radiasi elektromagnetik dengan λ tertentu memiliki energi tertentu pula. Apabila
berkas radiasi elektromagnetik dengan λ tertentu ditembakkan pada sampel, dan
apabila energi yang dimiliki oleh berkas radiasi elektromagnetik sesuai dengan
besarnya energi yang dibutuhkan elektron untuk bertransisi ke tingkat energi yang
lebih tinggi, maka akan terjadi penyerapan. Besarnya penyerapan adalah Pa.
Namun tidak semua energi diserap oleh elektron dalam medium, ada pula yang
diteruskan atau ditransmisikan. Besarnya energi yang ditransmisikan tampak
Berdasarkan hukum Beer dan Lambert menunjukkan hubungan berikut [Khopkar,
1990] :
A abc P P T o
t = =
=
−log log( ) (2.2)
dengan a adalah tetapan absorbtivitas, b adalah jarak tempuh optik, c
adalah konsentrasi, A adalah absorbansi, dan T adalah transmitasi.
Pada UV/Vis spektrofotometer SP8-400 pengukuran absorbansi atau
transmitasi dalam spektroskopi ultraviolet (190-380 nm) dan daerah tampak
(380-780 nm) digunakan dalam pengukuran unsur kimia baik kualitatif maupun
[image:36.595.87.516.163.622.2]kuantitatif. Pengukuran secara kualitatif dilakukan dengan menganalisa bentuk
grafik penyerapan pada panjang gelombang. Bentuk grafik untuk tiap senyawa
berbeda-beda. Perbedaan ini dikarenakan senyawa tersusun oleh atom yang
jumlahnya berbeda sehingga energi yang diserap juga berbeda. Perbedaan inilah
yang menjadi dasar dalam pengukuran ini.
II.2.2 Gas Chromatography (GC)
Teknik kromatografi digunakan untuk menguraikan senyawa yang
terkandung di dalam biodiesel [Khopkar, 1990]. Pada GC, komponen yang
dipisahkan dibawa lebih dahulu oleh gas pembawa melewati kolom. Gas
pembawa yang digunakan adalah N2. Gas pembawa akan mendorong sampel
melewati kolom. Sampel akan berinteraksi dengan fase diam yang ada pada
kolom.
Interaksi antara komponen-komponen sampel dengan fase diam akan
koefisien distribusinya sehingga terjadi pemisahan [Gritter et all, 1991].
Pemisahan untuk tiap komponen bergantung dari jenis komponen tersebut.
Apabila interaksi komponen dengan fase diam terlalu kuat maka
pemisahan terjadi sangat lambat. Pemisahan lambat terjadi karena dibutuhkan
suhu yang lebih tinggi untuk memisahkan tiap komponen. Untuk mengatasi hal ini
diperlukan pengaturan suhu agar terjadi pemisahan.
Dengan meningkatnya suhu, maka ikatan antar atom semakin renggang
dan mudah terurai. Dengan demikian maka rantai karbon pun terurai. Terurainya
rantai karbon pada senyawa memiliki sifat yang berbeda-beda. Setiap senyawa
memiliki rantai karbon yang berbeda-beda sehingga dibutuhkan suhu yang
berbeda pula untuk menguraikannya. Ketika rantai karbon terurai (menguap)
maka akan terdeteksi oleh detektor. Waktu yang dibutuhkan untuk tiap senyawa
sampai terdeteksi (waktu retensi) berbeda-berbeda. Perbedaan inilah yang menjadi
dasar penentuan jenis senyawa.
Setiap senyawa memiliki waktu retensi yang berbeda-beda. Beberapa
senyawa mungkin mempunyai waktu tambat yang hampir sama atau berdekatan,
tetapi tiap senyawa hanya mempunyai satu waktu tambat saja.
II.3 Pengukuran Turbiditas
Turbiditas dapat didefinisikan sebagai ukuran relatif kejernihan air.
Kejernihan ini tergantung dari adanya partikel terlarut seperti lumpur, tanah liat,
dan mikroorganisme lainnya [Theofanis et all, 2010]. Turbiditas ganggang
oleh suatu larutan yang mengandung partikel terdispersi. Ketika cahaya melewati
medium transparan dimana partikel padat tersebar, cahaya tersebut akan
dihamburkan oleh partikel ke segala arah. Semakin banyak partikel berakibat pada
semakin banyak cahaya terhambur yang mengakibatkan air terlihat semakin keruh
atau semakin tidak jernih.
Hubungan konsentrasi terhadap hamburan pada radiasi sinar paralel
dalam suspensi encer digambarkan pada gambar 2.4 berikut :
Gambar 2.4 Peristiwa yang terjadi pada pengukuran turbiditas
Berdasar gambar di atas, dapat dituliskan persamaan berikut :
(2.3) b
oe P P= −τ
dengan Po dan P adalah kekuatan berkas sebelum dan setelah melewati panjang
tempat sampel b dari media keruh, dan τ adalah koefisien turbiditas, yang
nilainya sering ditemukan linear terkait dengan e konsentrasi dari hamburan
II.2.4 Pengukuran Viskositas
Viskositas adalah aliran fluida yang merupakan gesekan antara molekul
satu dengan yang lain. Viskositas sangat dipengaruhi oleh temperatur
lingkungannya. Perubahan temperatur akan berpengaruh pada perubahan
viskositas. Pada temperatur tinggi, viskositas menjadi rendah. Apabila temperatur
turun, viskositas akan kembali tinggi.
Pengukuran viskositas dilakukan dengan menggunakan prinsip Hukum
Poiseuille. Menurut hukum Poiseuille, debit cairan yang mengalir sepanjang pipa
seperti pada gambar 2.5 dibawah ini yang penampangnya bundar berjari-jari R
dengan panjang L adalah [Sianoudis, 2008] dituliskan pada persamaan berikut
ini :
L P R
η π
8
4 0Δ
= Φ
(2.4)
dengan Φ adalah debit cairan (m3/s), R0 adalah jari-jari pipa kapiler (m), ΔP
adalah perubahan tekanan cairan (N/m2), η adalah viskositas dinamik (kg/ms), L
h
(t)
R
L
P
[image:40.595.86.511.99.701.2]h
0
Gambar 2.5 Perubahan yang terjadi pada penampung 1 saat pengukuran biodiesel karena biodiesel mengalir ke penampung 2 yang terletak di bawahnya.
Debit cairan tersebut mengalir pada sebuah pipa dengan volume tertentu.
Saat cairan mengalir turun, terjadi penurunan ketinggian volume cairan.
Perubahan ketinggian akan mempengaruhi perubahan tekanan. Perubahan tekanan
yang terjadi ini secara lebih jelas dipaparkan pada persamaan berikut ini :
) (t h g P= Δ
Δ
ρ
, (2.5)
dengan Δh(t) =h0 −h(t)
(N/m2), g adalah tetapan gravitasi (m/s2), h(t) adalah perubahan tinggi cairan
terhadap waktu (m), h0 adalah tinggi awal cairan (m).
Dari persamaan (2.4) dan (2.5) didapatkan persamaan untuk menentukan
nilai viskositas dinamik suatu zat [White, 1988] :
L
gh
R
tΦ
=
8
) ( 4 0πρ
η
(2.6)dengan Φ adalah debit cairan (m3/s), R 0adalah jari-jari pipa kapiler (m), ρ adalah
massa jenis cairan (kg/m3), η adalah viskositas dinamik (kg/ms), L adalah
panjang pipa kapiler (m), g adalah tetapan gravitasi (m/s2), h(t) adalah perubahan
tinggi cairan terhadap waktu (m).
Dari persamaan 2.6 di atas ditunjukkan bahwa viskositas dinamik suatu
cairan dipengaruhi oleh massa jenisnya. Pada pengukuran viskositas suatu cairan
dengan alat ukur dan metode yang sama untuk dua jenis zat yang berbeda, maka
jari-jari pipa kapiler ( ), panjang pipa kapiler (L), π, dan g bernilai tetap seperti
pada persamaan di bawah ini : 4 0 R k L g R = 8 4
0π (2.7)
Dalam pengukuran ini, perubahan ketinggian cairan dalam penampung 1
persatuan waktu berbeda-beda, begitu pula dengan perubahan luasan permukaan
dan persamaan 2.7 dituliskan pada persamaan berikut ini.
Φ = h(t)
kρ η , t V h k Δ Δ = / (t) ρ , t h t A t h k Δ Δ Δ Δ Δ Δ = / ) / ( / ρ , ) /
( A t
k
Δ Δ
= ρ
(2.8)
dengan ρ adalah massa jenis cairan (kg/m3), ∆v/∆t adalah perubahan volume
cairan persatuan waktu (m3/s), Δh/Δt adalah perubahan ketinggian cairan
penampung 1 persatuan waktu (m/s),ΔA/Δtadalah perubahan luasan permukaan
cairan penampung 1 persatuan waktu (m2/s).
Dari persamaan 2.8 di atas, perubahan ketinggian persatuan waktu
(Δh/Δt) dan perubahan luasan permukaan cairan persatuan waktu (ΔA/Δt)
akan mempengaruhi perubahan volume cairan persatuan waktu ( ). Proses
ini terjadi selama cairan mengalir berpindah turun dari penampung 1 ke
penampung 2.
t
V Δ
Δ /
Pengukuran di atas ditujukan untuk menghitung viskositas dinamik cairan.
Viskositas kinematik cairan diperoleh dari viskositas dinamik dibagi dengan
massa jenis cairan itu sendiri.
ρ η
υ = ,
Atau massa jenis untuk tiap cairan tidak mempengaruhi perhitungan.
Seperti diuraikan pada persamaan berikut ini :
)
/
(
A
t
k
Δ
Δ
=
ρ
υρ
ρ ρ υ ) /( A t
k Δ Δ = , ) /
( A t
k Δ Δ = , A t k Δ Δ = (2.10)
Dari persamaan (2.10) di atas maka viskositas kinematik untuk cairan
standar dan cairan sampel adalah sebagai berikut :
Viskositas kinematik cairan standar :
standar standar standar
A
t
k
Δ
Δ
=
υ
(2.11)dengan standar
standar standar
υ
t
A
k
Δ
Δ
=
Viskositas kinematik cairan sampel :
sampel sampel sampel
A
t
k
Δ
Δ
=
υ
(2.12)cairan standar dan cairan sampel untuk metode pengukuran yang sama, maka nilai
k dapat disubstitusikan. Seperti diuraikan pada persamaan berikut :
sampel standar sampel standar standar sampel
A
t
t
A
Δ
Δ
Δ
Δ
=
υ
υ
(2.13)Karena perubahan luasan permukaan sampel sama dengan perubahan
luasan permukaan standar maka:
standar sampel
A
A
=
Δ
Δ
standar sampel standar sampelt
t
Δ
Δ
=
υ
υ
.(2.14)dengan mengetahui viskositas kinematik cairan standar (υstandar) pada suhu
tertentu, waktu alir cairan standar (∆tstandar) dan waktu alir cairan sampel (∆tsampel),
maka persamaan (2.14) dapat digunakan untuk menghitung viskositas kinematik
BAB III
METODE PENELITIAN
III.1 Tempat Penelitian
Penelitian ini dilaksanakan di Laboratorium Analisa Kimia Fisika Pusat
Fakultas Sains dan Teknologi, Kampus III Universitas Sanata Dharma Yogyakarta.
III.2 Alat dan Bahan
Pada peneilitian ini dibutuhkan alat dan bahan untuk membuat biodiesel,
mengukur parameter biodiesel, dan menganalisanya.
III.2.1 Alat
III.2.1.1 Alat-alat Pembuatan Biodiesel
Alat-alat yang dibutuhkan dalam pembuatan biodiesel adalah sebagai berikut :
a. Mixer
Mixer digunakan sebagai media pencampur antara jelantah, metanol,
dan NaOH.
b. Pengendap
Pengendap adalah alat yang digunakan untuk mengendapkan hasil
campuran jelantah, metanol, dan NaOH, agar dihasilkan biodiesel.
c. Pemanas
Pemanas yang digunakan adalah kompor listrik. Pemanasan
dilakukan pada jelantah sebelum proses pencampuran. Pemanasan bertujuan
agar ikatan antar atom pada jelantah makin lemah dan mudah bereaksi.
Pemanasan juga dilakukan pada biodiesel untuk menghilangkan kadar air.
d. Pompa Udara
Pompa udara digunakan sebagai penghasil gelembung udara, yang
membantu proses pencucian. Udara yang naik ke permukaan akan membawa
air, dan ketika air turun, akan mengikat kotoran yang bercampur dengan
biodiesel.
e. Pengukur suhu, waktu, dan volume
Stopwatch dan termometer digunakan sebagai pengontrol waktu dan
suhu pada proses pengadukan, pencucian dan penghilangan kadar air
biodiesel. Dalam penelitian ini juga digunakan gelas ukur sebagai alat untuk
menentukan volume pada proses pembuatan.
III.2.1.2 Alat-alat yang dibutuhkan dalam pengukuran kualitas biodiesel a. Neraca Ohause
Neraca Ohause digunakan sebagai pengukur massa NaOH dan juga
sebagai alat bantu dalam proses pengukuran waktu alir biodiesel dalam
b. Turbidimeter
Turbidimeter digunakan untuk mengukur tingkat kekeruhan biodiesel.
c. Satu unit komputer berikut vernier logger pro
Satu unit komputer yang disertai dengan vernier logger pro digunakan
untuk menampilkan hasil dalam setiap pengukuran. Pengukuran pada GC,
turbiditas, dan viskositas, membutuhkan bantuan komputer. Selain untuk
menampilkan data, penggunaan komputer dapat mengetahui apakah proses
pengukuran berjalan sesuai yang diinginkan atau tidak.
d. UV/Vis spektrofotometer SP8-400
UV/Vis spektrofotometer SP8-400 digunakan untuk membandingkan
senyawa yang terkandung dalam biodiesel sampel dengan biodiesel standar.
e. Gas Chromatography (GC)
GC digunakan untuk membandingkan senyawa yang terkandung
dalam biodiesel sampel dengan biodiesel standar. Prinsip dari alat ini adalah
penguraian rantai senyawa biodiesel.
III.2.2 Bahan yang digunakan dalam membuat biodiesel a. Jelantah
Jelantah digunakan sebagai bahan baku dalam pembuatan biodiesel.
Jelantah yang digunakan adalah 500 ml untuk pembuatan setiap biodiesel
b. Pereaksi
Pereaksi yang digunakan adalah metanol.
c. Katalis
NaOH digunakan sebagai katalisator pada reaksi minyak jelantah
dengan metanol. NaOH yang digunakan dalam membuat biodiesel adalah
sebanyak 3 gram untuk tiap sampel.
d. Pembanding
Pembanding yang digunakan dalam menentukan senyawa yang
terkandung dalam biodiesel sampel adalah biodiesel produksi BPPT
berbahan baku minyak sawit/crude palm oil (CPO).
e. Hexane, formazin, dan aquades
Hexane digunakan sebagai pelarut pada pengukuran kandungan
senyawa menggunakan GC. Komposisi hexane yang digunakan sebagai
pelarut adalah 90% untuk tiap sampelnya. formazin dan aquades digunakan
sebagai pengkalibrasi pada pengukuran turbiditas.
III.3 Pembuatan Biodiesel
Dalam pembuatan biodiesel dilakukan beberapa tahapan sebagai berikut:
a. Persiapan Bahan
Bahan yang digunakan adalah jelantah atau minyak sisa dari
sehingga minyak benar-benar bersih. Setelah itu, jelantah dipanaskan hingga
suhunya mencapai 60 0C, kemudian metanol dicampur dengan NaOH.
Variasi komposisi metanol yang digunakan adalah 60 ml, 70 ml, 80 ml, 90
ml, dan 100 ml. Komposisi metanol tersebut dicampur dengan NaOH
sebanyak 3 gram.
b. Pencampuran
Metanol yang telah bercampur dengan NaOH kemudian dicampur
dengan minyak jelantah. Proses pencampuran ini dilakukan selama kurang
lebih 1 jam dengan suhu 50-60 0C.
c. Pengendapan
Setelah melalui proses pengadukkan selama 1 jam, proses selanjutnya
adalah pengendapan. Pengendapan ini dimaksudkan agar biodiesel terpisah
dari gliserin. Minyak biodiesel akan terletak di bagian atas dan gliserin akan
terletak di bagian bawah. Pemisahan ini terjadi karena perbedaan massa
jenis. Proses pengendapan ini berlangsung kurang lebih 1 jam.
d. Pemisahan Biodiesel dari Gliserin
Biodiesel yang sudah tampak terpisah dari gliserin kemudian
dipisahkan dengan pipa berdiameter ± 0,2 cm. Setelah itu proses selanjutnya
adalah pencucian menggunakan air hangat dengan suhu 40-50 0C sebanyak
setengah dari volume biodiesel. Pencucian ini menggunakan alat bantu
dilakukan selama 1 jam. Setelah proses pencucian, biodiesel didiamkan
beberapa saat agar air terpisah dari biodioesel. Selanjutnya air dikeluarkan
melalui pipa kecil.
e. Penghilangan Kadar Air
Untuk menghilangkan kadar air pada biodiesel, dilakukan pemanasan
biodiesel hingga 100 0C menggunakan kompor listrik. Proses dari awal
Minyak jelantah (500 ml)
Metanol + NaOH Pengadukkan
waktu= 1 jam T = 50 0-60 0C
Biodiesel
Gliserin
Gliserin
Biodiesel
Air
Pencucian (sebanyak 3 kali)
waktu= 1 jam
Biodiesel
Air Biodiesel
Air Pemanasan
100 0C
Biodiesel siap pakai
Gambar 3.1 Skema pembuatan biodiesel berbahan baku jelantah dan metanol menggunakan katalisator NaOH.
III.3 Pengukuran
III.3.1 Pengukuran Kandungan Senyawa menggunakan UV/Vis spektrofotometer SP8-400
Analisa senyawa menggunakan UV/Vis spektrofotometer SP8-400. Untuk
menganalisa senyawa yang terkandung dalam biodiesel maka yang pertama
dilakukan adalah mengukur serapan oleh molekul pada senyawa yang terkandung
pada biodiesel standar dan sampel. Biodiesel standar diukur terlebih dahulu
menggunakan UV/Vis spektrofotometer SP8-400, kemudian baru biodiesel sampel.
Setelah itu data diolah dan ditampilkan dalam bentuk grafik serapan terhadap panjang
gelombang elektromagnetik. Melalui grafik ini dapat diketahui apakah senyawa yang
terkandung pada biodiesel sampel sama dengan biodiesel standar.
III.3.2 Pengukuran Kandungan Senyawa menggunakan GC
Analisa menggunakan GC adalah analisa dengan mengandalkan interaksi
materi dengan fase diam dan perbedaan titik didih. Pengukuran dilakukan dengan
cara membandingkan kandungan senyawa dalam biodiesel sampel dengan biodiesel
standar.
Biodiesel sampel dan biodiesel standar terlebih dahulu dicampur dengan
pelarut hexane. Dengan komposisi biodiesel 1 ml dan hexane 9 ml. Pencampuran
dilakukan di dalam labu ukur. Setelah larutan tercampur, maka larutan tersebut
GC. Setelah biodiesel diinjeksikan, maka akan timbul grafik dengan
puncak-puncaknya yang ditampilkan melalui komputer. Masing-masing puncak menunjukkan
jenis unsur yang terkandung dalam molekul biodiesel.
III.3 Pengukuran Turbiditas
Pengukuran turbiditas membutuhkan satu unit komputer berikut vernier
logger pro dan turbidimeter. Sebelum melakukan pengukuran turbiditas biodiesel,
maka dilakukan kalibrasi terlebih dahulu. Kalibrasi dilakukan untuk memberi range
pada pengukuran turbiditas biodiesel. Untuk nilai 100 NTU menggunakan larutan
formazin standard dan aquades sebagai range minimum turbidimeter yaitu 0 NTU.
Pengukuran dilakukan dengan cara memasukkan biodiesel kedalam gelas
tabung pada turbidimeter. Data yang diambil sebanyak 20 sampel untuk beberapa
detik. Dengan waktu pengambilan sampel 0,01 s/sampel.
III.4 Pengukuran Viskositas Kinematik
Pengukuran viskositas kinematik biodiesel dilakukan dengan cara pengukuran
relatif. Pengukuran ini dilakukan dengan metode dan kondisi yang sama untuk dua
jenis cairan yang salah satunya telah diketahui viskositas kinematiknya. Viskositas
kinematik yang telah diketahui adalah viskositas kinematik biodiesel standar.
Selanjutnya dengan dasar teori seperti pada persamaan 2.14, maka yang harus diukur
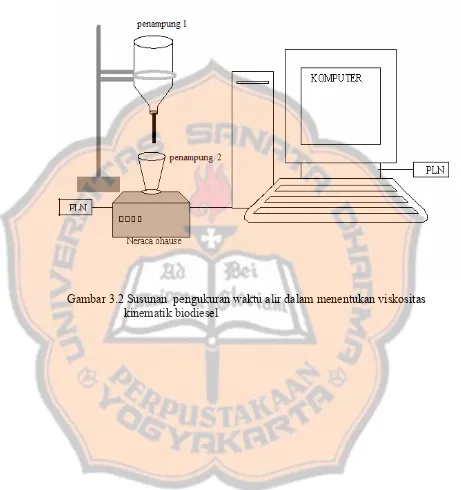
Waktu alir yang diukur adalah waktu alir biodiesel pada volume 50 ml untuk
mengalir turun dari penampung 1 ke penampung 2, seperti tampak pada gambar 3.2
di bawah ini. Perhitungan waktu alir ini menggunakan alat ukur yaitu neraca ohause.
Neraca ohause mencatat setiap perubahan massa persatuan waktu saat biodiesel
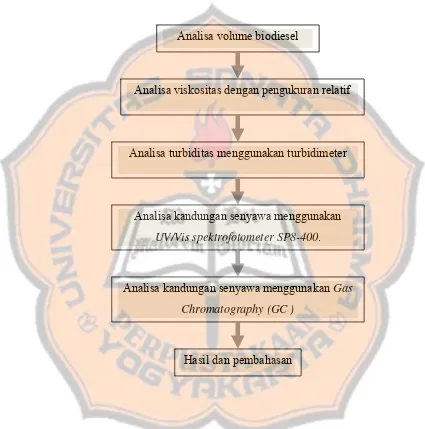
Secara keseluruhan, metode analisa parameter pada biodiesel dilakukan
seperti pada gambar 3.4 berikut.
Analisa volume biodiesel
Analisa viskositas dengan pengukuran relatif
Hasil dan pembahasan
Analisa turbiditas menggunakan turbidimeter
Analisa kandungan senyawa menggunakan
UV/Vis spektrofotometer SP8-400.
Analisa kandungan senyawa menggunakan Gas
[image:56.612.92.517.171.600.2]Chromatography (GC )
BAB IV
HASIL DAN PEMBAHASAN
IV.1 HASIL
Dalam penelitian ini biodiesel diperoleh setelah melalui tiga proses yaitu transesterifikasi, pemisahan, dan pencucian/pengeringan. Setelah biodiesel dihasilkan maka langkah selanjutnya adalah menganalisa dengan cara membandingkan pada biodiesel standar produksi BPPT. Parameter-parameter yang menjadi pembanding adalah kandungan senyawa, turbiditas, dan viskositas kinematik pada biodiesel.
IV.1.1 Analisa Kandungan Senyawa dalam Biodiesel
Analisa kandungan senyawa dalam biodiesel ditujukan untuk mengetahui apakah biodiesel yang dihasilkan sudah sesuai dengan biodiesel standar. Pengukuran kandungan senyawa dilakukan dengan menggunakan instrumen UV/Vis spektrofotometer SP8-400 dan GC.
IV.1.1.1 Perbandingan senyawa yang terkandung dalam biodiesel menggunakan radiasi berkas elektromagnetik pada UV/Vis spektrofotometer SP8-400.
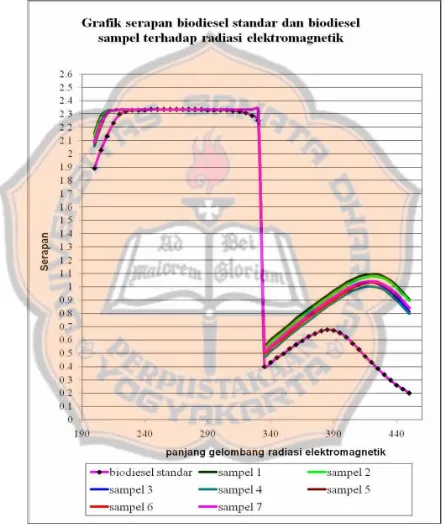
Pada pengukuran kandungan senyawa terjadi penyerapan radiasi berkas elektromagnetik pada panjang gelombang 200–450 nm. Hasil pengukuran ini secara lebih jelas ditampilkan pada gambar 4.1 di bawah ini.
Gambar 4.1 menunjukkan grafik hubungan serapan biodiesel standar dan biodiesel sampel terhadap panjang gelombang radiasi berkas elektromagnetik dengan panjang gelombang 200-450 nm pada berbagai sampel biodiesel. Secara umum bentuk grafik yang dihasilkan memiliki bentuk yang sama. Ini terlihat pada panjang gelombang 200-450 nm besarnya serapan pada biodiesel standar dan sampel adalah sama.
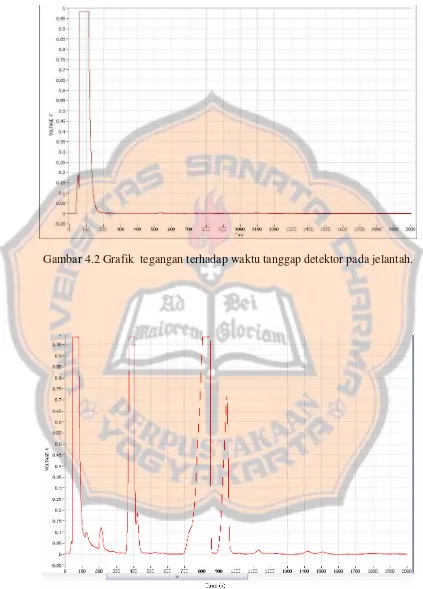
IV.1.2 Perbandingan jenis senyawa yang terkandung dalam biodiesel menggunakan GC.
Gambar 4.2 Grafik tegangan terhadap waktu tanggap detektor pada jelantah.
Gambar 4.4 Grafik tegangan terhadap waktu tanggap detektor pada biodiesel sampel 2.
Gambar 4.6 Grafik tegangan terhadap waktu tanggap detektor biodiesel sampel 4.
Gambar 4.8 Grafik tegangan terhadap waktu tanggap detektor pada biodiesel sampel 6.
Gambar 4.10 Grafik tegangan terhadap waktu tanggap detektor pada biodiesel standar.
Gambar 4.2 grafik tegangan terhadap waktu tanggap detektor pada jelantah, menggambarkan komponen yang ada pada jelantah. Grafik ini berbeda dengan gambar 4.3 sampai gambar 4.10. Perbedaan bentuk grafik ini menunjukkan bahwa senyawa penyusun jelantah berbeda dengan senyawa penyusun biodiesel sampel dan biodiesel standar. Perbedaan senyawa menunjukkan bahwa biodiesel berbeda dengan jelantah. Sedangkan untuk gambar 4.3 sampai gambar 4.10 secara umum tidak terdapat perbedaan. Ini menunjukkan bahwa senyawa yang ada pada biodiesel sampel sama dengan biodiesel standar.
sama ini juga dilakukan pada seluruh biodiesel sampel, yang datanya dilampirkan pada lampiran.
IV.1.3 Pengukuran turbiditas dan viskositas kinematik biodiesel.
Selain melihat kandungan senyawa yang dihasilkan, pada penelitian ini juga dibahas mengenai turbiditas dan viskositas kinematik biodiesel. Grafik hasil pengukuran turbiditas dapat dilihat pada lampiran dan viskositas kinematik biodiesel secara lebih jelas ditampilkan pada tabel 4.1 berikut ini :
Tabel 4.1 Turbiditas awal dan akhir dan viskositas kinematik biodiesel dengan komposisi NaOH 3 gram dan jelantah 500 ml pada suhu 28 0C
Biodiesel sampel Metanol (ml) Turbiditas awal (NTU) Turbiditas akhir (NTU) Viskositas kinematik (mm2/s)
Volume biodiesel (ml)
1 60 41,25 5,92 6,494 250
2 70 5,66 0,80 5,263 260
3 80 13,02 0,69 4,815 283
4 90 10,25 8,36 4,815 358
5 100 12,95 5,34 4,199 406
6 100 15,39 12,52 4,143 370
7 100 4,255 359
Penurunan ini menunjukkan bahwa konsentrasi partikel telah mengendap. Pengendapan partikel pada biodiesel terjadi selama 75 hari setelah pengukuran.
Selain pengukuran kandungan senyawa dan turbiditas biodiesel, juga dilakukan pengukuran viskositas kinematik biodiesel. pengukuran ini bertujuan untuk mengetahui tingkat kekentalan kinematik biodiesel. Pengukuran viskositas kinematik biodiesel sampel dilakukan pada suhu kamar. Perhitungan dalam pengukuran viskositas biodiesel dilakukan dengan cara dibandingkan dengan viskositas kinematik biodiesel standar.
Dengan mengetahui viskositas kinematik biodiesel standar (υstandar) yaitu sebesar 4,199 mm2/s pada suhu 40 0C, waktu alir biodiesel standar ( ) dan waktu alir biodiesel sampel (
dar s
t tan Δ
sampel
t
Δ ), maka persamaan (2.14) dapat digunakan
untuk menghitung viskositas kinematik biodiesel sampel (υsampel).
Gambar 4.11 Grafik pertambahan massa terhadap waktu pada biodiesel standar dengan menggunakan neraca ohause.
Biodiesel bervolume 50 ml mengalir dari penampung 1 ke penampung 2. Penampung 2 merupakan sebuah penampung yang terletak tepat di atas neraca ohause seperti terlihat pada gambar 3.2 pada Bab 3 Eksperimen. Biodiesel akan
mengalir turun ke penampung 2 dalam waktu tertentu. Untuk biodiesel dengan volume 50 ml, memiliki massa tertentu tergantung dari massa jenisnya.
Biodiesel bervolume 50 ml dialirkan. Kemudian perpindahan biodiesel ini dicatat sebagai fungsi massa terhadap waktu. Seperti terlihat pada gambar 4.11 grafik pertambahan massa terhadap waktu pada biodiesel standar menggunakan neraca ohause. Massa yang terukur pertama kali adalah sebanyak 0,23 gram
memiliki massa total 42,92 gram berpindah dari penampung 1 ke penampung 2 membutuhkan waktu 75 sekon. Waktu 75 sekon didapat dari selisih waktu perhitungan waktu akhir dikurangi waktu awal massa terukur oleh neraca ohause.
[image:68.595.88.507.220.626.2]Proses dan hasil perhitungan relatif berdasar waktu alir biodiesel, terlampir pada Lampiran E Perhitungan viskositas kinematik untuk masing-masing biodiesel. Nilai untuk masing-masing biodiesel tertera secara jelas pada gambar 4.12 berikut ini :
Grafik viskositas kinematik biodiesel terhadap komposisi metanol 4 4.5 5 5.5 6 6.5 7
55 65 75 85 95 105
Volume metanol (ml)
V is kos it as ki ne m a ti k bi odi es el (m m 2 /s )
Gambar 4.12 Grafik hubungan viskositas kinematik terhadap komposisi metanol pada biodiesel berbahan baku jelantah 500ml dan NaOH 3gram.
IV.2 PEMBAHASAN
Jelantah merupakan salah satu jenis lemak, yaitu trigliserida. Trigliserida terdiri dari ester asam lemak dan gliserin. Untuk mendapatkan ester asam lemak atau biodiesel, ester asam lemak yang ada pada jelantah harus dipisahkan terlebih dahulu dari gliserin. Pemisahan dilakukan dengan bantuan pereaksi metanol dan dipercepat dengan katalisator NaOH.
Biodiesel bervolume rendah berkisar antara 250-283 ml. Biodiesel ini dibuat dengan komposisi metanol 60-80 ml. Biodiesel bervolume rendah ini menunjukkan bahwa reaksi yang terjadi tidak mampu memisahkan seluruh ester asam lemak dari gliserin. Akibatnya masih ada ester asam lemak yang tergabung dengan gliserin dalam jelantah. Hasil ini berbeda dengan volume biodiesel yang dihasilkan dengan komposisi metanol 90-100 ml, yaitu berkisar antara 358-406 ml.
Analisa yang sangat penting adalah menganalisa apakah kandungan senyawa biodiesel sampel sama dengan biodiesel standar. Analisa awal adalah dengan melihat kandungan senyawa dari bentuk grafik serapan terhadap radiasi berkas elektromagnetik. Pengukuran ini menggunakan UV/Vis spektrofotometer SP8-400.
[image:69.595.86.517.230.617.2]Bentuk grafik yang sama menunjukkan bahwa terjadi serapan energi yang sama pada berkas elektromagnetik oleh molekul biodiesel sampel dan biodiesel standar. Energi dari radiasi berkas elektromagnetik diserap oleh molekul yang ada di dalam biodiesel sampel dan biodiesel standar. Besarnya serapan energi tergantung dari keadaan molekul. Peristiwa serapan ini dapat mengidentifikasi molekul yang terkandung dalam biodisel sampel dan biodiesel standar. Bentuk serapan yang sama pada panjang gelombang 200-450 nm menunjukkan bahwa terdapat molekul yang sejenis. Kesamaan ini terlihat dari bentuk grafik yang dihasilkan, sedangkan besar serapan menunjukkan besarnya konsentrasi senyawa tertentu dalam biodiesel. Dengan demikian ditinjau dari kandungan senyawa dapat dikatakan bahwa biodiesel sampel yang dihasilkan sudah sesuai dengan biodiesel standar. Untuk mengetahui lebih jelas, maka tahapan selanjutnya akan dilihat data hasil pengukuran menggunakan GC. Pada pengukuran menggunakan GC terjadi dua proses. Proses yang pertama adalah biodiesel didorong oleh fase gerak yaitu N2, selanjutnya proses yang kedua adalah sampel akan berinteraksi dengan fase diam yang ada pada kolom. Interaksi senyawa pada sampel biodiesel dengan fase diam tingkatannya berbeda-beda. Setelah itu senyawa biodiesel terlepas dari interaksi dengan fase diam dan kemudian akan mengalami penguapan dan terurai.
Analisa lainnya yang juga menentukan kualitas biodiesel adalah turbiditas dan viskositas kinematik biodiesel. Pengukuran turbiditas dilakukan secara bertahap. Pengukuran turbiditas awal dan pengukuran turbiditas akhir atau setelah 75 hari pengukuran turbiditas awal. Pengukuran viskositas kinematik dilakukan dengan pengukuran relatif.
Dari hasil pengukuran turbiditas akhir, setelah 75 hari pengukuran turbiditas awal, didapatkan perbedaan nilai turbiditas. Pada biodiesel sampel 1 turbiditas menurun seiring dengan waktu. Proses ini terlihat dari hasil pengukuran yang menunjukkan bahwa terjadi penurunan nilai turbiditas setelah 75 hari pengukuran. Pada waktu pengukuran awal, nilai turbiditas sampel 1 sebesar 41,25 NTU dan pada pengukuran akhir didapatkan nilai turbiditas sebesar 5,92 NTU.
Dari hasil pengukuran turbiditas didapatkan nilai 0,69 NTU, 0,80 NTU, 5,34 NTU, 5,92 NTU, 8,36 NTU, 12,52 NTU, dan 13,72 NTU pada biodiesel sampel. Nilai ini tidak jauh berbeda dari pengukuran turbiditas pada biodiesel standar yaitu 4,22 NTU. Dengan menggunakan biodiesel standar sebagai pembanding, maka dapat disimpulkan nilai turbiditas pada biodiesel sampel masih sesuai dengan standar dan tidak mempengaruhi komponen senyawa penyusun biodiesel. Hal ini dapat dilihat kembali dari hasil pengukuran kandungan senyawa menggunakan UV/Vis spektrofotometer SP8-400 dan Gas Chromatography (GC).
Dari hasil pengukuran viskositas kinematik biodiesel didapatkan nilai 4,199-6,494 mm2/s pada suhu kamar (28 0C). Nilai ini masih sesuai bila dibandingkan dengan nilai viskositas kinematik biodiesel standar pada suhu 40 0C yaitu sebesar 4,143 mm2/s. Pengukuran viskositas kinematik biodiesel sampel pada suhu kamar (28 0C) memiliki nilai yang lebih tinggi dibanding dengan pengukuran pada suhu 40 0C. Semakin tinggi suhu maka semakin rendah pula viskositas biodiesel.
BAB V
KESIMPULAN DAN SARAN
IV.1 KESIMPULAN
Berdasarkan penelitian yang telah dilakukan didapatkan biodiesel berbahan baku jelantah dan metanol dengan NaOH sebagai katalisator. Bahan baku jelantah yang digunakan untuk setiap sampel adalah sebanyak 500 ml jelantah, NaOH 3 gram, dan variasi metanol yang digunakan adalah 60 ml, 70 ml, 80 ml, 90 ml, dan 100 ml.
Dari hasil pengukuran uji kualitas biodiesel yang dibuat dengan menggunakan pembanding biodiesel standar produksi BPPT berdasar parameter kandungan senyawa, turbiditas, dan viskositas kinematik adalah sebagai berikut :
1. Grafik pengukuran menggunakan UV/Vis spektrofotometer SP8-400 pada panjang gelombang 200-450 nm, didapatkan bahwa biodiesel sampel memiliki bentuk grafik yang menyerupai bentuk grafik pada biodiesel standar. Bentuk grafik yang sama ini terjadi karena terdapat molekul yang sama pada biodiesel sampel dan biodiesel standar.
2. Grafik pengukuran menggunakan GC diketahui bahwa bentuk grafik penguraian komponen pada biodiesel sampel mirip dengan bentuk grafik biodiesel standar. Bentuk grafik yang mirip ini terjadi karena adanya molekul yang sama pada biodiesel sampel dan biodiesel standar.
[image:73.612.99.534.114.598.2]3. Nilai turbiditas biodiesel sampel sebesar 0,69–13,72 NTU dan biodiesel standar produksi BPPT sebesar 4,22 NTU.
4. Nilai viskositas kinematik berkisar antara 4,143– 6,494 mm2/s.
Berdasarkan Berdasarkan hasil uji kualitas biodiesel berdasarkan empat parameter di atas, dapat disimpulkan bashwa biodiesel sampel yang dibuat sudah sesuai dengan biodiesel standar produksi BPPT.
IV.2 SARAN
Gritter, J.R., 1991, Pengantar kromatografi, Bandung : Penerbit ITB.
Harris, C. D., 1995, Quantitative Chemical Analysis, 4th.Ed., New York:W.H.Freeman and Company.
Kopkar, S.M., 1990, Konsep Dasar Kimia Analitik, Jakarta : Penerbit Universitas Indonesia.
Marcelo Alonso, 1994, Dasar-daras Fisika Universitas, 2nd. Ed., Jakarta : Erlangga. Prihandana, R., 2006, Menghasilkan Biodiesel Murah, Jakarta : Agromedia.
Rahmadi, A., 2008, “Pengembangan Biodiesel Indonesia Dengan Teknologi Bangsa Sendiri : Kesempatan dan Tantangan”, http://www.google.co.id/#hl=id&q=
biodiesel+menurut+E.+ Duffy+dan +J.+Patrick+filetype%3Apdf.,diakses pada tanggal 20 Januari 2009.
Sianoudis, I.A., and Drakaki. E. 2008. An approach to Poiseuille’s law in an undergraduate laboratory experiment. Greece : European Journal of Physics.
Skoog, D.A. West, M. Donald. Holler, F. James., 1965, Analitical Chemistry an Introduction, US America.
……….Statistik Ekonomi Energi, http://www.ask.com/web?l=dis&o=
15671&qsrc=2869&q= Sumber+%3A+Departemen +Energi+dan+Sumber+ Daya+Mineral%2C+BPS+dan+Handbook+Statistik+Energi+Indonesia+2006. pdf., diakses tanggal 27 Maret 2008.
Theofanis, P.,Christos C.A., and Christos, G.P., 2010, “A Nephelometric Turbidity System for Monitoring Residential Drinking Water Quality”,
http://www.springerlink.com/content/j8710m581420604x/fulltext.pdf?page=1. , diakses tanggal 15 Maret 2010.
White, F.M., 1988, Mekanika Fluida, Jakarta: Penerbit Erlangga.
LAMPIRAN A
Hasil pengukuran kandungan senyawa
[image:76.612.96.524.245.704.2]A.1. Pengukuran Kandungan senyawa menggunakan UV/Vis spektrofotometer SP8-400
Tabel A.1. Penyerapan biodiesel terhadap panjang gelombang pada radiasi gelombang elektromagnetik pada panjang gelombang 200 - 450 nm.
A.2. Pengukuran kandungan senyawa menggunakan GC
Pada pengukuran ini parameter tetapnya adalah temperatur injektor 1800C, temperature kolom 1800C, tekanan udara 2,85 bar, tekanan H2 1,4 bar, tekanan N2 0,8 bar dan volume injeksi 1 μl.
[image:78.612.95.529.189.595.2]Hexane
LAMPIRAN B Pengukuran turbiditas
Pengukuran turbiditas dilakukan secara bertahap. Yang pertama adalah pengukuran turbiditas awal biodiesel. Pengukuran ini dilakukan setelah biodiesel dihasilkan. Pengukuran turbiditas selanjutnya adalah pengukuran turbiditas setelah 75 hari pengukuran turbiditas awal.
[image:79.612.100.525.224.610.2]Pengukuran turbiditas awal
Gambar B.2 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 2.
Gambar B.4 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 4.
Gambar B.6 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 6.
Pengukuran turbiditas setelah 75 hari pengukuran.
Gambar B.8 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 1.
Gambar B.10 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 3.
Gambar B.12 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 5.
Gambar B.14 Grafik turbiditas terhadap waktu pengendapan pada biodiesel sampel 7.
Dari grafik turbiditas awal dan turbiditas setelah 75 hari pengukuran awal didapatkan nilai turbiditas sebagai berikut. Nilai turbiditas ini didapat dari nilai rata-rata pada grafik turbiditas.
Tabel B.1 Turbiditas awal dan akhir biodiesel
LAMPIRAN C
Pengukuran waktu alir untuk menentukan viskositas kinematik biodiesel.
Pada pengukuran waktu alir ini parameter tetapnya adalah volume biodiesel 50 ml dan diukur pada suhu kamar (28 0C).
[image:88.612.105.523.219.605.2]Waktu Alir Biodiesel Sampel
Gambar C.2 Grafik pertambahan massa terhadap waktu pada biodiesel sampel 2 dengan menggunakan neraca ohause.
dengan menggunakan neraca ohause.
Gambar C. 4 Grafik pertambahan massa terhadap waktu pada biodiesel sampel 4 dengan menggunakan neraca ohause.
Gambar C. 6 Grafik pertambahan massa terhadap waktu pada biodiesel sampel 6 dengan menggunakan neraca ohause.
dengan menggunakan neraca ohause.
Dari grafik di atas didapatkan waktu alir untuk masing-masing biodiesel. Tabel D.1 Waktu alir biodiesel
No MeOH (ml)
waktu alir (s)
1 60 116
2 70 94
3 80 86
4 90 86
5 100 75
6 100 74
7 100 76
LAMPIRAN D
Perhitungan viskositas kinematik biodiesel Persamaan 2.14 dar s sampel dar s sampel
t
t
tan tanΔ
Δ
=
υ
υ
Biodiesel sampel 1
s mm s s x s mm / 494 , 6 75 116 ) / 199 , 4
( 2 2
=
Biodiesel sampel 2
s mm s s x s mm / 263 , 5 75 94 ) / 199 , 4 ( 2 2 =
Biodiesel sampel 3
s mm s s x s mm / 815 , 4 75 7686 ) / 199 , 4
( 2 2
=
Biodiesel sampel 4
s mm s s x s mm / 815 , 4 75 76 ) / 199 , 4
( 2 2
=
Biodiesel sampel 5
s mm s s x s mm / 255 , 4 75 76 ) / 199 , 4
( 2 2
=
Biodiesel sampel 6
s mm s s x s mm / 143 , 4 75 74 ) / 199 , 4
( 2 2
=
Biodiesel sampel 7
s mm s s x s mm / 255 , 4 75 76 ) / 199 , 4
( 2 2