HUBUNGAN PROFIL KROMATOGRAFI DARI EKSTRAK ANGKAK DENGAN AKTIVITAS ANTIOKSIDANNYA
Djadjat Tisnadjaja dan Bustanussalam
Pusat Penelitian Bioteknologi – LIPI, Bogor
ABSTRAK
Dalam penelitian ini telah dipelajari proses ekstraksi dari angkak melalui metode refluks dan diikuti dengan partisi dengan menggunakan sistem dua pelarut serta hubungannya dengan profil kromatografi. Ekstraksi dilakukan dengan menggunakan etanol 75%. sementara partisi dengan menggunakan air – etil asetat, air – diklorometan dan air – n-heksan. Profil kromatografi yang diperoleh baik dari hasil ekstraksi maupun partisinya hampir sama namun berbeda dalam kandungan senyawa statinnya. Sesuai dengan kegunaannya, yaitu umum digunakan sebagai pengekstraksi awal, etanol memberikan ekstrak dengan profil kromatografi yang memiliki banyak senyawa. Dengan menggunakan tiga jenis pelarut organik yang berbeda polaritasnya, terlihat bahwa jumlah senyawa statin pada hasil partisi menurun dengan semakin menurunnya polaritas pelarut organik yang digunakan. Perbedaan polaritas pelarut yang digunakan pada proses partisi tunggal ini juga menghasilkan ekstrak dengan aktivitas antioksidan yang berbeda. Aktivitas antioksidan menurun seiring menurunnya polaritas dari pelarut organik yang digunakan pada proses partisi. Meskipun tingkat aktivitas antioksidan menunjukkan hubungan searah dengan konsentrasi senyawa statin yang diwakili oleh lovastatin dan atorvastatin, namun tidak bisa disimpulkan bahwa aktivitas antioksidan ditentukan oleh kandungan statin. Dari tiga batch fermentasi yang dilakukan terlihat bahwa kandungan senyawa statin maupun aktivitas antioksidan memiliki hubungan dengan pembentukan pigmen merah dari hasil fermentasi.
Kata-kata kunci : Profil kromatografi, angkak, partisi, ekstrak, polaritas, DPPH, pigmen warna.
ABSTRACT
In this research work has been studied extraction process of red fermented rice through reflux method and follow by partition with two solvents system and it’s relation to chromatography profile. Extraction was carried out by using 75% ethanol, while partition by using water – ethyl acetate, water – dichloromethane and water – n-hexane. Chromatography profile obtained from extraction and partition are similar but has differences in statin content. As it common application, that is commonly use as initial extractor, ethanol given extract with many compounds in chromatography profile. By using three various polarities of organic solvents shown that statin content of partition result is decreased as polarity reduced. Different polarity of used solvent in this single partition is resulted with difference antioxidant activity of extract. Antioxidant activity is decreasing as polarity of organic solvent used in partition is reduced. Although antioxidant activity showed related to the concentration of statin compounds which are represent by lovastatin and atorvastatin, but can not be concluded that antioxidant activity is determined by statin content. From three batches of fermentation carried out showed that statin content as well as antioxidant activity is related to red pigment formation of fermentation product.
Keywords: chromatography profile, red fermented rice, partition, extract, polarity, DPPH, color pigment
PENDAHULUAN
ubuh manusia secara alami memiliki sistem antioksidan untuk menangkal reaktivitas radikal bebas secara berkelanjutan. Namun dengan pola hidup kurang sehat yang banyak dilakukan masyarakat modern serta kondisi lingkungan dengan tingkat polusi
udara yang tinggi maka radikal bebas dalam tubuh menjadi berlebih. Untuk mengimbangi keberadaan radikal bebas yang melebihi kondisi normal maka tubuh memerlukan asupan bahan yang mengandung aktivitas sebagai antioksidan. Kebutuhan akan antioksidan tambahan tersebut bisa dipenuhi
dengan mengkonsusmsi antara lain vitamin C, vitamin E, flavonoid dan karotin (Erguder et
al, 2007).
Beras merah hasil fermentasi atau secara umum lebih dikenal sebagai angkak adalah beras yang difermentasi dengan menggunakan kapang Monascus purpureus. Angkak sudah sejak lama digunakan di negeri Cina, baik dalam makanan maupun obat tradisional, untuk memperbaiki sirkulasi darah. Banyak metabolit sekunder yang diproduksi selama proses fermentasi angkak. Beberapa pigmen warna seperti pigmen kuning (ankaflavin dan monascin), pigmen orange (monascorubrin dan rubropunctanin), serta pigmen merah (monascorubramine dan rubropunctamine) merupakan metabolit sekunder utama yang terbentuk. Dalam hasil fermentasi ini juga terkandung senyawa penurun kolesterol yaitu monakolin K, senyawa antihipertensi gamma-aminobutyric acid (GABA) serta beberapa senyawa antioksidan (Su et al, 2003; Wang et
al, 2004).
Penelitian ini dilakukan untuk melihat hubungan antara hasil ekstraksi yang diikuti dengan partisi menggunakan polaritas pelarut yang berbeda dengan tingkat aktivitas antioksidannya.
TINJAUAN PUSTAKA
Antioksidan merupakan senyawa yang dapat menghambat reaksi oksidasi dengan mengikat molekul tidak stabil yang dikenal sebagai radikal bebas sehingga kerusakan sel akan dihambat. Inhibisi dari proses oksidasi yang dilakukan oleh antioksidan bahkan dapat terjadi pada konsentrasi yang relative kecil. Antioksidan juga memiliki peran fisiologis yang beragam dalam tubuh (Kumar, 2011). Kerusakan sel akibat radikal bebas bisa menjadi penyebab terjadinya kanker. Antioksidan terdapat dalam beberapa bentuk yaitu vitamin, mineral dan fitokimia. Beberapa contoh antioksidan antara lain adalah karotenoid, β-karoten (Roberfroid and Calderon, 1995), senyawa fenol, asam gallat (Theunissen, 1995), flavonoid, quecertin (Stafford and Ibrahim, 1992) dan senyawa-senyawa lain (Halliwell et al, 1995). Berbagai tipe antioksidan bekerjasama melindungi sel normal dan menetralisir radikal bebas (Andayani et al, 2008). Jadi antioksidan adalah substansi yang dapat menunda, mencegah, menghilangkan kerusakan oksidatif pada molekul target seperti lemak, protein dan DNA (Halliwell dan Gutteridge, 2000). Menurut Kumar (2011), mekanisme kerja antioksidan adalah memutuskan rantai reaksi
pembentukan radikal bebas dengan mentransfer atom H untuk berpasangan dengan elektron bebas dari radikal bebas tersebut.
Radikal bebas diduga dapat terbentuk pada setiap kejadian pembakaran, termasuk merokok, memasak, pembakaran bahan bakar pada mesin dan kendaraan bermotor. Paparan sinar ultraviolet yang terus-menerus, cemaran pestisida dan cemaran lain di dalam makanan kita juga bisa menjadi pemicu terbentuknya radikal bebas. Untuk menghadapi ini tubuh harus melakukan tindakan protektif dengan mengurangi paparannya serta mengoptimalkan pertahanan tubuh dengan asupan antioksidan. METODE PENELITIAN
a) Produksi beras merah hasil fermentasi Bahan penelitian berupa beras merah hasil fermentasi diproduksi melalui proses fermentasi fasa padat dengan menggunakan beras sebagai media atau sumber karbon utama. Dalam proses fermentasi ini digunakan kapang Monascus purpureus yang merupakan koleksi Puslit Bioteknologi-LIPI. Sementara pengembangan inokulum dan fermentasi fasa cair dilakukan dengan menggunakan media yang mengandung tepung beras (5%), potassium dihydrogen fosfat (0,25%), sodium nitrat (0,15%), magnesium sulfat (0,1%), MSG (0,1%), kalsium klorida (0,001%) dan keasaman atau pH diatur pada nilai 6,2 (Tisnadjaja, 2003). Media yang digunakan untuk proses fermentasi fasa padat adalah beras yang sebelumnya direndam di dalam larutan yang mengandung 2% Na asetat dan 0,3% glukosa dimana perbandingan antara beras dan larutan perendam adalah 1:1. Setelah direndam, beras yang akan digunakan sebagai media tersebut ditiriskan sampai tidak ada air yang menetes dan dimasukkan ke dalam botol fermentasi masing-masing sebanyak 100 g dan kemudian di sterilisasi dengan cara pengukusan selama 2 jam (Tisnadjaja, 2003).
Fermentasi fasa cair atau submerged yang digunakan untuk mengembangkan inokulum, dilakukan dengan menggunakan Erlenmeyer ukuran 250 ml yang diisi dengan media sebanyak 50 ml. Inkubasi dilakukan pada rotary shaker dengan kecepatan putaran 100 rpm pada suhu ruang selama 7 hari. Sementara proses fermentasi fasa padat, dengan media utama beras, dilakukan dengan menggunakan botol jam sebagai reaktor dan inkubasi (kecuali dinyatakan lain) dilakukan selama 14 hari pada suhu ruang.
b) Ekstraksi
Ekstraksi dilakukan dengan metode refluks menggunakan pelarut etanol 75% selama 3 jam, dimana perbandingan antara bahan yang diekstraksi dengan pelarut adalah 1 : 3 (Tisnadjaja & Irawan, 2006). Ulangan dilakukan sebanyak tiga kali. Hasil ekstraksi dipekatkan dengan menggunakan vakum evaporator hingga diperoleh ekstrak kental, dan dilanjutkan dengan pengeringan didalam lemari pengering dengan suhu 50 oC.
c) Partisi
Ekstrak kering etanol kemudian ditimbang menjadi 3 bagian dengan berat masing-masing 15 gram dan dilarutkan dengan 150 mL aquadest. Setiap bagian tersebut dipartisi tunggal dengan menggunakan 50 mL pelarut etilasetat, diklorometan dan n-heksan dengan 3 kali ulangan. Masing-masing fraksi (etilasetat, diklorometan dan n-heksan)
kemudian dipekatkan dengan vakum evaporator hingga diperoleh ekstrak kental lalu dikeringkan.
d) Analisis KCKT
Analisis KCKT (kromatografi cair kinerja tinggi) dilakukan dengan alat merek Shimadzu dengan kondisi analisis sebagai berikut : Fase diam = µ Bondapak C18 3.9 x 330
mm
Fase gerak = Asetonitril : Air (85 : 15) Flow rate = 1 mL/menit
Detektor = UV/Vis
Panjang gelombang = 245 nm Volume injeksi = 20 µL
Sementara sebagai senyawa standar digunakan tiga bentuk senyawa statin yaitu, simvastatin, lovastatin dan atorvastatin. HASIL DAN PEMBAHASAN Fermentasi angkak
Fermentasi dilakukan dalam tiga batch yang berbeda dan dari tiga batch fermentasi ini diperoleh hasil berupa angkak dengan kepekatan warna merah yang berbeda. Perbedaan warna merah ini terjadi kemungkinan karena adanya sebagian dari beras yang tidak tampak mengalami perubahan warna yang signifikan. Hal ini mungkin terjadi akibat kurang meratanya pengadukan yang dilakukan selama proses fermentasi sehingga menghambat terjadinya kontak antara sel
Monascus purpureus dengan media. Dari tiga
batch fermentasi ini terlihat bahwa warna merah pada batch kedua lebih baik dibandingkan dua batch lainnya, dan batch pertama memberikan angkak dengan kepekatan warna merah yang paling rendah (Gambar 1).
Gambar 1. Perbedaan tingkat kemerahan pada ketiga batch fermentasi .
Analisis KCKT terhadap standar statin Dalam analisis KCKT ini digunakan tiga jenis senyawa statin sebagai standar yaitu lovastatin, simvastatin dan atorvastatin. Dari hasil analisis KCKT terhadap standar lovastatin terlihat bahwa puncak yang terbentuk oleh senyawa ini memiliki waktu retensi 4.367 menit (Gambar 2).
Minutes 0 1 2 3 4 5 6 7 8 V o lt s 0.0000 0.0025 0.0050 0.0075 0.0100 0.0125 0.0150 V o lt s 0.0000 0.0025 0.0050 0.0075 0.0100 0.0125 0.0150 1 .8 0 0 2 .1 9 2 2 .3 5 8 3 .3 8 3 3.7 2 5 4 .3 6 7 Detector A (235nm) Lovastatin 100 ppm (3) Lovastatin 100 ppm (3) Retenti on Ti me
Gambar 2. Waktu retensi dari puncak lovastatin
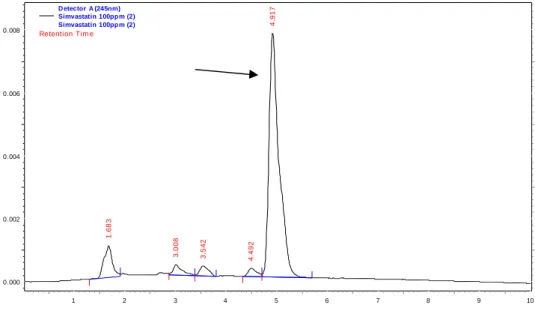
Sementara puncak yang terbentuk oleh senyawa simvastatin terjadi pada waktu retensi 4.917 menit (Gambar 3), dan senyawa atorvastatin membentuk puncak pada waktu retensi 4.975 menit. Akan tetapi pada kromatogram standar atorvastatin ini terlihat
bahwa puncaknya tidak terlihat baik dimana puncaknya hanya terlihat kecil dan mendatar, hal ini bisa terjadi dikarenakan fase gerak dan/atau fasa diam yang digunakan tidak cocok untuk analisis (Gambar 4).
Minutes 1 2 3 4 5 6 7 8 9 10 V o lt s 0.000 0.002 0.004 0.006 0.008 V o lt s 0.000 0.002 0.004 0.006 0.008 1 .6 8 3 3 .0 0 8 3 .5 4 2 4 .4 9 2 4 .9 1 7 D etector A (245nm) Simvastatin 100pp m (2) Simvastatin 100pp m (2) Retention Tim e
Minutes 1 2 3 4 5 6 7 8 9 10 V o lt s 0.0000 0.0005 0.0010 0.0015 0.0020 V o lt s 0.0000 0.0005 0.0010 0.0015 0.0020 1 .6 8 3 3 .1 4 2 3 .5 0 0 4 .9 7 5 Detector A (245nm) Atorvastatin 100ppm (2) Atorvastatin 100ppm (2) Retention T ime
Gambar 4. Waktu retensi dari puncak atorvastatin
Profil KCKT dari ekstrak etanol beras merah hasil fermentasi dan hasil partisinya
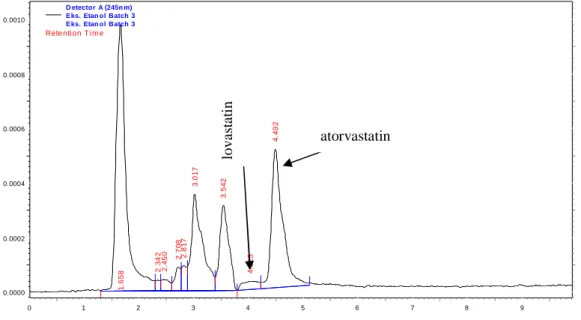
Hasil kromatogram KCKT ekstrak etanol (Gambar 5) menunjukkan adanya puncak dengan waktu retensi yang berdekatan dengan waktu retensi standar lovastatin dan atorvastatin. Hal ini menunjukkan bahwa pada
ekstrak etanol dari beras merah hasil fermentasi terkandung senyawa monakolin yang menyerupai senyawa lovastatin dan atorvastatin, tapi tidak terdeteksi adanya senyawa simvastatin. Kandungan senyawa lovastatin pada ekstrak etanol ini (0,0037%) lebih kecil bila dibandingkan kandungan atorvastatinnya (0,59%). Minutes 0 1 2 3 4 5 6 7 8 9 V o lt s 0.0000 0.0002 0.0004 0.0006 0.0008 0.0010 V o lt s 0.0000 0.0002 0.0004 0.0006 0.0008 0.0010 1 .6 5 8 2.3 4 2 2 .4 5 0 2.70 8 2 .8 1 7 3 .0 1 7 3 .5 4 2 4 .0 2 5 4 .4 9 2 D etector A (245n m) Eks. Etan ol Batch 3 Eks. Etan ol Batch 3
Rete nti on T i m e
Gambar 5. Profil KCKT dari ekstrak etanol
Kandungan lovastatin dan atorvastatin masih terdapat pada fraksi etil asetat dari hasil partisi dari ekstrak etanol tersebut di atas dengan menggunakan pelarut air – etil asetat.
Pada hasil partisi dengan etil asetat ini kandungan lovastatin yang terukur adalah 0,0052% dan kandungan atorvastatinnya adalah 0,8496%. Kandungan lovastatin atorvastatin lova st a ti n
maupun atorvastatin pada hasil partisi dengan etil asetat ini lebih besar dibandingan pada ekstrak etanolnya. Ini menunjukkan bahwa partisi dengan menggunakan pelarut semi polar etil asetat ini mampu memisahkan senyawa statin dari beberapa senyawa lain yang terkandung pada ekstrak etanol.
Ketika ekstrak etanol seperti dijelaskan di atas dipartisi dengan menggunakan pelarut air – diklorometan, kandungan lovastatin (0,0023%) maupun atorvastatin (0,3772%) menjadi lebih kecil bila dibandingkan ketika partisi dilakukan dengan menggunakan etil asetat. Ini menunjukkan bahwa pelarut diklorometan tidak mampu menarik senyawa lovastatin maupun atorvastatin sebaik yang bisa dilakukan oleh etil asetat. Hal ini ditunjukkan pula dengan kenyataan bahwa kandungan lovastatin maupun atorvastatin pada fraksi diklorometan ini lebih kecil dibandingkan pada ekstrak etanol. Kandungan lovastatin lebih rendah lagi terjadi ketika ekstrak etanol dari beras merah hasil fermentasi seperti disebutkan di atas dilanjutkan dengan partisi menggunakan pelarut air – n-heksan. Pada fraksi n-heksan dari hasil partisi ini kandungan lovastatin terukur adalah 0,0014%, sementara kandungan atorvastatin bahkan tidak terdeteksi.
Uji aktivitas antioksidan dengan metode peredaman radikal bebas
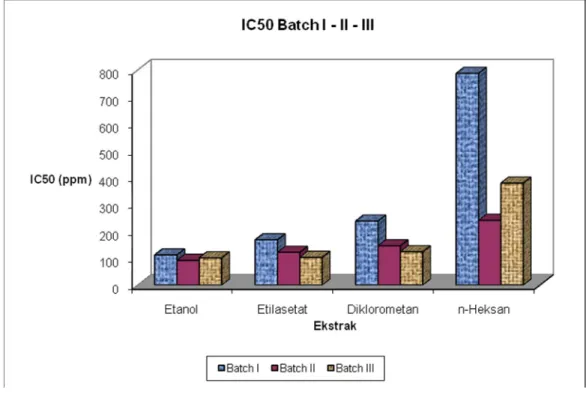
Berdasarkan nilai IC50 yang diperoleh,
urutan ekstrak yang memiliki aktivitas antioksidan dari yang tertinggi sampai terendah adalah sebagai berikut : ekstrak etanol, etilasetat, diklorometan dan n-heksan (Gambar 6). Ekstrak etanol memiliki nilai IC50
dengan kisaran 90 – 110 ppm, nilai IC50
ekstrak etanol tersebut lebih rendah dibandingkan nilai IC50 ekstrak yang lain
sehingga aktivitas antioksidan ekstrak etanol lebih aktif dibandingkan dengan ekstrak lain. Hasil ini juga menunjukkan bahwa ekstrak etanol dari angkak memiliki aktivitas antioksidan yang kuat karena memiliki nilai IC50 kurang dari 100 ppm. Sementara ekstrak
etil asetat dan diklorometan tergolong antioksidan sedang dan ekstrak n-heksan antioksidan yang sangat lemah. Menurut Bios (1958) dalam Molyneux (2004) suatu senyawa dikatakan sebagai antioksidan yang sangat kuat apabila nilai IC50 kurang dari 50 ppm, kuat
apabila nilai IC50 antara 50 – 100 ppm,
aktivitas sedang apabila nilai IC50 antara 100 –
150 ppm dan lemah bila nilai IC50 antara 150 –
200 ppm
Sebagai penjelasan yang paling mungkin untuk hal ini adalah dikarenakan ekstrak etanol banyak mengandung kelompok senyawa-senyawa polar yang memiliki aktivitas sebagai antioksidan seperti kelompok polifenol dan asam-asam lemak. Seperti dilaporkan oleh Ismail et al (2010), bahwa aktivitas antioksidan sangat berhubungan dengan komposisi atau keberadaan asam-asam lemak.
Sementara Chairote et al (2009) menunjukkan bahwa aktivitas antioksidan dari ekstrak angkak ini kemungkinan berhubungan dengan keberadaan senyawa fenolik dan pigmen warna merah. Hal ini ditunjukkan dengan adanya hubungan dimana aktivitas antioksidan lebih tinggi ketika warna merah dari hasil fermentasi pada lebih pekat, seperti terlihat pada tiga batch fermentasi yang dilakukan (Tabel 1).
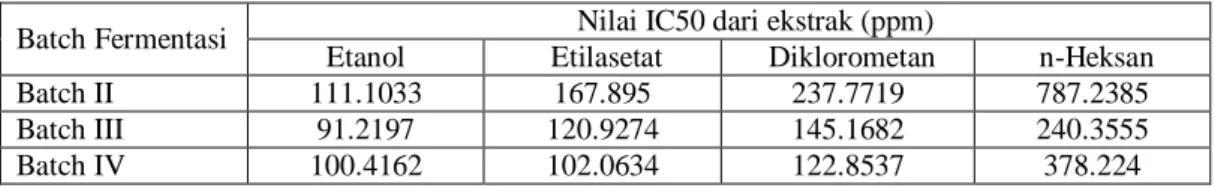
Tabel 1. Nilai IC50 dari batch fermentasi yang berbeda dan ekstrak yang berbeda
Batch Fermentasi Nilai IC50 dari ekstrak (ppm)
Etanol Etilasetat Diklorometan n-Heksan
Batch II 111.1033 167.895 237.7719 787.2385
Batch III 91.2197 120.9274 145.1682 240.3555
Batch IV 100.4162 102.0634 122.8537 378.224
Berdasarkan nilai IC50 terlihat bahwa meskipun ekstrak etanol dari angkak ini tergolong antioksidan yang kuat, namun masih jauh lebih lemah bila dibandingkan dengan nilai IC50 dari vitamin C yang hanya 3 ppm.
Hal ini karena molekul vitamin C mempunyai dua tempat abstraksi hydrogen yang terhubung secara internal, sehingga ada abstraksi lanjutan setelah abstraksi hydrogen pertama oleh radikal dari DPPH, sehingga dua molekul DPPH dapat diredam atau direduksi oleh satu molekul vitamin C.
KESIMPULAN
Dari hasil penelitian ini dapat ditarik kesimpulan bahwa disamping kandungan senyawa antikolesterol, beras merah hasil fermentasi atau angkak memiliki kandungan senyawa yang bersifat sebagai antioksidan. Senyawa antioksidan yang terkandung pada angkak ini kemungkinan adalah senyawa-senyawa metabolit sekunder yang membentuk pigmen warna merah. Meskipun tingkat aktivitas antioksidan terlihat berhubungan dengan tingkat kandungan senyawa statin atau monakolin namun hal ini masih perlu dibuktikan lebih lanjut.
Dengan nilai IC50 kurang dari 100 ppm, ekstrak etanol dari angkak tergolong sebagai antioksidan kuat.
DAFTAR PUSTAKA
Andayani, R., L. Yovita, & Maimunah, 2008. Penentuan aktivitas antioksidan, kadar fenolat total dan likofen pada buah tomat (Solanum lycopersicum I). J.
Sains dan Teknologi Farmasi,
13(1):31-37.
Chairote, E-o., Chairote, G. and Lumyong, S. 2009, Red yeast rice prepared from Thai glutinous rice and the antioxidant activities, Chiang
Mai J. Sci. 2009; 36(1): 42-49.
Erguder, B., Avci, A., Devrim, E. & Durak, I. 2007. Effects of cooking techniques on antioxidant enzyme activities of some fruits and vegetables.
Turk. J. Med. Sci.,
37(3):151-156
Halliwell,B., Aeschbach, R., Loliger, J., & Aruoma, O.I., 1995. The characterization of antioxidants.
Food Chem., 33(7): 601-617.
Halliwell, B., & J.M.C. Gutteridge. 2000, Free radical in biology and medicine. Ed.4th . Oxford University Press. New York. Kumar, S. 2011, Free radicals and
antioxidants: human and food system. Adv. In Appl. Sci. Res. 2 (1): 129-135.
Molyneux, P. 2004, The use of the stable free radical diphenyl picrylhydrazyl (DPPH) for estimating antioxidant activity.
J. Sci. Technol. 26(2):211-219
Roberfroid, M. and Calderon, P.B., 1995.
Free radicals and oxidation
phenomena in biological
systems. Marcel Dekker Inc.
USA
Stafford, H.A. and Ibrahim, R.K. 1992.
Phenolic metabolism in plants.
Plenum press, USA
Su,Y.C., Wang J.J., Lin, T.T., & Pan, T.M. 2004. Production of the
secondary metabolism β-aminobutyric acid and Monacolin K by Monascus.
J.Ind Microbiol Biotechnol.,
2003;30:41-46.
Theunissen J.D. 1995. Phenolic compounds in the leaves of ecotypes of the graminoides in the semi-arid grasslands of southern Africa. J. Arid. Envi. 31: 45-53.
Tisnadjaja, D., 2003, Pengaruh Penambahan Glukosa dan Sodium asetat pada Proses Produksi Bahan Penurun Kolesterol Monascus Powder,
Nusa Kimia, Jurnal Ilmu-Ilmu Kimia, Vol. 3, No. 1. ISSN
1412467-467X, 34-41.
Tisnadjaja, D., dan H. Irawan, 2006, Pengaruh penggunaan etanol dan kloroform pada proses pemisahan senyawa aktif lovastatin dari angkak, Nusa
Kimia, Jurnal Ilmu-ilmu Kimia
Vol. 6 No. 2.
Wang,J.J., Lee,C.L.,& Pan,T.M.,2004. Modified mutation method for screening low citrinin-producing strains of Monascus
purpureus on rice culture. J.Agric Food Chem, 2004;
52:6977-6982.
Yen Gow-Chin, Chen Hui-Yin. 1995. Antioxidant Activity of Various Tea Extract in Relation to Their Antimutagenecity. Journal
Agricultural and Food
Chemistry. Vol. 43. USA:
American Chemical Society. p. 27-32.
TANYA JAWAB Dody Priadi
Dari data yang ditunjukkan terlihat bahwa ada hubungan antara tingkat aktivitas antioksidan dengan besarnya kandungan senyawa statin atau monakolin dari hasil fermentasi. Apakah ini menunjukkan bahwa senyawa statin atau monakolin itu bersifat sebagai antioksidan ?
Djadjat Tisnadjaja
Data yang diperoleh memang menunjukkan bahwa pada saat kandungan senyawa statin atau monakolin dari hasil fermentasi lebih tinggi maka tingkat aktivitas antioksidan juga lebih tinggi. Namun demikian kami belum bisa menyimpulkannya demikian. Bahkan kami lebih cenderung untuk menyimpulkan bahwa tingkat aktivitas antioksidan adalah dipengaruhi oleh kuantitas metabolit sekunder dalam bentuk pigmen warna merah. Hal ini didukung oleh fakta bahwa ketika hasil fermentasi memberikan angkak dengan warna yang lebih merah maka aktivitas antioksidannya menjadi lebih tinggi.