LAPORAN AKHIR PENELITIAN
HIBAH BERSAING
PENJERNIHAN AIR SUNGAI MENGGUNAKAN DEDAK
KULIT PADI YANG DITAMBAHI MIKROORGANISME
EFEKTIF
Deni Rusmaya, ST., MT (NIDN: 0410057701)
Dr. Fadjari Lucia Nugroho, Dra., M.Sc., DEA (NIDN: 0414015202)
UNIVERSITAS PASUNDAN
OKTOBER, 2016
Kode/ Nama Rumpun Ilmu: 422/ TEKNIK LINGKUNGAN
RINGKASAN
Kualitas air sungai, terutama yang terdapat di daerah perkotaan, sering teridentifikasi tercemar berat. Sumber pencemar utama air sungai tersebut adalah air buangan domestik yang memiliki kandungan COD, TSS dan Coliform yang tinggi. Pengendalian pencemaran ini dapat dilakukan dengan cara pengolahan terpusat menggunakan sistem perpipaan, pengolahan setempat, dan komunal. Upaya tersebut sudah dilakukan oleh pemerintah, namun masih banyak pembuangan limbah cair domestik yang langsung masuk ke badan sungai tanpa pengolahan. Hal ini terutama berasal dari rumah yang berada di pinggir sungai. Oleh sebab itu, perlu dilakukan pengolahan air sungai dengan metode lain, yaitu dengan upaya pembersihan langsung di sungai. Penelitian ini bertujuan untuk memperoleh efisiensi pengolahan air sungai untuk parameter COD, TSS dan Coliform dengan cara memasukkan dedak kulit padi yang telah ditambahi oleh mikroorganisme efektif. Metode ini telah dilakukan oleh suatu komunitas masyarakat di Jepang, namun tingkat efisiensinya belum pernah diteliti. Secara teori ilmiah, dedak kulit padi merupakan media adsorban yang dapat digunakan untuk menyisihkan pencemar melalui mekanisme penyerapan (adsorpsi), sedangkan mikroorganisme efektif dapat menguraikan materi-materi organik di perairan. EM yang digunakan terdiri dari EM 1, EM 2 dan EM 3. Hasil penelitian terdahulu juga teridentifikasi bahwa Mikroorganisme yang terkandung dalam
mudballs menghasilkan penicillium yang bisa berfungsi sebagai
desinfektan/pembunuh bakteri merugikan. Dengan mengkombinasikan kedua materi tersebut, diperkirakan akan terjadi penyisihan COD, TSS dan Coliform. Metode penelitian yang digunakan adalah percobaan skala laboratorium dengan reaktor batch menggunakan air sungai buatan yang diatur konsentrasi COD, TSS dan Coliform nya. Hasil studi pendahuluan mendapatkan hasil bahwa proses aktivasi EM tidak perlu menggunakan molase dan waktu yang dibutuhkan hanya 1 hari. Semua jenis EM yang digunakan tidak menghasilkan produk yang akan merubah sifat air menjadi asam atau basa (hasil akhir pH tetap 6 atau sama dengan kondisi awal penelitian). Penelitian awal terhadap kemampuan setiap EM dalam menguraikan COD memberikan hasil yang relatif baik untuk EM 2 dan EM 3 dengan prosen penyisihan masing-masing 49 % dan 67 % sedangkan EM 1 hanya mampu menyisihkan sebesar 25%. Tahapan selanjutnya yaitu mencari korelasi antara jumlah mikroorganisme yang ada dengan jumlah penyisihan COD, hasil menunjukkan pertumbuhan mikroorganisme untuk EM 3 lebih cepat dibanding untuk EM 2 (puncak pertumbuhan EM 3 dicapai dalam waktu 8 jam sementara EM 2 20 jam) sehingga untuk penelitian selanjutnya dipakai EM3. Selain itu EM 3 juga memberikan hasil penyisihan COD yang tertinggi sebesar 55 % dibanding jenis EM 2. Komposisi dedak yang dipakai untuk membuat mudballs dipilih yang 20 % karena memberikan waktu dan kondisi pertumbuhan mikroorganisme yang lebih baik. Diameter mudballs optimum sebesar 2,5 cm karena pada media tersebut pertumbuhan mikroorganisme efektif lebih baik. Hasil identifikasi menunjukkan bahwa mikroorganisme efektif terdiri dari bakteri Lactobacillus dan Bacillus coagulans, Jamur terdiri dari Penicillium dan Mucor sp.
PRAKATA
Dengan mengucapkan syukur Alhamdulillah kehadirat Allah SWT, hanya dengan limpahan rahmat dan hidayah-Nya, penulis dapat menyelesaikan Laporan Akhir Penelitian Hibah Bersaing dengan judul “Penjernihan Air Sungai Menggunakan Dedak Kulit Padi yang ditambahi Mikroorganisme Efektif”.
Dalam penyusunan Laporan Kemajuan ini penulis banyak mendapat bantuan dari berbagai pihak. Untuk itu penulis mengucapkan terima kasih dengan tulus dan sedalam-dalamnya kepada semua pihak yang telah banyak membantu sehingga penulisan ini selesai.
Penulis menyadari bahwa Laporan Kemajuan Penelitian ini masih jauh dari sempurna untuk itu segala kritik dan saran yang bersifat membangun dari semua pihak selalu penulis harapkan.
Bandung, Oktober 2016
DAFTAR ISI HALAMAN PENGESAHAN 2 RINGKASAN 3 PRAKATA 4 DAFTAR ISI 5 DAFTAR TABEL 7 DAFTAR GAMBAR 8 BAB 1. PENDAHULUAN 9
BAB 2. TINJAUAN PUSTAKA 10
2.1 Pencemaran di Perairan 10
2.2 Pencemaran Organik 10
2.3 COD (Chemical Oxygen Demand) 12
2.4 DO (Dissolved Oxygen) 13
2.5 TSS 14
2.6 Karakteristik Dedak Kulit Padi 15
2.7 Mikroorganisme Efektif 16
2.8 Adsorpsi 20
2.9 Penelitian yang Pernah Dilakukan 29
2.10 Peta Jalan Penelitian 32
BAB 3. TUJUAN DAN MANFAAT PENELITIAN 34
3.1 Tujuan Penelitian 34
3.2. Manfaat Penelitian 34
BAB 4. METODE PENELITIAN 34
4.1 Tahapan Penelitian 34
BAB 5. HASIL PENELITIAN DAN PEMBAHASAN 36
5.1 Penentuan Waktu Aktivasi EM 1, EM 2 dan EM 3 36
5.2 Pemilihan EM 1, EM 2 dan EM 3 38
5.3 Pembuatan Mudballs 44
5.4 Diameter Mudballs Efektif 47
5.5 Identifikasi Mikroorganisme Efektif 49
BAB 6. KESIMPULAN 51
DAFTAR PUSTAKA 52
DAFTAR TABEL Tabel 1 Tabel 2 Tabel 3 Tabel 4 Tabel 5 Tabel 6 Nilai pH
Penyisihan COD 6 hari Penyisihan COD 36 jam
Pertumbuhan Mikroorganisme 36 jam Kontrol Nilai COD 36 jam
Pertumbuhan Mikroorganisme pada Mudballs
39 40 41 42 43 44
DAFTAR GAMBAR Gambar 1 Gambar 2 Gambar 3 Gambar 4 Gambar 5 Gambar 6 Gambar 7 Gambar 8 Gambar 9 Gambar 10 Gambar 11 Gambar 12 Gambar 13 Gambar 14
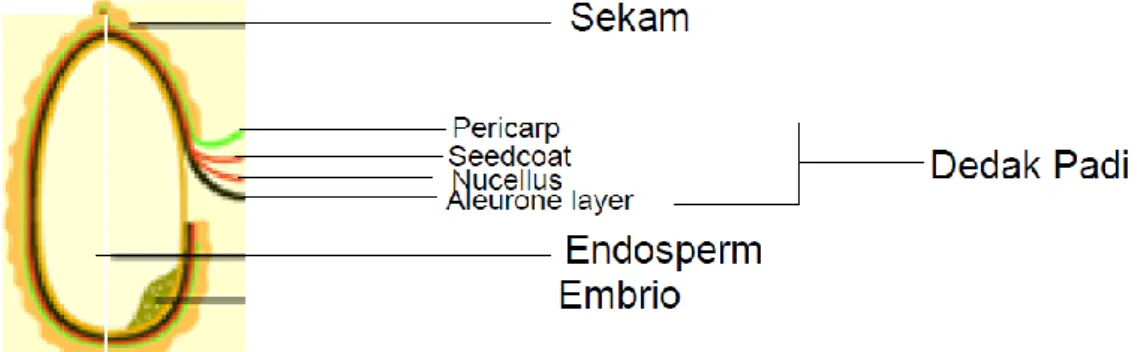
Tahapan dalam Self Purification Struktur Biji Padi
Grafik untuk persamaan sorpsi Langmuir Grafik untuk persamaan sorpsi Freundlich Grafik untuk persamaan sorpsi BET Peta Jalan Penelitian
Fishbone Diagram Penelitian Diagram alir penelitian tahun ke-2
Pertumbuhan mikroorganisme EM 1, EM 2 dan EM 3 Grafik Pengukuran pH
Grafik Penyisihan COD 6 hari Grafik Penyisihan COD 36 jam
Grafik Pertumbuhan Mikroorganisme 36 jam
Gambar Pertumbuhan Mikroorganisme pada Mudballs
12 15 27 28 29 33 35 36 38 39 40 42 43 47
BAB 1. PENDAHULUAN
Tingginya beban pencemaran yang masuk ke dalam badan air perkotaan mengakibatkan kondisi sungai menjadi rusak secara kualitas maupun estetika. Hal ini terjadi akibat pembuangan limbah cair, terutama limbah cair domestik ke sungai tanpa melalui proses pengolahan terlebih dahulu. Beberapa upaya pengendalian pencemaran telah dilakukan, yaitu dengan pengolahan limbah cair secara terpusat menggunakan sistem perpipaan, pengolahan setempat menggunakan biofilter atau septic tank, dan pengolahan secara komunal. Akan tetapi, hingga saat ini masih banyak terdapat limbah cair dari rumah tangga yang langsung dibuang ke sungai tanpa pengolahan, yaitu yang berasal dari perumahan di pinggir sungai. Air limbah domestik ini memiliki kandungan organik yang tinggi dengan indikator COD, TSS, pH asam, dan Coliform.
Salah satu upaya penanggulangan pencemaran sungai akibat limbah domestik ini adalah dengan menyisihkan langsung kontaminan dari air sungai tersebut. Metode yang digunakan oleh suatu komunitas masyarakat di Jepang dalam memperbaiki kualitas air sungainya adalah dengan memasukkan dedak kulit padi yang telah ditambahkan dengan mikroorganisme efektif. Secara teoritis, dedak kulit padi dapat berfungsi sebagai adsorban pencemar, misalnya COD dan zat warna (Kader, dkk., 2013). Sedangkan mikroorganisme efektif akan mendegradasi materi organik dalam air limbah. Dengan dasar teori tersebut, maka diperkirakan campuran dedak kulit padi dan mikroorganisme efektif akan dapat menyisihkan COD serta TSS pada air sungai. Walaupun metode ini telah dapat diperkirakan secara teoritis, namun penelitian detail terhadap efisiensi penyisihannya belum pernah dilakukan. Oleh sebab itu, penelitian ini akan dilakukan dengan tujuan mengetahui tingkat efisiensi penyisihan COD dan TSS yang terjadi menggunakan dedak kulit padi yang ditambahi dengan mikroorganisme efektif.
Apabila hasil penelitian menunjukkan nilai efisiensi yang baik, maka metode ini dapat diterapkan untuk membersihkan sungai-sungai yang tercemar, yang selama ini sangat sulit untuk dikendalikan. Dengan meningkatnya kualitas air sungai, maka
keanekaragaman biota yang dapat hidup di dalamnya juga meningkat dan penyakit bawaan air akan berkurang serta nilai sungai juga bertambah baik.
BAB 2. TINJAUAN PUSTAKA
2.1 Pencemaran di Perairan
Air permukaan seperti danau, sungai dan kolam harus dapat mendukung kehidupan akuatik dan persyaratan estetika. Air permukaan diklasifikasikan berdasarkan penggunaannya dengan syarat kualitas fisik, kimia, dan biologi. Kriteria untuk menentukan kualitas air terutama bila dikaitkan dengan masalah pencemaran air yaitu oksigen terlarut, zat padat tersuspensi, bakteri koliform, pH, suhu, dan parameter fisik kimia lainnya sesuai dengan kebutuhan serta peruntukannya.
Sumber pencemaran disebabkan oleh gejala alami (banjir, longsor) dan kegiatan manusia/ anthropogenik (aktifitas kehidupan sehari-hari, MCK, dan industri). Pencemaran yang sangat tinggi akan menimbulkan gangguan kesehatan bahkan kematian baik pada biota hewan, tumbuhan, maupun manusia. Kontaminan yang terkandung di air sungai seringkali menyebabkan bau yang tidak enak dan TSS tinggi serta pemandangan yang tidak estetik.
2.2 Pencemaran Organik
Zat organik di perairan digunakan mikroorganisme sebagai sumber energi dan bahan makanan yang diperlukan untuk pertumbuhan. Proses penguraian zat organik merupakan reaksi biokimia yang memerlukan oksigen yang terlarut di dalam air, sehingga dapat menyebabkan berkurangnya kandungan oksigen terlarut. Jika ketersediaan oksigen dalam air lebih rendah daripada oksigen yang diperlukan, maka akan menyebabkan matinya beberapa biota air dan akan timbul kondisi septik yang berbau sebagai hasil proses dalam kondisi anaerob.
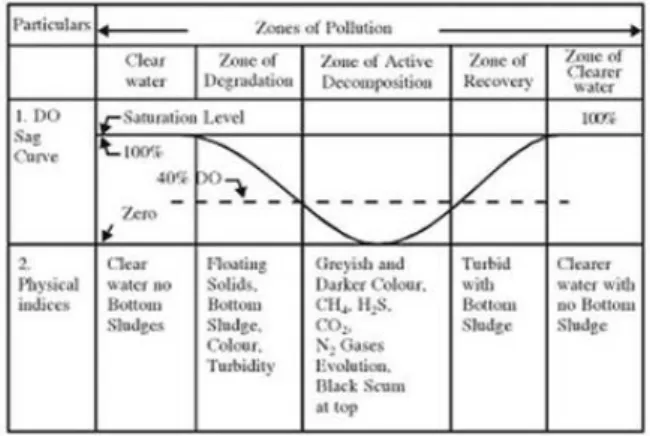
Penguraian zat organik di perairan yang mengalir akan menimbulkan perubahan kualitas air yang dibagi menjadi empat zona, yaitu :
1. Zona Degradasi (Zone of degradation)
Pada zona ini proses pencemaran dimulai dan mencapai puncak aktifitasnya. Air buangan domestik atau limbah mulai mengalami degradasi. Karena terjadi proses dekomposisi atau penguraian, maka dibutuhkan oksigen, sehingga kadar oksigen terlarut dengan cepat berkurang sampai menjadi kurang lebih 40%. Air menjadi kotor dan keruh sinar matahari tidak dapat menembus. Pada kondisi tersebut, kehidupan algae serta mikroorganisme aerob akan mati dan hilang dari sistem perairan. Karena terhentinya proses fotosintesis dari algae, maka tersedianya oksigen terlarut makin berkurang. Kehidupan ikan masih dapat bertahan terutama untuk ikan–ikan besar yang tahan terhadap kondisi dengan kandungan oksigen rendah seperti ikan lele.
2. Zona Dekomposisi Aktif (Zone of active decomposition)
Oksigen terlarut berkurang mulai dari 40% sampai 0% pada zone ini. Tetapi pada akhir zona ini oksigen mulai naik lagi hingga 40%. Hal ini terjadi bila pencemaran tidak terus berlangsung di dalam badan air. Dalam zona ini tidak ada kehidupan ikan. Warna air berubah menjadi keabu-abuan dan suasana anaerob terjadi. Dari proses dekomposisi dalam suasana anaerob, terbentuk gas–gas seperti metan, hidrogen, nitrogen, hidrogen sulfida. Bila proses dekomposisi berkurang karena jumlah pencemar senyawa organik juga berkurang, maka kadar oksigen terlarut mulai meningkat kembali sedikit demi sedikit.
3. Zona Pemulihan (Zone of recovery / rehabilitatif)
Pada zona ini kadar oksigen terlarut meningkat secara berangsur–angsur. Kehidupan makroskopis mulai nampak. Air menjadi lebih jernih dibandingkan dengan zona-zona sebelumnya. Jamur–jamur serta mikroorganisme heterotrof lainnya mulai hilang dan algae mulai timbul kembali.
4. Zona Penjernihan Kembali (Zone of cleaner water)
Zona ini ditandai dengan meningkatnya oksigen terlarut secara optimal sampai jenuh kembali yang diakibatkan dari beberapa mekanisme yang telah mampu normal kembali. Baik melalui fotosintesa maupun dengan terlarutnya oksigen dari atmosfir ke dalam air.
Gambar 1 Tahapan dalam Self Purification (Meenakshi, 2012)
2.3 Chemical Oxygen Demand (COD)
Parameter COD digunakan secara luas untuk menentukan tingkat pencemaran oleh senyawa organik dari suatu air limbah domestik maupun air limbah industri. COD menggambarkan jumlah oksigen yang dibutuhkan agar buangan organik yang ada dalam air dapat teroksidasi secara kimiawi. Bahan buangan organik akan dioksidasi oleh Kalium Bichromat menjadi gas CO2, H2O dan
ion Chrom. Jumlah oksigen yang diperlukan untuk reaksi oksidasi terhadap bahan buangan organik sama dengan jumlah Kalium Bichromat yang dipakai pada reaksi oksidasi (Wardhana, 2004).
Oksidator kuat yang sudah lama digunakan untuk mengukur konsentrasi senyawa organik yang dapat dioksidasi adalah KMnO4, satuan yang digunakan
adalah mg/L KMnO4. Oksidator lain yang diteliti untuk COD adalah CeSO4,
KIO3 dan K2Cr2O7. Ternyata oksidator K2Cr2O7 dipilih sebagai oksidator
untuk COD karena kemampuannya, hampir semua senyawa organik dapat dioksidasi dalam suasana asam dan panas.
Senyawa organik yang mudah menguap akan hilang selama pemanasan, untuk mencegah penguapan tersebut, pengukuran COD dilakukan dengan kondensor atau refluk secara tertutup (Sawyer & Mc Carty, 1994).
Reaksi oksidasi zat organik oleh K2Cr2O7 adalah sebagai berikut:
CnHaOb + cCr2O7-2 + 8c H+ → n CO2 + (a+8c)/2 H2O + 2c Cr+3
Dimana: c = 2/3 n + a/6 – b/3.
2.4 Dissolved Oxygen (DO)
Oksigen terlarut dalam air sangat penting untuk kelangsungan kehidupan organism air. Oksigen terlarut juga penting digunakan untuk menguraikan atau mengoksidasi bahan-bahan organik dan anorganik pada proses aerobik dalam air. Sumber utama oksigen dalam perairan berasal dari udara melalui proses difusi dan hasil fotosintesis organisme di perairan tersebut. Dalam kondisi aerobik, oksigen berperan dalam mengoksidasi bahan organik dan anorganik dengan hasil akhir berupa nutrient yang dapat meningkatkan kesuburan perairan (Salmin, 2005).
Konsentrasi kandungan unsur oksigen dalam aliran air ditentukan oleh besarnya suhu perairan, tekanan dan aktivitas biologi yang berlangsung di dalam air. Dari perspektif biologi, kandungan gas oksigen di dalam air merupakan salah satu unsur penentu karakteristik kualitas air yang terpenting di dalam lingkungan kehidupan akuatis. Konsentrasi oksigen dalam air mewakili status kualitas air pada tempat dan waktu tertentu. Proses dekomposisi bahan organik di dalam air berlangsung secara perlahan-lahan dan memerlukan waktu yang relatif lama. Perubahan konsentrasi oksigen di dalam air juga secara perlahan-lahan sebagai respon oleh adanya proses oksidasi serta respon berbagai macam organisme terhadap suplai bahan makanan. Dengan kata lain, keberadaan dan besar kecilnya muatan oksigen di dalam air dapat dijadikan indikator ada tidaknya pencemaran di suatu perairan (Asdak, 2007). Semakin banyak pencemar di dalam air, semakin banyak
oksigen yang dibutuhkan untuk dekomposisi bahan organik sehingga konsentrasi oksigen dalam air menurun.
Idealnya, konsentrasi oksigen terlarut pada air alam adalah mendekati konsentrasi jenuhnya. Namun dengan kehadiran bahan organik, oksigen tersebut akan digunakan pada proses oksidasi secara alami. Tentu hal ini akan mengakibatkan nilainya akan lebih kecil dari nilai konsentrasi jenuhnya. Kelarutan oksigen dalam air berkisar dari 14,6 mg/l pada temperatur 0°C hingga sekitar 7 mg/l pada temperatur 35°C pada tekanan 1 atm. Nilai DO jenuh selalu lebih kecil pada perairan yang tercemar, dimana perbandingan nilai kejenuhan DO antara air bersih dengan air tercemar dilambangkan oleh β. Sedangkan laju absorpsi oksigen di perairan tercemar umumnya lebih kecil dari air bersih dan nilai rasionya dilambangkan oleh α. Nilai β berkisar 0,8 dan nilai α berkisar 0,4 di dalam air limbah. Baik α dan β keduanya merupakan faktor penting dalam pemilihan desain peralatan aerasi (Sawyer, dkk., 1994)
2.5 TSS
Padatan tersuspensi / total suspended solid adalah padatan yang dapat meningkatkan kekeruhan air, tidak terlarut dan tidak dapat mengendap langsung. Kandungan padatan tersuspensi dalam air akan mengurangi penetrasi sinar/cahaya ke dalam air sehingga mempengaruhi regenerasi oksigen dalam proses fotosintesa (Fardiaz, 1992).
Padatan tersuspensi berkorelasi positif dengan kekeruhan. Semakin tinggi nilai padatan tersuspensi, maka nilai kekeruhan juga semakin tinggi. Kekeruhan pada perairan yang tergenang (lentik) seperti danau lebih banyak disebabkan oleh bahan tersuspensi yang berupa koloid dan partikel-partikel halus, sedangkan kekeruhan pada sungai yang sedang banjir disebabkan oleh bahan-bahan tersuspensi yang berukuran lebih besar yang berupa lapisan permukaan tanah yang terbawa oleh aliran air pada saat hujan (Effendi, 2003)
2.6 Karakteristik Dedak Kulit Padi
Dedak kulit padi, limbah pertanian yang bersifat lignocellulosic, merupakan bahan yang banyak dihasilkan dalam proses penggilingan padi dan mencapai jumlah sebesar 20% dari total produksi berasnya (Feng et al., 2004). Kebanyakan limbah ini tidak digunakan lagi. Pengelolaan limbah yang buruk bahkan membakar atau menumpukkan dedak ini begitu saja di lahan terbuka dapat mengakibatkan pencemaran lingkungan yang serius. Abu yang ditimbulkan dari proses pembakaran kulit padi seringkali menyebabkan beberapa masalah dalam pembuangannya (Naiya et al., 2009). Hanya sebagian kecil saja sekam padi digunakan untuk proses gasifikasi biomasa, ketel uap air, dan pembangkit listrik. (Arvanitoyannis and Tserkezou, 2008). Dedak kulit padi, juga dikenal sebagai sumber silika dan silikat yang murni dan murah dalam penggunaan teknologi pemisahan kromatografi, industri deterjen, semen, dan baja (Kalapathy et al., 2002). Penggunaan lain dari sekam padi ini adalah sebagai biosorban untuk penyisihan ion logam (Krishnani et al., 2008; Naiya et al., 2009). Bagian organik dari dedak kulit padi ini juga dapat meningkatkan produksi asam asetat, (Hsieh et al., 2009), xylose, furfural, xylitol, etanol, dan lignosulphonic acid (Chandrasekhar et al., 2003 dikutip dari Kuan, C.Y., etl.al, 2011).
2.7 Mikroorganisme Efektif
Mikroorganisme efektif, sebutan larutan berisi mikroorganisme yang memiliki kemampuan mendegradasi limbah dan menyuburkan tanah, pada awalnya dikembangkan oleh Dr. Higa dari Jepang pada sekitar tahun 1980an dengan memproduksi EM1. EM1 berisi campuran optimum dari bakteri asam laktat, khamir, dan bakteri fotosintentik yang bekerja secara bersama dan sinergis menghasilkan suatu sistem saling mendukung dan menguntungkan (Footer, 2014). Mikroorganisme efektif dapat memberikan kontribusi yang berarti pada proses degradasi secara biologis untuk menyisihkan pencemar organik dan logam berat. (Malik, et.al., 2012). Mikroba efektif ini, termasuk di dalamnya bakteri fotosintesis, bakteri lactic acid, bakteri nitrifikasi, sporangiumn bacillus, digunakan untuk mendekomposisi dan menyerap nitrogen organik, nitrogen ammonia, nitrogen nitrit dalam air limbah dan mengubah materi tersebut menjadi materi yang tidak berbahaya atau bahkan yang bermanfaat (Fukushi, et.al, 2010). Seiring dengan waktu terjadi penelitian dan pengembangan untuk penyempurnaan bagi kemampuan EM 1.
Higa dan Widiana (1991), menyatakan EM4 merupakan kultur campuran dari mikroorganisme yang bermanfaat bagi pertumbuhan dan produksi tanaman, dapat dimanfaatkan dalam bidang peternakan. EM4 mampu mempercepat dekomposisi bahan organik dan meningkatkan ketersediaan hara tanaman serta telah diterapkan pada berbagai jenis tanaman dan kondisi tanah. EM4 mampu meningkatkan dan memperbaiki kualitas produksi tanaman, melindungi tanaman dari serangan hama dan penyakit, meningkatkan klorofil dan fotosintesis serta meningkatkan fiksasi N2. Higa (1993) menyatakan EM4
merupakan kultur yang terdiri dari lima jenis mikroorganisme utama yaitu : bakteri fotosintetik, bakteri asam laktat, Actinomycetes, ragi dan jamur fermentasi yang bekerja secara sinergis.
EM4 merupakan biofertilizer yang diaplikasikan sebagai inokulan untuk meningkatkan keragaman dan populasi mikroorganisme di dalam tanah. EM4 mampu mempercepat dekomposisi limbah dan sampah organik, meningkatkan ketersediaan nutrisi tanaman, dan menekan aktivitas mikroorganisme
pathogen. Selain itu EM4 juga dapat digunakan untuk membersihkan air limbah, serta meningkatkan kualitas air pada tambak udang dan ikan (Indriani 1999). Menurut Condor et al (2007) Mikroorganisme yang terdapat dalam EM terdiri dari lima kelompok mikroorganisme yaitu bakteri fotosintetik, bakteri asam laktat, Khamir (Yeast), Actinomycetes, dan jamur fermentatif.
Bakteri Fotosintetik (bakteri fototropik) adalah mikroorganisme yang menyediakan makanan sendiri. Bakteri ini mensintesis asam amino, asam nukleat, zat bioaktif dan gula, senyawa-senyawa dari hasil sekresi akar, dengan menggunakan sinar matahari dan panas tanah sebagai sumber energi. Bakteri ini menggunakan energi dari sinar inframerah radiasi matahari dengan panjang gelombang 700 nm sampai 1200 nm untuk menghasilkan bahan organik, sedangkan tanaman tidak bisa melakukannya. Sehingga efisiensi tanaman meningkat. Metabolit-metabolit ini langsung diserap oleh tanaman dan juga dapat bertindak sebagai substrat pertumbuhan bakteri sehingga meningkatkan keanegaragaman hayati mikroflora. Penambahan bakteri fotosintetik ke dalam tanah meningkatkan populasi mikroorganisme efektif lainnya. Misalnya populasi VA (versikular arbskular) mikoriza yang ada di rhizosfer meningkat karena adanya senyawa-senyawa nitrogen (asam amino) yang disebabkan oleh bakteri fotosintetik yang digunakan oleh VA mikoriza sebagai substrat. Pertumbuhan VA mikoriza meningkatkan kelarutan fosfat di tanah sehingga memasok fosfor yang tadinya tidak dapat dipakai oleh tanaman. VA mikoriza dapat hidup berdampingan dengan Azobaktor, suatu bakteri pengikat nitrogen sehingga meningkatkan kemampuan polong-polongan untuk mengikat nitrogen.
Bakteri asam laktat menghasilkan asam laktat dari gula. Makanan dan minuman seperti yoghurt dan acar dibuat menggunakan bakteri asam laktat. Namun asam laktat adalah pensteril yang kuat sehingga dapat menekan mikroorganisme yang berbahaya dan mempercepat dekomposisi bahan organik. Selain itu bakteri asam laktat meningkatkan penguraian senyawa organik seperti lignin dan selulosa dan memfermentasi senyawa-senyawa ini yang biasanya memerlukan waktu yang lama. Bakteri asam laktat memiliki
kemampuan menekan penyebaran dari Fusarium yang merupakan mikroorganisme penyebab penyakit pada sistem penanaman berkelanjutan. Fusarium merangsang kondisi yang menyebabkan peningkatan nematoda yang berbahaya. Nematoda akan menghilang secara bertahap, karena bakteri asam laktat mencegah penyebaran dan fungsi Fusarium.
Khamir (Yeast) mensintesis senyawa antimikroba dan zat yang berguna untuk pertumbuhan tanaman dari asam amino dan gula yang disekresikan oleh bakteri fotosintetik, materi organik dan akar tanaman. Zat bioaktif seperti hormon dan enzim yang diproduksi oleh khamir meningkatkan sel aktif dan pembelahan akar. Hasil sekresi dapat berfungsi sebagai substrat yang berguna untuk mikroorganisme efektif seperti bakteri asam laktat dan Actinomycetes. Actinomycetes adalah struktur perantara antara struktur bakteri dan jamur, menghasilkan zat anti mikroba dari asam amino yang disekresikan oleh bakteri fotosintetik dan bahan organik. Zat antimikroba ini menekan pertumbuhan jamur dan bakteri berbahaya. Actinomycetes dapat hidup berdampingan dengan bakteri fotosintetik. Dengan demikian kedua spesies ini meningkatkan kualitas lingkungan tanah dengan meningkatkan aktivitas antimikroba dari tanah. Jamur fermentasi seperti Aspergillus dan Penicillium menguraikan bahan organik dengan cepat menghasilkan alkohol, ester dan zat antimikroba. Ini menekan bau dan mencegah infestasi dari serangga dan belatung yang berbahaya.
Ada beberapa macam EM, antara lain EM1, EM2, EM3, dan EM4. Menurut Higa, 1988 prinsip perbedaan yang ada disebabkan oleh kandungan mikrooganisme masing-masing jenis EM tersebut. EM1 merupakan merk dagang asli yang dihasilkan dan mengandung sekelompok bakteri utamanya bakteri asam laktat (menghasilkan asam laktat dalam metabolismenya), khamir, dan bakteri fotosintetik. EM1 hanya mengandung ketiga genera mikroorganisme tersebut dengan proporsi yang ideal. EM2 merupakan campuran dari lebih banyak mikroorganisme, yaitu sekitar 10 genera dan 80 spesies. Mikroorganisme tersebut, seperti halnya pada EM1, juga eksis bersama-sama sebagai sebuah konsorsium. Mikroba utama yang ada dalam
EM2 adalah bakteri fotosintesis, jamur, khamir atau kapang, dan sebagainya. Kulturnya dibuat pada medium cair dengan pH 7 dan disimpan pada pH 8,5. Populasi mikroorganisme dalam larutan adalah sekitar 109 atau 1 milyar sel setiap gram cairan. EM3 terdiri atas sekitar 95% bakteri fotosintesis dan sisanya adalah mikroorganisme yang lain. EM3 ini dikultur dan disimpan pada pH 8,5. Populasi mikroorgaisme dalam cairan yang dihasilkan juga adalah sekitar 109 atau 1 milyar sel setiap gram cairan. EM4 terdiri atas 90%
lactobacillus sp. dan microorganisme yang menghasilkan asam laktat lainnya. EM dibuat dengan kultur pada medium cair ber pH asam yaitu 4,5. Jumlah mikrooganisme tetap dipertahankan sama dengan di atas, yaitu 1 milyar per gram cairan. Prinsip EM adalah konversi ekosistem yang terdegradasi yang penuh dengan mikroba berbahaya menjadi suatu ekosistem yang produktif dan mengandung mikroorganisme yang bermanfaat. Prinsip sederhana ini adalah dasar teknologi EM di bidang pertanian dan pengelolaan lingkungan (Higa, 1993). Saat ini ada banyak versi yang berbeda dari cara menggunakan formula EM. Beberapa sulit dipahami dan beberapa membingungkan. Namun demikian aplikasi EM pada umumnya sama, tergantung pada jenis dan skala aplikasi, lokasi, kondisi fisik dan geografis (Zakaria et al, 2010).
Salah satu penggunaan EM adalah digunakan dalam pembuatan mudball. Tujuan utama dari penggunaan mudballs adalah untuk menghentikan pertumbuhan ganggang, untuk menguraikan lumpur, untuk menekan mikroorganisme patogen, dan untuk menghilangkan bau busuk yang disebabkan oleh tingginya kadar amonia, hidrogen sulfida dan metana. Selain itu, saat ini sedang dilangsungkan penelitian dan pengembangan untuk mengendalikan kadar total padatan tersuspensi (SS), oksigen terlarut (DO), kebutuhan oksigen kimia (COD), kebutuhan oksigen biologis (BOD) dan pH. EM teknologi bertindak sebagai alternatif teknologi konvensional berbasis proses kimia dengan harapan memulihkan kembali sungai yang tercemar (Zakaria et al, 2010).
2.8 Adsorpsi
Adsorpsi merupakan peristiwa menempelnya suatu zat ke permukaan zat lain pada permukaan atau pengumpulan substansi pada permukaan dari adsorban padat. Bagian yang menempel dapat disebut adsorbat, sedangkan bagian tempat menempel disebut adsorben. Peristiwa adsorpsi ini disebabkan oleh gaya tarik molekul-molekul di permukaan adsorben.
Menurut Watts 1998 (dalam Notodarmojo, 2005) bahwa adsorpsi adalah pemisahan suatu senyawa dari larutannya yang kemudian terdeposisi pada permukaan padatan, pada bidang kontak antara padatan dengan larutan, sedangkan desorpsi merupakan kebalikan dari adsorpsi, yaitu pelepasan senyawa dari padatannya dimana senyawa terdeposisi atau menempel ke dalam larutannya. Proses mekanisme adsorpsi berlangsung 3 tahap yaitu (Metcalf And Eddy, 2004) :
1. Perpindahan molekul adsorbat
Molekul adsorbat dipindahkan dari bagian larutan ke permukaan adsorben yaitu masuk ke dalam eksternal fluida film. Fase ini disebut difusi film atau difusi eksternal.
2. Difusi adsorbat melalui lapisan film
Difusi adsorbat melalui lapisan film menuju pori-pori adsorben. Fase ini disebut difusi pori-pori
3. Adsorpsi
Adsorpsi melibatkan penempelan molekul adsorbat pada permukaan adsorben, dengan luas permukaan yang tersedia pada adsorben. Fase ini disebut sebagai difusi permukaan.
Pada permukaan solid yang kontak dengan larutan cenderung berakumulasi di lapisan permukaan molekul larutan yang disebabkan oleh ketidakseimbangan gaya permukaan. Pada umumnya senyawa dengan berat molekul tinggi lebih mudah diadsorpsi daripada senyawa dengan berat molekul rendah. Faktor-faktor yang mempengaruhi daya serap adsorpsi adalah sebagai berikut (Suprihanto, 2005) :
1. pH Larutan
Kondisi pH berpengaruh pada sorpsi, karena akan mempengaruhi sifat elektrokimia larutan dan muatan permukaan partikel atau koloid tanah. Untuk sorpsi kation, umumnya pH tinggi lebih meningkatkan daya adsorpsi tanah, dan sebaliknya untuk anion. Sementara itu, kehadiran ion lain dalam solute akan menyebabkan “persaingan” untuk menempati bagian aktif partikel tanah, sehingga akan mengurangi daya sorpsi suatu jenis ion tertentu. Rasio antara tanah dengan larutan tanah (soil: solution ratio) juga berpengaruh pada sorpsi. Pada sorpsi oleh tanah yang didominasi liat dan lempung, semakin tinggi rasio tanah terhadap larutan tanah menunjukkan peningkatan adsorpsi.
2. Ukuran Molekul
Ukuran molekul dari solute juga mempengaruhi sorpsi, walaupun sampai saat ini penelitian mengenai hal ini belum konklusif. Untuk larutan ionik dan Polar, semakin kecil ukuran molekul, daya sorpsi umumnya akan lebih baik. Hal ini berbeda bila dibandingkan dengan proses sorpsi dari molekul organik tak bermuatan ionik (nonionik), di mana semakin besar molekul, fenomena sorpsi mungkin menjadi lebih intensif akibat gaya van der Waals. Keberadaan ion atau molekul lain akan menimbulkan efek kompetitif antara ion satu dengan ion lainnya, sehingga menurunkan sorpsi kontaminan yang diamati.
3. Temperatur
Temperatur, berpengaruh positif pada proses sorpsi, terutama yang bersifat chemisorption. Dalam hal ini, persamaan Arrhenius dapat digunakan untuk menjelaskan mengapa laju proses adsorpsi dipengaruhi oleh temperatur. Tetapi pada sorpsi organik, kecenderungannya tidak konsisten dan tidak proporsional. Sebagai proses eksotermik, maka peningkatan temperatur cenderung menurunkan sorpsi.
4. Komposisi Sorbat
Komposisi sorbat mempengaruhi sorpsi suatu senyawa yang ditinjau. Bila dibandungkan dengan sorpsi larutan tunggal atau ”pure solution”
dari suatu kontaminan, maka sorpsi suatu zat atau senyawa yang terjadi dalam sobat yang terdiri dari berbagai macam komponen akan lebih rendah. Hal ini terjadi karena adanya persaingan (kompetisi) antara senyawa atau zat satu dengan lainnya untuk memperebutkan “sorption site” yang ada pada permukaan sorbent.
Konsentrasi dan viskositas cairan, ukuran partikel adsorben dan intensitas pengadukan berpengaruh terhadap kurva kesetimbangan. Pengadukan akan mempercepat terjadinya kontak antara cairan partikel dengan partikel adsorben, sehingga proses adsorpsi dapat dipercepat (Ghozali, et, al. 1996). Ada beberapa faktor yang mempengaruhi proses adsorpsi, yaitu : ( Sudarjanto, 1998)
1. Karakteristik fisika dan kimia adsorben, seperti luas permukaan, ukuran pori dan komposisi kimia.
2. Karakteristik kimia dan fisika adsorbat, seperti ukuran molekul, struktur kimia, polaritas kimia dan komposisi kimia.
3. Kelarutan zat dan kensentrasinya dalam larutan. 4. Keadaan cairan, seperti temperatur dan pH 5. Waktu detensi dalam sistem.
Mekanisme proses adsorpsi pada dasarnya adalah cukup kompleks. Hal ini dapat dijelaskan dengan menggunakan berbagai tipe adsorpsi. Berbagai jenis adsorpsi melibatkan peristiwa fisika maupun kimia. Adsorpsi terhadap zat pengotor atau zat organik ke permukaan karbon aktif dapat digolongkan sebagai adsorpsi fisik. Proses adsorpsi kimia, umumnya terbatas pada berbagai ikatan kimia antara atom-atom atau molekul pada permukaan zat padat (Ghazali, et al, 1996). Proses adsorpsi dapat dibedakan menjadi 2 yaitu adsorpsi fisik dan kimia. Adsorpsi fisik terjadi apabila molekul adsorben ditahan secara fisik yaitu oleh gaya tarik Van Der Waals, sedangkan adsorpsi kimia terjadi akibat adanya pertukaran elektron atau adanya ikatan kimia antara adsorbat dengan permukaan adsorben. Karena itu proses adsorpsi tidak
bolak-balik (Tanzis dalam Wiranta, 2010). Kedua adsorpsi tersebut terjadi saat molekul dalam fase cair melekat pada permukaan zat padat sebagai akibat gaya tarik menarik pada permukaan zat (adsorben/zat yang menyerap) untuk mengatasi energi kinetik molekul pada fase cair (adsorbat/zat yang diserap) (Marlina dalam Wiranta, 2010).
Adsorpsi fisik terjadi apabila terdapat perbedaan energi dan gaya Van Der Waals antara molekul adsorbat dan permukaan adsorben. Ketika gaya tarik menarik molekul antara adsorbat dengan permukaan adsorben lebih besar daripada gaya tarik menarik antara bahan terlarut dengan pelarutnya maka bahan terlarut akan diadsorpsi di atas permukaan adsorben. Ciri adsorpsi fisik antara lain (Ghazali, et al, 1996) :
o Panas kondensasi harganya lebih besar bila dibandungkan panas penguapan (laten)
o Proses berlangsung secara reversible (bolak-balik) o Temperatur adsorpsi relatif lebih rendah.
Proses adsorpsi yang dipicu oleh proses kimia disebut adsorpsi kimia. Adsorpsi yang disebabkan oleh ikatan kimia akan lebih kuat dan permanen bila dibandingkan dengan ikatan atau adsorpsi akibat gaya fisik dan relatif tidak reversible (Notodamojo, 2005). Adsorpsi kimia terjadi ketika dihasilkan oleh reaksi antaran molekul adsorbat dan molekul adsorben (Cheremisinoff, 1978). Proses adsorpsi kimia umumnya terbatas pada berbagai ikatan kimia antara atom-atom molekul pada permukaan zat padat (Ghazali, et al, 1996). Ciri adsorpsi kimia antara lain (Ghazali, et al, 1996) :
o Gaya adsorpsi dikenal sebagai activated adsorption
o Panas reaksi yang dibebaskan, umumnya relatif lebih besar dibandingkan terhadap adsorpsi fisika
o Proses yang berlangsung tidak bolak-balik berlaku semua gas
o Laju adsorpsi relatif lebih cepat dan digunakan untuk berbagai reaksi kimia yang melibatkan katalis.
Padatan yang berfungsi untuk mengadsorpsi dikenal dengan adsorben. Adsorben (untuk adsorpsi fisik) adalah bahan padat dengan luas permukaan
dalam yang sangat besar. Permukaan yang luas ini terbentuk karena banyaknya pori halus pada padatan tersebut. Adsorben dapat berbentuk serbuk atau butiran (granular) dan penggunaannya tergantung operasi yang dilakukan. Pada umumnya partikel adsorben tersebut berdiameter antara 0,005 cm – 1,27 cm. Salah satu faktor yang penting dalam proses adsorpsi adalah luas permukaan adsorben per satuan berat adsorben. Bila dibandingkan terhadap ukuran partikel, luas permukaan internal pada pori-pori partikel lebih berpengaruh pada proses adsorpsi. (Indarti, et al, 1996). Luas permukaan mempunyai peranan penting dalam proses adsorpsi. Struktur pori berhubungan dengan luas permukaan, semakin kecil pori-pori adsorben akan menyebabkan luas permukaan adsorben semakin besar. Dengan demikian kecepatan adsorpsi akan meningkat.
Biosorpsi agak sulit untuk didefinisikan karena banyak mekanisme yang mempengaruhi keseluruhan proses tergantung pada substansi yang diserap, biosorben yang digunakan, faktor lingkungan dan berlangsung atau tidaknya proses metabolisme pada organisme hidup. ”Bio” huruf di depan menunjukkan keterlibatan entitas biologi yaitu organisme hidup, komponen atau produk yang berasal dari organisme hidup. ”Sorpsi” adalah istilah yang digunakan pada absorpsi dan adsorpsi. Istilah-istilah ini sering membingungkan. Absorpsi adalah penggabungan suatu zat dalam fase tertentu dengan zat lain dalam fase lain (seperti air yang diabsorb oleh padatan atau gas yang diabsorb oleh air) menjadi matriks tiga dimensi. Adsorpsi adalah adhesi fisik atau pengikatan ion-ion dan molekul-molekul ke permukaan molekul lain, yaitu ke permukaan dua dimensi. Dalam hal ini bahan yang terakumulasi pada antarmuka adalah adsorbat dan permukaan padat adalah adsorben (Gadd, 2009). Biosorpsi dapat didefiniskan sebagai penyisihan zat dari larutannya oleh bahan biologis. Zat-zat tersebut dapat berupa organik, anorganik dan dalam bentuk larutan atau tidak larut. Biosorpsi adalah proses fisika-kimia dimana mekanismenya dapat berupa absorpsi, adsorpsi, pertukaran ion, pengkompleksan permukaan, dan pengendapan. Biosorpsi menggunakan biomassa hidup dan biomassa mati (termasuk hasil ekskresi dan produk-produk turunan). Proses metabolisme dalam organisme hidup dapat mempengaruhi mekanisme biosorpsi
fisika-kimia. Serta bioavailabilitas polutan, jenis zat kimia dan akumulasi atau transformasi oleh sifat-sifat yang bergantung pada metabolisme (Gadd, 2009). Faktor-faktor yang mempengaruhi biosorpsi antara lain (Gadd et al, 2014) :
a. pH larutan merupakan faktor paling penting pada proses biosorpsi karena mempengaruhi spesies kimia polutan, aktivitas kelompok fungsional dalam biosorben, dan persaingan antara ion-ion yang ada dalam larutan (Vijayaraghavan Ana Yun, 2008). Meningkatkan pH meningkatkan penyisihan logam kation atau zat warna alkalin, tetapi mengurangi penyisihan logam anion atau zat warna asam.
b. Kekuatan ion larutan yang meningkat, mengurangi kemampuan daya serap karena bersaing dengan adsorbat untuk diikat oleh biosorbent. c. Konsentrasi awal polutan yang besar, meningkatkan jumlah polutan
yang diserap per satuan berat biosorben, tetapi menurunkan efisiensi penyisihan.
d. Pengaruh polutan lain termasuk persaingan untuk diikat atau gangguan lainnya. Meningkatnya konsentrasi polutan pesaing biasanya akan mengurangi penyisihan zat polutan yang ditargetkan. Namun muatan kation biomassa dapat meningkatkan biosorpsi kation lain karena adanya efek penyangga (buffer) pH.
e. Sifat biosorben dan ketersediaan tempat mengikat, pola pertumbuhan dan perlakuan, modifikasi fisika atau kimia, dosis dan ukuran sangat penting dalam kinerja.
f. Peningkatan temperatur, biasanya meningkatkan daya penyisihan biosorben terhadap polutan dan adanya peningkatan aktivitas permukaan dan energi kinetik adsorbat, tapi dapat juga merusak struktur fisik biosorben.
g. Meningkatkan kecepatan pengadukan dalam sistem larutan meningkatkan laju penyisihan polutan oleh biosorben dengan meminimalkan resistensi perpindahan massa, tapi dapat merusak struktur fisik biosorben.
Isoterm adopsi merupkan gambaran dari suatu hubungan antara jumlah zat terlarut yang diserap (sorbat) per satuan berat massa (sorben) dengan konsentrasi kesetimbangan, yaitu konsentrasi larutan setelah waktu ekuilibrasi selama 18 atau 24 jam, dengan menjaga agar tidak terjadi perubahan temperatur selama proses berlangsung (Suprihanto, 2005). Selain itu, isoterm adsorpsi juga mengungkapkan banyaknya pori yang diisi oleh adsorbat. Isoterm adsorpsi dilakukan untuk memperoleh data tentang kapasitas adsorpsi suatu adsorben terhadap zat terlarut atau adsorbat. Kapasitas adsorpsi suatu adsorben untuk zat pencemar dapat ditentukan dengan menghitung dari persamaan isoterm adsorpsi. Persamaan isoterm adsorpsi yang sering digunakan adalah persamaan isoterm sorpsi Freundlich, isoterm sorpsi Langmuir dan isoterm sorpsi BET.
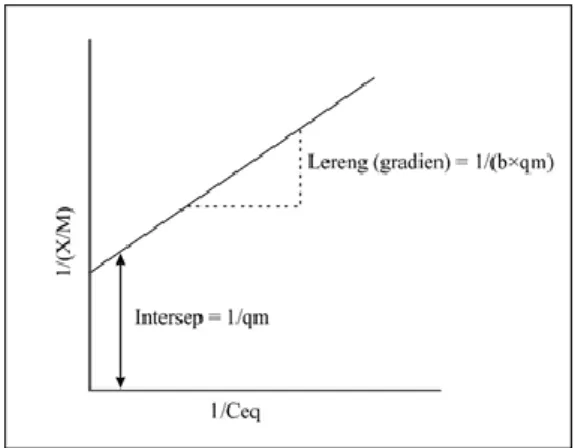
Isoterm sorpsi yang dikemukakan oleh Langmuir mempunyai asumsi bahwa adsorpsi terjadi pada satu lapisan (mono layer) atau lapisan tunggal dan digunakan pada permukaan adsorben yang homogen. Permukaan adsorben yang homogen menyatakan bahwa energi adsorpsi (kekuatan adsorpsi antara permukaan dan molekul yang teradsorpsi) adalah sama untuk semua lokasi (Cooney, 1999 dalam Haerani, 2007). Isoterm Langmuir mengasumsikan jumlah terbatas lokasi adsorpsi seragam dan tidak adanya interaksi lateral antara spesies yang diserap. Asumsi ini jelas tidak valid untuk sebagian besar sistem yang kompleks termasuk materi biologis. Dalam banyak kasus, isoterm Langmuir hanya mampu menggambarkan adsorpsi pada konsentrasi sorbat rendah (Gadd, 2009). Isoterm adsorpsi Langmuir dapat dilihat dalam persamaan sebagai berikut (Weiber dan Digiano, 1995):
Dimana:
b : konstanta kesetimbangan Langmuir
X/M : Jumlah zat yang teradsorpsi pada adsorben (mg/gr) Ceq : konsentrasi larutan pada kesetimbangan (mg/l)
qm : konstanta yang menunjukkan kapasitas adsorpsi maksimum dimana
Gambar 3 Grafik untuk persamaan sorpsi Langmuir
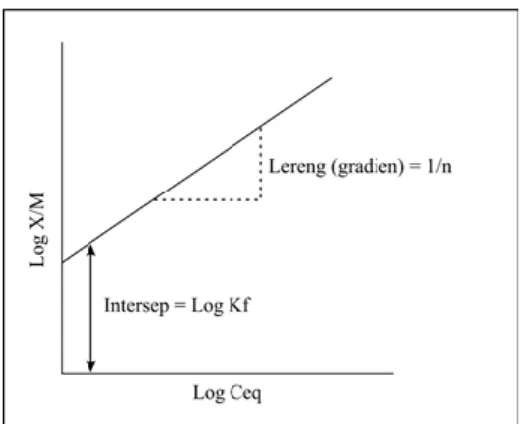
Freundlich (1926) mengajukan suatu isotherm yang dikembangkan secara empiris, walaupun kemudian penjelasan ilmiah dari formula empiris matematikanya dapat disajikan oleh Hendry (Weber & DiGiano, 1996). Ada dua pendekatan untuk menjelaskan mekanisme isoterm Freundlich, yaitu yang didekati berdasarkan persamaan Gibbs untuk kondisi larutan encer, atau dengan menganggap isoterm Freundlich tersusun dari beberapa isoterm Langmuir untuk permukaan yang heterogen (Gambar 2.2). karena bentuknya yang sederhana, formula Freundlich banyak digunakan untuk menganalisa fenomena transpor zat pencemar dalam tanah (Suprihanto, 2005). Isoterm sorpsi Freundlich dibangun atas asumsi bahwa adsorpsi terjadi pada lapisan ganda dan berlangsung pada permukaan adsorben yang heterogen. Permukaan adsorben heterogen ini mempunyai asumsi bahwa tingkat adsorpsi berbeda menurut energi/kekuatan dari lokasi. Beberapa lokasi/permukaan menarik adsorbat dengan kuat sementara beberapa lokasi lainnya menarik adsorbat dengan lemah. Tingkat adsorpsi/desorpsi berbeda menurut energi/kekuatan dari permukaan (Cooney, 1999 dalam Haerani, 2007).
Isoterm sorpsi Freundlich dapat dilihat dalam persamaan sebagai berikut : (Metcalf Ana Eddy, 2004)
= Kf × Ceq 1/n...(2.1)
Dimana :
Kf : konstanta Freundlich yang menunjukkan kapasitas adsorpsi (mg/gr)
X/M : jumlah zat yang teradsorpsi pada adsorbat (mg/gr) Ceq : konsentrasi larutan pada kesetimbangan (mg/l)
Gambar 4 Grafik untuk persamaan sorpsi Freundlich
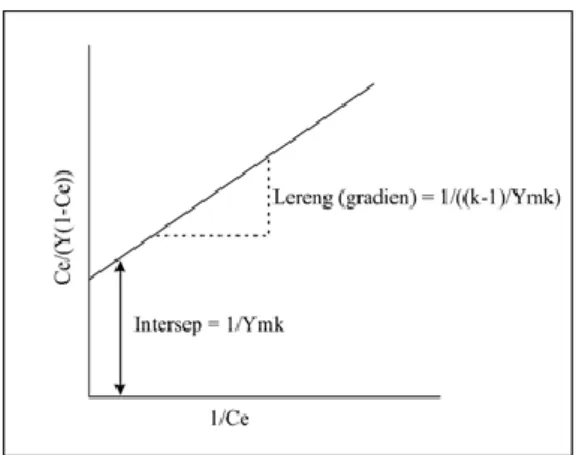
Persamaan isoterm BET digunakan untuk penyerapan molekul oleh padatan dan mulai digunakan sejak tahun 1938 oleh para peneliti di atas. Pada awalnya, persamaan ini dikembangkan untuk menjelaskan adsorpsi gas oleh permukaan padatan, kemudian dikembangkan untuk sorpsi larutan Langmuir. Model ini berdasarkan pada penyerapan lapisan ganda. Lapisan molekul pertama dianggap diikat oleh gaya fisis (gaya van der Waals), kemudian lapisan berikutnya oleh gaya yang lebih lemah, dan seterusnya. Selain terserap oleh partikel padat melalui mekanisme penyerapan lapisan ganda pada senyawa Polar, senyawa tersebut dalam tanah dapat terserap secara tidak langsung oleh tanah. Hal tersebut juga berlaku untuk gas dalam tanah. Pertama, gas tersebut diserap oleh air, kemudian melauli mekanisme penyerapan air oleh partikel, gas yang terlarut seolah-olah terserap oleh padatan (Suprihanto, 2005). Isoterm BET merupakan isoterm adsorpsi dengan multilayer pada permukaan absorben dan mengasumsikan bahwa persamaan Langmuir berlaku untuk setiap lapisan. Asumsi selanjutnya bahwa lapisan tertentu tidak perlu benar-benar selesai terbentuk sebelum terbentuk lapisan berikutnya (Gadd, 2009).
Isoterm BET merupakan metode umum untuk menentukan luas permukaan adsorben dari adsorpsi, dengan persamaan:
Dimana :
Ce : Konsentrasi adsorbat setelah diadsorpsi pada kondisi setimbang, mg/L
Y=X/M: jumlah adsorbat (X) yang diadsorpsi per unit berat adsorban (M), mg/g
K : Konstanta
Ym : Kapsitas adsorpsi maksimum, mg/g
Gambar 5 Grafik untuk persamaan sorpsi BET
2.9 Penelitian yang Pernah Dilakukan
Pembuatan mudball yang dilakukan oleh Zakaria, et al (2010). Larutan konsentrat EM1 diperlukan untuk membuat EMAS (Effective Microorganisme Active Solution) atau bisa disebut juga larutan EM aktif. Konsentrat EM mengandung mikroorganisme yang hidup tetapi dalam keadaan dorman (tidak aktif). Untuk mengaktifkan mikroorganisme, larutan EM1 diencerkan dengan air, dan aktivasi lebih lanjut dapat dilakukan dengan menambahkan molase yang bertindak sebagai sumber makanan. Secara umum EMAS merupakan campuran dari molase dan EM yang dilarutkan dalam air yang tidak mengandung klorin atau air bilasan beras yang menyediakan mineral untuk pertumbuhan mikroorganisme. Larutan ini disimpan dalam lingkungan tempat hangat (20oC – 35oC). Proses fermentasi terjadi setelah hari kedua dan EMAS
siap digunakan setelah 7-10 hari inkubasi. Setelah 7-10 hari, larutan memiliki pH 3,5 – 4,0, mengeluarkan bau manis asam yang menyenangkan, warna coklat kekuningan dan harus dipakai dalam waktu dua minggu. Mudball dibuat dengan mencampurkan tanah liat, tanah merah atau pucuk tanah dengan EMAS, kemudian dibentuk menjadi seperti bola tenis. Beberapa mudballs memiliki campuran tambahan Bokashi, suatu produk hasil fermentasi senyawa organik yang dibuat dari dedak, tepung ikan, serbuk geregaji dan lain-lain. Penelitian yang dilakukan GN Wididana (2006). Tujuan penelitian ini adalah untuk mengetahui pengaruh EM4 pada peningkatan kualitas air limbah. Penelitian dilakukan di dua lokasi pabrik permen, yaitu Nestle dan Trebor di Jakarta. Penelitian pertama dilakukan di perusahaan Nestle antara September 1994 sampai Oktober 1994, penelitian dilakukan pada tiga variasi sampel, yang pertama control yaitu limbah yang diperlakukan dengan SGB (Super Growth Bacteria) dan Mikroorganisme Starbio dengan dosis 1g/L dari air limbah. Sampel yang kedua adalah limbah yang ditambah 1 ml EM4 / 1 L air limbah tanpa pengkondisian pH (pH 4,01), dan yang ketiga adalah air limbah yang diperlakukan dengan 1 ml EM4 / 1 L air limbah dengan mengkondisikan pH (pH 7,0). Semua sampel dimasukkan ke dalam gelas kimia dan diaerasi dengan pompa dan diukur setiap hari sampai hari ke-11. Di hari ke-11 sampel tanpa pengkondisian pH (pH 4,01) dan dengan pengkondisian pH (pH 7,0) mengalami penurunan COD sebesar 80,3% dan 76%. Penyesuaian pH tidak mempengaruhi penurunan COD. Penelitian kedua dilakukan di perusahaan Trebor antara September 1994 sampai Oktober 1994, penelitian ini dilakukan dengan menambahkan 50 mL EM4 ke dalam bak aerasi dengan volume 84 m3 atau dengan konsentrasi 0,57 ml EM4/L air limbah. Penambahan EM4 dilakukan secara berkala setiap 10 hari dan dilakukan selama 40 hari. Selama 10 hari pertama setelah pengolahan dengan EM4, maka COD, BOD dan SS berkurang masing-masing 40%-55%, 42%-55% dan 44%-77%. Pengolahan dengan EM4 secara kontinyu setiap 10 hari menurunkan COD, BOD dan SS. Penelitian yang dilakukan Jasmiati et. al (2010), bioremediasi limbah cair industri tahu menggunakan Efektif Mikroorganisme (EM4). Penelitian ini
dilakukan untuk mengetahui pengaruh EM4 pada limbah tahu dilakukan percobaan 15 hari. Perlakuan terdiri dari dua, yaitu: a) limbah tahu diberikan EM4 dengan perbandingan 1:20; b) limbah tahu diberikan EM4 dengan perbandingan 1:10 dan c) dilengkapi dengan kontrol, dimana limbah tahu tanpa penambahan EM4. EM4 terlebih dahulu diaktifkan sebelum ditambahkan ke dalam limbah cair tahu yang dijadikan sebagai perlakuan, yaitu mencampurkan EM4 dan air bersih dengan perbandingan 1:20 dan difermentasi selama 5-7 hari. Penurunan konsentrasi BOD untuk perlakuan A dan B sebesar 97,87% dan 93,61%, sedangkan penurunan COD pada perlakuan A dan B sebesar 98,65% dan 89,5%.
Penelitian yang dilakukan Munawaroh et al. (2013). Penyisihan paramaeter pencemar lingkungan pada limbah cair industri tahu menggunakan Efektif Mikroorganisme 4 (EM4) serta pemanfaatannya. EM4 diaktifkan terlebih dahulu dengan mengencerkan EM4 dengan aquades dengan perbandingan 1/20 (5%) kemudian difermentasikan selama 5-7 hari di suhu ruang. Penelitian dilakukan secara batch di dalam reaktor berkapasitas 8 liter selama 20 hari dengan variasi perlakuan (P1) limbah cair tahu 6.000 mL, (P2) limbah cair tahu 5.700 mL+300 mL {5%} EM4 aktif dan (P3) limbah cair tahu 5.400 mL+600 mL {10%} EM4 aktif. Pengukuran BOD, COD, TSS dan pH dilakukan setiap 5 hari. Hasil penelitian menunjukkan pengolahan limbah cair tahu menggunakan EM4 pada perlakuan P2 mampu menurunkan nilai BOD sebesar 97%, COD sebesar 96% di hari ke 5. Serta meningkatkan pH di hari ke-20 dan TSS sebesar 1546 mg/L (awal 330) di hari ke-20.
Dedak kulit padi merupakan sumber karbon dan media biofilm dalam proses denitrifikasi biologis pengolahan air buangan yang telah diteliti untuk skala laboratorium menggunakan reaktor aliran ke atas. (Shao, et.al, 2009). Pada penelitian ini, limbah dilewatkan ke dalam suatu reaktor yang berisi sekam padi yang telah diinokulasi dengan mikroorganisme melalui pembubuhan lumpur aktif lokal. Hasil dari penelitian ini menunjukkan bahwa efisiensi penyisihan nitrat adalah 90,6%-97,8%. Selain nitrat, COD juga mengalami
penurunan konsentrasi secara tajam pada 10 hari pertama, dan terus menurun hingga hari ke-30.
Penelitian lainnya menunjukkan penyisihan yang tinggi terhadap COD dalam sungai hingga 99,33-99,99% menggunakan abu sekam padi (Kader, M.A, et.al.). Penelitian ini menggunakan air sungai yang tercemar dalam percobaannya.
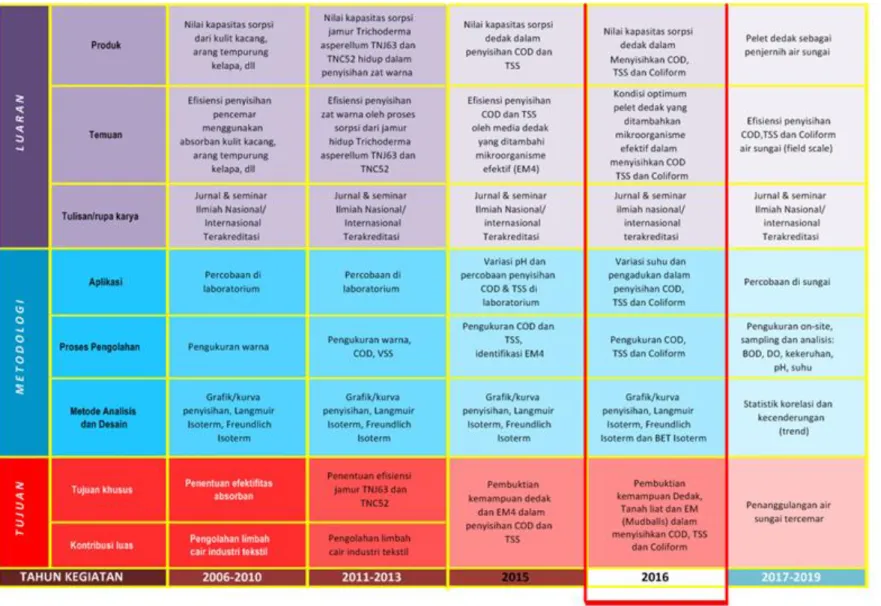
2.10 Peta Jalan Penelitian
Penelitian mengenai proses sorpsi materi pencemar ini telah dilakukan selama beberapa tahun belakangan ini. Media yang digunakan antara lain serbuk gergaji, arang tempurung kelapa, dan jamur. Sedangkan limbah yang diolah adalah buangan cair industri tekstil, dan materi yang disisihkan adalah zat warna. Selain itu, beberapa penelitian juga yang telah dilakukan peneliti lain terhadap kemampuan sekam dan dedak kulit padi ini untuk menyisihkan zat pencemar. Salah satu di antara penelitian tersebut adalah penelitian yang dilakukan oleh Shao, dkk., (2009) dalam denitrifikasi pada air limbah. Berangkat dari penelitian-penelitian tersebut, maka disusunlah suatu rencana penelitian untuk mengolah air sungai yang tercemar limbah domestik menggunakan media sorpsi berupa dedak kulit padi yang telah ditambahkan mikroorganisme efektif. Peta perjalanan dari penelitian ini dapat dilihat pada Gambar 2.5 berikut. Dedak kulit padi dipilih menjadi adsorban karena mudah diperoleh dengan harga murah dan sebenarnya merupakan limbah pertanian dari proses penggilingan padi. Tidak dilakukan perlakuan lagi terhadap dedak tersebut dan hanya ditambahkan dengan mikroorganisme efektif.
BAB 3. TUJUAN DAN MANFAAT PENELITIAN 3.1 Tujuan Penelitian
Tujuan Penelitian ini adalah untuk mengetahui kemampuan mudball (dedak, tanah liat dan EM 1, 2 dan 3) dalam menyisihkan COD, TSS dan Coliform yang ada dalam air sungai buatan.
3.2 Manfaat Penelitian
Manfaat Penelitian ini adalah bisa menjadi salah satu alternatif teknologi untuk proses pemulihan kualitas air sungai yang tercemar.
BAB 4. METODE PENELITIAN 4.1 Tahapan Penelitian
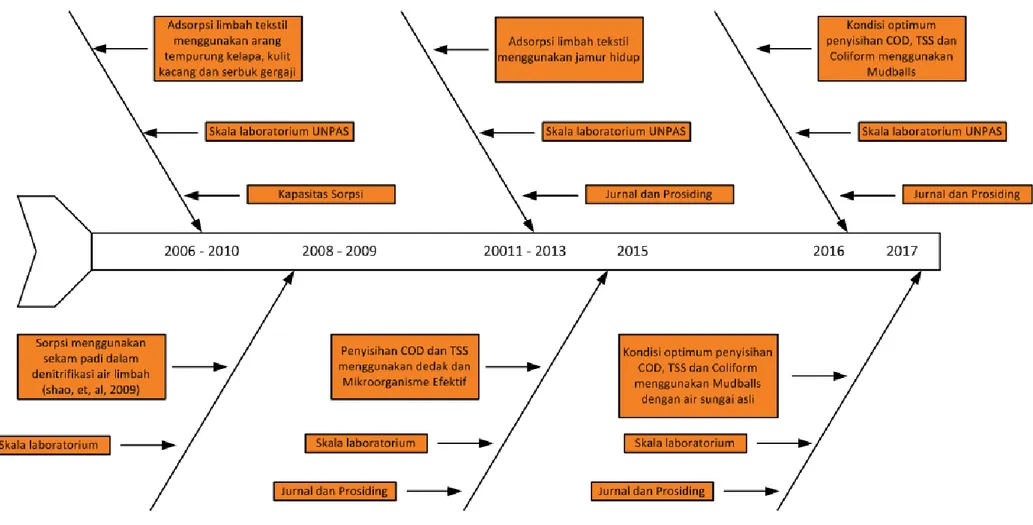
Fishbone diagram untuk penelitian dapat dilihat pada Gambar 3.1. Sedangkan diagram alir penelitian tahun ke dua dapat dilihat pada Gambar 3.2.
Berdasarkan hasil penelitian yang telah di peroleh pada tahun ke satu maka untuk tahun ke dua penelitian akan dilakukan sebagai berikut :
Pembiakan EM 1, EM 2 atau EM 3
Identifikasi Mikroorganisme yang terkandung dalam EM 1, EM 2 atau EM 3
Pembuatan Mudballs dengan penambahan EM 1, EM 2 atau EM 3
Penentuan pH optimum dengan variasi pH 4 sampai 9
Penentuan suhu optimum dengan variasi suhu 250C dan 300C
Penentuan waktu kesetimbangan/Equilibrium time
Penentuan Sorpsi dengan Variasi berat 1 mg sampai 10 mg media
Penentuan Pola Sorpsi dengan menggunakan Isoterm Freundlich, Langmuir dan BET
36 Gambar 8. Diagram alir penelitian tahun ke-2.
4.2 Luaran Penelitian
Penelitian ini akan di publikasikan di seminar internasional yang akan diselenggarakan di Osaka Jepang, pada 21 – 23 November 2016.
BAB 5. HASIL DAN PEMBAHASAN
5.1 Penentuan Waktu Aktivasi EM 1, EM 2 dan EM 3
Pengaktifan EM (1, 2 dan 3) dilakukan dengan 2 macam variasi yaitu aktifasi tanpa molase dan dengan molase 5% sedangkan komposisi EM (1, 2 dan 3) yang digunakan tetap yaitu sebanyak 5%.
37
Untuk mengetahui pertumbuhan mikroorganisme maka biakan yang sudah diinkubasi akan di masukan ke media agar dengan metoda cawan tuang.
Hasil yang diperoleh adalah sebagai berikut : EM 1
Waktu inkubasi
1 3 7
Tanpa Molase Pertumbuhan
sedikit
Pertumbuhan baik Pertumbuhan baik
Molase 5 % Pertumbuhan
sedikit
Pertumbuhan baik Pertumbuhan baik
EM 2
Waktu inkubasi
1 3 7
Tanpa Molase Pertumbuhan baik Pertumbuhan baik Pertumbuhan baik Molase 5 % Pertumbuhan baik Pertumbuhan baik Pertumbuhan baik
EM 3
Waktu inkubasi
1 3 7
Tanpa Molase Pertumbuhan baik Pertumbuhan baik Pertumbuhan baik Molase 5 % Pertumbuhan baik Pertumbuhan baik Pertumbuhan baik
38 Gambar 9 Pertumbuhan mikroorganisme EM 1, EM 2 dan EM 3
Berdasarkan data di atas maka dapat disimpulkan bahwa semua EM baik EM 1, EM 2 maupun EM 3 mampu hidup dengan dan tanpa penambahan molase, untuk EM 1 waktu aktifasi yang dibutuhkan untuk mikroorganisme dapat tumbuh dengan baik adalah setelah 3 hari sedangkan untuk EM 2 dan EM 3 waktu aktifasi yang dibutuhkan untuk mikroorganisme dapat tumbuh dengan baik cukup 1 hari.
Berdasarkan data diatas maka jenis semua jenis EM baik EM 1, EM 2 dan EM3 dapat digunakan karena mampu tmbuh dengan baik.
5.2 Pemilihan EM 1, EM 2 Dan EM 3
Untuk menentukan EM yang akan digunakan selanjutnya, maka dilakukan pemilihan jenis EM. Tahapan yang dilakukan adalah dengan menumbuhkan semua jenis EM pada air sungai buatan dengan konsentrasi COD sebesar 120 mg/l pada pH 6.
Parameter yang diperiksa meliputi : o Pengukuran pH
39
Pengukuran pH
pH dikondisikan pada pH netral atau 6. Waktu penelitian selama 7 hari. Hasil yang diperoleh adalah sebagai berikut :
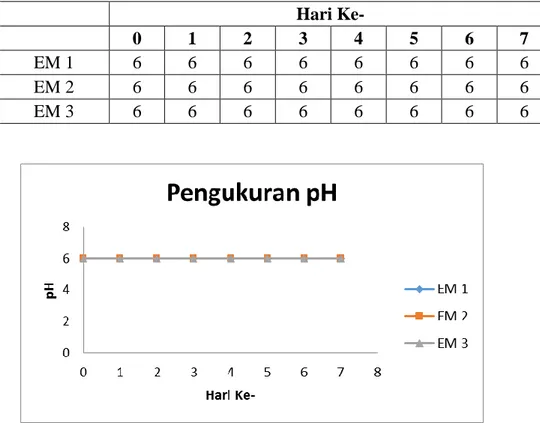
Tabel 1 nilai pH Hari Ke- 0 1 2 3 4 5 6 7 EM 1 6 6 6 6 6 6 6 6 EM 2 6 6 6 6 6 6 6 6 EM 3 6 6 6 6 6 6 6 6
Gambar 10 Grafik Pengukuran pH
Berdasarkan gambar di atas terlihat bahwa semua EM setelah waktu penelitian selama 7 hari tetap menunjukkan nilai pH yang tetap yaitu 6. Ini mengandung makna bahwa aktifitas mikroorganisme yang terjadi selama proses pengolahan limbah tidak membrikan dampak terhadap perubahan pH baik itu pH menjadi asam maupun basa. Hal ini penting karena jika terjadi perubahan pH baik menjadi asam maupum basa maka berpotensi untuk mengganggu mikroorganisme lainnya dan tidak memenuhi baku mutu yang telah ditetapkan pemerintah untuk perairan. Standar pH untuk perairan adalah 6 – 9.
40
Pengukuran Penyisihan COD
Konsentrasi COD yang digunakan untuk penelitian ini adalah 120 mg/l. Waktu penelitian adalah 6 hari. Berikut ini adalah hasil penelitian yang dilakukan.
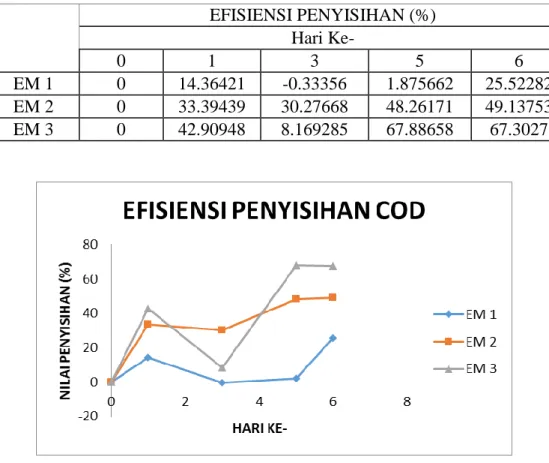
Tabel 2 Penyisihan COD 6 hari EFISIENSI PENYISIHAN (%) Hari Ke- 0 1 3 5 6 EM 1 0 14.36421 -0.33356 1.875662 25.52282 EM 2 0 33.39439 30.27668 48.26171 49.13753 EM 3 0 42.90948 8.169285 67.88658 67.3027
Gambar 11 Grafik Penyisihan COD 6 hari
Berdasarkan gambar di atas terlihat bahwa setelah waktu pengolahan selama 6 hari maka yang mampu menyisihkan COD cukup signifikan adalah EM 3 dan EM 2 dimana keduanya mampu menyisihkan COD sebesar 67 dan 49 % sedangkan untuk EM 1 hanya mampu menyisihkan sebesar 25 %. Berdasarkan data di atas maka di putuskan EM yang dipilih untuk penelitian selanjutnya adalah EM 2 dan EM 3.
41
Pengukuran COD dan Jumlah Mikroorganisme
Kondisi penelitian yang dilakukan sebelumnya pada reaktor adalah secara batch sehingga waktu pengolahan 6 hari dianggap terlalu lama karena tidak ada aliran nutrien/makanan yang masuk ke dalam reaktor selama waktu pengolahan. Atas dasar itu maka dilakukan kembali penelitian dengan waktu dan interval waktu pengukuran yang lebih singkat. Waktu pengolahan dilakukan selama 36 jam dengan interval pengukuran tiap 4 jam.
Selain itu juga untuk memastikan bahwa proses penyisihan COD yang ada di dalam rekator dilakukan oleh mikroorganisme maka jumlah mikroorganisme juga di hitung. Berikut ini adalah hasil penelitian yang dilakukan.
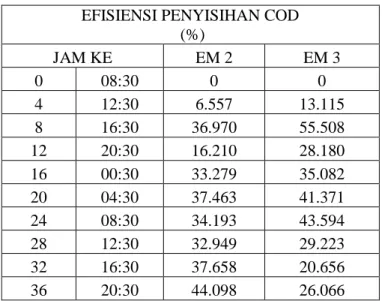
Tabel 3 Penyisihan COD 36 jam EFISIENSI PENYISIHAN COD
(%) JAM KE EM 2 EM 3 0 08:30 0 0 4 12:30 6.557 13.115 8 16:30 36.970 55.508 12 20:30 16.210 28.180 16 00:30 33.279 35.082 20 04:30 37.463 41.371 24 08:30 34.193 43.594 28 12:30 32.949 29.223 32 16:30 37.658 20.656 36 20:30 44.098 26.066
42 Gambar 12 Grafik Penyisihan COD 36 jam
Tabel 4 Pertumbuhan Mikroorganisme 36 jam PERTUMBUHAN MIKROORGANISME (Koloni/ml)
JAM KE EM 2 EM 3 0 08:30 91500 100000 4 12:30 155000 175500 8 16:30 260500 310500 12 20:30 210000 249500 16 00:30 244500 282000 20 04:30 287000 305000 24 08:30 256500 353000 28 12:30 227500 267000 32 16:30 299500 221500 36 20:30 359500 239500
43 Gambar 13 Grafik Pertumbuhan Mikroorganisme 36 jam
Tabel 5 Kontrol Nilai COD 36 jam COD KONTROL JAM KE NILAI 0 08:30 120.992 4 12:30 120.992 8 16:30 120.992 12 20:30 120.992 16 00:30 120.992 20 04:30 120.992 24 08:30 120.992 28 12:30 120.992 32 16:30 120.992 36 20:30 120.992
Berdasarkan data di atas, terlihat bahwa terdapat hubungan yang sangat erat antara jumlah mikroorganisme terhitung dengan nilai COD yang tersisihkan. Semakin banyak jumlah mikroorganisme maka semakin besar COD yag terolah. Pertumbuhan Mikroorgansme EM 3 lebih cepat di bandingkan dengan EM 2 dapat dilihat pada jam ke 8 COD yang tersisihkan oleh EM 3 mencapai 55 %b dengan jumlah
44 mikroorganisme mencapai 310.500 pada saat yang sama untuk EM 2 penyisihannya baru mencapai 37 % dengan jumlah mikroorganisme terhitung sebanyak 260.500. Berdasarkan hal tersebut maka EM yang dipilih untuk penelitian selanjutnya adalah EM 3.
5.3 Pembuatan Mudball
Mudballs di buat dengan 2 variasi yaitu
o Variasi 1 komposisi dedak 10 %, tanah liat 90 % dan EM 40 % o Variasi 2 komposisi dedak 20 %, tanah liat 80 % dan EM 40 %
Selanjutnya mudballs yang telah di buat diinkubasi dengan disimpan di dalam plastik dengan waktu inkubasi 7 hari.
Pertumbuhan mikroorganisme dalam mudballs kemudian di amati. Berikut ini adalah hasil pengamatan terhadap pertumbuhan mikroorgansime dalam mudballs.
47 Gambar 14 Gambar Pertumbuhan Mikroorganisme pada Mudballs
5.4 Penentuan Diameter Mudballs
Penentuan diameter mudball yang dipergunakan berdasarkan nilai penyisihan COD dan TSS. Hasilnya dapat dilihat pada gambar berikut.
48 Gambar 15 Nilai COD pada Mudballs
Gambar 16 Penyisihan TSS pada Mudballs
Berdasarkan gambar di atas terlihat bahwa pada diameter 2,5 cm konsentrasi COD awal yang diberikan lebih kecil dibanding dengan diameter 2 cm, kemudian nilai TSS yang mampu disisihkan oleh mudball dengan diameter 2 cm maupun 2,5 cm memberikan hasil yang sama. Oleh karena itu diameter yang terpilih adalah diameter 2,5 cm.
49
5.5 Identifikasi Mikroorganisme Efektif
Untuk mengetahui mikroorganisme yang berperan dalam penyisihan COD maka dilakukan proses identifikasi. Berikut ini adalah hasil identifikasi dari mikroorganisme yang dilakukan.
5.5.1 Identifikasi Bakteri
Gambar 17 Identifikasi Bakteri pada Mudballs
Berdasarkan gambar di atas, bakteri yang teridentifikasi ada 2. Bakteri ke 1 dengan ciri-ciri gram positif, tidak membentuk spora serta dapat berbentuk bulat maupun batang dan diidentifikasi sebagai Lactobacillus. Bakteri yang ke 2 memiliki ciri-ciri gram positif, berbentuk batang dan memiliki spora dan diidentifikasi sebagai Bacillus coagulans.
50 5.5.2 Identifikasi Jamur
Gambar 18 Identifikasi Jamur pada Mudballs (Mucor sp)
Berdasarkan gambar di atas jamur ke 1 dengan ciri-ciri memiliki hifa vegetatif, sporangium tidak memiliki rhizoid dan berbatang sporangiofor dan diidentifikasi sebagai Mucor sp.
51 Berdasarkan gambar di atas jamur ke 2 dengan ciri-ciri memiliki hifa bersefta, konidium sporangium dan memiliki phialides dan diidentifikasi sebagai Penicillium.
BAB 7. KESIMPULAN
Berdasarkan penelitian yang dilakukan dapat diambil kesimpulan : 1. Aktivasi EM tidak perlu menggunakan molases
2. Waktu aktivasi cukup 1 hari
3. Proses pengolahan limbah dengan menggunakan EM 1, EM 2 dan EM 3 tidak mengubah pH air
4. EM 2 dan EM 3 dipilih karena mampu menyisihkan COD cukup tinggi diatas 50 %
5. Terdapat hubungan yang sangat erat antara jumlah COD yang disisihkan dengan jumlah mikoorganisme yang terdapat pada reaktor
6. EM 3 dipilih untuk tahap penelitian berikutnya karena memiliki waktu tumbuh yang relatif cepat dibanding EM 2 dan memiliki persen penyisihan COD lebih tinggi
7. Komposisi dedak untuk mudballs yang dipilih adalah 20 % karena mampu menumbuhkan mikroorganisme dengan baik
52
9. Hasil identifikasi mikroorganisme untuk jenis bakteri terdiri dari Lactobacillus dan Bacilus Koagulans sedangkan untuk jamur terdiri dari Mucor sp dan Penicillium.
DAFTAR PUSTAKA
American Water Works Association, 2003., Water Quality, Principle and Practice of Water Supply Operations, Third Edition.
Fukushi, K., Hassan, K.M., Honda, R., Sumi, A., 2010, Sustainability in Food and Water, an Asian Perspective. Springer.
Footer, A., 2014, Bokashi Composting, Scraps to Soil in weeks, New Society Publisher, Canada.
Indarti, Retno., Ghozali, Mukthar & Harita., Operasi Teknik Kimia, Pusat Pengembangan Pendidikan Politeknik Bandung, Bandung, 1996
Kader, M.A., Hasan, M. T., Rahman, M. A., Alam, M.I., 2013. Effective use of rice husk ash to treat highly polluted water: case study in the Dhalassori River, Bangladesh. American Academic and Scholarly Research Journal. Vol. 5, No. 5, July 2013, pp.54-62.
Kuan, C.Y., Yuen, K.H., 2011, Physical, chemical, and physicochemical characterization of rice husk, British Food Journal, Vol. 114 no.6, 2012. Pp. 853-867. Malik, A., Grohmann, E., 2012. Environmental Protection Strategies for Sustainable Development, Springer.
Naiman, R., Kantor, S., Bibly, R. E., 2013, River Ecology and Management: Lessons from the Pacific Coastal Ecoregion, Springer.
Sawyer, C. N., McCarty, P.L., Parkin, G.F., 2003, Chemistry for Environmental Engineering and Science, Fifth Edition, McGraw Hill, New York.
Shao, L., Xu, S.X., Jin, W., Yin, H.L., 2009, Rice Husk as Carbon Source and Biofilm Carrier for Water Denitrification, Polish Journal of Environmental Study, Vol. 18, no. 4, 2009, pp. 693-699.
53
LAMPIRAN
FORMULIR EVALUASI ATAS CAPAIAN LUARAN KEGIATAN
Ketua : Deni Rusmaya, ST., MT
Perguruan Tinggi : Universitas Pasundan Bandung
Judul : Penjernihan Air Sungai Menggunakan Kulit Dedak
Padi yang DItambahkan Mikroorganisme Efektif
Waktu Kegiatan : Tahun ke 2 dari rencana 2 tahun
Luaran yang direncanakan dan capaian tertulis dalam proposal awal :
No Luaran yang direncanakan Capaian
1 Kondisi Optimum Komposisi Mudballs
Komposisi Mudballs (Dedak, tanah liat dan EM3)
2 Publikasi Seminar Nasional/Internasional
Hasil penelitian akan di presentasikan di seminar Internasional Second International
Conference on Science, Engineering & Environment, Osaka City, Japan, Nov.21-23, 2016
Publikasi Jurnal Nasional/Internasional
Hasil penelitian akan masukkan di Jurnal “International Journal of GEOMATE” Pembicara pada Pertemuan Ilmiah (Seminar/Simposium)
Nasional Internasional
Judul Makalah Effect Of Temperature On Removal Of Cod
And Tss From Artificial River Water By Mudballs Made From Em4, Rice Bran And Clay Soil
Nama Pertemuan Ilmiah Second International Conference on
Science, Engineering & Environment
Tempat Pelaksanaan Osaka, Jepang
Waktu Pelaksanaan 21 – 23 November 2016
-. Draft Makalah - -. Sudah Dikirim - -. Sedang di review √ -. Sudah dilaksanakan - Bandung, Oktober 2016 Ketua, Deni Rusmaya, ST., MT
54
PERSONALIA TENAGA PENELITI DAN KUALIFIKASINYA
A. Identitas Diri
1 Nama Lengkap (dengan gelar)
Deni Rusmaya, ST., MT
2 Jenis Kelamin L
3 Jabatan Fungsional Lektor
4 NIP/ NIK/Identitas lainnya 151 103 34 NIPY
5 NIDN 041 005 7701
6 Tempat dan Tanggal Lahir Ciamis/ 10 Mei 1977
7 E-mail denirusmaya@gmail.com
8 No.telepon/HP 081321588592
9 Alamat Kantor Jurusan Teknik Lingkungan-Universitas Pasundan Jl. Dr. Setiabudhi 193 Bandung 40153
10 Nomor telepon/Fax 022 2001985/ 022 2009574 11 Lulusan yang telah
dihasilkan
S1= 15 orang, S2=0, S3=0 12 Matakuliah yang diampu 1. Menggambar Teknik
2. Statistik Teknik Lingkungan 3. Mekanika Fluida
4. Matematika Rekayasa B. Riwayat Pendidikan
S-1 S-2
Nama Perguruan Tinggi Universitas Pasundan ITB
Bidang Ilmu Teknik Lingkungan Teknik Lingkungan
Tahun Masuk-Lulus 1995 - 2000 2003 - 2006
Judul
Skripsi/Tesis/Disertasi
Isolasi dan Seleksi Mikroorganisme
Pendegradasi Zat Warna C.I Reactive Blue 5 (CIRB 5)
Sorpsi Limbah Nikel menggunakan Kulit Kacang Tanah Nama Pembimbing/
Promotor
Dr. Fadjari Lucia Nugroho, MSc., DEA / Dr. Gatut Sudarjanto, ST., MT
Dr. Tripadma Damanhuri
C. Pengalaman Penelitian Dalam 5 Tahun Terakhir (Bukan skripsi, tesis, atau disertasi)
No. Tahun Judul Penelitian Pendanaan
Sumber* Jumlah (Juta Rp) 1 2015 Penjernihan Air Sungai
Menggunakan Dedak Kulit Padi Yang Ditambahi Mikroorganisme Efektif Hibah Bersaing 57,5,- 2. 2012 Integrasi system pengumpulan dan Hibah Bersaing Rp.37,-