BAB 2
TINJAUAN PUSTAKA
2.1 TPA Namo Bintang
Tempat pembuangan akhir (TPA) Namo Bintang telah beroperasi sejak tahun 1987. Pengelolaan sampah di TPA ini masih menggunakan sistem pembuangan terbuka (open dumping). Timbunan sampah padat dan kurangnya sanitasi menyebabkan polusi lingkungan dan terancamnya komunitas masyarakat yang tinggal di sekitar TPA. TPA Namo Bintang yang memiliki luas lebih kurang 14 hektar tidak memiliki sarana saluran dan kolam penampungan air lindi. Air lindi yang dihasilkan dari biodegradasi sampah yang ditumpuk di lahan TPA berpotensi untuk mengkontaminasi air tanah disekitar kawasan TPA. Sebagian besar masyarakat menggunakan air sumur sebagai air bersih dan juga sebagai air minum (Ashar, 2015).
Regulasi di Indonesia tidak mengeluarkan pedoman mengenai pengoperasiaan TPA yang menggunakan metode open dumping, namun justru berdasarkan UU No.18 tahun 2008 tentang pengelolaan persampahan dinyatakan bahwa TPA yang beroperasi dengan sistem open dumping harus sudah ditutup paling lama lima tahun setelah undang–undang ini di berlakukan. Oleh sebab itu, pada tahun 2013 pemerintah kota medan wajib tidak mengoperasikan TPA Namo Bintang. Menurut Standar Nasional Indonesia (SNI) No.03 3241 1994 tentang cara pemilihan TPA, disebutkan bahwa lokasi pemukiman terdekat dengan TPA adalah 500 meter, sedangkan pada kenyataannya masyarakat yang bermukim di sekitar TPA hanya berjarak 100 meter (Ashar, 2015).
2.2 Pengertian Air
Air merupakan kebutuhan hidup manusia yang sangat vital. Secara langsung air diperlukan untuk minum, mandi, mencuci dn lain-lain. Secara tidak langsung air dibutuhkan sebagai bagian ekosistem yang dengannya kehidupan di bumi dapat berlangsung. Walaupun air merupakan sumber daya yang dapat diperbarui, tetapi air akan mudah terkontaminasi oleh aktivitas manusia (Azwar, 1996) .
Kebutuhan manusia akan air sangat kompleks, antara lain untuk minum, masak, mandi, mencuci dan lain sebagainya. Dengan demikian untuk kelangsungan hidup, air harus tersedia dalam jumlah yang cukup dan berkualitas yang sangat memadai.Air minum merupakan salah satu kebutuhan manusia yang paling penting. Seperti diketahui, kadar air pada tubuh manusia mencapai 68%. Kebutuhan air minum setiap orang bervariasi dari 2,1 liter hingga 2,8 liter per hari, tergantung pada berat badan dan aktivitasnya (Suriawiria,1996).
Air terdapat bebas di alam dalam berbagai bentuk. Air bebas ini sangat penting juga dalam pertanian, pencucian dan sanitasi umum maupun pribadi, teknologi pangan dan sebagai air minum. Dalam pabrik pengolahan pangan, air diperlukan untuk berbagai keperluan misalnya : pencucian, pengupasan umbi atau buah, penentuan medium pemanasan atau pendingin,pembentukan uap, sterilisasi dan keperluan-keperluan lainnya. Sumber air dapat digolongkan menjadi dua, yaitu : air permukaan (run-off water) misalnya air danau, sungai, bendungan, air hujan, dan air dalam tanah misalnya sumur dan artesis (Sudarmadji,1989).
Berdasarkan kegunaannya, sumber air dapat dikategorikan menjadi empat golongan, yaitu :
1. Golongan A, yaitu air yang dapat digunakan sebagai air minum secara langsuntanpa diolah terlebih dahulu.
2.Golongan B, yaitu air yang dapat digunakan sebagai air baku untuk diolah sebagai air minum dan keperluan rumah tangga.
3.Golongan C, yaitu air yang dapat digunakan untuk keperluan perikanan dan peternakan.
2.2.1 Air minum
Bagi manusia, air minum adalah salah satu kebutuhan utama.Air minum seharusnya jernih, tidak berwarna, tidak berasa dan tidak berbau.Air minum pun seharusnya tidak mengandung kuman, patogen dan segala makhluk yang membahayakan kesehatan manusia.Tidak mengandung zat kimia yang dapat mengubah fungsi tubuh.Air itu seharusnya tidak korosif, tidak meninggalkan endapan pada seluruh jaringan distribusinya (Slamet, 1994).
Standar air minum yaitu suatu peraturan yang memberi petunjuk tentang konsentrasi berbagai parameter yang sebaiknya diperbolehkan ada di dalam air minum agar tujuan penyediaan air bersih dapat tercapai. Standar demikian akan berlainan dari setiapnegara , tergantung pada keadaan sosio-kultural termasuk kemajuan teknologi suatu negara. Penyediaan air bersih, selain kuantitasnya, kualitasnya pun harus memenuhi standar yang berlaku.Untuk ini perusahaan air minum, selalu memeriksa kualitas airnya sebelum didistribusikan kepada pelanggan. Karena air baku belum tentu memenuhi standar, maka seringkali dilakukan pengolahan air untuk memenuhi standar air minum.Tergantung kualitas air bakunya, pengolahan air minum dapat sangat sederhana sampai sangat kompleks. Apabila air bakunya baik, maka mungkin tidak diperlukan pengolahan samasekali. Apabila hanya ada kontaminan kuman, maka disinfeksi saja sudah cukup. Dan apabila air baku semakin jelek kualitasnya, maka pengolahan harus lengkap( Slamet,1994).
2.2.2Sumber Air
Air menguap akibat panasnya matahari. Penguapan ini terjadi pada air permukaan, air yang berada di dalam lapisan tanah bagian atas (evaporasi), air yang ada di dalam tumbuhan (transpirasi), hewan dan manusia (transpirasi, respirasi). Uap air ini memasuki atmosfir. Di dalam atmosfir uap ini akan menjadi awan dan dalam kondisi cuaca tertentu dapat mendingin dan berubah bentuk menjadi tetesan-tetesan air dan jatuh kembali ke permukaan bumi sebagai hujan.
Air hujan ini ada yang mengalir langsung masuk ke dalam air permukaan (run-off), ada yang meresap kedalam tanah (perkolasi) dan menjadi air tanah baik
yang dangkal maupun yang dalam. Air tanah dalam akan timbul ke permukaan sebagai mata air dan menjadi air permukaan. Air permukaan bersama-sama dengan air tanah dangkal, dan air yang berada di dalam tubuh akan menguap kembali untuk menjadi awan. Maka siklus hidrologis ini berulang (Slamet,J.1994).Sumber air dicirikan oleh tiga komponen utama, yaitu komponen hidrologi, komponen fisika-kimia, dan komponen biologi. Sumber-sumber air dapat dibagi menjadi beberapa bagian seperti berikut ini :
2.2.2.1 Air Permukaan
Air permukaan adalah air hujan yang mengalir di permukaan bumi. Air permukaan akan mendapat pengotoran selama pengalirannya, misalnya oleh lumpur, batang-batang kayu, daun-daun, kotoran industri dan lain sebagainya. Beberapa pengotoran untuk masing-masing air permukaan akan berbeda, tergantung pada daerah pengaliran air permukaan. Jenis pengotorannya merupakan kototan fisik, kimia, dan bakteriologi (Sutrisno, 2004).
2.2.2.2 Air Tanah (Groundwater)
Air tanah merupakan air yang berada di bawah permukaan tanah.Air tanah ditemukan pada akifer.Pergerakan air tanah sangat lambat, kecepatan arus berkisar antara 10-10-10-3m/detik dan dipengaruhi oleh porositas, permeabilitas dari lapisan tanah, dan pengisian kembali.Lapisan tanah yang bersifat porous (mampu menahan air) dan permeable (mampu melakukan atau memindahkan air) disebut akifer.Akifer terbagi menjadi, yaitu akifer dangkal dan akifer dalam.Pada akifer dangkal, maka air tanah biasanya lebih dipengaruhi oleh curah hujan.
Pada dasarnya, air tanah dapat berasal dari air hujan (presipitasi), baik melalui proses infiltrasi secara langsung ataupun secara tidak lagsung dari air sungai, danau, waduk, rawa, dan genangan air lainnya. Air tanah biasanya memiliki kandungan besi relatif tinggi. Jika air tanah mengalami kontak dengan udara akan mengalami oksigenasi, ion ferri pada ferri hidroksida yang banyak terdapat dalam air tanah akan teroksidasi menjadi ion ferro, dan segera mengalami presipitasi (pengendapan) serta membentuk warna kemerahan pada air(Effendi,2003).
2.3Jenis-jenis dari air tanah ada 3, yaitu : 2.3.1 Air Tanah Dangkal
2.3.2 Air Tanah Dalam
Air tanah dalam memiliki metode pengambilan yang jauh lebih sulit dibandingkan dengan air tanah dangkal. Biasanya untuk mengambil air tanah dalam ini digunakan suatu bor dan pipa yang dimasukkan hingga kedalaman 100-300 m lalu akan didapatkan suatu lapisan air. Air akan menyembur keluar jika terdapat tekanan yang cukup besar pada tanah dan biasanya disebut sebagai air sumur artesis. Jika air tidak dapat keluar maka digunakan pipa untuk mendorong air tanah dalam agar dapat dikeluarkan. Dari segi kualitas, air tanah dalam memiliki kualitas yang lebih baik daripada air tanah dangkal karena proses penyaringannya jauh lebih sempurna danbebas dari bakteri. Kandungan zat-zat kimia pada air tanah disusun sesuai dengan masing-masing lapisan-lapisan tanah yang dilalui (Sutrisno, 2004).
2.3.3 Air Atmosfer atau Air Hujan
2.4 Standar Kualitas Air Minum
Pengertian air minum menurut PERMENKES RI No.492/MENKES/IV/2010 adalah air yang melalui proses pengolahan atau tanpa proses pengolahan yang memenuhi syarat kesehatan (bakteriologis, kimiawi, radioaktif dan fisik) dan dapat langsung diminum. Kualitas air yaitu sifat air dan kandungan makhluk hidup, zat, energi atau komponen lain didalam air. Kualitas air dinyatakan dengan beberapa parameter, yaitu parameter fisika (suhu, warna, rasa, kekeruhan, padatan terlarut dan sebagainya), parameter kimia (pH, oksigen terlarut, BOD, kadar logam dan sebagainya), parameter biologi (keberadaan plankton, bakteri dan lain sebagainya) dan parameter radioaktif (Effendy, 2003).
2.4.1 Parameter Fisika
Parameter fisika yang biasa digunakan untuk menentukan kualitas air meliputi cahaya, suhu, warna dan bau, kecerahan dan kekeruhan, konduktivitas, padatan total, padatan terlarut, padatan tersuspensi dan salinitas.
Parameter fisika pada air, yaitu sebagai berikut :
1. Suhu
2. Kekeruhan
Kekeruhan menggambarkan sifat optik air yang ditentukan berdasarkan banyaknya cahaya yang diserap dan dipancarkan oleh bahan-bahan yang terdapat didalam air.Nilai kekeruhan maksimum yang diperbolehkan pada air minum yaitu sebesar 5 skala NTU.Kekeruhan dapat disebabkan karena adanya bahan organik dan anorganik yang tersuspensi dan terlarut (misalnya lumpur dan pasir halus). Tingginya nilai kekeruhan juga dapat mempengaruhi proses penyaringan dan mengurangi efektivitas pada proses penjernihan air (Effendy,2003).
Air dikatakan keruh, apabila air tersebut mengandung begitu banyak partikel bahan yang tersuspensi sehingga memberikan warna yang berlumpur dan kotor. Kekeruhan tidak merupakan sifat dari air yang membahayakan, tetapi ia menjadi tidak disenangi karena rupanya. Terdapatnya suhu, intensitas bau, rasa dan kekeruhan yang melebihi standar yang ditetapkan dapat menimbulkan kekhawatiran terkandungnya bahan-bahan kimia yang dapat mengakibatkan efek toksik terhadap manusia (Sutrisno,2004).
3. Warna dan Bau
4. Padatan Total, Terlarut, dan Tersuspensi
Padatan total adalah bahan yang tersisa setelah air sampel mengalami penguapan dan pengeringan pada suhu tertentu. Padatan tersuspensi total yaitu bahan-bahan
tersuspensi biasanya memiliki diameter sebesar>1 μm. Padatan tersuspensi total
terdiri dari lumpur dan pasir halus serta jasad-jasad renik. Padatan terlarut total adalah bahan-bahan terlarut dengan ukuran diameter yaitu <10-6 mm yang berupa senyawa-senyawa kimia (Effendy,2003).
2.4.2 Parameter Kimia
Air minum tidak boleh mengandung zat-zat kimia yang bersifat beracun dan kadarnya tidak boleh melampaui ambang batas yang telah ditentukan. Zat-zat mineral yang dibutuhkan oleh tubuh juga harus memiliki kadar yang sesuai sehingga tidak membahayakan bagi kesehatan manusia. Adapun yang menjadi parameter kimia untuk kualitas air meliputi derajat keasaman (pH), kesadahan, kandungan bahan organik maupun anorganik dan lain-lain. Berikut ini parameter-parameter kimia pada air, yaitu:
1. Derajat keasaman (pH)
2. Kesadahan
Kesadahan (hardness) yaitu gambaran kation logam divalen. Kation-kation ini dapat bereaksi dengan sabun membentuk endapan maupun dengan anion-anion akan membentuk karat pada peralatan logam. Kation utama penyebab kesadahan pada umumnya adalah kalsium dan magnesium.Kesadahan air berkaitan erat dengan kemampuan air untuk membentuk busa.Semakin besar kesadahan air, semakin sulit sabun untuk membentuk busa karena terjadi presipitasi.
Tebbut (1992) mengemukakan bahwa nilai kesadahan tidak memiliki implikasi langsung terhadap kesehatan manusia. Kesadahan yang tinggi dapat menghambat sifat toksik dari logam berat karena kation-kation penyusun kesadahan seperti kalsium dan magnesium membentuk senyawa kompleks dengan logam berat tersebut. Air permukaan biasanya memiliki kesadahan yang lebih kecil daripada air tanah. Menurut PERMENKES No.492/MENKES/PER/IV/2010 batas maksimum kesadahan pada air yaitu 500 mg/L.
3. Kandungan bahan organik dan anorganik
Bahan-bahan organik juga dibutuhkan untuk tubuh dalam jumlah tertentu.Tetapi apabila kandungan bahan organik sudah melewati batas maksimum yang ditentukan maka dapat menimbulkan gangguan kesehatan pada tubuh.Pada perairan alami, nilai kandungan bahan organik pada air berkisar antara 1-30 mg/L. Senyawa anorganik terdiri atas logam dan logam berat yang pada umumnya bersifat toksik. Biasanya senyawa ini dihasilkan dari limbah domestik dan industri. Kandungan bahan kimia anorganik yang terdapat didalam air, antara lain garam dan ion-ion logam seperti besi dan kalsium(Effendy,2003).
2.4.3 Parameter Mikrobiologi
2.4.4 Standar Baku Air
Standar mutu air atau air untuk kebutuhan rumah tangga ditetapkan berdasarkan peraturan menteri kesehatan republik Indonesia Nomor 492 Tahun 2010 tentang persyaratan kualitas air minum. Standarisasi kualitas air minum tersebut betujuan untuk memelihara, melindungi dan mempertinggi derajat kesehatan masyarakat, terutama dalam pengelolaan air atau kegiatan usaha mengolah dan mendistribusikan air minum untuk masyarakat umum. Adanya standarisasi tersebut, dapat dinilai kelayakan pendistribusian sumber air untuk rumah tangga maupun industri (Kusnaedi, 2010).
2.5 Logam Berat
Logam yang dapat menyebabkan keracunan adalah jenis logam berat saja. Logam ini termasuk logam yang esensial seperti Cu, Zn, Se dan yang non esensial seperti Hg, Pb, Cd, dan As. Terjadinya keracunan logam paling sering disebabkan pengaruh pencemaran lingkungan oleh logam berat, seperti penggunaan logam sebagai pembasmi hama (pestisida), pemupukan maupun karena pembuangan limbah pabrik yang menggunakan logam.Logam juga dapat menyebabkan timbulnya suatu bahaya pada makhluk hidup.Hal ini terjadi jika sejumlah logam mencemari lingkungan.Logam-logam tertentu sangat berbahaya bila ditemukan dalam konsentrasi tinggi dalam lingkungan (dalam air, tanah, dan udara), karena logam tersebut mempunyai sifat yang merusak jaringan tubuh makhluk hidup (Darmono,1995).
2.5.1 Besi (Fe)
Besi yang murni adalah logam berwarna putih-perak, yang kukuh dan liat. Ia melebur pada 1535 oC. Jarang terdapat besi komersial yang murni; biasanya besi mengandung sejumlah kecil karbida, silisida, fosfida, dan sulfida dari besi, serta sedikit grafit. Zat-zat pencemar ini memainkan peranan penting dalam kekuatan struktur besi. Asam nitrat 1+1 atau asam nitrat pekat yang panas melarutkan besi dengan membentuk gas nitrogen oksida dan ion besi(III) :
Fe + HNO3 + 3H+ Fe3+ + NO + 2H2O
Garam-garam besi(II) (atau fero) diturunkan dari besi(II) oksida, FeO. Dalam larutan, garam-garam ini mengandung kation Fe2+ dan berwarna sedikit hijau. Garam-garam besi(III) (atau feri) diturunkan dari oksida besi (III), Fe2O3. Mereka lebih stabil daripada garam besi(II). Dalam larutannya, terdapat kation-kation Fe3+ yang berwarna kuning muda (Vogel, 1985).
Beberapa hasil penelitian menunjukkan adanya keterkaitan antara Fe berlebih yang bisa mengakibatkan diabetes, kanker, meningkatkan resiko infeksi, reumatik, juga meningkatkan resiko terhadap penyakit jantung. Kadar Fe yang terlalu tinggi bisa mengakibatkan kerusakan sel akibat radikal bebas. Salah satu penyebab serangan jantung adalah tingginya kadar Fe dalam tubuh (Widowati, 2008).Kandungan besi didalam air dipengaruhi oleh beberapa faktor, antara lain kedalaman air didalam tanah semakin dalam air yang meresap maka semakin tinggi kelarutan besi, rendahnya pH air dan suhu yang tinggi menyebabkan berkurangnya kadar O2 dalam air menguraikan kadar besi. Air bersih yang mengandung besi biasanya menimbulkan rasa dan bau logam yang amis pada air (Atmaningsih,2007).
2.5.1.1 Toksisitas Besi
Mineral yang sering berada dalam air dengan jumlah besar adalah kandungan Fe. Apabila Fe tersebut berada dalam jumlah yang banyak akan muncul berbagai gangguan lingkungan. Tempat pertama yang mengontrol pemasukan logam besi (Fe) dalam tubuh ialah di dalam usus halus.Bagian usus ini berfungsi untuk absorpsi dan sekaligus sebagai eksresi yang tidak diserap.Besi dalam usus diabsorpsi dalam bentuk feritin, dimana bentuk ferro lebih mudah diabsorpsi daripada bentuk ferri.Feritin masuk ke dalam darah dan berubah bentuk menjadi senyawa transferin.
2.5.2 Logam Zink (Zn)
Zink adalah logam putih–kebiruan, mudah ditempa dan liat pada 110–1500C. Logam Zn melebur pada suhu 4100C dan mendidih pada 9060C (Svehla, 1985). Zn dapat bereaksi dengan asam, basa dan senyawa nonlogam. Zink (Zn) di alam tidak berada dalam keadaan bebas, tetapi dalam bentuk terikat dengan unsur lain berupa mineral, cat, produk karet, obat-obatan dan sebagainya (Widowati, 2008).
Pada manusia zink merupakan unsur yang terlibat dalam sejumlah besar enzim yang mengkatalisis reaksi metabolik yang vital. Karena fasilitasnya yang digunakan dalam sintesis DNA dan RNA dan dalam metabolisme protein, Zn juga esensial untuk pertumbuhan anak (Darmono, 1995).
2.5.2.1 Toksisitas Logam Zink
Administrasi Makanan dan Obat (Food and Drug Administration) menyatakan bahwa zink dapat merusak saraf dalam hidung dan menyebabkan terjadinya anosmia atau kehilangan kemampuan membau, baik secara permanen atau temporer dan hal ini dapat membahayakan karena penderita anosmia tidak dapat membedakan makanan yang masih segar dengan makanan yang sudah membusuk (Sembel, 2015).
2.5.2.2 Defisiensi Zink
Zn bukan merupakan senyawa toksik dan merupakan unsur esssensial bagi pertumbuhan semua jenis hewan dan tumbuhan. Zn akan bersifat toksik ketika berada dalam bentuk ionnya. Meskipun logam ini merupakan logam yang essensial namun jika dikonsumsi dalam dosis yang tinggi akan berbahaya dan bersifat toksik.Gejala defisiensi Zn antara lain pertumbuhan terhambat, rambut rontok, diare, berkurangnya fungsi indera penglihatan,danSebagainya
(Widowati,2008).
2.6Spektrofotometer Serapan Atom
2.6.1Intrumentasi Spektrofotometer Serapan Atom
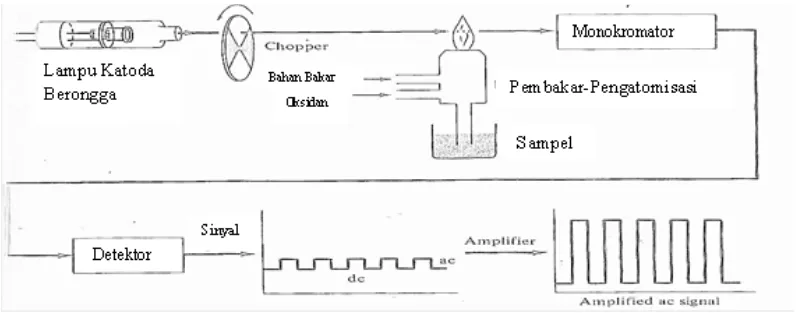
Instrumen spektrofotometer serapan atom dan bagiannya dapat dilihat pada gambar 2.1 berikut :
Gambar 2.1. Diagram Spektrofotomer Serapan Atom (Kennedy, 1984). Komponen-komponen Spektroskopi Serapan Atom (SSA):
1. Sumber Sinar
Sumber sinar yang lazim dipakai adalah lampu katoda berongga (hollow cathode lamp).Lampu ini terdiri atas tabung kaca tertutup yang mengandung suatu katoda
Akibat dari tabrakan-tabrakan ini membuat unsur-unsur gas mulia akan kehilangan elektron dan menjadi ion bermuatan positif. Ion-ion gas mulia yang bermuatan positif selanjutnya akan bergerak ke katoda dengan kecepatan dan energi yang tinggi pula. Sebagaimana disebutkan di atas, pada katoda terdapat unsur-unsur yang sesuai dengan unsur yang akan dianalisis. Unsur-unsur ini akan ditabrak oleh ion-ion positif gas mulia. Akibat tabrakan ini, unsur-unsur akan terlempar keluar dari permukaan katoda. Atom-atom unsur dari katoda ini kemudian akan mengalami eksitasi ke tingkat energi-energi elektron yang lebih tinggi dan akan memancarkan spektrum pancaran dari unsur yang sama dengan unsur yang akan dianalisis (Rohman, 2007).
2. Tempat sampel
Dalam analisis dengan spektrofotometri serapan atom, sampel yang akan dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam keadaan gas. Nyala dapat digunakan untuk mengubah suatu sampel menjadi uap atom-atomnya dan juga berfungsi untuk atomisasi. Pada cara spektrofotometri emisi atom, nyala ini berfungsi untuk mengeksitasikan atom dari tingkat dasar ke tingkat yang lebih tinggi.
Suhu yang dapat dicapai oleh nyala tergantung pada gas-gas yang digunakan, misalnya untuk gas batubara-udara, suhunya kira-kira sebesar 18000C, gas alam-udara 17000C, asetilen-udara 22000Cdan gas asetilen-dinitrogen oksida (N2O) sebesar 30000C.
3. Monokromator
4. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui tempat pengatoman.Biasanya digunakan tabung penggandaan foton (photomultiplier tube). Ada dua cara yang dapat digunakan dalam sistem deteksi yaitu yang
memberikan respon terhadap radiasi resonansi dan radiasi kontinyu dan yang hanya memberikan respon terhadap radiasi resonansi (Rohman, 2007).
5. Readout
Suatu alat sebagai sistem pencatat hasil.Pencatat hasil dilakukan dengan suatu alat yang telah terkalibrasi untuk pembacaan suatu angka transmisi atau absorbsi.Hasil pembacaan dapat berupa angka atau berupa kurva dari suatu recorder yang menggambarkan absorbansi atau intensitas emisi (Rohman, 2007).
2.7 Gangguan pada SSA dan Cara Mengatasinya.
Pada penentuan nilai serapan atom seringkali didapatkan suatu harga yang tidak sesuai dengan konsentrasi unsur sampel yang ditentukan.Penyebab dari gangguan ini adalah faktor matriks sampel, faktor kimia adanya gangguan molekuler yang bersifat menyerap radiasi. Sampel dalam bentuk molekul karena disosiasi yang tidak sempurna akan cenderung mengabsorpsi radiasi dari sumber radiasi.
Ada beberapa usaha untuk mengurangi gangguan kimia pada SSA yaitu: 1. Menaikkan temperature nyala agar mempermudah penguraian, untuk itu
dipakai gas pembakar campuran C2H2 + N2O yang memberikan nyala dengan temperatur yang tinggi.
2. Menambahkan elemen pengikat gugus atau atom penyangga, sehingga terikat kuat akan tetapi atom yang ditentukan bebas sebagai atom netral. Misalnya penentuan logam yang terikat sebagai garam, dengan penambahan logam yang lainnya akan terjadi ikatan lebih kuat dengan anion pengganggu.