SINTESIS DAN KARAKTERISASI HIDROGEL CRF
(CONTROLLED RELEASE FERTILIZER) BERBASIS
KOMPOSIT PVA-ALGA MERAH-CARBON NANOTUBE
SKRIPSI
Diajukan untuk Memenuhi Sebagian dari Syarat Memperoleh Gelar Sarjana Sains Progam Studi Kimia
Oleh
OCEU DWI PUTRI 1100723
PROGRAM STUDI KIMIA DEPARTEMEN PENDIDIKAN KIMIA
FAKULTAS PENDIDIKAN MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS PENDIDIKAN INDONESIA BANDUNG
SINTESIS DAN KARAKTERISASI HIDROGEL CRF
(CONTROLLED RELEASE FERTILIZER) BERBASIS
KOMPOSIT PVA-ALGA MERAH-CARBON NANOTUBE
Oleh
Oceu Dwi Putri
Sebuah skripsi yang diajukan untuk memenuhi salah satu syarat memperoleh gelar Sarjana Sains pada Fakultas Pendidikan Matematika dan Ilmu Pengetahuan Alam
© Oceu Dwi Putri 2015 Universitas Pendidikan Indonesia
Agustus 2015
Hak Cipta dilindungi undang-undang.
OCEU DWI PUTRI
SINTESIS DAN KARAKTERISASI HIDROGEL CRF (CONTROLLED
RELEASE FERTILIZER) BERBASIS KOMPOSIT PVA-ALGA MERAH-CARBON NANOTUBE
DISETUJUI DAN DISAHKAN OLEH PEMBIMBING:
Pembimbing I
Fitri Khoerunnisa, Ph.D NIP. 197806282001122001
Pembimbing II
Dr. Hendrawan, M.Si. NIP. 196309111989011001
Mengetahui,
Ketua Departemen Pendidikan Kimia FPMIPA UPI
PERNYATAAN
Saya menyatatakan bahwa skripsi yang berjudul “Sintesis Dan Karakterisasi Hidrogel CRF (Controlled Release Fertilizer) Berbasis Komposit PVA-Alga Merah-Carbon Nanotube” ini sepenuhnya karya saya sendiri. Tidak ada bagian didalamnya yang merupakan plagiat dari karya orang lain dan saya tidak melakukan penjiplakan atau pengutipan dengan cara – cara yang tidak sesuai dengan etika keilmuan. Atas pernyataan ini, saya siap menanggung risiko/sanksi yang dijatuhkan kepada saya apabila kemudian ditemukan adanya pelanggaran terhadap etika keilmuan dalam karya saya ini, atau ada klaim dari pihak lain terhadap keaslian karya saya ini.
Bandung, Agustus 2015 Yang membuat pernyataan,
ABSTRAK
Telah dilakukan penelitian tentang sintesis dan karakterisasi hidrogel CRF (controlled release fertilizer) berbasis komposit PVA-alga merah-carbon nanotube. Penelitian ini bertujuan untuk mengetahui komposisi optimum filler carbon nanotube (CNT) pada sintesis hidrogel komposit, mengetahui karakteristik hidrogel komposit, serta mengetahui kinerja hidrogel komposit sebagai material CRF. Penelitian yang dilakukan terdiri dari tiga tahap: (1) tahap optimasi komposisi CNT dalam hidrogel komposit, (2) tahap sintesis hidrogel komposit, dan (3) tahap karakterisasi hidrogel komposit. Komposisi optimum filler CNT dalam komposit PVA-alga merah adalah 5 mL CNT (dispersi) pada rasio komposisi PVA:Alga merah:CNT = 10:10:5, dimana kemampuan swelling (%SR) dan waktu retensi air optimum hidrogel komposit mencapai 840% dan 21 hari, secara berturut-turut. Hasil karakterisasi menunjukkan hidrogel komposit merupakan material berpori, serta penyisipan CNT dan nutrien dapat meningkatkan kristalinitas dari hidrogel komposit dimana interaksi prekursor hidrogel komposit (PVA-Alga merah-CNT-nutrien) berlangsung dengan melibatkan gugus fungsi C-O, C-N, C=O, C-H sp3 dan O-H, yang dikonfimasi dengan perubahan intensitas dan pergeseran puncak untuk serapan gugus fungsi tersebut. Penyisipan nutrien dapat meningkatkan kinerja dari hidrogel komposit yang dindikasikan oleh %SR dan waktu retensi mencapai 1419% dan 21 hari, secara berturut-turut. Selain itu, hidrogel komposit dapat digunakan sebagai material hidrogel CRF dengan kategori slow released dan hidrogel komposit berpotensi biodegradable.
ABSTRACT
A research on the synthesis and characterization of CRF hydrogel composite (controlled release fertilizer) based on PVA-Red Algae-Carbon Nanotubes has been done. This study aims to determine the optimum composition of the carbon nanotube (CNT) filler on the synthesis of hydrogel composite, to determine the characteristics of hydrogel composite, and to determine the performances of hydrogel composite as a CRF material. The study was conducted in three stages: (1) the optimization of CNT composition in hydrogel composite, (2) synthesis of hydrogel composite, and (3) the characterization of hydrogel composites. The optimum composition of CNT filler in hydrogel composite is 5 mL of CNT (dispersion) with the composition ratio of PVA: red algae: CNT = 10: 10: 5, where the ability of swelling (% SR) and optimum water retention time of hydrogel composite reached 840% and 21 days, respectively. The results showed that hydrogel composite is a porous material, and the insertion of CNT and nutrients could improved the crystallinity of the hydrogel composite, wherein the hydrogel precursor interaction (PVA-red algae-CNT-nutrient) took place with the involvement of functional groups C-O, C-N, C = O, C-H sp3 and O-H, which is confirmed by the changes in absorption peak’s intensity and the shifts of the functional group. Insertion of nutrients could improve the performances of hydrogel composite which is indicated by %SR and the retention time of 1419% and 21 days, respectively. In addition, the hydrogel composite can be used as CRF material with slow released category and the hydrogel composite is potentially biodegradable.
DAFTAR ISI
BAB II TINJAUAN PUSTAKA ...6
2.1.Controlled Release Fertilizer ...6
2.2.Hidrogel...8
2.3.Bahan Dasar Hidrogel ...10
2.3.1.Polivinil Alkohol (PVA) ...10
2.3.2.Crosslinker ...10
2.3.3.Gracilaria sp. ...13
2.3.4.Carbon Nanotubes (CNT) ...17
2.3.4.1.Klasifikasi Carbon Nanotubes ...18
2.3.4.2.Sintesis Carbon Nanotubes ...20
2.3.4.2.1.Electric Arc Discharge ...20
2.3.4.2.2.Laser Ablation ...21
2.3.4.2.3.Chemical Vapour Deposition (CVD) ...22
2.4.Makro dan Mikronutrien ...23
BAB III METODE PENELITIAN...27
3.1.Waktu dan Lokasi Penelitian ...27
3.2.Alat dan Bahan ...27
3.3.Metode Penelitian...28
3.4.1 Tahap Optimasi Komposisi ...30
3.4.1.1. Pembuatan Larutan Metanol 70% ...30
3.4.1.2. Pembuatan Larutan PVA 10% ...30
3.4.1.3. Pembuatan Larutan Metanol 50% ...30
3.4.1.4. Pembuatan Larutan Asam Asetat 10% ...30
3.4.1.5. Pembuatan Larutan Asam Sulfat 10%...30
3.4.1.6. Pembuatan Glutaraldehid (GA) 1,25% ...30
3.4.1.7. Pembuatan Larutan Crosslinker dengan Perbandingan volume (3:2:1:1) ...31
3.4.1.8. Dispersi CNT dalam Larutan Grafen Oksida ...31
3.4.1.9. Pembuatan Larutan Nutrien 20 g/L ...31
3.4.1.10.Preparasi Alga Merah ...31
3.4.1.11.Pembuatan Ekstrak Alga Merah ...31
3.4.1.12.Optimasi Komposisi CNT ...31
3.4.2 Tahap Sintesis ...32
3.4.2.1. Tahap Pemasukan Nutrien ke dalam Hidrogel ...32
3.4.3 Tahap Karakterisasi ...33
3.4.3.1. Swelling Ratio ...33
3.4.3.2. Retensi Air ...33
3.4.3.3. Release Behavior ...33
3.4.3.4. Biodegradasi ...34
3.4.3.5. Karakterisasi dengan SEM ...35
3.4.3.6. Karakterisasi dengan FTIR ...35
3.4.3.7. Karakterisasi dengan XRD ...35
BAB IV HASIL PENELITIAN DAN PEMBAHASAN ...37
4.1.Kondisi Optimum Sintesis Hidrogel Komposit ...37
4.2.Sintesis Hidrogel Komposit ...42
4.2.1.Karakterisasi Struktur dan Morfologi Hidrogel, Hidrogel Komposit dan Hidrogel Komposit-nutrien ...42
4.2.1.1.Karakterisasi FTIR ...43
4.2.1.2.Karakterisasi SEM ...45
4.2.1.3.Karakterisasi XRD ...47
4.2.2.Uji Kinerja Hidrogel Komposit dan Hidrogel Komposit-nutrien ..49
4.2.2.1. Uji Rasio Swelling ...49
4.2.2.2. Uji Retensi Air ...50
4.2.2.3.Release Behavior ...51
BAB V KESIMPULAN DAN SARAN ...54
5.1Kesimpulan ...54
5.2Saran ...54
DAFTAR PUSTAKA ...56
DAFTAR TABEL
Tabel
2.1. Sisi aktif Agen Crosslinking dan Gugus Fungsi yang Diserangnya ...11
2.2 Komposisi Kimia Alga Merah ...15
2.3 Sifat Mekanik Nanotubes ...18
2.4 Nutrien Essensial Tumbuhan ...23
2.5 Gejala Umum Defisiensi Makronutrien, Kemungkinan Penyebabnya serta Metode untuk Memperbaikinya ...24
2.6 Gejala Umum Defisiensi Mikronutrien, Kemungkinan Penyebabnya serta Metode untuk Memperbaikinya ...25
3.1. Perbandingan Volume PVA, Ekstrak Alga Merah, Crosslinker dan CNT ...32
4.1. Hasil Karakterisasi XRD Hidrogel, Hidrogel Komposit dan Hidrogel Komposit-nutrien ...49
DAFTAR GAMBAR
Gambar
2.1. Skema Rilis Pupuk Berbasis Hidrogel ... 8
2.2. Struktur Glutaraldehid ... 12
2.3. Reaksi Asetalisasi Glutaraldehid dan PVA... 13
2.4. Struktur Agarosa dan Agaropektin ... 16
2.5. Single walled Carbon Nanotubes... 19
2.6. Struktur MWCNT dan SWCNT dari Grafen yang Digulung ... 20
2.7. Skema alat arc-discharge untuk Produksi Fullrene dan Nanotubes ... 21
2.8. Skema alat Laser Ablation ... 22
2.9. Skema alat sintesis CNT dengan CVD menggunakan Katalis ... 23
3.1. Diagram Alir Penelitian ... 29
4.1. Hidrogel hasil Pencetakan: (a) bentuk tablet, (b) bentuk lembaran ... 37
4.2. Rasio swelling maksimum Hidrogel Komposit per hari: (a) bentuk tablet, (b) bentuk lembaran ... 38
4.3. Retensi air hidrogel tablet ... 40
4.4. Retensi air hidrogel lembaran ... 41
4.5. Spektra FTIR hidrogel, hidrogel komposit dan hidrogel komposit-nutrien ... 43
4.6. Foto SEM hidrogel, hidrogel komposit dan hidrogel komposit-nutrien ... 46
4.7. Difraktogram X-ray hidrogel, hidrogel komposit dan hidrogel komposit-nutrien ... 48
4.8. Rasio swelling hidrogel, hidrogel komposit dan hidrogel komposit-nutrien ... 49
4.9. Retensi air hidrogel, hidrogel komposit dan hidrogel komposit-nutrien ... 51
DAFTAR LAMPIRAN
1 Data Perhitungan ... 61
2 Tabel Swelling Ratio Tahap Optimasi Komposisi CNT Hidrogel Komposit Bentuk Lembaran... 64
3 Tabel Swelling Ratio Tahap Optimasi Komposisi CNT Hidrogel Komposit Bentuk Tablet... 65
4 Tabel Water Retention Tahap Optimasi Komposisi CNT Hidrogel Komposit Bentuk Lembaran ... 66
5 Tabel Water Retention Tahap Optimasi Komposisi CNT Hidrogel Komposit Bentuk Lembaran ... 67
6 Spektra FTIR Hidrogel Komposit-Nutrien ... 68
7 Spektra FTIR Hidrogel Komposit ... 69
8 Spektra FTIR Hidrogel ... 70
9 Karakterisasi Morfologi Hidrogel Menggunakan SEM ... 71
10 Karakterisasi Morfologi Hidrogel Komposit Menggunakan SEM ... 72
11 Karakterisasi Morfologi Hidrogel Komposit-Nutrien Menggunakan SEM ... 73
12 Difraktogram Hidrogel ... 74
1 3 Difraktogram Hidrogel Komposit ... 75
14 Difraktogram Hidrogel Komposit-Nutrien ... 76
15 Tabel Swelling Ratio Hidrogel, Hidrogel Komposit, Hidrogel Komposit-Nutrien ... 77
16 Tabel Water Retention Hidrogel, Hidrogel Komposit, Hidrogel Komposit-Nutrien ... 78
BAB I
PENDAHULUAN
1.1. Latar Belakang
Kebutuhan pangan yang semakin meningkat memicu peningkatan penggunaan
pupuk untuk pertanian setiap tahunnya. Menurut perkiraan Departemen Pertanian,
kebutuhan pupuk NPK di Indonesia tahun 2006 hingga 2015 mengalami
peningkatan yaitu dari 400.000 ton/tahun pada 2006 menjadi 6.589.227 ton/tahun
pada 2015 (APPI, 2009). Namun kegiatan pemupukan yang semakin meningkat
ini memiliki banyak dampak terhadap kualitas lingkungan di sekitar areal
pertanian. Ketika pupuk yang diberikan berlebih maka akan terjadi nutrient losses
karena kapasitas tanaman untuk menyerap nutrien terbatas, selain itu juga karena
adanya pencucian akibat run off oleh air hujan dan kelembaban tanah (Liu et al,
2014). Jika dilakukan secara berlebihan, penggunaan pupuk ini justru akan
merusak tanah karena sisa-sisa pupuk yang tidak terserap oleh tanaman akan
menurunkan pH tanah dan menyebabkan degradasi kualitas tanah.
Selain merusak tanah, penggunaan pupuk yang berlebihan juga dapat
berdampak pada lingkungan perairan di sekitar lahan pertanian tersebut.
Kandungan nitrat dan fosfat dalam pupuk/nutrien yang tidak terserap oleh
tanaman ini akan terbawa oleh air hujan maupun irigasi ke perairan sehingga akan
meningkatkan pertumbuhan yang berlebihan dari ganggang di air (Harfiana et al,
2013). Meledaknya populasi ganggang (eutrofikasi) akan menurunkan kadar
oksigen dalam perairan karena oksigen yang ada akan habis dikonsumsi oleh
ganggang tersebut. Jika kadar oksigen di air berkurang, maka fauna yang ada di
perairan pun akan kekurangan oksigen dan akhirnya mati.
Selain berpengaruh pada lingkungan perairan dan tanah, penggunaan pupuk
yang berlebihan juga berdampak pada atmosfer bumi. Sebagai hasil dari proses
denitrifikasi yang terjadi di tanah, baik nitrogen oksida dan oksida nitrat yang
terbentuk akan menyebabkan penipisan lapisan ozon yang mengakibatkan paparan
2
Salah satu alternatif untuk mengatasi permasalahan di atas adalah dengan
menggunakan suatu material yang dapat mengontrol laju pelepasan pupuk atau
nutrien yaitu controlled release fertilizer (CRF). Pada pemupukan konvensional
(misalnya dengan urea) pemupukan dilakukan 2-3 kali selama siklus pertumbuhan
tanaman, sedangkan dengan CRF nutrisi dilepas bertahap selama masa tanam dan
hanya perlu diterapkan sekali saja sehingga dapat menghemat waktu dan energi
(Lubkowski dan Grzmil, 2007). CRF juga menunjukkan banyak keunggulan
dibandingkan pupuk konvensional, seperti penurunan tingkat kehilangan pupuk
dari tanah oleh hujan atau air irigasi, menjaga ketersediaan air atau mineral untuk
waktu yang lama, meningkatkan efisiensi pupuk, pengaplikasian dengan frekuensi
yang lebih sedikit sesuai dengan kebutuhan tanaman normal, mengurangi dampak
negatif potensial yang terkait dengan over dosis dan mengurangi toksisitas (Han et
al, 2009).
Salah satu material yang sering digunakan untuk CRF adalah hidrogel.
Hidrogel berbentuk jaringan tiga dimensi, mempunyai kemampuan mengembang
(swelling) dan menciut (deswelling) dalam air. Hidrogel bersifat tidak larut dalam
air tetapi hanya menyerap dan akan melepaskan air dan nutrien secara
proporsional pada saat dibutuhkan oleh tanaman. Dengan demikian tanaman akan
selalu mempunyai persediaan air dan nutrien setiap saat. Oleh karena itu, hidrogel
berpotensi digunakan sebagai material CRF. Pada dasarnya, hidrogel memiliki
kekuatan mekanik yang rendah karena umumnya bahan dasar pembuatan hidrogel
adalah polimer/monomer. Untuk memperkuat strukturnya, hidrogel diikat silang
(crosslink) oleh agen-agen pengikatnya. Beberapa senyawa kimia yang digunakan
sebagai agen pengikat silang adalah senyawa epoksi dan aldehida (glutaraldehid),
senyawa yang memiliki dua atau lebih gugus fungsi seperti
1,6-heksametilendiisosianat, divinilsulfon, N,N-(3-dimetilaminopropil)-N-etil
karbodiimida (EDC) dan N,N’-metilenbisakrilamida (MBA) (Hennik dan Van
Nostrum, 2012; Kurnia, 2014; Sicilia et al, 2013).
Hidrogel berbahan polimer sintetis telah banyak dikembangkan, seperti
polietilen oksida (PEO), polivinil pirolidon (PVP), asam polilaktat (PLA), asam
3
sintetis ini memiliki beberapa kekurangan diantaranya tidak ramah lingkungan
karena sifatnya yang tidak biodegradable serta tidak ekonomis. Namun saat ini
mulai banyak dikembangkan sintesis hidrogel menggunakan polimer alam. Bahan
polimer alam memiliki banyak keunggulan dibanding bahan sintetis dimana
kebanyakan bahan alam bersifat biodegradable, ketersediaannya melimpah,
bernilai ekonomis, dan berkontribusi positif pada konservasi alam. Salah satu
bahan alam yang dapat dimanfaatkan adalah alga merah. Alga merah banyak
mengandung polisakarida dan protein. Alga merah memiliki struktur tiga dimensi,
dapat mengembang, menyusut dan membentuk gel. Hal ini sesuai dengan syarat
pembentukan hidrogel sehingga alga merah dapat digunakan sebagai bahan baku
alternatif yang dapat digunakan untuk membuat hidrogel (Chotimah, 2013). Pada
penelitian sebelumnya, hidrogel berbahan dasar alga merah yang dikompositkan
dengan polimer lain seperti polivinil alkohol (PVA) telah disintesis. PVA
digunakan karena memenuhi karakteristik yang baik sebagai bahan dasar hidrogel
(biokompatibilitas dan hidrofilisitasnya tinggi serta kemudahannya membentuk
gel), namun hidrogel berbahan polimer alam ini memiliki kekuatan mekaniknya
yang rendah. Kelemahan ini dapat diatasi dengan suatu material yang memiliki
kekuatan mekanik yang tinggi, salah satunya adalah carbon nanotube.
Carbon nanotubes (CNT) adalah suatu material yang berasal dari susunan
atom karbon yang berhibridisasi sp2 dan berikatan satu sama lain secara
heksagonal membentuk struktur sarang madu (honeycomb) yang tergulung
membentuk suatu silinder berukuran nanometer (Meyyappan, 2005). Penelitian
mengenai aplikasi CNT telah dilakukan selama lebih dari sepuluh tahun karena
sifat unik mekanik dan listriknya. CNT memiliki sifat intrinsik yang sangat baik
dan dapat digunakan sebagai pengisi/filler potensial dalam pembuatan membran
nanokomposit (Shirazi et al., 2011). Tong et al (2007) mengemukakan bahwa
sifat mekanis dan swelling hidrogel hibrida (komposit) yang disisipi CNT lebih
baik daripada hidrogel PVA yang tidak disisipi CNT. Tidak seperti komposit
polimer tradisional yang mengandung filler/pengisi skala mikron, penggabungan
CNT (filler skala nano) ke dalam sistem polimer menghasilkan jarak yang sangat
pendek antar filler, sehingga sifat komposit sebagian besar berubah bahkan pada
4
yang pernah ada (aspek rasio, diameter : panjang = 1 : 100.000.000). Sifat
mekanik yang sangat baik ini jika dikombinasikan dengan sifat fisik lainnya akan
menghasilkan nanokomposit CNT/polimer potensial. Selain itu, nanokomposit
CNT/polimer adalah salah satu sistem yang paling banyak dikembangkan karena
sistem komposit ini secara teknis mudah dibuat dan efisien secara ekonomis (Ma
et al., 2010).
Dalam penelitian ini, CNT disisipkan ke dalam matriks polimer campuran
PVA dengan ekstrak alga merah dengan pengikat silang (crosslinker)
glutaraldehid. Berdasarkan deskripsi di atas, pada penelitian ini akan disintesis
hidrogel komposit berbahan dasar PVA-alga merah-CNT dan kemudian dilakukan
karakterisasi dan pengujian kinerjanya.
1.2. Rumusan Masalah
Berdasarkan latar belakang di atas, maka rumusan masalah dalam penelitian
ini dapat diuraikan sebagai berikut:
1. Bagaimana komposisi optimum filler CNT dalam komposit PVA-alga
merah serta metode pencetakan terbaik pada sintesis hidrogel komposit?
2. Bagaimana karakteristik hidrogel komposit PVA-alga merah-CNT?
3. Bagaimana kinerja hidrogel komposit PVA-alga merah-CNT sebagai
material CRF?
1.3. Tujuan Penelitian
Tujuan dalam penelitian ini adalah sebagai berikut:
1. Mengetahui komposisi optimum filler CNT dalam komposit PVA-alga
merah serta metode pencetakan terbaik pada sintesis hidrogel komposit.
2. Mengetahui karakteristik hidrogel komposit PVA-alga merah-CNT.
3. Serta mengetahui kinerja hidrogel komposit PVA-alga merah-CNT sebagai
5
1.4. Manfaat Penelitian
Hasil dari penelitian ini diharapkan dapat memberikan manfaat sebagai:
1. Material alternatif bagi pengembangan teknologi dan praktek pertanian di
Indonesia terutama dalam meningkatkan efisiensi dan efektivitas
pemupukan.
2. Teknologi alternatif dalam pengolahan limbah alga merah sehingga dapat
meningkatkan nilai guna dan nilai ekonomisnya serta dapat mengatasi
BAB III
METODE PENELITIAN
3.1Waktu dan Lokasi Penelitian
Tahapan pada penelitian ini terdiri dari optimasi komposisi, sintesis dan
karakterisasi. Tahap optimasi komposisi, sintesis dan karakterisasi hidrogel
komposit yaitu uji kinerja dilakukan di Laboratorium Riset Kimia Lingkungan
FPMIPA UPI Bandung. Tahap karakterisasi hidrogel komposit dilakukan di
beberapa laboratorium sebagai berikut: (1) Laboratorium Karakterisasi
Jurusan Fisika UIN Sunan Gunung Djati Bandung untuk karakterisasi dengan
SEM, (2) Laboratorium Karakterisasi Metalurgi Departemen Pertambangan
ITB Bandung untuk karakterisasi dengan XRD, dan (3) Research Centre for
Energy and Environmental Science, Shinshu University, Jepang untuk
karakterisasi dengan FTIR. Waktu penelitian dimulai pada bulan September
2014 sampai Juli 2015.
3.2Alat dan Bahan
Bahan yang digunakan adalah alga merah kering, polivinil alkohol p.a
(merck), glutaraldehida 25% p.a (merck), metanol, asam sulfat, asam asetat
p.a (Merck), grafen oksida Madagascar, multiwall carbon nanotube
fungsionalized, pupuk NPK Mutiara, tanah, dan aquades.
Sedangkan alat yang digunakan adalah alat gelas standar dan
instrumentasi. Alat gelas standar meliputi gelas kimia 400 mL dan 100 mL,
gelas ukur 100 mL, 50 mL, 25 mL dan 10 mL, labu ukur 250 mL dan 100 mL,
kaca arloji, spatula, pipet tetes, mikropipet ukuran 2 mL, 5 mL dan 10 mL,
batang pengaduk, corong buchner, labu erlenmeyer vakum 250 mL.
Instrumentasi yang digunakan meliputi spektrofotometer Fourier Transform
Infra Red (FTIR), Scanning Electron Spectroscopy (SEM), X-Ray Diffraction
28
3.3Metode Penelitian
Penelitian ini dilakukan dengan berbagai tahap yaitu tahap optimasi
komposisi, sintesis dan karakterisasi. Tahap optimasi komposisi meliputi
penentuan kondisi optimum komponen penyusun hidrogel disiapkan dengan
berbagai variasi komposisi CNT dengan dua metode pencetakan hidrogel
yaitu dalam bentuk tablet dan lembaran. Tahap ini dilakukan untuk
mendapatkan hidrogel dengan sifat mekanik dan kinerja sebagai CRF meliputi
uji swelling dan retensi air yang optimum. Komposisi hidrogel dengan kinerja
optimum digunakan untuk mensintesis kembali hidrogel untuk kemudian
disisipkan larutan nutrien. Hidrogel hasil sintesis kemudian dikarakterisasi
melalui uji kinerja swelling rasio, retensi air, release behavior, dan
biodegradasi serta karakterisasi morfologi dan struktural dengan
29
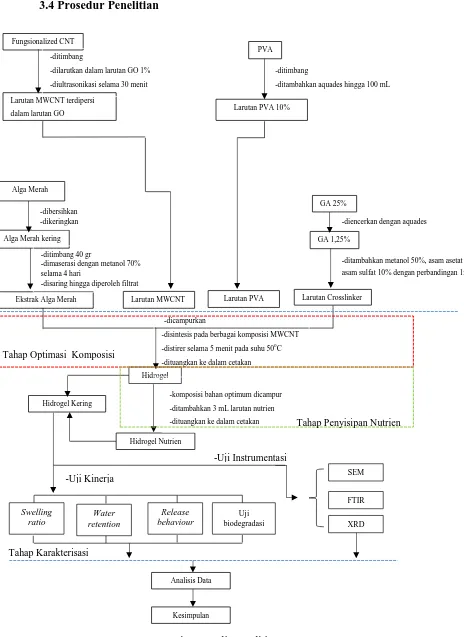
-dilarutkan dalam larutan GO 1% -diultrasonikasi selama 30 menit
-dimaserasi dengan metanol 70% selama 4 hari
-disaring hingga diperoleh filtrat
PVA
Larutan PVA 10% -ditimbang
-ditambahkan aquades hingga 100 mL
GA 25%
GA 1,25%
Larutan Crosslinker
-diencerkan dengan aquades
-ditambahkan metanol 50%, asam asetat 10%, asam sulfat 10% dengan perbandingan 1:3:2:1
Larutan MWCNT
-dicampurkan
Larutan PVA
Hidrogel
-disintesis pada berbagai komposisi MWCNT -distirer selama 5 menit pada suhu 500C -dituangkan ke dalam cetakan
Hidrogel Nutrien Hidrogel Kering
30
3.4.1 Tahap Optimasi Komposisi
3.4.1.1Pembuatan Larutan Metanol 70%
Larutan metanol 96% dipipet sebanyak 182,3 mL, kemudian
dimasukkan ke dalam labu ukur 250 mL dan ditambahkan aquades sampai
tanda batas kemudian dihomogenkan.
3.4.1.2Pembuatan Larutan PVA 10%
PVA ditimbang sebanyak 10 gram, kemudian dilarutkan ke dalam
100 mL aquades, distirer dan dipanaskan pada suhu 900C selama ± 3 jam
hingga larut.
3.4.1.3Pembuatan Larutan Metanol 50%
Larutan metanol 96% dipipet sebanyak 52,08 mL, kemudian
dimasukkan ke dalam labu ukur 100 mL dan ditambahkan aquades sampai
tanda batas kemudian dihomogenkan.
3.4.1.4Pembuatan Larutan Asam Asetat 10%
Larutan asam asetat glasial dipipet sebanyak 10,20 mL, kemudian
dimasukkan ke dalam labu ukur 100 mL dan ditambahkan aquades sampai
tanda batas kemudian dihomogenkan.
3.4.1.5Pembuatan Larutan Asam Sulfat 10%
Larutan asam sulfat 97% dipipet sebanyak 10,31 mL, kemudian
dimasukkan ke dalam labu ukur 100 mL dan ditambahkan aquades sampai
tanda batas kemudian dihomogenkan.
3.4.1.6Pembuatan Larutan Glutaraldehida 1,25%
Larutan glutaraldehida 25% dipipet sebanyak 5 mL, kemudian
dimasukkan ke dalam labu ukur 100 mL dan ditambahkan aquades sampai
31
3.4.1.7Pembuatan Larutan Crosslinker Dengan Perbandingan 3:2:1:1
Larutan metanol 50% ditambahkan larutan asam asetat 10%, larutan
asam sulfat 10% dan larutan glutaraldehida 1,25% dengan perbandingan
3:2:1:1, kemudian campuran diaduk hingga homogen.
3.4.1.8Dispersi CNT dalam Larutan Grafen Oksida
Grafen oksida (GO) koloid ditimbang sebanyak 1 gram dan
dilarutkan ke dalam 100 mL aquades (1% w/v) kemudian diaduk. CNT
ditimbang sebanyak 1 mg kemudian dimasukkan ke dalam larutan GO 1%
dan diultrasonikasi selama 30 menit.
3.4.1.9Pembuatan Larutan Nutrien 20 g/L
Pupuk NPK mutiara dengan perbandingan 16:16:16 ditimbang
sebanyak 2 gram kemudian dilarutkan ke dalam 100 mL aquades.
3.4.1.10 Preparasi Alga Merah
Alga merah diperoleh dari daerah pantai di Garut, Jawa Barat. Alga
merah dicuci terlebih dahulu dengan air untuk menghilangkan pasir, garam
dan mikroorganisme yang menempel pada alga merah. Alga merah yang
telah dicuci kemudian dikeringkan di udara terbuka tanpaterkena sinar
matahari langsung selama beberapa minggu. Alga merah yang telah kering
kemudian diblender hingga halus dan diayak menggunakan ayakan 100
mesh.
3.4.1.11Pembuatan Ekstrak Alga Merah
Alga merah yang telah halus ditimbang sebanyak 40 gram dan
dimasukkan ke dalam gelas kimia. Kemudian dimaserasi dengan 200 mL
larutan metanol 70% selama 4 hari. Setelah 4 hari, larutan disaring hingga
diperoleh ekstrak alga merah.
3.4.1.12. Optimasi Komposisi CNT
32
mengetahui komposisi optimum dari filler CNT dalam hidrogel dimana
variabel tetap dalam tahap optimasi ini adalah volume PVA, volume ekstrak
alga merah, volume crosslinker, serta suhu dan waktu pemanasan yaitu pada
suhu 500C selama 5 menit (kondisi optimum masing-masing variabel tetap
mengikuti hasil penelitian Chotimah, 2013).
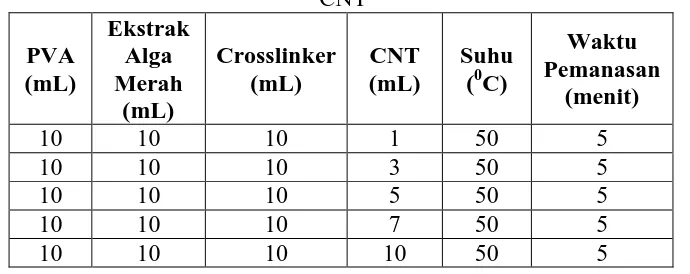
Larutan PVA 10% ditambahkan ekstrak alga merah, larutan
crosslinker dan larutan CNT dengan perbandingan masing-masing seperti
pada tabel di bawah. Kemudian diaduk selama 5 menit dengan menggunakan
magnetic stirer hingga homogen dengan bantuan pemanasan pada suhu
500C. Kemudian dituangkan ke dalam cetakan berbentuk tablet dan cetakan
bar coating plate dan dibiarkan mengering selama ± 5 hari.
Tabel 3.1 Perbandingan volume PVA, ekstrak alga merah, crosslinker dan
CNT
3.4.2.1. Tahap Pemasukan Nutrien ke dalam Hidrogel
Hidrogel dengan komposisi optimum kemudian disisipkan larutan
nutrien. Metode penyisipan yang dilakukan yaitu larutan nutrien dicampurkan
bersamaan dengan bahan pembuat hidrogel CRF pada saat sintesis hidrogel (in
situ). Nutrien disisipkan dengan perbandingan PVA:ekstrak alga merah:crosslinker:CNT:nutrien yaitu 10:10:10:5:3 sesuai dengan penelitian
sebelumnya (Chotimah, 2013; Koswara, 2006). Makronutrien yang disisipkan
adalah pupuk NPK dengan konsentrasi 20 g/L. Selanjutnya hidrogel plus nutrien
33
3.4.3. Tahap Karakterisasi
3.4.3.1.Swelling Rasio
Pengujian swelling rasio dilakukan dengan metode gravimetri.
Swelling rasio diperlukan untuk mengetahui tingkat elastisitas hidrogel.
Hidrogel kering ditimbang (Wd) lalu direndam dalam 25 mL aquades dalam
gelas kimia 100 mL. Setiap 10 menit, hidrogel diangkat dan permukaannya
dikeringkan dengan menggunakan tissue. Kemudian hidrogel tersebut
ditimbang kembali berdasarkan waktu yang telah ditentukan yaitu setiap satu
hari sampai sepuluh hari setelah perendaman pertama. Berat hidrogel setelah
dilakukan perendaman dilambangkan dengan Ws. Rasio swelling (SR) pada
hidrogel CRF dipelajari dengan menggunakan persamaan berikut.
% =� −�� � % (3.1)
3.4.3.2.Retensi Air
Faktor retensi air dalam hidrogel berfungsi untuk mempertahankan
kelembaban dan kandungan nutrisi dalam tanah pertanian. Untuk mempelajari
retensi air tanah yang mengandung hidrogel CRF, sampel hidrogel CRF
kering dibenamkan di dalam 40 g tanah kering yang ditempatkan dalam gelas.
Sejumlah 40 g tanah kering lain tanpa hidrogel CRF ditempatkan dalam gelas
lain, kemudian setiap gelas ditimbang (W). Setelah itu, air suling sebanyak
25mL ditambahkan ke dalam kedua gelas dan ditimbang kembali (Wo). Gelas
tersebut disimpan pada kondisi suhu kamar yang sama dan ditimbang setiap
hari (Wt) sampai berat tanah kembali seperti sebelum ditambahkan air suling.
Retensi air (%WR) dari tanah kemudian dihitung dengan persamaan sebagai
berikut.
%� =� −���−� � (3.2)
3.4.3.3.Release Behaviour
34
serapan/absorpsi cahaya ultra violet (uv) atau visible (vis) oleh atom-atom
suatu unsur dalam keadaan dasar yang berada di dalam nyala api. Cahaya UV
atau vis yang diserap berasal dari energi yang diemisikan oleh sumber energi
tertentu.
Besarnya cahaya yang diserap oleh suatu atom dalam keadaan dasar
sebanding dengan konsentrasinya. Hal ini berdasarkan Hukum
Lambert-Beer yang secara sederhana dirumuskan sebagai berikut :
A = a b C (3.3)
ditentukan (Wiji et al, 2012).
Penentuan konsentrasi desorbsi nutrien pada hidrogel dilakukan dengan
menggunakan metode AAS untuk mengetahui perubahan konsentrasi pada
hidrogel setelah pelepasan nutrien dengan cara kurva kalibrasi. Hidrogel yang
telah disisipi nutrien dipotong-potong dengan ukuran 2 cm x 2 cm direndam
dalam masing-masing 25 mL aquades selama beberapa variasi waktu yaitu
selama 1, 2, 3, 4, 5, 6 dan 7 hari, kemudian diangkat dan ditiriskan.
Konsentrasi logam kalium pada nutrien yang terdesorpsi dalam aquades hasil
rendaman tersebut di uji menggunakan instrumentasi AAS dengan panjang
gelombang 766,5 nm, energi 68%, int.time 0,7 detik, dan dilakukan secara
triplo.
3.4.3.4.Biodegradasi
Hidrogel dipotong dengan ukuran 1 cm x 1 cm, setiap spesi yang telah
ditimbang ditempatkan pada tanah pertanian yang ada didalam sebuah gelas.
Gelas tersebut dibiarkan selama 30 hari dalam kondisi ambient. Variasi
35
3.4.3.5.Karakterisasi dengan SEM
Pengujian ini bertujuan untuk mengetahui penampang muka dan
penampang melintang hidrogel serta untuk mengetahui ukuran pori hidrogel.
Sebelum diuji, hidrogel terlebih dahulu dikeringkan dan kemudian dihaluskan.
Setelah itu, sampel ditempatkan pada wadah sampel kemudian diuji bentuk
morfologinya menggunakan alat SEM JCM-6000 NeoScope Benchtop.
3.4.3.6.Karakterisasi dengan FTIR
Pengujian ini bertujuan untuk menentukan gugus fungsi pada hidrogel.
Alat yang digunakan adalah Thermo Scientific Nicolet 6700, diujikan tiga
sampel yaitu hidrogel, hidrogel komposit dan hidrogel komposit-nutrien.
Sampel dihaluskan kemudian dipadatkan dan dianalisis dalam bentuk pelet
KBr. Spektrum direkam dalam daerah bilangan gelombang dari 4000 cm-1
sampai 500 cm-1. Kemudian hasil spektrum yang diperoleh dibandingkan satu
sama lain untuk melihat pengaruh nutrien dalam pembentukan gugus fungsi
pada hidrogel.
3.4.3.7.Karakterisasi dengan XRD
Untuk menentukan kristalinitas yang terbentuk pada hidrogel CRF
digunakan instrumentasi XRD dengan spesifikasi alat Philips Analytical
PW1710 BASED dan energi yang digunakan 40 kV/30 mA dengan sumber
x-ray CuKα. Sebelum diuji, hidrogel terlebih dahulu dikeringkan dan kemudian
dihaluskan. Setelah itu, sampel ditempatkan pada wadah sampel kemudian
diuji kristalinitasnya dan diperoleh difraktogram dari sampel. Jarak interlayer
dan kristalinitas sampel dapat ditentukan dengan analisis menggunaakan
persamaan Bragg dan Scherrer.
36
Dimana d adalah jarak interlayer, � adalah panjang gelombang, n adalah orde
difraksi dan � adalah sudut difraksi.
Persamaan Scherrer:
� =
� � ��� (3.5)BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan penelitian yang telah dilakukan, dapat ditarik beberapa
kesimpulan sebagai berikut :
1.
Komposisi optimum filler CNT dalam komposit PVA-alga merah adalah 5mL CNT (dispersi) pada rasio komposisi PVA:Alga merah:CNT = 10:10:5,
dimana kemampuan swelling (%SR) dan waktu retensi air optimum hidrogel
komposit mencapai 840% dan 21 hari, secara berturut-turut, dengan metode
pencetakan dalam bentuk lembaran.
2. Karakterisasi XRD menunjukkan bahwa hidrogel komposit-nutrien memiliki
kristalinitas yang lebih tinggi dibandingkan dengan hidrogel komposit.
Karakterisasi FTIR menyatakan bahwa interaksi prekursor hidrogel/hidrogel
komposit (PVA-Alga merah-CNT-nutrien) berlangsung dengan melibatkan
gugus fungsi C-O, C-N, C=O, C-H sp3 dan O-H, yang dikonfimasi dengan
perubahan intensitas dan pergeseran puncak untuk serapan gugus fungsi
tersebut. Sedangkan karakterisasi SEM mengkonfirmasi bahwa pada hidrogel
komposit merupakan material berpori.
3. Penyisipan nutrien dapat meningkatkan kinerja dari hidrogel komposit
PVA-Alga merah-CNT dengan %SR mencapai 1419% dan waktu retensi selama 21
hari. Uji release behavior menunjukkan bahwa hidrogel komposit-nutrien
dapat digunakan sebagai material hidrogel CRF dengan kategori slow release.
Sedangkan uji kemampuan biodegradasi mengindikasikan hidrogel komposit
dapat bersifat biodegradable.
5.2 Saran
Dari penelitian yang telah dilakukan terdapat beberapa kekurangan yang
dapat diperbaiki dalam penelitian selanjutnya, diantaranya :
1. Diperlukan metode dispersi CNT yang lebih baik agar CNT dapat
2. Sebaiknya dilakukan pengontrolan thickness dari hidrogel komposit agar
tidak terjadi blocking saat pengambilan gambar SEM.
3. Porositas dari hidrogel komposit sebaiknya diuji dengan porosimetri agar
informasi mengenai ukuran pori lebih akurat.
4. Sebaiknya dilakukan uji mekanik agar kekuatan mekanik dari hidrogel
komposit dapat diketahui.
5. Uji biodegradasi sebaiknya dilakukan melalui uji dengan bakteri untuk
memastikan bahwa pengurangan massa hidrogel komposit disebabkan oleh
degradasi biologis.
6. Sebaiknya konsentrasi N dan P pada uji release behavior juga diukur untuk