KIMIA INTI DAN RADIOKIMIA
Stabilitas Nuklir dan Peluruhan Radioaktif
Oleh :
Arif Novan 12030234001/KA12
Fitria Dewi N. 12030234226/KA12 Wijo Kongko K. Y. S. 12030234018/KB12 Ruwanti Dewi C. N. 12030234216/KB12
UNIVERSITAS NEGERI SURABAYA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM JURUSAN KIMIA
KIMIA NUKLIR
A. Stabilitas Nuklir dan Peluruhan Radioaktif
Radioaktivitas adalah proses peluruhan inti atom, yang menghasilkan radiasi energi tinggi. Tiga jenis radiasi nuklir yang umum diantaranya radiasi alfa (α), beta (β), dan gamma ( ). Partikel alfa adalah inti helium ( ), partikel beta adalah elektron-elektron nuklir, dan radiasi gamma adalah radiasi elektromagnetik energi tinggi dengan panjang gelombang yang sangat pendek dan frekuensi tinggi ( ~ 10-13 m; ~ 1021
s-1).
Nuklida merujuk pada inti atom dengan jumlah proton dan neutron tertentu, kedua partikel tersebut disebut sebagai nukleon. Nuklida diidentifikasi oleh nomor atom (Z) dan nomor massa (A): ZAX. Inti yang tidak stabil disebut nuklida radioaktif.
Bahan radioaktif pertama kali ditemukan oleh Antoine-Henri Becquerel pada tahun 1896 ketika ia menemukan bahwa mineral yang mengandung uranium yang dibungkus dengan kertas dan disimpan bersama-sama dalam gelap dengan beberapa kertas fotografi menyebabkan isi tersebut terkena cahaya. Dia juga menemukan bahwa radiasi dari zat radioaktif menyebabkan ionisasi molekul udara. Kemudian, zat radioaktif ditemukan oleh Marie Curie. Dia juga menetapkan bahwa intensitas radiasi berbanding lurus dengan konsentrasi zat, namun tidak untuk sifat senyawa alam di mana unsur terbentuk. Curie juga menunjukkan bahwa peluruhan radioaktif tidak berpengaruh terhadap suhu, tekanan, atau kondisi fisik dan kimia lainnya.
a. Persamaan untuk Reaksi Nuklir
Peluruhan radioaktif selalu menghasilkan perubahan nomor atom dan seringkali pada nomor massa atom. Misalnya,
238
92U 90 234
Th + 42α
Dalam reaksi nuklir jumlah nukleon (neutron dan proton) adalah kekal - nomor massa dan nomor atom harus sama pada kedua sisi persamaan.
238 92U 90 234 Th + 42α Nomor massa : 238 234 + 4 Nomor atom : 92 90 + 2
b. Stabilitas Nuklir dan Bentuk Peluruhan
Dalam inti, proton dan neutron terikat bersama oleh energi ikat nuklir yang sangat kuat, yang hanya efektif selama jarak yang sangat pendek (dalam ~ 10-15 m). Kedua partikel nuklir tersebut juga muncul dalam serangkaian kulit energi yang terkuantisasi, disamakan pada kulit elektronik dalam atom. Bilangan ajaib tertentu ada untuk kedua proton dan neutron, seperti pada elektron. Artinya, inti yang memiliki nomor proton dan neutron tertentu sangat stabil. Mereka diasumsikan menjadi jumlah angka kulit nuklir yang terisi. Bilangan ajaib tersebut disamakan, tetapi tidak harus sama dengan jumlah elektron pada kulit elektronik yang memberikan gas mulia stabilitas khusus.
1) Bilangan ajaib untuk elektron: 2, 10, 18, 36, 54, dan 86; 2) Bilangan ajaib untuk proton: 2, 8, 20, 28, 40, 50, dan 82; 3) Bilangan ajaib untuk neutron: 2, 8, 20, 40, 50, 82, dan 126.
Bukti untuk mendukung model kulit nuklir dan bilangan ajaib adalah:
a. Banyak peluruhan radioisotop oleh radiasi alfa. Partikel alfa memiliki 2 bilangan ajaib untuk proton dan neutron, yang memberinya kestabilan khusus.
b. Hasil akhir pada peluruhan radioaktif alami menunjukkan keberadaan bilangan ajaib. Misalnya, hasil akhir peluruhan U-238 adalah Pb-206, yang memiliki bilangan ajaib 82 untuk proton. Peluruhan beruntun radioisotop berat lainnya menghasilkan Pb-207 atau Pb-208, yang terakhir juga memiliki bilangan ajaib 126 untuk neutron.
c. Pemasangan tampaknya terjadi antara proton dan neutron, seperti yang terjadi pada elektron. Pasangan seperti proton dan neutron sepertinya terkait
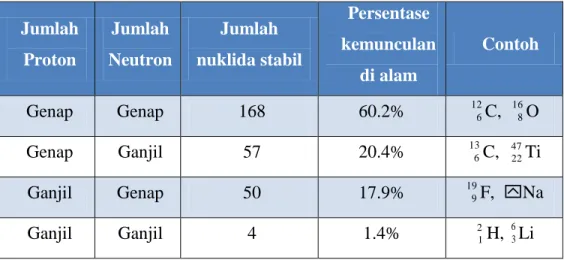
dengan stabilitas nuklir. Misalnya, persentase alami isotop stabil yang muncul secara alami dengan jumlah proton dan neutron yang genap lebih tinggi dibandingkan dengan jumlah proton dan atau neutron yang ganjil.
Tabel 1 Jumlah Isotop Stabil dengan Nomor Genap dan Ganjil Proton dan Neutron Jumlah Proton Jumlah Neutron Jumlah nuklida stabil Persentase kemunculan di alam Contoh Genap Genap 168 60.2% 126C, 168O Genap Ganjil 57 20.4% 136C, 4722Ti
Ganjil Genap 50 17.9% 199F, Na
Ganjil Ganjil 4 1.4% 21H, 63Li
c. Pita Kestabilan dan Jenis Peluruhan Radioaktif
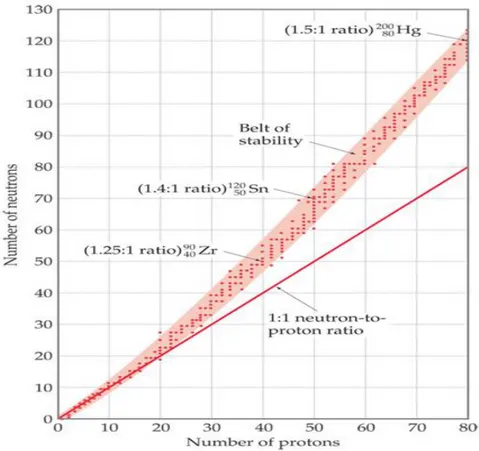
Ketika sejumlah neutron pada berbagai isotop diplotkan terhadap sejumlah proton, pita yang dihasilkan disebut pita kestabilan. Pita ini sesuai dengan perbandingan n/p untuk isotop-isotop stabil. Pita kestabilan menunjukkan bahwa unsur-unsur ringan dengan nomor atom Z = 1 sampai 20, perbandingan n/p untuk isotop stabil adalah 1. Untuk unsur dengan Z > 20, perbandingan n/p meningkat secara bertahap dan mencapai 1.52 pada Pb dan Bi. Disarankan bahwa sebagai inti yang memiliki lebih banyak proton, lebih banyak neutron diperlukan untuk menstabilkan inti.
Karena jumlah proton terlalu besar (Z > 83) tolakan proton-proton menjadi terlalu besar sehingga inti yang stabil tidak dapat dipertahankan. Bahkan, tidak ada nuklida stabil untuk unsur dengan nomor atom yang lebih besar dari 83. Semua unsur dengan Z = 83 atau kurang memiliki setidaknya satu isotop stabil, kecuali untuk technetium (Tc, Z = 43) dan promethium (Pm, Z = 61).
Gambar 1 Kurva
Isotop dengan perbandingan n/p yang berada di luar pita kestabilan bersifat radioaktif. Mereka meluruh sedemikian rupa sehingga produk nuklida akan memiliki perbandingan n/p yang kecil dalam pita kestabilan. Kriteria berikut ini berguna untuk memprediksi jenis peluruhan radioaktif:
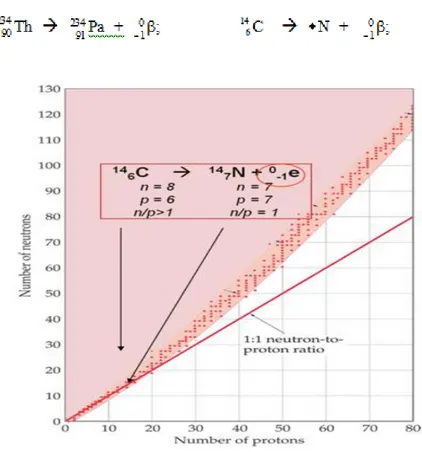
1) Nuklida dengan perbandingan n/p lebih besar dari “perbandingan stabil" cenderung meluruh dengan memancarkan radiasi beta. Emisi ini mengubah neutron menjadi proton, yang membawa rasio n/p ke pita kestabilan.
Misal :
2) Nuklida dengan perbandingan n/p lebih rendah dari pita kestabilan meluruh melalui emisi positron atau penangkapan elektron. Nomor atom nuklida yang lebih rendah (Z < 20) cenderung meluruh melalui emisi positron.
Misal:
Isotop dengan nomor atom > 30 cenderung melakuka penangkapan elektron, karena elektron kulit terdalam (pada n = 1) sangat dekat dengan inti dan mudah diserap oleh kedua. Sebagai contoh,
[Catatan: proton menjadi neutron ketika positron hilang,
atau ketika elektron ditangkap .
3) Nuklida berat diluar bismuth (Bi) memiliki terlalu banyak proton dan tidak stabil. Mereka umumnya meluruh melalui emisi-, yang menurunkan baik jumlah proton dan neutron.
Misal :
d. Jenis peluruhan Radiasi 1) Peluruhan Alpha
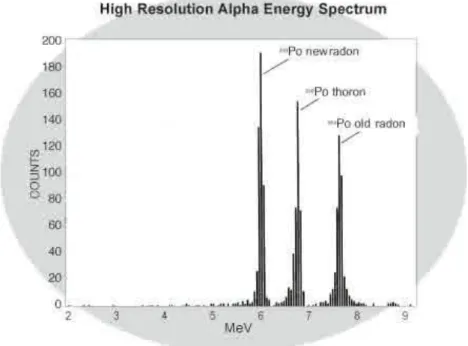
Kebanyakan isotop berat dengan Z > 83 meluruh melalui emisi partikel alfa. Inti-inti radioaktif secara spontan menjadi inti turunan yang kadang-kadang memancarkan partikel α. Pada umumnya diikuti pula dengan peluruhan radiasi gamma. Radiasi alpha mempunyai spektrum energi yang diskrit. Radioisotop yang memancarkan radiasi alpha maka nomor massa akan berkurang 4 dan nomor atomnya berkurang 2, sehingga radiasi alpha disamakan dengan pembentukan inti Helium yang bermuatan +2 ( ).
Contoh:
Berdasarkan hukum kekekalan jumlah muatan dan nucleon maka peluruhan partikel α memenuhi hubungan yang dapat dinyatakan sebagai berikut:
X adalah unsur induk dan Y adalah unsur turunan. Contoh peluruhan α terjadi pada peluruhan Plutonium:
Energi yang dilepaskan pada saat peluruhan, disebut energi disintegrasi atau energi peluruhan yaitu:
Q = (mx-mY-mα)c2
Pada gambar dibawah ini merupakan gambar spektrum energi peluruhan alpha yang berbentuk diskrit.
Gambar 2 Kurva (Sumber: 2) Peluruhan beta
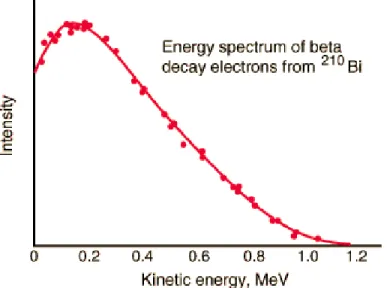
Peluruhan beta (β) adalah suatu proses peluruhan radioaktif dengan muatan inti berubah tetapi jumlah nukleonnya tetap. Radiasi beta minus disamakan dengan pemancaran elektron dari suatu inti atom. Bentuk peluruhan ini terjadi pada inti yang kelebihan neutron dan pada umumnya disertai juga dengan radiasi gamma. Radiasi beta (baik yang positif maupun yang negatif) mempunyai spektrum energi yang sinambung (continous) serta diikuti oleh antineutrino yang membawa kelebihan energi yang dimiliki oleh zarah beta. Seperti halnya pada radiasi Alpha, makin tinggi energi yang dimiliki maka makin pendek umurnya. Pada radiasi Beta minus, nomor atomnya akan bertambah satu, sedang nomor massanya tetap. Reaksi secara umum dapat ditulis sebagai:
⊽ disebut antineutrino yang merupakan partikel netral dengan kelajuan c dan tidak mempunyai massa. Energi dari antineutrino bersifat kinetic. Energi yang dilepas pada saat peluruhan yaitu:
Q = (mx-mY)c2
Beberapa radioisotop berat seperti Thorium-234 dan radioisotop yang paling ringan, seperti karbon-14, meluruh dengan memancarkan partikel beta. Misal :
Gambar 3 Kurva (Sumber: )
Partikel beta adalah elektron yang ditemukan dalam neutron; hilangnya partikel beta mengubah neutron menjadi proton:
Pada gambar berikut merupakan gambar spektrum energi peluruhan beta yang berbentuk spektrum kontinu.
Gambar 4 Kurva (Sumber: ) 3) Emisi Gamma ()
adalah radiasi elektromagnetik energi tinggi yang menyertai banyak peluruhan radioaktif. Proses nuklir sering mengakibatkan inti tereksitasi dan ketika inti ini rileks ke keadaan yang lebih stabil, energi dalam bentuk radiasi- dipancarkan. Beberapa radiasi- dari frekuensi yang berbeda dapat dipancarkan sebagai inti tereksitasi rileks ke keadaan dasar. Sebagai contoh,
Emisi dari sinar- tidak mengubah nomor atom atau nomor massa nuklida tersebut. Suatu inti unsur radioaktif yang mengalami peluruhan, baik peluruhan α maupun peluruhan β atau mengalami tumbukan dengan netron biasanya berada pada keadaan tereksitasi. Pada saat kembali ke keadaan dasarnya inti tersebut akan melepas energi dalam bentuk radiasi gamma.
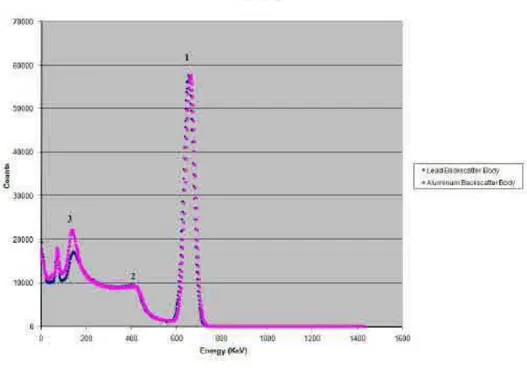
Radiasi gamma mempunyai energi yang diskrit. Gambar 2.9. menunjukkan salah satu contoh energi gamma dari atom cesium 137 (137Cs).
Gambar 5 Spektrum energi peluruhan gamma atom cesium-137 (Rapach, 2010) Radiasi gamma mempunyai energi yang diskrit. Energi sinar gamma (γ) akan berkurang atau terserap oleh suatu material yang dilewatinya. Karena ada penyerapan energi olah bahan maka intensitas dari sinar gamma akan berkurang setelah melewati material tersebut.
I = Io.e-μx
I : intensitas sinar gamma yang berhasil melewati material Io : intensitas mula-mula
x : tebal material
μ : koefisien atenuasi linier atau koefisien pembanding yang besarnya tergantung sifat material penyerap dan energi sinar gamma.
4) Emisi Positron
Positron adalah partikel nuklir bermuatan positif dengan massa yang sama dengan yang ada pada partikel beta dan disimbolkan . Sebagai contoh, isotop boron-9, karbon-11, dan nitrogen-13 semuanya meluruh melalui emisi positron:
Gambar 6 Kurva (Sumber: )
Ketika positron meninggalkan inti, diserap oleh elektron dan reaksi tersebut menghasilkan radiasi gamma 10
1
0 . Proses ini disebut
annihilation; positron terkadang disebut sebagai sebuah antimateri terhadap
elektron. Tabrakan antara materi dan antimateri menghasilkan energi radiasi sebagai dua partikel yang saling menghancurkan.
Bentuk peluruhan ini terjadi pada inti yang kelebihan proton. Pancaran positron dapat terjadi apabila perbedaan energi antara inti semula dengan inti hasil paling tidak sebesar 1,02 MeV. Menurut Pauli, radiasi beta plus sama
dengan perubahan proton menjadi neutron sehingga nomor atomnya akan berkurang satu. Reaksi secara umum dapat ditulis sebagai berikut:
v adalah neutrino yaitu partikel sejenis dengan antineutrino dengan spin yang
berlawanan. Contoh peluruhan beta plus adalah sebagai berikut:
Energi disintegrasi atau energi peluruhannya yaitu: Q = (mx – mY + 2me)c2
Pada radiasi Beta plus akan selalu diikuti dengan peristiwa Annihilasi, karena begitu terbentuk zarah beta plus maka akan langsung bergabung dengan elektron dan menghasilkan radiasi Gamma:
5) Penangkapan Elektron
Dalam proses Electron Capture (EC), sebuah elektron dari kulit terdalam (n = 1) diserap oleh inti, dimana ia bergabung dengan proton untuk membentuk neutron. Sebuah nuklida baru dengan nomor atom yang lebih rendah terbentuk 1 1p + 1 0e 1 0n; 79 195Au + 1 0e 78 195Pt
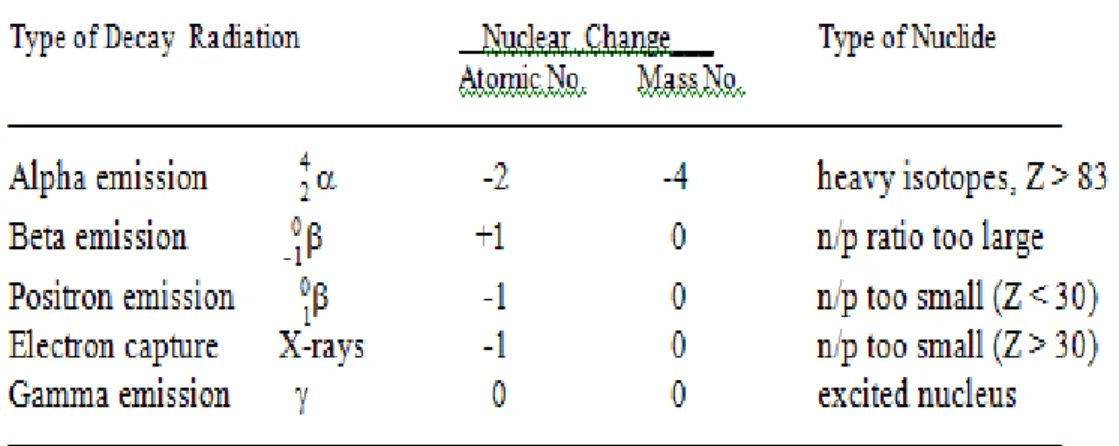
Tabel 2 Jenis peluruhan radioaktif
e. Rangakain peluruhan
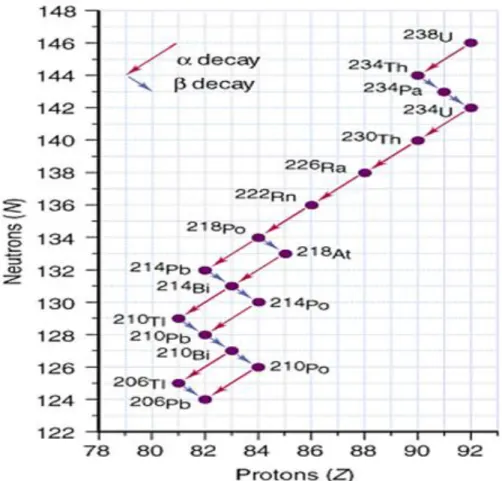
Isotop berat seperti radium, thorium, uranium, dll, menjalani serangkaian peluruhan sampai isotop stabil terbentuk. Sebagai contoh, uranium-238 mengalami serangkaian peluruhan dan hingga timbal-206 terbentuk. Dapatkah Anda mengidentifikasi partikel radioaktif apa yang dihasilkan pada setiap langkah peluruhan?
238 92U 90 234 Th 23491Pa 92 234U 90 230 Th 22688Ra 22286Rn 21884 Po21482Pb 83 214Bi 84 214Po 82 210Pb 83 210Bi 84 210Po 82 206Pb
Gambar 7 Reaksi keseluruhan peluruhan radioaktif dari u-238 menjadi Pb-206 (Sumber: )
Terjadi reaksi fisi pada uranium-235:
Sebagai contoh adalah energi yang dihasilkan pada pembelahan 235 gram uranium-235 adalah ekivalen dengan energi yang dihasilkan pada pembakaran 500 ton batubara. Selain besarnya jumlah energi yang besar, ciri penting dari fisi uranium-235 adalah adanya kenyataan bahwa lebih banyak neutron yang dihasilkan dibandingkan dengan yang semula ditangkap dalam prosesnya. Sifat ini memungkinkan berlangsungnya reaksi rantai inti, yaitu serangkaian reaksi fisi yang dapat berlangsung sendiri tanpa bantuan. Neutron yang dihasilkan selama tahap awal dari fisi dapat mengakibatkan terjadinya fisi dalam inti uranium-235 lain, yang selanjutnya menghasilkan neutron lebih banyak dan seterusnya. Dalam waktu kurang dari satu detik, reaksi dapat menjadi tak
terkendali, membebaskan banyak sekali kalor ke lingkungan. Agar reaksi rantai terjadi, harus ada cukup uranium-235 dalam sampel untuk menangkap neutron, sehingga dikenal istilah massa kritis, yaitu massa minimum material terfisikan yang diperlukan untuk membangkitkan reaksi rantai inti yang dapat berlangsung sendiri.