20 4.1. Bahan
4.1.1. Bahan untuk Penelitian
Bahan yang digunakan untuk pembuatan jelly drink dalam penelitian ini adalah:
1. Alang-alang segar (gemuk, berair dan berwarna kuning) yang diperoleh dari Pasar Tradisional Pucang, Surabaya
2. Karagenan diperoleh dari CV. Tristar Chemical, Surabaya 3. Natrium sitrat diperoleh dari CV. Tristar Chemical, Surabaya 4. Gula pasir “Gulaku”
5. Air minum komersial
6. Cup plastik diperoleh dari Toko Plastik di Jalan Pucang, Surabaya 4.1.2. Bahan untuk Analisa
Bahan yang dibutuhkan untuk analisa adalah asam nitrat (HNO3)
pekat (p.a), asam perklorat (HClO4) (p.a), asam klorida (HCl) (p.a), kertas
saring, amilum (p.a), arsen trioksida (As2O3) (p.a), yodium (I2) (p.a),
kalium iodida (KI) (p.a), natrium hidroksida (NaOH) (p.a), natrium bikarbonat (NaHCO3) (p.a), larutan standar natrium, natrium karbonat
(Na2CO3) (p.a), reagen Folin-Ciocalteu, 2,2-diphenyl-1-picrylhydrazyl
(DPPH), metanol, akuades, asam galat, vitamin C (p.a)
4.2. Alat
4.2.1. Alat untuk Proses
Alat yang dibutuhkan untuk proses pembuatan jelly drink alang-alang adalah gunting, panci, mangkuk, kompor, pengaduk, saringan, gelas
ukur 1 L, termometer 150oC, timbangan top loading (Acculab Sartorius Group), refrigerator (RSA).
4.2.2. Alat untuk Analisa
Alat yang digunakan untuk analisa yaitu alat pengukur daya hisap, Flame Photometer (BWB-XP), instrumen Kjeldahl (Schott Duran), alat distilasi, labu takar (Iwaki Pyrex), pipet volume (Iwaki Pyrex), pipet ukur (Iwaki Pyrex), erlenmeyer (Iwaki Pyrex), buret (Iwaki Pyrex), statif dan klem, gelas ukur (Iwaki Pyrex), corong, beaker glass (Iwaki Pyrex), botol semprot, bulb, sendok, pengaduk, water bath, UV spektrofotometer (Shimadzu UV-1700 Pharmaspec), neraca kasar (Mettler Toledo), neraca analitis (Sartorius), botol timbang (25x40), oven (Binder), eksikator, pH meter (microBENCH T12100), refraktometer (ATAGO NAR-1TLiquid).
4.3. Waktu dan Tempat Penelitian
Penelitian pendahuluan telah dilakukan pada bulan Juni 2010 hingga Agustus 2010, dan penelitian utama akan dilakukan pada bulan April hingga Juni 2011 di Laboratorium Teknologi Pengolahan Pangan, Laboratorium Pengujian Sensoris Pangan, Laboratorium Kimia-Biokimia Pangan dan Gizi, Laboratorium Kimia, Laboratorium Analisa Pangan dan Laboratorium Penelitian Fakultas Teknologi Pertanian, Universitas Katolik Widya Mandala Surabaya.
4.4. Rancangan Penelitian
Rancangan penelitian yang digunakan adalah Rancangan Acak Kelompok (RAK) dengan 2 (dua) faktor, yaitu:
Faktor 1: konsentrasi karagenan yang terdiri atas tiga level, yaitu: K1 = karagenan 0,050%
K2 = karagenan 0,075%
Faktor 2: konsentrasi natrium sitrat yang terdiri atas tiga level, yaitu: N1 = natrium sitrat 0%
N2 = natrium sitrat 0,05%
N3 = natrium sitrat 0,10%
Dari kombinasi kedua faktor tersebut diperoleh 9 (sembilan) kombinasi perlakuan yang diulang sebanyak 3 (tiga) kali. Kombinasi perlakuan ditunjukkan pada Tabel 4.1.
Tabel 4.1. Kombinasi Perlakuan Jelly Drink Alang-alang
Natrium sitrat Karagenan
0,050% (K1) 0,075% (K2) 0,100% (K3)
0% (N1) K1N1 K2N1 K3N1
0,05% (N2) K1N2 K2N2 K3N2
0,10% (N3) K1N3 K2N3 K3N3
Data yang diperoleh dari hasil pengamatan kemudian dianalisa secara statistik menggunakan uji ANOVA (Analysis of Variance) pada α = 5% untuk mengetahui apakah perlakuan memberikan pengaruh nyata terhadap sifat fisik (daya hisap, tingkat sineresis) dan organoleptik (rasa, daya hisap, mouthfeel) jelly drink alang-alang. pH jelly drink juga diukur sebagai data penunjang. Apabila hasil uji ANOVA menunjukkan Fhitung
lebih besar daripada Ftabel pada taraf 5% berarti faktor memberikan
pengaruh nyata terhadap parameter-parameter penelitian, maka dilanjutkan dengan Uji DMRT (Duncan’s Multiple Range Test) pada α = 5% untuk menentukan perlakuan mana yang memberikan perbedaan nyata.
Rimpang alang-alang yang akan digunakan pada setiap kali ulangan diuji kadar airnya untuk mengetahui karakteristik dan sebagai indikator kesegaran bahan baku yang digunakan untuk penelitian. Sari alang-alang yang dihasilkan pada setiap ulangan diuji pH dan total padatan terlarut (TPT) sebagai data penunjang hasil penelitian. Sari alang-alang dan jelly drink alang-alang-alang-alang dengan perlakuan terbaik berdasarkan
uji pembobotan kemudian dilakukan pengujian lanjutan yang meliputi uji kadar natrium, vitamin C, total fenol dan aktivitas antioksidan. Tujuan pengujian ini adalah untuk mengetahui kadar natrium, vitamin C, total fenol dan aktivitas antioksidan dari jelly drink alang-alang yang dihasilkan, serta mengetahui pengaruh proses pengolahan terhadap kadar natrium, vitamin C, total fenol dan aktivitas antioksidannya.
4.5. Pelaksanaan Penelitian
Penelitian akan dilaksanakan dalam dua tahap yang meliputi penelitian pendahuluan dan penelitian lanjutan. Tujuan dilakukan penelitian pendahuluan adalah untuk mengetahui formulasi jelly drink alang-alang yang tepat dan menentukan kisaran perlakuan yang tepat, sedangkan penelitian lanjutan dilakukan untuk mengetahui pengaruh perlakuan yang diteliti. Formula jelly drink alang-alang yang digunakan dalam penelitian ditunjukkan pada Tabel 4.2. Sari alang-alang dibuat terlebih dulu dan setelah itu diambil untuk setiap perlakuan.
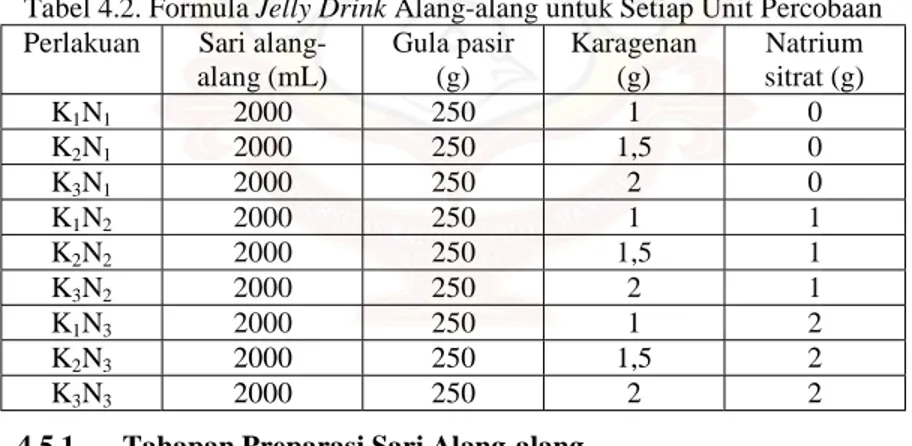
Tabel 4.2. Formula Jelly Drink Alang-alang untuk Setiap Unit Percobaan Perlakuan Sari
alang-alang (mL) Gula pasir (g) Karagenan (g) Natrium sitrat (g) K1N1 2000 250 1 0 K2N1 2000 250 1,5 0 K3N1 2000 250 2 0 K1N2 2000 250 1 1 K2N2 2000 250 1,5 1 K3N2 2000 250 2 1 K1N3 2000 250 1 2 K2N3 2000 250 1,5 2 K3N3 2000 250 2 2
4.5.1. Tahapan Preparasi Sari Alang-alang
Tahap pertama dalam pembuatan jelly drink alang-alang adalah mengekstrak sari dari rimpang alang. Proses ekstraksi sari alang-alang ditunjukkan pada Gambar 4.1.
Gambar 4.1. Proses Ekstraksi Sari Alang-alang Sumber: Techaratanakrai et al. (2007) dengan modifikasi* 1. Sortasi
Sortasi dilakukan untuk memilih rimpang alang-alang yang masih baik dan segar sehingga didapatkan sari alang-alang yang maksimal. Tanda rimpang alang-alang yang masih baik adalah gemuk dan berair.
2. Pencucian
Pencucian dilakukan untuk membersihkan rimpang alang-alang dari tanah dan cemaran fisik lain agar tidak mencemari sari alang-alang yang akan diekstrak.
3. Pengecilan ukuran
Pengecilan ukuran dilakukan dengan memotong rimpang alang-alang hingga panjangnya sekitar 3 cm. Tujuan dilakukan pengecilan ukuran adalah untuk memaksimalkan kontak alang-alang dengan air dan merusak sel rimpang alang-alang sehingga semakin banyak sari alang-alang yang terekstrak.
Sari alang-alang Rimpang alang-alang
Pencucian*
Perebusan (90±2oC, 30’) Air (Rimpang:Air = 1:3)* (b/v) Sortasi *
Pengecilan ukuran (panjang ± 3 cm)*
Penyaringan
Uji kadar air
Analisa: - Uji pH - Uji TPT
4. Perebusan
Rimpang alang-alang direbus dalam air dengan perbandingan rimpang:air adalah 1:3 (b/v). Perbandingan ini diperoleh dari hasil orientasi dimana pada perbandingan ini didapatkan sari alang-alang paling banyak dan paling efektif. Ekstraksi dilakukan pada suhu 90oC selama 30 menit.
5. Penyaringan
Penyaringan dilakukan untuk memisahkan rimpang alang-alang dari sari alang-alang dan sekaligus untuk memisahkan kotoran-kotoran halus yang berasal dari rimpang alang-alang.
4.5.2. Tahapan Pembuatan Jelly Drink Alang-alang
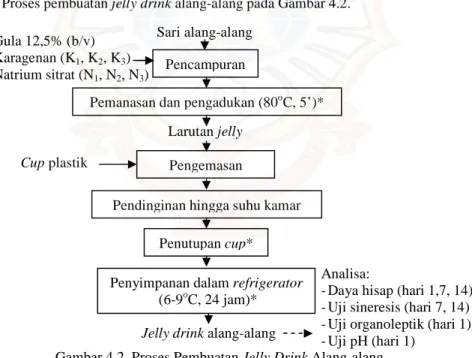
Jelly drink alang-alang dibuat dengan menambahkan gelling agent dan natrium sitrat pada sari alang-alang sesuai dengan perlakuan. Proses pembuatan jelly drink alang-alang pada Gambar 4.2.
Gambar 4.2. Proses Pembuatan Jelly Drink Alang-alang Sumber: Prayogo (2007) dengan modifikasi*
Sari alang-alang Pencampuran Gula 12,5% (b/v)
Karagenan (K1, K2, K3)
Natrium sitrat (N1, N2, N3)
Pemanasan dan pengadukan (80oC, 5’)* Larutan jelly
Pengemasan
Pendinginan hingga suhu kamar
Jelly drink alang-alang Cup plastik
Penutupan cup* Penyimpanan dalam refrigerator
(6-9oC, 24 jam)*
Analisa:
- Daya hisap (hari 1,7, 14) - Uji sineresis (hari 7, 14) - Uji organoleptik (hari 1) - Uji pH (hari 1)
Uraian proses pembuatan jelly drink alang-alang adalah sebagai berikut: 1. Pencampuran
Pada tahap ini, gula, karagenan dan natrium sitrat dicampur terlebih dulu sebelum dicampurkan ke dalam sari alang-alang. Hal ini dilakukan untuk mempermudah memperoleh larutan jelly yang homogen dan meminimalkan penggumpalan karagenan.
2. Pemanasan dan pengadukan
Pemanasan dilakukan pada suhu 80oC selama 5 menit untuk membantu karagenan membentuk gel. Pemilihan suhu ini didasarkan pada suhu hidrasi maksimal karagenan, dimana menurut Moirano yang disitasi dalam Sadar (2004), hidrasi sempurna kappa dan iota karagenan yang didapatkan pada suhu di atas 70oC. Pengadukan dilakukan selama pemanasan untuk membantu pelarutan karagenan, gula dan natrium sitrat dan meratakan penyebaran panas dalam larutan.
3. Pengemasan
Larutan jelly kemudian didinginkan sebentar dan dikemas dalam cup plastik 50 mL.
4. Pendinginan hingga suhu kamar
Tahap ini dilakukan untuk mengeluarkan uap panas dari larutan jelly sebelum dilapkukan penutupan cup. Hal ini dilakukan agar tidak terjadi pengembunan pada saat cup ditutup. Pengembunan akan menyebabkan bagian permukaan jelly drink dan mengganggu pengamatan tingkat sineresis.
5. Penutupan cup
Larutan jelly dalam cup yang telah dingin kemudian ditutup untuk melindungi jelly drink dari kontaminan selama penyimpanan.
6. Penyimpanan dalam refrigerator
Larutan jelly dalam cup disimpan dalam refrigerator selama 24 jam untuk memberi waktu karagenan membentuk gel.
4.6. Metode Analisa
4.6.1. Uji Daya Hisap (Anggraini, 2008)
Jelly drink yang telah setting diukur daya hisapnya dengan menggunakan syringe yang dilengkapi pegas. Cara kerjanya adalah sebagai berikut:
1. Menekan syringe hingga skala di nol.
2. Memasukkan syringe ke bagian tengah jelly drink dalam cup x mL. 3. Melepaskan tekanan di syringe.
4. Menghitung waktu naiknya jelly drink ke bagian atas syringe dengan menggunakan stopwatch.
5. Mencatat waktu menggunakan satuan y detik/x ml jelly drink. 6. Pengamatan dilakukan pada hari ke 7 dan 14 penyimpanan. 4.6.2. Uji Sineresis (Imeson1, 1992)
1. Memasukkan jelly drink ke dalam cup plastik dengan berat yang sama untuk setiap perlakuan.
2. Menyimpan jelly drink selama beberapa hari dalam suhu refri. 3. Mengamati tingkat sineresis jelly drink pada hari ke 1, 7 dan 14
penyimpanan dengan mengambil air yang terpisah dari jelly drink kemudian ditimbang beratnya.
Menghitung tingkat sineresis dengan rumus:
Tingkat sineresis = 100% ) ( )) ( ( ) ( ( x g awal berat g akhir berat g awal berat − Keterangan:
Berat akhir = berat jelly drink dalam cup setelah dilakukan pemisahan air yang terlepas dari sistem gel
4.6.3. Uji Organoleptik (Kartika dkk., 1988)
Uji organoleptik dilakukan untuk mengetahui tingkat kesukaan konsumen terhadap produk jelly drink alang-alang yang dihasilkan pada beberapa parameter. Parameter yang dinilai dalam uji organoleptik ini meliputi kesukaan terhadap rasa, mouthfeel dan kemudahan dihisap. Metode penilaian yang digunakan adalah hedonic test. Pengujian organoleptik dengan hedonic test memungkinkan panelis bebas memberikan nilai terhadap tingkat kesukaan terdapat parameter yang diuji. Panelis memberikan nilai dengan skala numerik dengan kisaran nilai 1-10 pada setiap parameter yang diuji. Semakin tinggi nilai yang diberikan berarti semakin tinggi tingkat kesukaan panelis. Pengujian dilakukan kepada 80 orang panelis yang tidak terlatih. Pengujian organoleptik dilakukan pada hari pertama penyimpanan. Contoh kuesioner uji organoleptik jelly drink alang-alang ditunjukkan pada Lampiran 1.
4.6.4. Uji Pembobotan (DeGarmo et al., 1993)
1. Setiap parameter diberi bobot variabel dengan angka 0-1. Besar bobot variabel masing parameter berbeda tergantung kepentingan tiap parameter.
2. Bobot normal setiap parameter ditentukan dengan cara membagi bobot variabel dengan bobot normal.
3. Menghitung nilai efektifitas dengan rumus: Nilai efektivitas = ) ( ) ( terjelek nilai terbaik nilai terjelek nilai perlakuan nilai − −
(nilai perlakuan-nilai terjelek)/(nilai terbaik-nilai terjelek)
4. Nilai hasil masing-masing parameter ditentukan dari hasil perlakuan antara nilai efektivitas dan bobot normal.
5. Nilai total semua kombinasi perlakuan dihitung dengan menjumlahkan semua nilai hasil setiap parameter.
6. Nilai total terbesar menunjukkan hasil perlakuan terbaik.
Uji pembobotan dilakukan untuk parameter pengujian organoleptik yang meliputi rasa, daya hisap dan mouthfeel dengan bobot masing-masing sebagai berikut:
a. rasa : 0,8 b. daya hisap : 1,0 c. mouthfeel : 0,9
5.6.5. Uji Kadar Air (Sudarmadji dkk., 1997)
1. Menimbang 1-2 g sampel yang telah dihaluskan. Dalam botol timbang yang telah diketahui beratnya.
2. Mengeringkan dalam oven pada suhu 100-105oC selama 3-5 jam. 3. Mendinginkan dalam eksikator dan kemudian ditimbang. 4. Memanaskan lagi dalam oven selama 30 menit.
5. Mendinginkan dalam eksikator dan kemudian ditimbang.
6. Pemanasan diulangi hingga tercapai berat konstan (selisih penimbangan berturut-turut kurang dari 0,2 mg).
7. Pengurangan berat merupakan banyaknya air dalam sampel.
5.6.6. Uji Keasaman (pH) dengan Manual pH Meter microBENCH T12100
1. Membilas elektroda dan temperature probe dengan akuades 2. Menyalakan pH meter.
3. Mencelupkan elektroda pada sampel.
4. Menunggu sampai pembacaan pada layar stabil dan indikator autolock muncul pada layar.
5. Mencatat angka yang tertera pada pH meter.
5.6.7. Uji Total Padatan Terlarut (TPT) (ATAGO NAR-1TLiquid) 1. Membuka dan membersihkan permukaan kaca prisma refraktometer
dengan kertas lensa.
2. Meneteskan larutan jelly drink (2-3 tetes) ke atas permukaan refraktometer dan ditutup.
3. Memutar knob hingga garis batas terlihat di bagian refraksi.
4. Memutar knob kompensator warna untuk mengakromatisasi garis batas sehingga terlihat lebih jelas.
5. Bagian bawah akan menunjukkan nilai total padatan terlarut sampel. 6. Suhu larutan harus dijaga sehingga konstan.
7. Pengamatan dilakukan pada hari pertama.
5.6.8. Analisa Kadar Natrium Metode Flame Photometry (BWB, 2006)
Prinsip analisa kadar natrium dengan metode flame photometry adalah pelepasan ion-ion yang ada dalam sampel melalui proses penguapan yang menyebabkan ion-ion tersebut terdisosiasi menjadi atom-atom. Beberapa dari atom-atom tersebut menghasilkan energi yang sangat tinggi ketika kembali ke bentuk yan lebih stabil. Energi yang dipancarkan merupakan sinar visible dan diukur dengan spektrum elektromagnetik pada panjang gelombang 423 nm.
Preparasi Larutan Standar:
1. Dipipet larutan standar natrium 10.000 ppm sebanyak 10 mL dan ditambahkan deionized water dalam labu takar 100 mL (1.000 ppm). 2. Dipipet larutan standar natrium 1.000 ppm sebanyak 20 mL dan
ditambahkan deionized water dalam labu takar 50 mL (400 ppm). 3. Dipipet larutan standar natrium 1.000 ppm sebanyak 15 mL dan
ditambahkan deionized water dalam labu takar 50 mL (300 ppm). 4. Dipipet larutan standar natrium 1.000 ppm sebanyak 10 mL dan
5. Dipipet larutan standar natrium 1.000 ppm sebanyak 5 mL dan ditambahkan deionized water dalam labu takar 100 mL (100 ppm). 6. Standar dengan konsentrasi 0 ppm dilakukan dengan menambahkan
deionized water pada labu takar hingga volume 50 mL. 7. Kalibrasi Flame Photometer.
Pengujian Kadar Natrium Sampel:
1. Dipipet 5 mL sampel dan dimasukkan dalam labu Kjeldahl 100 mL. 2. Sampel dioksidasi dengan 5 mL HNO3 pekat dan dipanaskan
(lakukan dalam lemari asam).
3. Setelah asap orange hilang, ditambahkan 1 mL HClO4 dan
dipanaskan kembali sampai sampel menjadi jernih.
4. Sampel didinginkan dan ditambahkan 10 mL HCl : deionized water = 1 : 1, kemudian dipanaskan sampai mendidih.
5. Labu diangkat dari pemanas dan didinginkan. 6. Sampel disaring menggunakan kertas saring. 7. Diencerkan sampai volume 50 mL.
8. Diukur kadar natrium menggunakan Flame Photometer. 9. Pengujian dilakukan triplo.
4.6.9. Analisa Vitamin C Cara Titrasi Yodium (Jacobs, 1958) Standarisasi Larutan Standar Yodium 0,01N:
1. Menimbang 0,2473 g As2O3.
2. Melarutkan dalam 2 mL NaOH 10% (b/v) 3. Mengencerkan hingga volume 200 mL. 4. Menetralkan dengan HCl 1 N
5. Menambahkan 2 g NaHCO3.
6. Mengencerkan hingga volume 500 mL 7. Memipet 10 mL larutan As2O3.
8. Menambahkan 10 mL akuades, 2 g NaHCO3 hingga pH 6,5 dan 2 mL
9. Menitasi dengan larutan yodium. 10. Pengujian dilakukan triplo. Penentuan Kadar Vitamin C:
1. Mengambil 5 mL filtrat dengan pipet volum dan dimasukkan ke dalam erlenmeyer 125 mL.
2. Menambahkan 2 mL larutan amilum 1% dan 20 mL akuades. 3. Titrasi dengan larutan standar yodium 0,01N.
4. Perhitungan: 1 mL larutan standar yodium 0,01 N = 0,88 mg asam askorbat.
5. Pengujian dilakukan triplo.
4.6.10. Analisa Total Fenol Metode Folin-Ciocalteu (Waterhouse, 2001 dengan modifikasi)
1. Membuat larutan standar asam galat dengan konsentrasi 0, 50, 100, 150 dan 250 mg asam galat/mL.
2. Memipet 0,1 mL sampel dan memasukkan dalam labu takar 10 mL. 3. Menambah sedikit akuades dan 0,5 mL reagen Folin-Ciocalteu,
kemudian dihomogenkan.
4. Didiamkan selama 30 detik hingga 8 menit. 5. Menambah 1,5 mL larutan natrium karbonat 20%.
6. Menambah akuades hingga tanda batas dan dihomogenkan. 7. Inkubasi pada suhu 20oC selama 2 jam atau 40oC selama 30 menit. 8. Mengukur absorbansi pada λ 765 nm.
4.6.11. Analisa Aktivitas Antioksidan Metode DPPH (Matthäus yang disitasi oleh Rababah et al., 2010 dengan modifikasi) Aktivitas antioksidan diukur sebagai penurunan serapan larutan DPPH yang terjadi akibat berkurangnya antioksidan atau karena terjadi reaksi dengan senyawa radikal. Cara kerjanya adalah sebagai berikut: 1. Menimbang 6 g sampel dan mengekstraksi dalam 50 mL metanol
2. Membuat seri larutan ekstrak 10, 25, 50, 100, 200 μg/mL dari larutan induk.
3. Memipet 3,8 mL larutan ekstrak pada setiap konsentrasi.
4. Menambahkan 0,2 mL larutan DPPH (50 mg DPPH dilarutkan dalam 100 mL metanol).
5. Menambahkan metanol hingga total volume larutan 4 mL.
6. Kontrol dibuat dengan memipet 0,2 mL larutan DPPH dan menambahkan 3,8 mL metanol.
7. Mendiamkan pada ruang gelap selama 30 menit. 8. Mengukur absorbansi pada λ 515 nm.
9. Nilai serapan larutan DPPH sebelum dan sesudah penambahan ekstrak tersebut dihitung sebagai persen inhibisi (% inhibisi) dengan rumus sebagai berikut:
% inhibisi =
x
100
%
A
A
A
kontrol sampel kontrol−
Keterangan:Akontrol = absorbansi tidak mengandung sampel
Asampel = absorbansi mengandung sampel
10. Menghitung IC50 yang diperoleh dari grafik hubungan antara
konsentrasi dan % inhibisi. 11. Pengujian dilakukan triplo.
12. Hasil IC50 sampel dibandingkan dengan IC50 vitamin C pada
33
Anggraini, D.S. 2008. Pengaruh Konsentrasi Karagenan dan Tripotasium Sitrat Terhadap Sifat Fisikokimia dan Organoleptik Jelly Drink, Skripsi S-1, Fakultas Teknologi Pertanian Universitas Katolik Widya Mandala Surabaya, Surabaya.
Anonymous1. 2010. Kugon.
http://www.filipinoherbshealingwonders.filipinovegetarianrecipe .com/kugon.htm (30 Oktober 2010).
Anonymous2. 2009. Jelly Drink.
http://ptp2007.wordpress.com/2009/11/22/jelly-drink/ (30 Oktober 2010).
Arini, L.N. 2010. Kajian Perbedaan Proporsi Konjac dan Karagenan serta Konsentrasi Sukrosa terhaap Sifat Fisikokimia dan Organoleptik Jelly Drink Jambu Biji Merah, Skripsi S-1, Fakultas Teknologi Pertanian Universitas Katolik Widya Mandala Surabaya, Surabaya.
Barber, J.R. 2002. Elasticity 2nd ed. Netherland: Kluwer Academic Publishers.
Belitz, H. D. dan W. Grosch. 1987. Food Chemistry. Berlin: Springer. Buckle, K.A., R.A. Edwards, G.H. Fleet, dan M. Wootton. 1987. Ilmu
Pangan. Terjemahan oleh Hari Purnomo dan Adiono Jakarta : Penerbit Universitas Indonesia.
BWB. 2006. A Guide to Flame Photometer Analysis. UK Ltd.
Chandra, N. 2009. Pengaruh Perbedaan Proporsi Air dengan Jumlah Ekstrak Angkak yang Ditambahkan dan pH terhadap Sifat Fisik, Jumlah Bacillus sp. Dan Organoleptik pada Jelly Drink, Skripsi S-1, Fakultas Teknologi Pertanian Universitas Katolik Widya Mandala Surabaya, Surabaya.
Charley, H. 1982. Food Science 2nd edition. New York: John Wiley and Sons.
Dalimartha, S. 2006. Atlas Tanaman Obat Indonesia jilid 4. Jakarta: Puspa Swara.
De Garmo, E. P., W.G. Sullivan dan J.A. Bontadelli. 1993. Engineering Economy. New York: Macmillans Publishing Company.
deMan, J.M. 1999. Principles of Food Chemistry 3rd ed. Maryland: An Aspen Publication.
Departemen Perindustrian Badan Penelitian dan Pengembangan Industri. 1982. Identifikasi dan Isolasi Akar Rumput Alang-alang. Banjarbaru: Pengarang.
Doores, S. 1990. pH Control Agents and Acidulants, (dalam Food Additives 2nd edition Revised and Expanded, Branen, A.L., P.M. Davidson, S. Salminen dan J.H. Thorngate III, Eds.), Marcel Dekker Inc., New York.
Emerton, V. 2003. Essential Guide to Food Additives 2nd ed. United Kingdom: Leatherhead International Limited.
FAO. 2010. Properties, Manufacture and Application of Seaweed Polysaccharides Agar, Carrageenan and Algin. http://www.fao.org/docrep/field/003/ab730e/ab730e03.htm (25 Agustus 2010).
Fennema, O.R. 1985. Food Chemistry 2nd ed Revised and Expanded. New York: Marcel Dekker, Inc.
Glicksman, M. 1983. Food Hydrocolloid. Florida : C.R.C. Press.
Granato, D., G.F. Branco, F. Nazzaro, A.G. Cruz dan J.A.F. Faria. 2010. Functional Foods and Nondairy Probiotic Food Development: Trends, Concepts, and Products. Comprehensive Reviews on Food Science and Food Safety, 9, 292-302.
http://onlinelibrary.wiley.com/doi/10.1111/j.1541-4337.2010.00110.x/pdf (3 Oktober 2010).
Hanani, E., A. Mun’im dan R. Sekarini. 2005. Identifikasi Senyawa Antioksidan dalam Spons Callispongia Sp dari Kepulauan Seribu. Majalah Ilmu Kefarmasian 2(3):127-133. http://staff.ui.ac.id/internal/130353812/material/endang0203.pdf. (8 April 2011).
Imeson1, A.E. 1992. Carrageenans, (dalam Handbook of Hydrocolloids, J. O Philips dan P. A. Williams, Eds.), Woodhead Publishing Ltd., New York.
Imeson2, A.E. 2009. Food Stabilizers, Thickeners and Gelling Agents. UK: Blackwell Publishing.
Istini, S., A. Zatnika dan Suhaimi. 2006. Manfaat dan Pengolahan Rumput Laut. http://rumputlaut.org/datalama/Pengolahan%20Agar,%20Karage nan,%20dan%20Alginat.pdf (27 Agustus 2010).
Jacob, G. 2009. Hypertension (High Blood Pressure). http://www.holisticonline.com/remedies/heart/hypert_diet_thera py.htm (5 November 2010).
Kartika, B., P. Hastuti, dan W. Supartono. 1998. Pedoman Uji Inderawi Bahan Pangan. Yogyakarta: Pusat Antar Universitas Pangan dan Gizi Universitas Gadjah Mada.
Koh, H.L., Kian C.T. dan Tan C.T. 2009. A Guide to Medicinal Plants: an Illustrated, Scientific and Medicinal Approach. Singapore: World Scientific Publishing, Co. Pte. Ltd.
Lai, V.M.F., L. Wong dan C.Y. Lii. 2000. Effects of Cation Properties of Sol-gel Transition and Gel Properties of κ-carrageenan. J. of
Food Sci., 65(8), 1332-1337. http://lib3.dss.go.th/fulltext/Journal/Journal%20of%20food%20s
cience/2000%20v.65/no.8/jfsv65n8p1332-1337ms19991118%5B1%5D.pdf (25 Agustus 2010).
MacDonald, G.E. 2007. Cogongrass (Imperata cylindrica) : Biology, Distribution and Impacts in the Southeastern U.S. http://www.cogongrass.org/conference07 /macdonald.pdf (17 Juni 2010).
Machfiyyah, D. 2008. Pengaruh Konsentrasi Karagenan terhadap Kadar Serat, Vitamin C dan Organoleptik Jelly Drink Wortel, Abstrak, Jurusan Biologi Universitas Muhammadiyah, Malang.
http://student-research.umm.ac.id/research/download/umm_student_research_a bstract_3234.pdf (26 November 2010).
Pambayun, R., M. Gardjito, S. Sudarmadji dan K.R. Kuswanto. 2007. Kandungan Fenol dan Sifat Antibakteri dari Berbagai Jenis Ekstrak Produk Gambir (Uncaria gambir Roxb). Majalah
Farmasi Indonesia 18(3): 141-146. http://mfi.farmasi.ugm.ac.id/files/news/5._18-3-2007-rindit.pdf
(10 Oktober 2010).
Pomeranz, Y. 1991. Functional Properties of Foond Components 2nd ed. New York: Academic Press, Inc.
Prayogo, T.L. 2007. Perencanaan Unit Sanitasi Pembuatan Jeli Cup 10 ml Kapasitas 20.000 Cup/Hari, Tugas Perencanaan Unit Pengolahan Pangan, Fakultas Teknologi Pertanian Universitas Katolik Widya Mandala Surabaya, Surabaya.
Rababah, T.M., F. Banar, A. Rababah, K. Ereifej dan W. Yang. 2010. Optimization of Extraction Conditions of Total Phenolics, Antioxidant Activities, and Anthocyanin of Oregano, Thyme, Terebinth, and Pomegranate. J. Food Sci., 75(7), C626-C632 Rosenthaal, A.J. 1999. Food Texture: Measurement and Perception.
Maryland: An Aspen Publishers, Inc.
Sadar, L.N. 2004. Rheological dan Textural Characteristics of Copolymerized Hydrocolloidal Solutions Containing Curdlan Gum, Thesis, Faculty of the Graduate School of the University of
Maryland, College Park.
http://drum.lib.umd.edu/bitstream/1903/1850/1/umi-umd-1843.pdf (5 November 2010).
Savary, G., C. Moreau dan N. Cayot. 2009. Impact of The Composition of polysaccharide Composite Gels on Small Molecules Diffusion: A Rheological and NMR Study.Elsevier Appl. Sci. Pbl., 43, 364-368.
Shilling, G.D. 1997. Ecology, Physiology, and Management of Cogongrass (Imperata cylindrica). http://www1.fipr.state.fl.us/fipr/fipr1.nsf/129fc2ac92d3
37ca85256c5b00481502/578586808575536e85256b2f0054a507/ $FILE/03-107-1 4 0Final.pdf (27 Agustus 2010).
Sudarmadji, S., B. Haryono dan Suhardi. 1997. Prosedur Analisa Untuk Bahan Makanan dan Pertanian edisi keempat. Yogyakarta: Liberty.
Suhardi. 1990/1991. Petunjuk Laboratorium Analisa Produk Buah-buahan dan Sayuran. Yogyakarta: Proyek Peningkatan Perguruan Tinggi Universitas Gadjah Mada.
Techaratanakrai, B., S. Chaiwanichiri dan K. Laohasongkram. 2007. Effects of Infusion Temperature and Time on Antioxidant Activity of Herbal Infusions. http://www.scisoc.or.th/stt/33/sec_g/ paper/stt33_G_G0028.pdf (30 Agustus 2010).
Therkelsen, G. H. 1993. Carrageenan, (dalam Industrial Gums: Polysaccharides and Their Derivatives 3rd ed, R.L. Whistler dan J.N. BeMiller, Eds.), Academic Press, Inc., San Diego.
USDA. 2010. Imperata cylindrica (L.) P. Beauv./Cogongrass. http://plants.usda.gov/java/profile?symbol=IMCY (25 Agustus 2010).
Waterhouse, A. 2001. Folin-Ciocalteau Micro Method for Total Phenol in Wine. http://waterhouse.ucdavis.edu/phenol/folinmicro.htm (8 April 2011).
Widjanarko, S. B. 2008. Proses Pembuatan Minuman Jelly. http://id.wordpress.com /tag/jelly-drink/ (5 Desember 2010). Winarno, F.G. 2004. Kimia Pangan dan Gizi. Jakarta: PT. Gramedia
Pustaka Utama.
Zapsalis C. dan B.A. Beck. 1985. Food Chemistry and Nutritional Biochemistry. Canada: John Wiley and Sons.
Zuhra, C.T., J.B. Tarigan dan H.Sitohang. 2009. Aktivitas Antioksidan Senyawa Flavonoid dari Daun Katuk (Sauropus androgunus (L) Merr.). Jurnal Biologi Sumatra 3(1):7-10.