i
Puslitbang tekMIRAJl. Jend. Sudirman No. 623 Bandung 40211
Telp : 022-6030483 Fax : 022-6003373
E-mail: [email protected] Draft Laporan Akhir
Kelompok Teknologi Pengolahan
dan Pemanfaatan Mineral
EKSTRAKSI LOGAM SELENIUM (Se), PLATINA (Pt), DAN
PALADIUM (Pd) DARI LUMPUR ANODA DENGAN PROSES
HIDROMETALURGI
Oleh : Isyatun Rodliyah Pramusanto Muchtar Aziz Nuryadi Saleh Yuhelda Dahlan Tutik Astuti Pipih Hanafiah Edi SuyatnoKEMENTERIAN ENERGI DAN SUMBER DAYA MINERAL PUSAT PENELITIAN DAN PENGEMBANGAN
TEKNOLOGI MINERAL DAN BATUBARA 2012
1
I. PENDAHULUAN1.1. Latar Belakang
Dasar hukum yang terkait dengan penelitian ini adalah sebagai berikut : Undang-Undang Republik Indonesia No.4 Tahun 2009 tentang
Pertambangan Mineral dan Batubara
Peraturan Pemerintah No.23 Tahun 2010 tentang pelaksanaan kegiatan usaha pertambangan mineral dan batubara
Peraturan Menteri ESDM No.7 Tahun 2012 tentang peningkatan nilai tambah mineral khususnya pada Bab 2 Pasal 5 ayat (1) bahwa produk samping/ sisa hasil pengolahan atau pemurnian komoditas tambang mineral tembaga berupa lumpur anoda dan tembaga telurid wajib dilakukan pengolahan dan/atau pemurnian wajib dilakukan di dalam negeri
Pasal 626 ayat (e) Peraturan Menteri Energi dan Sumber Daya Mineral Nomor 0030 Tahun 2005, tentang Organisasi dan Tata Kerja Departemen Energi dan Sumber Daya Mineral
Pasal 46, Keputusan Kepala Pusat Penelitian dan pengembangan Teknologi Mineral dan Batubara Nomor 23.K/70/BLP/2006 tanggal 12 April 2006 tentang Penjabaran Tugas, Fungsi, Susunan Organisasi dan Tata Kerja Pusat Penelitian dan Pengembangan Teknologi Mineral dan batubara.
Platinum group metals (PGMs) adalah logam-logam yang sangat mahal dan logam-logam tersebut memiliki sifat fisika dan kimia yang spesifik sehingga dapat digunakan dalam industri elektronik, kimia, dan automobil. Platina, paladium dan rhodium juga digunakan sebagai katalis dalam automobil untuk menurunkan tingkat emisi dari gas buang[1]. Keberadaan PGMs tidak hanya dari bijih yang ada di alam, tetapi juga dapat ditemukan dari produk samping proses di industri. Keberadaan PGMs ini sangat terbatas jumlahnya. Di Indonesia, logam-logam berharga seperti platina, paladium dan selenium dapat ditemukan di lumpur anoda PT. Smelting Gresik. Lumpur anoda merupakan produk samping dari proses pemurnian tembaga yang mengendap di bawah anoda. Pada lumpur anoda ini terkandung logam-logam berharga seperti Au, Ag, Pt, Pd, Bi, dll.
2
Kandungan logam-logam berharga yang terdapat dalam lumpur anoda tersebut cukup tinggi, hal ini dapat dilihat dari hasil analisis yang dilakukan oleh PT. Smelting tahun 2011, yaitu; emas (Au) 2,12%; perak (Ag) 5,03%; selenium (Se) 15,76%; telerium (Te) 0,33%; bismuth (Bi) 4,47%; platina (Pt) 13 ppm dan palladium (Pd) 185 ppm. Jika dihitung dari lumpur anoda yang dihasilkan oleh PT. Smelting sebesar 1500 ton/tahun dengan asumsi recoveri proses 99,99% maka akan didapatkan emas 31,8 ton/tahun; perak 75,45 ton/tahun; selenium 236,4 ton/tahun; telerium 4,95 ton/tahun; bismuth (Bi) 67,05 ton/tahun; platina 19,5 kg/tahun dan palladium 277,5 kg/tahun. Hingga saat ini, lumpur anoda tersebut langsung dijual ke pembeli di Luar Negeri karena PT. Smelting telah melakukan kontrak panjang dengan Mitshubishi Corporation sebagai off taker lumpur anoda tersebut.Perkembangan dalam proses pemisahan yang efektif untuk merecover platinum dan paladium dari sumber keberadaannya menjadi sangat penting karena kegunaan dari logam-logam tersebut khususnya untuk katalis automobil dan harganya juga sangat mahal. Di Indonesia sendiri, kebutuhan platina dan paladium sebagai bahan dasar pembuatan emas putih masih diimpor. Menurut Undang-Undang No. 4 tahun 2009 tentang pertambangan mineral dan Batubara yang bertujuan untuk memaksimalkan pengolahan mineral dan batubara di dalam negeri guna menjamin tersedianya mineral dan batubara sebagai bahan baku dan/atau sebagai sumber energi untuk kebutuhan dalam negeri, maka peluang mengolah lumpur anoda di dalam negeri sudah harus menjadi prioritas utama, karena sampai saat ini kebutuhan platina, palladium, dan selenium masih mengandalkan impor dari luar negeri sedangkan kekayaan alam kita masih banyak yang belum diolah di dalam negeri.
Penelitian mengenai pengolahan dan pemanfaatan mineral dari dalam negeri menjadi penting. Di Indonesia, penelitian mengenai pengolahan lumpur anoda ini masih sangat terbatas, khususnya untuk merecover platina, paladium, dan selenium. PT. Antam UBPP Logam Mulia telah melakukan visibility study tentang pengolahan lumpur anoda dengan jalur piro-hidrometalurgi (teknologi autotec) dan telah menyatakan kesiapannya untuk mendirikan pabrik pengolahan lumpur anoda PT. Smelting tersebut[2]. Walaupun begitu, masih diperlukan lagi penelitian mengenai pengolahan lumpur anoda tersebut khususnya untuk merecover platina, paladium, dan selenium secara lebih mendalam dengan berbagai
3
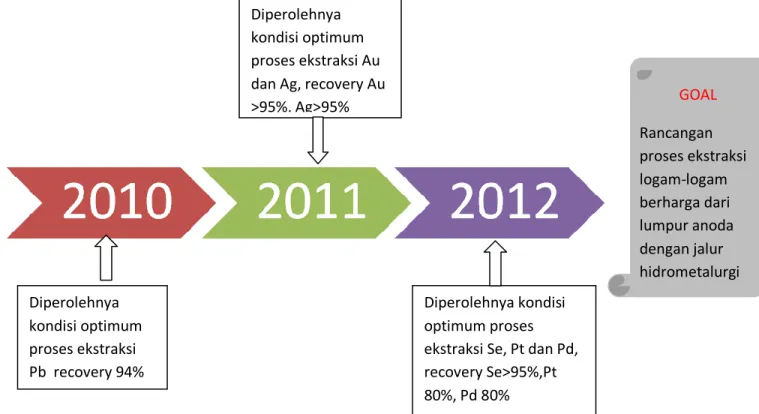
proses yang telah berkembang agar dapat menentukan pengolahan yang lebih efisien, ekonomis, dan ramah lingkungan.Penelitian ini merupakan penelitian lanjutan, dimana pada tahun anggaran 2010 penelitian difokuskan untuk ekstraksi Pb dan pada tahun anggaran 2011 penelitian difokuskan untuk ekstraksi Au dan Ag. Sehingga pada penelitian tahun anggaran 2012 akan dilakukan ekstraksi selenium (Se), platina (Pt), dan palladium (Pd). Roadmap kegiatan penelitian ini dapat dilihat pada Gambar 1.1.
Gambar 1.1. Roadmap Kegiatan Penelitian 1.2. Ruang Lingkup Kegiatan
Ruang lingkup kegiatan terdiri dari 3 (tiga) tahapan utama yang terdiri dari persiapan,ekstraksi logam-logam berharga, analisis data dan pembuatan laporan akhir. Persiapan meliputi studi literatur, pembuatan Rencana Operasional, dan penyiapan peralatan yang ada di laboratorium pengolahan mineral Puslitbang Diperolehnya kondisi optimum proses ekstraksi Pb recovery 94% Diperolehnya kondisi optimum proses ekstraksi Au dan Ag, recovery Au >95%, Ag>95%
Diperolehnya kondisi optimum proses ekstraksi Se, Pt dan Pd, recovery Se>95%,Pt 80%, Pd 80% GOAL Rancangan proses ekstraksi logam-logam berharga dari lumpur anoda dengan jalur hidrometalurgi
4
tekMIRA yang hendak digunakan. Tahap ekstraksi logam-logam berharga terdiri dari proses ekstraksi selenium, platina, dan paladium. Setiap tahapan proses ekstraksi di analisis secara fisik maupun kimia untuk memperoleh data hasil setiap tahapan. Semua hasil kegiatan di buat dalam satu laporan akhir yang juga dapat dibuat makalah ilmiah yang dapat dipublikasikan.1.3. Tujuan
Tujuan penelitian ini adalah untuk mendapatkan hasil yang optimal pada proses ekstraksi logam Se, Pt dan Pd dari lumpur anoda dengan jalur hidrometalurgi serta diperoleh recoveri yang tinggi dari logam-logam berharga tersebut.
1.4. Sasaran
Sasaran kegiatan penelitian ini adalah mendapatkan persen ekstraksi Se>95%, Pt >80% dan Pd>80%.
1.5. Lokasi
Proses kegiatan penelitian dilakukan di laboratorium pengolahan dan pemanfaatan mineral.
5
II. TINJAUAN PUSTAKALumpur anoda (anode slimes) adalah produk/pengotor yang tidak larut dalam larutan elektrolit, tertinggal dilarutan atau terkumpul di bawah anoda selama proses elektrorefining tembaga berlangsung. Komposisi kimia lumpur anoda ini bergantung pada bijih utama yang dihasilkan di anoda dan mekanisme pelarutannya. Logam-logam yang umumnya terdapat dalam lumpur anoda adalah Cu, Ni, Se, Te, Ag, Au, logam-logam Grup Platina (Platinum Groups/PGMs), Pb, Fe, Ba, dll [3] sedangkan dalam bentuk mineralnya adalah CuSO4.5H2O, NiO, Cu2Te, Cu2Se, Ag2Se dan CuAgSe, dll. Proses pengolahan lumpur anoda harus melihat pada komposisi dan morphologi dari lumpur anoda tersebut.
Teknologi proses yang telah dikembangkan untuk ekstraksi logam-logam berharga dari lumpur anoda adalah dengan proses gabungan piro-hidroelektro-metalurgi yang dikenal dengan proses Outotec yaitu dengan melebur lumpur anoda dalam furnace khusus untuk memperoleh selenium dari gas yang dihasilkan, selanjutnya untuk mengambil logam-logam mulia digunakan proses elektrolisis perak kemudian proses pemurnian emas[4]. Proses lainnya adalah dengan hidrometalurgi yaitu yang dikenal dengan proses Hoffman meliputi; pelindian dengan cara klorinasi basah, pemisahan emas dengan cara ekstraksi pelarut, reduksi selenium dan telurium dengan gas sulfur dioksida dan reduksi perak dengan gula (dekstrose)[5].
Teknologi proses yang digunakan dalam penelitian ini adalah dengan hidrometalurgi. Proses hidrometalurgi untuk pengolahan lumpur anoda memiliki beberapa keuntungan dibandingkan dengan proses piro-hidro-elektro metalurgi. Keuntungan proses hidrometalurgi tersebut adalah[6]:
1. Konsumsi energi rendah karena semua proses dilakukan pada suhu dibawah 100 0C. 2. Recoveri yang tinggi tidak hanya untuk emas dan perak tetapi juga untuk platina dan
palladium.
3. Ukuran partikel untuk proses ini adalah sangat halus, sehingga mudah untuk dilakukan pelindian.
Namun, proses secara hidrometalurgi ini memiliki beberapa kekurangan, yaitu:
1. Prosesnya akan membutuhkan banyak reagen kimia, dan harga dari reagen tersebut sangat mahal karena ada yang harus diimpor.
6
2. Prosesnya sangat rumit, banyak tahapannya3. Banyak menghasilkan limbah cair.
2.1. Reduksi dan Recoveri Selenium
Selenium diambil dari rafinate yang bebas emas (dari hasil proses ekstraksi pelarut Au pada tahun 2011) dengan cara mereduksi H2SeO3 dalam larutan menjadi logam Se. Reduktan yang digunakan dalam penelitian ini adalah gas SO2. Reaksi yang terjadi pada proses reduksi Se adalah :
H2SeO3 + 2SO2 + H2O Se + 2H2SO4
Reduksi akan lebih baik apabila dilakukan pada suhu diatas 75 0C untuk menghindari akumulasi selenium monoklin berwarna merah di dalam reactor. Pada suhu reduksi yang tinggi absorbsi SO2 kurang baik. Proses reduksi biasanya dilakukan 6 hingga 8 jam. Setelah pengendapan selenium selesai, slurry kemudian disaring dan filtercake-nya kemudian dicuci dengan HCl encer dan selanjutnya dengan air panas. Filtercake selenium kemudian dikeringkan dengan suhu akhir sekitar 105 0C.
Filtercake yang sudah dikeringkan kemudian didistilasi untuk mengambil produk
murni yang sesuai untuk pasar. Proses distilasi dapat dilakukan dengan distilasi atmosperik maupun vakum. Distilasi atmosperik memiliki keuntungan karena relative sederhana, sedangkan distilasi vakum dapat mengurangi persoalan emisi. Kemurnian distilat dari kedua proses distilasi ini pada dasarnya sama. Residu dari distilasi akan mengandung logam-logam seperti Au, Ag, Pt dan Pd.
2.2. Reduksi dan Recoveri Platina dan Paladium dengan Pelindian dalam Aqua Regia
Logam platina dapat dilarutkan dalam pelarut aqua regia pada suhu 90 0C. Residu dari hasil distilasi yang mengandung logam Pt, Pd dan juga Au (yang belum terekstrak) akan larut dalam aqua regia. Larutan tersebut kemudian ditambahkan dengan ferrous sulfate (FeSO4) untuk mengendapkan emas yang masih tersisa. Platina dan palladium yang terdapat dalam larutan setelah reduksi emas berada dalam bentuk Pt(IV) dan Pd(II), Pd(IV)
7
sudah direduksi menjadi Pd(II) dengan FeSO4. Terlebih dahulu platina dipresipitasi (diendapkan) dengan NH4Cl menjadi ammonium kloroplatinate[7]. Reaksi yang terjadi adalah:PtCl4 + 2 NH4Cl (NH4)2 [PtCl6]
Senyawa ammonium kloropentanate ini dapat terdekomposisi dengan pemanasan menghasilkan sponge crude platinum, yang selanjutnya dimurnikan dengan melarutkan kembali dalam aqua regia dan pengendapan dengan NH4Cl. Produk dari kalsinasi adalah
sponge pure platinum.
Filtrat dari proses pengendapan platina diolah dengan ammonia (NH3) untuk mengubah Pd(II) menjadi senyawa kompleks tetraamin. Reaksi yang terjadi adalah:
PdCl2 + 4NH3 [Pd(NH3)4]Cl2
Senyawa kompleks tetraamin kemudian diubah menjadi senyawa kompleks diamin yang tidak larut dengan penambahan HCl. Reaksi yang terjadi adalah:
[Pd(NH3)4]Cl2 + 2HCl [Pd(NH3)2]Cl2 + 2NH4Cl
Endapan senyawa kompleks diamin kemudian dilindi dengan HCl dan selanjutnya disementasi dengan besi (Fe) sehingga menghasilkan konsentrat Pd[7].
2.3. Recoveri Platina dan Paladium dengan Ekstraksi Pelarut
Pemisahan dan pemurnian dari platina dan paladium adalah proses yang paling sulit dilakukan dibandingkan proses pemisahan logam yang lain. Hal ini disebabkan karena platina dan paladium memiliki sifat kimia yang hampir sama dalam media larutan klorida (dalam penelitian ini, sebelumnya dilakukan proses recoveri emas dengan klorinasi basah yaitu menggunakan media asam klorida). Sifat kimia yang paling khas dari platina dan paladium dalam larutan klorida adalah kecenderungan yang kuat untuk membentuk senyawa kompleks anion dengan ion klorida[8]. Ketika konsentrasi dari platina dan paladium sangat kecil, maka metode pertukaran ion dan ekstraksi pelarut sangat mungkin dilakukan untuk memisahkan dan merecoveri logam-logam tersebut[1]. Pelarut yang digunakan dalam proses ekstraksi pelarut platina dan paladium adalah pelarut-palarut an-ionik, alamine336
8
(tertiary amine, R3N, R=CH3(CH2(CH2(CH2)7). Proses ekstraksi pelarut terdiri dari berbagai tahapan proses, yaitu:- Ekstraksi, dimana platina dan paladium ditransfer menuju ke phasa organik
- Scrubbing, proses reduksi atau penghilangan pengotor-pengotor yang ikut terekstraksi.
- Stripping, proses transfer kembali Pt dan Pd menuju phasa larutan organik murni untuk merecover Pt dan Pd dan proses selanjutnya.
- Solvent make-up, pemurnian kembali larutan organik untuk digunakan kembali dalam proses ekstraksi.
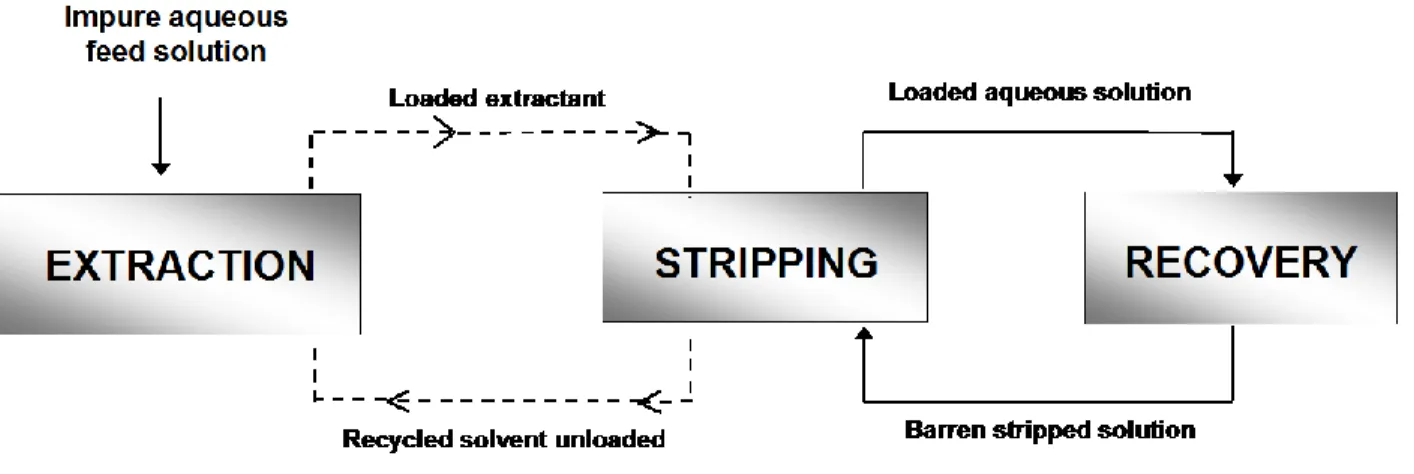
Gambaran proses ekstraksi pelarut secara keseluruhan dapat dilihat pada Gambar 2.1 dibawah ini.
Gambar 2.1. Tahapan-tahapan Proses dalam Ekstraksi Pelarut
Ekstraksi pelarut untuk logam platina dalam larutan asam klorida menggunakan pelarut alamine336 membentuk reaksi sebagai berikut:
R3Norg + HCl ⟶ R3NHClorg
Dalam proses klorinasi basah platina bereaksi dengan HCl membentuk ion kompleks PtCl6 2-. Reaksi yang terjadi antara ion klompleks dengan pelarut alamine336 adalah:
9
PtCl62- + 2 R3NHClorg ⟶ PtCl6(R3NH)2,org + 2Cl-Sedangkan untuk paladium dalam proses klorinasi basah berekasi dengan HCl membentuk ion kompleks PdCl42-. Paladium dapat diekstrak dengan menggunakan pelarut cyphos® iL 101 (trihexyl phopphonium chloride) dalam toluen[8].
2.4. Recoveri platina dan paladium dengan pengendapan selektif
Platina dapat diendapkan dengan amonium klorida menjadi endapan amonium kloroplatinat. Garam platina yang dihasilkan kemudian dipanaskan untuk menghasilkan endapan platina yang lebih murni. Endapan tersebut dilarutkan kembali dalam aqua regia, pengendapan ini dilakukan lebih dari satu kali dengan amonium klorida untuk menghasilkan logam yang murni. Paladium yang tidak ikut mengendap, yang masih tertinggal dilarutan, diendapkan dengan amonia. Garam paladium yang dihasilkan dengan penambahan amonia direcoveri melalui penyaringan, kemudian dilarutkan kembali dalam amonia dan endapan yang terbentuk merupaka garam paladium dengan kualitas yang tinggi.
10
III. PROGRAM KEGIATANKegiatan optimasi ekstraksi logam-logam berharga dari lumpur anoda meliputi beberapa kegiatan sebagai berikut :
3.1 Persiapan
Persiapan dalam kegiatan ini meliputi penulisan rencana operasional, persiapan peralatan agar siap pakai dan studi literatur mendukung kegiatan penelitian yang dilakukan melalui pencarian literatur terkait dari internet, laporan penelitian sebelumnya yang terkait yang telah dilakukan di Puslitbang tekmira maupun instansi penelitian lainnya seperti LIPI, BPPT, Batan dan perguruan tinggi. 3.2 Pengolahan sampel dan analisis data
Tahapan kegiatan ini terdiri dari pengolahan sampel, karakterisasi sampel serta produk, dan koordinasi kegiatan untuk memperoleh metode pendukung selama proses pengolahan sampel berlangsung. Pengolahan sampel dilakukan melalui beberapa kegiatan, yaitu
- Preparasi lumpur anoda dan karakterisasi
Lumpur anoda yang akan digunakan berasal dari sampel yang telah ada di Laboratorium Puslitbang tekMIRA yang sebelumnya digunakan untuk tim lumpur anoda T.A. 2010 dan 2011. Lumpur anoda terlebih dahulu dipreparasi melalui proses kominusi (pengecilan ukuran) hingga diperoleh ukuran butir -150 mesh dan -200 mesh untuk keperluan karakterisasi lumpur anoda. Lumpur anoda yang digunakan telah terlebih dahulu mengalami proses decopperizing dan detelurizing yang dilakukan di PT. Smelting.
Lumpur anoda yang sudah dipreparasi dilakukan karakterisasi dengan metode fire assay dan ICP yang dilakukan di Laboratorium Geoservices untuk menentukan kandungan logam Selenium (Se), Platina (Pt), dan Paladium (Pd) karena karakterisasi lumpur anoda yang dilakukan pada T.A. 2010 dan 2011 tidak bisa ditentukan karena keterbatasan alat yang terdapat di Laboratoium
11
Puslitbang Tekmira. Kandungan awal dari logam Se, Pt, dan Pd penting diketahui karena dapat ditentukan jumlah reaktan dalam proses ekstraksi Se, Pt, dan Pd secara stoikiometri.- Recoveri Au dari larutan hasil proses klorinasi dengan ekstraksi pelarut Recoveri Au dari larutan kaya hasil proses klorinasi yang dilakukan pada T.A. 2011 dilakukan dengan ekstraksi pelarut menggunakan DBC (Dibuthyl Carbhitol). Ekstraksi pelarut dilakukan dalam dua tahap ekstraksi. Parameter-parameter yang dipelajari adalah waktu pelindian dan suhu proses. Fasa organik yang kaya akan Au kemudian dipisahkan dari rafinat. Fasa organik selanjutnya dilakukan pencucian dengan HCl encer (1-2 M) dan diendapkan dengan asam oksalat.
Rafinat hasil pemisahan kemudian dianalisis dengan AAS untuk mengetahui kandungan Au, Ag, Pt, Pd, dan Se.
- Recoveri Pt dari rafinat hasil proses ekstraksi pelarut Au
Proses recoveri Pt dilakukan dengan metode ekstraksi pelarut menggunakan ekstraktan alamine 336 dan pengendapan selektif menggunakan amonium klorida. Parameter-parameter yang dipelajari dalam proses ini adalah konsentrasi waktu proses, dan suhu proses. Fasa organik dan endapan yang dihasilkan dipisahkan dari fasa rafinat dan larutannya.
Fasa rafinat dan larutan hasil penyaringan kemudian dianalisis dengan AAS untuk mengetahui kandungan Au, Ag, Pt, Pd, dan Se.
- Recoveri Pd dari rafinat hasil proses ekstraksi pelarut Pt
Proses recoveri Pd dilakukan dengan metode ekstraksi pelarut menggunakan ekstraktan trihexyltetradecylphosphonium chloride (cyphos) dan pengendapan selektif menggunakan amonium hidroksida. Parameter-parameter yang dipelajari dalam proses ini adalah konsentrasi waktu proses, dan suhu proses. Fasa organik dan endapan yang dihasilkan dipisahkan dari fasa rafinat dan larutannya.
12
Fasa rafinat dan larutan hasil penyaringan kemudian dianalisis dengan AAS untuk mengetahui kandungan Au, Ag, Pt, Pd, dan Se.- Recoveri Se dari larutan hasil proses pengendapan selektif Pd
Recoveri Se dilakukan terhadap larutan hasil proses pengendapan selektif Pd menggunakan natrium disulfit sebagai reduktornya. Percobaan dilakukan pada suhu 90oC dan waktu pengendapan 6 jam.
Endapan Se hasil penyaringan kemudian dianalisis dengan ICP untuk mengetahui kandungan Se yang mengendap.
3.3. Pembuatan laporan akhir
Seluruh proses dan hasil kegiatan penelitian dievaluasi dan dijabarkan dalam sebuah laporan akhir tahunan kegiatan 2012. Dalam proses pembuatan laporan akhir juga diperlukan pencarian literatur pendukung untuk mengetahui fenomena yang dihasilkan dalam proses kegiatan penelitian. Selain itu, juga dibuat ringkasan eksekutif dan makalah ilmiah teknologi mineral dari hasil kegiatan yang telah dilakukan.
13
IV. METODOLOGI4.1. Peralatan
Penggunaan peralatan disesuaikan dengan tahapan kegiatan ekstraksi selenium, platina, dan paladium yang dilakukan. Tahapan kegiatan terdiri dari 4 (empat) yaitu ekstraksi pelarut emas dengan DBC, ekstraksi selenium, ekstraksi pelarut untuk platina, dan ekstraksi pelarut untuk paladium. Peralatan yang dipakai untuk setiap tahapan kegiatan adalah sebagai berikut :
1. Ekstraksi pelarut emas dengan DBC, filtrat hasil proses klorinasi basah pada kondisi proses yang optimum dilakukan proses ekstraksi pelarut dengan DBC untuk merecover emas. Selanjutnya emas yang terdapat dalam phasa organik kemudian diendapkan dengan asam oksalat. Peralatan yang digunakan adalah settler, alat destilasi, corong pemisah, hot plate yang dapat diatur suhu dan kecepatan pengaduknya, beaker glass, magnetic stirer, gelas ukur, termometer, labu ukur. Selain itu diperlukan masker, sarung tangan sebagai alat bantu keamanan kerja; 2. Ekstraksi selenium, menggunakan hot plate yang dapat diatur suhu dan kecepatan
pengaduknya. Peralatan lain yang digunakan adalah beaker glass, magnetic stirer, gelas ukur, termometer, labu ukur. Selain itu diperlukan masker, sarung tangan sebagai alat bantu keamanan kerja;
3. Ekstraksi platina dan paladium dilakukan dengan settler, corong pemisah dan alat-alat pelindian menggunakan alat-alat-alat-alat gelas beserta hotplate stirrer yang dapat diatur suhu dan kecepatan pengaduknya.
4.2. Bahan
Bahan-bahan yang diperlukan untuk kegiatan penelitian adalah sebagai berikut : 1. Dibutyl Carbitol untuk proses ekstraksi emas;
2. Kertas saring Whatman untuk penyaringan; 3. Asam oksalat untuk proses pengendapan emas; 4. Natrium disulfit digunakan untuk mereduksi selenium; 5. Asam klorida untuk proses klorinasi basah;
14
6. Alamine336 untuk pelarut dalam ekstraksi Pt7. Cyphos® il 101 untuk pelarut dalam ekstraksi Pd 8. Toluen untuk pelarut dalam proses ekstraksi pelarut
9. pH indikator untuk mengetahui pH dari masing-masing proses 10. amonium klorida untuk pengendapan platina
11. amoniak untuk pengendapan paladium
4.3. Metode
Lumpur anoda yang digunakan sebelumnya telah mengalami decopperizing dan
detelurizing di PT. Smelting. Lumpur anoda tersebut dipreparasi dan dilakukan
pemercontoh untuk dikarakterisasi dengan ICP. Larutan hasil proses klorinasi yang dilakukan pada T.A. 2011 juga dianalisis dengan ICP untuk mengetahui kandungan Au, Ag, Pt, Pd, dan Se.
Metode yang dilakukan secara garis besar dibagi menjadi 4 (empat) tahap. Tahap 1 (satu) adalah proses recoveri Au dari larutan kaya hasil proses klorinasi dengan ekstraksi pelarut menggunakan DBC. Larutan fasa organik yang kaya akan Au selanjutnya dilakukan pencucian dengan larutan HCl encer (1-2 M). Selanjutnya fasa organik yang telah dicuci tersebut direaksikan dengan asam oksalat untuk mengendapkan Au. Larutan dalam fasa organik dan fasa aqueus dianalisis kandungan Au, Ag, Pt, Pd, dan Se dengan ICP. Pada proses ekstraksi pelarut Au dipelajari kondisi proses yang dapat menghasilkan persen ekstraksi Au tertinggi dengan melakukan analisis variabel kondisi proses terdiri dari konsentrasi DBC (20, 40, dan 50% v/v) dan waktu pelindian (5, 10 dan 15 menit).
Tahap 2 (dua) adalah tahap recoveri Pt dengan proses ekstraksi pelarut menggunakan alamine 336 dan pengendapan selektif dengan amonium klorida. Larutan rafinat dari hasil proses ekstraksi pelarut Au dianalisis kandungan Au, Ag, Pt, Pd dan Se-nya menggunakan ICP untuk mengetahui kandungan logam berharga apa saja yang masih terdapat dalam rafinat. Pada proses ekstraksi Pt ini juga dipelajari kondisi proses yang dapat menghasilkan persen ekstraksi Pt tertinggi
15
dengan melakukan analisis variabel kondisi proses yang terdiri dari suhu pelindian (30, 60, 90, dan 120 oC) dan waktu pelindian (5, 10, 15, 20, 25, dan 45 menit).Tahap 3 (tiga) adalah tahap recoveri Pd dari rafinat hasil proses ekstraksi pelarut Pt dan larutan dari proses pengendapan Pt menggunakan ekstraksi pelarut Cyphos® il 101 dan pengendapan selektif menggunakan amonium hidroksida. Pada ekstraksi pelarut Pd dan pengendapan selektif juga dipelajari kondisi proses yang dapat menghasilkan persen ekstraksi Pd tertinggi dengan melakukan analisis variabel kondisi proses yang terdiri dari suhu pelindian (30, 60, 90, dan 120 oC) dan waktu pelindian (5, 10, 15, 20, 25, dan 45 menit). Rafinat dan larutan dari hasil proses ini akan dianalisis kandungan Au, Ag, Pt, Pd dan Se menggunakan ICP.
Lumpur anoda karakterisasi
Pelindian Pb Ammonium asetat residu Pelindian Au (klorinasi basah) babasahbasah) HCl + H2O2 HCl + NaClO deklorinasi filtrat Ekstraksi pelarut Au residu Natrium karbonat Pelindian Ag amonia filtrat Analisis AAS analisis Pb-Ac DBC
Fasa organik Rafinat analisis
pengendapan Au
As-oksalat Ekstraksi
pelarut Pt
16
Gambar 4.1. Bagan alir proses ekstraksi logam-logam berharga dari lumpuranoda Au powder
Fasa organik Rafinat analisis
Ekstraksi pelarut Pd pengendapan Pt Amonium klorida Pt powder cyphos
Fasa organik Rafinat
Pengendapan Se pengendapan Pd Amonium hidroksida Pd powder Se powder analisis filtrat
17
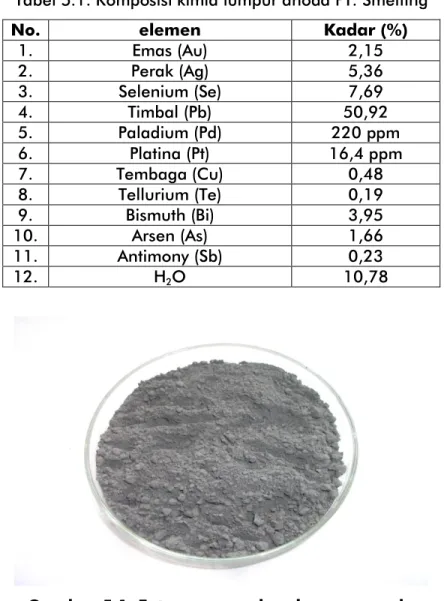
V. HASIL DAN PEMBAHASANKarakterisasi lumpur anoda pada penelitian T.A. 2012 dilakukan dengan analisa ICP yang dilakukan di Laboratorium PT. Geoservices. Hasil analisa ICP adalah seperti pada tabel 5.1. di bawah ini. Gambar penampakan lumpur anoda dapat dilihat pada Gambar 5.1.
Tabel 5.1. Komposisi kimia lumpur anoda PT. Smelting
No. elemen Kadar (%)
1. Emas (Au) 2,15 2. Perak (Ag) 5,36 3. Selenium (Se) 7,69 4. Timbal (Pb) 50,92 5. Paladium (Pd) 220 ppm 6. Platina (Pt) 16,4 ppm 7. Tembaga (Cu) 0,48 8. Tellurium (Te) 0,19 9. Bismuth (Bi) 3,95 10. Arsen (As) 1,66 11. Antimony (Sb) 0,23 12. H2O 10,78
Gambar 5.1. Foto penampakan lumpur anoda 5.1. Hasil-hasil Penelitian T.A. 2010 dan T.A. 2011
Pada penelitian T.A. 2010 dan 2011, ekstraksi Au dari lumpur anoda PT. Smelting Gresik dilakukan dengan proses klorinasi basah menggunakan oksidator H2O2 dan NaOCl setelah proses pemisahan Pb dari lumpur anoda dengan cara pelindian 2 tahap dalam larutan
18
ammonium asetat. Hasil-hasil percobaan pendahuluan menunjukkan bahwa pelindian lumpur anoda PT. Smelting secara langsung dalam larutan HCl (tanpa didahului penghilangan Pb) menghasilkan persen ekstraksi Au <95%, dimana >30% Pb ikut terlarut. Recoveri Pb dalam bentuk campuran PbSO3 dan PbSO4 dilakukan dengan menambahkan ammonium sulfit (NH4SO3) ke dalam larutan hasil pelindian Pb. Larutan ammonium asetat diregenerasi melalui proses kristalisasi ammonium asetat trihidrat dalam filtrat pengendapan Pb yang dilanjutkan dengan pelarutan kristal ammonium asetat-trihidrat dalam metanol.Hasil-hasil percobaan menunjukkan bahwa Pb dapat dipisahkan dari lumpur anoda PT. Smelting secara efektif melalui proses pelindian 2 tahap dalam larutan ammonium asetat dengan persen ekstraksi total tertinggi 94,9%. Persen ekstraksi tersebut dicapai pada konsentrasi amonium asetat 8 M, suhu 70oC, persen solid 20% dan waktu pelindian 120 menit. Pengendapan Pb dari larutan hasil pelindian dengan menambahkan ammonium sulfit yag menghasilkan endapan Pb-sulfit memberikan persen pengendapan Pb 99,9%. Gambar filtrat hasil percobaan pelindian Pb dan endapan Pb-sulfit yang dihasilkan dari proses pengendapan dengan amonium sulfit dapat dilihat pada Gambar 5.2. dan 5.3. Larutan ammonium asetat yang diregenerasi dari larutan hasil pelindian memiliki konsentrasi sekitar 3 molar (0,43x dari konsentrasi awalnya).
19
Gambar 5.3. Endapan Pb-sulfit dari hasil proses pengendapan Pb dengan amonium sulfitPelindian Au dari residu pelindian Pb dengan menggunakan oksidator H2O2 menghasilkan persen ekstraksi Au tertinggi 99,99% pada konsentrasi HCl 7 M, suhu 60oC, H2O2 0,5 M, waktu 180 menit, dan persen solid 20%. Kehilangan Ag pada kondisi ini hanya 0,6%. Pelindian Au dengan oksidator NaOCl menghasilkan persen ekstraksi Au tertinggi 98,86% pada konsentrasi HCl 5 M, suhu 40oC, NaOCl 20% (v/v), waktu 120 menit, dan persen solid 20%. Kehilangan Ag pada proses ini 2–3 %. Pelindian Ag dengan ammonia setelah proses deklorinasi terhadap residu klorinasi terlebih dahulu dapat menghasilkan persen ekstraksi Ag 94,9% pada konsentrasi ammonia 5 M, suhu 25oC, waktu pelindian 60 menit, dan persen solid 20%. Hasil-hasil percobaan pelindian Au dapat dilihat pada Gambar 5.4.
20
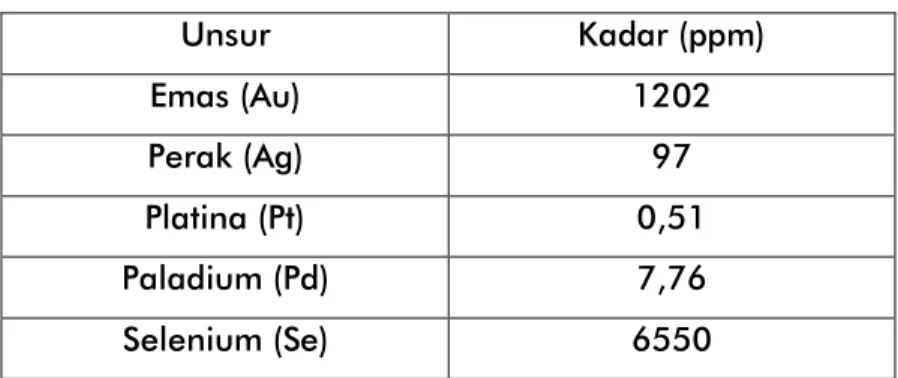
5.2. Proses Recoveri Au dengan Ekstraksi Pelarut menggunakan DBCEkstraksi pelarut Au dilakukan setelah proses klorinasi basah. Ekstraksi ini dilakukan terhadap filtrat hasil proses klorinasi yang bertujuan untuk mendapatkan larutan kompleks organologam. Karakterisasi awal filtrat hasil proses klorinasi dapat diihat pada Tabel 5.1.
Tabel 5.1. Karakterisasi awal filtrat hasil proses klorinasi
Unsur Kadar (ppm) Emas (Au) 1202 Perak (Ag) 97 Platina (Pt) 0,51 Paladium (Pd) 7,76 Selenium (Se) 6550
Pelarut yang digunakan adalah dari jenis ester yaitu DBC (Dibuthyl Carbitol) dengan rumus kimianya (C4H9OCH2CH2)2O. Reaksi yang terjadi pada pembentukan kompleks organologam adalah:
2DBC + 2HAuCl4 → 2DBC-HAuCl4
Pada proses ini spesi logam akan meninggalkan fasa aqueous dan masuk kedalam fasa organik. Diagram alir proses ekstraksi pelarut ini ditunjukkan pada Gambar 5.5.
21
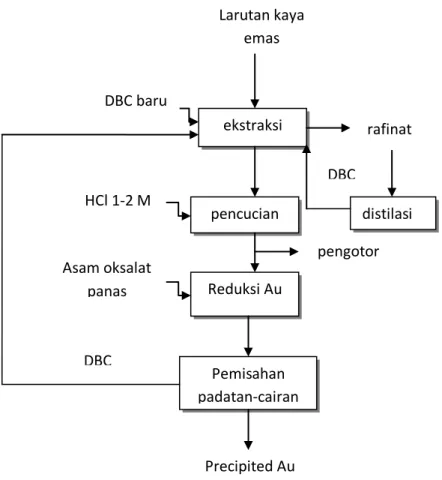
Gambar 5.5. Diagram alir proses ekstraksi pelarut emas dengan DBC
Loaded DBC dari hasil proses ekstraksi tahap awal selanjutnya dilakukan pencucian
menggunakan asam klorida encer sekitar 1-2 M. Pencucian tersebut dimaksudkan menghilangkan logam-logam pengotor seperti selenium, telurium, antimoni, arsen, timah, perak dan bismuth yang ikut terekstrak pada saat proses klorinasi. Pencucian ini biasanya dilakukan hingga tiga sampai lima tahap pencucian. Rafinat tahap pertamanya kemudian diproses lebih lanjut dalam tahap kedua ekstraksi pelarut. Karena mahalnya harga DBC, maka DBC dapat diregenerasi dari rafinat dengan menggunakan distilasi uap. Loaded DBC (larutan dalam fasa organik) dapat dilihat pada Gambar 5.6.
ekstraksi pencucian Reduksi Au Pemisahan padatan-cairan distilasi Larutan kaya emas DBC baru rafinat DBC baru pengotor HCl 1-2 M Asam oksalat panas DBC baru Precipited Au
22
Gambar 5.6. Loaded DBC (larutan dalam fasa organik) hasil proses ekstraksi pelarut AuPada percobaan ini dilakukan parameter-parameter percobaan yaitu; waktu ekstraksi dan konsentrasi DBC. Hasil-hasil percobaan untuk parameter waktu ekstraksi yang dilakukan terhadap persen ekstraksi Au, Pt, Pd dan Se dapat dilihat pada Gambar 5.7.
Gambar 5.7. Grafik waktu ekstraksi terhadap persen ekstraksi Au, Pd, dan Se
Dari grafik di atas dapat dilihat bahwa persen ekstraksi Au pada waktu ekstraksi 5 menit, konsentrasi DBC 40% (v/v), konsentrasi HCl 7 M, suhu 25oC, waktu pendiaman 15 menit adalah menghasilkan persen ekstraksi Au yang tertinggi pada fasa organik yaitu 99,31% sedangkan untuk unsur-unsur yang lain yang dianggap sebagai pengotor dalam proses ini yaitu Pd dan Se sangat rendah yaitu sekitar 1% dan Pt tidak terdeteksi.
23
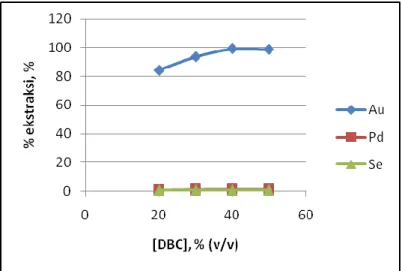
Setelah mendapatkan kondisi waktu ekstraksi yang menghasilkan persen ekstraksi Au yang tertinggi, selanjutnya dilakukan percobaan dengan parameter konsentrasi DBC yaitu pada konsentrasi 20%, 30%, 40%, dan 50% (v/v). Hasil-hasil percobaan untuk variasi konsentrasi DBC terhadap persen ekstraksi Au, Ag, Pt, Pd, dan Se dapat dilihat pada pada Gambar 5.8.Gambar 5.8. Grafik konsentrasi DBC terhadap persen ekstraksi Au, Ag, Pd, dan Se Gambar 5.8. memperlihatkan bahwa semakin tinggi konsentrasi DBC, semakin tinggi pula persen ekstraksi Au yang dihasilkan. Namun, saat konsentrasi dinaikkan menjadi 50% (v/v), persen ekstraksi Au yang dihasilkan cenderung konstan. Sehingga ditetapkan kondisi optimum ditetapkan pada konsentrasi DBC 40% (v/v).
Parameter suhu pada percobaan recoveri Au dengan ekstraksi pelarut tidak dilakukan karena sudah dihasilkan persen ekstraksi Au yang tinggi yaitu 99,31% pada kondisi suhu 25oC. Dari serangkain percobaan ekstraksi pelarut Au diperoleh kondisi optimum yaitu; waktu ekstraksi 5 menit, [DBC] 40% (v/v), suhu 25oC, waktu settler (pendiaman) 15 menit, dan [HCl] 7 M.
5.3. Recoveri Pt dan Pd dengan ekstraksi pelarut dan pengendapan selektif
Proses recoveri Pt dan Pd dilakukan terhadap rafinat dari hasil proses ekstraksi pelarut Au dengan DBC. Hasil analisis kimia rafinat dari hasil proses ekstraksi Au dapat dilihat pada Tabel 5.2.
24
Tabel 5.2. Hasil analisis kimia rafinat dari hasil proses ekstraksi AuUnsur Kadar (ppm) Emas (Au) 5,13 Perak (Ag) 95 Platina (Pt) 15 Paladium (Pd) 120 Selenium (Se) 1600
Recoveri Pt dan Pd dilakukan dengan proses ekstraksi pelarut. Ekstraksi pelarut untuk Pt dilakukan dengan alamine 336 menggunakan pelarut toluen. Sedangkan untuk ekstraksi pelarut Pd menggunakan cyphos® il 101 dengan pelarut toluen. Parameter percobaan untuk ekstraksi Pt dan Pd yang sudah dilakukan adalah waktu ekstraksi; 5, 10, 15, 20 menit dengan konsentrasi alamine 20% (v/v) dan toluen 60% (v/v) untuk ekstraksi Pt serta konsentrasi cyphos® il 101 50% (v/v)) dan toluen 50%(v/v). Proses ekstraksi pelarut Pt dan Pd ini mengalami kendala, karena larutan hasil proses (fasa organik dan rafinat) tidak bisa dianalisis di Laboratorium PT. Geoservices disebabkan terdapatnya senyawa organik yang dapat mengganggu alat yang digunakan dan memberikan hasil yang tidak akurat.
Dalam mengatasi kendala pada proses ekstraksi pelarut Pt dan Pd, maka dilakukan penggantian metode untuk recoveri Pt dan Pd yaitu dengan pengendapan selektif. Diagram alir proses recoveri Pt dan Pd dengan pengendapan selektif dapat dilihat pada Gambar 5.9.
25
Gambar 5.9. Diagram alir proses recoveri Pt dan Pd dengan pengendapan selektif 5.3.1. Recoveri Pt dengan pengendapan selektifRecoveri Pt dilakukan dengan pengendapan selektif menggunakan amonium klorida. Platina dalam larutan rafinat setelah proses ekstraksi pelarut Au berada dalam bentuk Pt(IV). Platina dapat dipresipitasi (diendapkan) dengan NH4Cl menjadi ammonium kloroplatinat. Reaksi yang terjadi adalah:
PtCl4 + 2 NH4Cl (NH4)2 [PtCl6]
Senyawa ammonium kloroplatinat ini dapat terdekomposisi dengan pemanasan menghasilkan sponge crude platinum, yang selanjutnya dimurnikan dengan melarutkan kembali dalam aqua regia dan pengendapan dengan NH4Cl. Produk dari kalsinasi adalah
sponge pure platinum. Parameter percobaan yang dilakukan pada recoveri Pt dengan
Rafinat dari SX-Au
Pengendapan Pt NH4Cl Endapan Pt Larutan Pd dipanaskan Pelarutan kembali NH4Cl Pengendapan Pt kalsinasi Pt Pengendapan Pd NH3 endapan Pd Aqua regia
26
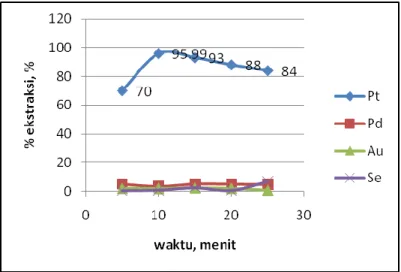
pengendapan selektif ini adalah suhu proses (30, 60, 90, dan 120oC) dan waktu pengadukan (5, 10, 15, 20, dan 25). Hasil-hasil percobaan variasi waktu proses terhadap persen ekstraksi Au, Pt, Pd, dan Se dengan variabel tetap suhu 25oC dan konsentrasi amonium klorida 2N disajikan pada Gambar 5.10.Gambar 5.10. Grafik variasi waktu proses terhadap persen ekstraksi Au, Pt, Pd, dan Se Gambar 5.10. menunjukkan bahwa pada waktu pengadukan dari 5 menit sampai 10 menit dan suhu proses 25oC terjadi peningkatan persen ekstraksi Pt yang cukup signifikan yaitu dari 70% menjadi 95,99%. Hal ini disebabkan platina telah bereaksi sempurna dengan amonium klorida membentuk senyawa kompleks amonium kloroplatinat. Namun setelah waktu pengadukan ditambah menjadi 15 menit sampai 25 menit persen ekstraksi Pt yang diperoleh cenderung menurun. Sehingga diperoleh kondisi yang menghasilkan persen ekstraksi Pt tertinggi pada waktu pengadukan 10 menit. Sedangkan untuk logam-logam lain yaitu Pd, Au, Se pada kondisi pengadukan 10 menit persen ekstraksi yang dihasilkan sangat rendah yaitu antara 1-5%.
Setelah mendapatkan kondisi waktu pengadukan yang optimum, maka percobaan selanjutnya adalah variasi suhu proses dengan variabel tetap waktu pelindian 10 menit, konsentrasi amonium klorida 2N. Grafik variasi suhu proses terhadap persen ekstraksi Pt, Pd, Au, Se ditunjukkan pada Gambar 5.11.
27
Gambar 5.11. Grafik variasi suhu proses terhadap persen ekstraksi Pt, Pd, Au, SeGambar 5.11. menunjukkan bahwa suhu tidak berpengaruh terhadap persen ekstraksi Pt yang diperoleh. Semakin tinggi suhu proses, persen ekstraksi Pt cenderung menurun. Hal ini kemungkinan disebabkan bahwa ketika suhu dinaikkan dari suhu ruangan, maka senyawa kompleks yang terbentuk larut kembali sehingga Pt yang bereaksi dengan amonium klorida semakin berkurang. Kondisi optimum untuk suhu proses adalah 25oC.
Dari serangkaian percobaan untuk recoveri Pt dengan pengendapan selektif diperoleh kondisi proses yang menghasilkan persen ekstraksi Pt tertinggi yaitu 95,99% dicapai pada waktu pengadukan 10 menit, suhu proses 25oC, dan konsentrasi amonium klorida 2N. 5.3.2. Recoveri Pd dengan pengendapan selektif
Recoveri Pd dilakukan dengan pengendapan selektif menggunakan amonium hidroksida. Filtrat dari proses pengendapan platina diolah dengan ammonia (NH3) untuk mengubah Pd(II) menjadi senyawa kompleks tetraamin. Reaksi yang terjadi adalah:
PdCl2 + 4NH3 [Pd(NH3)4]Cl2
Senyawa kompleks tetraamin kemudian diubah menjadi senyawa kompleks diamin yang tidak larut dengan penambahan HCl. Reaksi yang terjadi adalah:
28
Endapan senyawa kompleks diamin kemudian dilindi dengan HCl dan selanjutnya disementasi dengan besi (Fe) sehingga menghasilkan konsentrat Pd.Parameter percobaan yang dilakukan pada recoveri Pd dengan pengendapan selektif ini adalah suhu proses (30, 60, 90, dan 120oC) dan waktu pengadukan (5, 10, 15, 20, dan 25). Hasil-hasil percobaan variasi waktu proses terhadap persen ekstraksi Au, Pt, Pd, dan Se dengan variabel tetap suhu 25oC dan konsentrasi amonium hidroksida 2N disajikan pada Gambar 5.12.
Gambar 5.12. Grafik variasi waktu proses terhadap persen ekstraksi Pd, Pt, Au, dan Se Gambar 5.12. menunjukkan bahwa pada waktu pengadukan berpengaruh terhadap persen ekstraksi Pd yang dihasilkan. Semakin lama waktu pengadukan, persen ekstraksi Pd cenderung meningkat. Pada waktu pengdukan dari 5 menit sampai 20 menit terjadi peningkatan persen ekstraksi Pd yang cukup signifikan yaitu dari 57,86% menjadi 79,64%. Namun setelah waktu pengadukan ditambah menjadi 25 menit persen ekstraksi Pd yang diperoleh cenderung konstan yaitu 78,61%. Sedangkan untuk logam-logam lain yaitu Pt dan Au pada kondisi pengadukan 20 menit persen ekstraksi yang dihasilkan sangat rendah yaitu antara 4-10%. Sedangkan untuk persen ekstraksi Se pada kondisi ini masih cukup tinggi yaitu sekitar 20%.
Setelah mendapatkan kondisi waktu pengadukan yang optimum, maka percobaan selanjutnya adalah variasi suhu proses dengan variabel tetap waktu pelindian 25 menit, konsentrasi amonium hidroksida 2N. Grafik variasi suhu proses terhadap persen ekstraksi Pd, Pt, Au, Se ditunjukkan pada Gambar 5.13.
29
Gambar 5.13. Grafik variasi suhu proses terhadap persen ekstraksi Pd, Pt, Au, Se Gambar 5.13. menunjukkan bahwa suhu berpengaruh terhadap persen ekstraksi Pd yang diperoleh. Kenaikan yang cukup berarti terlihat pada saat suhu dinaikkan dari 30oC menjadi 60oC yaitu diperoleh persen ekstraksi Pd mencapai 96,33% yang semula hanya 84,29%. Sehingga diperoleh kondisi optimum untuk suhu proses adalah 60oC. Foto penampakan untuk endapan Pd yang dihasilkan dari proses pengendapan selektif dapat dilihat pada Gambar 5.14.Gambar 5.14. Foto penampakan untuk endapan Pd yang dihasilkan dari proses pengendapan selektif
Dari serangkaian percobaan untuk recoveri Pd dengan pengendapan selektif diperoleh kondisi proses yang menghasilkan persen ekstraksi Pd tertinggi yaitu 96,33% dicapai pada waktu pengadukan 25 menit, suhu proses 60oC, dan konsentrasi amonium hidroksida 2N.
30
5.4. Recoveri Se dengan pengendapan selektifSelenium diperoleh dari filtrat/larutan hasil proses pengendapan selektif Pd dengan cara mereduksi H2SeO3 dalam larutan menjadi logam Se. Hasil analisis kimia untuk larutan hasil proses pengendapan selektif Pd dapat dilihat pada Tabel 5.3.
Tabel 5.3. Hasil analisis kimia untuk larutan hasil proses pengendapan selektif Pd
Unsur Kadar (ppm) Emas (Au) <0,1 Perak (Ag) 1,1 Platina (Pt) <0,5 Paladium (Pd) 0,51 Selenium (Se) 5276
Pereduksi yang dapat digunakan untuk pengendapan Se adalah gas SO2 dan hidrazin. Pada percobaan ini reduktan yang digunakan adalah natrium disulfit sebagai sumber gas SO2. Reaksi yang terjadi dari proses reduksi H2SeO3 dengan SO2 dan hidrazin adalah[9]:
H2SeO3 + 2SO2 + H2O → Se + 2H2SO4
Proses reduksi lebih baik dilakukan pada suhu diatas 75 0C untuk menghindari akumulasi selenium monoklin berwarna merah. Proses reduksi biasanya membutuhkan waktu enam hingga delapan jam. Setelah reduksi selenium selesai, slurry hasil proses kemudian disaring. Residu hasil penyaringan kemudian dicuci dengan HCl encer dan dilanjutkan dengan air panas. Residu tersebut kemudian dikeringkan sebelum didistilasi. Suhu pengeringan sekitar 105 0C. Selama proses pengeringan harus diperhatikan agar tidak terjadi penggumpalan partikel produk selenium.
Pada percobaan ini dilakukan proses pengendapan dengan natrium disulfit yang dilakukan pada suhu 90oC dengan waktu pengendapan adalah 6 jam yang dihasilkan Se yang mengendap adalah 83,7%. Rendahnya recoveri Se yang dihasilkan disebabkan karena reduktor yang digunakan adalah bukan gas SO2 murni tetapi dari bahan kimia yang dapat menghasilkan SO2 secara tidak langsung yaitu natrium disulfit.
31
VI. KESIMPULAN DAN SARAN6.1. KESIMPULAN
Hasil-hasil percobaan yang diperoleh pada penelitian T.A. 2012 adalah:
Recoveri Au dengan ekstraksi pelarut dihasilkan persen ekstraksi Au yang tinggi yaitu 99,31% pada kondisi suhu 25oC, waktu ekstraksi 5 menit, [DBC] 40% (v/v), waktu settler (pendiaman) 15 menit, dan [HCl] 7 M.
Recoveri Pt dengan pengendapan selektif diperoleh kondisi proses yang menghasilkan persen ekstraksi Pt tertinggi yaitu 95,99% dicapai pada waktu pengadukan 10 menit, suhu proses 25oC, dan konsentrasi amonium klorida 2N. Recoveri Pd dengan pengendapan selektif diperoleh kondisi proses yang
menghasilkan persen ekstraksi Pd tertinggi yaitu 96,33% dicapai pada waktu pengadukan 25 menit, suhu proses 60oC, dan konsentrasi amonium hidroksida 2N. Recoveri Se dilakukan dengan pengendapan menggunakan natrium disulfit yang
dilakukan pada suhu 90oC dan 6 jam yang dihasilkan Se yang mengendap adalah 83,7%.
6.2. SARAN
Perlu dilakukan percobaan terhadap sampel yang berbeda dengan lumpur anoda degan proses dan kondisi-kondisi percobaan yang sama.
DAFTAR PUSTAKA
1. Lee, M; Lee, Y.; Kumar, J.; Kim, S.; Sohn, J. Solvent Extraction of PtCl4 from Hydrochloric Acid Solution with Alamine336, Material Transactions, 2008, Vol.49, No.12, 2823-2828
2. Hadi, A., dan Anwar, A., (2008) : Readiness of PT. Antam Tbk UBPP Logam Mulia to Process Decopprized Anode Slimes from PT. Smelting Gresik, Proceeding of Indonesian Process
Metallurgy, ITB, Bandung.
3. Hait, Jhumki; Jana, R.K; Kumar, Vinay; and Sanyal, S.K. Some Studies on Sulfuric Acid Leaching
32
4. Bjorn Ludvigsson, Stig R Lasson, Anode Slimes Treatment; The Boliden Experience, JOM,April 2003, 41-42
5. Hoffmann, J.E. 1990, The wet chlorination of electrolytic refinery slimes. JOM, 42(8), 50-54. 6. Aviciena, A. Hadi, 2007. Studi optimasi proses klorinasi basah dari anode slime ex PT.
Smelting Gresik dengan oksidator sodium klorat dan hydrogen peroksida dalam media asam klorida. Ilmu material, Fakultas MIPA. UI. Jakarta.
7. Habashi, Fathi,1993. A Textbook of hidrometallurgy. Metallurgy Extractive Quebec, Enr., Canada.
8. Cieszynsha, A.; Wisniewski, W. Extraction of Palladium (II) from Chloride Solutions with
Cyphos®IL 101/toluene Mixtures as Novel Extractant, Separation & Purification Technology,
Vol.73, Issue 2, 2010