BAB II
KAJIAN PUSTAKA
Pada bab ini akan dibahas beberapa penelitian terdahulu yang berkenaan dengan teknologi biogas dan adanya pengotor hidrogen sulfida dalam proses pemurnian biogas. Bab ini digunakan sebagai landasan berfikir dari mulai proses penelitian sampai analisa hasil eksperimen.
2.1 Pengertian Biogas
Biogas adalah campuran dari gas yang dihasilkan oleh bakteri metanogen selagi bertindak sesuai dengan bahan-bahan yang biodegradabel dalam satu kondisi anaerob. Biogas adalah sebagian besar terdiri atas 55 sampai 75 metana (gas) %, 25 sampai 45 % gas asam-arang (CO2) dan jumlah rendah dari yang lain
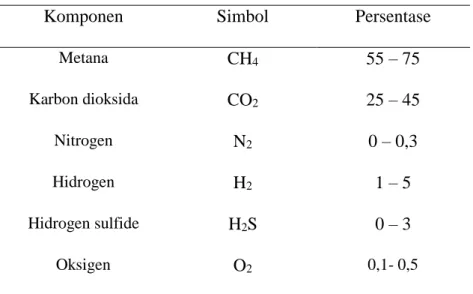
gas-gas seperti yang ditunjukkan di Tabel 1. Tabel 1 Komposisi Biogas
Komponen Simbol Persentase
Metana CH4 55 – 75 Karbon dioksida CO2 25 – 45 Nitrogen N2 0 – 0,3 Hidrogen H2 1 – 5 Hidrogen sulfide H2S 0 – 3 Oksigen O2 0,1- 0,5 Sumber : Kusrijadi dkk, 2009
Sifat Biogas adalah 20% lebih ringan dari udara dan mempunyai satu suhu nyala di sekitar 650 s.d. 750 derajat Celsius. Biogas adalah suatu gas tidak berwarna dan yang tidak berbau serta dapat membakar dengan lidah api biru yang bersih serupa dengan gas LPG (Rahman, 2005). Nilai kalor nya adalah 20 Mega
Joules (MJ) per m3 dan membakar dengan efisiensi 60 persen di suatu dapur
biogas yang konvensional. Salah satu energi terbarukan yang dapat dihasilkan dengan teknologi tepat guna yang relatif lebih sederhana dan sesuai untuk daerah pedesaan adalah energi biogas dengan memproses limbah bio atau bio massa di dalam alat kedap udara yang disebut digester.
Biomassa berupa limbah dapat berupa kotoran ternak bahkan tinja manusia, sisa-sisa panenan seperti jerami, sekam dan daun-daunan sortiran sayur dan sebagainya. Namun, sebagian besar terdiri atas kotoran ternak. Reaktor biogas bukanlah teknologi baru. Sejak tahun 1970 an, Denmark telah melakukan riset, pengembangan, dan aplikasi teknologi ini; mereka tercatat memiliki 20 instalasi pengolahan biogas tersentralisasi (centralized plan) dan 35 instalasi farming plan. China juga telah membangun 7 juta unit reaktor biogas pada tahun 1980 an, sedangkan India juga mencanangkan tak kurang dari 400,000 reaktor biogas pada kurun waktu yang sama (Rahman,2005). Dari lamanya pengembangan dan aplikasi teknologi biogas di dunia, dapat dikatakan bahwa teknologi ini sudah cukup mapan dan terbukti dapat memproduksi energi non-BBM yang sekaligus ramah lingkungan. Terdapat beberapa teknologi yang dapat digunakan untuk mengkonversi limbah (organik) menjadi energi, diantaranya: pembakaran langsung, konversi kimia, dan konversi biologi. Diantara teknologi tersebut,
biogas (konversi biologi) termasuk teknologi yang memiliki efisiensi tinggi karena residu proses biogas juga dapat dimanfaatkan sebagai pupuk berkualitas tinggi. Tanpa keterlibatan teknologi pengolahan sampah, methana hasil penguraian limbah secara natural akan terlepas (dan mencemari) atmosfer tanpa termanfaatkan. Dari sudut pandang itulah dapat disimpulkan bahwa teknologi biogas termasuk teknologi ramah lingkungan.
2.2. Proses Terbentuknya Biogas
Teknologi biogas pada dasarnya memanfaatkan proses pencernaan yang dilakukan oleh bakteri methanogen yang produknya berupa gas methana (CH4).
Gas methana hasil pencernaan bakteri tersebut bisa mencapai 60% dari keseluruhan gas hasil reaktor biogas, sedangkan sisanya didominasi CO2. Bakteri
ini bekerja dalam lingkungan yang tidak ada udara (anaerob), sehingga proses ini juga disebut sebagai pencernaan anaerob (anaerob digestion). Bakteri Metanogen adalah bakteri yang bertindak sesuai dengan metana (gas) bahan organik dan hasil dan gas-gas lain sedang dalam proses daur hidup perlengkapan mereka dalam satu kondisi anaerob. Seperti kehidupan organisme, mereka cenderung untuk menyukai kondisi-kondisi tertentu dan bersifat peka terhadap iklim tropis. Ada banyak jenis dari metanogen dan variasi ciri-ciri mereka. Sesuatu yang pantas dipertimbangkan tingkat pengetahuan dan ketrampilan yang diwajibkan secara ilmiah adalah untuk mengisolasikan bakteri metanogen di dalam biakan murni dan memelihara mereka disuatu laboratorium. Bakteri metanogen berkembang
pelan-pelan dan bersifat peka pada suatu perubahan yang mendadak di dalam kondisi-kondisi kimia dan secara fisik.
Bakteri methanogen akan secara natural berada dalam limbah yang mengandung bahan organik, seperti kotoran binatang, manusia, dan sampah organik rumah tangga. Keberhasilan proses pencernaan bergantung pada kelangsungan hidup bakteri methanogen di dalam reaktor, sehingga beberapa kondisi yang mendukung berkembangbiaknya bakteri ini di dalam reaktor perlu diperhatikan, misalnya temperatur, keasaman, dan jumlah material organik yang hendak dicerna (Subowo,2009). Tahap lengkap pencernaan material organik adalah sebagai berikut:
1. Hidrolisis. Pada tahap ini, molekul organik yang komplek diuraikan menjadi bentuk yang lebih sederhana, seperti karbohidrat (simple sugars), asam amino, dan asam lemak.
2. Asidogenesis. Pada tahap ini terjadi proses penguraian yang menghasilkan amonia, karbon dioksida, dan hidrogen sulfida.
3. Asetagenesis. Pada tahap ini dilakukan proses penguraian produk acidogenesis; menghasilkan hidrogen, karbon dioksida, dan asetat. 4. Methanogenesis. Ini adalah tahapan terakhir dan sekaligus yang paling
menentukan, yakni dilakukan penguraian dan sintesis produk tahap sebelumnya untuk menghasilkan gas methana (CH4). Hasil lain dari
proses ini berupa karbon dioksida, air, dan sejumlah kecil senyawa gas lainnya.
Di dalam reaktor biogas, terdapat dua jenis bakteri yang sangat berperan, yakni bakteri asam dan bakteri methan. Kedua jenis bakteri ini perlu eksis dalam jumlah yang berimbang. Kegagalan reaktor biogas bisa dikarenakan tidak seimbangnya populasi bakteri methan terhadap bakteri asam yang menyebabkan lingkungan menjadi sangat asam (pH kurang dari 7) yang selanjutnya menghambat kelangsungan hidup bakteri methan. Keasaman substrat/media biogas dianjurkan untuk berada pada rentang pH 6.5 s/d 8 (Garcelon dan Clark, 2011). Bakteri methan ini juga cukup sensitif dengan temperatur. Temperatur 35 -oC diyakini Di dalam reaktor bakteri-bakteri methan mengolah limbah bio atau biomassa dan menghasilkan biogas methan.
Dengan pipa yang didesain sedemikian rupa, gas tersebut dapat dialirkan ke kompor yang terletak di dapur. Gas tersebut dapat digunakan untuk keperluan memasak dan lain-lain. Biogas dihasilkan dengan mencampur limbah yang sebagian besar terdiri atas kotoran ternak dengan potongan-potongan kecil sisa-sisa tanaman, seperti jerami dan sebagainya, dengan air yang cukup banyak. Untuk pertama kali dibutuhkan waktu lebih kurang dua minggu sampai satu bulan sebelum dihasilkan gas awal. Campuran tersebut selalu ditambah setiap hari dan sesekali diaduk, sedangkan yang sudah diolah dikeluarkan melalui saluran pengeluaran. Sisa dari limbah yang telah dicerna oleh bakteri methan atau bakteri biogas, yang disebut slurry atau lumpur, mempunyai kandungan hara yang sama dengan pupuk organik yang telah matang sebagaimana halnya kompos sehingga dapat langsung digunakan untuk memupuk tanaman, atau jika akan disimpan atau
diperjualbelikan dapat dikeringkan di bawah sinar matahari sebelum dimasukkan ke dalam karung.
2.3. Jenis Reaktor Biogas
Biodigester/pembangkit biogas adalah suatu konstruksi yang secara fisik, biasanya yang dikenal sebagai kilang biogas. Karena berbagai bahan kimia dan reaksireaksi mikrobiologi berlangsung di dalam biodigester, ini juga yang dikenal sebagai reaktor biogas/bioreaktor atau reactor anaerob. Fungsi utama dari konstruksi ini adalah untuk menyediakan kondisi anaerob didalamnya, sebagai suatu ruang yang kedap udara dan air. Dapat dilakukan dari berbagai bahan-bahan konstruksi dan di dalam bentuk dan ukuran yang berbeda. Dilihat dari sisi konstruksinya, pada umumnya reaktor biogas bisa digolongkan dalam dua jenis, yakni fixed dome (kubah tetap) dan floating drum (terapung). Fixed dome mewakili konstruksi reaktor yang memiliki volume tetap sehingga produksi gas akan meningkatkan tekanan di dalam reaktor. Sedangkan floating drum berarti ada bagian pada konstruksi reaktor yang bisa bergerak untuk menyesuaikan dengan kenaikan tekanan reaktor. Pergerakan bagian reaktor tersebut juga menjadi tanda telah dimulainya produksi gas di dalam reaktor biogas (Karki dkk,1984).
Model terapung dikembangkan di India yang terdiri atas sumur pencerna dan diatasnya ditaruh drum terapung dari besi terbalik yang berfungsi untuk menampung gas yang dihasilkan oleh reaktor. Sumur dibangun dengan menggunakan bahan-bahan yang biasa digunakan untuk membuat fondasi rumah, seperti pasir, batu bata, dan semen. Karena dikembangkan di India, maka reaktor
ini disebut juga model India. Pada tahun 1978/79 di India terdapat 80.000 unit dan selama kurun waktu 1980-1985 ditargetkan pembangunan sampai 400.000 unit alat ini. Model kubah adalah berupa reaktor yang dibangun dengan menggali tanah kemudian dibuat bangunan dengan bata, pasir, dan semen yang berbentuk seperti rongga yang ketat udara dan berstruktur seperti kubah (bulatan setengah bola). Model ini dikembangkan di China sehingga disebut juga Model kubah atau model China. Tahun 1980 sebanyak tujuh juta unit alat ini telah dibangun di China dan penggunaannya meliputi untuk menggerakkan alat-alat pertanian dan untuk generator tenaga listrik. Terdapat dua macam model ukuran kecil untuk rumah tangga dengan volume 6-10 meter kubik dan tipe besar 60-180 meter kubik untuk kelompok (Karki dkk,1984).
India dan China adalah dua negara yang tidak mempunyai sumber energi minyak bumi sehingga mereka sejak lama sangat giat mengembangkan sumber energi alternatif, di antaranya biogas. Bila dilihat dari aliran bahan baku (limbah), reaktor biogas juga bisa dibagi dua, yakni model batch (bak) dan continuous (mengalir). Pada tipe bak, bahan baku reactor ditempatkan di dalam wadah (ruang tertentu) dari awal hingga selesainya proses pencernaan. Ini hanya umum digunakan pada tahap eksperimen untuk mengetahui potensi gas dari suatu jenis limbah organik. Sedangkan pada jenis mengalir, ada aliran bahan baku masuk dan residu keluar pada selang waktu tertentu. Lamanya (waktu) bahan baku berada di dalam reaktor biogas disebut sebagai waktu retensi hidrolik (hydraulic retention
time/HTR) (Indartono,2009). Skema reaktor biogas jenis fixed dome dan floating drum dapat dilihat pada gambar berikut ini:
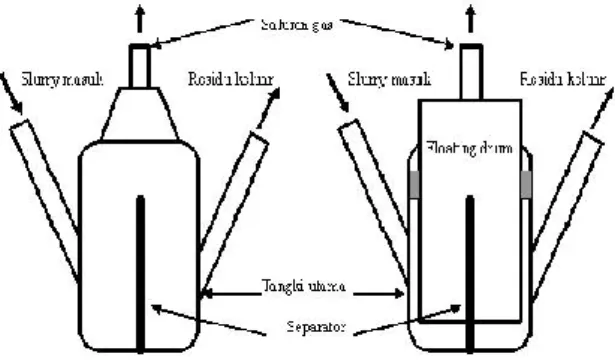
Gambar 2.1. Skema reaktor biogas untuk kotoran hewan jenis fixed dome (kiri) dan floating dome (kanan). (Sumber : Indartono,2009.)
Dari Gambar 2.1. dapat dilihat bahwa kedua jenis konstruksi reaktor biogas tersebut tidak jauh berbeda, keduanya memiliki komponen tangki utama, saluran slurry masuk dan residu keluar, separator (optional), dan saluran gas keluar. Perbedaan yang ada antara keduanya adalah pada bagian pengumpul gasnya (gas collector). Pada konstruksi fixed dome, gas yang terbentuk akan langsung disalurkan ke pengumpul gas di luar reaktor berupa kantung yang berbentuk balon (akan mengembang bila tekanannya naik).
(a) (b) Gambar 2.2. (a). Penampang potongan tipe fixed dome
(b). Penampang potongan tipe floating dome (Sumber : Indartono,2009.)
Fixed dome type Kantong gas Floating dome type
Gambar 2.3. Gambar nyata fixed and floating dome type serta kantong gas (Sumber : Subowo,2009)
2.4. Pemurnian dan proses penyimpanan Biogas
Komposisi biogas bervariasi tergantung dengan asal proses anaerobik yang terjadi, namun rata-rata dapat menghasilkan biogas dengan kadar CH4. Sebesar 55-75%. Selain metana terdapat beberapa senyawa yang dihasilkan yang sifatnya dapat menurunkan kualitas dari pembakaran biogas. Nilai kalori 1 meter kubik biogas sekitar 6000 jam yang setara dengan setengah liter minyak diesel. Oleh karena itu biogas sangat cocok digunakan sebagai bahan bakar alternatif yang ramah lingkungan pengganti minyak tanah, LPG, butana, batubara, maupun bahan-bahan lain yang berasal dari fosil (Kusrijadi dkk, 2009).
Jika biogas dibersihkan dari pengotor secara baik akan memiliki karakteristik yang sama dengan gas alam atau LNG. Komponen pengotor berupa air (H2O), hidrogen sulfida (H2S), karbondioksida (CO2) dan partikulat harus
dihilangkanuntuk mencapai gas kualitas pipeline. Secara teknis pemakaian biogas yang belum mengalami pemurnian, biasanya dicampur dengan gas alam untuk
meningkatkan pembakaran. Proses penghilangan pengotor dalam biogas dapat dilakukan dengan proses desorbsi.
Desorbsi air dan CO2 dapat menggunakan absorber yang berbasis alkali,
silika atau polimer (Mittal, 1996 dan Eyn dan Fileti, 2009). Proses eliminasi H2S
dapat dilakukan dengan menggunakan absorber yang dibuat dari besi yang direaksikan dengan asam klorida dan larutan NaEDTA membentuk Fe-EDTA
(Iron Chelated Solution). Penelitian lain dilakukan dengan proses penjerapan
asam disulfida dengan menggunakan absorber berbasis Besi-oksida (Bedall, 1996).
Abdulkareem (2003), menggunakan arang aktif sebagai absorber gas CO2
dengan karbon aktif berukuran 6 mesh, 10 mesh dan 14 mesh dalam kolom adsorpsi berukuran tinggi 180 cm, dan diameter kolom 3,75 cm. Ukuran karbon aktif yang memberikan hasil terbaik adalah karbon aktif berukuran 14 mesh dengan effisiensi removal CO2 optimum 59,61%, dengan kecepatan biogas masuk
absorber 1000 ml/menit, kandungan gas CO2 masuk = 18,42% volume, CH4
masuk = 76,32% volume dan gas CO2 keluar pada posisi kesetimbangan = 7,44%
volume, CH4 keluar pada posisi kesetimbangan = 69,99% volume. Biogas yang
dihasilkan dalam penelitian ini mempunyai komposisi CH4 = 76,32%, CO2 =
18,42%, NH3 = 1,62%, dan H2S = 0,28%.
Ofori (2005) telah melakukan proses pemurnian dan pengemasan bertekanan biogas dan aplikasinya pada proses pembangkitan energi listrik dan pengganti bahan bakar fosil. Menunjukkan hasil pemurnian biogas mendekati 100% CH4 dengan tingkat efisiensi hasil listrik dan pembakaran pada mesin mobil
mencapai 97 %. Ofori (2005) telah melakukan pemurnian biogas dan peningkatan tekanan dalam sistem penyimpanannya, memperlihatkan tingkat efisiensi pemanasan meningkat sampai 97 %. Hal ini menunjukkan keberhasilan pemurnian biogas dengan menggunakan CaO, Ca(OH)2 dan NH4OH sebagai
penyerap CO2 serta penyerap gas H2S.
Gas Hidrogen sulfida (H2S) yang terkandung dalam gas hasil fermentasi
mengurangi umur pakai (lifetime) dari sitem pemipaan pada instalasi yang menggunakan biogas. Gas ini juga beracun dan sangat korosif untuk sebagian besar jenis logam yang terbuat dari besi (Deublein dan Steinhauser,2008). Jika Hidrogen sulfida yang terkandung dalam biogas terbakar maka akan berubah menjadi sulphur oksida yang akan menyebabkan korosi pada komponen yang terbuat dari logam dan membuat asam minyak pelumas mesin jika digunakan misalnya pada mesin CHP (Combines Heat and Power Generation). Agar dapat mencegah kerusakan yang ditimbulkan oleh hidrogen sulfida maka gas ini harus dihilangkan minimal dikurangi kandungannya (Deublein dan Steinhauser,2008).
2.5. Reaksi Oksidasi Besi Oksida dengan Oksigen dan Air
Senyawa yang terbentuk dari hasil reaksi dengan oksigen dinamakan oksida sehingga reaksi antara oksigen dan suatu unsur dinamakan reaksi oksidasi. Karat besi adalah senyawa yang terbentuk dari hasil reaksi antara besi dan oksigen (besi oksida). Persamaan reaksi pembentukan oksida besi dapat ditulis sbb :
Pada reaksi tersebut, besi mengalami oksida dengan cara mengikat oksigen menjadi besi oksida. Kebalikan dari reaksi oksidasi dinamakan reaksi reduksi. Pada reaksi reduksi terjadi pelepasan oksigen. Besi oksida dapat direduksi dengan cara direaksikan dengan gas hidrogen, persamaannya menjadi sbb:
Fe2O3(s) + 3H2(g) 2Fe(s) + 3H2O(g) . . . (2.2)
Proses pengkaratan adalah istilah umum untuk serangkaian oksida besi. Dalam penggunaan sehari-hari, istilah ini digunakan untuk oksida merah (red
oxides, dibentuk oleh reaksi dari besi dan oksigen dengan adanya air. Karat terdiri
dari besi oksida (Fe2O3) dan besi hidroksida (Fe(OH3)). Karat besi merupakan
proses elektrokimia yang dimulai dengan mentransfer electron dari besi dengan oksigen. Tingkat korosi ini dipengaruhi oleh air dan dipercepat oleh elektrolit, seperti kasus-kasus korosi pada kendaraan. Reaksi utama dari reduksi oksigen ini adalah sbb :
O2 + 4 e- + 2H2O 4 OH- . . . (2.3)
Karena ini merupakan bentuk ion hidroksida maka proses ini sangat dipengaruhi oleh adanya asam. Korosi terbesar kebanyakan dari logam dan dipercepat dengan adanya oksigen pada tingkat pH yang rendah. Pemberian elektron untuk reaksi diatas adalah oksida besi yang digambarkan seperti reaksi berikut :
Reaksi redoks ini dapat terjadi dengan adanya air yang sangat penting untuk pembentukan besi oksidasi :
4Fe2+ + O2 4 Fe3+ + 2 O2- . . . (2.5)
Selain itu, reaksi asam-basa mempengaruhi proses besi hidroksida berikutnya :
Fe2+ + 2H2O Fe(OH)2 + 2 H+
Fe3+ + 3H
2O Fe(OH)3 + 3H+ . . . (2.6)
Sehingga kesetimbangan reaksinya menjadi :
Fe(OH)2 + H FeH2O
Fe(OH)3 FeO (OH) + H2O
2 FeO (OH)2O Fe3 + H2O . . . (2.7)
Dari persamaan diatas terlihat bahwa terbentuknya besi oksida dan besi hidroksida ditentukan oleh adanya air dan oksigen.
2.6. Proses Terdahulu Pemurnian Gas pada Biogas 2.6.1. Pemurnian dengan mereaksikan Fe2O3
Teknik ini merupakan teknik paling tua yang digunakan untuk memurnikan gas dari H2S. Proses dilakukan dengan melewatkan gas yang mengandung H2S ke
serbuk besi yang dicampur dengan serbuk gergajian kayu (Polprasert, 1989) seperti tampak pada Gambar 2.4.
Gas dimasukkan pada bagian 1 dari gambar 2.4, selanjutnya gas akan melewati sela- sela serbuk besi yang dicampur dengan serbuk gergajian kayu pada bagian 2 sehingga terjadi reaksi seperti reaksi 2.8.
Fe2O3 + 3H2S Fe2S3 + H2O . . . (2.8)
Gambar 2.4. Teknik memurnikan gas dari H2S dengan
mereaksikan dengan Fe2O3 (Sumber : Polprasert, 1989)
Untuk mengembalikan Fe2S3 menjadi Fe2O3 dapat dilakukan dengan
mereaksikan dengan O2 dengan melewatkan udara sesuai reaksi 2.9.
2Fe2S3 + 3O2 2Fe2O3 + 3S2 . . . (2.9) 3
2 2
Sumber Fe2O3 dengan cara ini menggunakan serbuk besi hasil pengikiran
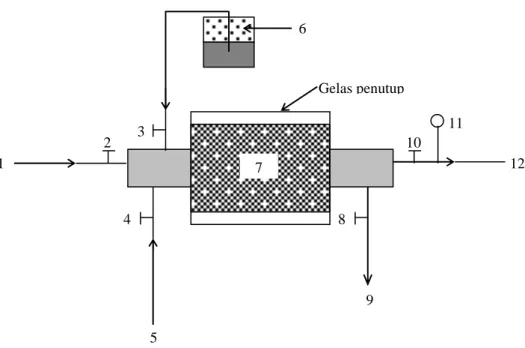
atau penggerindaan, pembubutan, ataupun hasil proses permesinan lainnya. Penggunaan serbuk gergajian kayu pada teknik yang dikemukakan oleh Polprasert (1989), sering menyebabkan tersumbatnya saluran gas. Untuk menghindari penggunaan serbuk gergajian kayu tersebut maka Winhester (2002), mengembangkan teknik baru dengan menggunakan tanah diatom (diatomite) sebagai bahan pengikat. Winchester (2002), menciptakan media penyaring (filtering media) terbuat dari 5-10% ferric ion yang diikat dengan tanah diatom yang dikalsinasi. Kecepatan gas melewati media penyaring dijaga pada 5ft/min dengan menggunakan uap air. Proses selengkapnya dari metode yang dikembangkan oleh Winchester (2002), dapat dilihat pada gambar 2.5. Pada saat beroperasi, gas dimasukkan melalui bagian 1, katup 2 dan 10 dibuka sedangkan katup 3, 4, dan 8 ditutup. Gas selanjutnya melewati media penyaring (bagian 7). Apabila aliran terlalu cepat yaitu melebihi 5 ft/min, maka katup 3 dibuka agar terjadi semprotan air dari bagian 6 sehingga pori-pori media penyaring (bagian 7) menjadi menyempit dan aliran dapat diperlambat. Kecepatan aliran diukur dengan flow meter pada bagian 11. Gas yang telah bersih dari H2S mengalir melewati
bagian 12. melalui gelas penutup dapat diamati saat filter bereaksi dengan H2S
maka media akan berwarna semakin gelap, karena telah terbentuk Fe2S3. untuk
mengembalikan menjadi Fe2O3 maka katup 2, 3 ,dan 10 ditutup, sedangkan katup
4 dan 8 dibuka. Udara selanjutnya dialirkan melewati katup 4 melewati media penyaring bagian 7 dan keluar melalui katup 8.
Gambar 2.5. Mekanisme pemurnian gas dari pengotor H2S dengan media
penyaring terbuat dari Fe2O3 dengan pengikat tanah diatom
(Sumber : Winchester, 2002) 2.6.2. Pemurnian dengan mereaksikan O2
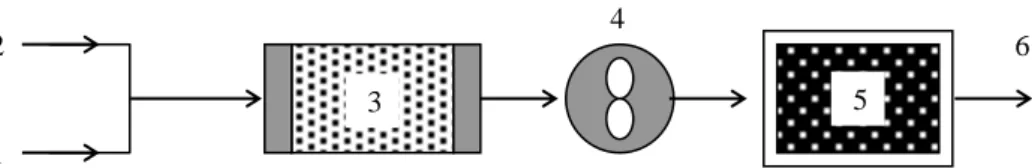
Smith dkk. (1998), mengembangkan teknik untuk memurnikan gas dari kandungan pengotor H2S dengan mereaksikan terlebih dahulu dengan oksigen
yang diperoleh dari udara seperti tampak pada Gambar 2.6.
Gambar 2.6. Teknik memurnikan gas dari pengotor H2S dengan mereaksikan
terlebih dahulu dengan O2, mereaksikan dengan SO2, selanjutnya
mengendapkan belerang dalam air (Sumber : Smith dkk, 1998)
1 2 4 7 8 4 6 3 6 7 8 11 10 9 3 2 4 12 5 1 Gelas penutup
Gas yang akan dimurnikan dimasukkan pada bagian 1 dari gambar 2.6, bersamaan dengan itu dilewatkan pula udara sebagai sumber O2 pada bagian 2.
hembusan udara dijaga agar reaksi yang terjadi tidak memenuhi stokiometri sehingga masih tersisa H2S dengan hasil reaksi lainnya berupa SO2. H2S dan SO2
selanjutnya direaksikan pada bagian 3 dengan bantuan pengaduk dengan penggerak motor pada bagian 6 yang setengahnya tenggelam dalam campuran belerang dan air. Reaksi yang terjadi pada bagian 3 ini sesuai dengan reaksi 2.10. 2H2S + SO2 3S + 2H2O … (2.10)
Gas yang telah dimurnikan pada bagian 3 dikeluarkan melalui saluran 7 dan dimurnikan sekali lagi pada bagian 6 dengan cara yang sama dengan di bagian 3. Gas yang telah murni dari H2S selanjutnya dikeluarkan melalui saluran 8.
Proses ini menghasilkan endapan belerang dan air di bagian 3 dan 5.
Pengontrolan reaksi dengan O2 agar tidak tercapai stoikiometri merupakan
kesulitan utama. Disamping itu penggunaan pengaduk listrik juga tidak menghasilkan reaksi H2S dan SO2 yang sempurna dalam 1 reaktor sehingga
dpelukan 2 reaktor. Untuk itu Smith dkk. 2003, mengembangkan cara baru dengan mereaksikan langsung gas yang mengandung pengotor H2S dengan suatu
Gambar 2.7. Pemurnian Gas dari pengotor H2S dengan
mereaksikan langsung dengan SO2 (Sumber : Smith dkk, 2003)
Gas yang akan dimurnikan dimasukkan pada bagian 1 dari Gambar 2.7. Pada bagian 2 dihembuskan SO2 sehingga terjadi reaksi sesuai dengan reaksi 2.10.
Hasil reaksi kemudian dilewatkan dalam air yang dialirkan dari bagian 7. Gas yang telah dimurnikan bergerak ke bagian 3 untuk selanjutnya dilewatkan ke bagian 6. Endapan belerang akan terkumpul di bagian bawah reaktor (bagian 5) untuk selanjutnya dikeluarkan melalui katup 8.
Trocciola dkk. (1999) juga menemukan cara untuk memurnikan gas dari kandungan pengotor H2S dengan mereaksikan dengan O2, namun tidak
menggunakan air sebagai cara untuk mengendapkan belerang seperti cara dari
2 6 5 4 3 7 8
Smith dkk. (1998) dan Smith (2003), melainkan menggunakan carbon aktif untuk menyerap belerang.
Gambar 2.8 Pemurnian gas dari pengotor H2S dengan mereaksikan dengan O2,
menggunakan karbon aktif untuk menyerap belerang hasil reaksi. (Sumber : Trocciola dkk, 1999)
Gas yang akan dimurnikan dimasukkan pada bagian 1 dari gambar 2.8, selanjutnya dihembuskan udara dari bagian 2 sebagai sumber O2. reaksi diatur
agar sesuai dengan stikiometri sehingga terjadi reaksi seperti reaksi 2.11. H2S + ½ O2 H2O + S . . . (2.11)
Hasil reaksi dilewatkan terlebih dahulu pada penyaring 3 yang menangkap pengotor berupa padatan, cairan, maupun butiran (droplet) air. Gas selanjutnya dihisap dengan menggunakan blower 4 dan dilewatkan pada karbon aktif di bagian 5 untuk penyerapa belerang. Karbon aktif yang digunakan adalah karbon yang diaktifkan dengan potasium. Gas yang telah dimurnikan dikeluarkan melalui saluran 6.
2.6.3. Pemurnian dengan melewatkan H2S dalam air
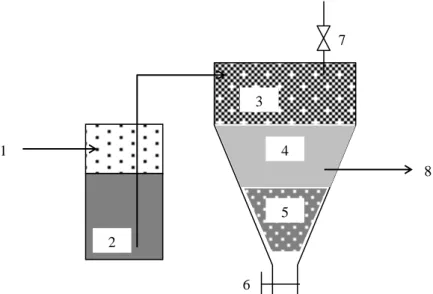
Falkner(2000), menemukan cara untuk memisahkan H2S yang larut dalam
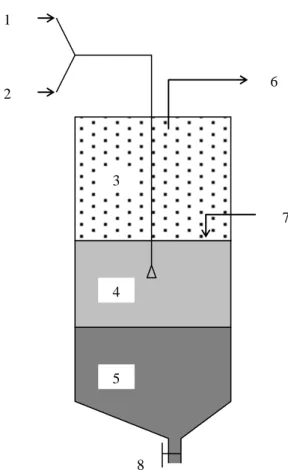
air seperti tampak pada gambar 2.9. Air yang mengandung H2S terlarut 2 1 3 4 5 6
dimasukkan kedalam tangki pada bagian 2 dari gambar 2.9. tekanan dalam tangki selanjutnya ditingkatkan dengan memopakan udara ke dalamnya. Dengan tekanan tinggi yang ada di dalam tangki maka air akan disemprotkan ke dalam tangki yang mengerucut ke bawah. Tekanan dalam tangki diatur pada tekanan 55 psi melalui katup pengatur tekanan 7. H2S yang larut dalam air dalam kondisi diuapkan akan
menjadi jenuh dan terjadi pengendapat belerang di bagian bawah tangki 5 , sedangkan uap air akan secara perlahan berubah menjadi cair di bagian 4. Air yang telah bersih dari H2S dikeluarkan melalui saluran 8, dan endapan belerang
dikeluarkan melalui katup 6.
Gambar 2.9. Pemurnian air dari kandungan H2S
(Sumber : Falkner, 2000)
2.6.4. Pemurnian dengan melarutkan dalam NaOH
Teknik ini dikemukakan oleh Polprasert (1989), diperuntukkan untuk memurnikan gas metana secara sekaligus dari pengotor H2S dan pengotor lainnya
yaitu CO2. Dengan melewatkan gas pada bagian 1 dari gambar 2.10. kedalam 6 7 1 3 4 5 2 8
larutan NaOH (bagian 5) maka kedua jenis gas pengotor tersebut dapat dimurnikan secara bersamaan. Menurut reaksi 2.12, 2.13, 2.14.
2NaOH + CO2 Na2CO3 + H2O . . . (2.12)
Na2CO3 + CO3 2NaHCO3 . . . (2.13)
Na2CO3 merupakan endapan yang terbentuk pada bagian 6, yang dapat
dipisahkan dari larutan. Na2CO3 yang terbentuk dari persamaan 2.12 selanjutnya
bereaksi dengan H2S sesuai dengan reaski 2.14.
H2S + Na2CO3 NaHs + NaHCO3 . . . (2.14)
Untuk mempercepat reaksi maka digunakan pengaduk (bagian 4) yang digerakkan motor (bagian 9).
Gambar 2.10. Pemurnian gas dari kandungan pengotor H2S dan CO2
secara bersamaan dengan melarutkan dalan NaOH. (Sumber : Polprasert, 1989) 9 1 2 4 6 8 5