Polypoidal Choroidal Vasculopathy
Oleh :
Dr. I Putu Budhiastra.Sp.M (K)
BAGIAN ILMU KESEHATAN MATA
FAKULTAS KEDOKTERAN UNIVERSITAS UDAYANA
RSUP SANGLAH DENPASAR 2016
PENDAHULUAN
Polypoidal choroidal vasculopathy (PCV) adalah kelainaan sirkulasi koroid yang ditandai adanya tonjolan aneurisma pada jaringan pembuluh darah koroid, terlihat secara klinis berupa strukur menyerupai polyp, bulat berwarna kemerahan.. Penyakit ini terkait dengan multiple rekuren RPE serosanguinus detachment dan kebocoran retina sekunder serta perdarahan dari kelaunan struktur pembuluh darah koroid ( Ryan, 2006 ).
Istilah PCV dikenali selama hampir 2 dekade. Yannuzzi dan rekannya pada tahun 1990 pertama kali mendeskripsikan idiopatik vasculopathy choroidal polypoidal yakni suatu kelainan vaskulopati koroid yang menyebabkan makula hemoragik dan eksudatif degenerasi pada 11 pasien. Polypoidal choroidal vasculopathy ( PCV ) pertama diidentifikasi pada tahun 1985. Awalnya dianggap langka, namun saat ini PCV sering didiagnosis pada pasien keturunan Afrika dan Asia Pasien-pasien memiliki lesi vaskular polifoid subretinal yang terkait dengan detachment dari epitel pigmen retina (RPE) ( Coppens, 2011 ). Penyakit ini umumnya ditemukan pada populasi Asia dan Afrika-Amerika daripada populasi Kaukasia. Populasi Afrika-Amerika juga dikenal rentan terhadap PCV, meskipun tidak ada studi epidemiologi untuk ras kulit hitam yang telah dilaporkan sampai saat ini. Jenis kelamin laki laki lebih umum didapatkan dengan PCV dibandingkan wanita pada populasi Asia (22 - 37%), tetapi sebaliknya diamati di ras Kaukasia lebih sering terjadi pada wanita dibanding laki-laki (52-65%). Tahun 1990-an, Yannuzzi dan rekan memperluas spektrum klinis idiopatik vasculopathy choroidal polypoidal dan menegakkan konsep PCV ( Mori, 2012 ).
Pasien dengan PCV mungkin menunjukkan gejala yang bervariasi sehingga dapat menyulitkan penegakkan diagnose PCV.Pasien dapat memilikivVA yang baik dan tidak menunjukkan gejala, namun sebagian besar pasien memiliki satu atau lebih gejala visual yang dapat termasuk penglihatan kabur atau redup, floaters serta skotoma sentral atau paracentral, distorsi penglihatan ( objek tampak bengkok dan bergelombang ), dan sudden loss vision di mata yang terkena Spaide dan rekannya pada tahun 1995 mengidentifikasi kelainan choroidal lebih terperinci terkait dengan PCV dan memeriksanya menggunakan indocyanine green angiography. Indocyanine green angiography menunjukkan dua perubahan vaskular choroidal dasar: jaringan pembuluh bercabang di inner koroid dan dilatasi vaskular polypoidal di perbatasan dari jaringan pembuluh darah. Indocyanine green angiography merupakan diagnosis definitif PCV. Ijima dan koleganya ditahun 1999, dengan
menggunakan OCT untuk menunjukkan bahwa gambar dari inner koroid pada mata dengan PCV , terdapat lesi oranye-merah yang menonjol ke arah anterior.
Meskipun gambaran klinis tampak sangat jelas, pemeriksaan lebih lanjut dengan indocyanine green angiography sangat diperlukan, untuk menegakkan diagnosis PCV.
Indocyanine green angiography dan OCT, merupakan perangkat diagnostik yang relatif baru, berguna untuk pemahaman patofisiologi dan untuk mendiagnosis PCV. Patogenesis dan penyebab dari PCV yang sampai saat ini masih belum bisa dipahami secara jelas ( Mori, 2012 ). Terapi untuk PCV semakin berkembang dengan ditunjang kemampuan identifikasi abnormalitas koroidal lewat pemeriksaan penunjang yang semakin canggih termasuk penggunaan laser termal dan terapi photodynamic ( Ryan S, 2006 ). Sebuah multicenter randomized controlled trial berjudul "EVEREST" menunjukkan bahwa pengobatan PCV dengan kombinasi verteporfin terapi photodynamic ( PDT ) ditambah suntikan ranibizumab yang ditoleransi dengan baik dan sangat efektif dalam mencapai regresi lengkap dari lesi polypoidal pada kasus PCV ( Matthew F, Eric K, James C, 2014 ).
Penulisan sari pustaka ini bertujuan meningkatkan pengetahuan mengenai PCV beserta penegakan diagnosisnya. Mengingat kasus PCV saat ini semakin berkembang dalam 15 tahun terakhir dan sering tidak terdiagnosa dengan tepat dari beberapa publikasi. Pemahaman yang lebih baik tentang PCV seharusnya dimiliki oleh seluruh tenaga kesehatan utamanya dokter spesialis mata. Dokter spesialis mata diharapkan mampu mendiagnosis pasien termasuk rencana tatalaksananya sehingga dapat lebih optimal dalam memberikan pelayanan kesehatan.
EPIDEMIOLOGI
Rentang usia pasien dalam study yang pernah dilakukan adalah antara usia 21-93 tahun, dan rata-rata adalah 68,4 tahun yang. Penyakit ini umumnya ditemukan pada populasi Asia dan Afrika-Amerika daripada populasi Kaukasia. Penelitian sebelumnya melaporkan bahwa PCV mencapai 23,0-54,7% pada pasien dengan AMD neovascular di Jepang, 49% di Taiwan, 22,3-24,5% di Cina dan 22,2 -24,6% pada populasi Korea, tetapi hanya sekitar 8-13% dari Kaukasia. Populasi Afrika-Amerika juga dikenal rentan terhadap PCV, meskipun tidak ada studi epidemiologi untuk ras kulit hitam yang telah dilaporkan sampai saat ini. Jenis
kelamin laki laki lebih umum didapatkan dengan PCV dibandingkan wanita pada populasi Asia (22 - 37%), tetapi sebaliknya diamati di ras Kaukasia (52-65%). Tercatat juga bahwa PCV sering mempengaruhi wanita Afrika-Amerika. Kasus bilateral dilaporkan di 9-18% dari Asia (Jepang) dan 21-55% dari Kaukasia. Mayoritas PCV (62-94%) yang terjadi di daerah makula ditemukan pada populasi asia( Jepang ), sedangkan PCV yang sering ditemukan pada bagian peripapiler diamati (18-75%) pada populasi Amerika dan Eropa. Kasus PCV pada beberapa study didapatkan lesi di bawah makula dan lesi yang jauh dari makula ditemukan secara bersamaan. Tidak diketahui mengapa variasi etnis tersebut berpengaruh dalam epidemiologi PCV.
Studi genetik terbaru menunjukkan bahwa beberapa faktor genetik dapat dikaitkan dengan fitur klinis PCV , yang bisa menjadi alasan untuk variasi etnis seperti dalam studi PCV . Mereka melaporkan bahwa 41-45% pasien PCV memiliki hipertensi sistemik. Laporan lain menunjukkan bahwa tingkat protein C-reaktif meningkat pada pasien dengan PCV. Merokok merupakan faktor risiko yang kuat untuk PCV dan riwayat chorioretinopathy serosa sentral adalah faktor risiko yang signifikan untuk PCV ( Honda S, Matsumiya W, Negi A, 2013 ).
ANATOMI
Retina berasal dari 2 lapisan yang bertumpuk yaitu lapisan neural retina (inner surface) dan lapisan pigmen epitel retina (outer surface).Lapisan neural retina berkembang secara konsentris ,dimulai dari tengah area mangkuk optik dan melebar kearah perifer. Proses laminasi dari lapisan ini terjadi pada minggu 8-12 gestasi. Sel-sel ganglion ikut berdiferensiasi secara cepat memasuki trimester kedua. Vaskularisasi retina mengikuti pola konsentris yang sama dan mulai terjadi pada bulan ke 4 mencapai perifer pada bulan ke 9 kehamilan (AAO Staf, 2014-2015).
Retina adalah lembaran jaringan saraf berlapis yang tipis dan semitransparan yang melapisi dua pertiga posterior bola mataLapisan retina dari luar ke arah dalam yaitu retinal pigmen epithelium, fotoreceptor, external limiting membrane, outer nuclear layer, outer flexiform layer, inner nuclear 3 layer, inner plexiform layer, ganglion cell layer, nerve fiber layer, internal limiting membrane (Guyton, 2006; AAO staf, 2014-2015; Sharma, 2003).
Gambar 1. Lapisan retina (AAO Staf, 2014-2015 )
Retina melapisi bagian dalam bola mata mulai dari sejauh korpus siliar dan berakhir pada ora serrata. Pada orang dewasa, ora serrata berada sekitar 6,5 mm di belakang garis schwalbe pada sisi temporal dan 5,7 mm di belakang garis ini pada sisi nasal. Retina mempunyai tebal 0,1 mm pada ora serrata dan 0,56 mm pada kutub posterior. Makula berdiameter 5,5-6 mm yang secara klinis dinyatakan sebagai daerah yang dibatasi oleh cabang-cabang pembuluh darah retina temporal terletak di tengah-tengah retina posterior. Daerah ini ditetapkan oleh ahli anatomi sebagai area sentralis yang secara histologis merupakan bagian retina yang ketebalan lapisan sel ganglionnya lebih dari satu lapis (AAO Staff, 2011-2012; Riordan-Eva P , Whitcher JP, 2004).
Makula terletak di retina bagian polus posterior di antara arteri retina temporal superior dan inferior dengan diameter ±5.5 mm. Makula merupakan suatu daerah cekungan yang terletak di temporal dari saraf optik. Makula dibagi menjadi daerah fovea, foveola, free avascular zone (FAZ), dan umbo di bagian 3 sentral. Tepi fovea memiliki ketebalan sekitar 0,55 mm sama dengan ketebalan maksimal retina. Umbo memiliki ketebalan sekitar 0,13 mm, dan ini merupakan bagian retina yang paling tipis. Secara histologis, makula terdiri dari lima lapisan yaitu membran limitan interna, lapisan pleksiform luar (lapisan ini lebih tebal dan padat di daerah makula karena akson sel batang dan sel kerucut menjadi lebih oblik saat
meninggalkan fovea dan dikenal sebagai lapisan serabut Henle), lapisan nukleus luar, membran limitan 4 eksterna, dan sel-sel fotoreseptor limitan eksterna, dan sel-sel fotoreseptor (AAO Staff, 2014-2015).
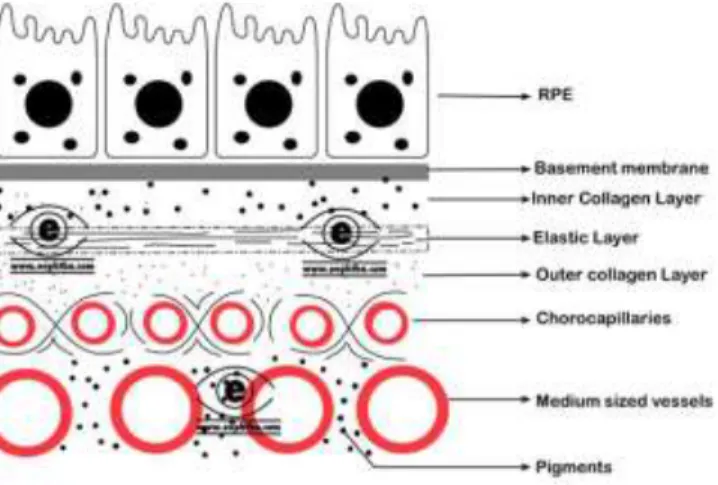
Koroid adalah membran tipis tapi mengandung banyak vaskular yang melapisi permukaan dalam sclera. Memanjang dari anterior ora serrata ke saraf optik di posterior. Memiliki permukaan luar kasar yang melekat sklera di saraf optik dan ujung vena vortex. Permukaan bagian dalam halus dari koroid melekat pada epitel berpigmen retina (RPE) .Choroid kemudian berlanjut menjadi piamater dan arakhnoid di saraf optik. Koroid biasanya ketebalan 100-220 µm, ketebalan tertinggi pada makula 500- 1000 µm ( Dutta M, 2013 ).
Gambar 2. Anatomy koroid ( Dutta M, 2013 )
Koroid terdiri terutama dari pembuluh darah yang dikelilingi oleh melanosit, saraf dan jaringan ikat. Koroid dapat dibagi menjadi beberapa lapisan secara histologis yang meliputi lamina suprachoroid, stroma, lamina choriocapilaris, dan membran Bruch. Lamina Suprachoroid (lamina fusca) terdiri dari serat kolagen, fibroblas dan melanosit. Lamina suprachoroid berada diatas ruang potensial antara sklera dan koroid dikenal sebagai ruang suprachoroidals. Ruang potensial ini berisi arteri siliaris posterior panjang dan saraf.
Tidak seperti jaringan iris, di mana stroma menempati bagian utama dari jaringan. Stroma choroidal jarang sebagai penyusun utama koroid yang terdiri dari choriocapillaries. Stroma choroidal adalah jaringan ikat longgar berpigmen yang mengandung beberapa unsur. Pembuluh darah dari koroid tersusun berlapis-lapis. Pembuluh yang lebih besar yang terletak di sisi luar dari lapisan medial yang disebut lapisan Hallers. Pembuluh lapisan cabang lapisan
ini memiliki struktur pembuluh berukuran sedang. Lapisan ini dikenal sebagai lapisan Sattler. Pembuluh darah akan berlanjut bercabangbmembentuk pembuluh yang lebih kecil dan kapiler. Venues dari koroid akan mengalir menuju pembuluh darah yang akhirnya mengalir ke empat vena vortex (satu dari masing-masing kuadran mata). Serat saraf merupakan unsur penyusun setelah pembuluh darah. Unsur selanjutnya yaitu sel Melanosit, fibrocytes, sel mast dan sel plasma adalah sel yang dominan ditemukan di stroma choroidal. Melanosit didistribusikan lebih di bagian luar dari lapisan dan dekat disc optik. Di antara sel-sel non berpigmen, fibroblas adalah yang sel paling umum dapat ditemukan. Jaringan ikat berupa kollagen fibril tersebar ke segala arah dan mengelilingi pembuluh darah.
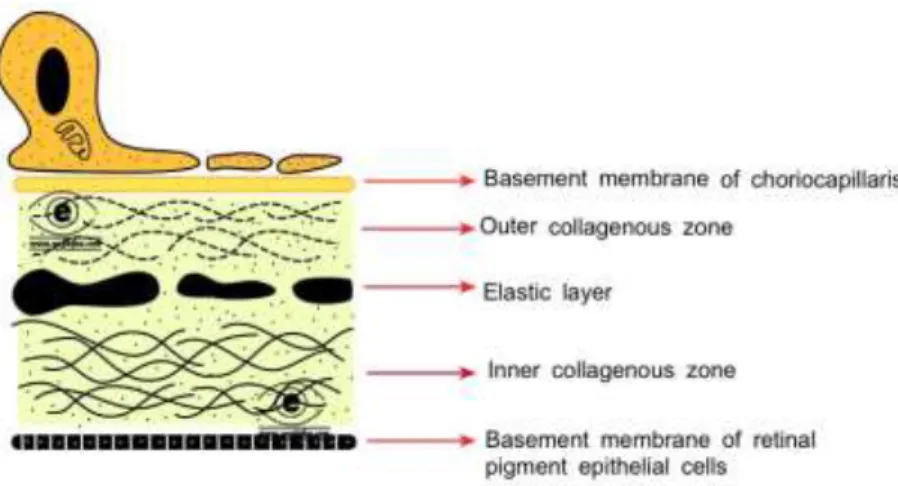
Lapisan selanjutnya penyusun koroid yaitu lapisan koriokapilaris. Lapisan ini adalah satu lapisan kapiler yang lebih besar dari kapiler normal tubuh kita. Diperkirakan bahwa lumen kapiler ini tiga sampai empat kali lebih besar dari kapiler normal. Dinding kapiler yang menyerupai lumen dan berisi pericytes. Koriokapilaris mengandung membran basal. Koriokapilaris yang tebal dan paling melimpah berada di daerah submacular. Studi menemukan bahwa choriocapillaries tersusun membentuk struktur lobular dimana feeding arteriol adalah di pusat vena drainase berada di pinggir. Lapisan terdalam dari koroid yaitu membran Bruch adalah lapisan terdalam dari koroid dan juga dikenal sebagai lamina vitrea. Membran Bruch memiliki bagian paling tebal di dekat disk optik (2-4 mikroM) dan ketebalan makin berkurang menuju pinggiran. Membran Bruch terdiri dari 5 lapisan dan dari internal ke eksternal, yang bila diurutkan adalah membran basal dari RPE, zona kolagen dalam, lapisan jaringan elastis, zona kolagen luar serta membran basal dari koriokapilaris.
. v
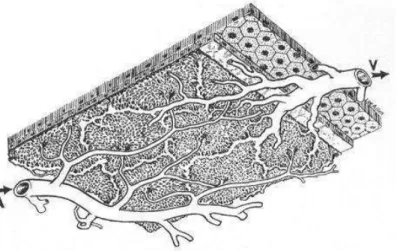
Koroid adalah bagian posterior uveal track dan merupakan pembuluh darah high flow yang terdiri dari arteri, vena, melanosit, dan choriocapillaris, serta jaringan ikat mendukung diselingi dengan sistem saraf. Chorio-capillaris memiliki bentuk lobular di pole posterior. 1 ° dari arteri koroid feeder pusat, awal arteriol prekapiler, masing-masing memasok tiap lobulus kriocapiller (Gambar 1-7). Arteriol memasuki lobulus bagian tengah, dan venula berada di tepi lobular, mendraniase ke dalam pembuluh darah koroid. Fluorescein dan ICG dye akan bocor di junction yang longgar pada pemeriksaan angiografi oleh karena koroid organ high flow asupan darah.
Gambar 4. Struktur lobular koroid. Arterioles memasuki bagian pusat tiap lobulus dan drainase vena di bagian tepi dari lobular ( Dutta M, 2013 )
Retina menerima darah dari dua sumber yaitu koriokapilaris yang berada tepat di luar membran Bruch yang menyuplai darah sepertiga luar retina termasuk lapisan pleksiform luar dan lapisan inti luar, fotoreseptor dan lapisan epitel pigmen retina, serta cabang dari arteri retina sentralis yang menyuplai darah dua pertiga dalam retina (AAO Staff, 2011-2012; Riordian-Eva P, 2004). Arteri retina sentralis merupakan cabang dari arteri opthalmica yang merupakan cabang utama dari arteri karotid interna. Arteri ini menyuplai darah untuk lapisan permukaan diskus optikus. Arteri retina sentralis selanjutnya akan menyuplai keempat kuadran retina. Pada 30 persen mata dan 50 persen orang, bagian dalam retina yang mengandung banyak fotoreseptor juga disuplai oleh arteri cilioretina yang merupakan percabangan dari sirkulasi siliar (AAO Staff, 2011-2012; Riordian-Eva P, 2004).
EMBRYOLOGI
Retina berasal dari 2 lapisan yang bertumpuk yaitu lapisan neural retina (inner surface) dan lapisan pigmen epitel retina (outer surface).Lapisan neural retina berkembang secara konsentris ,dimulai dari tengah area mangkuk optik dan melebar kearah perifer. Proses laminasi dari lapisan ini terjadi pada minggu 8-12 gestasi. Sel-sel ganglion ikut berdiferensiasi secara cepat memasuki trimester kedua. Vaskularisasi retina mengikuti pola konsentris yang sama dan mulai terjadi pada bulan ke 4 mencapai perifer pada bulan ke 9 kehamilan (AAO Staf, 2014-2015).
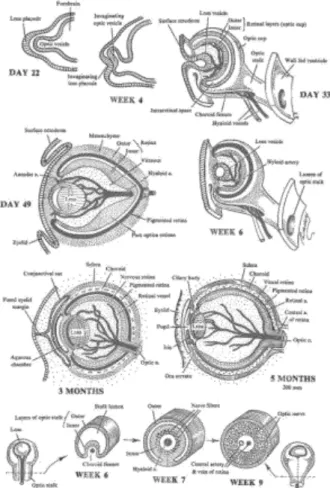
Koroid dan sclera merupakan lapisan yang berdekatan yang melapisi mata dan berfungsi dalam fungsi vaskularisasi serta proteksi. Organ tersebut terbentuk dari neural crest dan lapisan mesoderm dimana berasal dari lapisan mesenkim yang terkondensasi di sekitar optic cup dan lensa pada minggu ke- 5 dan 7 perkembangan bola mata primitif. Pembuluh darah pertama kali muncul di lapisan koroid mendekati minggu ke-15 dan pada minggu ke-23 arteri dan vena sudah dapat dibedakan. Proses induktif diperkirakan memainkan peran penting selama pembentukan koroid dan sclera, dengan RPE menginduksi diferensiasi mesenkim di sekitarnya dimana pada saat yang sama mesenkim berperan membentuk komponen penyusun RPE yaitu melanosit. Selain memiliki peran fungsional tersendiri, koroid dan sclera primitive juga merupakan komponen penyusun badan siliar dan kornea. Pada bola mata yang matang, koroid akan berlanjut menjadi badan siliar, sedangkan sclera berlanjut menjad kornea.
Gambar 5. Perkembangan koroid primitive ( Hill M, 2012 )
ETIOPATOGENESIS
Patogenesis dari PCV sampai saat ini masih kontroversial, satu study menyebutkan adanya mekanisme yang melibatkan CNV sedangkan study lain menyebutkan keterkaitan perkembangan dari abnormalitas vascular koroid ( Yuzawa M, Mori R, Kawamura A, 2010 ).
Patogenesis PCV masih belum bisa dipahami dengan jelas sampai saat ini. Tidak ditemukan kaitan yang jelas antara PCV dan penyakit sistemik yang berhubungan yang mana di masa lalu PCV diduga disebabkan oleh proses penyakit mikrovaskular seperti hipertensi dan diabetes. Study lain menunjukkan prevalensi penyakit mikrovaskuler sistemik setara antara populasi umum dan populasi subset dengan polypoidal CNV ( Ryan S, 2006 ).Koji dan rekan melaporkan subtype dari PCV dan mengkategorikan PCV sebagai polypoidal choroidal neovascularization (CNV) dan typical PCV. Tipe yang pertama mempunyai gambran baik pembuluh darah penyuplai dan penguras terlihat pada indocyanine green
angiography serta terdapat jaringan pembuluh darah yang banyak. Tipe yang kedua berlawanan dengan yang pertama, dimana tidak ada pembuluh penyuplai dan draining vessels yang bisa dideteksi pada pemeriksaan indocyanine green angiography serta jumlah jaringan pwnbuluh sangat sedikit. Okubo dan rekan juga melaporkan PCV dapat dikelompokkan menjadi 2 jenis, yaitu tipe kecil-pendek dan tipe besar-panjang dimana tipe yang kecil-pendek digambarkan sebagai lesi kecil dengan periode singkat gangguan penglihatan. Tipe besar-panjang digambarkan dengan lesi luas dan periode gangguan penglihatan lebih lama. Prognosis penglihatan dan kondisi klinis berbeda pada kedua tipe. Temuan histopatologis juga dilaporkan terdapat variasi kondisi PCV yaitu yang pertama yang terkait dengan abnormalitas vasculature dan yang kedua terkait dengan CNV (Tanaka K, 2011). Matsuoka dan rekan mengklasifikasikan PCV menjadi 3 tipe (Yuzawa et al. 2005). Tipe yang pertama merupakan PCV yang disebabkan adanya kelainan dari abnormalitas pembuluh darah inner koroid bukan dari CNV.Tipe yang kedua adalah tipe polypoidal yaitu perluasan lesi di bawah RPE, yang akhirnya membentuk lesi polypoidal pada pembuluh darah terminal. Tipe yang ketiga adalah radiation-associated choroidal vasculopathy, yang dianggap merupakan komplikasi dari radiasi (Spaide et al. 1999). Yuzawa dan rekan meyebutkan dengan demikian PCV dikasifikasikan menjadi beberapa tipe utama yaitu PCV karena abnormalitas pembuluh darah koroid dan PCV dengan polpoidal NCV dengan bantuan SD-OCT dalam menemukan perbedaan antara kedua tipe tersebut (Yuzawa 2012).
Para peneliti telah mengusulkan teori kemungkinan peran mediator biokimia vasogenesis, termasuk faktor pertumbuhan endotel vaskular (VEGF), yang mungkin bertanggung jawab atas neovaskularisasi seperti terlihat pada PCV. Berbagai laporan menunjukkan ekspresi yang kuat dari VEGF pada spesimen PCV dan juga peningkatan regulasi dalam aqueous humor di mata. Studi terbaru juga menyebutkan faktor pelengkap gen H memiliki peranan sebagai faktor yang memungkinkan PCV. Link genetik umum juga telah ditemukan antara PCV . Gotoh dan rekan menemukan varian genetik ARMS2 ( LOC387715 ) pada pasien Jepang dengan asosiasi yang kuat dengan PCV ( Yuzawa M, Mori R, Kawamura A, 2010 ).
Jaringan pembuluh darah abnormal pada PCV secara histopatologi biasanya berasal dari arteri posterior siliaris pendek serta percabangannya yang berkembang melalui defek pada membrane Bruch. Lokasi tepatnya dari jaringan pembuluh darah ini masih belum dapat diketahui secara jelas. Studi klinikopatologi melaporkan struktur bulat berdinding tipis ini
sebagai struktur sub-RPE, didalam jaringan fibrovaskular membrane Bruch. Okubo et al menyebutkan bahwa lesi ini dapat lebih tepat dianggap sebagai degenerasi membran-choriocapillaris kompleks RPE-Bruch dan pelebaran inner koroid venula dan arteriol, dari jaringan fibrovascular membrane intra-Bruch ( Yuzawa M, Mori R, Kawamura A, 2010 )
Studi pada pemeriksaan OCT menunjukkan bahwa lesi ini menyebabkan penonjolan tajam dari RPE seperti terlihat pada indocyanine green angiography dan pemeriksaan klinis. Lesi ini paling sering terletak di daerah peripapiler, disusul pada makula, dan dapat terjadi juga di fundus Lesi juga bisa tunggal dan terisolasi, atau meluas dan multiple.
Kondisi PCV umumnya dianggap sebagai penyakit bilateral karena banyak pasien yang memiliki lesi unilateral apda awalnya, kemudian berkembang menjadi bilateral seiring perkembangannya. Beberapa kasus di mana pasien telah diikuti selama lebih dari 10 tahun didapatkan tidak menunjukkan perkembangan kearah lesi bilateral ( Laudel A, Tan C, 2010 )
Dari pemeriksaan biomicroscopy dan oftalmoskopi menunjukkan kelainan vaskular PCV berada pada lapisan antara RPE dan membran Bruch, Uyama et al menyimpulkan bahwa pada pasien Jepang, PCV adalah variasi bentuk dari CNV. Uyama et al juga menggambarkan lesi disebut polypoidal CNV. Tateiwa et al mendeskripsikan varian pembuluh darah yang besar , meluas melewati arcade vaskular, di 20 % mata dalam kasus PCV pada studinya. Jaringan pembuluh darahl melebar dan menyebar secara radial. Sho dkk mencatat progresi penyakit yang lambat dari kelainan pembuluh darah dan sedikit proliferasi fibrovascular subretinal, menunjukkan PCV yang memiliki sedikit asosiasi dengan CNV klasik ( Uyama M, 2002 ).
Terasaki et al dari penelitiannya melaporkan bahwa spesimen menunjukkan pelebaran pada lapisa intra-Bruch, pembuluh berdinding tipis tanpa pericytes, yang terwarnai positif untuk faktor pertumbuhan endotel vaskular (VEGF) di sel endotel, menunjukkan itu adalah neovascular alami. Matsuoka et al menemukan ekspresi Faktor VEGF dan pigmen epitel yang diturunkan di kedua spesimen dari CNV and PCV, menunjukkan sifat neovascular dari kondisi terakhir. Nakajima et al melaporkan dua kasus PCV dengan terkait CNV saat diperiksa di bawah mikroskop cahaya. Okubo et al melaporkan pada pemeriksaan histopatologi spesimen, didapatkan aterosklerosis arteriole intra-choroidal, dengan disertai pelebaran venula, yang menunjukkan kompresi venular choroidal dan mungkin disebabkan oleh adanya stasis. Kuroiwa et al mengamati perubahan terutama dalam besar arteriol
choroidal, menunjukkan gangguan elastisitas lapisan dalam dinding pembuluh darah, dan deposisi basement membran ( seperti material kolagen pada dinding pembuluh ), menunjukkan bahwa aterosklerosis dari inner arteriol choroidal mungkin penting.
Nakashizuka et al melaporkan hialinisasi pembuluh darah koroid, diduga yang mendasari proses aterosklerosis pada PCV. Sasahara et al menemukan bahwa terjadi hiperpermeabilitas choroid, temuan umum pada kasus CSCR pada pemeriksaan indocyanine green angiography, yang terjadi pada 10% dari serangkaian kasus PCV. Walaupun PCV mungkin juga hadir pada kasus CSCR, hubungan kausatif antara hyperpermeabilitas pembuluh darah koroid, CSCR, dan PCV saat ini masih belum jelas ( Uyama M, 2002 ).
MANIFESTASI KLINIS
Pasien dengan PCV mungkin memiliki ketajaman penglihatan yang baik dan tidak menunjukkan gejala, namun sebagian besar pasien memiliki satu atau lebih gejala visual yang dapat termasuk penglihatan kabur atau redup, floaters serta skotoma sentral atau paracentral, distorsi penglihatan ( objek tampak bengkok dan bergelombang ), dan sudden loss vision di mata yang terkena .Sesuai dengan literatur, PCV ditandai dengan: (1) penonjolan berwarna jingga kemerahan di kutub posterior retina (atau kadang-kadang di retina perifer), dan / atau (2) lesi polypoidal ditemukan oleh angiography hijau indocyanine. Lesi polypoidal sayangnya tidak dapat ditemukan pada kondisi penyumbatan perdarahan atau kualitas gambar tidak cukup baik dalam beberapa kasus, yang membuat diagnosis PCV sulit. Kasus tersebut dapat diklasifikasikan sebagai 'suspek PCV', tetapi seringkali sangat sulit untuk membedakan kasus-kasus dari AMD ( Ryan S, 2006 ).
Lesi PCV biasanya muncul sebagai lesi berwarna kemerahan atau epitel pigment detachment (PED) yang tidak berwarna kemerahan dan kadang-kadang disertai dengan retinal detachment serosa (SRD), perdarahan subretinal, material fibrinous subretinal, hard eksudat dan drusens. Temuan funduskopi pada kunjungan awal dapat bervariasi tergantung saat pasien mengunjungi rumah sakit. Uyama dkk melaporkan bahwa sekitar 83% (10 dari 12 kasus) dari pasien PCV menunjukkan SRD pada kunjungan pertama, Sho dkk. melaporkan bahwa sekitar 52% dari pasien PCV menunjukkan SRD. Bessho dkk dalam laporan terbarunya telah mengamati SRD di 91% dari pasien, dan perdarahan subretinal di 62% dari pasien dengan PCV pada kunjungan pertama. Studi sebelumnya telah melaporkan bahwa lesi
polip sebagian besar hadir di margin dan di dalam PED serosanguinus, yang mungkin hadir sebagai “Notch Sign” antara PED, termasuk lesi polip dan PED yang terhubung, yang meliputi pembuluh jaringan yang abnormal. Kasus PED mungkin dapat ditemukan meluas sampai di kutub posterior retina, atau ditemukan lebih dari 2 lesi independen ( yaitu satu lesi pada makula dan yang lainnya di retina bagian nasal ).
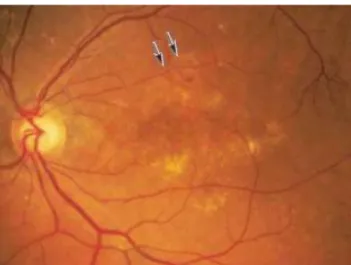
Gambar 5. Foto fundus pasien dengan PCV (A) Beberapa lesi berwarna oranye terlihat di area macula (panah). Perdarahan terlihat diantara lesi oranye dan diskus optikus (B) Penegakkan diagnosa PCV dikonfirmasi dengan indocyanine green
angiography (ICGA). Jaringan abnormal vascular koroid dan lesi polip yang khas
terlihat di makula, sesuai dengan gambaran lesi yang terlihat foto fundus berwarna ( Li M, 2010 )
Ketajaman visual di kunjungan awal dapat bervariasi tergantung pada tingkat perubahan eksudatif. Kasus-kasus tanpa perdarahan subretinal atau sedikit SRD memiliki VA yang baik, sedangkan VA dalam kasus-kasus dengan perubahan eksudatif parah mungkin akan lebih buruk. Pasien PCV umumnya memiliki VA yang lebih baik daripada di AMD pada awal pemeriksaan. Hal ini mungkin karena lesi PCV tetap berada di bawah RPE pada tahap awal, sementara AMD sesekali berkembang menjadi CNV dalam ruang subretinal ( yang disebut tipe 2 CNV), yang dapat mempengaruhi retina sensorik langsung ( Honda S, Matsumiya W, Negi A, 2013 )
Lesi karakteristik PCV disebutkan juga berupa jaringan abnormal aneurisma pembuluh darah koroid dalam yang mengarah ke luar, terlihat secara klinis sebagai struktur polypoidal berwarna oranye kemerahan. Lesi ini predominan berlokasi terutama di daerah
peripapiler dan makula. Lesi pada mid- perifer yang menimbulkan perdarahan subretinal juga telah dilaporkan baru-baru ini ( Peck L, Monique W, Gibson J, 2000 )
DIAGNOSIS
Fluoresensi Angiografi (FA) dan Optical Coherence Tomography (OCT) merupakan sarana penunjang pemeriksaan yang berguna mendiagnostik serta menyingkirkan diferensial diagnosis, dan juga indocyanine green angiography merupakan gold standard untuk penegakan diagnosis dari polypoidal choroidal vasculopati. Pemeriksaan OCT umumnya sering memperlihatkan PCV yang ditandai dengan gambaran PED, tinggi PED melebihi biasanya, dan edema intraretinal yang lebih ringan jika dibandingkan pasien dengan AMD eksudatif.
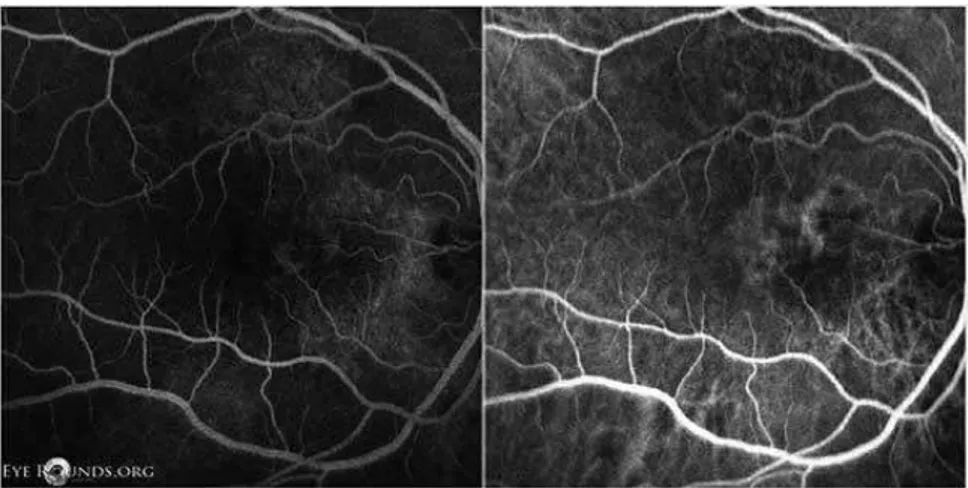
Gambar 6. OD FFA (kiri) dan indocyanine green angiography (kanan) menunjukkan lesi fluorescein punctate pada bagian temporal ke saraf optik di makula nasalis, sebagian besar merupakan lesi polifoid ( Ryan S, 2006 )
.
gambar 7. Struktur vaskular Polypoidal di bawah RPE dikelilingi oleh perdarahan kecil ( panah ) diamati di bagian superonasal ke fovea ( Ryan S, 2006 )
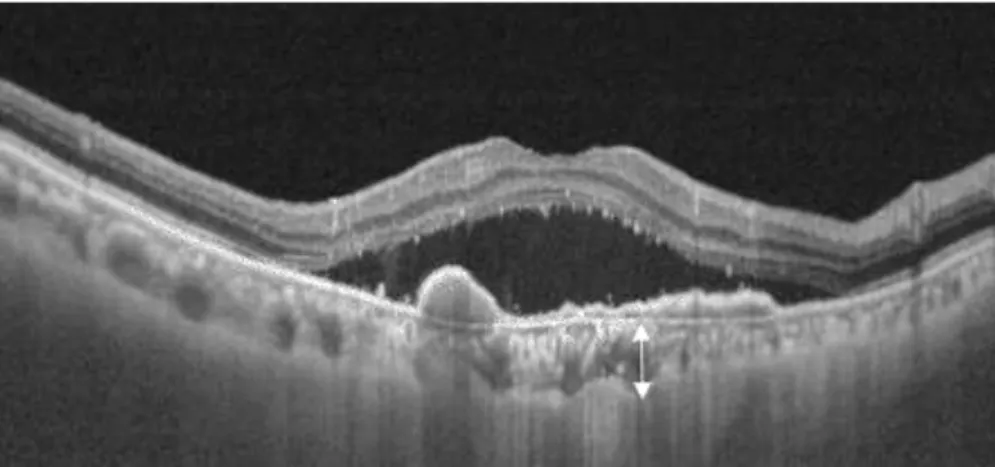
Gambar 8. Gambaran pemeriksaan OCT pada kasus PCV : Spectral
domain OCT menunjukkan peak like elevation pada RPE dengan
peninggian PED didasarnya (asterisk), kedudukan tomographic di lapisan PED ( panah putih ) dan double layer sign, yang terdiri dari 2 garis hiperreflektif ( kepala panah ) ( Wong C, 2015 )
Gambar 9. Gambaran pemeriksaan OCT pada kasus PCV : visualisasi penebalan koroid di dasar lesi PCV ( panah ) ( Wong C, 2015 )
Lesi PCV pada FA menyerupai lesi CNVM dan bila submacular, sering terkecoh dengan AMD. Oleh karena itu, indocyanine green angiography mampu memperlihatkan pembuluh darah choroidal yang mana merupakan standar untuk diagnosis lesi polypoidal. Pada indocyanine green angiography, jaringan percabangan dari PCV mudah dilihat. Polip terlihat sebagai tempat lesi hiperfloresensi local. Stadium lanju dapat menunjukkan pola pewarnaan terbalik dengan stadium awal, yaitu terlihat dengan pusat lesi menjadi hypofluorescent dan sekitarnya menjadi hyperfluorescent. Fenomena "wash-out" dari lesi yang terlihat pada lesi PCV tidak bocor pewarna bisa terlihat pada tahap akhir. OCT tidak hanya membantu dalam identifikasi cairan subretinal atau sub-RPE, juga dapat menggambarkan lesi polypoidal. Lesi ini menyerupai ketinggian kubah-seperti dari RPE dengan reflektifitas internal yang moderat. Garis yang sangat reflektif di bawah lesi ini terdiri dari lokasi jaringan percabangan pembuluh darah juga bisa ditemukan dalam kebanyakan kasus. Lapisan ganda yang terlihat tersebut juga disebut "double-layer sign," dan terlihat pada 59% dari mata dengan PCV ( Vinay A, Leo K, 2015 ).
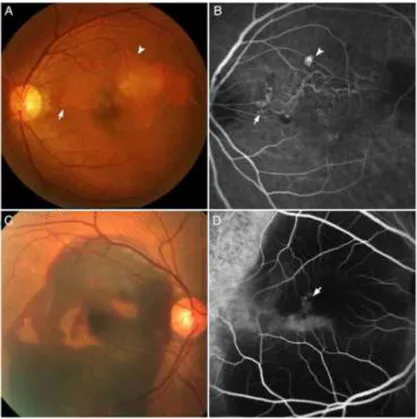
Gambar 10. Gambaran PCV yang terlihat pada indocyanine green angiography dan Fundus fotografi warna (A) Fundus Warna menunjukkan nodul oranye subretinal (panah) dan pigmen epitel detachment (kepala panah). (B) indocyanine green
angiography dari mata yang sama menunjukkan bagian nodul hyperfluorescence
(panah), muncul dalam 5 menit pertama, dengan halo dari hypofluorescence sekitar nodul ( kepala panah). Sebuah percabangan jaringan pembuluh darah (BVN) terlihat di superior fovea, mensuplai polip yang terletak di pinggiran BVN (C) Foto fundus warna yang menunjukkan besar perdarahan submacular di posterior pole. (D) indocyanine green angiography menunjukkan daerah dari hyperfluorescence (panah) yang sesuai dengan polip. Tidak ada BVN yang terlihat pada angiogram ini ( Colin S, Wei K, Jian P, Nikolle W, Tock H, 2014 )
DIAGNOSIS BANDING
Diagnosis banding meliputi penyakit lain yang dapat menyebabkan neovaskularisasi subretinal. Riwayat dan presentasi klinis akan membedakan PCV dari penyakit lain, diantaranya berkaitan dengan AMD (tipe 1 atau tipe 2), chorioretinopathy serosa sentral ( Vinay A, Leo K, 2015 ). Pemeriksaan OCT spectral-domain menunjukkan gambaran cystoid macular edema, deposit lipid, subretinal hemorrhage, and hemorrhagic pigment epithelial
detachment lebih banyak terlihat pada pasien PCV dibandingkan CSCR, sehingga pemeriksaan ini sangatlah membantu dalam penegakan diagnosis polypoidal choroidal vasculopati. Pemeriksaan pada kasus AMD biasanya menunjukkan frekuensi PED yang lebih jarang jika dibandingkan dengan PCV ( Ladas ID, 2004 ).
Diferensial diagnosis PCV mencakup spektrum proses penyakit yang melibatkan CNV, dan eksudatif serta hemoragik retinopati. Misdiagnosis paling umum dari PCV adalah AMD dengan melihat banyak kesamaan klinis yang ada. Maruko dan rekan melaporkan tingkat prevalensi 54% untuk PCV di mata pasien Jepang yang sebelumnya didiagnosis dengan AMD. Ahuja dan rekan menemukan bahwa di mata yang diwujudkan hemoragik besar dan eksudatif retina neurosensorik dan RPE detasemen lebih besar dari 2 mm dengan diameter dan dengan tidak adanya drusen konsisten dengan polypoidal choroidal vasculopati, semua kasus yang dikonfirmasi PCV dengan pemeriksaan indocyanine green angiography.
Diferensial diagnosa lainnya dapat dipertimbangkan myopia patologis dengan neovaskularisasi serta melanoma. Beberapa pasien dengan PCV hadir dengan eksudasi lebih dominan merupakan serosa, menyerupai chorioretinopathy serosa sentral ( Audrey C, Carlo J, 2010 ).
PENATALAKSANAAN
Sebuah multicenter randomized controlled trial berjudul "EVEREST" menunjukkan bahwa pengobatan PCV dengan kombinasi verteporfin terapi photodynamic ( PDT ) ditambah suntikan ranibizumab yang ditoleransi dengan baik dan sangat efektif dalam mencapai regresi lengkap dari lesi polypoidal pada kasus PCV ( Matthew F, Eric K, James C, 2014 ).
Hasil riset menunjukkan keefektifan terapi dengan Verteporfin untuk polypoidal choroidal vasculopati. Clinical trial lain menunjukkan injeksi intravitreal agen anti-VEGF mampu menstabilkan ketajaman penglihatan dan edema macula serta mencapai regresi polip polypoidal choroidal vasculopati. Pendekatan terapi kombinasi juga telah dicoba seperti pada EVEREST trial ( Boughton,2010 )
Kombinasi PDT ditambah ranibizumab 0,5 mg injeksi yang diberikan 3x dengan interval 1 bulan secara khusus menunjukkan regresi polypoid lengkap dalam 77,8% dari pasien dibandingkan 71,4% untuk PDT monoterapi dan 28,6% untuk ranibizumab monoterapi. Hasil visual jangka panjang terapi kombinasi menunjukkan bahwa 88,2% pasien
dengan polypoidal choroidal vasculopati, ketajaman penglihatannya dapat dipertahankan atau ditingkatkan sampai 3 tahun setelah pengobatan pada studi lain. Pasien dengan regresi polip yang tidak sempurna setelah pengobatan kombinasi awal yang dinilai oleh ICG pada 3 bulan follow-up, dianjurkan melanjutkan terapi dengan PDT monoterapi atau kombinasi PDT / ranibizumab. Kebocoran yang masih terdeteksi dengan FFA atau indocyanine green angiography dan disertai gejala yang masih aktif, pemberian ranibizumab monoterapi merupakan pilihan yang tepat. Monoterapi ranibizumab meskipun efektif dalam mengurangi cairan subretinal, namun masih kurang efektif dalam mencapai regresi polip. Monoterapi intravitreal dapat dipilih dibanding terapi kombinasi PDT / ranibizumab pada pasien yang memiliki ketajaman visual yang baik, atau yang memiliki kontraindikasi untuk PDT (misalnya tes fungsi hati yang abnormal). Belum ada bukti yang cukup untuk mendukung penggunaan kortikosteroid dalam PCV ( Matthew F, Eric K, James C, 2014 ).
Dalam studi non-randomized comparative yang dilakukan Kwok et al pada kasus PCV dengan pemberian terapi laser fotokoagulasi termal untuk polip, diapatkan hasil ketajaman penglihatan yang lebih baik dibandingkan dengan kasus yang tidak diberi terapi laser fotokoagulasi termal, meskipun perbedaan itu tidak signifikan secara statistik. Vilaplana et al, melaporkan hasil visual yang buruk dalam serangkaian kecil kasus.
KESIMPULAN
Pemahaman PCV sebagai suatu diagnosa penyakit telah mengalami evolusi yang cepat dalam tiga dekade terakhir meskipun dapat dibedakan oleh fitur khusus di indocyanine green angiography, pemahaman saat ini penyakit tersebut masih menunjukkan kerancuan dengan CSR atau AMD eksudatif. Presentasi klinis PCV sering mirip dengan CSR atau eksudatif AMD. Diagnosa PCV agaknya sulit ditegakkan tanpa bantuan pencitraan indocyanine green angiography. Indocyanine green angiography harus dipertimbangkan pada pasien yang memiliki terlihat tanda bintil oranye-merah subretinal, perdarahan spontan subretinal besar atau PED hemoragik, atau kurangnya respon terhadap therapy anti-VEGF. Kasus dengan kondisi demikian, kegagalan respon untuk berbagai perawatan standar untuk CSR yang pada akhirnya membutuhkan pencitraan ICG dan mengarah pada diagnosis polypoidal choroidal vasculopati. Terapi sampai saat ini masih dipercayakan pada kombinasi agen VEGF dan PDT. Untuk pasien dengan VA yang cukup baik, pemberian terapi ranibizumab monoterapi
dan dilanjutkan dengan PDT jika tidak ada perbaikan kondisi cairan subretinal atau terdapat penurunan tajam penglihatan.
DAFTAR PUSTAKA
Adrian H, Greg T, Richard F. 2012. Update on Polypoidal Choroidal Vasculopathy. Diunduh dari http://www.aao.org/assets/december-2012-clinical-update-retina-pdf.
Ahuja R, Stanga P, Vingerling J, Reck A, Bird A. 2000. Polypoidal choroidal vasculopathy in exudative and haemorrhagic pigment epithelial detachments. Br J Ophthalmol 2000;84:479–484
Amaro M, Roller A, Motta C, Motta M. 2011. Polypoidal choroidal vasculopathy causing cystoid macular edema and the response to ranibizumb intravitreal treatment. Rev Bras Oftalmol ; 70 (4): 252-6
American Academy of Ophthalmology Staf a. 2014-2015. Retina and Vitreous. Basic and Clinical Science Course. Sec.12. San Francisco: AAO, p. 7-11.
American Academy of Opthalmology, Staff. 2011-2012. Fundamentals and Principles of Opthalmology. In: Basic and Clinical Science Course. Sec. 2. San Francisco : AAO ; p. 291-302.
Anantharaman G, Ramkumar G, Gopalakrishnan M, Rajput A. 2010. Clinical features, management and visual outcome of polypoidal choroidal vasculopathy in Indian patients. Indian J Ophthalmol ;58:399-405
Audrey C dan Carlo J. Pelino. Polypoidal Choroidal Vasculopathy: A Retinal Masquerader. 2010. Diunduh dari: http://www.reviewofoptometry.com/content/c/19392
Chee W, Tien Y dan Chui M. 2015. Polypoidal Choroidal Vasculopathy in Asians J. Clin. Med ; 4: 782-821.
Coppens G, Spielberg L, Leys A. 2011. General Review Polypoidal Choroidal Vasculopathy Diagnosis and Management. Belge Ophtalmol ; 317: 39-44.
Hwang D, Yang C, Lee F, Hsu S. 2005. Idiopathic Polypoidal Choroidal Vasculopathy. J Chin Med Assoc ; 70 : 84-88
Honda S, Matsumiya W, Negi A. 2013. Polypoidal Choroidal Vasculopathy: Clinical Features and Genetic Predisposition. Ophthalmologica ;231:59–74
Lim T, Laude A, Tan C. 2009. Polypoidal choroidal vasculopathy: an angiographic discussion. Cambridge Ophthalmology Symposium. Diunduh dari ttttp://www.nature.com/eye/journal/v24/
Mori F dan Shuichiro E. 2012. Polypoidal choroidal vasculopathy. Br J Ophthalmol ;91:1104–1105.
Peck L, Monique W. Jonathan M, Gibson. 2000. Idiopathic polypoidal choroidal vasculopathy: a disease with diverse clinical spectrum and systemic associations. Diunduh dari http://www.nature.com/eye/journal/v14/n5/abs/eye2000186a.html
Ryan S.J. 2006.Retina Volume I : Basic science and inherited Retinal disease. Elsevier Mosby ; 956-957
Vinay A dan Leo A. 2001. Polypoidal Choroidal Vasculopathy. Br J Ophthalmol;86:696–701
Yuzawa M, Mori R, Kawamura A. 2010. The origins of polypoidal choroidal vasculopathy. Br J Ophthalmol ;89:602–607