ZYMOMONAS MOBILIS
DISUSUN OLEH :
MOHAMMAD YATIM 0831010011
JURUSAN TEKNIK KIMIA FAKULTAS TEKNOLOGI INDUSTRI
UNIVERSITAS PEMBANGUNAN NASIONAL ”VETERAN” JAWA TIMUR SURABAYA
SKRIPSI
PEMANFAATAN LIMBAH KULIT KOPI MENJADI BIOETANOL DENGAN PROSES FERMENTASI MENGGUNAKAN BAKTERI
ZYMOMONAS MOBILIS
Oleh :
MOHAMMAD YATIM 0831010011
Telah Diterima dan Disetujui Untuk Diseminarkan
Mengetahui, Dosen Pembimbing
KATA PENGANTAR
Dengan mengucapkan puji syukur kehadirat Allah SWT yang telah
melimpahkan karunia beserta rahmat-Nya kepada kita semua, sehingga kami
diberikan kekuatan dan kelancaran dalam menyelesaikan laporan penelitian kami
yang berjudul “Pemanfaatan Limbah Kulit Kopi menjadi Bioetanol dengan Proses
Fermentasi menggunakan Bakteri Zymomonas Mobilis”.
Adapun penyusunan penelitian ini merupakan salah satu syarat yang harus
ditempuh dalam kurikulum program studi S-1 Teknik Kimia dan untuk
memperoleh gelar Sarjana Teknik Kimia di Fakultas Teknologi Industri UPN
“Veteran” Jawa Timur, Surabaya.
Laporan penelitian yang kami dapatkan tersusun atas kerjasama dan berkat
bantuan dari berbagai pihak. Oleh karena itu pada kesempatan ini kami
mengucapkan terima kasih kepada:
1. Bapak Ir. Sutiyono, MT selaku Dekan Fakultas Teknologi Industri UPN
“Veteran” Jawa Timur.
2. Ibu Ir. Retno Dewati, MT selaku Ketua Jurusan Teknik Kimia UPN
“Veteran” Jawa Timur.
3. Ibu Nana Dyah Siswati, MKes selaku Dosen Pembimbing Penelitian.
4. Ibu Ir. Lucky Indrati. U, MT selaku Dosen penguji Penelitian.
5. Ibu Ir. Suprihatin, MT selaku Dosen penguji Penelitian.
6. Kedua orang tua yang telah memberikan dukungan moril dan material
dalam pelaksanaan dan penyusunan laporan penelitian.
7. Seluruh teman-teman yang telah memberikan dorongan semangat dalam
Akhir kata, kami menyampaikan maaf atas kesalahan yang terdapat dalam
laporan penelitian ini, semoga dapat memenuhi syarat akademis dan bermanfaat
bagi kita semua. Kritik dan saran yang bersifat membangun demi perbaikan
penyusun berikutnya, penyusun mengucapkan terima kasih.
Surabaya, Agustus 2011
DAFTAR ISI
BAB II TINJAUAN PUSTAKA 2.1. Kopi...4
2.2. Limbah Kulit Kopi...5
2.3. Sellulosa...7
BAB III METODOLOGI PENELITIAN 3.1 Bahan- bahan yang digunakan...16
3.2. Alat-alat yang digunakan...16
3.3. Gambar susunan Alat...17
3.4. Variabel...19
3.3. Prosedur penelitian...19
BAB IV HASIL DAN PEMBAHASAN
4.1. Hasil...34
4.2. Pembahasan...38
BAB V KESIMPULAN DAN SARAN 5.1.Kesimpulan...43
5.2. Saran...44
DAFTAR PUSTAKA...45
APPENDIKS...48
hanya biji kopi. Pada proses pengolahan kopi akan menghasilkan 35% limbah
kulit kopi yang merupakan sumber bahan organic berkadar selulosa cukup tinggi
dan tersedia melimpah di Indonesia, sehingga limbah kulit kopi dapat
dimanfaatkan menjadi bioetanol. Sebagai energy alternative pengganti BBM,
bioetanol memiliki kelebihan dibanding dengan BBM, diantaranya memiliki
kandungan oksigen yang lebih tinggi (35%) sehingga terbakar lebih sempurna,
bernilai oktan lebih tinggi (118) dan lebih ramah lingkungan karena mengandung
emisi gas CO lebih rendah 19–25 % (Indartono Y., 2005). Proses pembuatan
bioetanol dilakukan dengan menghidrolisis kulit kopi menjadi glukosa
menggunakan katalis H2SO4 (10, 20, 30 % v/v) dan HCl (10, 20, 30 % v/v). Selanjutnya glukosa difermentasi menjadi bioetanol menggunakan bakteri
Zymomonas Mobilis. Dengan variabel waktu Fermentasi (2, 3, 4, 5, 6, 7, 8 hari),
dan konsentrasi starter Zymomonas mobilis ( 9, 10, 11 % v/v). Penelitian
menunjukkan bahwa kulit kopi dapat digunakan sebagai bahan baku alternative
pembuatan bioetanol dengan proses hidrolisis dan fermentasi, hasil terbaik
diperoleh pada konsentrasi starter 11 %, waktu fermentasi 7 hari menghasilkan
BAB I
PENDAHULUAN
1.1. Latar Belakang
Seiring dengan peningkatan jumlah penduduk dunia, kebutuhan akan
energi semakin hari semakin meningkat. Sementara itu sumber daya alam yang
dapat menghasilkan energi selama ini semakin terkuras. Hal inilah yang
mendorong berbagai negara berusaha keras untuk mengadakan efisiensi dan
penghematan energi serta mencari sumber energi baru sebagai energi alternatif.
Salah satu teknologi yang berpeluang dikembangkan untuk mendukung
pengadaan energi adalah produksi bioetanol. Bioetanol memiliki kelebihan
dibanding dengan BBM, diantaranya memiliki kandungan oksigen yang lebih
tinggi (35%) sehingga terbakar lebih sempurna, bernilai oktan lebih tinggi (118)
dan lebih ramah lingkungan karena mengandung emisi gas CO lebih rendah
19–25% (Indartono Y., 2005). Selain itu bioetanol dapat diproduksi oleh
mikroorganisme secara terus menerus. Produksi bioetanol di berbagai negara telah
dilakukan dengan menggunakan bahan baku yang berasal dari hasil pertanian dan
perkebunan (Sarjoko, 1991). Oleh karena itu dilakukan upaya mencari bahan baku
alternatif lain dari sektor non pangan untuk pembuatan etanol. Bahan selulosa
memiliki potensi sebagai bahan baku alternatif pembuatan etanol. Salah satu
contohnya adalah limbah kulit kopi.
Limbah kopi dibedakan menjadi dua macam, yaitu limbah pada
pengolahan kopi merah (masak) dan limbah pengolahan kopi hijau (mentah).
Pengolahan kopi merah diawali dengan pencucian, perendaman, dan pengupasan
kulit luar. Proses ini akan menghasilkan 65% biji kopi dan 35% limbah kulit
kopi.
Limbah kulit kopi merupakan sumber bahan organik yang tersedia cukup
melimpah di sentra produksi kopi. Areal perkebunan kopi di Indonesia mencapai
lebih dari 1,291 juta hektar dimana 96% diantaranya adalah areal perkebunan kopi
bahwa pada tahun 2009 produksi kopi Indonesia mencapai total 689 ribu ton.
Produksi kopi robusta mencapai 81% dari total produksi (sekitar 557 ribu ton) dan
19% untuk produksi kopi Arabika (sekitar 131 ribu ton).
Limbah Kulit kopi selama ini tidak mengalami pemrosesan di pabrik
karena yang digunakan hanya biji kopi yang kemudian dijadikan bubuk kopi
instan (Baon, 2005). Namun saat ini kulit kopi sudah dapat dimanfaatkan oleh
penduduk setempat. Kulit cangkang kopi atau yang disebut Parchment (hull,
endocarp) digunakan untuk pakan ternak dan kulit buah kopi dibiarkan
menumpuk disekitar area perkebunan hingga menjadi pupuk kompos. Limbah
kulit kopi. Dengan adanya kandungan serat kasar tersebut memungkinkan untuk
dimanfaatkan sebagai bahan baku untuk produksi bioetanol.
Bioetanol yang dibuat dari limbah kulit kopi dilakukan dengan
menghidrolisis menjadi glukosa dengan menggunakan asam, kemudian
dilanjutkan dengan proses fermentasi. Ada berbagai macam jenis mikroorganisme
yang dipakai untuk memproduksi bioetanol, salah satu mikrooganisme yang
paling banyak digunakan di perusahaan bioetanol di dunia adalah Zymomonas
Mobilis. Bakteri ini memiliki kemampuan yang dapat melampaui Saccharomices
cerevisiae, kelebihan bakteri ini antara lain dapat tumbuh secara anaerob fakultatif
dan mempunyai toleransi suhu yang tinggi, mempunyai kemampuan untuk
mencapai konversi yang lebih tinggi, tahan terhadap kadar etanol yang tinggi dan
pH yang rendah. Banyak para peneliti yang telah membuktikan kemampuan
bakteri ini dan hasilnya sangat luar biasa, bakteri ini mampu menghasilkan yield
etanol 92% dari nilai teoritisnya (Gunasekaran et al, 1999).
1.2. Tujuan Penelitian
Tujuan dari penelitian ini adalah untuk mencari jenis katalis untuk proses
hidrolisis, konsentrasi starter dan waktu fermentasi yang terbaik dalam proses
1.3. Manfaat Penelitian
Manfaat yang diharapkan dari penelitian ini antara lain :
1. Mengurangi banyaknya limbah kulit kopi.
2. Memberikan nilai tambah dari limbah padat kopi dengan menjadikan sebagai
bahan baku alternatif untuk pembuatan bioetanol.
3. Memberi informasi tentang teknologi fermentasi bioetanol dari limbah kulit
BAB II
TINJAUAN PUSTAKA
2.1. Kopi
Kopi (Coffea sp.) adalah kelompok tumbuhan berbunga dari genus Coffea yang bijinya diolah menjadi minuman berkafein. Anggota suku Rubiacceae ini
tersebar di berbagai negara seperti Brazil, Kolombia, Ethiopia, Uganda, India dan
Indonesia. Perkebunan kopi di Indonesia umumnya terdapat di Pulau Jawa,
terutama Jawa Tengah dan Jawa Timur serta Pulau Sumatra. Untuk pertumbuhan
yang optimum kopi sebaiknya ditanam pada daerah dengan ketinggian sekitar
300 - 1700 m di atas permukaan laut, temperatur sekitar 16 – 26 oC dan curah
hujan sekitar 1500 – 2000 mm per tahun.
Tiga spesies kopi yang banyak dibudidayakan karena memiliki nilai
ekonomi yang tinggi adalah kopi arabika (Coffea Arabica), kopi robusta (Coffea
canephora var Robusta) dan kopi Liberia (Coffea liberica).
Gambar 1. Buah Kopi
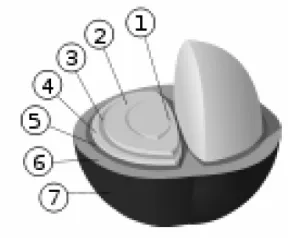
Gambar 2. Struktur Lapisan Penyusun Buah Kopi (Anonim, 2008)
Keterangan Gambar 2 :
1. Inti biji
2. Biji (endosperm)
3. Silver skin (testa, epidermis)
4. Parchment (hull, endocarp)
5. Lapisan pektin
6. Kulit (mesocarp)
7. Kulit terluar (pericarp, exocarp)
2.2. Limbah Kulit Kopi
Limbah kopi dibedakan menjadi dua macam, yaitu limbah pada
pengolahan kopi merah (masak) dan limbah pengolahan kopi hijau (mentah). Pada
suatu proses Pengolahan kopi akan menghasilkan 65% biji kopi dan 35% limbah
kulit kopi. Limbah Kulit kopi selama ini tidak mengalami pemrosesan di pabrik
karena yang digunakan hanya biji kopi yang kemudian dijadikan bubuk kopi
instan (Baon, 2005). Namun saat ini kulit kopi sudah dapat dimanfaatkan oleh
penduduk setempat. Kulit cangkang kopi atau yang disebut Parchment (hull,
endocarp) digunakan untuk pakan ternak dan kulit buah kopi dibiarkan
Berikut ini adalah gambar limbah kulit kopi merah dibiarkan menumpuk di
sekitar area produksi kopi.
Gambar 3. Limbah Kulit Kopi
Kandungan zat nutrisi yang terdapat pada kulit kopi, seperti dapat kita
lihat pada Tabel 1.
Tabel 1. Kandungan Zat Nutrisi Pada Kulit Kopi.
No. Zat nutrisi prosentase (%)
1 Komposisi dari buah 6
2 Bahan kering 94,3
3 Energi bruto (Mj/kg) 18,76
4 Protein kasar 4,61
5 Lemak 0,46
6 Serat kasar 65,2
7 Abu 2,2
8 Kalsium 0,34
9 Phosphor 0,01
10 Kecernaan protein 51,43
2.3. Selulosa
Selulosa (C6H10O5)n adalah polimer berantai panjang polisakarida
karbohidrat, dari beta-glukosa. Selulosa berfungsi sebagai bahan struktur dalam
jaringan tumbuhan dalam bentuk campuran polimer homolog dan biasanya
disertai polosakarida lain dan lignin dalam jumlah yang beragam. Molekul
selulosa memanjang dan kaku, meskipun dalam larutan. Gugus hidroksil yang
menonjol dari rantai dapat membentuk ikatan hidrogen dengan mudah,
mengakibatkan kekristalan dalam batas tertentu. Derajat kekristalan yang tinggi
menyebabkan modulus kekenyalan sangat meningkat dan daya regang serat
selulosa menjadi lebih besar dan mengakibatkan makanan yang mengangung
selulosa lebih liat (John,1997). Selulosa yang merupakan polisakarida terbanyak
di bumi dapat diubah menjadi glukosa dengan cara hidrolisis asam
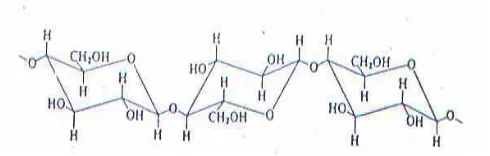
(Groggins,1958). Adapun rumus bangun selulosa dapat dilihat pada Gambar 4.
Gambar 4. Rumus Bangun Selulosa
2.4. Bioetanol
Bioetanol merupakan cairan hasil proses fermentasi gula dari polisakarida
menggunakan bantuan mikroorganisme. Bioetanol dapat dibuat dari berbagai
bahan hasil pertanian. Secara umum bahan - bahannya dapat dibagi dalam 3
golongan yaitu :
1. Bahan yang mengandung turunan gula (sakarin) : molase, gula tebu, gula bit,
sari buah.
2. Bahan yang mengandung pati : biji - bijian, kentang, tapioka.
3. Bahan yang mengandung selulosa : kayu, dan beberapa limbah pertanian
Bahan - bahan yang mengandung sakarin dapat langsung di fermentasi,
akan tetapi bahan yang mengandung pati dan selulosa harus dihidrolisis terlebih
dahulu menjadi komponen yang sederhana. Meskipun pada dasarnya fermentasi
dapat langsung menggunakan enzim tetapi saat ini industri fermentasi masih
memanfaatkan mikroorganisme karena cara ini jauh lebih mudah dan murah,
mikroba yang banyak digunakan dalam proses fermentasi adalah khamir, kapang
dan bakteri (Agus Krisno, 2002).
2.5. Hidrolisis
Hidrolisis merupakan proses pemecahan suatu senyawa menjadi senyawa
yang lebih sederhana dengan bantuan molekul air. (Kirck Othmer, 1967).
Menurut Groggins (1958), jenis hidrolisis ada lima macam yaitu sebagai
berikut :
1. Hidrolisis murni
Pada proses ini hanya melibatkan air saja. Proses ini tidak dapat
menghidrolisis secara efektif karena reaksi berjalan lambat. Hidrolisis murni
ini biasanya hanya untuk senyawa yang sangat reaktif dan reaksinya dapat
dipercepat dengan memakai uap air.
2. Hidrolisis dengan larutan asam
Menggunakan larutan asam sebagai katalis. Larutan asam yang
digunakan dapat encer atau pekat, seperti H2SO4 atau HCl.
3. Hidrolisis larutan basa
Menggunakan larutan basa encer maupun pekat sebagai katalis. Basa
yang digunakan pada umumnya adalah NaOH atau KOH. Selain berfungsi
sebagai katalis, larutan basa pada proses hidrolisis berfungsi untuk mengikat
asam sehingga kesetimbangan akan bergeser ke kanan.
4. Alkali fusion
Hidrolisis ini dilakukan tanpa menggunakan air pada suhu tinggi,
5. Hidrolisis dengan enzym
Hidrolisis ini dilakukan dengan mengunakan enzym sebagai katalis. Enzym
yang digunakan dihasilkan dari mikroba seperti enzym α-amylase yang dipakai
untuk hidrolisis pati menjadi glukosa dan maltosa.
Hidrolisis asam adalah hidrolisis dengan mengunakan asam yang dapat
mengubah polisakarida (pati, selulosa) menjadi gula. Dalam hidrolisis asam
biasanya digunakan asam chlorida (HCl) atau asam sulfat (H2SO4) dengan kadar
tertentu. Hidrolisis ini biasanya dilakukan dalam tangki khusus yang terbuat dari
baja tahan karat atau tembaga yang dihubungkan dengan pipa saluran pemanas
dan pipa saluran udara untuk mengatur tekanan dalam udara (Soebijanto, 1986).
Reaksi hidrolisis secara kimia dapat dilakukan dengan menggunakan asam
encer maupun asam pekat. Penggunaan asam encer pada proses hidrolisis
dilakukan pada temperatur dan tekanan tinggi dengan waktu reaksi yang singkat
(beberapa menit). Temperatur yang dibutuhkan adalah mencapai 200oC. Asam
encer yang digunakan adalah 0,2 - 4% berat (Nguyen and Tucker, 2002).
Penggunaan asam encer untuk menghidrolisis selulosa biasa mampu mencapai
konversi reaksi sampai 50% (Badger, 2002). Konversi yang rendah ini disebabkan
oleh degradasi gula hasil hidrolisis yang terbentuk karena temperatur reaksi yang
digunakan tinggi. Proses hidrolisis menggunakan asam encer terdiri dari dua
tahap. Tahap pertama adalah konversi bahan berselulosa menjadi gula sederhana
dan tahap kedua adalah degradasi gula sederhana yang terbentuk menjadi struktur
kimia yang lain. Degradasi gula tersebut tidak hanya menurunkan konversi reaksi,
namun juga dapat meracuni mikroorganisme pada saat reaksi fermentasi pada
pembentukan etanol.
Selain asam encer, proses hidrolisis juga dapat dilakukan dengan
menggunakan asam pekat. Penggunaan asam pekat pada proses hidrolisis selulosa
dilakukan pada temperatur yang lebih rendah daripada asam encer. Konsentrasi
asam yang digunakan adalah 10 - 30% (Zimbardi et.al). Sumber asam yang biasa
digunakan adalah asam sulfat. Temperatur reaksi adalah 100oC dan membutuhkan
degradasi gula. Keuntungan dari penggunaan asam pekat ini adalah konversi gula
yang dihasilkan tinggi, yaitu bisa mencapai konversi 90% (Badger, 2002).
2.6. Fermentasi
Fermentasi adalah proses produksi energi dalam sel dalam keadaan
anaerobik (tanpa oksigen). Secara umum, fermentasi adalah salah satu bentuk
respirasi anaerobik, akan tetapi terdapat definisi yang lebih jelas yang
mendefinisikan fermentasi sebagai respirasi dalam lingkungan anaerobik dengan
tanpa elektron eksternal (Dirmanto,2006).
Prinsipnya reaksi proses pembentukan etanol dengan fermentasi sebagai
berikut :
……(1)
Faktor - faktor yang mempengaruhi dalam proses fermentasi antara lain
sebagai berikut :
1. Nutrien
Unsur-unsur dasar untuk suplai zat gizi mikroba adalah karbon,
nitrogen, hidrogen, oksigen, sulfur, fosfor, magnesium, zat besi dan sejumlah
kecil logam lainnya. Karbon dan sumber energi untuk hampir semua bakteri
yang berhubungan dengan bahan pangan, dapat diperoleh dari jenis gula
karbohidrat sederhana seperti glukosa. Tergantung dari spesiesnya, kebutuhan
nitrogen dapat diperoleh dari sumber-sumber anorganik seperti (NH4)2SO4
atau NaNO3 atau sumber-sumber organik seperti asam amino dan protein.
Molekul-molekul kompleks dari zat-zat organik seperti polisakarida, lemak
dan protein harus dipecahkan terlebih dahulu menjadi unit yang lebih
sederhana sebelum zat tersebut dapat masuk ke dalam sel dan dipergunakan.
Pemecahan awal ini dapat terjadi akibat ekskresi enzim ekstraseluler – suatu
sifat yang sangat erat hubungannya dengan pembusukan bahan pangan. C6H12O6 2 C2H5OH + 2CO2
2. Suhu
Suhu adalah salah satu faktor lingkungan terpenting yang
mempengaruhi kehidupan dan pertumbuhan organisme. Beberapa
mikroorganisme dapat tumbuh pada kisaran suhu yang luas. Berkaitan dengan
suhu pertumbuhan dikenal suhu minimum, maksimum dan optimum. Suhu
minimum adalah suhu yang paling rendah dimana kegiatan mikroba masih
berlangsung. Suhu optimum adalah suhu yang paling baik untuk kehidupan
jasad. Sedangkan suhu maksimum adalah suhu tertinggi yang masih dapat
menumbuhkan mikroba tetapi pada tingkat kegiatan fisiologi yang paling
rendah.
3. pH
Setiap organisme mempunyai kisaran nilai pH dimana pertumbuhan
masih memungkinkan. Masing-masing mikroorganisme biasanya mempunyai
pH optimum.untuk menjaga agar pH dalm medium konstan, maka perlu
ditambahkan zat-zat buffer, misalnya KH2PO4 dan K2HPO4. Dalam campuran
garam tersebut garam-garam dibasis akan mengadsorbsi ion-ion H, sedangkan
garam-garam monoabsis akn menyerap ion OH.
4. Jumlah Starter
Kuantitas starter yang ditambahkan dalam media bergantung pada
temperatur inkubasi, kurang lebih 5 – 10 % (v/v). Pada umumnya jumlah
starter yang ditambahkan tergantung pada keasaman starter, suhu dan lama
fermentasi yang diinginkan.
5. Lama Fermentasi
Lama fermentasi adalah waktu yang dibutuhkan oleh suatu
mikroorganisme untuk merombak bahan menjadi lebih sederhana. Media bisa
berupa karbohidrat atau protein. Lama fermentasi dipengaruhi oleh
konsentrasi gula, kultur yang digunakan dan suhu fermentasi
2.7. Zymomonas mobilis
Zymomonas mobilis adalah bakteri yang berbentuk batang,termasuk dalam
bakteri garam negatif, tidak membentuk spora, dan merupakan bakteri yang dapat
bergerak (Lee, et al, 1979). Zymomonas mobilis mempunyai klasifikasi ilmiah
sebagai berikut :
Kerajaan : Bakteri
Filum : Proteobacteria
Kelas : Alpha Proteobacteria
Order : Sphingomonadales
Keluarga : Sphingomonadaceae
Genus : Zymomonas
Spesies : Z. mobilis
Bakteri ini banyak digunakan di perusahaan bioetanol karena
menghasilkan kemampuan yang dapat melampaui ragi dalam beberapa aspek.
Menurut Gunasekaran, 1999 Zymomonas Mobilis memiliki beberapa kelebihan
dibandingkan dengan Sacharomyces Cerevisieae yaitu:
1. Dapat tumbuh secara anaerob fakultatif dan mempunyai toleransi suhu yang
tinggi.
2. Mempunyai kemampuan untuk mencapai konversi yang lebih tinggi.
3. Tahan terhadap kadar etanol yang tinggi dan pH yang rendah.
4. Mampu menghasilkan yield etanol 92% dari nilai teoritisnya.
Bakteri ini awalnya terisolasi dari minuman beralkohol seperti tuak Afrika,
Meksiko pulque , dan juga sebagai kontaminan dari sari buah apel dan bir di
negara - negara Eropa. Suhu optimum proses fermentasi dengan menggunakan
Zymomonas mobilis adalah pada kisaran pH 4 – 7. Karakteristik menarik
Zymomonas mobilis adalah bahwa perusahaan membran plasma mengandung
hopanoid, senyawa pentasiklik mirip dengan eukariotik sterol. Hal ini
memungkinkan untuk memiliki toleransi yang luar biasa untuk kondisi lingkungan
Beberapa penelitian fermentasi etanol dari berbagai substrat dengan menggunakan mikroba Zymomonas mobilis telah dilakukan, diantaranya dengan menggunakan substrat glukosa dengan Zymomonas mobilis mutan oleh Muspahaji (2008) dan Alfena (2009), glukosa dengan Zymomonas mobilis amobil (Pancasning, 2008), sukrosa dengan Z. mobilis ATCC 10988 oleh Hany (2009), sari buah pisang dengan Zymomonas mobilis FNCC 0056 oleh Imamah (2006),sari buah pepaya oleh Sujito (2008), limbah karet alam oleh Tripetchul, dkk (1992), buah dan limbah nanas dengan. Zymomonas mobilis ATCC 10988 oleh Tanaka, dkk (1999).
2.8. Landasan Teori
Selulosa dari kulit kopi dapat diubah menjadi bioetanol dengan proses
hidrolisis asam dengan kadar tertentu. Proses hidrolisa selulosa harus dilakukan
dengan asam pekat agar dapat menghasilkan glukosa yang tinggi (Fieser, 1963)
lalu difermentasi hingga terbentuk bioetanol. Mekanisme reaksi seperti di bawah
ini :
selulosa Hidrolisis Glukosa Fermentasi Etanol
Hidrolisis merupakan proses pemecahan suatu senyawa menjadi senyawa
yang lebih sederhana dengan bantuan molekul air (Kirck Othmer, 1967). Ada
berbagai macam hidrolisis yaitu hidrolisis dengan larutan asam hidrolisis larutan
basa alkali fusion, dan hidrolisis dengan enzim. Hidrolisis yang paling sering
digunakan untuk menghidrolisis selulosa adalah hidrolisis secara asam. Beberapa
asam yang umum digunakan untuk hidrolisis asam antara lain adalah asam sulfat
(H2SO4), asam perklorat, dan HCl. Berikut ini adalah reaksi hidrolisa sellulosa
menjadi glukosa :
H2SO4 / HCl
(C6H10O5)n + n H2O C6H12O6 ... (2)
Sellulosa Glukosa
Hidrolisis asam dapat dikelompokkan menjadi hidrolisis asam pekat dan
hidrolisis asam encer (Taherzadeh & Karimi, 2007). Penggunaan asam pekat pada
proses hidrolisis selulosa dilakukan pada temperatur yang lebih rendah daripada
asam encer. Konsentrasi asam yang digunakan adalah 10 – 30% (Zimbardi et.al).
Temperatur reaksi adalah 100oC dan membutuhkan waktu reaksi antara 2 – 6 jam.
Temperatur yang lebih rendah meminimalisasi degradasi gula. Keuntungan dari
penggunaan asam pekat ini adalah konversi gula yang dihasilkan tinggi, yaitu bisa
mencapai konversi 90% (Badger, 2002), kemudian glukosa difermentasi dengan
menggunakan bakteri atau ragi yang dapat mengkonversi gula menjadi bioetanol.
Bioetanol yang dihasilkan dari proses fermentasi biasanya mempunyai
kadar yang masih rendah. Untuk mempertinggi kadar bioetanol dalam produk
sering kali hasil fermentasi di distilasi dan kadar alkohol yang dihasilkan antara
29 – 50 %.
Dalam proses fermentasi ini, glukosa dari hasil fermentasi diubah menjadi
etanol dengan reaksi sebagai berikut :
Zymomonas mobilis
C6H12O6 2C2H5OH + 2CO2 ... (3)
Glukosa Etanol
Proses fermentasi merupakan salah satu cara yang banyak dilakukan untuk
mendapatkan bioetanol dalam dunia industri dengan memanfaatkan kemampuan
mikroorganisme. Adapun mikroorganisme yang digunakan untuk memproduksi
bioetanol dalam penelitian ini adalah bakteri Zymomonas mobilis, karena
memiliki toleransi suhu yang tinggi, kemampuan untuk mencapai konversi yang
lebih cepat, lebih tahan terhadap kadar ethanol yang tinggi yang dihasilkan pada
proses fermentasi apabila dibandingkan Saccharomices cerevisiae. Bakteri ini
mampu menghasilkan yield etanol 92% dari nilai teoritisnya. Suhu optimum
proses fermentasi dengan menggunakan Zymomomobilis adalah pada kisaran
pH 4 - 7. (Gunasekaran, 1999). Bioetanol hasil fermentasi dapat dimurnikan lagi
2.9. Hipotesis
Adanya kandungan selulosa yang terdapat didalam limbah kulit kopi
memungkinkan untuk dapat dijadikan bioetanol dengan cara menghidrolisis
selulosa menjadi glukosa menggunakan asam, yang kemudian dilanjutkan dengan
proses fermentasi. Pada proses fermentasi diduga konsentrasi starter dan waktu
BAB III
METODE PENELITIAN
3.1. Bahan-Bahan yang Digunakan
9. Pipet
19. Seperangkat alat hidrolisa
20. Seperangkat alat fermentasi
21. Seperangkat alat destilasi
3.3. GAMBAR SUSUNAN ALAT
Gambar 5. Alat Hidrolisis
Keterangan Gambar 5 :
1. Labu leher tiga 5. Kondensor
2. Pemanas listrik 6. Air masuk
Gambar 6. Alat Fermentasi
Gambar 7. Alat Destilasi
Keterangan Gambar 7 :
1. Kompor listrik 4. Kondensor
2. Labu destilasi 5. Statif & klem
3. Thermometer 6. Penampung destilasi
Keterangan Gambar 6 :
1. Botol fermentasi
2. Selang
3. Botol yang berisi air
1 2 3
2
1
5
4
3.4. Variabel
1. Proses Hidrolisis
Kondisi yang ditetapkan :
a.Massa kulit kopi = 100 gram
Variabel yang dijalankan :
a. Volume H2SO4 = 10, 20, 30 ( % v/v )
b. Volume HCl = 10, 20, 30 ( % v/v )
2. Proses Fermentasi
Kondisi yang ditetapkan :
a. Suhu Fermentasi = 30oC
b. pH awal Fermentasi = 6
c. Volume filtrat = 500 ml
Variabel yang dijalankan :
a. Waktu Fermentasi = 2, 3, 4, 5, 6, 7, 8 (hari)
b. Starter Zymomonas mobilis = 9, 10, 11 (% v/v )
3.5. Prosedur Penelitian 1. Persiapan Alat
Alat-alat yang akan digunakan dalam penelitian ini harus dibersihkan
2. Persiapan Bahan Baku
1. Bersihkan Kulit kopi dari kotoran-kotoran.
2. Keringkan dengan menggunakan oven pada suhu 100oC selama 2 jam.
3. Hancurkan Kulit kopi dengan cara diblender / digiling hingga berbentuk
serbuk.
4. Ayak kulit kopi pada ayakan 80 mesh.
5. Analisa kandungan sellulosanya dengan dengan spektrofotometer.
3. Proses Hidrolisis
1. Timbang Serbuk kulit kopi sebanyak 100 gram.
2. Tambahkan aquadest dan larutan H2SO4 pekat dengan perbandingan volume
10, 20, 30 % (v/v) hingga total larutan 1 liter.
3. Masukkan kedalam labu hidrolisis dan hidrolisis dengan suhu 100oC selama
4 jam.
4. Saring larutan hasil hidrolisis dan filtrat diambil untuk dianalisa kadar
glukosanya dengan spektrofotometer.
5. Ulangi langkah 2 – 4, tetapi menggunkan larutan HCl 10, 20, 30 % (v/v)
4. Pembuatan Media Nutrient Agar
1. Nutrient agar sebanyak 20 gr dan aquadest 200 ml dimasukkan kedalam
erlenmeyer / beaker gelas, lalu dipanaskan sampai larut semua.
2. Sterilkan dalam autoclave selama 15 menit dengan suhu 121oC
3. Dinginkan sampai kira-kira 70oC, lalu pindahkan dalam tabung reaksi yang
steril, lalu tabung dimiringkan.
4. Media padat dalam tabung siap ditanami.
5. Pembuatan Media Cair untuk Pembiakkan Kultur dan Pengukuran
Kurva Pertumbuhan
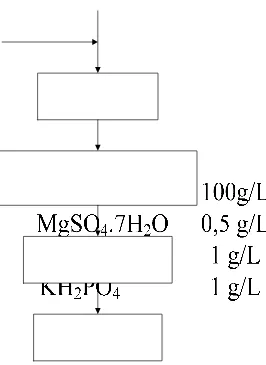
1. Media dan bahan-bahan nutrien dimasukkan kedalam erlenmeyer dengan
komposisi sebagai berikut : 10 g/L ekstrak ragi 100 g/L glukosa 0,5 g/L MgSO4.7H2O
1 g/L (NH4)2SO4
1 g/L KH2PO4
2. Aduk bahan-bahan tersebut hingga bercampur.
3. Erlenmeyer berisi media yang telah dibuat ditutup dengan menggunakan
penutup kapas yang dilapisi dengan alumunium foil.
4. Sterilkan media dalam autoklaf pada suhu 121oC selama 15 menit.
Gambar 11. Diagram Alir Pembuatan Media Cair untuk Pembiakkan
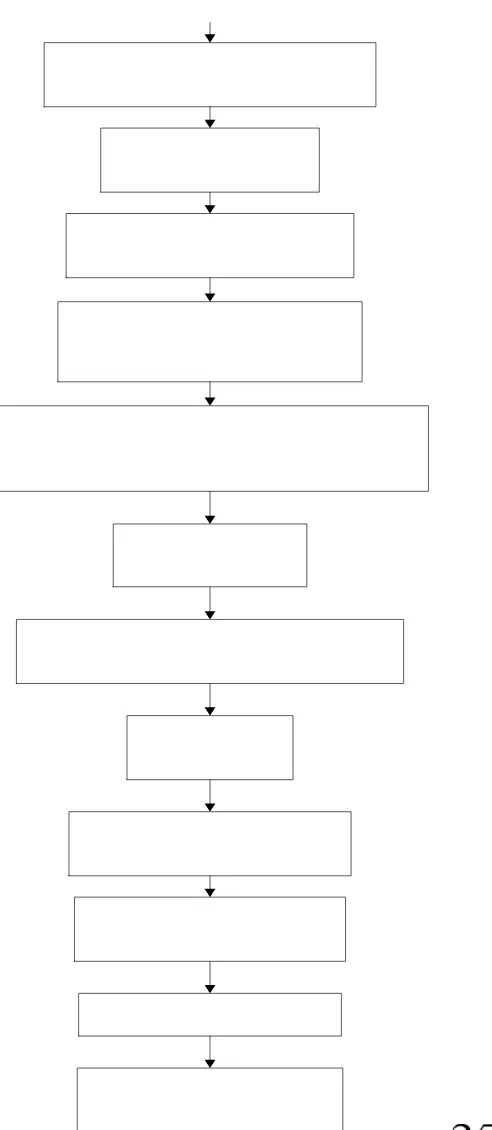
6. Persiapan untuk Pengukuran Kurva Pertumbuhan Zymomonas mobilis.
1. Zymomonas mobilis ditumbuhkan pada media nutrien agar miring.
2. Media yang telah diinokulasi ini kemudian diinkubasi pada suhu 30oC
selama 24 jam.
3. Ambil tiga ose sel Zymomonas mobilis dari agar miring kemudian
dimasukan ke dalam 25 ml larutan media cair.
4. Inkubasikan selama 48 jam dengan dishaker pada kecepatan 120 rpm dan
suhu 30oC.
5. Ambil 25 ml media cair yang telah diinkubasi selanjutnya diinokulasikan
kembali ke dalam 225 mL media cair dan dishaker 120 rpm selama 48
jam.
6. Setiap 2 jam sekali diambil sample ( contoh ) untuk dianalisa sel keringnya
( sebentar – sebentar dikocok / dishaker ).
7. Analisa sel keringnya dengan cara sebagai berikut:
Ambil sample setiap 2 jam sekali sebanyak 10 ml, lalu disaring,
kemudian dioven pada suhu 105oC – 110oC selama 30 menit, lalu
dimasukkan ke eksikator. Setelah dingin ditimbang, kemudian dioven lagi
dan seterusnya sampai beratnya konstan.
Gambar 12. Diagram Alir Persiapan untuk Pengukuran Kurva
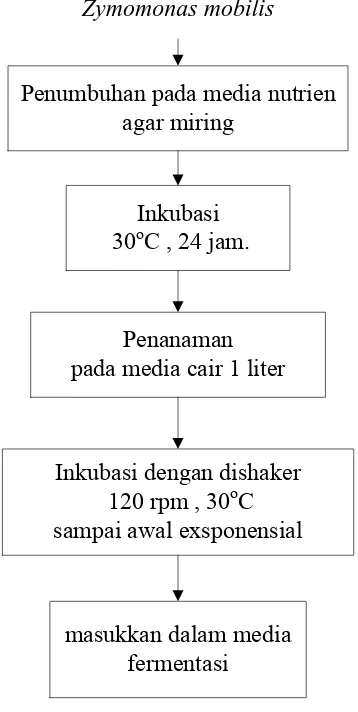
7. Pembuatan Starter Untuk Fermentasi
1. Zymomonas mobilis ditumbuhkan pada media nutrien agar miring.
2. Media yang telah diinokulasi ini kemudian diinkubasi pada suhu 30oC
selama 24 jam.
3. Ambil satu ose sel Zymomonas mobilis dari agar miring kemudian
dimasukan ke dalam 1 liter larutan media cair.
4. Inkubasi dengan dishaker pada kecepatan 120 rpm dan suhu 30oC, sampai
awal exsponensial kemudian masukkan dalam media fermentasi.
Zymomonas mobilis
Penumbuhan pada media nutrien agar miring
Inkubasi 30oC , 24 jam.
Penanaman pada media cair 1 liter
Inkubasi dengan dishaker 120 rpm , 30oC sampai awal exsponensial
masukkan dalam media fermentasi
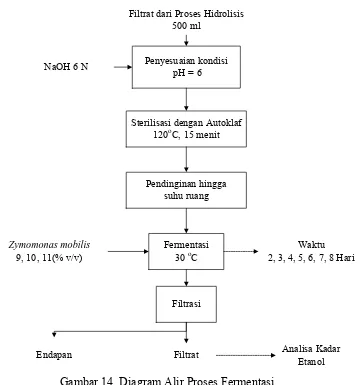
8. Proses Fermentasi
1. Ambil filtrat dari proses hidrolisis sebanyak 500 ml dan tambahkan
NaOH 6 N hingga pH = 6.
2. Sterilkan dalam autoklaf pada suhu 120oC selama 15 menit.
3. Dinginkan hingga suhu ruang.
4. Masukkan starter Zymomonas mobilis dengan variabel volume starter 9,
10, 11 % v/v dan dikocok.
5. Tutup botol fermentasi hingga rapat dan gas dialirkan kedalam botol lain
yang berisi air.
6. Fermentasi sesuai dengan variabel waktu fermentasi yaitu 2, 3, 4, 5, 6, 7
dan 8 hari dengan suhu fermentasi 30oC.
7. Saring dan ambil filtrat untuk proses destilasi.
Fermentasi
9. Proses Destilasi
Filtrat hasil fermentasi didestilasi pada suhu 80oC untuk mendapatkan
kadar yang lebih tinggi sesuai yang diinginkan dan kemudian dianalisa kadar
etanolnya.
Gambar 15. Diagram Alir Proses Destilasi
3.6. Prosesdur Analisa
1. Analisa Kadar Sellulosa
a. Analisa Kadar ADF
1. Timbang contoh sebanyak 0,5 gr.
2. Tambahkan aquadest 10 ml dan larutan aseton sebanyak 5 ml.
3. Kocok hingga merata.
4. Baca absorbansinya Pada λ = 520 nm spektofotometer
b. Analisa Kadar Lignin
1. Timbang contoh sebanyak 0,5 gr dan tambahkan aquadest 10 ml
2. Tambahkan H2SO4 72 % sebanyak 5 ml dan larutan aseton sebanyak 5 ml.
3. Kocok hingga merata.
Perhitungan :
Kadar Sellulosa = Kadar ADF – Kadar Lignin
2. Analisa Kadar Glukosa
1. Pipet contoh sebanyak 0,5 ml.
2. Etanol diuapkan dengan aliran udara pada suhu kamar.
3. Sample diencerkan hingga 100 ml.
4. Sample diambil 2,0 ml dengan pipet
5. Tambahkan 0,1 ml larutan fenol 80 % lalu ditambahkan 0,5 ml H2SO4
pekat dan Dikocok selama 10 menit, lalu diinkubasi pada 25–30oC dalam
pemanas air selama 20 menit
3. Analisa Kadar Etanol
1. Pipet 1,5 ml Larutan NaNO2.
2. Tambahkan 5 ml 4 - Nitro Aniline dan kocok.
3. Diamkan selama 2 menit hingga larutan berwarna putih tulang.
4. Tambahkan cairan sample sebanyak 25 ml dan 2 ml Na2NO3
5. Kocok selama 10 menit
6. Baca absorbansinya Pada λ = 470 nm spektofotometer.
BAB IV
HASIL DAN PEMBAHASAN
4.1. Hasil
Seluruh analisa dalam proses pembuatan bioetanol dari kulit kopi ini,
dianalisakan di Balai Penelitian dan Konsultasi Industri (BPKI) Surabaya dengan
methode spektrofotometri.
4.1.1. Analisa Bahan Baku
Berdasarkan hasil analisa bahan awal ( limbah kulit buah kopi ) diperoleh
data sebagai berikut :
Tabel 2. Hasil Analisa Limbah Kulit Kopi
Sumber : Balai Penelitian dan Konsultasi Industri (BPKI) Surabaya (2011)
4.1.2. Analisa Kadar Glukosa Pada Proses Hidrolisis
Pada proses hidrolisis dengan variabel katalis yang dijalankan didapatkan
hasil analisa glukosa sebagai berikut :
Tabel 3. Hasil Analisa Kadar Glukosa setelah Proses Hidrolisis
KADAR KATALIS KADAR GLUKOSA
JENIS KATALIS
Sumber : Balai Penelitian dan Konsultasi Industri (BPKI) Surabaya (2011)
NAMA SAMPEL KADAR SELULOSA
4.1.3. Pengukuran Kurva Pertumbuhan Bakteri Zymomonas Mobilis
Untuk mengetahui kurva pertumbuhan bakteri Zymomonas mobilis
dilakukan analisa secara gravimetri dengan melakukan pengamatan selama 48
jam, dan didapatkan data sebagai berikut :
Tabel 4. Hasil Pengukuran Kurva Pertumbuhan Bakteri Zymomonas mobilis
secara Gravimetri
PENGAMATAN MASSA BAKTERI PENGAMATAN MASSA BAKTERI
JAM KE ( gr ) JAM KE ( gr )
0 0.0144 26 0.0792
2 0.0156 28 0.0787
4 0.0316 30 0.0723
6 0.0498 32 0.0687
8 0.0606 34 0.0649
10 0.0702 36 0.0611
12 0.0781 38 0.0581
14 0.0787 40 0.0542
16 0.0788 42 0.0508
18 0.0789 44 0.0478
20 0.0793 46 0.0414
22 0.0795 48 0.0323
4.1.4. Analisa Kadar Etanol Pada Proses Fermentasi
Proses fermentasi berlangsung selama 7 hari dengan variable konsentrasi
starter. Setelah proses fermentasi berlangsung didapatkan kadar etanol sebagai
berikut :
Tabel 5. Analisa Kadar Etanol setelah Proses Fermentasi
STARTER WAKTU FERMENTASI KADAR ETANOL
( % ) ( HARI ) ( % )
4.1.5. Analisa Glukosa Sisa Setelah Proses Fermentasi
Setelah Proses fermentasi berlangsung sesuai dengan variabel yag
dijalankan, maka telah didapatkan kondisi terbaik untuk memperoleh kadar etanol
yang terbaik. Kondisi yang terbaik yaitu pada konsentrasi starter 11 % dengan
waktu fermentasi selama 7 hari. Untuk melihat prosentase glukosa yang dapat
terkonversi maka dilakukan analisa kadar sebelum proses fermentasi ( glukosa
awal ) dan kadar glukosa setelah proses fermentasi ( glukosa sisa ) pada kondisi
terbaik tersebut. Adapun hasil analisa kadar glukosanya adalah sebagai berikut :
Tabel 6. Hasil Analisa Kadar Glukosa Sisa setelah Proses Fermentasi pada
Kondisi terbaik ( Konsentrasi Starter 11 % dan Waktu Fermentasi 7 Hari )
NAMA SAMPEL KADAR GLUKOSA ( % )
Larutan sebelum proses fermentasi
( glukosa awal ) 8,96
Larutan setelah proses fermentasi
( glukosa sisa ) 0,18
4.2. Pembahasan
Dari hasil analisa yang didapat, maka diperlukan pembahasan yang lebih
mendetail agar dapat diambil kesimpulan pada setiap tahapan proses.
4.2.1 Hasil Proses Hidrolisis
Gambar 19. Pengaruh Konsentrasi Katalis terhadap hasil glukosa pada
proses hidrolisis
Pada Gambar 19 terlihat bahwa pengunaan katalis yang terbaik adalah
pada konsentrasi katalis 20 % (v/v), Hal ini disebabkan karena pada konsentrasi
10 % terjadi degradasi glukosa yang terbentuk menjadi struktur kimia yang lain
sehingga dapat menurunkan konversi reaksi. Sedangkan pada konsentrasi yang
lebih tinggi yaitu 30 % terjadi proses pembakaran selulosa sehingga selulosa yang
dirubah menjadi glukosa menjadi sedikit dan pada akhirnya glukosa yang
dihasilkan juga sedikit. Katalis HCl menghasilkan glukosa lebih tinggi jika
dibandingkan H2SO4, Hal ini diakibatkan H2SO4 bersifat membakar selulosa sedangkan HCl tidak, sehingga glukosa yang dihasilkan lebih sedikit.
Menurut Zimbardi et.al penggunaan asam pekat pada proses hidrolisis
selulosa dilakukan pada temperatur 100oC dan membutuhkan waktu reaksi antara 2 - 6 jam. Konsentrasi asam yang digunakan adalah 10 – 30 %. Keuntungan dari
mencapai konversi 90% (Badger, 2002). Namun pada penelitian kali ini hasil
glukosa yang didapatkan tidak terlalu tinggi hal ini terjadi karena adanya lignin
yang berada didalam kulit kopi. Lignin ini mengikat selulosa sehingga
mengganggu berlangsungnya proses hidrolisis. Didalam limbah kulit kopi
mengandung lignin sebanyak 7,63 % (Balai Penelitian dan Konsultasi Industri
(BPKI) Surabaya, 2011)
Dari grafik dapat dilihat bahwa kondisi terbaik proses hidrolisis yaitu pada
penggunaan katalis HCl dengan konsentrasi 20 % (v/v) menghasilkan glukosa
sebesar 10,04 %. Kondisi terbaik ini dipilih untuk proses selanjutnya yaitu proses
fermentasi.
4.2.2. Kurva Pertumbuhan Bakteri Zymomonas mobilis
Gambar 20. Kurva Pertumbuhan Bakteri Zymomonas mobilis
Pada Gambar 20 menunjukkan bahwa kurva pertumbuhan bakteri
Zymomonas mobilis mengalami empat fase yaitu fase lag yang mana bakteri
mulai beradaptasi untuk tumbuh yaitu pada waktu 0 - 2 jam. Kemudian
waktu 12 – 28 jam terjadi fase stasioner dan waktu selanjutnya merupakan fase
kematian. Sehingga berdasarkan data, waktu yang terbaik untuk memasukkan
starter ke dalam filtrat hidrolisis adalah pada waktu 2 jam. Hal ini dikarenakan
pada waktu tersebut bakteri Zymomonas mobilis mulai tumbuh dan siap untuk
mengkonversi gukosa menjadi etanol.
4.2.3. Hasil Proses Fermentasi
Gambar 21. Hubungan antara kadar etanol hasil fermentasi terhadap
waktu fermentasi
Pada Gambar 21 dapat diketahui bahwa adanya hubungan yang linier
antara waktu fermentasi dengan kadar etanol. Semakin lama waktu fermentasi
maka semakin tinggi kadar etanol yang dihasilkan. Waktu yang terbaik untuk
proses fermentasi diperoleh pada hari ke-7.
Hubungan atara konsentrasi starter dengan kadar etanol yang dihasilkan
juga linier, semakin tinggi konsentrasi starter maka kadar etanol yang dihasilkan
proses fermentasi adalah pada konsentrasi starter 11 % dengan waktu fermentasi
selama 7 hari yang menghasilkan kadar etanol sebesar 9,04 %. Dari kadar etanol
yang didapat dari kondisi terbaik tersebut didapatkan yield sebesar 51,02 %.
Setelah proses fermentasi dilanjutkan dengan proses destilasi selama 8 jam dan
menghasilkan bioetanol dengan konsentrasi 38,68 %.
4.2.3. Konversi Glukosa menjadi Etanol
Gambar 22. Konversi Glukosa pada kondisi terbaik fermentasi
( starter 11 % dan waktu 7 hari )
Pada proses hidrolisis telah didapatkan kondisi terbaik yaitu pada
penggunaan katalis HCl dengan konsentrasi 20 % yang menghasilkan kandungan
glukosa 10,04 %. Larutan ini masih bersifat asam dengan pH yang sangat rendah
( pH = 1 ), sedangkan kondisi yang di tetapkan untuk proses fermentasi adalah
larutan dengan pH = 6. Oleh sebab itu dilakukan proses netralisasi yang
kadar glukosa pada larutan hasil hidrolisis berkurang menjadi 8,96 % . Pada
kondisi terbaik proses fermentasi yaitu pada konsentrasi starter 11 % dan waktu 7
hari, menghasilkan kadar glukosa sisa sebesar 0,18 %. Sehingga konversi glukosa
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
1. Kadar Selulosa pada limbah kulit kopi sebesar 49,87 %.
2. Pada proses hidrolisis, kondisi terbaik diperoleh pada penggunaan
katalis HCl dengan konsentrasi 20 % (v/v) yang menghasilkan kadar
glukosa sebesar 10,04 %.
3. Pada proses hidrolisis hasil glukosa yang dihasilkan tidak terlalu tinggi,
hal ini terjadi karena adanya lignin yang berada didalam kulit kopi yang
mengikat selulosa sehingga mengganggu berlangsungnya proses
hidrolisis. Didalam limbah kulit kopi mengandung lignin sebanyak 7,63
% (Balai Penelitian dan Konsultasi Industri (BPKI) Surabaya, 2011)
4. Pada proses fermentasi kondisi terbaik diperoleh pada penambahan
starter dengan konsentrasi starter 11 % dan waktu fermentasi selama 7
hari yang menghasilkan kadar etanol sebesar 9,04 %.
5. Pada kondisi terbaik proses fermentasi bakteri Zymomonas mobilis
mampu mengkonversi glukosa sebesar 97,99 %.
6. Pada kondisi terbaik proses fermentasi didapatkan yield etanol sebesar
51,02 %.
7. Proses destilasi dilakukan selama 8 jam dan menghasilkan bioetanol
dengan konsentrasi 38,68 %.
8. Kulit kopi dapat digunakan sebagai bahan baku alternatif pembuatan
5.2. Saran
1. Melakukan proses delignifikasi ( menghilangkan lignin ) sebelum
melakukan proses hidrolisis, agar proses hidrolisis dapat berjalan
dengan sempurna dan menghasilkan kadar glukosa yang tinggi.
2. Diharapkan untuk penelitian selanjutnya menggunakan alat bioreaktor
yang standart sehingga dapat dihasilkan kadar etanol yang tinggi.
3. Diharapkan untuk penelitian selanjutnya menggunakan alat destilasi
DAFTAR PUSTAKA
Anonim, 2008. Perkembangan Industri Biofuel di Indonesia. Indonesian
Commercial Newsletter, (Online) , (http://www.datacom.co.id/Biofuel
2008 Ind. Html, di akses 14 Juli 2010).
Badger, PC., 2002. Ethanol from Cellulose : A General Review. In Trend in
New Crops and New Uses., J.Jannick and A.Whipkey (eds).
Alexandria,VA : ASHS Press.
Baon, J.B., Sukasih.R, Nurkholis, 2005. Laju Dekomposisi dan kualitas
kompos limbah padat kopi : Pengaruh Aktivator dan Bahan Baku
Kompos. Pelita Perkebunan : Universitas Jember.
Budiyanto, Krisno Agus.H.DR.MKes., 2002. Mikrobiologi Dasar, hal 71 – 75.
Malang : Universitas Muhammadiyah Malang.
Desmayati, Z dan Muladi, 1995. Pemanfaatan Limbah Kopi Ransum Ayam
Pedaging. Warta Penelitian dan Pengembangan Pertanian XII (3) : 79.
Dirjen Perkebunan, 2006. Statistik Perkebunan Indonesia 2003 – 2005 (kopi).
Jakarta : Departemen Pertanian.
Dirmanto, S., 2006. Fermentasi Anaerobik, (Online) (http://www.kompas.com,
diakses 1 Oktober 2010).
Gunasekaran, P., Karunakaran, T., Kasthuribai, M.. 1986. Fermentation
Pattern of Zymomonasmobilis strains of different substrate-a
comparative study. Department of Microbial Technology, School of
Biological Sciences, Madurai Kamaraj University, India. diambil dari
Ghani Arasyid dkk, (Online) , (
http://digilib.its.ac.id/public/ITS-Undergraduate-12522-Paper.pdf diakses 15 oktober 2010).
Gunasekaran, P. and Raj, K. C. 1999. Ethanol Fermentation Technology –
Zymomonas mobilis. Current Science. Vol. 77, #1, 56-68 diambil dari
Ghani Arasyid dkk, (Online) , (
Groggins P. H.,1958. Unit Process Inorganic Syntesis 5th Edition. Japan : Mc
Graw Hill Kogakusa, Ltd.
Indartono Y, 2005. Bioethanol, Alternatif Energi Terbarukan : Kajian Prestasi
Mesin dan Implementasi di lapangan. Fisika, LIPI.
Judoamidjoyo, M., A.a.Darwis dan E.G.Said, 1982. Teknologi Fermentasi.
Jakarta : Rajawali Pres.
Kim, K. H., & Hong, J. (2001). Supercritical CO2 pretreatment of
lignocellulose enhances enzymatic cellulose hydrolysis. Bioresource
Technology 77, hal 139-144, (online), (http//:isroi.wordpress.com
/2008/07/23/preatment, diakses 01 oktober 2010).
Lee, K.J., Tribe, D.E. and Rogers, P.L., 1979. Biotechnol. Lee, K.J., Suku,
D.E. dan Rogers, P.L, 1979. Biotechnol. Lett., 1 , 421. Lett 1.,, 421.
Louis F. Fieser, Mary Fieser, 1963. Pengantar Kimia Organik. Bandung :
Dhiwantara.
Melyani, V. 2009. Petani Kopi Indonesia Sulit Kalahkan Brazil.
(URL:http://www.Tempointeraktif.com/hg/bisnis/2009/07/02/brk,200
90702-184943,id.html, diakses 26 September 2010).
Najafpour, G. D., Lim, J. K. 2002. Fermentation of Ethanol , School of
Chemical Engineering, Universiti Sains Malaysia. diambil dari
Ghani Arasyid, dkk, (Online) ,(
http://digilib.its.ac.id/public/ITS-Undergraduate- 12522-Paper.pdf diakses 15 Oktober 2010).
Nguyen, Q. A.; Dickow, J. H.; Duff, B. W.; Farmer, J. D.; Glassner, D. A.;
Ibsen, K. N.; Ruth, M. F.; Schell, D. J.; Thompson, I. B. & Tucker, M.
P. (1996), ‘NREL/DOE ethanol pilot-plant: Current status and
capabilities’, Bioresource Technology 58(2), 189–196. (Online),
(http://www. Technology indonesia.com/columns.php?id=36 diakses
15 Oktober 2010).
Othmer, Kirk.,1967. Encyclopedia of Chemical Technology second edition vol
5. New York : Interscience Publisher a division of John Wiley &
Sons, Inc.
Parry, T. J & Powsey, R. K, 1973, Principles of Microbiology for Student of
Food Technology, diambil dari Purnomo Hari, dkk, 1987, Ilmu
Pangan, Universitas Indonesia, Jakarta.
Robert H. Perry, Perry’s Chemical Engineers Handbook 7th , New York, The McGraw Hill Companies, Inc.
Sarjdoko, 1991. Bioteknologi Latar Belakang dan Beberapa Penerapannya.
Jakarta : Gramedia Pustaka Umum.
Soebiyanto PT, 1986. HFS dan industri ubi kayu lainnya. PT Gramedia.
Jakarta.
Syukur, Abdul, dkk. 2005. Ensiklopedi Umum untuk Pelajar jilid 6. Jakarta:
PT Ichtiar Barovan Hoeve.
Taherzadeh, M. and Karimi, K. 2007. Acid-based Hydrolysis Processes for
Ethanol from Lignosellulosic Material : A Review, Bioresources 2
(3), 472-499, diambil dari Ghani Arasyid dkk, (Online),
(http://digilib.its.ac.id/public/ITS-Undergraduate-12522-Paper.pdf
diakses 15 oktober 2010).
Viola, E., Cardinale, M., Santarcangelo, R., Villone, A., & Zimbardi, F.
(2008). Ethanol from eel grass via steam explosion and enzymatic
hydrolysis. Biomass and Bioenergy , (in Press). (Online),
((http://www. Technology indonesia.com/columns.php?id=36 diakses
APPENDIKS
1. Pembuatan Larutan HCL 10 % (v/v) sebanyak 1 liter
=
Jadi memipet 100 ml HCl pekat sebanyak 100 ml lalu ditambahkan aquadest
hingga 1 liter.
NB : dengan cara yang sama untuk menghitung HCl 20 %, HCl 30 %, H2SO4 10 % , 20 % dan 30 %
2. Pembuatan Larutan NaOH 6 N sebanyak 1 liter
Massa NaOH = 240 gr
Jadi menimbang NaOH sebanyak 240 gr dan dilarutkan hingga 1 liter dengan
aquadest.
3. Perhitungan Konversi Glukosa
= 97,99 %
4. Perhitungan Kadar Etanol setelah Proses Destilasi
Diketahui : Berat pikno kosong = 11,2052 gr
Berat pikno isi = 20,5098 gr
Volume piknometer = 10 ml
Maka :
Dillihat pada Tabel 2-110 Perry edisi 7 didapatkan interpolasi data :
kadar ethanol = SG
38,68 %
Sehingga didapatkan konsentrasi bioetanol setelah proses destilasi sebesar
38,68 %.
5. Perhitungan Yield etanol
Diketahui :
Kadar etanol pada kondisi optimum = 9,04 %
Kadar glukosa awal sebelum fermentasi = 8,96 %
Volume larutan = 500 ml
etanol = 0,78075 gr/ml
glukosa = 1,544 gr/ml
Maka :
Volume etanol =
Massa etanol = Volume etanol x etanol
= 45,2 ml x 0,78075 gr/ml
= 35,2899 gr
Massa glukosa = Volume glukosa x glukosa
= 44,8 ml x 1,544 gr/ml
= 69,1712 gr