PEMBUATAN PIGMENT
(FETIO
3) SISA PENGOLA
Mohammad Taufi
1Jurusan Tekni
Jl. Prof. Soedarto, K
Abs
tract
Indonesia is a country that has a lot o raw material. The exact conditions for proc material pigments are not yet known. Impr research on natural raw material sources (Borneo), which contains 80-90% of Ilmeni concentration of salt catalyst (NH4Cl) on th titanium dioxide was separated by acid lea process adopted from Becher process which In this experiment, the fixed variables used The changing variables used were aeration and 3%. XRD (X-ray Diffraction) qualitativ the results showed an increase in TiO2 conte NH4Cl gave the best result. The greater the improving the grade of TiO2 was 4 hours, p gave a potential concentration of titanium d of 1%.
Keywords : TiO
2; Ilmenite; Aeration proces1.
PENDAHULUAN
Kebutuhan titanium dioksida (TiO2) di Ind tinggi sehingga berdampak pada pertumb dalam negeri. Untuk itulah harus dicarika agar jumlah impor TiO2 ini dapat kita k mencari alternatif lain yaitu memproduks memanfaatkan pasir ilmenite (FeTiO3) Indonesia. Mineral ilmenite banyak terdap samping penambangan timah di Pulau B kandungan ilmenite hingga 90% dan juga d di pantai selatan Jawa Tengah dengan kan hingga 6% (Hendratno 1999; Sumardi 199 titanium pada ilmenite dapat direaksikan de bahan aditif lain dan dapat menghasilkan s sangat baik untuk aplikasi ilmenite.
Penggunaan titanium dioksida (TiO2) sinte bentuk tetragonal rutile ataupun anatase dipakai dalam industriantara lain sebagai pig pigmen warna superior (warna putih), bahan untuk elektronik (BaTiO3), bahan baku un TiO2 polimeric precursor yang sangat pembuatan bahan-bahan keramik maju pelapisan optik (film-optic), bahan electro-o komposit polimer ceramik (Ceramer) (Fadli
NT TITANIUM DIOKSIDA (TIO
2) DA
LAHAN PASIR ZIRCONDENGANPR
ufik Mohar
1, Dewi Fatmawati
1, Setia Budi Sason
knik Kimia, Fakultas Teknik, Universitas Diponego
, Kampus UNDIP Tembalang, Semarang 50239, In
t of Ilmenite (FeTiO3), but as yet only plays the role of rocessing Ilmenite into products for sand proficiency le mproved grade of titanium dioxide as a separation pr es that can be used. One raw material is waste zircon
enite. The purpose of this research was to determine t n the transformation rate of iron (Fe) into iron oxide ( leaching process to produce pure titanium dioxide. Th ich is the process of oxidation, reduction, aeration, leach ed were time of oxidation and reduction of 3 hours and on time of 2, 4, 6, and 8 hours; and concentration of sal
tive analysis and GSAS (General Structure Analysis Sy ntent on all the variables. The process of increasing TiO the concentration of NH4Cl catalyst, the smaller the TiO s, proven by a very effective transformation of Fe into m dioxide was 45.86% with aeration process time of 4 h
cess; NH4Cl; Becher process
ndonesia semakin mbuhan ekonomi ikan jalan keluar kurangi dengan ksi TiO2 dengan ) yang ada di apat dalam hasil Bangka dengan a dalam pasir besi andungan Ilmenit 999). Kandungan dengan beberapa n sifat baru yang
ntetis baik dalam e sangat banyak pigment pemutih, an utama keramik untuk pembuatan t penting untuk aju, antara lain
optik dan bahan li A, 2004).
Metode peningkatan dioksidadiantaranya adalah yaituproses becher, proses su Biliton, proses termoklorida proses kaustik (soda) (Zhang salah satu proses yang sudah maju seperti Australia, Amer pembuatan pabrik TiO2 sa Indonesiauntuk mengetah potensialsesuai dengan baha berasal dari Indonesia (K dikarenakan sumber bahan industri cat yang sedang ber mempunyai keuntungan y menghasilkan pigment TiO berupa Fe2O3 juga dapat men
Kemurnian kandungan TiO2 pemisahan Besi dan TiO2 y pemisahan, besi perlu dihila menjadi besi oksida lalu leaching asam (H2SO4) Penelitian pengolahan Ilme pernah dilakukan oleh Justin dengan variasi katalis. Dar bahwa katalis NH4Cl merup
110
DARI ILMENITE
PROSES BECHER
ongko
1*)
goro
Indonesia
of an exporter of this important y levels as well as industrial raw process should be supported by con sand in Central Kalimantan e the effect of aeration time and e (Fe2O3), where iron oxide and . The titanium oxide purification aching, stripping, and calcination. nd time of calcination of 3 hours. salt catalyst (NH4Cl) of 1%, 2%, System) quantitative analysis on TiO2 content at a variable of 1% TiO2 increase. The best time for to Fe2O3. The result of research 4 hoursand NH4Cl concentration
kemurnian titanium
lah leaching dengan sulfat
sulfat yang diperbaiki oleh BHP da, proses leaching klorida, dan ng, 2011). Proses becher sebagai ah di terapkan di Negara-negara erika dan China. Oleh karena itu,
sangat penting diterapkan di tahui kondisi prosesyang ahan baku pasir ilmenite yang (Kalimantan tengah), hal ini an baku yang melimpah dan erkembang. Pemurnian Ilmenite yang lebih karena Selain iO2, hasil samping proses yang enjadi pigment berwarna merah.
untuk proses aerasi besi menjadi Fe2O3 s peningkatan kemurnian TiO2 yang signifika aerasi. Oleh karena itu kami menggunakan dalam meningkatkan kemurnian TiO2 konsentrasi katalis NH4Cl dan waktu p menjadi besi oksida, sehingga didapatkan ko sesuai untuk menghasilkan TiO2.
Dalam penelitian ini akan dikaji cara TiO2dengan Fe pada bahan baku Ilmenite pasir zircon yang berasal dari Kalima menganalisa kandungan TiO2 padaperubah katalis NH4Cl dan waktu aerasi pada pros variabel yang paling potensial, konstanta k pada tiap konsentrasi katalis NH4Cl, da dihasilkan.
2.
BAHANDAN METODE
Bahan Baku
Bahan baku berupa ilmenitesisa pasir zircon Kalimantan tengah. Bahan karbon yang proses reduksi berupa karbon batubara (coal dari provinsi banten. Sulfur, H2SO4, dan N dari toko kimia di daerah Tangerang Selatan
Preparasi Bahan Baku
Bahan baku Ilmenite, carbon, dan sulfur di disc mill dan dilakukan sieving dengan ukura Hasil sievingbahan baku Ilmenite dikarak XRD untuk mengetahui secara kualitatif kandungan bahan baku untuk diproses. Hasi bahan baku : FeTiO3 87,75%, ZrSiO4 12,25%
Proses Oksidasi
Proses oksidasi dilakukan dengan memasukk ilmenite≤ 200 Mesh ke dalam tube stainl berukuran H = 16 cm, ID= 3.65 cm kemudi ke tubular furnacepada suhu 1200 oC selam proses terbuka agar oksigen masuk ke furnacesehingga dihasilkan senyawa (Fe2TiO5).
4 FeTiO3(s) + O2(g)→ 2 Fe2O3·TiO2(s) +
Proses Mixing
Hasil oksidasi kemudian di milling kemba mill dan dilakukan sieving dengan ukuran Hasil sieving di campurkan dengan karbon s dan sulfur sebanyak 5% dari berat Ilmeni shaped mixer selama 45 menit.
sehingga terjadi ikan dalam proses an proses Becher dengan variasi perubahan besi konsentrasi yang
ara memisahkan ite (FeTiO3) sisa imantan Tengah, bahan konsentrasi roses oksidasi Fe, kecepatan reaksi dan yield yang
on yang berada di g dipakai untuk oal) yang di ambil NH4Cl diperoleh tan.
di milling didalam uran ≤ 200 Mesh. akterisasi dengan if dan kuantitatif asil Analisa XRD
5%.
ukkan bahan baku inless steel yang udian dimasukkan ama 3 jam dengan kedalam tubular pseudobrookite
+ 2 TiO2(s) (Zhang, 2011)
bali didalam disc an ≤ 200 Mesh.
n sebanyak 18,03% enite didalam V
Proses Reduksi
Hasil mixing kemudian di m steel lalu dimasukan ke dal 1200 oC selama 3 jamtanpa dan diberikan gas inert (A Oksida akan menghasilkan b magnet kuat.
Fe2O3·TiO2(s)+3CO(g)→ 2
Proses Aerasi pada reaktor
Hasil reduksi di milling ke dilakukan sieving dengan uku kemudian ditimbang seba variabel adalah 12 sehingga d yang sudah berukuran ≤325 klorida sesuai dengan variab 3%. Masukan 100 gr hasil r 325 mesh ke dalam beaker larutan ammonium klorida dengan penambahan udara berikan melalui kompresor. T sehingga besi akan semakin c ke bawah menjadi partikel ya
2Fe (s) + 3/2 O2(g)→ Fe2O
Proses Aerasi dilakukan sesu garam NH4Cl 1%, 2% dan 3 dengan Volume larutan 700 m
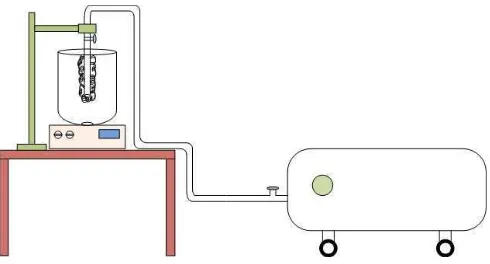
Gambar 1. Gambar Rang
Proses Leaching
Hasil reaksi pada Aerasi penghilangan Fe2O3 denga dalam larutan H2SO40,5 M menit. Larutan tersebut dis tersebut adalah Fe2(SO4)3 dan
Fe2O3(s) + 3H2SO4(aq)→ Fe2(S
masukan kedalam tube stainless alam tubular furnacepada suhu pa diberikan Oksigen (tertutup) (Argon). Proses reduksi Besi n besi logam (Fe) yang bersifat
→ 2 Fe(s) + 2TiO2(s) + 3CO2(g) (Zhang, 2011)
or Bubble Batch
kembali didalam disc mill dan ukuran ≤325 Mesh. Hasil sieving banyak 100gr/sampel, jumlah a dibutuhkan 1,2 kg hasil reduksi Mesh. Buat larutan ammonium iabel ubah yaitu : 1%, 2%, dan il reduksi yang sudah berukuran ker glass (reaktor) yang berisi a sesuai dengan variabel ubah ra yang sudah terinstalasi di . Terjadi agitasi di dalam reaktor in cepat berkarat dan mengendap yang sangat halus.
O3(Zhang, 2011)
esuai variabel konsentrasi katalis n 3% selama 2, 4, 6 dan 8 Jam 0 ml pada suhu 80oC.
angkaian Alat Proses Aerasi
si dilanjutkan dengan proses nganmelakukan leaching asam M pada suhu 90 oC selama 90 disaring dan didapatkan filtrat an padatan tersebut adalah TiO2.
(SO4)3(aq) + 3H2O(l)
Proses Striping
Hasil padatan dari leaching asam adalah Ti banyak mengandung asam sehingga haru dengan aquades agar sifat asam hilang, pad dalam aquadest dengan volume 800 ml. Lar selama 1 hari hingga padatan terpisah dan bawah.
Proses Kalsinasi
Padatan hasil striping dimasukan kedalam c dandilakukan kalsinasi dalam furnace denga selama 3 jam. Timbang berat akhir padatan Analisis hasil kalsinasi yang telah ditimban menggunakan XRD.
Metode Analisis
Analisa Hasil dilakukan dengan alat instru Difraction (XRD) Shimadzu 7000 di Badan Nasional (BATAN) Pusat Penelitian Ilmu Pe Teknologi (PUSPIPTEK)Serpong, Tange Proses hasil analisis dilakukan dengan cara kuantitatif. Analisa kualitatif dilaku mencocokan hasil peak dari XRD lalu di sam dengan jenis mineral yang sama, dilakukan d software Match yang dilengkapi dengan d Analisa kuantitatif menggunakan software structure analysis system) dengan kalib material (kisi, sudut, dan ordinat kristal) terle
3.
HASIL DAN PEMBAHASAN
Pengaruh Waktu dan Katalis NH
Persentase TiO2 pada Proses Aerasi
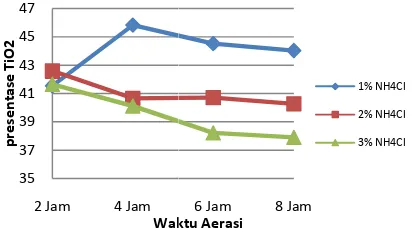
Grafik1 menunjukan bahwa penambahan yang berlebih justru mengurangi Persentase dikarenakan penambahan NH4Cl y mengakibatkan kandungan oksigen did semakin kecil sehingga mempengaruhi ter oksida (Fe2O3) yang selanjutnya akan dipi proses leaching. Pada proses aerasi, NH4 dengan Fe dan TiO2akan tetapi berfungsi karena laju korosi akan semakin cepa penghantar electron didalamnya seperti NH4 berfungsi untuk mencegah pasivasi. Na penggunaan larutan NH4Cl harus s konsentrasinya yaitu pada kondisi konsentr yang mana akan lebih menguntungkan dalam (Paten US, 1997). adatan dilarutkan arutan didiamkan an mengendap ke
cawan porselen, ngan suhu 800 oC an hasil kalsinasi. ang berat dengan
trumentasi X-Ray an Tenaga Nuklir Pengetahuan dan ngerang Selatan. ara kualitatif dan akukan dengan samakan peaknya n dengan bantuan database kristal. re GSAS (general librasi parameter erlebih dahulu.
H4Cl terhadap
an katalis NH4Cl tase TiO2. Hal ini yang berlebih didalam larutan terbentuknya besi ipisahkan dengan
4Cltidak beraksi si sebagai katalis epat ketika ada H4+ dan Cl- yang Namun demikian sesuai dengan ntrasi rendah 1 % alam proses aerasi
Grafik 1. Pengaruh Persent Salah satu proses yang me adalah kesempurnaan pemisa (Fe), oleh karena itu proses sempurna yang selanjutnya ak Faktor yang mempengaruh kelarutan oksigen.Oksigen ya terjadinya korosi pada be bertambah dengan meningkat air. Kelarutan oksigen dalam tekanan, temperatur dan kand 1 atm dan temperatur kamar ppm dan kelarutannya bertambahnya temperatur da 2012).Penambahan Ammoniu menghambat reaksi Aerasi semakin tinggi konsentrasi A rendah kadar oksigen ya pengkaratan tersebut (Walter
Pengaruh Waktu dan Persentase Fe2O3pada Prose
Pengkaratan mengacu pada mengendap di dalam pori-por zat besi tinggi dalam produk r
2Fe 2Fe2+ + 4e-
O2 + 2H2O + 4e- 4OH
-Grafik 2. Pengaruh Persen
Dapat dilihat pada grafik 2 penurunan persentase Fe2O3. akhir proses adalah Fe yang entase TiO2 pada Waktu Aerasi
meningkatkan kandungan TiO2 isahan antara TiO2 dengan besi ses oksidasi besi harus berjalan a akan di leaching dengan H2SO4. uhi laju oksidasi besi adalah yang terlarut akan menyebabkan besi. korosi pada besi akan katnya kandungan oksigen dalam lam air merupakan fungsi dari andungan klorida. Untuk tekanan ar, kelarutan oksigen adalah 10 a akan berkurang dengan dan konsentasi garam (Junaidi, nium Klorida lebih dari 1% akan asi. Hal ini juga dikarenakan i Ammonium maka akan semakin yang terlarut dalam proses ter Hoecker, 1997).
Katalis NH4Cl terhadap
oses Aerasi
da proses di mana oksida besi pori ilmenite sehingga kadar total
proses kalsinasi Fe, Fe berubah menjadi Fe 2, dapat disimpulkan bahwa pada waktu 4 tidak signifkan bereaksi menjadi Fe2O3. S dilihat perancangan yang optimum pada pr batch adalah 4 jam. Pada pemilihan kons konsentrasi katalis yang paling efektif ada katalis NH4Cl sebesar 1%.
Proses oksidasibesi (Fe) oleh oksigen terlaru larutan NH4Cl encer. Amonium klorida manfaat dalam peningkatan laju korosi pengikatan NH4+ ini sangat penting un pasivasi (Mandyczewsky, 1997). Ion am menghapus lapisan pasif udara yang terbent besi selama proses aerasi.
Ammonium klorida ditambahkan sebagai mempercepat proses aerasi. Pengaruh ion klorida tentu saja sangat relevan dengan Dalam proses aerasi, besi teroksidasi cepat m komplek dengan penambahan ammonium keluar dari pori-pori (Kim et al, 1997). Mole berinteraksi langsung dengan atom besi un lapisan aktif yang terbentuk di permukaan kadar total komponen besi tinggi (pemb tinggi).
Pengaruh Waktu Aerasi terhadap Konver
Plot Konversi Besi (Fe) sebagai fungsi wak pada grafik 3.Dapat dilihat setiap jam reaksi akan terus meningkat, akan tetapi terja setelah 4 jam dan mulai stabil. Dari grafik dilihat peningkatan konversi yang tajam p berlangsung selama 4 jam. katalis yang efe adalah dengan komposisi 1% NH4Cl.
Grafik 3. Hubungan Konversi Fe deng
Konversi (XFe) = onsentrasi katalis, dalah konsentrasi
larut terjadi dalam rida memberikan si besi, tindakan untuk mencegah amonium mampu entuk pada logam
gai katalis untuk on amonium dan n proses Becher. t menjadi ion besi m dan kemudian olekul ammonium untuk menghapus an besi, sehingga bentukan korosi
versiFe
aktu ditunjukkan ksi maka konversi rjadi pelambatan fik tersebut dapat pada saat reaksi efektif digunakan
ngan Waktu
(1)
Dari Persamaan (1) d diperoleh dari berat Fe y banyaknya berat Fe mula-m merupakan berat besi mula-m Fe sisa dapat dihitung dari pada hasil kalsinasi dengan m adalah sempurna.
2Fe +
Pada reaksi di reaktor, Fe leaching dengan H2SO4 sehin berekasi menghasilkan seny proses, Fe yang masih belum berada pada padatan yang b yang kemudian dicuci menghilangkan sisa asam ya kembali terbentuk ketika pro dilakukan. Sehingga hasil ak yang tidak bereaksi di dalam
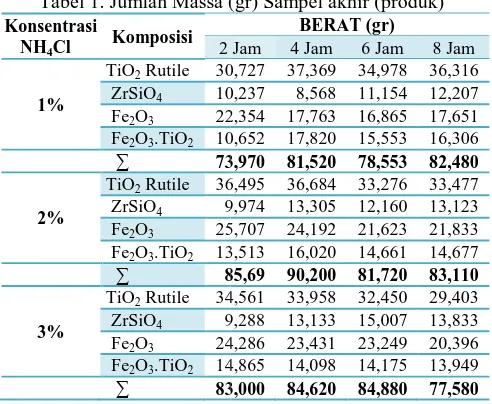
Hasil analisa GSAS XRD persentase, sedangkan ber ditimbang, sehingga diketahu reaksi).
Tabel 1. Jumlah Massa ( Konsentrasi
Prediksi Model Kinetika Re
Pada proses oksidasi besi re fase gas (udara O2) dan fase Lascaray (1949) reaksi pada sehingga kinetika reaksi dite gas ke dalam fase solid dan fase solid yang dapat dis kecepatan proses
Fe + ¾ O2 ½ Fe2O3 A + ¾ B ½
C
Kecepatan difusi gas ke fase -rB = kb (CB* - CB1) mgre mula dikurangi besi sisa. Berat ri jumlah Fe2O3 yang terbentuk n menganggap reaksi yang terjadi
O2 Fe2O3 roses kalsinasi pada suhu 800oC akhir Fe2O3 merupakan Fe sisa m reaktor.
RD dapat dinyatakan dalam berat awal dan akhir sudah hui berat awal dan akhir (setelah
a (gr) Sampel akhir (produk) BERAT (gr)
eaksidimungkinkan terjadi pada se solid (Fe), akan tetapi menurut da fase solid lah yang dominan ditentukan oleh kecepatan difusi an reaksi antara gas dan solid di disajikan ke dalam persamaan
ase solid:
Dengan :
CB* = konsentrasi gas di fase solid yang se konsentrasi gasdifasesolid atau CB*=k CB1 = konsentrasi gas di fase solid , mgrek / CB2 = konsentrasi gas di fase gas
kb = konstanta kecepatan difusi gas ke fase
Kecepatan reaksi di fase solid:
rB = rA = k1 CA CB1 dengan : CB1 = konsentrasi gas di fase solid
CA= konsentrasi solid (Fe)
Untuk mencari langkah yang mengontrol reaksi, disusun neraca massa gas dan neraca fase solid sebagai berikut :
= kb (CB* - CB1) – k1 CA CB1
Bila jumlah gas berlebihan dan transfer mas solid sangat cepat, maka fase solid diangga dengan gas, maka CB1 = CB*yang bernilai suhu tertentu,
= – k1 CA CB1
Karena udara yang diberikan berlebihan menjadi orde 1 semu, k1 CB1 = k’ sehingga :
= -k’ CA
(7)
ln#1 X& ln#1 X& y ( )
dimana:
k’ = konstanta kecepatan reaksi orde satu t = waktu reaksi, jam
(Le
Tabel 2. Hasil Perhitungan Konstanta Kece
Konsentrasi NH4Cl
t(x) Xa
1%
0 0
2 0,534 4 0,629 6 0,648 8 0,632
2%
0 0
2 0,464 4 0,495 6 0,549 8 0,545
3% 0 0
seimbang dengan =k CB2
/ g solid
ase solid, menit-1
(3)
rol pada kinetika aca massa solid di
(4)
assa gas ke fase ggap selalu jenuh ilai konstan pada
(5)
an, maka reaksi a :
(6)
(8) (9) (10)
atu semu, 1/jam
Levenspiel, 1999)
ecepatan Reaksi
Dari tabel2, diperoleh hasil k satu semu sebagai berikut:
k’ Fe pada variabel NH4C k’ Fe pada variabelNH4Cl k’ Fe pada variabel NH4C
Variabel yang Potensial
Pada Tabel 3 menunjukkan potensial terdapat pada var NH4Cl 1% karena mengandu sama dengan variabel lain setelah proses adalah 81,52 g 4 jam dengan katalis NH4Cl 1
Tabel 3. Persentase Sam
Konsentrasi NH4Cl
Komposisi
2 Ja
1% TiO2Rutile 41
ZrSiO4 13
Fe2O3 30
Fe2O3.TiO2 14
2% TiO2Rutile 42
ZrSiO4 11
Fe2O3 30
Fe2O3.TiO2 15
3% TiO2Rutile 41
ZrSiO4 11
Fe2O3 29
Fe2O3.TiO2 17
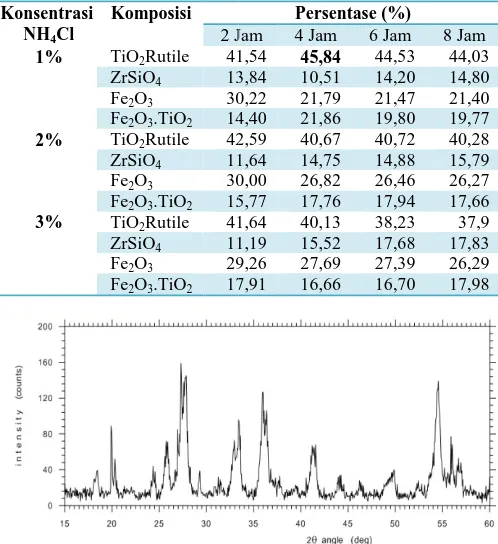
Gambar 1. Hasil Analis 1% NH
Dari gambar 1, banyak pea puncak tersebut dimiliki senyawa tertentu. TiO2 berad intesitas peak tersebut sang semua jenis senyawa yang ad kualitatif dengan software ma
Berikut ini adalah hasil analis baku Ilmenite dan hasil produ
114
2 0,493 4 0,511 6 0,515 8 0,575
l konstanta kecepatan reaksi orde
Cl 1% = 0,113995/jam Cl 2% = 0,087379/jam
Cl 3% = 0,087785/jam
an bahwa kondisi yang paling variabel 4 jam dengan katalis ndung 45,84% TiO2. Berat awal n yaitu 100 gr dan berat akhir 2 gr, terlihat dari tabel 1 variabel
l 1%.
ampel Ilmenite hasil Akhir
Persentase (%)
2 Jam 4 Jam 6 Jam 8 Jam
41,54 45,84 44,53 44,03
13,84 10,51 14,20 14,80
30,22 21,79 21,47 21,40
14,40 21,86 19,80 19,77
42,59 40,67 40,72 40,28
11,64 14,75 14,88 15,79
30,00 26,82 26,46 26,27
15,77 17,76 17,94 17,66
41,64 40,13 38,23 37,9
11,19 15,52 17,68 17,83
29,26 27,69 27,39 26,29
17,91 16,66 16,70 17,98
lisa XRD, Ilmenite variabel H4Cl 4 jam
eak puncak yang terlihat. Peak ki oleh komponen-komponen rada pada sudut 27,5 yang mana ngat tinggi. Untuk menentukan ada pada powder perlu di analisa
match.
menentukan komponen yang terkandung variabel tersebut.:
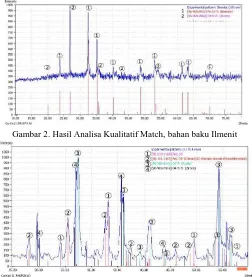
Gambar 2. Hasil Analisa Kualitatif Match, baha
Gambar 3. Hasil Analisa Kualitatif Match, Il
1% NH4Cl 4 jam
Dari gambar 2 dan 3 dapat dilihat TiO2 da dari bahan baku Ilmenite. Pada gambar 4.2 dimiliki oleh 2 komponen, yaitu Ilmenite peak nomer 1 dan ZrSiO4 pada peak nomer 4.3 peak tersebut dimiliki oleh 4 komponen peak nomer 3, Fe2O3 pada peak nomer (Fe2TiO5) pada peak nomer 2, dan ZrSiO4 pa 4. Pada gambar 4.3 TiO2 merupakan ko intensitasnya paling terlihat diantara kompo Untuk mengetahui presentase jumlah kom harus melakukan uji analisa kuantitatif (general structure analysis system) yang senyawa harus dikalibrasi dengan paramet masing – masing. Yaitu jenis kristal, sud kristal dan nilai x, y, z nya.
ng didalam hasil
ahan baku Ilmenit
Ilmenite variabel
dapat didapatkan 4.2 peak tersebut ite (FeTiO3) pada er 2. Pada gambar en yaitu TiO2 pada er 1, Fe2O3.TiO2
pada peak nomer komponen yang ponen yang lain. omponen tersebut dengan GSAS ang mana setiap eter kristalografi sudut kristal, kisi
CHI**2 = 1.732
GENLES Version Win32
Gambar 4. Hasil Analisa Kuanti
NH4Cl
Dari tabel 4 hasil analisa G kandungan Fe2O3.TiO2 pada menunjukkan proses reduk sehingga menyebabkan Fe2O menjadi Fe dan TiO2sehingg impuritas pada hasil produk T
Tabel 4. Hasil Analisa GSA
NH4Cl
Spesifikasi F
TiO2 ZrS
Nomer Fasa 1
Fraksi 7,77 0
Penggeseran -0,16 0
Fraksi berat 0,46 0
Yield tiap Variabel
Berat reaktan mula-mula = 10
Tabel 5. Yield Ilm
Variabel Konsentrasi
NH4Cl
jam
1%
2 4 6 8
2%
2 4 6 8
3%
2 4 6 8
Dari Tabel 5, terlihat bahwa variabel yang dihasilkan sebe dihasilkan masih sedikit. Hal yang dilakukan kurang e dihasilkan sedikit. Untuk m TiO2, perlu penambahan 3 efektifan peningkatan kemur magnetic separator pada pem zircon, hydrocyclone untu terbentuk setelah proses di r classifier untuk memastika terbawa kembali setelah prose
n32 Jun 13 02:16:45 2013
ntitatif GSAS, Ilmenite variabel 1% Cl, 4 jam
GSAS, terlihat masih terdapat adahasil akhir produk. Hal ini duksi yang kurang sempurna O3.TiO2 tidak terkonversi total gga pada akhir produk menjadi k TiO2.
SAS pada variabel Optimum (1% Cl, 4 jam)
Fasa/Unsur Fraksi
ZrSiO4 Fe2O3 Fe2O3.TiO2
2 3 4
0,39 0,62 0,62
0,37 -0,02 -0,01
0,11 0,22 0,22
100 gr
Ilmenite tiap Variabel
Produk (gr)
Yield = Produk / reaktan
73,97 0,7397
81,52 0,8152
78,55 0,7855
82,48 0,8248
85,69 0,8569
90,20 0,9020
81,72 0,8172
83,11 0,8311
83,00 0,8300
84,62 0,8462
84,88 0,8488
77,58 0,7758
wa yield dari masing - masing besar 70-90%, namun TiO2 yang al ini disebabkan karena proses efektif sehingga TiO2 yang meningkatkan hasil kandungan 3 buah alat yang membantu ke urnian TiO2 yaitu penambahan pemisahan raw material dengan ntuk memisakan Fe2O3 yang i reaktor bubble batchdan spiral tikan larutan Fe2(SO4)3 tidak
4.
KESIMPULAN
Dari hasil analisa XRD, titanium dioksida bahan baku Ilmenitedengan kemurnian men variabel yang potensial pada Proses Aerasi Katalis NH4Cl 1% dan waktu proses s Penambahan Katalis NH4Cl yang b mengurangi Persentase TiO2karena dapa reaksi oksidasi pada proses aerasi. Waktu ya untuk peningkatan TiO2 adalah 4 jam perubahan Fe menjadi Fe2O3 secara ef konsentrasi TiO2 tinggi. Konstanta kec besidengan katalis NH4Cl 1%, 2%, 3% ya 0,0874/jam; 0,0878/jam dan yield yang masing-masing variabel berkisar 70-90%.
Ucapan Terima Kasih
Ucapan terimakasih kami sampaikan kepa Nano Center Indonesia,khususnya Bap Taufiqqu Rachman, M.Eng yang sudah me dalam pembiayaan penelitian, peminjaman Penelitian Metalurgi LIPI dan juga pengu Badan Tenaga Nuklir Nasional (BATAN) Yuswono yang sudah membantu penulis sela penelitian.
DAFTAR PUSTAKA
[1] El-Hazek, N., A, T., El Sheikh Hydrometallurgical criteria for TiO2 Rosetta ilmenite by hydroc Hydrometallurgy., 87, 45-90.
sidaterbentuk dari encapai 45,84%, asi menggunakan selama 4 jam. berlebih justru pat menghambat yang paling baik m karena terjadi efektif sehingga kecepatan reaksi yaitu 0,114/jam; g dihasilkan dari
pada seluruh tim apak Dr. Nurul membantu penulis an lab di Pusat gujian sampel di serta Bapak Ir. selama melakukan
ikh, R., (2007),
2 leaching from rochloric acid.
[2] Fadli, A., (2004), Pe Dioksida (TiO2) dar Pengolahan Timah Di Skripsi, Teknik Kimia F [3] Hendratno, A., (199
Pertambangan di Wil Prosiding Lokakarya pengolahan Sumberday Jurusan Teknik Geolo Yogyakarta.
[4] Hoecker,W., (1997), P synthetic rutile. United [5] Hugo, v., (2012), synthe
Australia.
[6] Levenspiel, O., (1 Engineering Third Editi Amerika.
[7] Mark, J, W., (1999), C Ilmenite. Curtin Univer [8] Mandyczewsky, R.,
University of Western A [9] Sasikumar, C., S, D.,
(2007), Dissolution stud Manavalakurichi ilmen Hydrometallurgy., 88, 1 [10] Sumardi, C., (1999), Pe dari Ilmenit Hasil Sa Bangka. Prosiding Loka dan Pengolahan Sum Teknik, Jurusan Teknik Mada. Yogyakarta. [11] Zhang, W., Zhu, Z., Y
review of titanium Hydrometallurgy., 106,
116
Pembuatan Pigment Titanium dari Ilmenit Hasil Samping i PT Tambang Timah Bangka. ia FT UNRI, Indonesia.
999), Pengembangan Industri ilayah DIY Bagian Selatan. a Eksploitasi, Eksplorasi dan daya Mineral, Fakultas Teknik, logi. Universitas Gadjah Mada.
Process for the production of ed Stated Patent, No. 5601630.
thetic Rutile Production. Iluka’s,
(1999), Chemical Reaction dition. John Wiley & Sons : USA
, Catalysed Aeration of Reduced ersity of Technology. Australia. ., (1964), Honours Thesis, n Australia.
D., Srikanth, S., K, N., P, S., studies of mechanically activated enite with HCl and H2SO4. , 154-169.
Pembuatan Rutil (TiO2) Sintesis Samping Penambangan Timah okakarya Eksploitasi, Eksplorasi Sumberdaya Mineral. Fakultas nik Geologi Universitas Gadjah
, Yong, C., (2011), A literature um metallurgical processes.