BAB II
TINJAUAN PUSTAKA 2.1 Uraian Kacang Panjang
2.1.1 Daerah Tumbuh
Kacang Panjang merupakan tanaman perdu semusim. Daunnya majemuk, tersusun atas tiga helai. Batangnya liat dan sedikit berbulu. Akarnya mempunyai bintil yang dapat mengikat nitrogen (N) bebas dari udara. Hal ini bermanfaat untuk menyuburkan tanah (Haryanto, dkk., 1995).
Bunga kacang panjang berbentuk kupu-kupu. Ibu tangkai bunga keluar dari ketiak daun. Setiap ibu tangkai bunga mempunyai 3-5 bunga. Warna bunganya ada yang putih, biru, atau ungu. Bunga kacang panjang menyerbuk sendiri (Haryanto, dkk., 1995).
Tidak setiap bunga dapat menjadi buah, hanya 1-4 bunga yang dapat menjadi buah. Buahnya berbentuk polong bulat panjang dan ramping. Panjang polong sekitar 10-80 cm. Warna polong muda hijau sampai hijau keputihan setelah tua warna polong putih kekuningan. Polong yang muda sifatnya renyah dan mudah patah. Setelah tua menjadi liat. Pada satu polong dapat berisi 8-20 biji kacang panjang (Haryanto, dkk., 1995).
2.1.2 Klasifikasi Tanaman Kacang Panjang
Susunan klasifikasi tanaman kacang panjang secara lengkap menurut Haryanto, dkk., (1995) adalah sebagai berikut:
Kelas : Angiospermae Subkelas : Dicotyledonae Ordo : Rosales
Famili : Papilionaceae/Leguminosae/Fabaceae Genus : Vigna
Spesies : Vigna unguiculata (l.) Walp 2.1.3 Kandungan Kacang Panjang
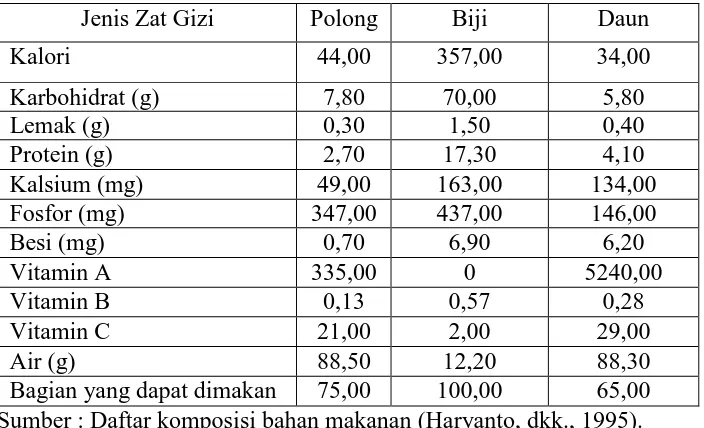
Menurut Haryanto (1995), kacang panjang penting sebagai sumber vitamin dan mineral. Sayuran ini banyak mengandung vitamin A, vitamin B, dan vitamin C terutama pada polong muda. Bijinya banyak mengandung protein, lemak dan karbohidrat. Dengan demikian komoditi ini merupakan sumber protein nabati yang cukup potensial. Pada tabel berikut di uraikan kandungan gizi pada polong, biji, dan daun kacang panjang.
Tabel 1. Komposisi Zat Gizi Kacang Panjang Per 100 gr Bahan. Jenis Zat Gizi Polong Biji Daun
2.2 Mineral
Tubuh tidak mampu mensintesa mineral sehingga unsur-unsur ini harus disediakan lewat makanan yang diperlukan dalam jumlah sedikit disebut muatan (trace element). Unsur-unsur mineral terdapat di dalam jaringan tulang, gigi dan protein. Mineral merupakan unsur esensial bagi fungsi normal sebagian enzim dan sangat penting dalam pengendalian komposisi cairan tubuh 65% adalah air dalam bobot tubuh. Mineral merupakan konstituen esensial pada jaringan, lemak, cairan dan steletan (yang mengandung mineral tubuh dalam proporsi yang besar) (Budiyanto, 2001).
Mineral merupakan bagian dari tubuh dan memegang peranan penting dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ maupun fungsi tubuh secara keseluruhan, juga berperan dalam berbagai tahap metabolisme, terutama sebagai kofaktor dalam aktivitas enzim-enzim, serta menjaga keseimbangan ion-ion tubuh (Almatsier, 2004).
Mineral digolongkan dalam mineral makro dan mineral mikro. Mineral makro adalah mineral yang dibutuhkan tubuh lebih dari 100 mg sehari seperti natrium, kalium, kalsium, magnesium, dan fosfor. Sedangkan mineral mikro adalah mineral yang dibutuhkan tubuh kurang dari 100 mg sehari seperti tembaga, mangan, besi, zink, dan iodium (Almatsier, 2004).
Menurut Budiyanto (2001), mineral dalam tubuh memiliki tiga fungsi yaitu:
2. Mineral membentuk garam-garam yang dapat larut sehingga dapat
mengendalikan komposisi cairan tubuh. Na dan Cl merupakan unsur penting dalam cairan ekstra seluler dan darah. Sedangkan Fe, Mg dan P merupakan unsur penting dalam cairan intraseluler.
3. Mineral turut membangun enzim dan protein dan merupakan bagian dari asam amino misalnya sistein.
2.2.1 Besi
Besi merupakan mineral makro yang paling banyak terdapat di dalam tubuh manusia dan hewan, yaitu sebanyak 3-5 gram di dalam tubuh manusia dewasa. Angka kecukupan besi untuk laki-laki dewasa 13 mg/hari dan untuk wanita dewasa 14-26 mg/hari. Sumber baik besi adalah makanan hewani, seperti daging, ayam dan ikan. Sumber baik lainnya adalah telur, serelia tumbuk, kacang-kacangan, sayuran hijau dan beberapa jenis buah (Altmatsier, 2004).
Menurut Budiyanto (2001), fungsi dari besi adalah sebagai berikut: 1. Untuk pembentukan hemoglobin baru.
2. Untuk mengembalikan hemoglobin kepada nilai normalnya setelah terjadi pendarahan.
3. Untuk mengimbangi sejumlah kecil zat besi yang secara konstant dikeluarkan oleh tubuh, terutama lewat urin, feces, dan keringat.
4. Untuk menggantikan kehilangan zat besi lewat darah tubuh.
2.2.2 Kalsium
Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh, yaiut 1,5 – 2 % dari berat badan orang dewasa atau kurang lebih sebanyak 1 kg. Di dalam cairan ekstraselular dan intraselular kalsium memegang peranan penting dalam mengatur fungsi sel, seperti untuk transmisi saraf, kontraksi otot, penggumpalan darah, dan menjaga permeabilitas membran sel (Almatsier, 2004).
Menurut Budiyanto (2001), fungsi lain dari kalsium ialah:
a. Dalam cairan jaringan berfungsi untuk pengendali kerja jantung serta otot skeleton.
b. Iribilitas syaraf otot
c. Proses pembekuan darah (dalam sintesis trombin)
d. Memberikan kekerasan dan ketahanan terutama pengeroposan
e. Transmisi impuls
f. Relaksasi dan Kontraksi
Angka kecukupan rata-rata sehari kalsium yang dianjurkan bagi orang dewasa ialah 500 – 800 mg/hari. Sumber utama kalsium adalah susu dan hasil susu, seperti keju. Ikan, serelia, kacang-kacangan dan sayuran hijau (Almatsier, 2004).
2.2.3 Magnesium
zat besi dalam ikatan hemoglobin di dalam darah pada manusia yaitu untuk pernafasan. Magnesium terlibat dalam berbagai proses metabolisme. Magnesium di dalam tulang lebih banyak merupakan cadangan yang siap dikeluarkan bila bagian lain dari tubuh membutuhkan. Magnesium mencegah kerusakan gigi dengan cara menahan kalsium di dalam email gigi (Altmatsier, 2004).
Menurut Budiyanto (2001), fungsi dari magnesium adalah sebagai berikut: a. Sebagai aktifator enzim peptidase dan enzim lain yang memecah gugus
phospat
b. Sebagai obat pencuci perut c. Meningkatkan tekanan osmotik d. Membantu mengurangi getaran otot
Orang dewasa pria membutuhkan magnesium sebanyak 350 mg/hari dan untuk dewasa wanita membutuhkan megnesium sebanyak 300 mg/hari.
2.2.4 Kalium
Kalium merupakan ion bermuatan positif, akan tetapi berbeda dengan natrium, kalium terutama terdapat di dalam sel. Perbandingan natrium dan kalium di dalam cairan intraselular adalah 1:10, sedangkan di dalam cairan ekstraselular 28:1. Sebanyak 95% kalium tubuh berada di dalam cairan intraselular (Almatsier,2004).
Menurut Budiyanto (2001), fungsi kalium diantaranya adalah sebagai berikut:
a. Digunakan sebagai indeks untuk lean body mass ( bagian badan tanpa lemak). b. Membantu menjaga tekanan osmotik.
Kalium memegang peranan penting dalam memelihara keseimbangan cairan dan elektrolit serta keseimbangan asam dan basa. Bersama kalsium, kalium berperan dalam transmisi saraf dan relaksasi otot. Di dalam sel, kalium berfungsi sebagai katalisator dalam banyak reaksi biologik, terutama dalam metabolisme energi dan sintesis glikogen dan protein (Almatsier,2004).
2.3 Spektrofotometri Serapan Atom.
Metode spektrofotometri serapan atom berdasarkan pada absorbsi cahaya oleh atom. Atom- atom akan menyerap cahaya pada panjang gelombang tertentu, tergantung pada sifat unsurnya. Dasar analisis menggunakan teknik spektrofotometri serapan atom adalah bahwa dengan mengukur besarnya absorbsi oleh atom analit, maka konsentrasi analit tersebut dapat ditentukan (Ganjar dan Rohman, 2007).
Spektrofotometri serapan atom digunakan untuk analisis kuantitatif unsur-unsur logam dalam jumlah sekelumit (trace) dan sangat sekelumit (ultratrace). Cara analisis ini memberikan kadar unsur logam tertentu dalam suatu sampel. Cara ini cocok untuk analisis sekelumit logam karena mempunyai kepekaan yang tinggi, pelaksanaanya relatif sederhana, dan interferensinya sedikit. Spektrofotometri serapan atom didasarkan pada penyerapan energi sinar oleh atom-atom netral dalam bentuk gas (Ganjar dan Rohman, 2007).
tersebut. Sebagai contoh kalsium menyerap radiasi pada panjang gelombang 422,7 nm, dan besi menyerap radiasi pada panjang gelombang 248,3 nm.Dengan menyerap radiasi, maka atom akan memperoleh energi sehingga suatu atom pada keadaan dasar dapat ditingkatkan menjadi ke tingkat eksitasi (Gandjar dan Rohman, 2007).
Secara eksperimental akan diperoleh puncak-puncak serapan sinar oleh atom-atom yang dianalisis. Garis-garis spektrum serapan atom yang timbul karena serapan radiasi yang menyebabkan eksitasi atom dari keadaan azas ke salah satu tingkat energi yang lebih tinggi disebut garis-garis resonansi (Resonance line). Garis-garis resonansi ini akan dibaca dalam bentuk angka oleh Readout (Gandjar dan Rohman, 2007).
Menurut Gandjar dan Rohman (2007) instrumentasi spektrofotometer serapan atom adalah sebagai berikut:
a. Sumber Sinar
Sumber sinar yang umum dipakai adalah lampu katoda berongga (hollow cathode lamp). Lampu ini terdiri atas tabung kaca tertutup yang
mengandungsuatu katoda dan anoda. Katoda berbentuk silinder berongga yang dilapisi dengan logam tertentu sesuai dengan logam yang diperiksa.
b. Sumber atomisasi
aerosol. Aerosol biasa dihasilkan oleh nebulizer (pengabut) yang dihubungkan ke nyala oleh ruang penyemprot (chamber spray).
i. Dengan nyala (Flame)
Nyala digunakan untuk mengubah sampel yang berupa cairan menjadi bentuk uap atomnya dan untuk proses atomisasi. Suhu yang dapat dicapai oleh nyala tergantung pada gas yang digunakan, misalnya untuk gas asetilen-udara suhunya sebesar 2200ºC. Sumber nyala asetilen-udara ini merupakan sumber nyala yang paling banyak digunakan. Pada sumber nyala ini asetilen sebagai bahan pembakar, sedangkan udara sebagai bahan pengoksidasi.
ii. Tanpa nyala (Flameless)
Pengatoman dilakukan dalam tungku dari grafit. Sejumlah sampel diambil sedikit lalu diletakkan dalam tabung grafit, kemudian tabung tersebut dipanaskan dengan sistem elektris dengan cara melewatkan arus listrik pada grafit. Akibat pemanasan ini, maka zat yang akan dianalisis berubah menjadi atom-atom netral dan pada fraksi atom ini dilewatkan suatu sinar
yang berasal dari lampu katoda berongga sehingga terjadilah proses penyerapan energi radiasi yang memenuhi kaidah analisis kuantitatif.
c. Monokromator
Monokromator merupakan alat untuk memisahkan dan memilihspektrumsesuai dengan panjang gelombang yang digunakan dalam analisis yang dihasilkan lampu katoda berongga.
Detektor digunakan untuk mengukur intensitas cahaya yang melewati tempat pengatoman.
e. Amplifier
Amplifier merupakan suatu alat untuk memperkuat signal yang diterima
dari detektor sehingga dapat dibaca alat pencatat hasil (Readout).
f. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai
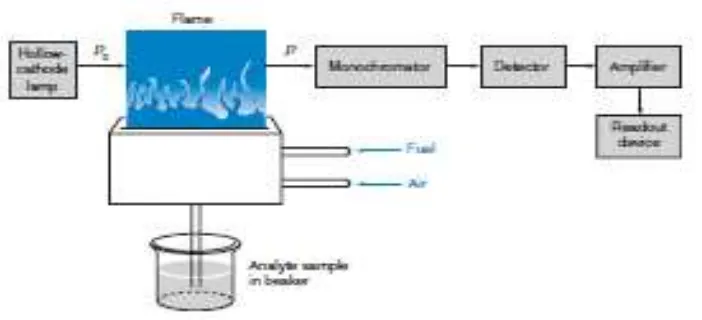
pencatat hasil. Hasil pembacaan dapat berupa angka atau berupa kurva yang menggambarkan absorbansi atau intensitas emisi. Komponen spektrofotometer serapan atom dapat dilihat pada Gambar 2.1.
Gambar 2.1 Gambar sistem peralatan spektrofotometer serapan atom(Harris, 2007).
a. Gangguan yang berasal dari matriks sampel yang mana dapat mempengaruhi banyaknya sampel yang mencapai nyala.
b. Gangguan kimia yang dapat mempengaruhi jumlah atau banyaknya atom yang terjadi di dalam nyala.
c. Gangguan oleh absorbansi yang disebabkan bukan oleh absorbansi atom yang dianalisis, yakni absorbansi oleh molekul-molekul yang tidak terdisosiasi. Adanya gangguan-gangguan di atas dapat diatasi dengan menggunakan cara-cara sebagai berikut:
1. Penggunaan nyala/suhu atomisasi yang lebih tinggi 2. Penambahan senyawa penyangga
3. Pengekstraksian yang akan dianalisis
4. Pengekstraksian ion atau gugus pengganggu
d. Gangguan oleh penyerapan non-atomik. Gangguan jenis ini berarti terjadinya penyerapan cahaya dari sumber sinar yang bukan berasal dari atom-atom yang akan dianalisis.
Menurut Gandjar dan Rohman (2007), pembentuk atom-atom netral dalam keadaan azas di dalamnyala seringterganggu oleh dua peristiwa kimia, yaitu:
a. Disosiasi senyawa-senyawa yang tidak sempurna disebabkan terbentuknya senyawa refraktorik (sukar diuraikan dalam api), sehingga akan
mengurangi jumlah atom netral yang ada di dalam nyala. b. Ionisasi atom-atom di dalam nyala akibat suhu yang digunakan
atom netral karena spektrum absorbansi atom-atom yang mengalami ionisasi tidak sama dengan spektrum atom dalam keadaan netral sehingga akan mempengaruhi hasil.
2.4 Validasi Metode Analisis
Menurut Harmita (2004), validasi metode analisis adalah suatu tindakan penilaian terhadap parametertertentuberdasarkanpercobaanlaboratorium untukmembuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya. Beberapaparameteranalisis yang harus dipertimbangkan dalam validasi metode analisis adalah sebagai berikut:
a. Kecermatan
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil analisis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan.
Kecermatan ditentukan dengan dua cara, yaitu:
i. Metode simulasi
ii. Metode penambahan baku
Metode penambahan baku (standard addition method) merupakan metode yang dilakukan dengan cara menambahkan sejumlah baku dengan konsentrasi tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode yang akan divalidasi. Hasilnya dibandingkan dengan sampel yang dianalisis tanpa penambahan sejumlah baku. Persen perolehan kembali ditentukan dengan menentukan berapa persen baku yang ditambahkan ke dalam sampel dapat ditemukan kembali (Harmita, 2004).
i. Keseksamaan (presisi)
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen (Harmita, 2004).
c. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuannya yang hanya mengukur zat tertentu secara cermat dan seksama dengan adanya komponen lain yang ada di dalam sampel (Harmita, 2004).
d. Linearitas dan rentang
e. Batas deteksi (LOD) dan batas kuantitasi (LOQ)
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan, sedangkan batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama (Harmita, 2004).
f. Ketangguhan Metode (Ruggedness)
Ketangguhan metode adalah derajat ketertiruan hasil uji yang diperoleh dari analisis sampel yang sama dalam berbagai kondisi uji normal, seperti laboratorium, analisis, instrumen, bahan pereaksi, suhu dan hari yang berbeda. Ketangguhan metode dinyatakan sebagai tidak adanya pengaruh perbedaan operasi atau lingkungan kerja terhadap hasil uji (Harmita, 2004).
g. Kekuatan (Robustness)