2
TINJAUAN PUSTAKA
2.1 Kemasan Cerdas/Intelligent Packaging
Intelligent packaging adalah sistem melekat sebagai label, yang dimasukkan ke dalam kemasan, atau dicetak ke bahan kemasan yang menawarkan kemungkinan ditingkatkan untuk memantau mutu produk (Kerry dan Buttler 2008). Kemasan cerdas ini dapat memberikan informasi kepada komsumen mengenai kerusakan produk apabila tidak diperlakukan sesuai syarat penyimpanan, melacak titik-titik kritis, dan memberikan informasi lebih rinci seluruh rantai suplai dan distribusi produk, sehingga keamanan produk konsumen lebih terjamin.Teknik kemasan cerdas yang ada saat ini di antaranya Time Temperature Indikator, indikator oksigen, indikator CO2, indikator patogen, indikator kesegaran, dan breakage indicator. Indikator ini bertujuan untuk menunjukkan apakah mutu produk di dalamnya sudah menurun dan mengalami kerusakan.
Galagan dan Su (2008) melaporkan bahan kemasan cerdas berupa indikator oksigen yang dapat berubah warna apabila terpapar oksigen. Kemasan cerdas ini berupa tinta fadable yang di aplikasikan pada kertas atau plastik. Tinta terbuat dari anthraquinone b-sulfonate yang dicampur dengan sodium hydrosulfite
sehingga berwarna merah, namun apabila tinta tersebut terpapar oleh oksigen maka akan berubah menjadi warna krem. Kesensitifan tinta tersebut terhadap oksigen disimpulkan dapat digunakan sebagai indikator untuk memantau kesegaran makanan. Hong dan Park (2000) melakukan penelitian mengenai kemasan cerdas untuk produk kimchi, dengan menggunakan perubahan suhu dan pH sebagai sensor untuk mendeteksi umur simpan dan fermentasi kimchi, seiring dengan perubahan suhu dan pH ruangan dalam kemasan maka akan menyebabkan perubahan warna pada kemasan cerdas yang diletakkan di dalam kemasan primer produk.
Rukchon(2011) melaporkan kemasan cerdas untuk mendeteksi kerusakan pada produk stik sayap ayam segar, dengan menggunakan senyawa volatil yang dihasilkan oleh mikroba yang terdapat pada stik sayap ayam segar selama penyimpanan dapat dijadikan indikator kerusakan pada stik sayap ayam segar yang dideteksi dengan perubahan warna pada kertas pH. Penelitian ini menghasilkan peningkatan jumlah senyawa volatil dalam hal ini amonia dapat menyebabkan perubahan warna kertas pH dari kuning menjadi hijau, sehingga dapat diaplikasikan sebagai kemasan cerdas untuk pendeteksi kerusakan stik sayap ayam segar. Selain pada ayam ada juga penelitian kemasan cerdas yang dilakukan oleh Kuswandi et al. (2012) yang menggunakan film polyaniline
sebagai indikator warna yang dapat berubah warna seiring dengan bertambahnya senyawa volatil yang dihasilkan oleh aktivitas mikroba pada penyimpanan ikan bandeng. Kemasan cerdas untuk produk ikan juga dilakukan oleh Hasnedi (2009), yang melakukan pengembangan kemasan cerdas (smart packaging) dengan sensor berbahan dasar kitosan-asetat, polivinil alkohol, dan pewarna indikator
bromthynol blue sebagai pendeteksi kebusukan filet ikan nila, menghasilkan smart packaging yang dapat secara visual memberikan perubahan warna dari kuning menjadi hijau kebiruan.
Sementara di negara-negara maju banyak paten dan merek komersial yang dikeluarkan mengenai kemasan cerdas, diantaranya 3M Monitor Mark yang merupakan merek paten dari USA yang mengembangkan kemasan cerdas berupa indikator kesegaran untuk produk dingin yang dapat mendeteksi adanya perubahan suhu selama penyimpanan produk, Fresh-check (USA) yang mengembangkan kemasan cerdas untuk mengetahui kerusakan pada produk segar. Pembuktian penggunaan 3M Monitor Mark dan Fresh-check dilakukan oleh Smolander (2004) yang menggunakan kedua merek kemasan cerdas komersial tersebut sebagai indikator kerusakan potongan ayam broiler segar yang dikemas dalam kemasan modifikasi atmosfir. Merek lain adalah OnVu yang merupakan produk dari Switzerland yang digunakan untuk mendeteksi kerusakan produk yang disimpan pada suhu dingin, juga COX Technologies yang mengeluarkan produk Fresh Tag untuk mendeteksi kesegaran seafood, yaitu berupa plastik chip
yang diletakkan di dalam kemasan dan akan berubah warna menjadi bright pink
ketika semakin banyaknya zat volatil yang terdapat pada ruangan di dalam kemasan seafood tersebut (Han et al. 2005). SensorQTM juga merupakan salah satu merek komersial yang merupakan kemasan cerdas yang dapat mendeteksi kebusukan pada daging segar yang disimpan dalam kemasan, SensorQTM bereaksi seiring dengan pertumbuhan bakteri pada daging selama penyimpanan, label akan berubah warna dari orange yang menujukkan daging masih segar dengan jumlah bakteri sedikit atau tidak ada menjadi warna sawo matang yang menujukkan daging sudah mengandung banyak mikroba atau busuk.
Penelitian tentang kemasan cerdas berupa indikator warna sebagai indikator kesegaran juga dilakukan oleh Nopwinyuwong et al. (2010), yaitu indikator warna yang berupa label film nylon/LLDPE dengan pewarna
bromothymol blue dan methyl red untuk memonitor kebusukan pada dessert khas Thailand yaitu golden drop. Penelitian tersebut melaporkan CO2 yang dihasilkan oleh produk selama penyimpanan dan juga penurunan pH dapat menyebabkan perubahan warna pada label indikator warna dari warna hijau sebagai indikator kesegaran dan warna orange sebagai indikator kebusukan.
Salah satu pengembangan dari Intelligent Packaging adalah Time-Temperature Indicators (TTI) dan Temperature indicators (TI). Alat ini akan menunjukkan jika terjadi kesalaham dalam suhu penyimpanan, dan juga menduga sisa umur dari produk pangan. TTI memberikan perubahan suhu yang masuk untuk menunjukkan kumulatif dari perubahan suhu di atas suhu kritis dan lamanya perubahan suhu itu terjadi. TI memberikan informasi apakah suhu berada di atas atau di bawah suhu kritis.
Pada umumnya, TTI dan TI ini berupa perubahan atau pergerakan warna, atau kombinasi keduanya (Kerry dan Buttler 2008). Label TI yang diletakkan pada kemasan pangan, akan memberikan informasi mengenai panas yang masuk ke dalam kemasan selama distribusinya, biasanya ditunjukkan dengan respon yang dapat dilihat dalam bentuk deformasi mekanis, perubahan warna atau pergerakan warna. Salah satu penelitian mengenai TTI dilakukan juga oleh Wanihsuksombat
et al. (2010) yang membuat prototypeTTI berdasarkan difusi asam laktat, dalam hal ini menggunakan agar yang akan berubah warna dari hijau menjadi merah seiring dengan penurunan pH, suhu dan waktu penyimpanan. Prototype ini dapat digunakan untuk melihat kinetika perubahan suhu penyimpanan pada produk buah dan sayuran segar. Vaikousi et al.(2008) juga mengembangkan prototype TTI
untuk produk yang disimpan pada suhu dingin, yaitu berupa TTI berupa media agar yang disimpan pada suhu 0-16oC yang akan mengalami perubahan warna dari merah menjadi kuning seiring dengan penurunan pH sebagai hasil dari metabolisme mikroba didalam media. Penelitian ini kemudian dilanjutkan oleh Vaikousi et al. (2009), yaitu dengan mengaplikasikan prototype TTI terhadap daging cincang yang disimpan pada suhu dan waktu tertentu.
2.2 Kitosan
Kitosan adalah produk terdeasetilasi dari kitin yang merupakan biopolimer alami kedua terbanyak setelah selulosa. Kitin termasuk polimer karbohidrat yang terdapat pada serangga, fungi, dan kulit crustacea seperti kepiting, rajungan, dan udang dengan rumus β (1,4)-2-asetamido-2-deoksi-D-glucopyranosa, sedangkan kitosan β (1,4)-2-amino-2-deoksi-D-glucopyranose (Sanford dan Hutchings 1987). Kitosan dapat diperoleh dari limbah industri pengolahan udang. Selama ini limbah udang baru dimanfaatkan oleh industri kecil dalam pembuatan terasi, kerupuk udang, petis, dan campuran pakan ternak (Kim 2004). Kitosan telah lama digunakan sebagai edible film dan bahan alami untuk pharmaceutical, medical,
pembungkus kertas, dan industri pengolahan pangan (Sanford dan Hutchings 1987). Penggunaan kitosan sebagai pelapis pelindung antara lain sebagai pelapis semipermeabel terhadap perubahan fisik kimia pada sayuran dan buah selama penyimpanan. Struktur kimia kitin dan kitosan dapat dilihat pada Gambar 1.
Gambar 1 Struktur kimia kitin dan kitosan
Hoagland dan Parris (1996) mengemukakan alasan dalam membuat film dengan bahan dasar kitosan adalah : (i) kitosan merupakan turunan kitin, polisakarida paling banyak di bumi setelah selulosa; (ii) kitosan dapat membentuk film dan membran dengan baik; dan (iii) sifat kationik selama pembentukan film merupakan interaksi elektrostatik dengan anionik. Film dengan bahan dasar kitosan mempunyai sifat yang kuat, elastis, fleksibel dan sulit untuk dirobek sebanding dengan polimer komersial dengan kekuatan sedang (Buttler et al. 1996).
Kitosan memiliki gugus amino bebas polikationik, pengkelat dan pembentuk dispersi dalam larutan asam asetat. Apabila kitosan dilarutkan dalam asam maka kitosan akan menjadi polimer kationik dengan struktur linear sehingga dapat digunakan dalam proses flokulasi dan pembentuk film (Rinaudo 2006). Film sendiri sebenarnya merupakan salah satu bentuk polimer yang mudah dibentuk. Proses pembentukan polimer disebut sebagai proses polimerisasi. Polimer yang berupa larutan encer memiliki rantai bebas bergerak, sehingga kemungkinan terbentuk konfigurasi rantai yang beragam. Akan tetapi polimer dalam bentuk padat memiliki rantai tidak teratur sehingga gerakan dan konfigurasinya terbatas (Sumarto 2008).
Film yang terbuat dari bahan kitosan memiliki banyak keunggulan, antara lain sifat biodegradable yang telah dibuktikan Makarios-Laham dan Lee (1995). Di dalam tanah, PE-chitosan film memiliki tingkat degradasi lebih tinggi dibandingkan film komersial dengan bahan dasar tepung kanji. Selain itu Ban et al. (2005) membuktikan bahwa kitosan dengan konsentrasi 28 % mampu memberi kekuatan tarik 10 kali lipat dari film tepung kanji komersial. Sementara Chen et al. (2007) telah meneliti mengenai karakteristik ikatan yang terjadi pada film kitosan dan PVA menemukan bahwa pembentukan film kitosan dan PVA adalah melalui interaksi ikatan hidrogen antara kitosan dan PVA membuat struktur kimia film yang dihasilkan sangat kokoh yaitu ikatan hidrogen antar molekul antara NH3+ pada struktur khitosan dan OH- pada polivinil alkohol. Gugus amino (NH2) pada khitosan telah diprotonasi menjadi NH3+ dalam larutan asam asetat, dan gugus OH- pada polivinil alkohol akan berikatan dengan NH3+ membentuk ikatan hidrogen (Xu et al. 2004). Oleh karena itu pengembangan film dengan bahan kitosan dan PVA sangat potensial digunakan sebagai matrik pembawa warna untuk kemasan cerdas dengan indikator warna.
2.3 Polivinil Alkohol (PVA)
Polivinil alkohol adalah suatu kopolimer vinil alkohol yang tersusun dari komonomer unit vinil seperti ethylene dan prophylene. Pembentukan polivinil alkohol dilakukan melalui proses hidrolisis (saponifikasi) dari polivinil asetat. Reaksi ini dapat berjalan dengan adanya katalis yaitu garam palladium (II) klorida (Schonberger et al. 1997). Polivinil alkohol merupakan polimer sintetik yang mudah diuraikan secara biologi (biodegradable) dan tidak beracun. Pada pengembangannya, polivinil alkohol sudah diaplikasikan dalam bidang kesehatan, pelapis bahan, bahan pembuat detergen, lem, serta pengemulsi (Hodgkinson dan Taylor 2000).
Polivinil alkohol berbentuk serbuk yang berwarna putih dan dapat larut dalam air pada suhu 80oC serta memiliki densitas sebesar 1.20 – 1.30 g/cm3 (Sheftel, 2000). Polivinil alkohol dapat digunakan sebagai bahan pembuatan kemasan plastik film. Polivinil alkohol memiliki kuat sobek sekitar 147 – 834 N/mm, kuat tarik sebesar 44 – 64 MN/m2, serta persen pemanjangan sebesar 150 – 400 %. Dengan karakteristik tersebut, polivinil alkohol dapat dibentuk menjadi kemasan plastik film yang biodegradable (Hodgkinson dan Taylor 2000).
2.4 Stabilitas Warna Antosianin
Struktur dan konsentrasi antosianin merupakan salah satu faktor yang mempengaruhi stabilitas warna antosianin. Antosianin umumnya lebih stabil pada larutan asam dibandingkan pada larutan netral atau alkali. Dalam keadaan asam, struktur dominan antosianin berada dalam bentuk inti kation flavium yang terprotonisasi dan kekurangan elektron. Peningkatan nilai pH menyebabkan kation flavilum menjadi tidak stabil dan mudah mengalami transformasi struktural menjadi senyawa tidak bewarna seperti kalkon ( Jackman dan Smith 1996).
Oksigen dapat menstimulasi terjadinya proses degradasi antosianin secara langsung dan tidak langsung. Secara langsung oksigen mampu menyebabkan oksidasi antosianin membentuk senyawa tidak berwarna yang menurunkan stabilitas warna antosianin. Secara tidak langsung senyawa hidroksiradikal mampu menyebabkan oksidasi pada struktur antosianin membentuk senyawa tidak berwarna seperti kalkon yang merupakan indikator degradasi warna antosianin (Ningrum 2005).
Cahaya juga dapat menyebabkan terjadinya proses degradasi antosianin. Cahaya memiliki energi tertentu yang mampu menstimulasi terjadinya reaksi fotokimia (fotooksidasi) dapat menyebabkan pembukaan cincin karbon nomor dua. Pada akhirnya reaksi fotokimia (fotooksidasi) tersebut mampu membentuk senyawa yang tidak berwarna seperti kalkon yang merupakan indikator degradasi warna antosianin (Ningrum 2005). Degradasi lanjutan antosianin dapat membentuk senyawa turunan lain yang tidak berwarna seperti 2,4,6
trihidroksibenzaldehida dan asam benzoate tersubtitusi lainnya. (Jackman dan Smith 1996).
Suhu juga merupakan faktor yang mempengaruhi kestabilan antosianin. Peningkatan suhu pengolahan hingga penyimpanan dapat mengakibatkan kerusakan dan perubahan warna antosianin secara cepat, yaitu melalui tahapan : (i) terjadinya hidrolisis pada ikatan glikosidik antosianin dan menghasilkan aglikon-aglikon yang labil; dan (ii) terbukanya cincin aglikon sehingga terbentuk gugus karbinol dan kalkon yang tidak berwarna. Selanjutnya menurut Jackman dan Smith (1996), senyawa kalkon dapat mengalami degradasi membentuk senyawa tidak berwarna yang lebih sederhana yaitu asam karboksilat seperti asam benzoat tersubtitusi dan karboksi-aldehida seperti 2,4,6 trihidroksibenzaldehida.
2.5 Tanaman Erpa (Aerva sanguinolenta)
Salah satu tanaman yang merupakan sumber potensial pewarna antosianin adalah daun tanaman erpa (Aerva sanguinolenta) yang termasuk kedalam suku
Amaranthaceae dan genus Aerva. Tanaman ini memiliki nama dagang atau nama umum sambang colok. Tanaman erpa memiliki beberapa nama daerah yaitu Ki Sambang (Sunda), Sambang Colok (Jawa) dan Rebha et raedhan (Madura). Menurut Mardisiswojo dan Harsono (1985), tanaman ini tumbuh liar di halaman dan di ladang-ladang sampai di dataran setinggi kira-kira 1000 m dari permukaan laut. Ada juga yang ditanam orang di halaman-halaman sebagai tanaman hias. Heyne (1987) menambahkan bahwa tanaman sambang colok merupakan tanaman berbatang lemas dan tingginya sekitar 0.3-2 m. Daun sambang colok berbentuk
bulat hingga meruncing, bertepi rata dan berbulu, warnanya merah-coklat atau ungu. Bunganya berwarna merah atau merah muda. Daun inilah yang digunakan sebagai pewarna alami. Kandungan yang terdapat dalam daun sambang colok yaitu mengandung senyawa alkaloid, minyak atsiri, dan flavonoid(Restanti 1992).
Tanaman erpa merupakan tanaman berpotensi besar untuk dikembangkan sebagai pewarna antosianin terutama untuk produksi dalam skala besar, karena tanaman ini (i) memiliki umur panen relatif singkat, (ii) tahan terhadap hama dan penyakit (iii) mudah dibudidayakan dan dapat diproduksi sepanjang tahun (Ningrum 2005).
Gambar 2 Tanaman erpa (Aerva sanguinolenta)
2.5 Pengukuran Warna
Warna adalah spektrum cahaya yang dipantulkan oleh benda yang kemudian ditangkap oleh indra penglihatan kita (yakni mata) lalu diterjemahkan oleh otak sebagai sebuah warna tertentu. Warna yang diterima jika mata memandang objek yang disinari berkaitan dengan tiga faktor: sumber sinar, ciri kimia dan fisika objek, dan sifat-sifat kepekaan spektrum mata (Putri 2012). Pada produk pangan warna merupakan faktor yang menentukan mutu, indikator kematangan, indikator kesegaran dan juga indikator kerusakan pangan.
Terdapat berbagai metode dan alat yang bisa digunakan untuk pengukuran warna, beberapa contoh alat yang bisa digunakan dalam pengukuran warna adalah kromameter dan spektrofotometer. Kromameter biasanya digunakan untuk sampel padat sedangkan spektrofotometer digunakan untuk sampel dalam bentuk cair. Kromameter memiliki prinsip kerja berdasarkan pemantulan warna yang dihasilkan oleh sampel. Lampu getar yang terdapat di dalam kromameter akan memancarkan sinar xenon dan menghasilkan penyebaran serta penerangan cahaya yang merata pada permukaan sampel. Enam buah fotosel silikon yang memiliki sensitifitas tinggi dan filter untuk mencocokkan dengan respon standar CIE (Commission Internationale d'Eclairage) digunakan sebagai sistem pengukuran umpan balik berkas ganda untuk mengukur sinar yang dipantulkan. Kromameter dapat mendeteksi setiap deviasi sinar spectral yang berasal dari pancaran lampu getar xenon yang bekerja secara otomatis. Pada umumnya sistem
output data hasil pengukuran adalah tiga output yaitu sistem warna CIE; sistem warna Hunter Lab; dan sistem warna CIELAB (Joshi dan Brimellow 2002). Sistem CIELAB, terdapat beberapa atribut nilai warna yang terdiri dari nilai L, a, b, ohue, C, dan ∆E (MacDougall 2002).
Nilai L menunjukkan tingkat kecerahan warna dengan interval nilai 0 (hitam) hingga 100 (putih). Nilai a merupakan nilai yang menunjukkan cahaya
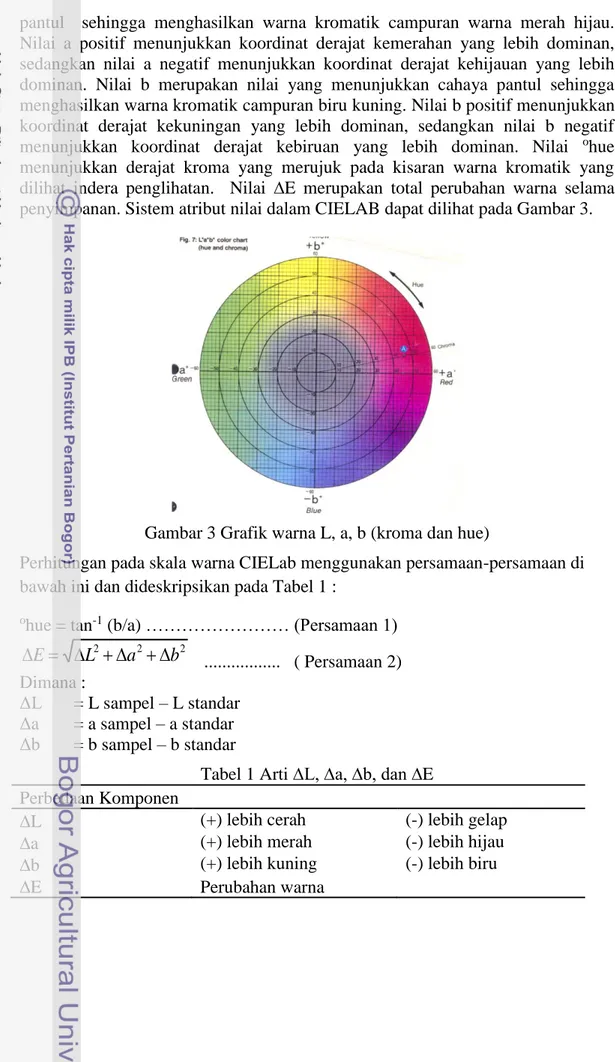
pantul sehingga menghasilkan warna kromatik campuran warna merah hijau. Nilai a positif menunjukkan koordinat derajat kemerahan yang lebih dominan, sedangkan nilai a negatif menunjukkan koordinat derajat kehijauan yang lebih dominan. Nilai b merupakan nilai yang menunjukkan cahaya pantul sehingga menghasilkan warna kromatik campuran biru kuning. Nilai b positif menunjukkan koordinat derajat kekuningan yang lebih dominan, sedangkan nilai b negatif menunjukkan koordinat derajat kebiruan yang lebih dominan. Nilai ohue menunjukkan derajat kroma yang merujuk pada kisaran warna kromatik yang dilihat indera penglihatan. Nilai ∆E merupakan total perubahan warna selama penyimpanan. Sistem atribut nilai dalam CIELAB dapat dilihat pada Gambar 3.
Gambar 3 Grafik warna L, a, b (kroma dan hue)
Perhitungan pada skala warna CIELab menggunakan persamaan-persamaan di bawah ini dan dideskripsikan pada Tabel 1 :
ohue = tan-1 (b/a) ……… (Persamaan 1) 2 2 2 b a L E ... ( Persamaan 2) Dimana : ΔL = L sampel – L standar Δa = a sampel – a standar Δb = b sampel – b standar
Tabel 1 Arti ∆L, ∆a, ∆b, dan ∆E Perbedaan Komponen
∆L (+) lebih cerah (-) lebih gelap ∆a (+) lebih merah (-) lebih hijau ∆b (+) lebih kuning (-) lebih biru ∆E Perubahan warna