Media Exacta Volume 10 No.2 Juli 2010
STUDI KINETIKA DEGRADASI PARAQUAT
(1,1-DIMETIL-4,4-BIPIRIDILIUM) DALAM LINGKUNGAN TANAH
PERTANIAN KABUPATEN KUPANG
1
Hermania Em Wogo*, Sherlly M.F. Ledoh* , Philiphi de Rozari*
ABSTRAK
Telah dilakukan penelitian tentang kajian kinetika degradasi paraquat dalam media
filtrat tanah pertanian kota Kupang pada dua kondisi, yaitu kondisi gelap dan terang
dengan penyinaran cahaya matahari secara langsung 8 jam perhari. Untuk mempelajari
pengaruh material tanah dan mikroorganisme dilakukan proses degradasi dalam dua
belas media yaitu media akuades steril dan tidak steril, media air sumur steril dan tidak
steril, media filtrat tanah Oematanunu steril dan tidak steril, media filtrat tanah Oesao
steril dan tidak steril, media filtrat tanah Nonbaun steril dan tidak steril, serta media
filtrat tanah Takari steril dan tidak steril. Pada setiap interval waktu tertentu, konsentrasi
paraquat tersisa ditentukan dengan spektrofotometer UV-Vis, dengan mengukur
absorbansi larutan hasil reduksi oleh natrium dithionit dalam suasana basa pada λ
maks=
604 nm. Hasil penelitian menunjukkan bahwa sinar matahari dapat meningkatkan laju
degradasi paraquat lebih besar dibandingkan degradasi paraquat akibat pengaruh
material tanah dan mikroorganisme. Degradasi paraquat dalam media yang dikaji
mengikuti kinetika degradasi orde satu. Konstanta laju degradasi dalam media filtrat
tanah Takari tidak steril (0,07467 ± 0,00556 hari
-1) > filtrat tanah Oesao tidak steril
(0,07281 ± 0,00527 hari
-1) > filtrat tanah Nonbaun tidak steril (0,07264 ± 0,00383 hari
-1
) > filtrat tanah Oematanunu tidak steril (0,06998 ± 0,00336 hari
-1) > filtrat tanah
Takari steril (0,06794 ± 0,00320 hari
-1) > filtrat tanah Oesao steril (0,06702 ± 0,00537
hari
-1) > air sumur tidak steril (0,06217 ± 0,00317 hari
-1) > filtrat tanah Nonbaun steril
(0,06148 ± 0,00319 hari
-1) > filtrat tanah Oematanunu steril (0,06086 ± 0,00285 hari
-1)
> air sumur steril (0,04720 ± 0,00182 hari
-1) > akuades tidak steril (0,03458 ± 0,00252
hari
-1) > akuades steril (0,02984 ± 0,00408 hari
-1).
Media Exacta Volume 10 No.2 Juli 2010
P
estisida merupakan salah satu bahan kimia yang banyak memberikan jasanya dalam bidang pertanian bahkan telah menjadi bagian dari sistem pertanian di Indonesia. Pestisida adalah semua zat kimia dan bahan lain serta jasad renik dan virus yang dipergunakan sebagai pemberantas atau pencegah hama atau penyakit yang dapat merusak tanaman atau hasil pertanian (Peraturan pemerintah No.7 Tahun 1973 dalam Sudarmo, 1988). Pestisida sering menjadi pilihan utama para petani dalam memberantas organisme pengganggu tanaman, sebab pestisida mempunyai daya bunuh yang tinggi, penggunaannya mudah dan hasilnya cepat diketahui. Penggunaan pestisida yang semakin meningkat dari tahun ke tahun juga disebabkan oleh formulasi produk pestisida yang telah terdaftarkan dan diizinkan penggunaannya di Indonesia semakin banyak (Sudarmo, 1988). Kebutuhan pestisida akan terus meningkat sebelum ditemukan adanya cara-cara lain yang lebih baik dalam mengendalikan organisme penggangu tanaman yang menyebabkan menurunnya produktivitas pertanian.Herbisida adalah salah satu jenis pestisida yang mengandung senyawa kimia beracun dan digunakan untuk mengendalikan gulma atau tumbuhan penggangu yang tidak dikehendaki. Karena herbisida aktif terhadap tumbuhan, maka herbisida bersifat fitotoksik. Penggunaan herbisida juga menguntungkan dalam menghemat waktu dan tenaga kerja.
Salah satu jenis herbisida yang banyak diproduksi dan dipasarkan serta digunakan secara luas di berbagai Negara termasuk di Indonesia adalah gramoxone. Bahan aktif gramoxone adalah paraquat (1,1-dimetil-4,4-bipirilidium). Paraquat merupakan salah satu herbisida golongan ammonium kuartener yang merupakan herbisida kontak (Sudarmo, 1988) dan bersifat tidak selektif (Bangun dan Pane, 1984). Paraquat dikenal sebagai senyawa yang sangat toksik. Keberadaannya di dalam tanah (20 ppm) mampu menghambat pertumbuhan bakteri Azetobacter dan Rhizobium yang berperan dalam fiksasi nitrogen sehingga dapat menghambat kesuburan tanah. Paraquat juga diketahui menghambat pertumbuhan bakteri E.coli dan alga di dalam tanah.
Penggunaan paraquat yang semakin meningkat dalam jangka panjang dapat mengganggu keseimbangan ekosistem oleh karena keberadaan residunya di dalam tanah. Jika hal tersebut dibiarkan berlanjut akan menimbulkan permasalahan lingkungan yang serius. Oleh karena itu perlu dilakukan penelitian guna memahami perilaku paraquat dalam tanah untuk mencegah bahaya yang ditimbulkannya terhadap lingkungan.
Degradasi merupakan salah satu proses selain adsorpsi dan desorpsi yang sangat penting untuk memperkirakan prilaku herbisida di dalam tanah, seperti penentuan laju dan mekanisme paraquat sehingga dapat digunakan sebagai bahan masukan untuk mengurangi dampak negatif penggunaan paraquat di lingkungan. Diketahui bahwa sinar matahari dapat meningkatkan jumlah paraquat yang terdegradasi, penyinaran selama 50 hari (± 8 jam/hari)
Media Exacta Volume 10 No.2 Juli 2010
mampu mendegradasi paraquat sebesar 76,91-96,77 % tergantung medianya (Wogo, 2004). Oleh karena itu dilakukan penelitian mengenai degradasi paraquat pada tanah Kota Kupang guna memperkirakan perilaku paraquat di dalam tanah yang dipengaruhi oleh material tanah dan keberadaan mikroorganisme. Sampel tanah yang diambil berasal dari empat lokasi yang berada di Kota Kupang yaitu : Desa Oematanunu Kecamatan Kupang Barat, Desa Oesao Kecamatan
Kupang Timur, Desa
Nonbaun Kecamatan Fatuleu dan Desa Takari Kecamatan Takari.
METODE PENELITIAN Alat dan Bahan Penelitian
Peralatan yang digunakan dalam penelitian ini adalah: spektrofotometer UV-Vis, oven, ayakan 60 dan 80 mesh, neraca analitik, sentrifius fischer, botol film, kertas karbon, kertas saring Whatman 42, pH meter, shaker, autoklaf, desikator dan peralatan penunjang berupa alat-alat gelas laboratorium.
Bahan yang digunakan dalam penelitian ini adalah: tanah pertanian yang berasal dari Kota Kupang (sampel tanah diambil dari empat lokasi yang mewakili jenis tanah yang dominan di Kota Kupang, yaitu : Desa Oematanunu Kecamatan Kupang Barat, Desa Oesao Kecamatan Kupang Timur, Desa Nonbaun Kecamatan Fatuleu dan Desa Takari Kecamatan Takari), larutan gramoxone 276 g/L, kristal natrium hidroksida, kristal natrium dithionit, kertas saring Whatman 42, air sumur dan akuades.
Cara Kerja
Preparasi sampel tanah pertanian
Sampel diambil pada kedalaman 0-30 cm dari permukaan tanah dan merupakan top soil. Sampel tanah dikering anginkan dan diayak menggunakan ayakan 60-80 mesh. Kemudian hasil ayakan dioven ± 4 jam pada suhu 70 oC untuk menurunkan kadar air dalam tanah. Jika belum digunakan untuk penelitian, tanah disimpan dalam desikator.
Persiapan pembuatan sampel
a. Seratus gram tanah pertanian desa Oematanunu Kecamatan Kupang Barat dicampur dengan satu liter air sumur sedikit demi sedikit dan diaduk dengan menggunakan shaker selama ± 3 jam. Campuran didiamkan selama ± 24 jam, disentrifius dan disaring dengan menggunakan kertas saring Whatman 42. Dengan cara yang sama dibuat sampel dari tanah pertanian Desa Oesao Kecamatan Kupang Timur, Desa Nonbaun Kecamatan Fatuleu dan Kecamatan Takari.
b. Lima ratus mililiter hasil penyaringan disterilkan dengan autoklaf. Selain itu dilakukan sterilisasi juga untuk akuades dan air sumur sebagai pembanding.
Media Exacta Volume 10 No.2 Juli 2010
c. Wadah yang digunakan adalah botol film sebanyak 480 buah. Sebelum digunakan, botol film dicuci dan dikeringkan. Dua ratus empat puluh botol diantaranya dibalut kertas karbon untuk kondisi gelap.
d. Membuat media A yaitu larutan hasil penyaringan tanpa sterilisasi. Diambil 1,1 mL larutan paraquat 2760 mg/L (hasil pengenceran 100 kali paraquat stok) dan diencerkan sampai 100 mL dengan larutan hasil penyaringan tanpa sterilisasi sehingga diperoleh larutan paraquat dengan konsentrasi 30,36 mg/L. Pengenceran dilakukan sebanyak empat kali sehingga diperoleh 400 mL larutan paraquat dengan pelarut filtrat tanah pertanian Desa Oematanunu Kecamatan Kupang Barat tidak steril 30,36 mg/L.
e. Membuat media B yaitu larutan hasil penyaringan dengan sterilisasi dengan cara yang sama seperti media A sehingga diperoleh 400 mL larutan paraquat dengan pelarut filtrat tanah pertanian Desa Oematanunu Kecamatan Kupang Barat yang disterilkan sehingga konsentrasinya 30,36 mg/L.
f. Media C dan D dibuat dari filtrat tanah pertanian Desa Oesao Kecamatan Kupang Timur tanpa sterilisasi dan dengan sterilisasi yang konsentrasinya 30,36 mg/L.
g. Media E dan F dibuat dari filtrat tanah pertanian Desa Nonbaun Kecamatan Fatuleu tanpa sterilisasi dan dengan sterilisasi yang konsentrasinya 30,36 mg/L.
h. Media G dan H dibuat dari filtrat tanah pertanian Desa Takari Kecamatan Takari tanpa sterilisasi dan dengan sterilisasi yang konsentrasinya 30,36 mg/L.
i. Membuat media I yaitu akuades steril dengan cara yang sama seperti media A sehingga diperoleh 400 mL larutan paraquat dengan pelarut akuades steril sehingga konsentrasinya 30,36 mg/L.
j. Membuat media J yaitu akuades tidak steril dengan cara yang sama seperti media A sehingga diperoleh 400 mL larutan paraquat dengan pelarut akuades tidak steril sehingga konsentrasinya 30,36 mg/L.
k. Membuat media K yaitu air sumur steril dengan cara yang sama seperti media A sehingga diperoleh 400 mL larutan paraquat dengan pelarut air sumur steril sehingga konsentrasinya 30,36 mg/L.
l. Membuat media L yaitu air sumur tidak steril dengan cara yang sama seperti media A sehingga diperoleh 400 mL larutan paraquat dengan pelarut air sumur tidak steril sehingga konsentrasinya 30,36 mg/L.
m. Larutan dari tiap media (A, B, C, D, E, F, G, H, I, J, K, L) masing-masing diambil 10 mL dan dimasukan ke dalam botol film sehingga terdapat 40 wadah dimana 20 wadah tanpa kertas karbon dan 20 wadah lain dibalut seluruh permukaan botolnya dengan kertas karbon untuk kondisi gelap.
Media Exacta Volume 10 No.2 Juli 2010
n. Seluruh sampel disinari dengan sinar matahari. Sampel yang dikondisikan untuk kondisi terang saat dijemur harus dibuka tutupan botolnya sehingga sinar matahari dapat masuk tanpa dihalangi. Sedang yang dikondisikan untuk kondisi gelap tetap tertutup seluruh permukaannya dengan kertas karbon. Penjemuran dilakukan selama 8 jam sehari dengan waktu antara jam 07:00 sampai 15:00 WITA. Kehilangan volume karena penguapan segera diganti sesudah dilakukan penjemuran sehingga volume sampel tetap. Sampel diambil untuk dianalisis pada hari ke 0, 1, 2, 5, 7, 10, 14, 26, 38 dan 50. Setiap pengambilan sampel langsung dilakukan preparasi dan ditentukan jumlah paraquat hari itu juga.
Penetapan panjang gelombang maksimum
a. Diambil 1 mL larutan paraquat stok (konsentrasi 276 gram/L) dan diencerkan 100 kali dengan akuades sehingga diperoleh larutan paraquat dengan konsentrasi 2760 mg/L.
b. Diambil 1,1 mL paraquat 2760 mg/L dan diencerkan 100 kali dengan akuades sehingga diperoleh larutan paraquat dengan konsentrasi 30,36 mg/L.
c. Ditimbang 0,05 gram natrium dithionit dan dilarutkan dengan 5 mL larutan NaOH 4 % b/v sehingga diperoleh larutan natrium dithionit 1 % dalam NaOH 4 % b/v.
d. Dari 10 mL larutan paraquat 30,36 mg/L kemudian ditambah 2 mL larutan 1 % natrium dithionit dalam NaOH 4 % dan direkam spektra absorbansinya pada λ antara 500 sampai 800 nm dengan menggunakan spektrofotometer. Hasil pengukuran absorbansi ditampilkan dalam bentuk grafik A vs λ dan dapat ditentukan panjang gelombang maksimumnya.
Penetapan konsentrasi paraquat dalam sampel dengan spektrofotometer
a. Pembuatan kurva standar untuk digunakan pada saat menetapkan konsentrasi sampel.
1. Paraquat dengan konsentrasi 27,6 mg/L diambil masing-masing 1,0; 2,0; 3,0; 4,0 dan 6,0 mL dan dimasukan pada labu takar 10 mL kemudian diencerkan dengan akuades, sehingga diperoleh seri larutan paraquat dengan konsentrasi berturut-turut: 2,76; 5,52; 8,28; 11,04; 13,8 dan 16,56 mg/L. Diambil juga 1,0 mL paraquat 27,6 mg/L dan dimasukan dalam labu takar 25 mL kemudian diencerkan dengan akuades sehingga diperoleh larutan paraquat dengan konsentrasi 1,104 mg/L.
2. Masing-masing konsentrasi larutan standar diambil 10 mL dan ditambah dengan 2,0 mL larutan natrium dithionit 1 % dalam larutan NaOH 4 % dan direkam absorbansinya pada panjang gelombang maksimum. Dari data tersebut dapat dibuat kurva standar Absorbansi lawan konsentrasi.
3. Untuk setiap pengukuran konsentrasi paraquat dalam sampel dibuat seri larutan standar terlebih dahulu.
Media Exacta Volume 10 No.2 Juli 2010
Pengukuran absorbansi sampel dilakukan pada hari ke 0, 1, 2, 5, 7, 10, 14, 26, 38 dan 50 dengan langkah-langkah sebagai berikut:
1. Setiap media diambil dua botol sampel yang dikondisikan dalam keadaan terang dan dua botol sampel yang lain dikondisikan dalam keadaan gelap.
2. Larutan sampel dengan volume 10 mL masing-masing ditambahkan 2 mL larutan natrium dithionit 1 % dalam larutan NaOH 4 % dan diukur absorbansinya pada panjang gelombang maksimum.
3. Penambahan 2 mL larutan natrium dithionit 1 % dalam NaOH 4 % dilakukan saat akan diukur absorbansi sampelnya dengan spektrofotometer UV-Vis.
c. Penetapan konsentrasi paraquat.
1. Data absorbansi sampel yang diperoleh diekstrapolasikan ke kurva standar dan diperoleh konsentrasi sampel dari tiap media pada masing-masing kondisi.
2. Hasil akhir berupa grafik konsentrasi vs waktu untuk tiap media yang masing-masing terdiri dari kondisi gelap dan terang.
3. Kemudian dilakukan penentuan konstanta laju degradasi paraquat pada kondisi terang dan gelap untuk mengetahui kinetika degradasi paraquat.
Penentuan pH sampel
Penentuan pH sampel dilakukan dengan menggunakan pH meter dan diukur untuk keadaan sampel sebelum dan setelah ditambahkan paraquat. Pengukuran pH sampel dilakukan sebagai pembanding untuk mengetahui keadaan sampel secara fisik.
HASIL DAN PEMBAHASAN
1. Analisis Paraquat Secara Spektrofotometri UV-Vis a. Penentuan Panjang Gelombang Maksimum
Paraquat (1,1-dimetil-4,4-bipiridilium) sebagai zat aktif dari Gramoxone merupakan salah satu golongan senyawa amonium kuartener. Kation paraquat memiliki kemampuan menyerap sinar UV sebagai akibat dari transisi elektronik π (π ke π*) pada ikatan rangkap terkonjugasi dalam gugus bipiridil. Oleh karena itu, analisis paraquat dapat dilakukan secara langsung dengan menggunakan spektrofotometer UV-Vis. Panjang gelombang serapan paraquat pada 260 nm (Hassal, 1982). Masalah yang dihadapi adalah hampir semua sampel yang berasal dari lingkungan telah banyak mengandung pengotor.
Salah satu cara untuk mengatasi kesulitan dalam menganalisis paraquat di lingkungan adalah mengikuti metode analisis yang dikembangkan oleh Constenla (1990), yaitu mereduksi paraquat dengan natrium ditionit dalam suasana basa. Reduksi paraquat akan menghasilkan warna biru pada larutan dengan serapan pada panjang gelombang sekitar 600 nm. Syarat
Media Exacta Volume 10 No.2 Juli 2010
terjadinya reaksi adalah dalam suasana basa maka digunakan larutan natrium dithionit 1 % yang dilarutkan dalam larutan NaOH 4 %.
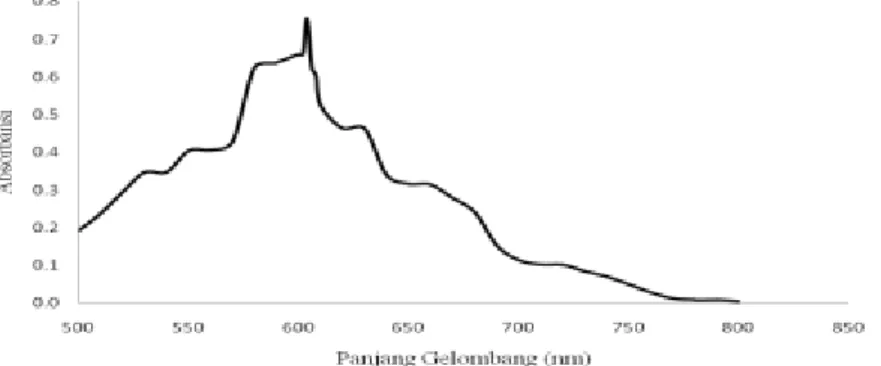
Pengukuran panjang gelombang serapan maksimum dilakukan pada panjang gelombang antara 500 sampai 800 nm, seperti terlihat pada Gambar 1. Hasil pengukuran dengan menggunakan spektofotometer UV-Vis diperoleh panjang gelombang serapan maksimum adalah 604 nm. Pada pengukuran absorbansi paraquat perlu diperhatikan stabilitas reduktor natrium dithionit, karena reduktor ini sangat menentukan besarnya nilai absorbansi yang akan diukur oleh alat. Hasil reduksi paraquat berupa radikal kation mempunyai sifat kurang stabil. Radikal kation berwarna biru ini akan mengalami autooksidasi karena keberadaan air dan oksigen sehingga terbentuk kembali ion paraquat yang tidak berwarna. Mengingat sifat paraquat tereduksi yang kurang stabil maka pengukuran absorbansi paraquat dengan metode ini dilakukan secepat mungkin.
Gambar 1. Spektra serapan maksimum paraquat tereduksi
b. Sensitivitas dan Batas Deteksi
Kurva kalibrasi dibuat pada rentang konsentrasi 1,104 mg/L sampai 16,56 mg/L untuk analisis sampel pada hari ke 0, 1, 2, 5, 7, 10, 14, 26, 38 dan 50. Pada setiap kurva kalibrasi diperoleh persamaan regresi linear (y = bx + a), dengan slop (b) dan intersep (a). Besarnya slop kurva kalibrasi menunjukkan nilai sensitivitas (Skoog, 1985). Jika dibandingkan slop dari kurva kalibrasi untuk tiap pengambilan sampel diketahui bahwa besarnya slop hampir sama (Tabel 1), dengan rata-rata sensitivitas adalah 0,04399 LA/mg. Batas deteksi adalah konsentrasi terendah yang dapat ditentukan berbeda sangat nyata secara statistik dari pengukuran blanko (Skoog, 1985). Penentuan batas deteksi menurut Miller dan Miller (1991) dapat dihitung sebagai konsentrasi yang menghasilkan absorbansi sebesar 3 x Sa (standar deviasi intersep). Pada setiap kurva kalibrasi diperoleh nilai koofisien korelasi (r), yaitu antara 0,9995 sampai 0,9999 (Tabel 1). Nilai koofisien yang mendekati satu menunjukan bahwa metode analisis paraquat memiliki ketelitian yang cukup tinggi.
Tabel 1. Data Kurva Kalibrasi dan Parameter Analitik
Media Exacta Volume 10 No.2 Juli 2010
Hari
Persamaan regresi linear r Sensitivitas
(LA/mg) Batas deteksi
0 Y = 0,03792x + 0,01705 0,99994 0,03792 0,14456 1 Y = 0,03854x + 0,05694 0,99958 0,03854 0,38546 2 Y = 0,03989x + 0,00857 0,99994 0,03989 0,14478 5 Y = 0,04242x + 0,01526 0,99953 0,04242 0,40741 7 Y = 0,04881x + 0,01445 0,99964 0,04881 0,35818 10 Y = 0,04707x + 0,00971 0,99980 0,04707 0,26397 14 Y = 0,05267x – 0,00344 0,99986 0,05267 0,22320 26 Y = 0,05075x – 0,00136 0,99968 0,05075 0,33677 38 Y = 0,04120x + 0,02549 0,99966 0,04120 0,34924 50 Y = 0,04058x + 0,02530 0,99972 0,04058 0,31739
2. Kinetika Degradasi Paraquat
Hasil yang diperoleh pada percobaan di atas diaplikasikan untuk mempelajari kinetika degradasi paraquat diklorida. Pada percobaan dilakukan dua macam perlakuan yaitu pada kondisi gelap dengan cara membalut seluruh permukaan wadah sampel dengan kertas karbon dan kondisi terang dengan pemaparan sinar matahari secara langsung. Perlakuan pada kondisi gelap dan terang dibedakan lagi berdasarkan kesterilan sampel, yaitu sampel yang disterilkan dengan autoklaf dan yang tidak disterilkan.
a. Pengaruh Sinar Matahari Terhadap Laju Degradasi Paraquat
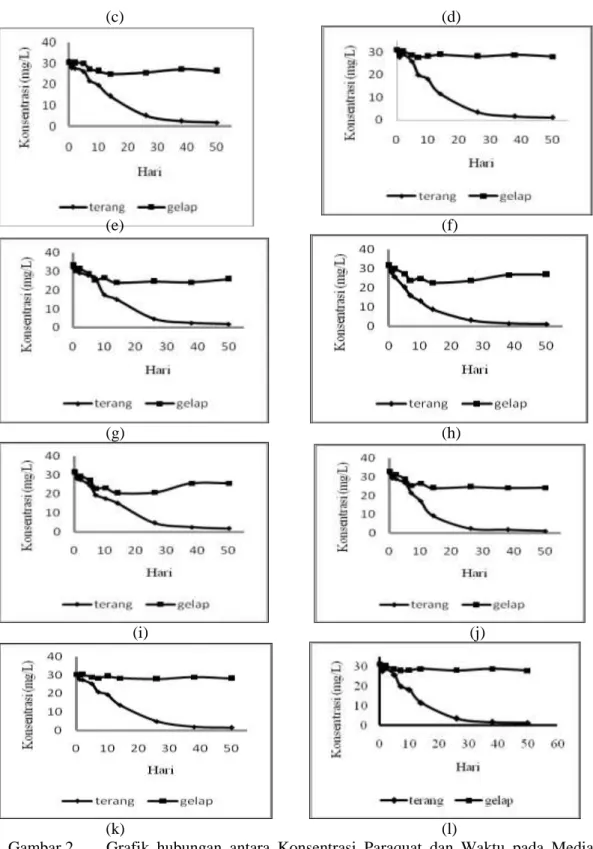
Hasil yang diperoleh dari percobaan menunjukan telah terjadi penurunan konsentrasi paraquat pada kondisi terang untuk dua belas media percobaan yang digunakan. Hal ini dapat dilihat pada Gambar 2 yang memperlihatkan penurunan konsentrasi paraquat pada kondisi terang yang dibandingkan dengan penurunan konsentrasi paraquat pada kondisi gelap.
(a) (b)
Media Exacta Volume 10 No.2 Juli 2010 (c) (d) (e) (f) (g) (h) (i) (j) (k) (l)
Gambar 2 Grafik hubungan antara Konsentrasi Paraquat dan Waktu pada Media: (a) akuades steril, (b) akuades tidak steril, (c) air sumur steril, (d) air sumur tidak steril, (e) filtrat tanah Oematanunu steril, (f) filtrat tanah Oematanunu tidak steril, (g) filtrat tanah Oesao steril, (h) filtrat tanah Oesao tidak steril, (i) filtrat tanah Nonbaun steril, (j) filtrat tanah Nonbaun tidak steril, (k) filtrat tanah Takari steril, (l) filtrat tanah Takari tidak steril
Media Exacta Volume 10 No.2 Juli 2010
Penurunan konsentrasi paraquat pada kondisi terang disebabkan adanya pengaruh sinar matahari secara langsung. Sinar UV yang dihasilkan oleh sinar matahari dan terdapat secara bebas pada atmosfer dapat diserap oleh paraquat sehingga terjadi pemutusan ikatan dalam molekul organik (Tinsley dalam Connell dan Miller, 1995). Penyerapan sinar UV oleh molekul paraquat diklorida dapat menyebabkan terjadinya pembukaan salah satu cincin piridin menghasilkan N-metil-4-karboksipiridinium (Hassal, 1982). Penurunan konsentrasi paraquat pada kondisi gelap tidak memberikan perbedaan cukup berarti. Hal ini berarti tidak terjadi peristiwa degradasi paraquat pada berbagai media percobaan untuk kondisi gelap.
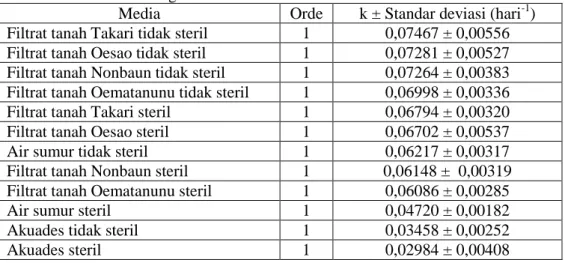
Kajian kinetika degradasi dilakukan dengan penentuan orde dan konstanta laju reaksi seperti disajikan pada Tabel 2. Pada Tabel 2 dapat dilihat urutan konstanta laju degradasi dari yang terbesar sampai yang terkecil berdasarkan media sampelnya.
Penyinaran dengan sinar matahari secara langsung selama 50 hari (8 jam/hari) mampu mendegradasi paraquat untuk masing-masing media pada kondisi terang dengan persentase penurunan konsentrasi paraquat yang bervariasi sesuai jenis medianya. Sinar UV dari sinar matahari mampu mendegradasi paraquat dengan persentase antara 71,66 sampai 96,64 % dengan penurunan konsentrasi terbesar adalah pada media yang berisi filtrat tanah Takari. Tabel 2. Data orde dan konstanta laju degradasi paraquat (k) pada berbagai media
di kondisi terang
Media Orde k ± Standar deviasi (hari-1)
Filtrat tanah Takari tidak steril 1 0,07467 ± 0,00556
Filtrat tanah Oesao tidak steril 1 0,07281 ± 0,00527
Filtrat tanah Nonbaun tidak steril 1 0,07264 ± 0,00383
Filtrat tanah Oematanunu tidak steril 1 0,06998 ± 0,00336
Filtrat tanah Takari steril 1 0,06794 ± 0,00320
Filtrat tanah Oesao steril 1 0,06702 ± 0,00537
Air sumur tidak steril 1 0,06217 ± 0,00317
Filtrat tanah Nonbaun steril 1 0,06148 ± 0,00319
Filtrat tanah Oematanunu steril 1 0,06086 ± 0,00285
Air sumur steril 1 0,04720 ± 0,00182
Akuades tidak steril 1 0,03458 ± 0,00252
Akuades steril 1 0,02984 ± 0,00408
b. Kinetika Degradasi Paraquat
Tanah merupakan salah satu faktor yang berperan penting dalam proses degradasi sebab dalam tanah terdapat material berupa bahan organik dan bahan anorganik tanah yang dapat mempengaruhi proses degradasi paraquat. Keempat sampel yang digunakan dalam penelitian mewakili jenis tanah yang mendominasi wilayah Kupang. Data jenis tanah dan kandungan material tanah dapat dilihat pada Tabel 3.
Tabel 3. Data kandungan material tanah pada sampel
No Sampel tanah pertanian Kandungan Mineral Bahan organik (%)
Media Exacta Volume 10 No.2 Juli 2010
%), kalsite (19 %) (Ndeo, 2010)
2 Oesao Calcite, magnesian, quartz,
montmorilonit (Seran, 2010)
10,265 (Seran, 2010)
3 Nonbaun lempung kaolinit dengan kadar
liat rendah dan bertekstur pasir (Nitsae, 2010)
2,77 - 7,22 (Nitsae, 2010)
4 Takari kuarsa, klorit dan montmorilonit
(Gadi, 2010)
10,3 (Gadi, 2010)
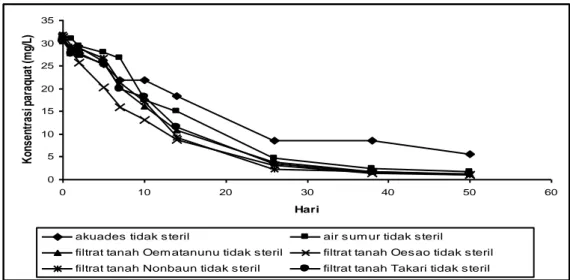
Data pada Tabel 3 menunjukkan bahwa umumnya semua sampel tanah memiliki kandungan bahan organik. Keberadaan material humat yang merupakan bahan organik tanah akan mempercepat fotodegradasi paraquat karena material ini sangat kuat menyerap sinar matahari dan berperan sebagai fotosensitiser (Binarjo, 2001). Degradasi paraquat yang dipengaruhi oleh material tanah dapat dilihat pada Gambar 3. Keberadaan material anorganik tertentu seperti Fe dalam media air sumur diduga dapat mempercepat laju degradasi paraquat dalam media tersebut. Konstanta laju degradasi paraquat dalam media akuades steril dan tidak steril jauh lebih kecil dibanding media lain karena tidak terdapatnya material tanah yang dapat meningkatkan laju degradasi paraquat dalam media tersebut.
0 5 10 15 20 25 30 35 0 10 20 30 40 50 60 Hari K o n s e n tr a s i p a ra q u a t (m g /L )
akuades steril air sumur steril filtrat tanah Oematanunu steril
filtrat tanah Oesao steril filtrat tanah Nonbaun steril filtrat tanah Takari steril
Media Exacta Volume 10 No.2 Juli 2010 0 5 10 15 20 25 30 35 0 10 20 30 40 50 60 Hari K on se ntr as i p ar aq ua t (m g/ L)
akuades tidak s teril air s um ur tidak s teril filtrat tanah Oem atanunu tidak s teril filtrat tanah Oes ao tidak s teril filtrat tanah Nonbaun tidak s teril filtrat tanah Takari tidak s teril
(b)
Gambar 3. Grafik hubungan antara konsentrasi paraquat dan waktu pada kondisi terang untuk media (a) steril dan (b) tidak steril
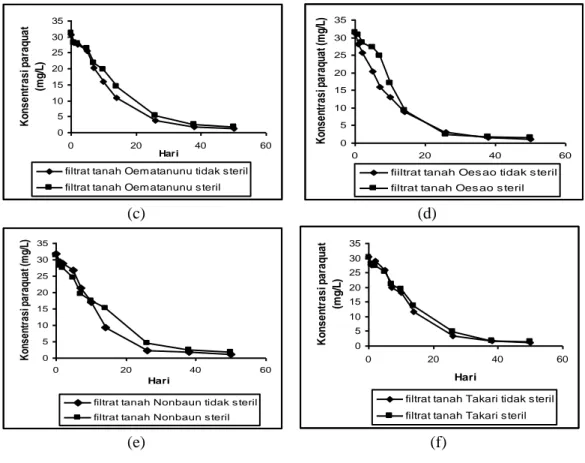
c. Pengaruh Mikroorganisme terhadap Kinetika Degradasi Paraquat
Pada Gambar 4 terlihat bahwa telah terjadi penurunan konsentrasi paraquat pada kondisi terang untuk sampel dalam dua belas media percobaan. Penurunan konsentrasi paraquat pada media filtrat tanah tidak steril lebih besar daripada penurunan konsentrasi paraquat pada media filtrat tanah steril. Hal ini menunjukkan bahwa degradasi paraquat lebih efektif pada media filtrat tanah yang tidak disterilkan. Demikian juga dalam media akuades dan air sumur dimana penurunan konsentrasi paraquat lebih efektif pada media tidak steril. Pada media filtrat tanah yang tidak disterilkan dimungkinkan mengandung mikroorganisme yang dapat meningkatkan laju degradasi paraquat karena mikroorganisme dapat mendegradasi paraquat menjadi CO2 dan produk alami lainnya. Proses degradasi paraquat oleh mikroorganisme dipengaruhi oleh konsentrasi paraquat dan kandungan bahan organik tanah. Senyawa organik menghasilkan unsur-unsur hara yang penting untuk kehidupan mikroorganisme.
0 5 10 15 20 25 30 35 0 20 40 60 Hari K on se ntr as i p ar aq ua t (m g/ L)
akuades tidak s teril akuades s teril
0 5 10 15 20 25 30 35 0 20 40 60 Hari K o n s e n tr a s i p a ra q u a t (m g /L )
air s um ur tidak s teril air s um ur s teril
Media Exacta Volume 10 No.2 Juli 2010 0 5 10 15 20 25 30 35 0 20 40 60 Hari K o n s e n tr a s i p a ra q u a t (m g /L )
filtrat tanah Oem atanunu tidak s teril filtrat tanah Oem atanunu s teril
0 5 10 15 20 25 30 35 0 20 40 60 Hari K on se ntr as i p ar aq ua t (m g/ L)
fiiltrat tanah Oes ao tidak s teril filtrat tanah Oes ao s teril
(c) (d) 0 5 10 15 20 25 30 35 0 20 40 60 Hari K on se ntr as i p ar aq ua t (m g/ L)
filtrat tanah Nonbaun tidak s teril filtrat tanah Nonbaun s teril
0 5 10 15 20 25 30 35 0 20 40 60 Hari K o n s e n tr a s i p a ra q u a t (m g /L )
filtrat tanah Takari tidak s teril filtrat tanah Takari s teril
(e) (f)
Gambar 4. Grafik hubungan antara konsentrasi paraquat dan waktu pada kondisi terang untuk media (a) akuades, (b) air sumur, (c) filtrat tanah Oematanunu, (d) filtrat tanah Oesao, (e) filtrat tanah Nonbaun, (f) filtrat tanah Takari
Salah satu faktor yang secara tidak langsung dapat mempengaruhi aktivitas mikroorganisme adalah pH tanah (Soetikno, 1992). pH media sampel mempengaruhi kehidupan mikroorganisme seperti bakteri, jamur dan actinomycetes. Jamur dominan pada lingkungan tanah asam, sedangkan bakteri dan actinomycetes tidak toleran pada lingkungan asam dan jumlahnya menurun pada pH 5,0. Rentang pH yang cocok untuk kehidupan actinomycetes adalah 6,5 sampai 8,0. Data pH media sampel paraquat yang digunakan dalam percobaan disajikan dalam Tabel 4.
Tabel 4. Data pH Media Sampel Paraquat
Media pH
Tanpa paraquat Dengan paraquat
Akuades steril 6,37 6,41
Akuades tidak steril 6,32 6,39
Air sumur steril 7,20 7,66
Air sumur tidak steril 8,29 8,44
Filtrat tanah Oematanunu steril 8,17 7,71
Filrat tanah Oematanunu tidak steril 8,33 8,07
Filtrat tanah Oesao steril 8,33 8,57
Filrat tanah Oesao tidak steril 8,76 9,19
Media Exacta Volume 10 No.2 Juli 2010
Filrat tanah Nonbaun tidak steril 8,10 8,93
Filtrat tanah Takari steril 8,32 8,59
Filrat tanah Takari tidak steril 8,42 8,87
KESIMPULAN
Berdasarkan hasil penelitian dan pembahasan yang telah dilakukan dapat diambil beberapa kesimpulan sebagai berikut :
1. Sinar matahari dapat meningkatkan laju degradasi paraquat. Material tanah berupa bahan organik dan bahan anorganik yang terdapat dalam filtrat tanah (Oematanunu, Oesao, Nonbaun dan Takari) baik steril maupun tidak steril serta keberadaan material anorganik dalam air sumur tidak steril dan air sumur steril dapat mempercepat laju degradasi paraquat. Selain itu, fraksi tanah terlarut tanpa sterilisasi mengandung mikroorganisme yang dapat meningkatkan laju degradasi paraquat.
2. Degradasi paraquat dalam media mengikuti tingkat reaksi orde 1 dengan tetapan laju pada media : filtrat tanah Takari tidak steril (0,07467 ± 0,00556 hari-1) > filtrat tanah Oesao tidak steril (0,07281 ± 0,00527 hari-1) > filtrat tanah Nonbaun tidak steril (0,07264 ± 0,00383 hari-1) > filtrat tanah Oematanunu tidak steril (0,06998 ± 0,00336 hari-1) > filtrat tanah Takari steril (0,06794 ± 0,00320 hari-1) > filtrat tanah Oesao steril (0,06702 ± 0,00537 hari -1
) > air sumur tidak steril (0,06217 ± 0,00317 hari-1) > filtrat tanah Nonbaun steril (0,06148 ± 0,00319 hari-1) > filtrat tanah Oematanunu steril (0,06086 ± 0,00285 hari-1) > air sumur steril (0,04720 ± 0,00182 hari-1) > akuades tidak steril (0,03458 ± 0,00252 hari-1) > akuades steril (0,02984 ± 0,00408 hari-1).
Media Exacta Volume 10 No.2 Juli 2010