Struktur dan fungsi protein
dr. Syazili Mustofa, M.Biomed
Departemen Biokimia dan Biologi Molekuler Fakultas kedokteran Universitas Lampung
syazili mustofa
Protein
• Berasal dari kata Yunani(proteos) : yang utama
• >50% berat kering sel/makhluk hidup adalah protein
• Keutamaan dlm mencerminkan keutamaan fungsi pasti berperan sgt penting dlm ¢.
• Sifat kimia & biologi protein sangat beragam # BM : bbp ratus D – bbp juta D
syazili mustofa
- dapat dikristalkantidak dpt dikristalkan # Kelarutan : sangat dipengaruhi pH lar.
- konsep pI dan pH optimum
_ pI : pH isoelektrik, pH yang muatan (+) dlm suatu mol protein = muatan (-):
1. Disbbkan o/ R aa yg membnt prot ybs 2. Pd pH=pI, kelarutan protein semata-mata
dipertahankan oleh mantel air pd pI, protein sangat mudah diendapkan, cukup dengan menarik mantel air
3. Pd pemisahan dengan elektroforesis, bila pH dapar elektroforesis=pI prot, ybs tdk bergerak dalam medan listriuk elektroforesis
_ pH optimum : suatu protein selalu punya fgs biologis. 1.Bila diamati/diukur pd bbg pH, fgs biologis tsb
suatu pH dg akt maksimum.
2.Di luar itu (pH</>), akt biol protein tsb <, sampai 0. Kurva bbnt. Parabola
3. Juga disbbkan oleh ionisasi R yg ada pd residu aa penyusun protein.
4.Pd pH = pHopt, ionisasi R str 3 D yg tepat, sehingga
prot ybs dapat menjalankan fgs
- pI adalah identitas fisikokimia suatu protein sbg molekul protein
syazili mustofa
•
Gabungan variasi BM dengan pI & pH
opt
masalah dlm isolasi & purifikasi protein dlm
jangka waktu lama.
•
Isolasi & purifikasi protein sll merupakan
usaha penjelajahan (eksplorasi), yang sll
mengandung ciri “coba-coba”, walau pun kini
sudah > terarah. Selalu ada pengaruh faktor
pengalaman unsur “seni” (arts)
syazili mustofa
• Definisi protein :
- Kimia : protein adalah heteropolimer aa yg satu
sama lain terikat dengan ikatan peptida
1.Tidak menjelaskan, bgmn heteropolimer tsb disusun dari aa yg berbeda
2.Tidak menjelaskan, bagaimana protein yang berbeda-beda disusun
3. Tidak menjelaskan bgmn protein yang sama tiap akan disintesis tidak boleh salah dlm & urutan aa
- Biologi : Protein adalah senyawa yang terbentuk
langsung sebagai hasil pengungkapan informasi genetik di dalam gen
syazili mustofa
pembentuknya terikat satu sama lain
3. Tidak menjelaskan identitas senyawa penyusun protein.
# Definisi Biokimia :
Protein adalah heteropolimer aa, terikat satu sama lain dengan ikatan peptida & merupakan
pengungkapan langsung dari informasi genetik di
dalam gen. (tertulis miring: kata kunci)
1. Heteropolimer aa :
a. ada >1 aa penyusun protein
b. konsep aa penyusun protein & aa bukan penyusun protein ciri-ciri kimia :
- gugus asam harus COOH
- Harus suatu asam amino a ( -COOH dan -NH2terikat
ke C yang sama, yaitu Cayang asimetrik) aa dg
gugus asam bukan –COOH (mis. sulfat, spt pd taurin) tdk pernah berada dalam suatu protein. Aa dg –COOH
& -NH2 terikat di tempat berbeda, tidak pernah
berada dalam protein (mis. b-alanin)
2. Ikatan peptida : ada bbp kemungkinan ikatan kovalen antar aa.
- Ikatan pembentuk protein adalah ikatan peptida: ikatan kovalen yg terbentuk sbg hsl pengawahidratan
–COOH aa yg satu dg –NH2aa yg lain.
- Ikatan kovalen lain mgkn ada dlm suatu protein, ttp bukan pembentuk rangka utama/tlg pgg protein.
syazili mustofa
3. Pengungkapan langsung informasi genetik :
- gen : unit informasi genetik dalam DNA / kromosom - Pengungkapan lgsg : hub gen dg protein 1 gen
untuk 1 polipeptida (Beadle & Tatum : One gene
one enzyme) bila gen u/ suatu protein tdk ada,
organisme ybs tdk dpt sintesis protein tsb.
- Karena prot tda aa jenis tertentu yg tdk boleh salah dalam & urutan hrs ada inf tertentu u/ tiap jenis aa kodon : unit informasi dlm gen yg
menyandikan suatu aa. Ada 20 aa penyusun
protein, ttp ada > 20 kodon 1 kodon
menyandikan 1 aa, ttp 1 aa disandikan oleh > 1 kodon. Kodon adalah tribasa dalam asam nukleat, yang mengandung makna 1 aa.
,
syazili mustofa
• Universalisme biologis :
Msk makhluk hidup sangat beragam, ada
universalisme mulai dari virus sampai manusia: - Menggunakan aa yang sama u/ menyusun protein,
jumlah hanya 20 jenis
- Menggunakan bahasa genetik yg sama u/
“mengucapkan” aa tsb : kodon dg arti yang sama. - Menggunakan alat penukar E yg sama, yaitu ATP.
syazili mustofa
• Struktur protein :
- kompleksitas molekul protein str yg rumit, yg hrs dibagi dlm bbp pengertian / konsep :
- Str. Primer, yaitu bagaimana aa disusun menurut urutan tertentu, tiap kali disintesis.
- Str. Sekunder : bagaimana interaksi antara gugus bermuatan yang berdekatan dari aa yg menyusun suatu protein dan menghasilkan suatu bentuk geometris tertentu.
- Str tersier : bagaimana gambaran global dari suatu protein, sebagai hasil dari str sekunder yang ada di dalamnya
- Str kuaterner : khusus u/ prot yang terdiri atas bbp polipeptida, bagaimana hub antar subunit
Asam amino
• ada 20 asam amino.
• Asam amino terdiri dari gugus karboksil
dan gugus amino yang terikat pada atom
karbon a
• Sebuah atom hidrogen dan sebuah rantai
samping (R) juga terikat atom karbon a
Prentice Hall c2002 Chapter 3 13
Struktur 4 asam amino alifatik
Prentice Hall c2002 Chapter 3 14 Proline mempunyai N pada sisitem cincin
alifatiknya
• Proline
(
Pro
,
P
) - has a three
carbon side chain bonded to
the a-amino nitrogen
• The heterocyclic pyrrolidine
ring restricts the geometry of
polypeptides
Prentice Hall c2002 Chapter 3 15
Struktur asam amino Aromatik
Prentice Hall c2002 Chapter 3 17 Pembentukan cystine
Prentice Hall c2002 Chapter 3 18 Asam amino dengan rantai samping gugus
alkohol
• Serine
(
Ser
,
S
) and
Threonine
(
Thr
,
T
) have
uncharged polar side chains
Prentice Hall c2002 Chapter 3 19
Structures of histidine, lysine and arginine
Struktur aspartate, glutamate, asparagine
dan glutamine
Struktur primer
kondensasi a-carboxyl satu asam amino dengan a-amino asam amino lainnya (hilangnya molekul H2O)
syazili mustofa
# Str sekunder :
- Interaksi ikatan kimia antara bbg gugus dari R dlm suatu protein pola-pola geometris 3 D dari suatu pggl / keseluruhan urutan aa
- Pola-pola tsb disbbk o/ keberadaan aa tertentu
- Str sekunder ditentukan oleh str primer - Pola tsb : heliks-a, lembar gelombang-b,
tekukan,simpai (loop) & sulur sebarang (random
coil)
- Suatu rantai polippt yg membentuk suatu protein dpt hanya mempunyai 1 str sekunder, dapat pula > 1.
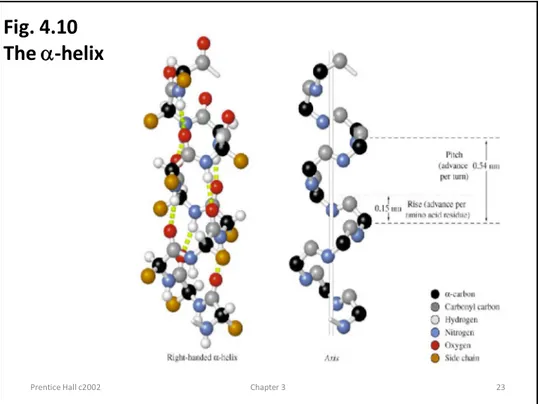
Prentice Hall c2002 Chapter 3 23 Fig. 4.10
The a-helix
Fig. 4.11 Stereo view of right-handed a helix
Prentice Hall c2002 Chapter 3 25
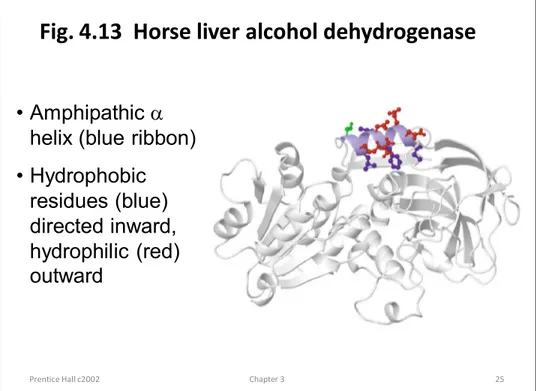
Fig. 4.13 Horse liver alcohol dehydrogenase
• Amphipathic a helix (blue ribbon) • Hydrophobic
residues (blue) directed inward, hydrophilic (red) outward
Prentice Hall c2002 Chapter 3 26
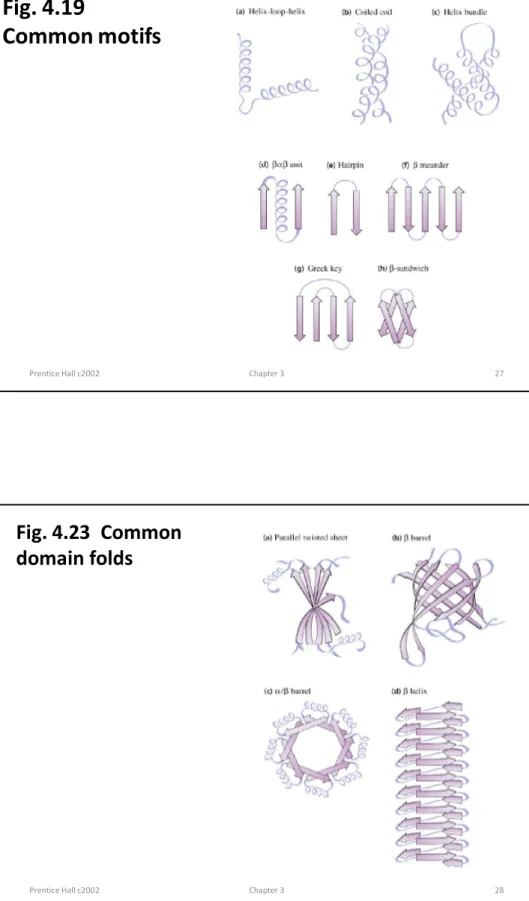
Prentice Hall c2002 Chapter 3 27
Common motifs
Fig. 4.23 Common domain folds
syazili mustofa
# Str tersier :
- Gambaran 3 D suatu mol protein / polippt tunggal - Hanya ada 2 : globuler & fibriler
- Hasil dari str sekunder dlm rantai polippt
- Bila rantai polippt punya >1 str sekunder protein globuler
- Bila hanya ada 1 str sekunder protein fibriler. Str sekunder tunggal tsb biasanya heliks-a saja atau lembar-b saja.
- Jenis str tersier menggambarkan fgs umum dari protein ybs
- Protein globuler umumnya protein regulator (enzim, mediator dlsb)
syazili mustofa
- Protein fibriler biasanya protein pendukung struktur (kolagen, keratin dll)
- Keberadaan suatu str sekunder di suatu penggal polippt menentukan lokasi & interaksi penggal tsb dg sesamanya atau dg mol lain
- jenis str sekunder menentukan str tersier (=str 3 D) & ini menentukan fgs protein
syazili mustofa Chapter 3 31
protein Globular
• Biasanya larut air, padat, berbentuk
lonjong.
• Bagian dalam Hidrofobik, bagian
permukaan hyirofilik
• Contohnya : enzim, protein pembawa dan
protein regulator
Protein Fibriler
• Berfungsi sebagai penyokong mekanik
• Sering berbentuk seperti kabel
• Contoh
•
a-Keratins: komponen utama rambut dan
kuku
Struktur kuaterner :
- Tidak semua protein punya str ini
- Hanya ada pd protein yg tdda bbp polippt sbg
subunit (protein oligomer) spt Hb, Ig, hormon
dll
- Tdk ada hub dg BM (insulin, Hb, albumin)
Prentice Hall c2002 Chapter 3 34 Fig 4.25 Quaternary structure of
Prentice Hall c2002 Chapter 3 35
Fig. 4.42 Hemoglobin tetramer
(a) Human oxyhemoglobin (b) Tetramer schematic
- Interaksi kimia antar subunit terjadi melalui 2 kemungkinan : ikatan –S-S- (Ig, insulin, hormon, toksin tetanus) atau ikatan –H (Hb).
- Interaksi ini sangat rentan akan perubahan aa yang langsung berkontak
- Perubahan 1 aa (str primer) mengubah str sekunder & ini mengubah str tersier gangguan fgs protein ybs
- Perubahan 1 aa (str primer) juga dpt mengubah titik interaksi antara polippt yg menjadi subunit suatu protein / mengganggu interaksi antar molekul (sesama protein, dg protein lain, atau dg molekul
syazili mustofa
• Hubungan struktur – fungsi :
- Str 3 D yg tepat menjamin fgs - Contoh : FSH, insulin & Ig (Ab)
- FSH kuda # FSH manusia, ttp bila salah satu disuntik dg FSH yg lain respon biologis yg sama. Hal yg sama dengan insulin & ATS
- Str primer (urutan aa) kedua hormon & ab yg berasal dari kedua sumber tsb berbeda
- Efek biologis sama disbb o/ pusat aktif protein tsb sama.
- Pusat aktif tsb tda aa tertentu yg sama/mirip str 3 D setempat sama dpt kenali & ikat str yg menjadi sasarannya
syazili mustofa
- Dapat dikatakan, bahwa urutan asam amino sebenarnya diperlukan untuk memperoleh suatu struktur yang tepat.
- Urutan itu sendiri, pada dirinya sendiri sebenarnya tidak berperan apa pun.
- Tampak pd campuran aa, bahkan juga pd protein denaturasi
- Urutan aa adalah usaha untuk mencapai suatu struktur tertentu, dalam kondisi fisik lingkungan tertentu.
- Str 3 D, dibentuk dengan cara apa pun, apa bila telah diperoleh dengan tepat, dapat menjalankan suatu fungsi biologis, meskipun tdk dpt dikendalikan. Rekayasa yg plg mdh u/ itu ialah dg gunakan ab.
syazili mustofa
• Perubahan str 3 D protein dpt terjadi secara
menetap sejak awal, atau sementara. # Perubahan str 3 D menetap sejak awal :
- Disebabkan oleh perubahan aa di suatu tempat (mutasi)
- Ok jenis aa di suatu tempat ditentukan oleh kodon, perubahan kodon
- Tdk dapat dipulihkan/diperbaiki dengan cara-cara fisikokimia
- Efek biologis beragam : mulai dari tidak ada
(sekedar variasi aa tanpa perubahan str 3 D berarti) yaitu suatu polimorfisme, sampai kepada kelainan yang berat.
# Perubahan str 3 D sementara disbb o/ pengaruh lingkungan
- Sangat penting u/ jalankan fgs protein
- Semua protein bekerja atas dasar perubahan str 3 D sementara ini (jelas pada enzim, mediator, efektor spt miosin dll)
- Pd dsrnya, terjadi karena perubahan kondisi tk lingk molekul yg reversibel
- Bila proses fgs biologis selesai dijalankan, protein kembali ke keadaan semula.
- Faktor lingkungan yg sgt penting u/ perubahan str 3 D ialah pH, todan reaksi/ikatan kimia.
syazili mustofa
- Pengaruh pH :
_ Mengubah ionisasi / muatan gugus R & gugus karbonil & imino
_ Menyebabkan fenomena pHoptimum
_ Biasanya denaturasi yg disbbkan perubahan pH bersifat reversibel
_ Menerangkan perlunya sistem dapar & mekanisme homeostasis
- Pengaruh to :
_ tomenggambarkan gerak termodinamik (gerak Brown)
dari molekul
_ E ini melawan E ikatan kimia, t.u lemah, yg
pertahankan str 3 D. Juga to
optimum
_ ireversibel bila E masuk >>.
syazili mustofa
- Pengaruh ikatan/reaksi kimia :
_ Pengikatan gugus tambahan ke suatu bag protein (gugus R) ubah str 3 D
_ Reversibel : terjadi mis a.l pd rx enzimatik, interaksi protein-ligan, protein lokomosi. Ada mekanisme u/ melepaskan diri dari ikatan kimia (+)an tsb
_ Ireversibel : fisiologis terjadi pada peristiwa
modulasi suatu reaksi enzimatik. Patologis terjadi pada peristiwa keracunan (logam berat, senyawa kimia lain bersifat racun seperti insektisida)
syazili mustofa Chapter 3 43