Hidrolisa Sebagai Alternatif Pengolahan Limbah Shaving Industri
Penyamakan Kulit
Sri Sutyasmi*
Balai Besar, Kulit, Karet dan Plastik, Jl Sokonandi 9,Yogyakarta 55166, Indonesia *Penulis korespondensi: Telp. +62 274 512929; 563939 – Fax +62 274 563655
E-mail: srisutyasmi@ymail.com
ABSTRAK
Limbah shaving dihasilkan oleh industri Penyamakan kulit yang berupa serutan kulit tersamak yang mengandung krom. Limbah padat ini mempunyai volume yang sangat besar, sekitar 99 -100 kg setiap ton kulit garaman yang diproses, limbah ini sangat ringan dan tidak mudah terdegradasi.Tujuan dari penelitian ini adalah untuk menangani masalah limbah shaving dari industri penyamakan kulit yang banyak mengandung krom dan pemanfaatan dari hasil hidrolisa limbah shaving tersebut. Penanganan limbah shaving yang paling tepat dan sederhana serta bisa dimanfaatkan adalah dengan hidrolisa menggunakan alkali (NaOH) dengan variasi NaOH 1,5%, 2,5% dan 3,5%. Perbandingan alkali dan limbah shaving untuk hidrolisa adalah 5 : 1. Hasil hidrolisa dipisahkan antara protein kolagen dan krom dengan cara penyaringan. Limbah shaving
sebelum dihidrolisa diuji kadar air, kadar protein dan kadar krom. Sedangkan protein kolagen diuji viscositas, kadar protein dan kadar krom. Protein kolagen bisa dimanfaatkan untuk industri yang menggunakan protein kolagen sedangkan krom bisa dimanfaatkan untuk penyamakan kulit dengan direcovery terlebih dahulu.
Hydrolysis is an Alternative for the Treatment of the Shaving
Waste on Tanning Industry
Sri Sutyasmi*
Balai Besar, Kulit, Karet dan Plastik, Jl Sokonandi 9,Yogyakarta 55166, Indonesia *Coresponding author: Telp. +62 274 512929; 563939 – Fax +62 274 563655
E-mail: srisutyasmi@ymail.com
ABSTRACT
Shaving wastes are produced by the leather tanning industry in the form of chrome-tanned leather shavings. This solid waste has a very large volume, about 99 -100 kg per ton of processed salt skin, this waste is very light and not easily degraded. The aim of this research is to deal with the waste shavings problem of the chrome-containing tannery industry and the utilization of the shaving waste hydrolysis results. The most appropriate and simple shaving waste treatment can be utilized is by using alkali (NaOH) hydrolysis with 1.5%, 2.5% and 3.5% NaOH variations. The ratio of alkali and waste shavings to hydrolysis is 5 : 1. The hydrolysis results are separated between collagen proteins and chromium with filtering. Shaving waste tests before hydrolysis included water content, protein content and chromium content. Collagen proteins were tested for viscosity, protein content and chromium content. Collagen proteins can be used for industries that use collagen proteins while chromium can be used for tannery with first recovered.
PENDAHULUAN
Pada pembuatan kulit jadi dengan bahan baku satu ton kulit mentah sapi akan menghasilkan
limbah padat 70 – 230 kg fleshing, 120 kg trimming kulit mentah 115 kg split wet blue, 100 kg
trimming + shaving wet blue dan 2 kg debu buffing (Sutyasmi, 2010). Limbah shaving adalah
serutan kulit tersamak yang merupakan limbah padat industri penyamakan kulit yang mengandung
krom, sehingga sulit terdegradasi, tahan terhadap perlakuan fisik, kimia dan mikrobiologi
(Sutyasmi, 2010). Limbah padat ini volumenya sangat besar yaitu sekitar 99 - 100 kg setiap ton
kulit yang diproses dan juga ringan sehingga mempunyai volume yang sangat besar. Limbah
shaving ini kebanyakan belum ditangani, hanya dibuang ke TPA (Tempat Pembuangan Akhir).
Penanganan yang paling tepat dan sederhana adalah dengan hidrolisa limbah shaving. Protein (asal
kata protos dari bahasa Yunani yang berarti “yang paling utama”) adalah senyawa organik
kompleks berbobot molekul tinggi yang merupakan polimer dari monomer-monomer asam amino
yang dihubungkan satu sama lain dengan ikatan peptide (Fredrick, et al.,2013).
Kolagen merupakan material yang mempunyai kekuatan rentang dan struktur yang
berbentuk serat. Protein jenis ini banyak terdapat dalam vertebrata tingkat tinggi. Hampir
sepertiga protein dalam tubuh vertebrata berada sebagai kolagen (Katili, 2009) . Karena adanya
sejumlah besar rantai samping yang hidrofil (suka air) dalam gelatin, maka dalam larutan air
membentuk suatu jaringan tidak teratur (Sharaf, at al, 2013). Dengan demikian kolagen termasuk
sebagai jaringan pengikat berkolagen terdiri dari serat. Struktur ini selanjutnya tersusun atas fibril
kolagen yang nampak seperti garis melintang.
Protein serabut (fibrous protein) terdiri dari peptida berantai panjang dan berupa serat-serat
yang tersusun memanjang dan memberikan peran struktural atau pelindung. Misalnya fibroin pada
sutera dan keratin pada rambut dan bulu domba. Protein ini tidak larut dalam air, asam, basa,
maupun etanol (Tahiri and M..De La Guardea, (2009)
Isolasi pemisahan protein kolgen dapat dilakukan dengan berbagai cara antara lain yaitu
dengan metode thermohidrolisis, hidrolisa secara asam, hidrolisa secara alkali, dan hidrolisa secara
ensimatis. Cincin utama serabut kolagen dihubungkan oleh ikatan asilamid, yang dapat dihidrolisa
pada suhu yang tinggi untuk mendapatkan protein kolagen yang dapat larut, tanpa aksi katalisis dari
asam, basa maupun ensim maka hidrolisa dari ikatan asilamid kolagen akan berjalan lambat, dan ini
akan sangat sulit apabila kolagen diikat kuat oleh bahan penyamak. (Ziwen, D, 2008). Sehingga
Catalina, at al, 2008 mengatakan bahwa ikatan asilamide dari jaringan kolagen mudah
dihidrolisa dengan alkali pada suhu tinggi, alkali akan dinetralisir oleh karboksil kolagen yang baru
dihasilkan dari kerusakan asilamide kolagen, sehingga alkali akan dikeluarkan pada saat hidrolisa
berlangsung. Hidrolisa jaringan kolagen secara alkali jauh lebih mudah dan lebih sempurna dari
pada pirolisis yang disebabkan oleh katalis alkali pada saat yang sama berat molekul dari protein
kolagen yang terisolasi jauh lebih kecil dibandingkan dengan protein yang dihasilkan oleh pirolisis
yang diakibatkan oleh hidrolisa dengan alkali (Pati, at al, 2014). Komponen kolagen dihidrolisa dari
limbah kulit dengan alkali dan akan larut dalam larutan air, tetapi garam krom dalam limbah kulit
tetap tidak akan larut dalam kondisi alkali, sehingga diperlukan pemisahan protein kolagen dan
garam krom (Hintermeyer.2008, Kanagaraj, at al, 2015).
Protein kolagen hasil dari hidrolisa secara alkali tergantung dari jenis dan jumlah alkali, suhu dan
waktu. Kandungan krom, kadar abu dan berat molekul juga tergantung pada jenis dan jumlah alkali,
suhu dan waktu hidrolisa (Odbaby, 2011, Jiang, at al, 2016,). Tujuan dari penelitian ini adalah
menangani limbah shaving yang mengandung krom dan bisa memperoleh bahan baku untuk
industri yang lain serta melindungi sumber daya tanah dan air.
BAHAN DAN METODE
Bahan
Bahan yang digunakan dalam penelitian ini adalah limbah shaving dari industri penyamakan
kulit, bahan untuk hidrolisa yaitu NaOH, asam sulfat, kertas saring, pH dan bahan untuk
pengawetan hasil hidrolisa protein kolagen yaitu formalin.
Alat
Alat yang digunakan dalam penelitian ini adalah waterbath untuk pemanasan, alat-alat gelas
(beker glass), pengaduk, saringan alat bantu plastik untuk wadah hasil hidrolisa.
Metode
Limbah shaving sebanyak 200g dihidrolisa dengan NaOH dengan variasi konsentrasi 1,5%,
2,5% dan 3,5%. Perbandingan antara larutan NaOH dan Limbah shaving adalah 5:1. Sehingga
limbah shaving 200g dimasukkan dalam larutan NaOH 1000 ml, dengan variasi seperti yang telah
disebutkan diatas. Campuran larutan ini dihidrolisa dengan suhu 90C, selama 1 jam, 2 jam dan 3
jam. Selanjutnya dipisahkan antara protein kolagen dan krom dengan cara penyaringan. Hasil
pemisahan protein kolagen dan krom dapat dimanfaatkan untuk panyamakan kulit. Protein kolagen
bisa digunakan untuk binder protein pada finishing kulit sedangkan krom hasil saringan dapat
HASIL DAN PEMBAHASAN
Hasil Uji Limbah shaving
Hasil uji limbah shaving sebelum dihidrolisa adalah sebagai berikut:
Tabel 1. Hasil Uji limbah shaving sebelum dihidrolisa
No Parameter Uji Hasil Uji Ulangan Rata-rata
1 Kadar Air,% 44,50 44,76 44,63
2 Kadar Krom, ppm 23468 22874 23171
3 Kadar Protein,% 53,30 53, 78 53,5
Dari data di atas dapat diketahui bahwa rata-rata kadar air adalah 44,63%, kadar krom adalah
23171 ppm dan kadar protein adalah 53,54%. Ini membuktikan bahwa kadar krom dan kadar
protein masuh tinggi dan bisa dimanfaatkan. Untuk itu perlu dihidrolisa dan dipisahkan antara krom
dan protein kolagen agar masing-masing bisa dimanfaatkan. Pemisahan hasil hidrolisa limbah
shaving ini menggunakan penyaringan dengan kertas saring.
Hasil Uji Hasil Hidrolisa Limbah Shaving (Potein Kolagen)
Hasil uji hidrolisa Limbah shaving dari industri penyamakan kulit ini bisa juga disebut dengan
protein kolagen, sedangkan krom yang telah dipisahkan dari protein kolagen dapat direcovery dan
digunakan untuk menyamak kulit. Hasil uji protein kolagen dapat dilihat pada Grafik berikut ini.
Hidrolisa yang dilakukan terhadap limbah shaving adalah divariasi waktu yaitu 1 jam, 2 jam
dan 3 jam dan variasi konsentrasi NaOH yaitu 1,5%, 2,5% dan 3,5% . Berikut adalah data atau
grafik hasil uji dari protein kolagen. Grafik hasil uji Protein Kolagen dengan waktu hidrolisa 1 jam,
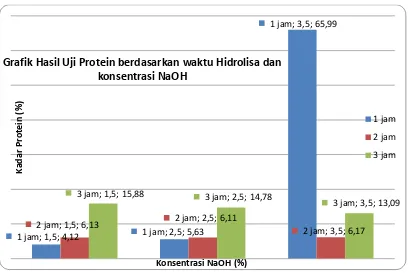
Gambar 1. Hasil uji protein dari hasil hidrolisa protein kolagen
Grafik hasil uji Protein dengan waktu hidrolisa 1 jam dan konsentrasi NaOH 1,5%
menunjukkan bahwa kadar protein adalah 4,12%. Sedangkan pada waktu Hidrolisa 2 jam dengan
konsentrasi yang sama yaitu 1,5% NaOH, maka terlihat ada sedikit kenaikan kadar protein yaitu
6,13%. Pada waktu hidrolisa 3 Jam dan konsentrasi NaOH 1,5% kadar protein terlihat tinggi yaitu
15,88%. Hal ini memperlihatkan bahwa penambahan waktu hidrolisa akan menambah kadar
protein, dan waktu hidrolisa 3 jam diperoleh kadar protein yang paling tinggi karena pada waktu
hidrolisa 3 jam maka watu hidrolisa sempurna dan pada waktu konsentrasi NaOH 1,5%.
Pada konsentrasi NaOH 2,5% dan waktu hidrolisa 1 jam maka pada grafik terlihat bahwa
kadar protein yang diperoleh adalah 5,63%, ini berarti juga ada kenaikan pada konsentrasi NaOH
yang digunakan, dari 4,12% (konsentrasi NaOH 1,5%) menjadi 5,63% (konsentrasi NaOH 2,5%
NaOH). Dengan demikian dengan bertambahnya konsentrasi NaOH maka kadar protein bertambah.
Sedangkan dengan waktu hidrolisa 2 jam dan konsentrasi NaOH 2,5% terlihat pada grafik ada
kenaikan kadar protein yaitu dari 5,63% menjadi 6,11% berarti ada kenaikan kadar protein sebesar
0,48%. Hal ini kemungkinan karena pada konsentrasi NaOH 2,5% dan waktu hidrolisa 2 jam sudah
terjadi hidrolisa yang sempurna sehingga dengan bertambahnya waktu hidrolisa maka kadar protein
juga bertambah. Pada waktu hidrolisa 3 jam dan konsentrsasi NaOH masih 2,5% hidrolisa makin
sempurna, sehingga ada kenaikan kadar protein sebesar 3,67%. Pada konsentrasi NaOH 3,5% dan
waktu hidrolisa 1 jam terlihat pada grafik bahwa kadar protein pada waktu hidrolisa 1 jam terlihat 1 jam; 1,5; 4,12 1 jam; 2,5; 5,63
Grafik Hasil Uji Protein berdasarkan waktu Hidrolisa dan konsentrasi NaOH
tinggi (65,99) karena hidrolisa cukup optimum. Namun pada waktu hidrolisa 2 jam kenaikan kadar
protein dari konsentrasi NaOh 2,5% menjadi konsentrasi 3,5% hanya ada sedikit kenaikan kasdar
protein yaitu dari 6,11% menjadi 6,17. Waktu hidrolisa 1 jam, 2 jam dan 3 jaam pada grafik terlihat
bahwa ada sedikit penurunan dari kadar protein dari konsentrasi 1,5% NaOH (15,88) menjadi
konsentrasi 2,5% NaOH (14,78) dan konsentrasi 3,5% waktu hidrolisa 3 jam terjadi penurunan
kadar protein. Hal ini kemungkinan karena dengan bertambahnya waktu hidrolisa dan konsentarsi
NaOH tidak akan menambah kadar protein yang dihasilkan karena hidrolisa sudah optimum. jadi
penambahan waktu hidrolisa dan konsentrasi NaOH tidak menabbah kadar protein tetapi malah
menurunkan karena hidrolisa sudah maksimum. Untuk mengetahui kekentalan dari larutan hasil
hidrolisa limbah shaving, selanjutnya diuji viskositas dari larutan. Hasil uji viskositas dapat dilihat
pada gambar berikut:
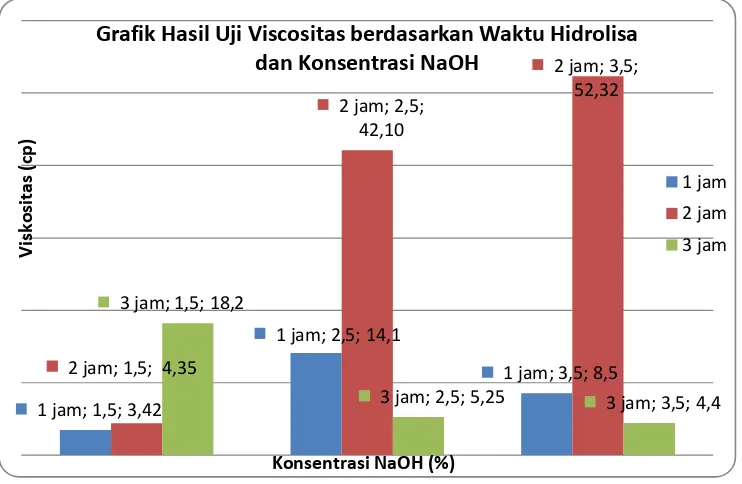
Gambar 2. Hasil uji viskositas dari hasil hidrolisa protein kolagen
Dari grafik diatas dapat diketahui bahwa pada waktu hidrolisa 1 jam dan konsentrasi NaOH
1,5% diperoleh viskositas dari larutan adalah 3,42 cp, waktu hidrolisa 2 jam adalah 4,35 cp dan
waktu hidrolisa 3 jam adalah 18,2 cp, Hal ini berarti dengan adanya kenaikan waktu hidrolisa pada
konsentrasi yang sama yaitu 1,5% NaOH vikositas semakin bertambah. Pada konsentrasi NaOH
2,5% dan waktu hidrolisa 2 jam viskositas mempunyai nilai 14,1 cp dan pada waktu hidrolisa 2 jam
dan konsentrasi sama yaitu 2,5% viskositas naik menjadi 42,10 cp. Pada waktu hidrolisa 3 jam
viskositas turun menjadi 5,25. Hal ini membuktikan bahwa pada konsentrasi NaOH 2,5%, dan
waktu hidrolisa 2 jam diperoleh viskositas paling tinggi yaitu 42,10 cp. 1 jam; 1,5; 3,42
Grafik Hasil Uji Viscositas berdasarkan Waktu Hidrolisa dan Konsentrasi NaOH
Pada konsentrasi NaOH 3,5%, waktu hidrolisa 1 jam nilai viscositas 8,5 cp dan pada waktu
hidrolisa 2 jam viskositas mencapai nilai tertinggi yaitu 52,32. Namun pada waktu hidrolisa 3 jam
dan konsentrasi NaOH 3,5% viskositas menurun menjadi 4,4cp. Apabila dilihat dari waktu hidrolisa
1 jam maka viscositas tertinggi adalah pada konsentrasi NaOH 2,5%. Dan apabila dilihat dari waktu
hidrolisa 2 jam maka viskositas semakin naik dan tertinggi pada konsentrasi NaOH 3,5% dengan
nilai 52,32 cp. Ini berarti bahwa dengan waktu hidrolisa 2 jam nilai viskositas cenderung naik. Pada
waktu hidrolisa 3 jam nilai viskositas semakin menurun. Hal ini kemungkinan karena waktu
hidrolisa 3jam sudah tidak efektif (terlalu lama sehingga larutan menjadi encer karena hidrolisa
terlalu lama.
Untuk mengetahui kadar krom dalam larutan hasil hidrolisa atau protein kolagen diuji kadar
krom dalam larutan protein kolagen. Hasil uji dapat dilihat pada grafik berikut:
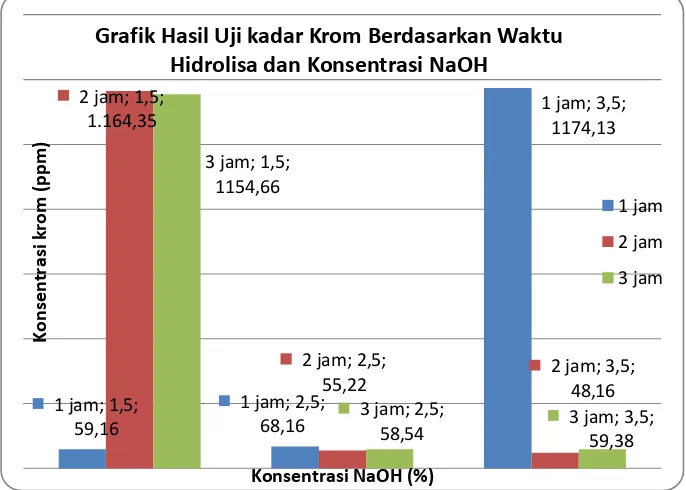
Gambar 3. Hasil uji kadar krom dalam larutan hasil hidrolisa (protein kolagen)
Dari gambar diatas dapat dilihat bahwa waktu hidrolisa 1 jam dan konsentrasi NaOH 1,5%
diperoleh kadar krom dalam larutan adalah 59,16 ppm. Dan pada waktu hidrolisa 2 jam dan
konsentrasi NaOH yang sama yaitu 1,5% kadar krom lebih tinggi yaitu 1164,35 ppm. Demikian
juga untuk waktu hidrolisa 3 jam dengan konsentrasi yang sama (1,5% NaOH), kadar krom adalah
1154,66 ppm. Hal ini kemungkinan karena dengan waktu hidrolisa 1 jam hidrolisa belum sempurna
(untuk konsentrasi NaOH 1,5%. Namun dengan konsentrasi 2 jam dan 3 jam hidrolisa limbah
shaving sudah mendekati sempurna sehingga kadar krom yang diperoleh jauh lebih besar. Pada
konsentrasi NaOH 2,5% dan waktu hidrolisa 1 jam terlihat bahwa kadar krom sedikit naik yaitu dari 1 jam; 1,5;
Grafik Hasil Uji kadar Krom Berdasarkan Waktu Hidrolisa dan Konsentrasi NaOH
50,16% menjadi 68,16%, dan waktu hidrolisa 2 jam dengan konsentrasi 2,5% NaOH adalah 55,22
ppm. Pada waktu hidrolisa 3 jam dan konsentrasi NaOH 2,5% maka nilai kadar krom adalah 58,54
ppm (kaar krom sedikit naik dengan konsentrasi NaOH yang sama), Pada waktu hidrolisa 1 jam
konsentrasi NaOH 3,5% diperoleh kadar kro tinggi yaitu 1174.13, selanjutnya masi dalam
konsentrasi NaOH yang sama yaitu 3,5% waktu hidrolisa 2 jam diperoleh kadar krom yang rendah
yaitu 48,16. Selanjutnya pada konsentrasi NaOH yang sama (3,5%) dan waktu hidrokisa 3 jam,
naiklagi menjadi 59,38 ppm. Hal ini kemungkinan karena sudah terjadi hidrolisa yang sempurna
pada watu hidrolisa 1 jam dan konsentrasi NaOH 3,5%. Pada waktu hidrolisa 2 jam dengan
konsentrasi NaOH 3,5%, maka terlihat kadar krom jauh menurun yaitu nilainya 18,16 ppm. Pada
waktu hidrolisa 3 jam dan konsentrasi NaOH 3,5% maka nilai kadar krom adalah 59,38 ppm. Ini
berarti ada kenaikan kadar krom dari waktu hidolisa 2 jam, yang semula 18,16 ppm menjadi 59,38
ppm. Hal ini kemungkinan karena penambahan konsentrasi NaOH (3,5%) sehingga hidrolisa sangat
sempuna dan efektif, walaupun waktu hidrolisa hanya 1 jam.
Apabila dilihat dari waktu hidrolisa maka kadar krom dengan waktu hidrolisa 1 jam ada
kecenderungan semakin tinggi konsentrasi NaOH maka kadar krom semakin tinggi. Sedangkan
pada wakktu hidrolisa 2 jam maka semakin tinggi konsentrasi NaOH kadar krom akan semakin
turun. Untuk waktu Hidrolisa 3 jam maka terlihat bahwa pada konsentrasi 2,5% NaOH kadar krom
sedikit menurun dengan nilai 55,22 ppm, dan pada konsentrasi 3,5% kadar krom sedikit naik
dengan nilai kadar krom adalah 59,38 ppm . Dengan demikian dapat dikatakan bahwa pada waktu
hidrolisa 1 jam dengan penambahan konsentrasi NaOH kadar krom akan naik/meningkat,waktu
hidrolisa 2 jam dengan konsentrasi NaOH, kadar krom turun dan waktu hidrolisa 3 jam dengan
kenaikan konsentrasi NaOH kadar krom juga turun.
Hasil Uji SEM/Morfologi Protein Kolagen
Hasil Uji morfologi kulit yang kami uji adalah hanya salah satu yaitu pada konsentrasi NaOH
3,5% dan waktu hidrolisa 1 jam karena pada waktu hidrolisa dan konsentrasi ini kadar protein yang
dihasilkan adalah paling tinggi. Hasil uji SEM/morfologi protein kolagen hasil hidrolisa dapat
Gambar 4. Morfologi protein kolagen
Morfologi Potein Kolagen yang bisa dimanfaatkan untuk binder Protein dengan NaOH 3,5%
dan waktu 1 jam dengan perbesaran 1000 kali dapat dilihat pada Gambar 4. Dilihat dari morfologi
dari protein kolagen tersebut maka terlihat bahwa protein ini belum tercampur sempurna (belum
homogen) sehingga masih perlu dilanjutkan penelitian nya agar protein tercampur sempurna
sehingga bila digunakan untuk binder protein akan lebih baik dan merata. Hal ini kemungkinan
karena kurang pengadukan.
KESIMPULAN
Limbah Shavings Industri Penyamakan Kulit dapat ditangani dengan Hidrolisa. Hasil
hidrolisa limbah shavings dapat ditangani dengan baik. Protein kolagen hasil hidolisa limbah
shavings dapat dimanfaatkan. Hasil uji protein kolagen yang tertinggi adalah pada konsentrasi
NaOH 3,5% dan waktu hidrolisa 1 jam. Sedangkan viskositas dari protein kolagen tertinggi adalah
pada konsentrasi NaOH 3,5% dan waktu hidrolisa 2 jam. Kadar krom terendah adalah pada
konsentrasi NaOH 2,5% dan watu hidrolisa 1 jam, 2 jam dan 3 jam. Hasil Uji morfologi dari protein
kolagen menunjukkan kurang homogen.
UCAPAN TERIMA KASIH
Penulis mengucapkan terimakasih kepada Kepala Balai Besar Kulit, Karet dan Plastik yang
telah memberi kepercayaan dan dana untuk melakukan penelitian, serta kepada semua team pokja
DAFTAR PUSTAKA
Catalina, M., Attenburrow, G., Cot, J., Covington, A. D., & Antunes, A.P.M. (2008). Isolation and characterization of gelatin obtained from chrome-tanned shavings, British School of Leather Technology, The University of Northampton; Boughton Green read; Northampton, NN2 7AL, United Kingdom. Consejo Superior de investigaciones Cientificas (CSIC); C/ Jordi Girona, 18-26, Barcelona 08034, Spain
Fredrick, W. S., Kumar, V. S., & Ravichandran, S. (2013). Protein analysis of the crab haemolymph collected from the trash. International journal of pharmacy and pharmaceutical sciences,
5(4), 304-308.
Hintermeyer, H. (2008). Separation of the chromium (III) present in tanning waste water by means of precipitation, reverse osmosis and adsotion. Journal of American applied research, 38, 63-71.
Kanagaraj, J., Senthilvelan, T., Panda, R.C., & Kavitha, S. (2015). Eco-friendly Waste Management Strategies for Greener Environment towards Sustainable Development in Leather Industry: A comprehensive Review. Journal of Cleaner Production, 89(2015), 1 -17. http://dx.doi.org/10.1016/j.jclepro.2014.11.013
Katili A.S. (2009). Struktur dan Fungsi Protein kolagen, Jurnal Pelangi Ilmu, 2(5), 19 – 29.
Odbaby, A. (2011). Waste from leather to the environment. J. Technical Transaction, 98, 43-48.
Pati, A., R Chaudhary, S Subramani, 2014, A review on management of chrome-tanned leather
shavings: A holistic paradigm to combat the environmental issues, Environmental Science and Pollution Research,21(19), 11266–11282.
Sharaf, S.A.A., Gurashi.A., Gasmelseed, & Musa, A. E. (2013). Extraction of Chromium Six from Chrome Shavings, Journal of forest products & industries, 2(2), 21-26
Sutyasmi, S. (2010), Pemisahan Protein Kollagen dalam Limbah shaving Industri Penyamakan Kulit, Prosiding workshop nasional Karya Tulis Ilmiah Journal Riset Industri, 137 – 146
Tahiri, M.. & De La Guardea. (2009), Treatment and Valorization of leather industry Solid wastes, A Review. American Leather Chemists Association, 104(2), 52- 57.