1
LEMBAR PENGESAHAN
Judul Kajian : Aplikasi Teknologi Analisa Mikotoksin Untuk Mendukung Sistem Kontrol Mutu Proses Produksi Pangan dari Jagung
Kode Ristek : F1.98
Fokus Bidang Penelitian : Pertanian Pangan Lokasi Penelitian : Sulawesi Tenggara
Keterangan Lembaga Pelaksana/Pengelola Penelitian A. Lembaga Pelaksana Penelitian
Nama Peneliti Utama Danang Waluyo, MEng.
Nama Lembaga/Institusi Badan Pengkajian dan Penerapan Teknologi Unit Organisasi Balai Pengkajian Bioteknologi
Alamat Gedung 630, Kawasan Puspiptek, Serpong,
Tangerang Selatan, Banten
Telepon/Faksimile/e-mail Phone : 021-7563120, Fax. : 021-7560208 e-mail : danang@biotek.bppt.go.id
B. Lembaga Lain Yang Terlibat/Mitra Nama
Direktur/Koordinator
Dr. Baharudin, MSi.
Nama Lembaga Kementerian Pertanian Unit Organisasi BPTP Sulawesi Tenggara Alamat Jl. Muh. Yamin No. 89, Kendari Telepon/Faksimile/e-mail 0401-3125871/0401-3123180/
bptp-sultra@litbang.deptan.go.id Rekapitulasi Biaya :
Dana Program Insentif : Rp. 250.000.000,- (Dua Ratus Lima Puluh Juta Rupiah)
No. Uraian Jumlah (Rp)
1 Gaji dan upah 68.320.000,-
2 Belanja Bahan 101.780.000,-
3 Perjalanan 55.390.000,-
4 Lain-lain 24.510.000,-
Jumlah (Rp) 250.000.000,-
Jakarta, September 2012
Peneliti Utama, Kepala Balai Pengkajian Bioteknologi,
2 DAFTAR ISI Hal LEMBAR PENGESAHAN 1 DAFTAR ISI 2 BAB I PENDAHULUAN 4 A. Latar Belakang 4 B. Pokok Permasalahan 7
C. Maksud dan Tujuan Kegiatan 8
D. Metodologi Pelaksanaan 8
1. Lokus Kegiatan 8
2. Fokus Kegiatan 8
3. Ruang Lingkup 8
4. Bentuk Kegiatan 9
BAB II PELAKSANAAN KEGIATAN 10
A. Tahapan Pelaksanaan Kegiatan 10
1. Perkembangan Kegiatan 10
2. Kendala dan Hambatan Pelaksanaan Kegiatan 22
B. Pengelolaan Administrasi Manajerial 22
1. Perencanaan Anggaran 22
2. Mekanisme Pengelolaan Anggaran 23
3. Rancangan dan Perkembangan Pengelolaan Aset 23 4. Kendala dan Hambatan Pengelolaan Administrasi Manajerial 23
BAB III METODE PENCAPAIAN TARGET KINERJA 24
A. Metode Pencapaian Target Kinerja 24
1. Kerangka-Rancangan Metode Penelitian 24
2. Indikator Keberhasilan Pencapaian 24
3
B. Potensi Pengembangan Ke Depan 25
1. Kerangka Pengembangan Ke Depan 25
2. Strategi Pengembangan Ke Depan 26
BAB IV SINERGI PELAKSANAAN KEGIATAN 27
A. Sinergi Koordinasi Kelembagaan-Program 27
1. Kerangka Sinergi Koordinasi 27
2. Indikator Keberhasilan Sinergi Koordinasi 27
3. Perkembangan Sinergi Koordinasi 27
B. Kerangka Pemanfaatan Hasil Litbangyasa 28
1. Kerangka dan Strategi Pemanfaatan 28
2. Indikator Keberhasilan Pemanfaatan 29
3. Perkembangan Pemanfaatan 29
BAB V PENUTUP 30
A. Kesimpulan 30
1. Tahapan Pelaksanaan Kegiatan dan Anggaran 30
2. Metode Pencapaian Target KInerja 30
3. Potensi Pengembangan Ke Depan 30
4. Sinergi Koordinasi Kelembagaan-Program 31
5. Kerangka Pemanfaatan Hasil Litbangyasa 31
B. Saran 31
1. Keberlanjutan Pemanfaatan Hasil Kegiatan 31
2. Keberlanjutan Dukungan Program Ristek 31
4
BAB I PENDAHULUAN
A. Latar Belakang
Jagung adalah salah satu produk kegiatan pertanian penting Indonesia. Produksi jagung nasional pada tahun 2005 sebesar 12,52 juta ton pipilan kering (PK). Meskipun pada tahun 2006 produksinya sempat turun menjadi 11,61 juta ton PK, pada tahun 2007 mampu ditingkatkan kembali menjadi 13,28 juta ton PK. Selanjutnya terus meningkat, menjadi 16,32 juta ton PK pada tahun 2008 dan menjadi 17,66 juta ton PK pada tahun 2009. Kenaikan produksi rata-rata mencapai sekitar 10% pertahun. Hal ini menjadikan Indonesia sebagai produsen jagung terbesar di Asia Tenggara. Sementara itu konsumsi jagung nasional pun meningkat. Pada tahun 2005 konsumsi jagung nasional mencapai angka 12,26 juta ton PK, dan naik menjadi 12,50 juta ton PK pada tahun 2006, 13,29 ton PK pada tahun 2007, 16,32 juta ton PK pada tahun 2008, dan 17,66 juta ton PK pada tahun 2009. (Sekretariat Negara Republik Indonesia, 2010). Hal ini menunjukkan pentingnya jagung sebagai salah satu komoditas pangan nasional.
Namun, di balik potensinya, masalah mutu dan keamanannya jagung masih perlu mendapat perhatian. Iklim tropis Indonesia dengan tingkat kelembaban yang tinggi menjadi faktor penyebab berkembangnya kapang yang mencemari jagung dan produk olahannya, terutama kapang yang menghasilkan mikotoksin. Mikotoksin merupakan senyawa organik beracun hasil metabolisme sekunder dari kapang (fungi, jamur, cendawan). Senyawa tersebut dapat membahayakan kesehatan manusia dan hewan ternak dengan berbagai bentuk perubahan klinis dan patologis.
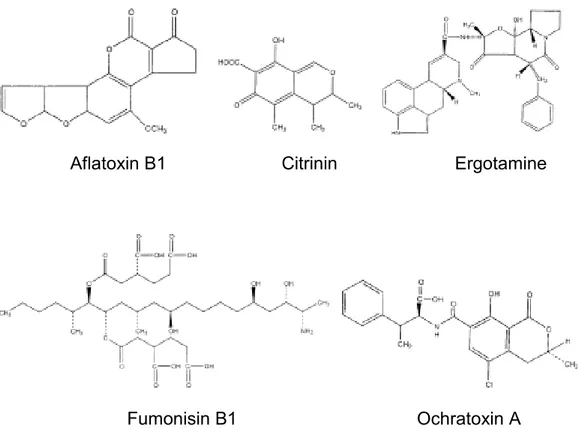
Ada lebih dari 400 jenis mikotoksin yang telah diidentifikasi dari 150 jenis kapang. Sedikitnya ada 7 grup mikotoksin utama yang menjadi berpotensi membahayakan kesehatan, yaitu: Aflatoxin (B1, B2, G1, G2), Ochratoxin A, Trichothecenes (T-2, HT-2, doxynivalenol), Zearalenone, Fumonisins, Ergot alkaloids, dan Patulin (Benneth&Klich, 2003) (Gambar 1). Efek mikotoksin terhadap kesehatan manusia dan hewan ternak bermacam-macam, seperti karsinogenik dan teratogenik, dan konsumsi pangan yang terkontaminasi
5
aflatoksin konsentrasi rendah secara terus-menerus dapat merusak hati serta menurunkan sistem kekebalan pada tubuh (Benneth&Klich, 2003).
Regulasi kandungan mikotoksin dalam produk pangan telah dikeluarkan oleh pemerintah di beberapa negara. Pemerintah Indonesia melalui Peraturan Pemerintah nomor 28 tahun 2004 tentang keamanan, mutu dan gizi pangan telah mengeluarkan aturan mengenai keamanan pangan dan pangan tercemar. Badan Pengawas Obat dan Makanan (BPOM) juga telah mengeluarkan regulasi mengenai cemaran mikotoksin dalam produk pangan. Melalui surat keputusan Kepala BPOM nomor HK.00.05.1.4057 tahun 2004 tentang batas maksimum Aflatoksin dalam kacang tanah dan produk pangan, yaitu sebesar 20 ppb untuk Aflatoxin B1 dan 35 ppb untuk Aflatoksin total (Badan Pengawas Obat dan Makanan, 2004). Jenis cemaran mikotoksin dalam produk makanan yang diatur meliputi Aflatoxin, Deoxynivalenol, Fumonisin B1 dan B2, Ochratoxin A, dan Patulin (Badan Pengawas Obat dan Makanan, 2009). Badan Standardisasi Nasional telah menentukan batas maksimum kandungan mikotoksin dalam produk pangan (Badan Standardisasi Nasional, 2009). Standard ini menyebutkan batas maksimum cemaran Aflatoxin B1 pada jagung dan produk olahannya adalah 15 ppb dan total Aflatoxin adalah 20 ppb. Negara-negara yang tergabung dalam Uni Eropa memiliki regulasi yang lebih ketat lagi. Melalui keputusan European Union Legislative, kandungan Aflatoxin dan ochratoxin A dalam produk makanan tidak boleh melebihi 0.1-10 µg/kg, dan di dalam sereal yang belum diproses tidak boleh mengandung deoxynivalenol lebih dari 1750 µg/kg (European Union Legislative, 2006&2007) (Tabel 1). Mengingat nilai batas maksimum cemaran ini cenderung ditetapkan berdasarkan kemampuan teknik analisa mikotoksin yang ada saat itu dibandingkan dengan pertimbangan efek medis terhadap tubuh manusia dan hewan ternak (Barnett&Klich, 2003), maka pengembangan teknologi analisa mikotoksin dalam produk makanan menjadi sangat penting.
6
Tabel 1. Batas ambang cemaran mikotoksin di beberapa negara Jenis
mikotoksin internasional Regulasi pangan Jenis Regulasi Indonesia Jenis pangan
Aflatoksin CODEX, 2006 SNI7385:2009
4-15
ppb Total Aflatoksin Jagung dan produk olahan
20
ppb Total Aflatoksin Jagung produk olahan dan 2-8
ppb Aflatoksin B1 Jagung dan produk olahan
15
ppb Aflatoksin B1 Jagung produk olahan dan
Fumonisin Cina, Bulgaria, Iran SNI7385:2009
1000
ppb Fumonisin B1 B2 Jagung dan produk olahan
2000
ppb Fumonisin B1 B2 Jagung produk dan olahannya sebagai bahan baku
Amerika Serikat 1000
ppb Fumonisin B1 B3 Produk olahan jagung siap konsumsi 4000
ppb Fumonisin B1 B2 B3 Biji utuh jagung 3000
ppb Fumonisin B1 B2 B4 Popcorn
Okratoksin A (OTA)
FAO, 2004 SNI7385:2009
5 ppb OTA Bahan baku
serealia 5 ppb OTA Serealia (padi, jagung, sorgum, gandum)
3 ppb OTA Produk
olahan serealia
3 ppb OTA Produk olahan
serealia siap konsumsi
Aflatoxin B1 Citrinin Ergotamine
Fumonisin B1 Ochratoxin A
7 B. Pokok Permasalahan
Berdasarkan ketentuan dalam regulasi tersebut di atas, metoda deteksi mikotoksin dalam produk pangan harus memiliki sensitivitas yang cukup untuk mendeteksi batas maksimum yang telah ditetapkan dan memiliki spesifisitas yang baik untuk mendeteksi jenis cemaran yang ada. Selain itu, untuk tujuan kepraktisan, metoda analisa mikotoksin diharapkan memiliki komprehensivitas yang baik agar dapat mendeteksi beberapa jenis cemaran secara simultan, dan memiliki kemampuan memprediksi cemaran lain yang merupakan derivat dari cemaran yang sudah ada, mengingat banyaknya jenis cemaran yang termasuk dalam mikotoksin.
Metoda ELISA (enzyme-linked immunoabsorbent assay) yang berbasis immunochemical menjadi metoda deteksi mikotoksin dalam produk makanan yang umum digunakan saat ini (Turner et al, 2009). Aflatoksin total menjadi target utama deteksi dengan metoda ini. Selain waktu deteksi yang cepat (sekitar 5 menit), batas deteksi minimal metoda ini dapat mencapai 20 ppb. Namun, metoda yang ada saat ini hanya melihat aflatoksin total, dan tidak spesifik untuk mendeteksi masing-masing jenis aflatoksin serta mikotoksin lainnya. Pengembangan metoda ELISA yang lebih spesifik untuk beberapa jenis mikotoksin sudah dilakukan oleh beberapa peneliti di dunia (Caveliere et al, 2005). Namun, mikotoksin tersebut tidak dapat dideteksi dalam waktu bersamaan secara simultan. Metoda analisa menggunakan kromatografi cair dengan detektor tandem mass spektrometri (LC-MS/MS, liquid chromatography-tandem mass spectrometry) telah dikembangkan untuk mendeteksi beberapa mikotoksin secara simultan (Caveliere et al, 2007). Namun, metoda ini hanya dapat menganalisa jenis-jenis toksin yang sudah ditentukan sebelumnya, sehingga jenis toksin yang tidak ditarget tidak dapat dideteksi. Dengan demikian, perlu adanya pengembangan teknologi analisa yang dapat mendeteksi mikotoksin dalam produk pangan secara komprehensif dan simultan dengan sensitivitas dan selektifitas yang tinggi.
UPLC-QTOF-MS (ultra performance liquid chromatography quadrupole time-of flight mass spectrometry) adalah alat analisa yang memiliki kemampuan untuk menganalisa berat molekul dan prediksi struktur suatu molekul. Kecepatan akuisisi data dan resolusi yang tinggi memungkinkan alat ini untuk dapat
8
menganalisa bermacam molekul secara simultan dalam waktu yang singkat. UPLC-QTOF-MS telah banyak digunakan untuk menganalisa metabolit secara komprehensif dan simultan (Han et.al., 2011; Ni et.al., 2010). Keunggulan alat ini dapat digunakan untuk pengembangan metoda deteksi dan analisa mikotoksin pada produk pangan.
C. Maksud dan Tujuan Kegiatan
Kegiatan ini dimaksudkan untuk mengembangkan teknologi analisa mikotoksin yang sensitif, selektif, komprehensif, dan simultan untuk produk makanan berbasis jagung.
Tujuan dari kegiatan ini adalah menguasai teknologi analisa dan ekstraksi mikotoksin dalam produk pangan dari jagung yang sensitif, selektif, komprehensif dan simultan untuk tujuan deteksi dan kuantitasi menggunakan UPLC-QTOF-MS.
D. Metodologi Pelaksanaan
1. Lokus Kegiatan
Sulawesi Tenggara
2. Fokus Kegiatan
Kegiatan ini difokuskan pada bidang pertanian pangan
3. Ruang Lingkup
A) Pengembangan metoda analisa mikotoksin 1. Pemilihan jenis senyawa mikotoksin target
2. Kalibrasi alat UPLC-QTOFMS dengan senyawa standar 3. Uji pemisahan senyawa standar mikotoksin
B) Pengembangan metoda ekstraksi mikotoksin 1. Pemilihan metoda ekstraksi mikotoksin 2. Uji metoda ekstraksi mikotoksin
9 4. Bentuk Kegiatan
1. Persiapan penelitian
Penelitian dimulai dengan mempersiapkan bahan kimia untuk analisa (termasuk senyawa standar mikotoksin) dan memeriksa kelayakan UPLC-QTOF-MS untuk digunakan dalam penelitian. Senyawa standar mikotoksin akan dibeli dari vendor yang terpercaya, mengingat senyawa ini menjadi acuan analisa mikotoksin. Kelayakan alat diperiksa dengan melakukan kalibrasi QTOF-MS menggunakan senyawa standar yang telah ditentukan (leucine enchaphaline) dan memeriksa kemampuan separasi kolom UPLC menggunakan senyawa uji standar yang direkomendasikan kolom. Senyawa standar yang akan diuji adalah aflatoksin B2, aflatoksin G1, aflatoksin G2, okratoksin A, fumonisin B1, dan sitrinin.
2. Pemisahan dan deteksi senyawa standar mikotoksin
Pemisahan senyawa standar dilakukan dengan UPLC yang kemudian dideteksi oleh QTOF-MS. Pemisahan akan dilakukan menggunakan kolom yang memiliki ligan C18. Jenis dan konsentrasi pelarut organik yang akan digunakan sebagai fasa gerak akan menjadi parameter yang akan dioptimasi. Kemampuan pemisahan metoda akan dievaluasi dari ketajaman bentuk peak, retensitas senyawa, serta ada tidaknya senyawa yang koelusi. Parameter detektor juga akan dioptimasi untuk mendapatkan intensitas dan selektifitas deteksi senyawa mikotoksin yang tinggi.
3. Ujicoba metoda untuk mendeteksi mikotoksin dalam produk pangan
Jagung pipilan kering akan ditambahkan senyawa standar mikotoksin dengan kadar tertentu yang telah diketahui. Setelah dihaluskan, senyawa mikotoksin akan diekstraksi dari sampel jagung menggunakan pelarut organik mengikuti prosedur yang telah dipublikasi (Cavaliere et.al., 2005). Kemampuan metoda uji dalam mendeteksi senyawa standar yang ditambahkan (spiked) ke dalam sampel jagung akan dikonfirmasi.
10
BAB II PELAKSANAAN KEGIATAN
A. Tahapan Pelaksanaan Kegiatan
1. Perkembangan Kegiatan
A) Persiapan penelitian
Persiapan penelitian meliputi pengumpulan senyawa standar mikotoksin, kalibrasi alat UPLC-QTOF/MS, dan penyusunan metoda analisa mikotoksin dan ekstraksi mikotoksin dari jagung.
Pengumpulan senyawa standar mikotoksin dilakukan dengan membeli senyawa tersebut dari vendor bahan kimia yang menyediakan. Hingga akhir kegiatan, sebanyak 6 jenis senyawa standar telah dikumpulkan. Keenam senyawa standar tersebut adalah aflatoksin B2, aflatoksin G1, aflatoksin G2, okratoksin A, fumonisin B1, dan sitrinin.
Gambar 2. Senyawa standar mikotoksin yang telah dikumpulkan
Kalibrasi alat UPLC-QTOF/MS dilakukan dengan mengukur nilai m/z dan intensitas senyawa standar leucine encephaline. Hasil kalibrasi menunjukkan bahwa senyawa standar dapat dideteksi oleh alat dengan tingkat kesalahan m/z kurang dari 1 ppm dan menunjukkan intensitas yang cukup sesuai dengan kriteria yang ditetapkan oleh vendor alat (Waters). Dengan demikian, alat dapat digunakan untuk pengujian mikotoksin.
Metoda analisa yang digunakan menyadur dari literatur (Han et.al., 2011; Ni et.al., 2010). Dua metoda ekstraksi mikotoksin dari jagung diuji
11
dalam kegiatan ini. Kedua metoda tersebut disadur dari literatur (Sulyok et.al., 2006; Frenich et.al., 2009).
Gambar 3. Alat UPLC-QTOF/MS
B) Pemisahan dan deteksi senyawa standar mikotoksin
Senyawa standar mikotoksin dianalisa menggunakan UPLC-QTOF/MS. Larutan baku mikotoksin (aflatoksin, okratoksin, sitrinin, fumonisin) yang akan disuntikkan ke dalam sistem UPLC disiapkan sesuai metode yang akan dikembangkan dari literatur. Metode ini digunakan untuk memisahkan senyawa standar ini. Kondisi pemisahan yang digunakan adalah sebagai berikut:
- Column : C-18 (1,8µm, 2.1 x 100 mm ID, Waters) - Suhu kolom : 30°C
- Fasa gerak : Eluent A= CH3OH:H2O:CH3COOH (10:89:1) (mengandung 5mM CH3COOH), Eluent B= CH3OH:H2O:CH3COOH (97:2:1) (mengandung 5mM CH3COOH)
- Laju alir : 350 µl/menit - Sistem elusi : Gradien
Menit Eluent A (%) Eluent B (%)
0 100 0
6 0 100
9 0 100
12
Standar mikotoksin dibuat dengan melarutkan senyawa tersebut di dalam asetonitril atau campuran asetonitril dan metanol (1:1 v/v). Rumus molekul dan m/z dari masing-masing standar adalah sebagai berikut.
Tabel 2. Senyawa standar mikotoksin yang menjadi target dalam kegiatan penelitian ini
Nama standar
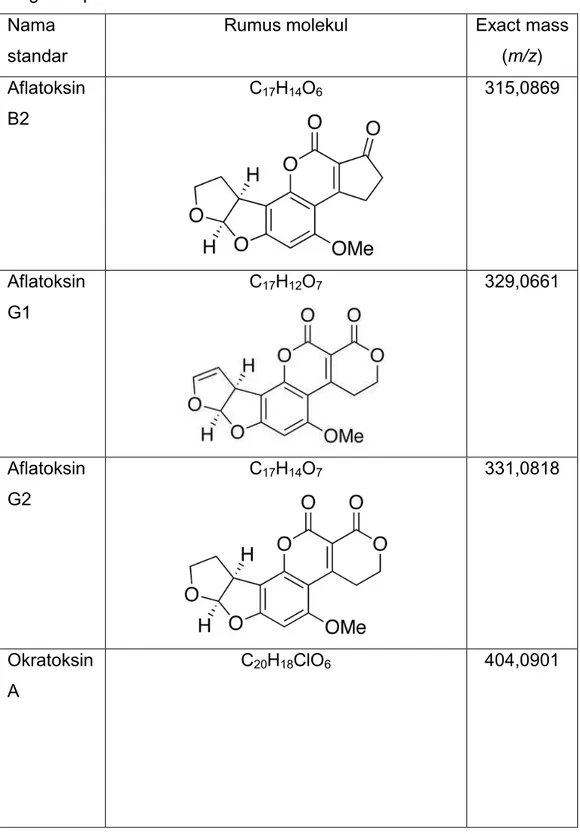
Rumus molekul Exact mass
(m/z) Aflatoksin B2 C17H14O6 315,0869 Aflatoksin G1 C17H12O7 329,0661 Aflatoksin G2 C17H14O7 331,0818 Okratoksin A C20H18ClO6 404,0901
13 Fumonisin
B1
C34H59NO15 722,3963
Sitrinin C13H14O5 251,0919
Hasil pengujian terhadap senyawa standar mikotoksin adalah sebagai berikut:
1. Pengujian aflatoksin
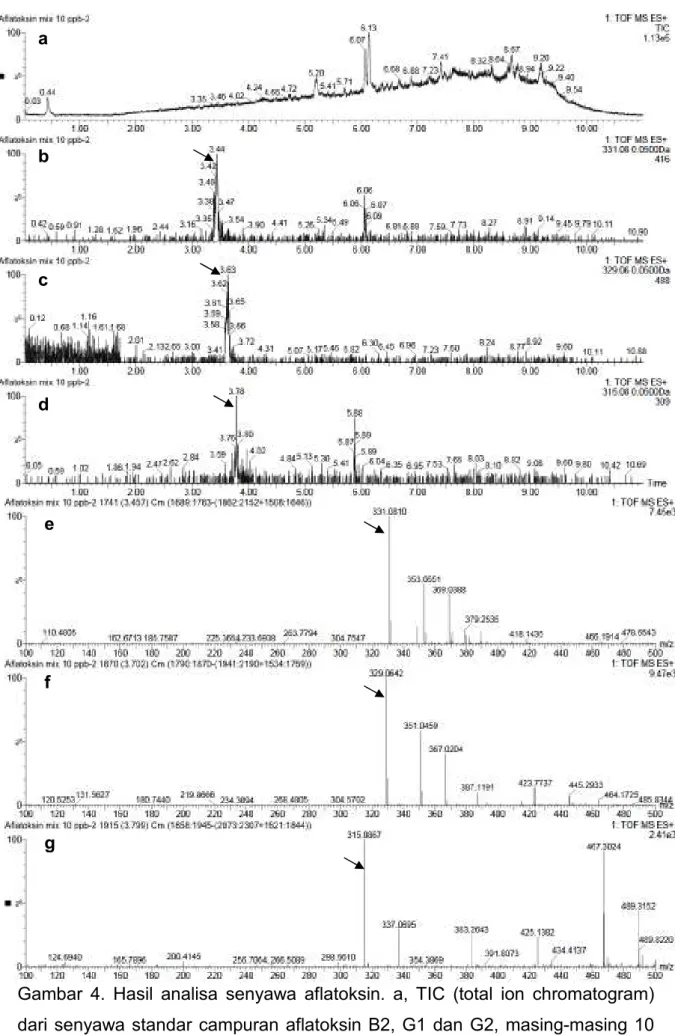
Senyawa standar aflatoksin B2, G1 dan G2 dicampur sehingga masing-masing senyawa memiliki konsentrasi 10 ppb. Campuran ini kemudian dianalisa dengan UPLC-QTOF/MS dengan kondisi pemisahan seperti tersebut di atas. Seperti yang terlihat pada gambar 4 di bawah, ketiga senyawa ini tidak dapat dideteksi dengan jelas pada TIC (total ion chromatogram) (gambar 4.a). Hal ini wajar, karena kromatogram yang ditampilkan tidak spesifik untuk senyawa target. Ketika kromatogram untuk masing-masing senyawa aflatoksin diekstraksi berdasarkan m/z, maka ketiga senyawa ini terlihat muncul dengan waktu retensi yang berbeda (gambar 4.b-d). Hal ini menunjukkan bahwa metoda analisa yang digunakan efektif untuk memisahkan senyawa target dengan intensitas yang cukup. Waktu retensi untuk aflatoksin B2, G1 dan G2 masing-masing adalah 3,78, 3,63, dan 3,44 detik. Integritas peak ini dikonfirmasi hasil mass chromatogram untuk masing-masing senyawa (gambar 4.e-g). Masing-masing peak menunjukkan nilai m/z yang sama dengan exact mass dari literature. Hal ini menunjukkan bahwa senyawa standar aflatoksin dapat dideteksi secara sensitif, komprehensif, dan simultan.
14
Gambar 4. Hasil analisa senyawa aflatoksin. a, TIC (total ion chromatogram) dari senyawa standar campuran aflatoksin B2, G1 dan G2, masing-masing 10 ppb; b, XIC (extracted ion chromatogram) pada m/z 331,08 untuk aflatoksin G2;
a b c d e f g
15
c, XIC pada m/z 329,06 untuk aflatoksin G1; d, XIC pada m/z 315,08 untuk aflatoksin B2; e, mass spectrogram pada waktu retensi 3,457 menit untuk aflatoksin G2; f, mass spectrogram pada waktu retensi 3,702 menit untuk aflatoksin G1; g, mass spectrogram waktu retensi 3,799 menit untuk aflatoksin B2.
2. Pengujian Okratoksin
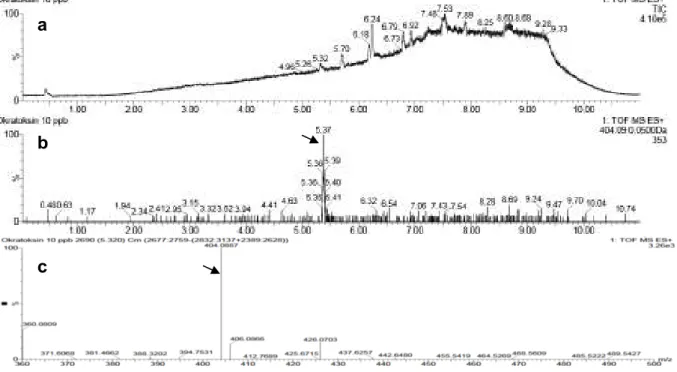
Senyawa standar okratoksin A dibuat dalam konsentrasi 10 ppb dalam asetonitril, kemudian dianalisa dengan UPLC-QTOF/MS dengan kondisi pemisahan sama dengan di atas. Hasil menunjukkan bahwa okratoksin dapat terdeteksi pada konsentrasi 10 ppb pada XIC m/z 404,09 (gambar 5.a-c). Nilai S/N (signal-to-noise ratio), nilai untuk menentukan integritas sebuah sinyal peak suatu senyawa, dari peak okratoksin A menunjukkan angka 36,47. Menurut ketentuan yang berlaku dalam dunia analisa, limit of detection (LOD) ditentukan bila suatu peak memiliki nilai S/N sebesar 3, sehingga LOD okratoksin A dengan metoda ini diperkirakan mencapai 1 ppb.
Gambar 5. Hasil analisa okratoksin A. a, TIC dari senyawa standar okratoksin A 10 ppb; b, XIC pada m/z 404,09 untuk okratoksin A; c, mass spectrogram pada waktu retensi 5,320 menit untuk okratoksin A.
a
b
16 3. Pengujian Fumonisin
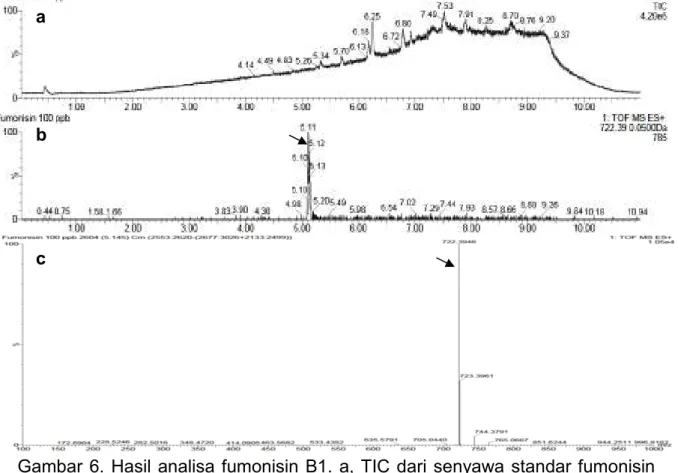
Senyawa standar fumonisin B1 dilarutkan di dalam asetonitril sehingga terbentuk larutan dengan konsentrasi 100 ppb, lalu dianalisa dengan UPLC-QTOF/MS dengan metoda analisa yang sama dengan di atas. Hasil menunjukkan bahwa fumonisin B1 dapat dideteksi pada waktu retensi 5,11 menit dari XIC pada m/z 722,39. Peak pada waktu retensi tersebut memiliki m/z untuk fumonisin B1, sehingga senyawa ini terdeteksi dengan baik dengan metoda analisa yang diuji (gambar 6.a-c). Nilai S/N peak ini mencapai 134,33, sehingga LOD fumonisin B1 diperkirakan mencapai 2,3 ppb.
4. Pengujian Sitrinin
Spectrum
Gambar 6. Hasil analisa fumonisin B1. a, TIC dari senyawa standar fumonisin B1 100 ppb; b, XIC pada m/z 722,39 untuk fumonosin B1; c, mass spectrogram pada waktu retensi 5,11 menit untuk fumonisin B1.
4. Pengujian Sitrinin
Senyawa standar sitrinin dilarutkan di dalam asetonitril dengan konsentrasi 100 ppb, lalu dianalisa dengan UPLC-QTOF/MS menggunakan metoda yang sama dengan di atas. Hasil menunjukkan a
b
17
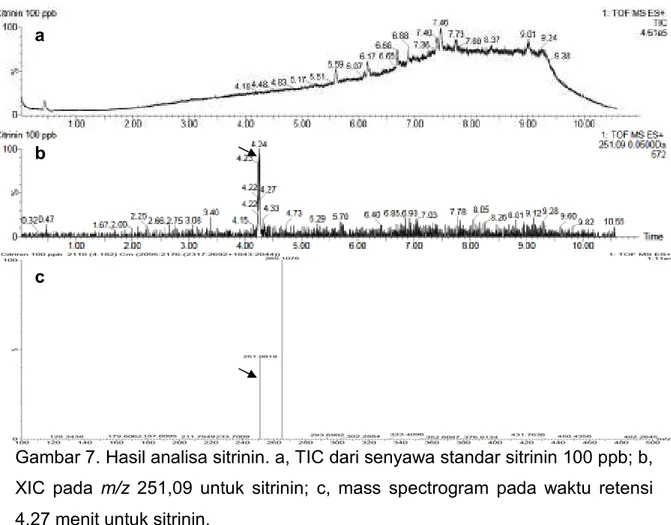
bahwa sitrinin dapat terdeteksi pada waktu retensi 4,24 menit pada XIC m/z 251,09. Hal ini dikonfirmasi dari mass spektrogram yang menunjukkan peak pada m/z sitrinin. Namun, selain peak senyawa ini, muncul peak lain yang lebih besar (m/z 265,11). Peak ini mengindikasikan adanya senyawa lain selain sitrinin yang terdapat dalam larutan senyawa standar. Senyawa lain ini mungkin berupa derivat atau modifikasi dari sitrinin yang terbentuk ketika perlakuan atau penyimpanan.
Gambar 7. Hasil analisa sitrinin. a, TIC dari senyawa standar sitrinin 100 ppb; b, XIC pada m/z 251,09 untuk sitrinin; c, mass spectrogram pada waktu retensi 4,27 menit untuk sitrinin.
C) Ujicoba metoda untuk mendeteksi mikotoksin dalam produk pangan
Untuk menguji apakah metoda analisa mikotoksin yang dikembangkan di atas dapat digunakan untuk menganalisa mikotoksin dalam jagung, senyawa standar mikotoksin (campuran aflatoksin B2, G1, dan G2, masing-masing 5 ppb) ditambahkan ke dalam jagung yang dijual di pasar tradisional setelah dihaluskan, lalu diekstrak dengan metoda ekstraksi mikotoksin yang ada di literatur. Pada kegiatan ini, dua metoda ekstraksi mikotoksin diujicoba untuk melihat performa metoda ekstraksi ini. a
b
18
Sebagai kontrol, air ditambahkan ke dalam jagung yang telah dihaluskan dan diekstrak dengan metoda yang sama.
Metoda yang diuji disadur dari Sulyok, et.al. (2006) dan Frenich, et.al. (2009). Metoda 1 (dari Sulyok et.al.) dilakukan dengan prosedur sebagai berikut.
0,5 gr sampel jagung, dihaluskan, tambahkan senyawa standar atau air
↓Ekstraksi dengan 2 mL asetonitril/air/asam asetat (79:20:1 v/v/v) ↓Shaker selama 90 menit
↓Sentrifuse 3000 rpm selama 2 menit ↓Ekstrak masukkan ke vial
↓ 350 µL aliquot diencerkan dengan asetonitril/air/asam asetat (20:79:1 v/v/v)
↓Campur
↓Analisa dengan UPLC-QTOF/MS sebanyak 5 µL
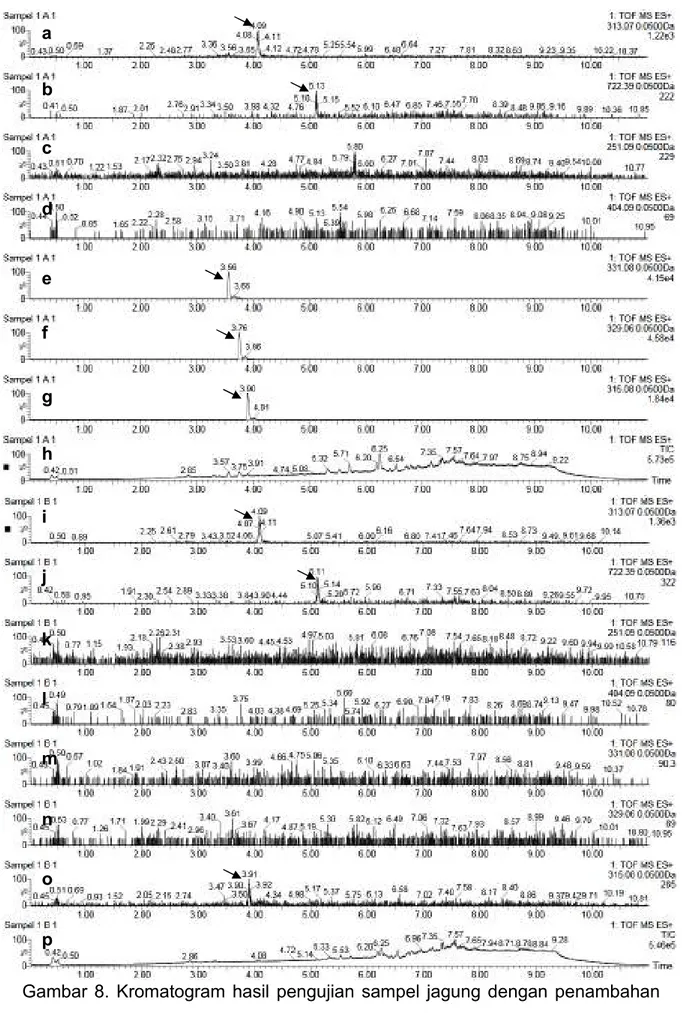
Hasil menunjukkan bahwa ketiga senyawa standar yang ditambahkan ke dalam sampel jagung dapat terdeteksi dengan baik (gambar 8). Sedangkan di dalam sampel jagung yang tidak ditambahkan senyawa standar, ketiga senyawa standar tersebut tidak terlihat. Yang menarik, di dalam sampel tanpa penambahan senyawa standar terdeteksi peak fumonisin B1. Hal ini mengindikasikan bahwa sampel jagung yang digunakan dalam pengujian ini telah tercemar fumonisin B1. Selain itu, ada suatu peak lain pada waktu retensi 4,09 dengan m/z 313,07 yang cukup signifikan. Karena spektrum MS/MS tidak diambil pada analisa kali ini, sehingga senyawa peak ini tidak dapat diprediksi. Namun, hal ini mengindikasikan bahwa ada senyawa lain diluar lingkup pengujian kali ini yang terdapat dalam sampel jagung dan terisolasi dengan metoda isolasi mikotoksin ini.
Dengan demikian, metoda 1 yang digunakan dalam pengujian ini dapat mendeteksi senyawa standar mikotoksin dengan baik dalam sampel jagung.
19
Gambar 8. Kromatogram hasil pengujian sampel jagung dengan penambahan (a-h) atau tanpa penambahan senyawa standar aflatoksin B2, G1, dan G2 (i-p).
a b c d e f g h i j k l m n o p
20
Kromatogram untuk m/z 313,07 (a,i), 722,39 (fumonisin B1, b,j), 251.09 (sitrinin, c,k), 404,09 (okratoksin A, d,l), 331,08 (aflatoksin G2, e,m), 329,06 (aflatoksin G1, f,n), 315,08 (aflatoksin B2, g,o), dan TIC (h,p).
Metoda kedua yang diuji adalah metoda yang dikembangkan oleh Frenich et.al. (2009). Metoda 2 ini dilakukan dengan mengikuti prosedur sebagai berikut.
5 gr sampel jagung, dihaluskan, ditambahkan senyawa standar atau air
↓Homogenkan
↓Masukkan kedalam tab. 50 mL
↓Ekstraksi dengan 10 mL asetonitril/air (80:20) ↓Vortex selama 2 menit
↓Letakkan di rotary agitator selama 10 menit 60 rpm ↓Sentrifuse 4500 rpm selama 5 menit
↓Ambil 2 mL supernatan
↓ Saring dengan menggunakan Millex-GN nylon filter (0.20 lm, Millipore, Carrightwohill, Ireland)
↓Analisa dengan UPLC-QTOF/MS
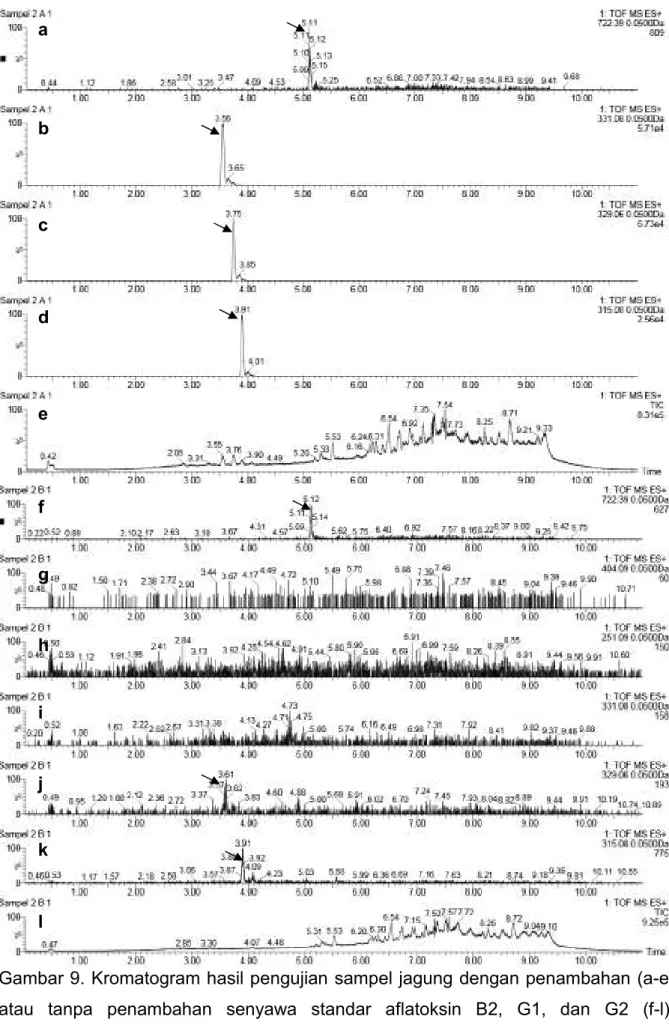
Hasil analisa menunjukkan bahwa senyawa standar yang ditambahkan ke dalam sampel jagung dapat terdeteksi semua dengan baik (gambar 9). Hal yang menarik, hasil analisa terhadap sampel jagung tanpa penambahan senyawa standar menunjukkan adanya peak yang untuk senyawa aflatoksin B2, G1 dan fumonisin B1. Ini menunjukkan bahwa metoda 2 ini dapat mengekstraksi lebih banyak jenis cemaran mikotoksin dibandingkan metoda 1.
21
Gambar 9. Kromatogram hasil pengujian sampel jagung dengan penambahan (a-e) atau tanpa penambahan senyawa standar aflatoksin B2, G1, dan G2 (f-l). Kromatogram untuk m/z 722,39 (fumonisin B1, a,f), 331,08 (aflatoksin G2, b,i),
a b c d e f g h i j k l
22
329,06 (aflatoksin G1, c,j), 315,08 (aflatoksin B2, d,k), TIC (e,l), 404,09 (okratoksin A, g), dan 251,09 (sitrinin, h).
2. Kendala dan Hambatan Pelaksanaan Kegiatan
Penggunakaan alat utama yang digunakan dalam kegiatan (UPLC-QTOF/MS) sering mengalami kendala, terutama disebabkan karena kondisi ruangan yang tidak menunjang pengujian (suhu ruangan dan pasokan listrik yang kurang stabil). Selain itu, mahalnya harga standar mikotoksin dan bahan kimia terkait menyebabkan jumlah senyawa target dalam kegiatan ini dibatasi hingga 6 jenis saja, padahal jenis mikotoksin yang ada lebih dari 20 jenis. Di masa mendatang, diharapkan jenis mikotoksin yang dianalisa dapat ditingkatkan jumlahnya.
Selain itu, lamanya proses pengadaan bahan, khususnya bahan kimia khusus untuk alat LC-MS dan senyawa standar, menjadi kendala utama dalam pelaksanaan pencapaian target. Untuk mengatasi kendala ini, perencanaan waktu pengadaan bahan diatur sedemikian rupa, sehingga tidak mengganggu jalannya riset untuk mencapai target kinerja.
B. Pengelolaan Administrasi Manajerial
1. Perencanaan Anggaran
Dana yang diterima untuk kegiatan pengembangan metoda ini sebagian besar (43%) dialokasikan untuk pembelian bahan yang diperlukan untuk kegiatan. Alokasi dana untuk bahan diarahkan untuk pembelian senyawa standar, mengingat tingginya harga senyawa standar tersebut. Sisanya digunakan untuk perjalanan dinas (23%) dalam rangka mengikuti pertemuan ilmiah dan koordinasi dengan pihak yang akan memanfaatkan hasil kegiatan, honor (25%) untuk para peneliti/perekayasa yang terlibat, dan biaya lain-lain (9%) meliputi biaya jasa pengujian dan biaya penunjang lainnya.
23 2. Mekanisme Pengelolaan Anggaran
Pada dua triwulan pertama, anggaran difokuskan untuk belanja bahan, mengingat waktu tunggu bahan hingga di dapat rata-rata memerlukan waktu yang cukup lama (1-2 bulan). Perjalanan dinas direalisasikan mulai akhir triwulan kedua hingga akhir kegiatan untuk koordinasi pemanfaatan hasil kegiatan, sedangkan honor direalisasikan setiap bulan selama masa kegiatan.
3. Rancangan dan Perkembangan Pengelolaan Aset
Jenis aset yang akan dihasilkan melalui kegiatan ini adalah aset layanan pengujian. Aset ini akan dimasukkan dalam ruang lingkup pengujian di laboratorium pengujian Balai Pengkajian Bioteknologi. Hingga kini, metoda yang dikembangkan telah mengikuti prosedur yang tercantum dalam buku panduan mutu.
4. Kendala dan Hambatan Pengelolaan Administrasi Manajerial
Ada beberapa bahan yang diperlukan dalam kegiatan, misal bahan kimia memerlukan waktu inden yang cukup lama (sekitar 2 bulan). Disamping itu, beberapa senyawa standar diantaranya berharga sangat tinggi sehingga tidak dapat terpenuhi dengan anggaran yang tersedia.
24
BAB III METODE PENCAPAIAN TARGET KINERJA
A. Metode Pencapaian Target Kinerja
1. Kerangka-Rancangan Metode Penelitian
Pengembangan metoda dimulai dengan optimasi dan validasi pemisahan dan deteksi senyawa-senyawa standar mikotoksin menggunakan teknik UPLC yang dikombinasi dengan QTOF-MS sebagai detektor. Optimasi yang akan dilakukan meliputi pemilihan kolom untuk kromatografi, kondisi separasi dan pemilihan parameter MS. Parameter metoda yang akan divalidasi meliputi repeatability, rentang ukur linear, limit deteksi, dan recovery. Kemampuan metoda yang dikembangkan ini akan diujicobakan di produk pangan dari jagung yang ditambahkan senyawa standar mikotoksin. Kegiatan yang dilakukan meliputi:
a) Persiapan penelitian, meliputi pengumpulan bahan dan pengecekan kesiapan alat
b) Pemisahan dan deteksi senyawa standar mikotoksin, meliputi pemilihan jenis kolom untuk separasi, penentuan jenis dan konsentrasi fasa gerak, dan penentuan kondisi separasi dan deteksi
c) Ujicoba metoda untuk mendeteksi mikotoksin di produk pangan.
2. Indikator Keberhasilan Pencapaian
Kegiatan ini ditujukan untuk mengembangkan metoda analisa mikotoksin dalam produk pangan berbasis jagung dengan sensitif, selektif, dan komprehensif. Dengan demikian, indikator keberhasilan kegiatan ini adalah didapatnya metoda analisa mikotoksin yang memiliki sensitivitas, selektifitas, dan komprehensifitas yang lebih tinggi dibandingkan dengan metoda konvensional (metoda ELISA). Dalam metoda ini, senyawa mikotoksin dapat dideteksi hingga batas ambang 20 ppb, dengan kemampuan seleksi target analisa untuk tiap golongan mikotoksin, serta hanya dapat menganalisa satu jenis senyawa mikotoksin dalam tiap batch analisa.
25
3. Perkembangan dan Hasil Pelaksanaan Penelitian
Seperti yang telah disampaikan pada bab II di atas, metoda hasil pengembangan dalam kegiatan ini telah menunjukkan hasil yang baik. Metoda ini dapat mendeteksi 6 jenis mikotoksin target secara simultan dan komprehensif dalam satu batch analisa. Di sisi lain, metoda ini juga memiliki tingkat sensitivitas pengujian yang tinggi, yaitu rata-rata dibawah 10 ppb. Lebih dari itu, masing-masing senyawa mikotoksin target dapat dipisahkan satu dengan lainnya, sehingga masing-masing dapat dideteksi secara terpisah. Hal ini menunjukkan bahwa metoda hasil pengembangan ini dapat menganalisa mikotoksin secara lebih sensitif, selektif, dan komprehensif dibandingkan dengan metoda konvensional. Dengan demikian, indikator keberhasilan pelaksanaan kegiatan penelitian dapat tercapai dengan baik.
B. Potensi Pengembangan Ke Depan
1. Kerangka Pengembangan Ke Depan
Pada penelitian kali ini, target senyawa mikotoksin yang diuji hanya 6 jenis, mengingat keterbatasan dana penelitian. Mengingat regulasi yang diterapkan meliputi beberapa jenis mikotoksin selain yang di uji di sini, maka perlu adanya pengembangan metoda pengujian untuk jenis mikotoksin tersebut.
Selain itu, mikotoksin sebagai kelompok senyawa racun yang diproduksi oleh jamur, dapat juga mencemari produk serealia selain jagung seperti kedelai dan gandum. Agar ketahanan pangan nasional dapat terjamin serta ekspor pangan berbasis sereal dapat meningkat di masa mendatang, perlu adanya pengembangan metoda pengujian cemaran mikotoksin di dalam komoditas sereal selain jagung.
Kegiatan penelitian kali ini difokuskan pada pengembangan metoda untuk mendeteksi cemaran mikotoksin. Karena regulasi kandungan cemaran mikotoksin mempersyaratkan kuantitas cemaran dalam produk pangan, maka perlu dilakukannya validasi metoda secara kuantitatif.
26 2. Strategi Pengembangan Ke Depan
Di masa mendatang, jumlah cemaran target yang dapat dianalisa dengan metoda ini akan ditingkatkan. Selain pada jagung, beberapa jenis mikotoksin juga banyak terdapat dalam produk tanaman sereal lain seperti kedelai. Dengan demikian, diharapkan metoda ini juga dapat diaplikasikan untuk pengujian cemaran mikotoksin pada komoditas selain jagung. Metoda analisa ini akan divalidasi agar mendapatkan metoda yang tangguh dalam menguji kandungan mikotoksin dalam berbagai jenis produk pangan dengan tingkat presisi yang tinggi yang memberikan hasil yang dapat dipercaya. Untuk tujuan ini, pengembangan metoda ke depan akan mengikuti kriteria yang diperlukan agar metoda ini dapat digunakan dalam laboratorium pengujian yang terakreditasi.
27
BAB IV SINERGI PELAKSANAAN KEGIATAN
A. Sinergi Koordinasi Kelembagaan-Program
1. Kerangka Sinergi Koordinasi
Kegiatan pengembangan metoda pengujian kadar cemaran telah menunjukkan hasil yang baik sesuai dengan rencana. Pengembangan metoda telah dilakukan dengan mengacu pada panduan SNI 17025-2000, sehingga diharapkan hasil dari kegiatan ini dapat dimanfaatkan oleh lembaga dalam bentuk layanan teknologi pengujian mikotoksin. Dalam panduan mutu laboratorium pengujian Balai Pengkajian Bioteknologi disebutkan bahwa metoda pengujian hasil pengembangan harus diuji kemampuannya serta divalidasi terlebih dulu sebelum digunakan dalam layanan pengujian. Pengujian kemampuan metoda yang dikembangkan ini telah dilakukan dengan hasil berupa sensitifitas analisa yang lebih baik dibandingkan dengan metoda pengujian konvensional menggunakan metoda ELISA.
2. Indikator Keberhasilan Sinergi Koordinasi
Ketentuan dalam SNI 17025-2000 mengenai pengembangan metoda baru yang akan digunakan dalam pengujian menyebutkan bahwa metoda harus dikembangkan agar menghasilkan hasil yang menjawab kebutuhan pelanggan (pengguna jasa). Untuk itu, perlu adanya sinergi antara kegiatan dengan lembaga yang akan menerapkan metoda pengujian hasil pengembangan ini sehingga dapat termanfaatkan dengan baik. Dengan demikian indikator keberhasilan sinergi koordinasi program-lembaga adalah masuknya metoda pengujian cemaran mikotoksin dalam produk pangan ini ke dalam ruang lingkup pengujian lembaga yang terakreditasi oleh Komite Akreditasi Nasional.
3. Perkembangan Sinergi Koordinasi
Metoda telah dikembangkan dan menunjukkan hasil yang lebih baik dibandingkan metoda pengujian konvensional. Dengan demikian, potensi
28
metoda ini agar dapat masuk dalam ruang lingkup pengujian di Balai Pengkajian Bioteknologi semakin besar.
Dalam panduan mutu laboratorium pengujian Balai Pengkajian Bioteknologi disebutkan bahwa metoda pengujian hasil pengembangan harus diuji kemampuannya serta divalidasi terlebih dulu sebelum digunakan dalam layanan pengujian. Pengujian kemampuan metoda yang dikembangkan ini telah dilakukan dengan hasil berupa sensitifitas analisa yang lebih baik dibandingkan dengan metoda pengujian konvensional menggunakan metoda ELISA. Pada kegiatan kali ini, pengembangan difokuskan pada pengujian kualitatif, sehingga validasi terhadap metoda belum dapat dilakukan sesuai dengan pedoman panduam mutu. Di masa mendatang, metoda ini akan dikembangkan lebih lanjut dengan menguji kemampuan kuantitasi serta melakukan validasi metoda.
B. Kerangka Pemanfaatan Hasil Litbangyasa
1. Kerangka dan Strategi Pemanfaatan
Teknologi ini juga diharapkan dapat membantu eksportir produk pangan dalam melakukan sertifikasi produknya sehingga kesesuaian spesifikasi produk dengan regulasi yang ditetapkan oleh pemerintah negara tujuan ekspor dapat dikonfirmasi terlebih dulu. Agar metoda hasil pengembangan ini dapat dimanfaatkan oleh badan regulasi (BPOM) maupun industri, metoda ini akan divalidasi dan diuji terlebih dulu kemampuannya dalam memenuhi standar regulasi yang berlaku. Penelusuran terhadap batas ambang yang ditetapkan oleh badan regulasi akan dilakukan, sehingga dapat dijadikan acuan dalam mengembangkan metoda yang dapat mengukur hingga batas ambang ini.
Selain itu, pengenalan hasil kegiatan penelitian ini kepada calon pengguna/pemanfaat dilakukan dengan melakukan diskusi dan tukar pikiran mengenai urgensi dan kemampuan metoda dalam menguji cemaran mikotoksin. Calon pengguna/pemanfaat metoda dapat meliputi badan regulasi cemaran pangan, industri pangan, atau badan litbang lainnya.
29 2. Indikator Keberhasilan Pemanfaatan
Metoda hasil pengembangan dapat dinilai bermanfaat bila telah digunakan untuk menguji cemaran mikotoksin dalam produk pangan berbasis jagung yang dimohonkan oleh calon pengguna/pemanfaat metoda ini. Sehingga, indikator keberhasilan pemanfaatan berupa diterimanya sampel dari pelanggan oleh laboratoriun penguji cemaran mikotoksin untuk diuji kandungan cemaran mikotoksinnya menggunakan metoda hasil pengembangan ini.
3. Perkembangan Pemanfaatan
Saat ini metoda sedang dalam tahap pengembangan. Hasil positif sudah dapat terlihat dari hasil yang telah dicapai. Mikotoksin dapat dideteksi dengan tingkat sensitivitas, selektivitas, dan komprehensifitas yang lebih tinggi dibandingkan metoda pengujian konvensional. Dengan demikian, dari sisi performanya, metoda hasil pengembangan ini sangat potensial untuk dapat dimanfaatkan sebagai metoda alternatif untuk menguji cemaran mikotoksin.
Agar bisa lebih dimanfaatkan, metoda ini perlu dikembangkan lebih lanjut agar mampu melakukan pengujian kuantitatif. Lebih dari itu, metoda ini perlu divalidasi terlebih dulu sebelum dimanfaatkan. Kedua hal ini akan dilakukan di masa mendatang.
30
BAB V PENUTUP
A. Kesimpulan
1. Tahapan Pelaksanaan Kegiatan dan Anggaran
Kegiatan dilaksanakan dalam tahapan sebagai berikut:
a. Persiapan penelitian, yang meliputi pengumpulan senyawa standar, kalibrasi alat UPLC-QTOF/MS, dan penetuan metoda analisa.
b. Pemisahan dan deteksi 6 jenis senyawa standar mikotoksin
c. Ujicoba metoda untuk mendeteksi mikotoksin dalam produk pangan Dari total anggaran yang diterima, sebagian besar digunakan untuk pembelian bahan yang digunakan dalam pengembangan metoda ini. Realisasi anggaran pada awal masa kegiatan difokuskan pada pembelian bahan kimia, diikuti dengan realisasi perjalanan dinas dan pembayaran honor peneliti/perekayasa yang terlibat.
2. Metode Pencapaian Target Kinerja
Pengumpulan senyawa standar mikotoksin dan bahan kimia penunjang menjadi fokus kegiatan pada awal kegiatan, mengingat waktu inden beberapa bahan kimia tersebut cukup lama. Selanjutnya, pengembangan metoda dilakukan dengan menguji masing-masing senyawa standar mikotoksin dengan alat UPLC-QTOF/MS yang telah dikalibrasi sebelumnya. Kemampuan metoda dalam menguji kadar mikotoksin dalam jagung juga diuji dengan menambahkan senyawa standar mikotoksin ke dalam sampel jagung, lalu dianalisa dengan alat pengujian setelah diekstraksi. Kemampuan metoda untuk mendeteksi senyawa tersebut akan dievaluasi dengan membandingkan hasil sampel kontrol berupa sampel jagung tanpa penambahan senyawa standar.
3. Potensi Pengembangan Ke Depan
Di masa mendatang, jumlah cemaran target yang dapat dianalisa dengan metoda ini akan ditingkatkan. Selain pada jagung, beberapa jenis mikotoksin juga banyak terdapat dalam produk tanaman sereal lain seperti kedelai.
31
Dengan demikian, diharapkan metoda ini juga dapat diaplikasikan untuk pengujian cemaran mikotoksin pada komoditas selain jagung.
4. Sinergi Koordinasi Kelembagaan-Program
Dalam panduan mutu laboratorium pengujian Balai Pengkajian Bioteknologi disebutkan bahwa metoda pengujian hasil pengembangan harus diuji kemampuannya serta divalidasi terlebih dulu sebelum digunakan dalam layanan pengujian. Pengujian kemampuan metoda yang dikembangkan ini telah dilakukan dengan hasil berupa sensitifitas analisa yang lebih baik dibandingkan dengan metoda pengujian konvensional menggunakan metoda ELISA.
5. Kerangka Pemanfaatan Hasil Litbangyasa
Pengembangan metoda analisa mikotoksin yang dilakukan melalui kegiatan ini telah menunjukkan hasil yang dapat memenuhi kriteria ambang batas cemaran yang telah ditentukan. Hal ini sejalan dengan kebijakan laboratorium pengujian Balai Pengkajian Bioteknologi yang mempersyaratkan bahwa metoda pengujian yang digunakan harus dapat menunjukkan hasil yang dapat memuaskan pelanggan.
B. Saran
1. Keberlanjutan Pemanfaatan Hasil Kegiatan
Agar pemanfaatan hasil kegiatan ini dapat berkelanjutan, konfirmasi terhadap ketahanan (robustness) metoda ini akan dilakukan dengan membuat metoda konfirmasi ketahanan metoda pengujian. Konfirmasi akan dilakukan dengan melakukan pengujian terhadap satu sampel standar yang disimpan pada kondisi tertentu. Konfirmasi akan ditentukan dengan melihat hasil pengujian konfirmasi dan membandingkannya dengan hasil pengujian yang lalu terhadap sampel yang sama.
2. Keberlanjutan Dukungan Program Ristek
Dalam rangka menjaga keberlanjutan kegiatan pengembangan metoda ini, perlu adanya dukungan dana riset yang akan digunakan untuk membeli
32
senyawa standar mikotoksin. Hal ini dipandang perlu, mengingat tingginya harga senyawa standar tersebut. Karena mikotoksin dapat ditemui di produk berbasis sereal selain jagung, maka diharapkan hasil kegiatan ini dapat diaplikasikan kepada produk makanan berbasis selain jagung.
33
BAB VI DAFTAR PUSTAKA
1. Sekretariat Negara Republik Indonesia (2010). Peran Teknologi Pertanian dalam Meningkatkan Produktivitas Tanaman Jagung. http://www.setneg.go.id/index.php? option=com_content&task=view&id=4360&Itemid=29 (16 November 2011)
2. Benneth,J.W. and Klich, M. (2003). Mycotoxins. Clin. Microbiol. Rev. 16:497-516 3. Badan Pengawas Obat dan Makanan (2004). Batas maksimum Aflatoksin Dalam
Produk Pangan. Keputusan Kepala Badan Pengawas Obat dan Makanan Nomor HK.00.05.1.4057 (9 September 2004).
4. Badan Pengawas Obat dan Makanan (2004). Penetapan batas maksimum cemaran mikroba dan kimia dalam makanan. Keputusan Kepala Badan Pengawas Obat dan Makanan Nomor HK.00.06.1.52.4011 (28 Oktober 2009) 5. Badan Standardisasi Nasional (2009). Batas maksimum kandungan mikotoksin
dalam pangan. SNI 7385:2009 (21 Juli 2009).
6. European Legislative (2006). Setting maximum levels for certain contaminants in foodstuffs. Commission Regulation (EC) NO. 1881//2006 (19 Desember 2006). 7. European Legislative (2007). Amending Regulation (EC) No. 1881/2006 setting
maximum levels for certain contaminants in foodstuffs as regards Fusarium toxins in maize and maize producs. Commission Regulation (EC) NO. 1126/2007 (23 Februari 2007).
8. Turner, N.W., Subrahmanyam, S., Piletsky, S.A. (2009) Analytical methods for determination of mycotoxins: A review. Anal Chim Acta 632:168-180.
9. Cavaliere, D., Ascenzo, G. D., Foglia, P., Pastorini, E., Samperi, R., Lagana, A. (2005) Determination of type B trichothecenes and macrocyclic lactone mycotoxins in field contaminated maize. Food Chem 92:559-568.
10. Caveliere, D., Foglia, P., Guarino, C., Motto, M., Nazzari, M., Samperi, R., Lagana, A., Berardo, N. (2007) Mycotoxins produced by Fusarium genus in maize: determination by screening and confirmatory methods based on liquid chromatography tandem mass spectrometry. Food Chem 105:700-710.
11. Han, H., Yang, L., Xu, Y., Ding, Y., Annie Bligh, S.W., Zhang, T., Wang, Z. (2011) Identification of metabolites of geniposide in rat urine using ultra-performance liquid chromatography combined with electrospray ionization quadrupole time-of-flight tandem mass spectrometry. Rapid Commun Mass Spectrom 25:3339-3350.
34
12. Ni, S., Qian, D., Duan, J.A., Guo, J., Shang, E. X., Shu, Y., Xue, C. (2010) UPLC-QTOF/MS-based screening and identification of constituents and their metabolites in rat plasma and urine after oral administration of Glechoma longituba extract. J Chromatogr B Analyt Technol Biomed Life Sci. 878:2741-2750.