Rev 0 1
1.
KARBOHIDRAT
1.
Pendahuluan
Karbohidrat merupakan makromolekul yang penting bagi tongkat kehidupan mahluk hidup. Senyawa karbohidrat menyumbangkan 70 – 80% sumber energi untuk aktivitas manusia. Konsumsi rata-rata karbohidrat dalam makanan sekitar 65% dan energi yang dihasilkan dari metabolisme selular karbohidrat tersebut akan digunakan untuk metabolisme biomolekul lainnya seperti protein, lemak dan asam nukleat. Selain itu, lebih dari 90% komponen penyusun tumbuhan kering adalah karbohidrat. Secara umum, karbohidrat merupakan senyawa polihidroksialdehid atau polihidroksiketon dan derivatnya dalam bentuk unit tunggal yang sederhana maupun unit kompleks.
Pada tumbuhan, glukosa disintesis dari karbon dioksida (CO2) dan air (H2O) melalui proses fotosintesis dan disimpan dalam bentuk pati atau selulosa. Binatang mensintesis karbohidrat dari lipid gliserol dan asam amino, akan tetapi derivat karbohidrat yang digunakan oleh binatang diambil dari tanaman. Glukosa bisa diabsorpsi langsung dalam aliran darah dan gula bentuk lain akan diubah menjadi glukosa dalam liver sehingga glukosa merupakan jenis karbohidrat yang penting. Sebagai sumber utama energi pada mamalia, glukosa dapat disintesis menjadi glikogen sebagai cadangan makanan, ribosa dan deoksiribosa pada asam nukleat, galaktosa pada laktosa susu, glikolipid dan kombinasi dengan protein (glikoprotein dan proteoglikan).
2.
Klasifikasi dan Nomenklatur Karbohidrat
Klasifikasi karbohidrat yaitu: 1) Monosakarida
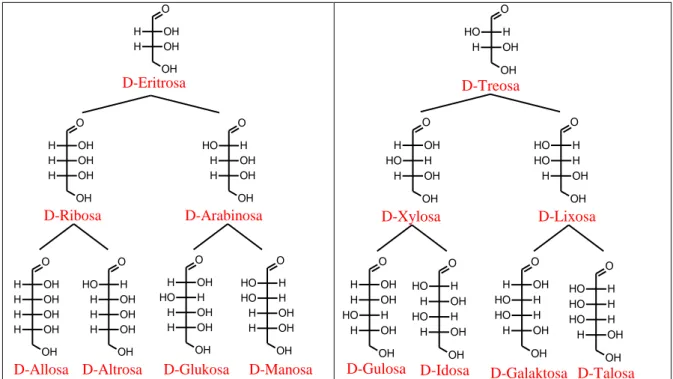
Monosakarida adalah jenis karbohidrat yang tidak dapat dihidrolisis menjadi gula yang lebih sederhana. Berdasarkan gugus fungsinya, jenis monosakarida ada dua yaitu aldosa yang memiliki gugus fungsi aldehid dan ketosa yang memiliki gugus fungsi keton. Berdasarkan jumlah atom karbonnya, monosakarida terdiri dari triosa, tetrosa, pentosa, dan heksosa.
Tabel 1.1 Klasifikasi Monosakarida Berdasarkan Jumlah Atom C
Jumlah atom C Aldosa Ketosa
Triosa (C3H6O3) Gliserosa Dihidrosiaseton
Tetrosa (C4H8O4) Eritrosa Eritrulosa
Pentosa (C5H10O5) Ribosa Ribulosa
Rev 0 2 O OH H OH H OH OH O H OH H OH H OH OH O O H H H OH H OH OH O H OH H OH H OH H OH OH O O H H H OH H OH H OH OH O H OH O H H H OH H OH OH O O H H O H H H OH H OH D-Eritrosa D-Ribosa D-Arabinosa
D-Allosa D-Altrosa D-Glukosa D-Manosa
OH O O H H H OH D-Treosa OH O H OH O H H H OH D-Xylosa OH O O H H O H H H OH D-Lixosa OH O H OH H OH O H H H OH D-Gulosa OH O O H H H OH O H H H OH D-Idosa OH O H OH O H H O H H H OH D-Galaktosa OH O O H H O H H O H H H OH D-Talosa Gambar 1.1 Klasifikasi Aldosa
2) Oligosakarida
Oligosakarida adalah hasil kondensasi dari dua sampai sepuluh monosakarida. Oligosakarida dapat berupa disakarida, trisakarida dan tetrasakarida. Disakarida merupakan hasil kondensasi dua unit monosakarida. Contohnya adalah laktosa, maltosa dan sukrosa. Trisakarida merupakan hasil kondensasi tiga unit monosakarida dan tetrasakarida terdiri dari empat unit monosakarida.
3) Polisakarida
Polisakarida merupakan hasil kondensasi dari lebih dari lebih dari dua puluh unit monosakarida. Polisakarida terdiri dari homopolisakarida dan heteropolisakarida. Homopolisarida adalah polisakarida yang terdiri dari unit monosakarida yang sama sedangkan heteropolisakarida terdiri dari unit monosakarida yang berbeda.
Tabel 1.2 Nomenklatur dan Klasifikasi Karbohidrat
Karbohidrat
Monosakarida Oligosakarida Polisakarida
Gugus fungsional
Jumlah
atom C Disakarida Trisakarida Tetrasakarida homopolisakarida heteropolisakarida Aldosa
(glukosa)
Triosa Maltosa Raffinosa Staciosa Dekstrin Asam hialuronik
Tetrosa Laktosa Selulosa Heparin
Ketosa (fruktosa)
Pentosa Sukrosa Glikogen Kondroitin sulfat
Heksosa Inulin Dermatan sulfat
Rev 0 3
3.
Monosakarida
Monosakarida biasanya tidak berwarna, berupa padatan kristal, larut dalam air dan sulit larut dalam larutan nonpolar. Struktur monosakarida terdiri dari gugus aldehid atau keton dengan dua atau lebih gugus hidroksil. Monosakarida yang memiliki gugus fungsional aldehid disebut dengan aldosa sedangkan yang memiliki gugus keton disebut ketosa. Aldosa paling sederhana adalah gliseraldehid yang terdiri dari tiga atom C sedangkan ketosa yang paling sederhana adalah dihidroksiaseton.
OH O H OH O H H H OH H OH OH O H H H OH H OH O OH
Glukosa (aldosa) Fruktosa (ketosa)
Gambar 1.2 Aldosa dan Ketosa
Atom C pada monosakarida biasanya berupa C kiral sehingga monosakarida memiliki stereoisomer. Oleh sebab itu, monosakarida memiliki enantiomer dan epimer. Enantiomer adalah stereoisomer yang merupakan bayangan kaca dari suatu molekul. Berdasarkan sifat stereoisomer, molekul monosakarida dibagi menjadi Dextro dan Levo. Dua jenis gula yang memiliki perbedaan pada satu atom karbon spesifik dinamakan dengan epimer. Contoh epimer adalah D-glukosa dan D-manosa yang memiliki perbedaan pada atom karbon nomor 2.
OH O H OH O H H H OH H OH O H O H O H OH H H O H H O H D-Glukosa L-Glukosa cermin
Rev 0 4
OH
O
H
OH
O
H
H
H
OH
H
OH
OH
O
O
H
H
O
H
H
H
OH
H
OH
D-Mannosa D-GlukosaOH
O
H
OH
O
H
H
O
H
H
H
OH
D-GalaktosaGambar 1.4 Contoh Epimer Monosakarida
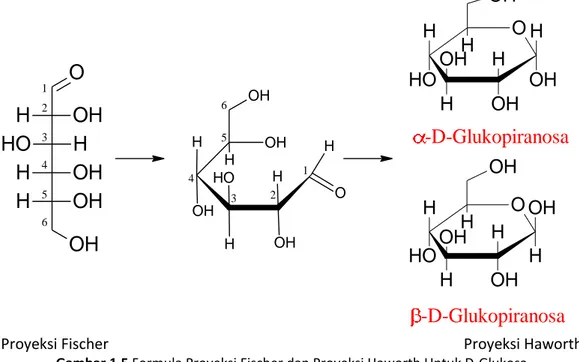
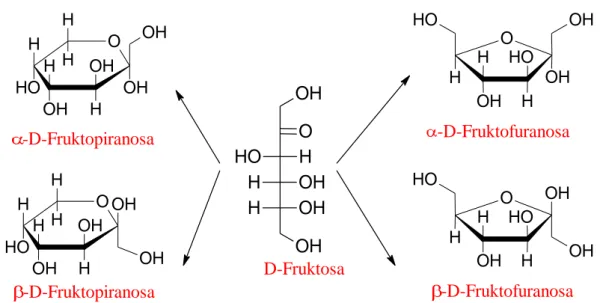
Selain proyeksi Fischer, monosakarida juga dapat digambarkan dengan proyeksi Haworth dalam bentuk piranosa atau furanosa. Aldosa biasanya membentuk struktur molekul piranosa. Piranosa merupakan struktur cincin yang terdiri dari 6 atom yang terbentuk karena ada reaksi gugus fungsi hidroksil alkoholik pada atom C 5 dengan aldehid pada atom C 1. Piranosa merupakan derivat senyawa heterosiklik piran. D-glukosa dapat membentuk D-glukopiranosa dengan dua bentuk isomer yaitu α dan β. Ketoheksosa juga dapat membentuk isomer α dan β serta biasanya membentuk srtuktur furanosa yang merupakan derivat furan. Cincin furanosa merupakan struktur cincin yang terdiri atas 5 atom dimana terbentuk karena ada reaksi antara gugus fungsi hidroksil alkoholik pada atom C 5 dengan gugus karbonil pada atom C 2.
OH
O
H
OH
O
H
H
H
OH
H
OH
1 2 3 4 5 6 OH OH OH O H OH O H H H H HO
OH
H
H
H
O
H
OH
H
OH
H
OH
-D-Glukopiranosa
O
H
H
H
H
O
H
OH
H
OH
OH
OH
-D-Glukopiranosa
1 2 3 4 5 6Proyeksi Fischer Proyeksi Haworth
Rev 0 5
OH
O
H
H
H
OH
H
OH
O
OH
O OH H O H OH H H O H OH-D-Fruktofuranosa
O OH H O H OH H H O H OH-D-Fruktofuranosa
O OH OH H H O H H OH H H OH-D-Fruktopiranosa
O OH H H O H H OH H OH H OH-D-Fruktopiranosa
D-Fruktosa
Gambar 1.6 Cincin Furanosa dan Cincin Piranosa
4.
Oligosakarida
Oligosarida terbentuk karena adanya ikatan glikosidik antara molekul monosakarida pada atom C 1 molekul satu dengan gugus hidroksil ( -OH) pada molekul lainnya. Biasanya ikatan glikosidik terbentuk antara C 1 pada satu molekul dengan C 3 pada molekul lainnya ( 1 3). Ikatan glikosidik yang umum adalah 1 3, 1 4 dan 1 6. Akan tetapi, ikatan glikosidik 1 1 dan 1 2 juga mungkin terjadi. Ikatan dapat terjadi dalam bentuk molekul α dan β.
1) Disakarida
Disakarida terdiri atas dua molekul monosakarida yang terikat dengan ikatan glikosidik. Beberapa contoh senyawa disakarida dapat dilihat pada Tabel di bawah ini.
Tabel 1.3 Beberapa Contoh Disakarida Nama Monosakarida
penyusun
Ikatan glikosidik
Nama umum
maltosa Glukosa + Glukosa 1 4 α-D-glikopiranosil-(1 4)-β-D-glukopiranosida
selobiosa Glukosa + Glukosa 1 4 β-D-glikopiranosil-(1 4)-β-D-glukopiranosida
gentiobiosa Glukosa + Glukosa 1 6 β-D-glikopiranosil-(1 6)-β-D-glukopiranosida
sukrosa Glukosa + fruktosa 2 1 β-D-fruktofuranosil-(2 1)-α-D-glukopiranosida
laktosa Glukosa + galaktosa 1 4 β-D-galaktopiranosil-(1 4)-β-D-glukopiranosida
trehalosa Glukosa + Glukosa 1 1 α-D-glikopiranosil-(1 1)-α-D-glukopiranosida
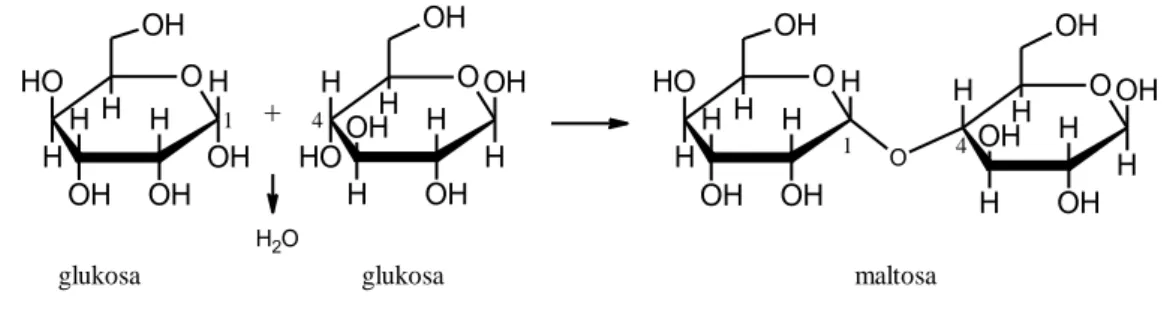
Rev 0 6 O OH H H O H H H OH OH H OH O H H H H O H OH H OH OH OH + O H H O H H H OH OH H OH O O H H H H OH H OH OH OH O H2 1 4 1 4
glukosa glukosa maltosa
Gambar 1.7 Dehidrasi Maltosa
2) Trisakarida
Trisakarida terdiri atas tiga molekul monosakarida dimana antarmolekul terikat dengan ikatan glikosodik. Sejumlah trisakarida dapat ditemukan bebas di alam seperti rafinosa (α-D-galaktopiranosil-(16)-α-D-glukopiranosil-(1 2)-β-D-fruktofuranosida) yang sering dinamakan dengan gula beet dan melezitosa (α-D-glukopiranosil-(13)-β-D-fruktofuranosil-(21)-α-D-glukopiranosida).
Gambar 1.8 Struktur Rafinosa
5.
Polisakarida
Polisakarida merupakan jenis karbohidrat kompleks yang terdiri atas unit monosakarida yang terikat dengan ikatan glikosidik. Secara nomenklatur, polisakarida dibagi menjadi dua, yaitu homopolisakarida dan heteropolisakarida. Polisakarida yang berfungsi sebagai bahan makanan cadangan yaitu pati dan glikogen, sedangkan pembentuk struktur molekul yaitu kitin dan selulosa.
1) Pati
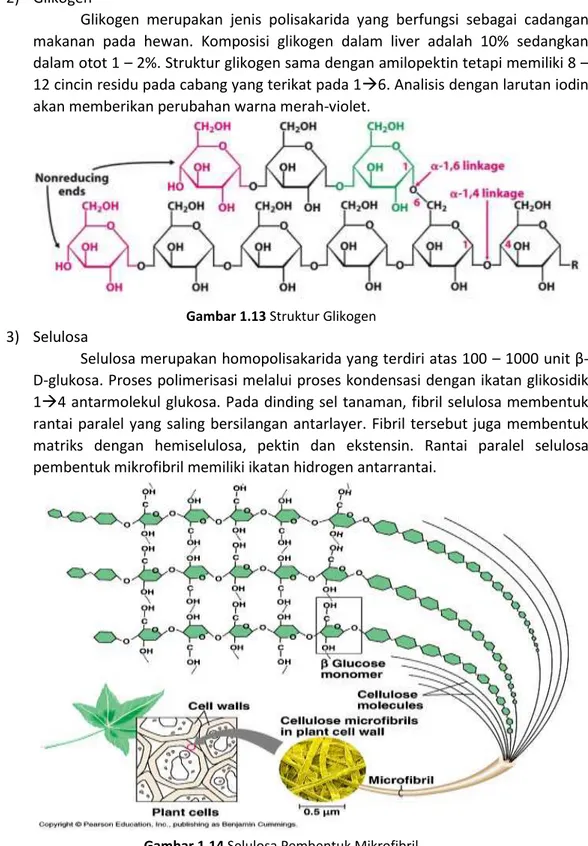
Pati merupakan senyawa cadangan pada tumbuhan yang terdiri atas unit glukosa. Pati terdiri atas dua komponen homopolisakarida yaitu amilosa dan amilopektin. Susunan komponen tersebut dalam tumbuhan yaitu 10 – 30% amilosa dan 70 – 90% amilopektin. Amilosa memiliki struktur rantai lurus yang terbentuk dari ikatan glikosidik 1 4 antara molekul α-D-glukosa. Amilosa dapat membentuk struktur heliks dimana rata-rata terdapat 8 molekul glukosa setiap putaran heliks. Amilosa memiliki sifat sukar larut dalam medium air tetapi dapat
Rev 0 7 membentuk suspensi miselar. Jika dianalisis dengan menggunakan iodin, amilosa akan membentuk kompleks berwarna biru.
Gambar 1.9 Struktur Amilosa
Gambar 1.10 Struktur Heliks Amilosa
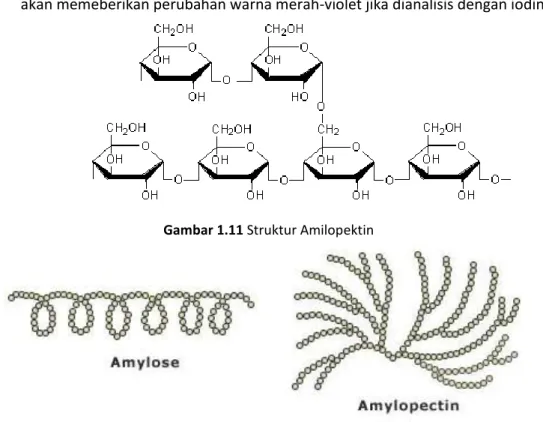
Amilopektin merupakan polimer glukosa yang terdiri atas rantai lurus dengan ikatan glikosidik 14 dan cabang yang terbentuk dengan ikatan 16. Amilopektin akan memeberikan perubahan warna merah-violet jika dianalisis dengan iodin.
Gambar 1.11 Struktur Amilopektin
Rev 0 8 2) Glikogen
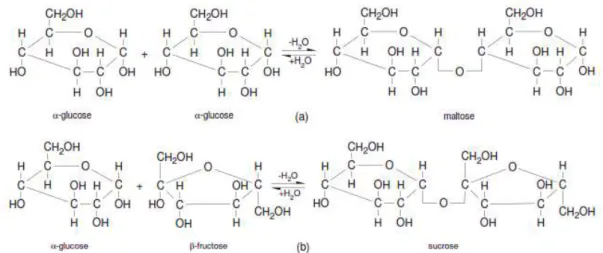
Glikogen merupakan jenis polisakarida yang berfungsi sebagai cadangan makanan pada hewan. Komposisi glikogen dalam liver adalah 10% sedangkan dalam otot 1 – 2%. Struktur glikogen sama dengan amilopektin tetapi memiliki 8 – 12 cincin residu pada cabang yang terikat pada 16. Analisis dengan larutan iodin akan memberikan perubahan warna merah-violet.
Gambar 1.13 Struktur Glikogen
3) Selulosa
Selulosa merupakan homopolisakarida yang terdiri atas 100 – 1000 unit β-D-glukosa. Proses polimerisasi melalui proses kondensasi dengan ikatan glikosidik 14 antarmolekul glukosa. Pada dinding sel tanaman, fibril selulosa membentuk rantai paralel yang saling bersilangan antarlayer. Fibril tersebut juga membentuk matriks dengan hemiselulosa, pektin dan ekstensin. Rantai paralel selulosa pembentuk mikrofibril memiliki ikatan hidrogen antarrantai.
Rev 0 9 Beberapa jenis polisakarida lainnya dapat dilihat pada Tabel 1.4.
Tabel 1.4 Beberapa Jenis Polisakarida Jenis
Polisakarida
Keterangan
Kitin Poliglukosa amina Ditemukan dalam dinding sel fungi dan eksoskeleton insekta
Kalosa Poli-1-3-glukosa Ditemukan dalam dinding phloem tubes Dekstran Poli-1-2, 1-3, dan 1-4
glukosa
Cadangan makanan pada fungi dan bakteri
Inulin polifruktosa Cadangan makanan pada tumbuhan
Agar Poligalaktosa sulfat Ditemukan pada algae dan digunakan untuk membuat agar plate
Murein Polimer gula-peptida Ditemukan pada dinding sel bakteria
Lignin Polimer kompleks Ditemukan pada dinding sel xylem,komponen utama kayu
6.
Analisis Kualitatif
Berdasarkan reagen tes yang digunakan, analisis kualitatif karbohidrat dibedakan dalam tiga jenis sesuai dengan tipe reaksi yang terjadi yaitu:
1) Asam dehidrasi. Reagen ini akan menyebabkan karbohidrat mengalami dehidrasi dan membentuk furfural (bentuk pentosa) atau 5-hidroksimetilfurfural (bentuk heksosa).
Rev 0 10 2) Reagen kondensasi. Reagen ini mendeteksi adanya furfuran atau
5-hidroksimetilfurfural melalui proses adisi. Jenis reagen yang masuk dalam kategori ini adalah reagen Molisch, Bial, dan Seliwanoff.
3) Reagen gula pereduksi. Biasanya reagen ini mengandung ion tembaga(II) dan dapat mereduksi karbohidrat dimana ion tembaga(II) akan direduksi menjadi larutan tembaga(I) oksida. Jenis reagen yang sering digunakan sebagai gula pereduksi adalah reagen Benedict dan Barfoed. Gula pereduksi yaitu semua gula yang termasuk dalam golongan aldosa baik dalam bentuk gugus aldehid bebas ataupun dalam bentuk siklik hemiasetal.
Gambar 1.16 (a) Disakarida Pereduksi; (b) Disakarida Nonpereduks
Tabel 1.5 Daftar Analisis Kualitatif Karbohidrat
No. Tes Hasil positif untuk Keterangan
1 Tes Molish Semua karbohidrat. Monosakarida menghasilkan warna ungu dengan cepat sedangkan polisakarida bereaksi lebih lambat
Hasil negatif (kiri) dan hasil positif (kanan)
2 Tes I2/KI Pati
Rev 0 11
3 Tes Barfoed
Gula pereduksi (monosakarida)
Hasil negatif (kiri) dan hasil positif (kanan)
4 Tes Seliwanoff
Ketosa
Hasil negatif (kiri) dan hasil positif (kanan)
5 Tes Benedict
Gula pereduksi
Hasil negatif (kiri) dan hasil positif (kanan)
6 Tes Bial Pentosa
Hasil negatif (kiri dan tengan) dan hasil positif (kanan)
Rev 0 12
Gambar 1.17 Flow Chart Identifikasi Contoh Karbohidrat
Analisis kualitatif glukosa pada contoh biokimia seperti urin dapat dilakukan dengan menggunakan tes Tromer, tes Fehling atau Tes Nilender.
1) Reaksi Tromer dan Fehling
Reagen yang digunakan pada tes ini adalah reagen Fehling yang dimodifikasi dengan reagen Tromer dimana garam Segnet akan bereaksi dengan bentuk antara yaitu Cu(OH)2. Dengan bantuan pemanasan, reagen yang berwarna biru akan membentuk larutan kuning dan akan menjadi merah dengan pemanasan lanjut. Jika tidak ada glukosa dalam urin maka warna reagen tidak berubah.
Tes Molisch
Bukan karbohidrat Karbohidrat Tidak ada reaksi ungu
Tes I2/KI Kompleks biru-hitam Karbohidrat sederhana Polisakarida (pati) Tidak ada reaksi
Tes Barfoed Endapan merah setelah 10 menit Monosakarida pereduksi Disakarida pereduksi Endapan merah setelah 2-3 menit Tes Benedict Endapan merah
Gula nonpereduksi Gula pereduksi Tidak ada reaksi merah aldosa Ketosa Hijau-biru jingga Tes Seliwanoff Pentosa Biru-hijau heksosa Coklat – abu-abu Pentosa Biru-hijau heksosa Coklat – abu-abu
Rev 0 13 2) Reaksi Nilander
Reaksi ini sangat sensitif dalam mendeteksi glukosa dalam kadar rendah hingga konsentrasi sekitar 0,5 g/l. Reagen Nilander, yang mengandung garam bismut, direksikan dengan contoh yang mengandung glukosa dan dilakukan pemanasan dengan menggunakan penangas air. Setelah beberapa menit, larutan akan semakin gelap dimana glukosa akan mereduksi Bi(OH)3 sampai terbentuk Bismut bebas dan endapan berwarna hitam terbentuk.
3) Reaksi Fischer
Glukosa, laktosa dan karbohidrat yang memiliki gugus aldehid bebas (aldosa) jika direaksikan dengan fenil hidrazin dan dibantu dengan pemanasan akan membentuk ozazone yang berupa kristal dengan bentuk spesifik. Kristal glukozazon berbentuk
whisk sedangkan kristal laktozazon berbentuk seperti bulu babi. Selain mengamati bentuk kristal ozazon dengan mikroskop, analisis kualitatif monosakarida juga dilakukan dengan menentukan titik leleh kristal ozazon yang terbentuk. Dimana glukozazon dan fruktozazon meleleh pada 210oC, galaktozazon meleleh pada 180oC dan pentozazon meleleh pada 160oC.
7.
Analisis Kuantitatif
Penentuan kadar gula dalam beberapa sampel biokimia dapat dianalisis dengan menggunakan instrumen spektrofotometri dan kromatografi. Beberapa contoh penentuan gula dijelaskan seperti di bawah ini.
1) Penentuan Kadar Glukosa Secara Colourmetric
Prinsip analisis ini berdasarkan pengukuran hasil reaksi oksidasi glukosa melalui proses enzimatis secara colourmetric. Dengan adanya oksigen, glukosa dioksidasi oleh glukosa oksidase (GOD) menjadi asam glukonik dan hidrogen peroksida (H2O2). Hidrogen peroksida akan bereaksi dengan 4-klorofenol dan 4-aminoantipirin dengan katalis peroksidase (POD) dan membentuk quinoneimine yang berwarna merah. Intensitas zat warna yang terbentuk memiliki proporsi yang sama dengan konsentrasi glukosa dan dapat diukur menggunakan spektrofotometer.
glukosa
+
O
2 GODasam glukonik
+
H
2O
2H
2O
2+
4-AA
POD
fenol
+
Quinoneimine (merah)
+
4H
2O
4-AA adalah 4-aminoantipirinContoh yang biasanya digunakan adalah serum darah bebas hemolisis dan plasma diambil dari heparin atau inhibitor glikolisis. Kondisi pengukuran dilakukan pada
Rev 0 14 panjang gelombang 500 nm dengan menggunakan kuvet dengan ketebalan 1 cm dan reaksi dilakukan pada temperatur 37oC. Reagen yang digunakan pada penentuan ini adalah buffer fosfat (pH 7,4), fenol, 4-aminoantipirin (4-AA), glukosa oksidase (GOD) dan Peroksidase (POD). Sedangkan larutan standar yang digunakan adalah larutan glukosa 5,55 mmol/l (100 mg/dl).
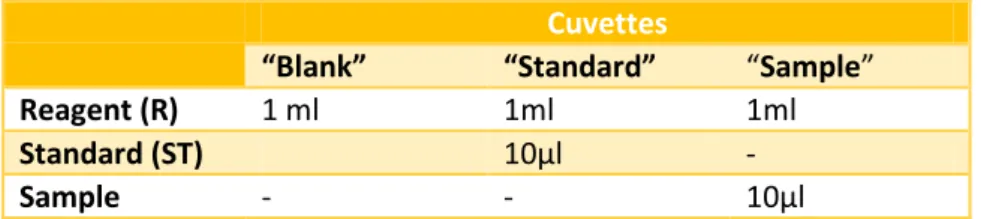
Cuvettes
“Blank” “Standard” “Sample”
Reagent (R) 1 ml 1ml 1ml
Standard (ST) 10µl -
Sample - - 10µl
Reaksi antara glukosa dan reagen dilakukan pada temperatur 37oC selama 15 menit agar reaksi enzimatik berjalan sempurna. Kalkulasi kadar glukosa dengan menggunakan standar tunggal dapat ditentukan dengan rumus:
Dimana faktor konversi 1 mg/dl x 0,0555 = 1 mmol/l dan 1 mg/dl x 0,01 = 1 g/l.
Tabel 1.6 Nilai Kadar Glukosa Pada Beberapa Contoh Biokimia
Contoh Nilai kadar glukosa
Serum darah 4,1 – 6,4 mmol/l
Darah kapiler 3,33 – 5,55 mmol/l
Larutan cerebrospinal 2,78 – 3,89 mmol/l 2) Penentuan Kadar Glukosa dengan Reaksi Fehling secara Titrimetri
Kadar glukosa dalam contoh urin dapat dianalisis dengan menggunakan prinsip reaksi Fehling. Reagen Fehling yang digunakan adalah CuSO4 (Fehling I), garam Segnet yang dicampurkan dengan larutan NaOH (Fehling II). CuSO4 pada reagen Fehling akan mengalami reduksi menjadi Cu2O, dimana 1 mL reagen fehling setara dengan 0,005 gram glukosa. Prosedur analisis ini yaitu campuran 2,5 mL Fehling I; 2,5 mL Fehling II dan 20 mL air terdistilasi dititrasi menggunakan contoh urin sambil dididihkan di atas pemanas. Warna biru pada larutan akan berubah menjadi hijau dan kemudian menjadi kuning. Ketika warna kuning menghilang, maka titik ekuivalen tercapai. Kadar glukosa dapat ditentukan dengan cara
Dimana a adalah volume contoh urin yang digunakan selama proses titrasi dan 5 adalah volume reagen Fehling yang digunakan.