CH
EM
ICA
L P
RO
CE
SS
SY
STE
M
UN
IT
OP
ER
AT
ION
UN
IT
OP
ER
AT
ION
RE
AC
TO
R
7RE
CY
CL
E
UN
IT P
EM
RO
SES
AN
PR
OD
UC
T
FEE
D
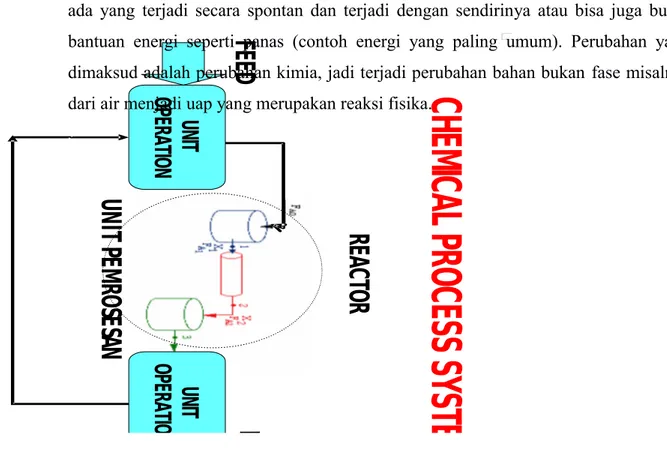
BAB I PENDAHULUAN 1.1. Latar BelakangDi Industri kimia, penggunaan reaktor merupakan “jantung” dari proses kimia untuk mendapatkan produk yang diinginkan. Untuk perancangan reaktor skala industri tersebut, dibutuhkan data-data kinetika sehingga dibutuhkan studi awal, seperti melakukan serangkaian percobaan dengan menggunakan reaktor skala laboratorium yang disesuaikan dengan jenis reaksi yang akan terjadi.
Reaktor adalah suatu alat proses tempat di mana terjadinya suatu reaksi berlangsung, baik itu reaksi kimia atau nuklir dan bukan secara fisika. Dengan terjadinya reaksi inilah suatu bahan berubah ke bentuk bahan lainnya, perubahannya ada yang terjadi secara spontan dan terjadi dengan sendirinya atau bisa juga butuh bantuan energi seperti panas (contoh energi yang paling umum). Perubahan yang dimaksud adalah perubahan kimia, jadi terjadi perubahan bahan bukan fase misalnya dari air menjadi uap yang merupakan reaksi fisika.
Gambar 1 Proses Reaksi Kimia
Untuk merancang sebuah reaktor diperlukan bekal pengetahuan tentang pengaruh variabel-variabel : Konsentrasi, suhu, tekanan, kecepatan aliran umpan pada persamaan kecepatan reaksi, yang dapat dipelajari dari materi kinetika dan katalisa. Sumber data yang diperlukan pada perancangan sebuah reactor dapat diperoleh dengan jalan melakukan :
1. Percobaan dengan reactor kecil di laboratorium. Biasanya percobaan dijalankan pada suhu konstan (secara isothermal) dengan mengubah-ubah variable :
Konsentrasi zat pereaksi, perbandingan zat pereaksi dan suhu untuk reactor batch, atau dengan mengubah-ubah variable kecepatan aliran dan suhu jika dipakai reactor alir pipa.
Dari data-data yang diperoleh diharapkan dapat diinterpretasi untuk menentukan persamaan kecepatan reaksi, harga konstanta kecepatan reaksi dan hubungan antara konstanta kecepatan reaksi dengan suhu.
2. Pilot Plant. Pada tahap ini dipakai reactor yang ukurannya lebih besar dibandingkan yang dipakai pada percobaan dilaboratorium. Percobaan dijalankan dengan jenis reactor yang sama pada suhu, tekanan, konsentrasi, kecepatan aliran umpan, perpindahan panas, yang sesuai dengan keadaan operasi reactor kimia yang akan dirancang.
Dari percobaan pilot Plant ini diharapakan diperoleh data-data tambahan untuk melihat penyimpangan yang terjadi jika dibandingkan dengan perhitungan teoritis yang diperoleh dari data laboratorium, akibat besarnya kapasitas reactor/kecepatan aliran umpan.
3. Mempelajari data operasi yang diperoleh dari industri yang sejenis. .2. Tujuan
a) Menjelaskan pengertian Reaktor secara umum
b) Mengetahui macam macam reaktor ditinjau dari prosesnya c) Mengetahui neraca massa dan neraca panas pada Reaktor d) Menghitung tinggi dan diameter Reaktor
BAB II PEMBAHASAN 2.1. Jenis- jenis Reaktor
Ditinjau dari bentuk, proses dan kondisi operasinya maka reaktor dibagi menjadi beberapa jenis yaitu :
1. Berdasarkan bentuknya: a) Reaktor tangki
Dikatakan reaktor tangki ideal bila pengadukannya sempurna, sehingga komposisi dan suhu didalam reaktor setiap saat selalu uniform. Dapat dipakai untuk proses batch, semi batch, dan proses alir.
b) Reaktor pipa
Biasanya digunakan tanpa pengaduk sehingga disebut Reaktor Alir Pipa. Dikatakan ideal bila zat pereaksi yang berupa gas atau cairan, mengalir didalam pipa dengan arah sejajar sumbu pipa.
2. Berdasarkan prosesnya : a) Reaktor batch
Batch Reactor adalah tempat terjadinya suatu reaksi kimia tunggal, yaitu reaksi yang berlangsung dengan hanya satu persamaan laju reaksi yang berpasangan dengan persamaan kesetimbangan dan stoikiometri.
Reaktor jenis ini biasanya sangat cocok digunakan untuk produksi berkapasitas kecil misalnya dalam proses pelarutan padatan, pencampuran produk, reaksi kimia, Batch distillation, kristalisasi, ekstraksi caircair,
polimerisasi, farmasi dan fermentasi.
Kelebihan penggunaan reaktor batch:
1. Ongkos atau harga instrumentasi rendah.
2. Penggunaannya fleksibel, artinya dapat dihentikan secara mudah dan cepat kapan saja diinginkan.
3. Penggunaan yang multifungsi.
4. Reaktor ini dapat digunakan untuk reaksi yang menggunakan campuran kuat dan beracun.
5. Mudah dioperasikan, dikontrol dan dibersihkan.
6. Dapat menangani reaksi dalam fase gas, cair dan cair-padat.
Kelemahan penggunaan reaktor batch :
1. Biaya buruh dan handling tinggi.
2. Kadang-kadang waktu shut downnya besar, yaitu waktu untuk mengosongkan, membersihkan dan mengisi kembali.
3. Pengendalian kualitas dari produk jelek atau susah. 4. Skala produksi yang kecil.
5. Tidak begitu baik untuk reaksi fase gas (mudah terjadi kebocoran pada lubang pengaduk)
Gambar 2. Reaktor Batch b) Reaktor semi batch
Biasanya berbentuk tangki yang berpengaduk dan cara operasinya dengan jalan memasukkan sebagian zat pereaksi ke dalam reaktor, sedangkan zat pereaksi yang lain atau sisanya dimasukkan secara kontinu ke dalam reaktor. Ada material masuk selama operasi tanpa dipindahkan. Reactant (massa) yang masuk bisa dihentikan dan product bisa dipindahkan selama operasi waktu tertentu.Tidak beroperasi secara steady state
Gambar 3. Reaktor Semi Batch c) Proses kontinyu (reaktor pipa, reaktor tanki)
Reaktor kontinyu mempunyai aliran masukan dan keluaran (inlet/outlet) yang terdiri dari campuran homogen/heterogen . Reaksi kontinue di operasikan pada kondisi steady. Dimana arus aliran masuk sama dengan arus aliran keluar .
Reaktor kontinyu dibagi menjadi dua jenis utama, yaitu :
1. Reaktor AlirTangki Berpengaduk (RATB) atau Continous Stirred Tank Reaktor (CSTR)
RATB adalah reaktor model berupa tangki berpengaduk dan diasumsikan pengaduk yang bekerja dalam tanki sangat sempurna sehingga konsentrasi tiap komponen dalam reaktor seragam sebesar konsentrasi aliran yang keluar dari reaktor. Model ini biasanya digunakan pada reaksi homogen di mana semua bahan baku dan katalisnya berfasa cair, atau reaksi antara cair dan gas dengan katalis cair.
Prinsip Kerja reaktor CSTR :
1. satu atau lebih reagen fluida dimasukkan pada tangki sebuah reaktor yang dilengkapi dengan kipas atau impeller
2. impeller mengaduk cairan untuk memastikan cairan tersebut tercampur rata
3. ada waktu suatu cairan berada di dalam tabung tersebut sebelum keluar
Beberapa aspek penting dalam CSTR :
1. Dalam keadaan tetap, fluida yang masuk harus sama dengan fluida yang keluar
2. Semua kalkulasi yang dilakukan CSTR diasumsikan sebagai pencampuran sempurna
3. Untuk mendapatkan hasil yang lebih banyak dalam waktu yang sama, dapat dilakukan dengan memparalelkan CSTR ini
Kelebihan penggunaan reaktor CSTR:
1. Operasi dalam keadaan tetap menyebabkan peralatan produk lebih stabil
2. Penggunaan energi yang kualitasnya meningkat
3. Produktivitas yang lebih tinggi dalam reduksi pada periode tidak aktif(pengisian, pemanasan, pendinginan, dan pengosongan). 4. Campuran lebih rata karena penggunaan teknik pengadukan
(stiring)
Kelemahan menggunakan CSTR:
1. Rata-rata reaksi volumetrik yang lebih rendah akan menghasilkan produktivitas rendah.
2. Tidak sesuai untuk keseluruhan emulsi proses polimerisasi pada tahap pertama penggunaan CSTR
3. Timbul endapan di dasar akibat gaya sentrifugal CSTR
4. Tidak dapat merubah grade dari RTD profile sesering mungkin karena dapat mengurangi fleksibilitas reaktor
5. Biaya tinggi, semakin besar CSTR yang digunakan atau semakin banyak CSTR kecil yang digunakan semakin besar biaya yang dikeluarkan
Gambar 4. Reaktor RATB / CSTR
2. Reaktor Alir Pipa (RAP) atu Plug Flow Reaktor (PFR).
Reaktor PFR (Plug Flow Reaktor ) merupakan suatu reaktor berbentuk pipa yang beroperasi secara kontinyu. Dalam PFR selama operasi berlangsung bahan baku dimasukkan terus menerus dan produk reaksi akan dikeluarkan secara terus menerus sehinga disini tidak terjadi pencampuran ke arah aksial dan semua molekul mempunyai waktu tinggal di dalam reaktor sama besar.
Reaktor plug flow Adalah suatu alat yang digunakan untuk mereaksikan suatu reaktan dalam hal ini fluida dan mengubahnya menjadi produk dengan cara mengalirkan fluida tersebut dalam pipa secara berkelanjutan (continuous). Biasanya reaktor ini dipakai untuk mempelajari berbagai proses kimia yang penting seperti perubahan kimia senyawa, reaksi termal, dan lain-lain.
Reaktor Plug Flow biasanya Untuk reaksi heterogen, misalnya antara bahan baku gas dengan katalis padat menggunakan model PFR. PFR mirip saringan air dari pasir. Katalis diletakkan pada suatu pipa lalu dari sela-sela katalis dilewatkan bahan baku seperti air melewati sela-sela pasir pada saringan. Asumsi yang digunakan adalah tidak ada perbedaan konsentrasi tiap komponen yang terlibat di sepanjang arah jari-jari pipa.
Kelebihan penggunaan RAP :
2. Bekerja dalam periode waktu yang cukup lama tanpa tenaga kerja sehingga upah produksi rendah
3. Perpindahan kalornya baik sekali 4. Operasinya terus-menerus
Kelemahan penggunaan RAP :
1. Sulit mengontrol temperaturnya
2. Tingginya temperature yang tidak diinginkan dapat terjadi 3. Proses pemberhentian dan pembersihannya mahal
Gambar 5.
Reaktor Alir Pipa / PFR 3. Berdasarkan keadaan operasinya:
1. Reaktor isotermal
Dikatakan isotermal jika umpan yang masuk, campuran dalam reaktor, aliran yang keluar dari reaktor selalu seragam dan bersuhu sama.
2. Reaktor Adiabatis
Dikatakan adiabatis jika tidak ada perpindahan panas antara reaktor dan sekelilingnya.
Jika reaksinya eksotermis, maka panas yang terjadi karena reaksi dapat dipakai untuk menaikkan suhu campuran di reaktor. ( K naik dan –rA besar sehingga waktu reaksi menjadi lebih pendek).
3. Reaktor Non-Adiabatis
1) Packed/Fixed bed reaktor (PBR).
Terdiri dari satu pipa/lebih berisi tumpukan katalis stasioner dan dioperasikan vertikal. Biasanya dioperasikan secara adiabatis.
Gambar 6. Fixed Bad Reaktor 2) Fluidized bed reaktor (FBR)
Reaktor dimana katalisnya terangkat oleh aliran gas reaktan.
Perbedaan dengan Fixed bed: pada Fluidized bed jumlah katalis lebih sedikit dan katalis bergerak sesuai kecepatan aliran gas yang masuk serta FBR memberikan luas permukaan yang lebih besar dari PBR
Fluidized Bad Reaktor b. Fluid-fluid reaktor
Biasa digunakan untuk reaksi gas-cair dan cair-cair.
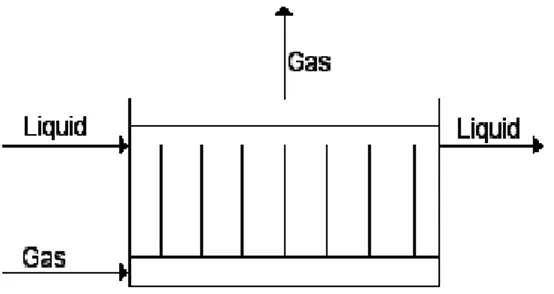
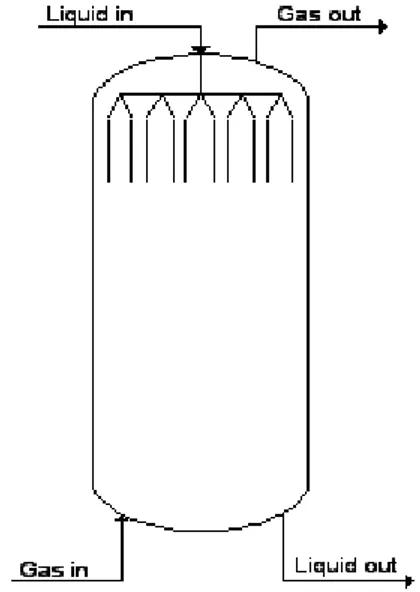
1)Bubble Tank.
Gambar 8. Bubble Tank Reaktor
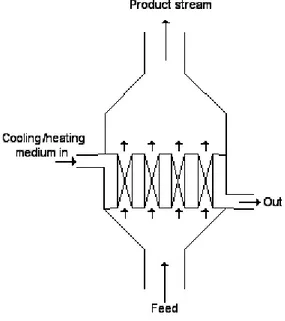
Gambar 9. Agitate Tank Reaktor 3)Spray Tower
Gambar 10. Spray Tower Reaktor
Pertimbangan dalam pemilihan fluid-fluid reaktor :
1. Untuk gas yang sukar larut (Kl <) sehingga transfer massa kecil maka Kl harus diperbesar .Jenis spray tower tidak sesuai karena kg besar pada Spray Tower
2. Jika lapisan cairan yang dominan, berarti tahanan dilapisan cairan kecil maka Kl harus diperbesar
» jenis spray tower tidak sesuai.
3. Jika lapisan gas yang mengendalikan (maka Kg <) » jenis bubble tank dihindari.
4. Untuk gas yang mudah larut dalam air » jenis bubble tank dihindari.
. Berdasarkan susunannya a. Reaktor Seri
1. Reaktor aliran plug susunan seri
Pada gambar menunjukkan sebuah sistem susunan seri reaktor aliran plug, dimana tidak terdapat sisa aliran antara reaktor berikutnya. Pada gambar tersebut terdapat tiga reaktor seri, tetapi ada beberapa kasus yang jumlah reaktornya lebih sedikit atau lebih banyak. Jumlah volume pada susunan seri untuk N reaktro, diekspresikan dalam bentuk keseimbangan mol untuk masing – masing reaktor.
Dengan kata lain, jumlah volume untuk semua reaktor diperoleh dengan mengintegralkan persamaan neraca mol input pada reaktor pertama dan cabang dari yang terakhir. Keseimbangan mol pada beberapa reaktor mungkin dapat dikalkulasikan pada bentuk sebuah konversi fraksi masukan (input) pada reaktor pertama.
Gambar 11.
Reaktor aliran plug susunan seri
2. CSTR dalam susunan seri
Sebuah sistem CSTR dalam susunan seri diilustrasikan pada gambar. Dalam hal ini, cabang dari satu reaktor membentuk aliran
yang ada pada reaktor yang berikutnya dalam susunan seri lainnya. Dalam bagian ini kita anggap bahwa tidak ada perubahan sistem antara reaktor. Persamaan konversi dapat diselesaikan untuk masing – masing reaktor dalam susunan seri.
Gambar 12.
CSTR dalam susunan seri
Total volume reaktor minimum untuk CSTR dalam susunan seri adalah dideterminasikan dari volume reaktor minimum yang dibutuhkan untuk memperoleh konversi pada kondisi yang ada pada reaktor pertama. Persamaan keseimbangan mol data ditulis untuk masing – masing CSTR, dengan konversi dalam beberapa reaktor yang ditentukan dalam bentuk nilai aliran molar A ada pada reaktor pertama. Nilai aliran Inlet dan outlet dibagi dengan nilai reaksi dapat di plot sebagai sebuah fungsi konversi untuk sistem reaktor ini. Minimisasi masssa dapat ditunjukan dalam bentuk nilai XAi yang
meminimumkan volume reaktor total.
Volume total minimum ditemukan dengan mengambil turunan volume total dengan mengikuti pada XA1, dan menyusun hasil yang
sma dengan mol. Lalu, ambil hasil penurunannya dengan mengikuti pada XA1 dan susun hasil dengan sama dengan nol. Susunan ulang
persamaan tersebut untuk memberikan kondisi yang memberikan volume minimum. Konstanta kesetimbangan untuk semua reaksi dalam bentuk konsentrasi adalah dengan mengasumsikan gas ideal.
Keuntungan dan Kekurangan dari rangkaian seri
o Keuntungan
- Menghasilkan produk yang sempurna
- Feed ( umpan ) diteruskan secara kontinyu
- Memberikan konversi produk yang lebih tinggi
- Kapasitas produk yang dihasilkan sedikit
- Membutuhkan waktu lama untuk operasi
b. Reaktor Paralel
1. Reaktor aliran plug dalam susunan paralel
Dalam sistem paralel reaktor aliran plug, sebuah aliran bertekanan dibagi dalam beberapa bentuk, masing – masing masukan pada sebuah reaktor aliran plug, seperti yang diilustrasikan pada gambar. Konversi keseluruhan dari sistem reaktor dapat didetermenasikan dengan pembentukan sebuah keseimbangan mol pada titik konvergen aliran cabang. Hal ini dapat ditunjukkan oleh temperatur dan total nilai molar, dimana konversi keseluran tertinggi yang diperoleh adalah sama pada masing – masing reaktor. Pada industri, umumnya reaktor tubulal terdiri dari banyak ( mungkin ratusan ) pipa yang paralel dengan ukuran yang sama, dimana masing – masing reaktor mempunyai kondisi operasi yang sama.
Gambar 13.
Reaktor aliran plug dalam susunan paralel
2. CSTR dalam susunan paralel
Pada gambar menunjukkan CSTR dalm susunan paralel dimana analisis sistem ini mirip pada analisis sistem paralel PFR, yang pada masing – masing reaktor dapat dianalisa secara terpisah. Untuk sebuah sistem paralel CSTR, konversi keseluran tertinggi didapat ketika konversi dimana pada masing-masing reaktor. Dengan kata lain, total nilai aliran dibagi berdasarkan reaktor-reaktor menurut volume yang ada. Sebuah sistem N paralel CSTR pada ruang dan waktu yang sama, akan memberikan konversi keseluran sama sebagai sebuah CSTR
tunggal dengan sebuah volume (Vt) sama untuk sejumlah volume total CSTR dalam susunan paralel.
Gambar 14.
CSTR dalam susunan paralel
Keuntungan dan kerugian dari rangkaian paralel
o Keuntungan
- Menghasilkan produk homogen
- Memperbesar kapasitas produk
- Waktu pengoperasiannya lebih cepat
o Kerugian
- Produk yang dihasilkan belum begitu sempurna
- Menghasilkan konversi produk yang sama
2.2. Pemilihan Reaktor
Dalam proses perancangan untuk pembuatan suatu reaktor kimia maka tujuan pemilihan reaktor adalah :
1. Mendapat keuntungan yang besar 2. Biaya produksi rendah
3. Modal kecil/volume reaktor minimum 4. Operasinya sederhana dan murah 5. Keselamatan kerja terjamin
6. Polusi terhadap sekelilingnya (lingkungan) dijaga sekecil-kecilnya
Pada pemilihan jenis reaktor yang tepat dan pemilihan keadaan operasi, harus mempertimbangkan dengan matang mengenai aspek-aspek berikut:
Pemilihan jenis reaktor dipengaruhi oleh :
1. Fase zat pereaksi dan hasil reaksi
2. Tipe reaksi dan persamaan kecepatan reaksi, serta ada tidaknya reaksi samping
4. Harga alat (reactor) dan biaya instalasinya
5. Kemampuan reactor untuk menyediakan luas permukaan yang cukup untuk perpindahan panas
Pemilihan keadaan operasi dipengaruhi oleh :
1. Harga Panas reaksi (Reaksi Eksotermis dan Endotermis)
2. Persamaan hubungan antara suhu dengan konstanta kecepatan reaksi dan konstanta kesetimbangan
3. Harga tenaga aktivasi dari masing-masing reaksi yang berlangsung
Keadaan Operasi yang dipilih berdasarkan :
1. Dapat menghasilkan produk yang sebanyak-banyaknya
2. Mudah/sedrhana cara kerjanya
3. Hemat energy, misalnya dengan mengoperasikan reaktor secara adiabatic
4. Diinginkan reaktor yang bekerja pada volume minimum, konversi yang optimum atau waktu reaksi yang optimum
2.3. Neraca Massa dan Neraca Panas Reaktor 1. Neraca Massa pada Reaktor
1. Neraca Massa dan Persamaan Karakteristik Reactor Alir Sumbat
Neraca massa pada reaktor alir pipa pada kondisi steady state sebagai berikut : CAo CAf
FAo FA FA+dFA FAf
XAo XA XA+dFA XAf
vo dv vf
L
Gambar 7.1 Skema neraca masa di dalam reaktor alir pipa Neraca masa di dalam segmen volume dV adalah sebagai berikut :
FA = ( -rA ) dV + ( FA + dFA ) (1)
A masuk = A yang hilang A yang keluar
karena reaksi
atau: - dFA = -rA dV (2)
karena - FA = FA0 ( 1 – XA ) maka persamaan (2) bisa ditulis dalam fungsi
XA , menjadi FA0 dXA = -rA dV (3)
atau,
---- = ---- = --- (4) dV FA0 υo CAo
Karena -rA merupakan fungsi dari XA, maka persamaan (4) biasanya ditulis
sebagai berikut :
dV dV dXA
---- = --- = --- (5)
FA0 υo CAo -rA
Besarnya konversi pada bagian keluaran (output) reaktor diperoleh dengan mengintegrasikan persamaan 5 , untuk seluruh volume reaktor V dengan harga batas antara XAo dan XA,
V XA dXA ---- = CAo ∫ --- (6) υo XA0 -rA dimana : V volume reaktor --- = --- = τp = space time
υo laju alir umpan
Kebalikan dari space time adalah space velocity τs = 1/ τp , yaitu
kecepatan alir umpan yang diizinkan per satuan volume reaktor untuk mendapatkan suatu harga konversi tertentu.
Persamaan (6) sekarang dapat dituliskan menjadi, XA dXA
τp = CAo ∫ --- (7)
XA0 -rA
Persamaan (7) disebut sebagai persamaan karakteristik reaktor alir pipa ( plug-flow reactor, PFR) kalau dibuatkan plot antara CAo/-rA sebagai fungsi
dari XA , maka τp merupakan luas bidang di bawah kurva dengan batas dari
CAo ---rA τp XAo XA1 XA
Gambar. Harga τp dinyatakan dalam luas di bawah kurva
2. Volume campuran tetap selama reaksi
Kalau volume campuran tidak berubah selama reaksi berlangsung, maka space time (τp) adalah identik dengan waktu tinggal campuran
tersebut di dalam reaktor. Untuk keadaan yang seperti ini persamaannya dapat ditulis sebagai berikut:
CA CA
τp = ∫ CAo dXA / -rA = ∫ dCA/ -rA ( 8 )
CAo CAo
Harga τp yang diperoleh adalah ekivalen dengan waktu reaksi t di
dalam sistim reaktor batch.
3. Volume campuran berubah selama reaksi
Berubahnya volume campuran karena adanya reaksi kimia akan mengakibatkan berubahnya laju alir campuran di setiap titik sepanjang reaktor. Besarnya perubahan ini akan tergantung pada derajat konversi yang di capai pada titik-titik tersebut. Makin jauh titik yang ditinjau dari titik inputnya, maka makin besar pula derajat konversinya sehingga laju alir volumenya akan makin berbeda dari laju alir volume asalnya.
Hubungan antara laju alir pada suatu konversi ( υ ) terhadap laju alir asal (υo) adalah identik dengan hubungan antara volume campuran ( V )
dengan volume campuran asal ( Vo) untuk reaktor batch yaitu :
υ = υo ( 1 + εA XA ) (9)
VXA =1 – VXA= 0
dimana εA = --- (10)
VXA=0
Adanya perubahan laju alir ini akan secara langsung mempengaruhi banyaknya hasil reaksi yang terjadi. Secara kuantitatif, pengaruh perubahan volume terhadap hasil yang diperoleh da diturunkan berdasarkan persamaan 7.
XA dXA
τp = CAo ∫
XA0 -rA
Karena Vp dan υo mempunyai harga – harga yang sudah tertentu , maka
space time (τp) akan selalu konstan dan tidak dipengaruhi oleh ada atau
tidaknya perubahan volume campuran selam areaksi . Variabel yang dipengaruhi oleh adanya perubahan ini hanyalah – rA yang merupakan fungsi
dari CA.
Misalnya untuk reaksi orde n.
-rA = k CAn (11) FA NA dimana CA = --- (12) ( ingat CA ≠ --- ) υ Vreaktor FA0 ( 1- XA) CA = --- (13) νo ( 1+ εAXA)
Korelasi antara space time ( τp ) dengan XA diperoleh dengan
memasukkan persamaan 11 dengan 7-13 ke dalam persamaan 7, yaitu : XA dXA
τp = CAo ∫ --- (14) 0 n ( 1 – XA )n k CAo ( 1 + εAXA )n Atau, CAo1-n XA ( 1 + εAXA )n τp = --- ∫ --- d XA (15) k 0 ( 1 – XA )n
Harga τp ini sering dipakai di dalam perhitungan perhitungan desain
suatu reaktor alir pipa, walaupun secara fisis besaran ini tidak menunjukkan waktu reaksi di dalam reaktor. Waktun reaksi yang dimaksud biasanya dituangkan dalam besaran waktu yang lain yang disebut waktu tinggal rata-rata campuran di dalam reaktor, dengan definisi sebagai berikut:
V
τ rata-rata = ∫ dV / υ = waktu tinggal rata-rata (16)
0
Hubungan τ rata-rata dengan XA diperoleh berdasarkan neraca massa
komponen A di dalam reaktor :
d V ( -rA ) = FAo dXA (17)
atau,
FAo dXA
dV = --- (18)
( -rA )
Karena υ merupakan fungsi XA menurut persamaan 7-9, maka waktu
tinggal rata-rata campuran di dalam reaktor dapat dinyatakan sebagai berikut : XA FAo dXA τ rata-rata = V/ υ = ∫ --- (19) 0 υo ( 1 + εA XA ) ( -rA ) atau XA dXA τ rata-rata = CAo ∫ --- (20) 0 ( 1 + εA XA ) ( -rA )
1) Reaksi orde nol
XA dXA XA dXA
τ rata-rata = CAo ∫ --- = CAo ∫ --- (21)
0 ( -rA ) 0 k
2) Reaksi orde satu irreversibel
A Produk dengan -rA = k CA NA NA0 ( 1 – XA ) ( 1 – XA ) CA = --- = --- = CA0 --- (22) V Vo ( 1 + εA XA) ( 1 + εAXA ) sehingga : XA dXA XA dXA τ rata-rata = CAo ∫ --- = CAo ∫ --- (23) 0 ( -rA ) 0 k CAo ( 1-XA )/ ( 1 + εAXA ) XA ( 1 + εAXA ) dXA = 1/k ∫ --- 0 ( 1-XA ) k τ = - ( 1 + εAXA ) ln ( 1 – XA ) - εAXA (24)
3) Reaksi orde satu reversible
A r R, dengan M = CR0 / CAo
- rA = k1 CA - k2 CR dan XAe = konversi reaksi pada kesetimbangan
XA dXA τ rata-rata = CAo ∫ --- (25) 0 k1 CA - k2 CR XA dXA τ rata-rata = CAo ∫ 0 k1 ( CA0 - CA0 XA ) - k2 ( CA0 M + CA0 XA )
M + r XAe XA
k 1 τ rata-rata = --- [ - ( 1 + εAXA ) ln ( 1 - --- ) - εAXA ) (26)
M + r XAe
2. Neraca Panas pada Reactor a. Panas Reaksi
Panas reaksi (Notasi ∆H) merupakan ukuran tentang banyaknya panas yang diserap atau dikeluarkan pada saat suatu reaksi berlangsung. Misalnya untuk reaksi berikut ini :
a A + b B r R + s S ∆Hr kkal/mol
Panas reaksi (∆Hr) didefinisikan sebagai panas yang
dibutuhkan/dihasilkan bil a mol zat A bereaksi dengan b mol zat B membentuk r mol zat R dan s mol zat S. Besarnya panas reaksi ini selain, selain tergantung pada temperatur dan tekanan operasinya, juga tergantung pada keadaan sistim itu sendiri, yaitu apakah sistim tempat reaksi berlangsung merupakan sistim terbuka atau tertutup.
1. Sistim terbuka
Gambar 8.1. Tinjauan Sistim Reaktor
Secara termodinamika bisa dibuktikan bahwa panas reaksi untuk sistim terbuka adalah sama dengan perbedaan entalpi produk total dengan entalpi reaktan total, atau :
∆Hr = ∑ ni hi (1)
di mana : hi adalah entalpi molar komponen i
Kalau entalpi produk total lebih besar dari pada entalpi reaktan total, maka ∆Hr akan berharga positif. Ini berarti bahwa sejumlah panas harus
ditambahkan agar reaksi dapat berlangsung. Reaksi yang semacam ini disebut reaksi endotermik. Untuk keadaan sebaliknya, yaitu ∆Hr < 0 , berarti bahwa
sejumlah panas akan dibebaskan pada saat reaksi berlangsung dan reaksi ini disebut reaksi eksotermik. Harga panas reaksi pada suhu standar untuk reaksi-reaksi tertentu biasanya telah tersedia di dalam tabel-tabel termodinamika. Bila seandainya untuk reaksi-reaksi tertentu data panas reaksinya tidak bisa diperoleh secara langsung, maka bisa saja ditempuh cara lain, yaitu dengan menghitungnya berdasarkan :
1. Data entalpi pembentukan standar (∆Hfo) atau
2. Data entalpi pembakaran (∆Hco).
2. Sistim Tertutup
Sistim tertutup dapat dibagi dalam 2 (dua) katagori, yaitu :
- Sistim tertutup pada tekanan konstan
Untuk sistim seperti ini, panas reaksi dihitung tepat sama dengan apa yang telah diturunkan untuk sistim terbuka, yaitu panas reaksi adalah sama dengan perbedaan entalpi produk dan reaktan.
- Sisitim tertutup pada volume konstan
Menurut hukum termodinamika panas reaksi untuk sistim tertutup pada volume konstan, adalah sama dengan perbedaan energi dalam (internal energi)antara produk dan reaktan, atau dituliskan :
∆Ur = ∑ ni Ui (2)
di mana : Ui adalah energi dalam molar senyawa i.
b. Estimasi Efek Panas
Penentuan panas reaksi biasanya dilakukan di dalam suatu alat yang disebut “Bomb calometri”. Alat ini berupa suatu sistim reaktor tertutup dengan volume konstan, sehingga panas reaksi yang kita dapatkan adalah sama dengan perubahan enrgi dalamnya.
Untuk merubah panas reaksi pada volume konstan menjadi panas reaksi pada tekanan konstan seperti dinyatakan dalam banyak literatur, dipakai korelasi sebagai berikut :
Perubahan entalpi pada temperatur dan tekanan konstan adalah :
∆HP,T = ∆UP,T + p(∆V)T (4)
di mana :
∆UP,T adalah perubahan energi dalam pada temperatur dan tekanan
konstan Untuk gas-gas yang mendekati hukum gas ideal dan perubahan tekanan di dalam alat bomb calorimeter tidak terlalu besar, nilai ∆UP,T
kira-kira sama dengan perubahan energi dalam pada temperatur dan volume konstan, atau dituliskan :
∆UP,T = ∆UV,T (5)
Sehingga persamaan (4) menjadi :
∆HP,T = ∆UV,T + p(∆V)T (6)
Apabila selama reaksi jumlah mol total adalah tetap (atau kalau di dalam sistim terjadi proses pengembunan, sehingga jumlah mol di dalam fasa adalah tetap), maka :
∆HP,T = ∆UV,T (7)
Apabila campuran reaksi di dalam reaktor dianggap mengikuti hukum gas ideal, maka :
p(∆V)T = ∆n RT (8)
Sehingga persamaan (8.6), dapat dituliskan menjadi :
∆HP,T = ∆UV,T + ∆n RT (9)
Pada perhitungan-perhitungan praktis harga p(∆V)T ini biasanya relatif
kecil dibandingkan dengan ∆UV,T , sehingga kalau diambil saja : ∆HP,T =
∆UV,T , kesalahan yang dibuat bisa diabaikan.
c. Pengaruh Temperatur Terhadap Panas Reaksi
Panas reaksi pada temperatur T2 (keadaan akhir) dapat ditentukan
berdasarkan data panas reaksi pada temperatur T1 (keadaan awal) yang
diketahui menurut korelasi sebagai berikut :
2 1 1 2 T T o r o r H CpdT H (10) di mana : Cp = Σ n i Cpio r o
r H
H 2 , 1
= panas reaksi molar pada temperatur T
1 dan T2
Karena panas jenis Cp dari masing-masing komponen biasanya dinyatakan dalam bentuk fungsi temperatur yaitu :
Cp = α + β T + γ T2
maka : ∫ CpdT dapat dituliskan menjadi :
∫ CpdT =
2 1 ) ( 2 T T T T dT di mana : ∆α = Σ ni α ∆β = Σ ni β ∆γ = Σ ni γSehingga persamaan (8.10) menjadi :
) ( 3 ) ( 2 ) ( 3 1 3 2 2 1 2 2 1 2 1 2 H T T T T T T H o r o r (11) Apabila panas jenis tiap komponen dalam campuran reaksi adalah konstan antara T1 dan T2, maka perbedaan panas jenis antara produk dan reaktan juga
konstan, sehingga panas reaksi pada temperatur T2 bisa dituliskan sebagai berikut : ) ( 2 1 1 2 H Cp T T HT T (12)
d. Neraca Energi untuk Reaktor Batch
Hal yang pertama diperhatikan untuk menurunkan persamaan neraca energi di dalam reaktor batch adalah diketahui dahulu apakah sistim operasi pada volume konstan atau pada tekanan konstan. Untuk keadaan yang pertama (volume konstan) setiap perubahan energi yang dialami sistim adalah ekivalen dengan perubahan energi dalamnya. Sedangkan untuk sistim yang kedua (tekanan tetap) setiap perubahan energi yang dialami sistim adalah ekivalen dengan perubahan entalpi.
Dengan demikian neraca energi untuk reaksi : a A + b B r R + s S dapat dituliskan sebagai berikut :
masuk reaksi terakumulasi Untuk sistim dengan volume tetap :
dt dT Cv M U V r Q( A) R( r) T (14) Untuk sistim dengan tekanan tetap :
dt dT Cp M H V r Q( A) R( r) T (15) di mana : VR = volume reaktor
MR = massa total campuran di dalam reaktor
Cv = panas jenis campuran pada volume tetap, kal/g. oC
Cp = panas jenis campuran pada tekanan tetap, kal/g.oC
∆Ur= panas reaksi per mol A (pada volume tetap)
a U bU aU sU rU a U r B A S R r 1( )
∆Hr = panas reaksi per mol A (pada tekanan tetap)
a H bH aH sH rH a H r B A S R r 1( )
Kedua prinsip diatas harus betul-betuk dipahami, walaupun di dalam perhitungan-perhitungan praktis seringkali hanya dipakai model persamaan (15), baik untuk sistim dengan volume tetap maupun sistim dengan tekanan tetap (konstan). Kesalahan yang terjadi relatif kecil sekali dan dapat diabaikan).
Reaktor Batch dengan Operasi Adiabatik
Dalam operasi adiabatik tidak ada sama sekali panas yang masuk maupun yang keluar dari sistim, atau :
Q = 0
Sehingga neraca energinya menjadi :
dt dT Cp M H V rA) R( r) T ( (16) dari definisi kecepatan reaksi, yaitu :
dt dX V N dt dN V r A R Ao A R A ) 1 ( (17) atau : ) tetap V untuk ( ) ( R dt dX C r A Ao A (18) substitusi ke persamaan (8.16) menjadi :
dt dT Cp M H V dt dX C A R r T Ao ( ) dt dT Cp V M H dX C R T r A Ao ( ) ) campuran densiti ( ) ( Ao A r mix mix dt dT Cp H dX C dt H Cp dX C T To r mix X A Ao A
0 (19) Apabila pada interval temperatur di mana operasi berlangsung harga ∆Hr dan Cp dapat dianggap konstan, maka persamaan (8.19) bisaditulisskan : A mix Ao r o X Cp C H T T (20) di mana :
To = temperatur pada awal reaksi (XA = 0)
T = temperatur campuran pada saat konversi reaksi XA.
Persamaan (8.20) menunjukkan perubahan temperatur selama reaksi berlangsung dan perubahan ini akan secara langsung mempengaruhi besarnya harga konstanta kecepatan reaksi (k).
Kalau pengaruh temperatur terhadap k mengikuti Arhenius, yaitu :
RT E o
e
ak
k
/maka dengan mengganti T pada persamaan di atas dengan T pada persamaan (8.20) akan diperoleh k sebagai fungsi derajat konversi reaksi XA, yaitu :
) ( / A mix Ao r o a X Cp C H T R E o
e
k
k
Persamaan neraca massa di dalam reaktor :
) ( A A k f X r ) ( ) ( / A X Cp C H T R E o A Ao k e f X dt dX C mix A Ao r o a (21) sedangkan waktu yang diperlukan untuk mendapatkan konversi XA
adalah :
A A mix Ao r o a X A X Cp C H T R E A o Ao X f e dX k C t 0 / ( ) ) ( (22) Persamaan di atas sangat sulit diselesaikan secara analitis, sehingga seringkali penyelesaiannya dilakukan secara integrasi grafis yaitu dengan membuat plot antara :A A X Cp C H T R E X X f e mix A Ao r o a vs ) ( 1 ) ( /
dengan menentukan luas bidang antara kurva tersebut dengan sumbu XA.
Reaktor Batch dengan Operasi Isotermal
Temperatur adalah konstan selama berlangsung, yang berarti bahwa semua panas yang dihasilkan/diserap adalah sama dengan panas yang dipindahkan melalui dinding media pemindah panas, sehingga tidak ada akumulasi panas di dalam sistim.
Persamaan neraca energi untuk sistim operasi semacam ini adalah :
Panas yang dihasilkan = Panas yang
reaksi dipindahkan
(rA)V(Hr) Q
= - UA (Tk – T) ...(23)
di mana :
T = temperatur reaksi
U = over all heat tranfer coefficient A = luas bidang penukar panas
Tk - T = perbedaan temperatur antara campuran reaksi dengan
media penukar panas
Jika sebagai medium penukar panas dipakai suatu fluida yang mengalir di dalam pipa (heat exchanger), dengan temperatur masuk dan keluar masing-masing adalah Tk1 dan Tk2, maka perbedaan temperatur rata-rata
antara medium pemindah panas dan campuran reaksi adalah :
) ( ) ( ln ) ( ) ( ) ( 1 2 1 2 T T T T T T T T T T k k k k rata rata k (24) Sehingga persamaan (8.23) dapat ditulis manjadi :
rata rata k r A V H UA T T r ) ( ) (( ) ( (25)
Waktu yang diperlukan untuk mencapai derajat konversi XA, adalah sama
seperti apa persamaan yang telah diturunkan sebelumnya untuk reaktor batch adalah :
XA A A Ao r dX C t 0 (26) Banyaknya panas yang dihasilkan atau diserap (Q) selama reaksi dapat dihitung berdasarkan jumlah A yang bereaksi (CAo XA V), atau :) )( (CAoXAV Hr
Q (27)
2.4. Contoh perhitungan Desain Reaktor
Rancangan CSTR untuk memproduksi 200 juta pon per tahun etilen glikol. Diinginkan untuk menghasilkan 200 juta pon per tahun etilen glikol. Reaktor itu dioperasikan pada kondisi isotermal. Konsentrasi etilen oksida yang diumpankan adalah 1 mol/ft3 , dan juga air diumpankan ke reaktor bersama
dengan 0,9 % berat katalis H2SO4. Jika konversi 80% akan dicapai, maka
desain lah reaktor tersebut. Diketahui persamaan reaksi sebagai berikut dengan k=0,311min-1.
Untuk kapasitas tangki >500 galon, maka safety factor yang digunakan adalah 10% [Bassel,1990].
maka volume reaktor, V = 1,1 x 5,6 m3
= 6,16 m3
Volum reaktor = volum silinder + (2 x volum tutup) Diasumsikan perbandingan Hs/Dt = 1,5
Volum silinder = �/4 x Dt x Hs
Volum silinder = �/4 x Dt x 1,5 Dt
Volum tutup toripherical = 0,0847 Dt3 (Brownell dan Young, 1959)
Volum reaktor = (�/4 x Dt x 1,5Dt) + (2 x 0,0847 Dt3)
6,16 m3 = 1,3469 D3
Diperoleh :
Dt = 1,104 m = 43,478 inch
Hs = 1,656 m = 65,2 inch
Tebal dinding silinder (shell, ts) dan tutup reaktor (head, th)
Bahan konstruksi reaktor : Loy Alloy SA-204 Grade C
Tegangan yang diizinkan : 18750 psi
Efisiensi sambungan : 0,8 (double welded butt-joint)
OD = ID + (2 x ts)
= 43,478 in + (2 x 0,1875 in)
Tinggi tutup, OA
Tinggi tutup reaktor dihitung dengan menggunakan rumus dari Brownell dan Young (1959). a = ID/2 = 47,625/2 = 23,8 in AB = a – icr = (23,8 – 3) in = 20,8125 in BC = r – icr = (48 – 3)in = 45 in AC = = 39,89 in b = r – AC = 48 in – 39,89 in = 8,1 in
Dari tabel 5.6 Brownell untuk th 0,1875 in, maka sf = 2 in
OA = th + b + sf
= 0,1875 in + 8,1 in + 2 in = 10,3 in
Tinggi total reaktor, Ht = Hs + (2 x OA)
= 71,4375 in + (2 x 10,3) in = 92,0167 in = 7,668 ft
Perancangan Pengaduk (impeller)
Perhitungan Pengaduk direncanakan menggunakan pengaduk tipe vertical blade turbine, serta tangki dilengkapi 4 baffle. bahn konstruksi Low Alloy SA 204 Grade C. konfigurasi design pengaduk ditentukan dari hubungan berikut:
dengan :
D = diameter tangki D = diameter impeller W = lebar impeller L = panjang impeller
E = jarak impeller dar dasar tangki J = lebar baffle
Perancangan Nozzle
Diameter nozzle pemasukan Laju alir volumetrik, q Faktor safety 10 %
q = 1,1 x 15,34 ft3/min= 0,28 ft3/det
asumsi aliran turbulen, maka diamter pipa optimum adalah Di opt = 3,9 . q0,45 . ρ0,13 (Pers. 15 Peter Timmerhaus)
Di opt = 3,9 . ( 0,28)0,45 . (67,808)0,13
Dari Q.Kern Tabel 11, dimensi pipa yang digunakan adalah : Nomonal Pipe Size : 4 in
ID : 4,026 in OD : 4,5 in
Dengan cara yang sama maka diperoleh diameter nozzle keluaran reaktor
Manhole
Manhole pada reaktor berguna untuk memudahkan pembersihan dan perbaikan alat. Manhole yang digunakan adalah ukuran standar dengan spesifikasi sebagai berikut (Brownell dan Young, 1959) :