IDENTIFIKASI DAN UJI PENDAHULUAN AKTIVITAS ANTIKANKER SENYAWA
NON FENOLIK DARI EKSTRAK DIKLOROMETANA BATANG TUMBUHAN
ASHITABA (Angelica keiskei)
IDENTIFICATION AND PRELIMINARY TESTING ANTICANCER ACTIVITY FROM
THE STEMS ASHITABA (Angelica keiskei) OF DICLOROMETHANE EXTRACT
Ririn Sri Hartini, Suyatno
Jurusan Kimia FMIPA Universitas Negeri Surabaya Jl. Ketintang Surabaya (60231), Telp. 031-8298761
Email :ririn_sh@yahoo.com
Abstrak.Tujuan penelitian ini adalah untuk mengetahui struktur molekul senyawa non fenolik dari
ekstrak diklorometana batang tumbuhan ashitaba (Angelica keiskei) dan uji pendahuluan aktivitas
antikankernya.Dalam penelitian ini, ekstraksi dilakukan dengan metode maserasi, pemisahan dilakukan
dengan metode kromatografi cair vakum (KCV) yang dimonitoring dengan kromatografi lapis tipis
(KLT), dan pemurnian dilakukan dengan metode rekristalisasi.Uji kualitatif dilakukan dengan pereaksi
Liebermann-Burchard dan struktur molekul senyawa hasil isolasi ditentukan dengan metode spektroskopi
(UV-Vis, IR, dan MS).Uji pendahuluan aktivitas antikanker dilakukan dengan metode BSLT. Dari hasil
penelitian diperoleh isolat berupa serbuk tak berwarna dengan titik leleh 70,23 ºC. Hasil uji kualitatif
senyawa hasil isolasi dengan pereaksi Liebermann-Burchard menunjukkan warna biru yang
mengindikasikan bahwa isolat merupakan senyawa steroid.Berdasarkan data spektroskopi, isolat
mengandung campuran dua senyawa steroid yaitu stigmasterol dan β-sitosterol.Berdasarkan hasil uji
BSLT, senyawa steroid hasil isolasi menunjukkan toksisitas berkategori sangat toksik terhadap Artemia
salina dengan nilai LC
50sebesar 119,048
µg/mL.Dengan demikian isolat berpotensi untuk dikembangkan
sebagai bahan antikanker.
Kata-kata kunci:
A
shitaba (Angelica keiskei), ekstrak diklorometana, steroid, uji BSLT.
Abstract.The aims of research is to determine the molecular structure of non phenolic compounds from
the stems ashitaba (Angelica keiskei) of dichloromethane extract and preliminary testing anticancer
activity. In this research, the extraction was carried by maceration method, separation by Vacuum Liquid
Chromatography (VLC) monitored using Thin Layer Chromatography (TLC), and purified by
recrystallization method. The qualitative test was carried by Liebermann-Burchard reagent and the
molecular structure of the isolate was determined by spectroscopic methods (UV-Vis, IR and MS).
Preliminary test of anticancer activity was performed by the BSLT. Based on the research, it was
obtained aisolates as colorless powderwith a melting point of 70.23 °C. The qualitative test to isolate
showed a blue color indicating that it was a steroid compound. Based on spectroscopic data, isolate was
contained a mixture of two steroid compounds, namely stigmasterol and β-sitosterol. The BSLT test
showed that it had toxicity of highly toxic category to Artemia salina with LC
50of 119,048
mg / mL. Thus
isolate had potency to be developed as an anticancer agent.
PENDAHULUAN
Kesehatan adalah hal yang penting bagi
semua manusia karena jika kesehatan terganggu,
maka setiap aktivitas manusia juga akan
terganggu.
Terganggunya
kesehatan
dapat
disebabkan karena tubuh seseorang terserang
penyakit.Salah satu penyakit yang hingga saat
ini menjadi masalah kesehatan di seluruh dunia,
termasuk juga di Indonesia adalah kanker.
Kanker
merupakan
penyakit
yang
disebabkan oleh sel tunggal yang tumbuh secara
tidak terkendali sehingga dapat merusak sel atau
jaringan normal[1]. Pengobatan kanker dapat
dilakukan secara tradisional maupun medis.
Pengobatan secara medis dapat dilakukan
dengan
beberapa
cara,
seperti
seperti
imunoterapi, kemotrapi, dan radioterapi. Tetapi
pengobatan tersebut dapat menimbulkan efek
negatif bagi tubuh karena pengobatan tersebut
tidak
bersifat
selektif
dan
juga
dapat
menyebabkan
rusaknya
jaringan
normal.
Pengobatan secara tradisional diharapkan dapat
bersifat selektif yang dilakukan dengan
obat-obatan herbal yang berasal dari tumbuhan yang
memiliki khasiat sebagai obat.
Indonesia memiliki kekayaan alam berupa
tumbuhan obat yang dapat dimanfaatkan sebagai
sumber obat tradisional.Obat tradisional sangat
penting bagi masyarakat karena lebih mudah
diperoleh dan relatif lebih murah karena dapat
diperoleh tanpa resep dokter [2].Salah satu
tumbuhan yang banyak dimanfaatkan oleh
masyarakat, baik sebagai bahan makanan
maupun obat-obatan adalah tumbuhan ashitaba
(
Angelica keiskei).
Masyarakat Indonesia belum banyak yang
mengetahui
tanaman
ashitaba,
namun
masyarakat Jepang sudah mengenal baik
tumbuhan
tersebut.Ashitaba
biasanya
ditambahkan pada makanan yang disajikan
sehari-hari.Di Indonesia, tumbuhan ini dapat
tumbuh subur hanya di beberapa tempat, salah
satunya di Desa Ketapanrame, Kec. Trawas,
Kab. Mojokerto.
Dari tumbuhan
Angelica keiskei
sudah
dilakukan isolasi maupun pengujian aktivitas
biologisnya.Ekstrak etil asetat batang tumbuhan
ashitaba (
Angelica keiskei
) berpotensi sebagai
antitumor [3].Penelitian uji aktivitas antidiabetes
dari ekstrak etanol akar ashitaba (
Angelica
keiskei
) berhasil diisolasi dua senyawa kalkon,
yaitu 4-hydroxyderricin dan xanthoangelol.
Isolat
tersebut
menunjukkan
kemampuan
mencegah kadar gula pada hewan uji [4].
Beberapa tanaman famili
Angelica
telah
berhasil diuji aktivitas antikankernya.Ekstrak
etanol tumbuhan
Angelica gigas
Nakai (AGN)
dapat menghambat pertumbuhan sel kanker
prostat PC-3 and DU145 yang diberikan pada
mencit [5].
Mengingat bahwa struktur molekul dari
senyawa non-fenolik batang ashitaba (
Angelica
keiskei
) dan aktivitas antikankernya belum
pernah dilaporkan, maka peneliti tertarik untuk
melakukan penelitian tentang uji pendahuluan
aktivitas antikanker senyawa non fenolik dari
ekstrak diklorometana batang tumbuhan ashitaba
(
Angelica keiskei
).Dalam penelitian ini uji
pendahuluan aktivitas antikanker ditentukan
berdasarkan
toksisitas
senyawa
terhadap
Artemia salina
.
BAHAN DAN METODE
Alat
Beberapa alat yang digunakan antara lain :
seperangkat alat ekstraksi dengan metode
maserasi, seperangkat alat penyaring Buchner,
rotary vacuum evaporator
(Heidolp laborata
4001), seperangkat alat kromatografi cair
vakum,
differential scanning calorimetry
(DSC),
spektrofotometer UV (Shimadzu Pharma Spec.
UV-1700), spektrofotometer IR (Perkin Elmer
USA
89485),
spektrofotometer
massa
digunakan dalam laboratorium organik bahan
alam.
Bahan
Bahan-bahan yang di butuhkan adalah
n
-heksana teknis, diklorometana teknis, etil asetat
teknis, kloroform p.a, asam sulfat pekat p.a,
metanol p.a, asam asetat anhidrida p.a, kiesegel
60 GF-254, pelat KLT silika gel F-254 (20 x 20;
0,25 mm), dan larva udang
Artemia salina
L.
Prosedur Penelitian
Tahap Pengumpulan dan Penyiapan Sampel
Tumbuhan
Sampel berupa batang tumbuhan ashitaba
yang
diperoleh
dari
Desa
Ketapanrame,
Kecamatan Trawas, Kabupaten Mojokerto
dibersihkan, dipotong hingga ukurannya kecil,
kemudian dikeringkan dengan cara
diangin-anginkan, dan selanjutnya digiling hingga
menjadi
serbuk
halus
yang siap
untuk
diekstraksi.
Ekstraksi dan Isolasi
Sampel berupa serbuk halus batang
tumbuhan ashitaba sebanyak 2 kg diekstraksi
dengan cara maserasi menggunakan pelarut
n
-heksana. Maserasi dilakukan selama 3 x 24 jam
dengan volume
n
-heksana 1 liter untuk setiap
maserasi.
Selanjutnya
dilakukan
maserasi
menggunakan pelarut diklorometana selama 3 x
24 jam dengan volume diklorometana 1 liter
untuk
setiap
maserasi.
Hasil
maserasi
diklorometana disaring dengan corong Buchner,
sehingga diperoleh ekstrak diklorometana dan
residu.Ekstrak diklorometana diuapkan dengan
rotary evaporator
dan didapatkan ekstrak pekat
dan pelarut diklorometana.
Kromatografi
cair
vakum
(KCV)
selanjutnya
digunakan
untuk
memisahkan
konponen-komponen yang ada dalam ekstrak
pekat yang telah didapatkan. Fasa diam yang
digunakan dalam metode ini adalah silika gel
GF-254 dan eluen yang digunakan adalah
n
-heksana, campuran
n
-heksana-etilasetat, dan etil
asetat.
Kromatografi
lapis
tipis
(KLT)
selanjutnya digunakan untuk memonitor hasil
pemisahan dengan menggunakan perbandingan
eluen
n
-heksana:etil asetat = 4:1. Fraksi-fraksi
yang nilai Rf-nya sama dan pada plat KLT
sudah menunjukkan satu noda kemudian
digabung. Selanjutnya dilakukan rekristalisasi
untuk pemurnian isolat yang telah didapat
menggunakan
pelarut
yang
sesuai.
Uji
kemurnian isolat dilakukan dengan penentuan
titik leleh menggunakan
Differential Scanning
Calorimetry
(DSC) dan KLT tiga sistem eluen.
Uji Pendahuluan Antikanker Senyawa Hasil
Isolasi
Sebanyak 5 mg isolat ditambah dengan 1 mL
kloroform dengan diaduk hingga isolat larut
seluruhnya.Larutan tersebut disebut larutan
induk
berkonsentrasi 5000 µg/mL.Larutan
tersebut masing-masing diambil sebanyak 10,
25, 50, 75, dan 100 µL dan dimasukkan dalam
vial yang berbeda.Masing-masing vial dibiarkan
hingga
pelarutnya
menguap,
kemudian
ditambahkan DMSO sambil diaduk hingga isolat
larut dan dimasukkan 10 ekor larva udang, diisi
sampai volumenya 5 mL dengan air laut dan
dibiarkan selama 24 jam. Jumlah larva udang
yang mati dihitung setelah 24 jam.Dilakukan
analisis probit pada hasil yang diperoleh
menggunakan program SPSS untuk menentukan
besarnya LC
50senyawa hasil isolasi[6].
HASIL DAN PEMBAHASAN
Hasil Ekstraksi dan Isolasi Senyawa Non
Fenolik dari Batang Tumbuhan Ahitaba
(Angelica keiskei)
Sebanyak 2 kg serbuk halus batang
tumbuhan ashitaba (
Angelica keiskei)
diekstraksi
dengan cara maserasi berurutan menggunakan
pelarut
n
-heksana teknis dan diklorometana
teknis.Penyaringan dilakukan pada ekstrak yang
diperoleh menggunakan penyaring Buchner
sehingga didapatkan ekstrak diklorometana dan
residu.
Ekstrak
diklorometana
selanjutnya
diuapkan
menggunakan
rotary
vacuum
evaporator
hingga didapatkan ekstrak pekat
diklorometana
berwarna
hijau
kehitaman
sebanyak 55,225 gram.
Dilakukan kromatografi cair vakum (KCV)
untuk memisahkan komponen-komponen yang
ada
dalam
ekstrak
pekat
diklorometana
menghasilkan 127 fraksi. Jenis eluen yang
digunakan
pada
saat
KCV
ditingkatkan
kepolarannya mulai dari eluen yang kurang
polar yaitu
n
-heksana sampai ke eluen yang
lebih polar yaitu etil asetat. Kromatografi lapis
tipis (KLT) dilakukan untuk memonitor hasil
pemisahan dari KCV fraksi 1-127 dengan eluen
n
-heksana – etil asetat = 4 : 1. Fraksi-fraksi yang
memiliki nilai Rf sama yaitu fraksi 50-63
digabung dan diuapkan hingga diperoleh berat
sebanyak 0,754 gram. Selanjutnya dilakukan
rekristalisas dengan pelarut metanol
dan
didapatkan 0,127 gram serbuk tak berwarna. Uji
kemurnian dilakukan pada serbuk tersebut
dengan pengukuran titik leleh dan KLT tiga
sistem eluen. Uji titik leleh isolat menggunakan
Differential Scanning Calorimetry
(DSC) dan
didapatkan hasil sebesar 70,23 ºC. Pada uji KLT
tiga sistem eluen, isolat diuji sebanyak 3 kali
dengan eluen yang berbeda. Perbandingan eluen
yang digunakan, yaitu
n
-heksana:etil asetat = 4:1
,
n
-heksana:etil
asetat
=
9:1,
n-heksana:kloroform = 1:1. Hasil uji KLT
menunjukkan satu noda dengan masing-masing
nilai Rf 0,65 ; 0,25 ; dan 0,325. Hasil uji
kualitatif menggunakan pereaksi
Liebermann-Burchard menghasilkan warna biru yang
mengindikasi bahwa senyawa hasil isolasi
adalah senyawa steroid.
Penentuan Struktur Molekul Senyawa Hasil
Isolasi
Hasil pengukuran spektrum ultraviolet-sinar
tampak (UV-Vis) senyawa hasil isolasi dalam
pelarut
n
-heksana terlihat bahwa senyawa hasil
isolasi menunjukkan puncak serapan maksimum
pada panjang gelombang 196,2 nm. Dengan
demikian senyawa hasil isolasi menunjukkan
adanya transisi elektron π→π*
. Hal ini
disebabkan oleh adanya ikatan rangkap C=C
yang
tidak
terkonjugasi
karena
panjang
gelombang serapan maksimumnya berada di
bawah 215 nm.
Berdasarkan data spektrum IR senyawa
hasil isolasi menunjukkan adanya tekuk C-H
alkil (1463,82 dan 1381,95 cm
-1) dan regang
C-H alkil (2918,17 cm
-1). Hal ini mendukung
bahwa dalam isolat terkandung kerangka
senyawa steroid. Regang C-O (1169,09 dan
1049,80 cm
-1) dan vibrasi regang O-H (3435,18
cm
-1) yang mendukung adanya senyawa steroid
pada isolat yang diperoleh karena memiliki
gugus hidroksil.
Selanjutnya dilakukan pengujian GC-MS
untuk
menentukan
struktur
dan
juga
massamolekul senyawa hasil isolasi. Hasil
analisis GC-MS menunjukkan bahwa terdapat
campuran 2 senyawa pada isolat yang
masing-masing memiliki massa molekul relatif 412 (1)
dan 414 (2) dengan persen luas area
masing-masing 66,61 dan 33,39 %. Senyawa 1
memberikan ion-ion fragmen pada m/z 394, 379,
369, 351, 327, 314, 300, 285, 271, 255, 241,
229, 213, 199, 185, 173, 159, 145, 133, 123,
105, 97, 83, 69, 55, dan 41.Senyawa 2
memberikan ion-ion fragmen pada m/z 396, 381,
354, 329, 303, 283, 273, 255, 241, 231, 213,
199, 187, 173, 159, 145, 133, 119, 107, 95, 81,
57, 43, dan 41.
Berdasarkan hasil analisis data uji kualitatif
dan spektroskopi (UV, IR, dan MS) dapat
disimpulkan bahwa senyawa non fenolik hasil
isolasi merupakan campuran senyawa steroid
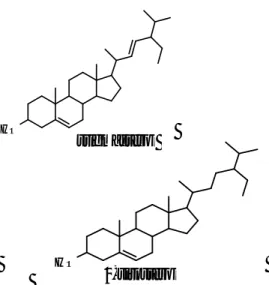
yaitu stigmasterol
dan
β
-sitosterol.Adanya
kandungan senyawa tersebut membuktikan
bahwa dalam batang tumbuhan ashitaba terdapat
senyawa golongan non fenolik.Struktur molekul
senyawa tersebut ditunjukkan pada Gambar 1.
HO
HO