i
PENGARUH FRAKSI KLOROFIL
SPIRULINA SP
TERHADAP SIFAT LISTRIK DENGAN STRUKTUR
DYE SENSITIZED SOLAR CELL
(DSSC)
Disusun Oleh :
FITRIA HASTAMI
M0207004
SKRIPSI
Untuk memenuhi sebagian
persyaratan mendapatkan gelar Sarjana Sains
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
UNIVERSITAS SEBELAS MARET
JANUARI, 2012
ii
HALAMAN PENGESAHAN
Skripsi dengan judul :
Pengaruh Fraksi KlorofilSpirulina spterhadap Sifat Listrik dengan StrukturDye Sensitized Solar Cell(DSSC)
Yang ditulis oleh :
Nama : Fitria Hastami
NIM : M0207004
Telah diuji dan dinyatakan lulus oleh dewan penguji pada :
Hari : Selasa
Tanggal : 3 Januari 2012
Dewan Penguji
1. Dr. Yofentina Iriani, S.Si., M.Si ………. NIP.19711227 199702 2 001
2. Sorja Koesuma, S.Si., M.Si ……….
NIP.19720801 200003 1 001
3. Dr. Agus Supriyanto, S.Si., M.Si ………. NIP.19690826 199903 1 001
4. Dr. Eng. Risa Suryana, S.Si., M.Si ………. NIP.19710831 200003 1 005
Disahkan Oleh :
Ketua Jurusan Fisika
Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sebelas Maret Surakarta
Ketua Jurusan Fisika
Ahmad Marzuki, S.Si.,Ph.D NIP.19610223 198601 10001
iii
PERNYATAAN
Dengan ini saya menyatakan bahwa isi intelektual dari skripsi saya yang berjudul “Pengaruh Fraksi Klorofil Spirulina sp terhadap Sifat Listrik dengan Struktur Dye Sensitized Solar Cell (DSSC)” adalah hasil kerja keras dan sepengetahuan saya. Dalam skripsi ini tidak berisi tentang materi yang telah dipublikasikan atau ditulis oleh orang lain serta materi yang telah diajukan untuk mendapatkan gelar kesarjanaan di Universitas Sebelas Maret Surakarta ataupun di Perguruan Tinggi lainnya kecuali telah dituliskan dalam daftar pustaka skripsi ini dan segala bentuk bantuan dari semua pihak telah ditulis.
Surakarta, 3 Januari 2012
Penulis
Fitria Hastami
iv ABSTRAK
PENGARUH FRAKSI KLOROFILSPIRULINA SP TERHADAP SIFAT
LISTRIK DENGAN STRUKTURDYE SENSITIZED SOLAR CELL(DSSC)
Fitria Hastami
Jurusan Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sebelas Maret
Telah dilakukan penelitian mengenai pengaruh fraksi klorofilSpirulina sp terhadap sifat listrik dengan struktur Dye Sensitized Solar Cell (DSSC). DSSC merupakan sel surya fotoelektrokimia yang menggunakan energi cahaya untuk reaksi kimia yang menghasilkan energi listrik. Susunan DSSC terdiri dari substrat kaca FTO (Flourine doped Tin Oxide) yang dilapisi titanium dioksida, dye, larutan Iodine, dan kaca FTO yang dilapisi karbon dari grafit pensil kayu. Dye
Sensitizer yang digunakan adalah klorofil alami yang berasal dari ekstrak
Spirulina sp. Optimasidye dalam DSSC menggunakan fraksi yang diperoleh dari
hasil kromatografi yang digunakan yaitu Sp1, Sp2, dan Sp3. Pengukuran sifat listrik dengan karakterisasiI-V denganKeithley 2602A. Nilai Responsivitas untuk DSSC dengan dye Sp1 sebesar 1,83x10-8 (A/[Watt/m2]), DSSC dengan dye Sp2 1,66x10-8 (A/[Watt/m2]), dan DSSC dengan dye Sp3 0,54x10-8 (A/[Watt/m2]). Hasilnya menunjukan bahwa fraksi klorofil Spirulina sp memiliki pengaruh terhadap sifat listrik dengan struktur DSSC.
Kata kunci : DSSC, fraksi klorofil, sifat listrik
v ABSTRACT
THE INFLUENCE OF CHLOROPHYLL FRACTIONS OF SPIRULINA SP ON DYE SENSITIZED SOLAR CELL (DSSC) STRUCTURED
ELECTRICAL PROPERTIES
Fitria Hastami
Departement of Physics. Faculty of Science Sebelas Maret University
The influence of chlorophyll fractions Spirulina sp on Dye Sensitized Solar Cell (DSSC) structured electrical properties have been investigated. DSSC is the type of photoelectrochemistry solar cell which used solar energy to perform chemistry reaction to produce electric energy. The structure of DSSC consist of FTO (Flourine doped Tin Oxide) as a glass substrat with titanium dioxide film, dye, electrolyte Iˉ, and FTO glass with carbon catalyst. Dye which used as dye sensitizer is natural dye from extract of Spirulina sp. Chlorophyll fraction from chromatografi separation which used is Sp1, Sp2, and Sp3. Measurement of electrical properties with I-V characterization with Keithley 2602A. And responsivity value for DSSC with dye Sp1is 1,83x10-8(A/[Watt/m2]), DSSC with dye Sp2 is 1,66x10-8 (A/[Watt/m2]), and DSSC with dye Sp3 is 0,54x10-8 (A/[Watt/m2]). The result showed that the fraction of chlorophyll Spirulina sp has an influence on the electrical properties with DSSC structured .
Key words : DSSC, Chlrophyll fraction, electrical properties
vi
MOTTO DAN PERSEMBAHAN
Allah, tidak ada Tuhan melainkan Dia Yang Hidup kekal lagi terus menerus mengurus
(Makhluk-Nya); tidak mengantuk dan tidak tidur . Kepunyaan-Nya apa yang dilangit dan di
bumi, Siapakah yang dapat memberi syafa’at di sisi Allah tanpa izin-Nya?Allah mengetahui
apa apa yang dihadapan mereka dan di belakang mereka, dan mereka tidak mengetahui apa
apa dari ilmu Allah melainkan apa yang di kehendaki-Nya. Kekuasaan Allah meliputi langit
dan bumi. Dan Allah tidak merasa berat memlihara keduanya, dan Allah Maha Tinggi Lagi
Maha Besar
( QS AL-Baqarah 255)
Don’t be afraid of missing opportunities. Behind every failure is an opportunity somebody
wishes they had missed.
( Lily Tomlin )
Berkat Rahmat Allah SWT, dapat saya persembahkan skripsi ini untuk :
Bapak Mochtar Sardi dan Ibu Rahayu Tercinta
Maria, mbak lina, mas yudhi
Almamater Universitas Sebelas Maret
vi
MOTTO DAN PERSEMBAHAN
Allah, tidak ada Tuhan melainkan Dia Yang Hidup kekal lagi terus menerus mengurus
(Makhluk-Nya); tidak mengantuk dan tidak tidur . Kepunyaan-Nya apa yang dilangit dan di
bumi, Siapakah yang dapat memberi syafa’at di sisi Allah tanpa izin-Nya?Allah mengetahui
apa apa yang dihadapan mereka dan di belakang mereka, dan mereka tidak mengetahui apa
apa dari ilmu Allah melainkan apa yang di kehendaki-Nya. Kekuasaan Allah meliputi langit
dan bumi. Dan Allah tidak merasa berat memlihara keduanya, dan Allah Maha Tinggi Lagi
Maha Besar
( QS AL-Baqarah 255)
Don’t be afraid of missing opportunities. Behind every failure is an opportunity somebody
wishes they had missed.
( Lily Tomlin )
Berkat Rahmat Allah SWT, dapat saya persembahkan skripsi ini untuk :
Bapak Mochtar Sardi dan Ibu Rahayu Tercinta
Maria, mbak lina, mas yudhi
Almamater Universitas Sebelas Maret
vi
MOTTO DAN PERSEMBAHAN
Allah, tidak ada Tuhan melainkan Dia Yang Hidup kekal lagi terus menerus mengurus
(Makhluk-Nya); tidak mengantuk dan tidak tidur . Kepunyaan-Nya apa yang dilangit dan di
bumi, Siapakah yang dapat memberi syafa’at di sisi Allah tanpa izin-Nya?Allah mengetahui
apa apa yang dihadapan mereka dan di belakang mereka, dan mereka tidak mengetahui apa
apa dari ilmu Allah melainkan apa yang di kehendaki-Nya. Kekuasaan Allah meliputi langit
dan bumi. Dan Allah tidak merasa berat memlihara keduanya, dan Allah Maha Tinggi Lagi
Maha Besar
( QS AL-Baqarah 255)
Don’t be afraid of missing opportunities. Behind every failure is an opportunity somebody
wishes they had missed.
( Lily Tomlin )
Berkat Rahmat Allah SWT, dapat saya persembahkan skripsi ini untuk :
Bapak Mochtar Sardi dan Ibu Rahayu Tercinta
Maria, mbak lina, mas yudhi
Almamater Universitas Sebelas Maret
vii
KATA PENGANTAR
Segala puji syukur penulis panjatkan atas kehadirat Allah SWT, atas rahmat, hidayah, serta inayahNya penulis dapat menyelesaikan skripsi yang berjudul Pengaruh Fraksi Klorofil Spirulina sp terhadap Sifat Listrik dengan Struktur Dye Sensitized Solar Cell (DSSC). Sebagai salah satu syarat meraih gelar sarjana Sains di jurusan Fisika FMIPA UNS.
Dalam penyusunan skripsi ini, penulis mendapatkan bimbingan, bantuan , dan dukungan dari berbagai pihak. Oleh karena itu pada kesempatan ini perkenankanlah penulis menyampaikan ucapan terima kasih kepada :
1. Bapak Dr. Agus Supriyanto,S.Si., M.Si selaku pembimbing I 2. Bapak Dr. Eng. Risa Suryana, S.Si., M.Si selaku pembimbing II 3. Bapak Mochtar Sardi dan Ibu Rahayu atas do’a, dukungan,
semangatnya
4. Maria, mbak lina, mas yudhi ,mbak novi, mas abdul, ponakan mungilku azhar, terima kasih support nya
5. Nugroho, Sisil, imel, wulan, atas motivasi dan semangatnya 6. Teman – teman tim material organik.
7. Teman teman angkatan 2007
8. Adik - adik dan kakak - kakak tingkat, terima kasih sudah menjadi teman dan motivasiku
Semoga Allah SWT melimpahkan rahmatNya untuk kita semua. Amin. Penulis sadar bahawa skripsi ini jauh dari sempurna, maka kritik dan saran yang membangun sangat penulis harapakan. Akhir kata semoga Skripsi ini bermanfaat.
Surakarta, 3 Januari 2012
vii
KATA PENGANTAR
Segala puji syukur penulis panjatkan atas kehadirat Allah SWT, atas rahmat, hidayah, serta inayahNya penulis dapat menyelesaikan skripsi yang berjudul Pengaruh Fraksi Klorofil Spirulina sp terhadap Sifat Listrik dengan Struktur Dye Sensitized Solar Cell (DSSC). Sebagai salah satu syarat meraih gelar sarjana Sains di jurusan Fisika FMIPA UNS.
Dalam penyusunan skripsi ini, penulis mendapatkan bimbingan, bantuan , dan dukungan dari berbagai pihak. Oleh karena itu pada kesempatan ini perkenankanlah penulis menyampaikan ucapan terima kasih kepada :
1. Bapak Dr. Agus Supriyanto,S.Si., M.Si selaku pembimbing I 2. Bapak Dr. Eng. Risa Suryana, S.Si., M.Si selaku pembimbing II 3. Bapak Mochtar Sardi dan Ibu Rahayu atas do’a, dukungan,
semangatnya
4. Maria, mbak lina, mas yudhi ,mbak novi, mas abdul, ponakan mungilku azhar, terima kasih support nya
5. Nugroho, Sisil, imel, wulan, atas motivasi dan semangatnya 6. Teman – teman tim material organik.
7. Teman teman angkatan 2007
8. Adik - adik dan kakak - kakak tingkat, terima kasih sudah menjadi teman dan motivasiku
Semoga Allah SWT melimpahkan rahmatNya untuk kita semua. Amin. Penulis sadar bahawa skripsi ini jauh dari sempurna, maka kritik dan saran yang membangun sangat penulis harapakan. Akhir kata semoga Skripsi ini bermanfaat.
Surakarta, 3 Januari 2012
vii
KATA PENGANTAR
Segala puji syukur penulis panjatkan atas kehadirat Allah SWT, atas rahmat, hidayah, serta inayahNya penulis dapat menyelesaikan skripsi yang berjudul Pengaruh Fraksi Klorofil Spirulina sp terhadap Sifat Listrik dengan Struktur Dye Sensitized Solar Cell (DSSC). Sebagai salah satu syarat meraih gelar sarjana Sains di jurusan Fisika FMIPA UNS.
Dalam penyusunan skripsi ini, penulis mendapatkan bimbingan, bantuan , dan dukungan dari berbagai pihak. Oleh karena itu pada kesempatan ini perkenankanlah penulis menyampaikan ucapan terima kasih kepada :
1. Bapak Dr. Agus Supriyanto,S.Si., M.Si selaku pembimbing I 2. Bapak Dr. Eng. Risa Suryana, S.Si., M.Si selaku pembimbing II 3. Bapak Mochtar Sardi dan Ibu Rahayu atas do’a, dukungan,
semangatnya
4. Maria, mbak lina, mas yudhi ,mbak novi, mas abdul, ponakan mungilku azhar, terima kasih support nya
5. Nugroho, Sisil, imel, wulan, atas motivasi dan semangatnya 6. Teman – teman tim material organik.
7. Teman teman angkatan 2007
8. Adik - adik dan kakak - kakak tingkat, terima kasih sudah menjadi teman dan motivasiku
Semoga Allah SWT melimpahkan rahmatNya untuk kita semua. Amin. Penulis sadar bahawa skripsi ini jauh dari sempurna, maka kritik dan saran yang membangun sangat penulis harapakan. Akhir kata semoga Skripsi ini bermanfaat.
Surakarta, 3 Januari 2012
viii
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PENGESAHAN ...ii
HALAMAN PERNYATAAN ...iii
HALAMAN ABSTRAK ...iv
HALAMAN ABSTRACT ...v
HALAMAN MOTTO DAN PERSEMBAHAN ...vi
KATA PENGANTAR...vii
DAFTAR ISI ...viii
DAFTAR TABEL ...xi
DAFTAR GAMBAR...xii
DAFTAR LAMPIRAN ...xiv
BAB I PENDAHULUAN ...1
1.1 Latar Belakang ... 1
1.2 Rumusan Masalah... 2
1.3 Batasan Masalah ... 2
1.4 Tujuan Penelitian... 3
1.5 Manfaat Penelitian ... 3
BAB II LANDASAN TEORI... … .... 4
2.1 DSSC... ……. 4
2.1.1 Prinsip Kerja DSSC ... ... 4
2.2 Material DSSC ... 6
2.2.1 Substrat ... 6
2.2.2 Semikonduktor TiO2... 7
2.2.3Dye ... 7
2.2.3.1 Klorofil sebagaidye... 8
ix
2.2.3.3 Kandungan Klorofil ... 10
2.2.3.4 Karakterisasi Sifat Optik dan Sifat Listrik... 11
2.2.3.4.1 Karakterisasi Sifat Optik... 11
2.2.3.4.2 Karakterisasi Sifat Listrik ... 13
2.2.4 Elektrolit... 14
2.2.5 Elektroda lawan ... 15
2.3 Responsivitas Fotodioda ... 15
BAB III METODOLOGI PENELITIAN... 17
3.1 Tempat dan Waktu Penelitian ... 17
3.2 Alat dan Bahan ... 17
3.2.1 Alat Penelitian ... 17
3.2.2 Bahan Penelitian ... 18
3.3 Diagram Alur Penelitian ... 20
3.3.1 Persiapan ... 21
3.3.2 Isolasidyeklorofil ... 21
3.3.2.1 EkstraksiSpirulina sp...21
3.3.2.2 Kromatografi... 22
3.3.3 Karakterisasi OptikDye Spirulina sp ...24
3.3.4 Karakterisasi I-Vlarutan klorofil ... 25
3.3.5 Preparasi Elektroda Kerja... 26
3.3.6 Preparasi Larutan Elektrolit... 26
3.3.7 Preparasi Elektroda Lawan... 27
3.3.8 Perangkaian DSSC... 27
3.3.9 Pengujian KarakteristikI-VDSSC ... 28
BAB IV HASIL DAN PEMBAHASAN... 29
4.1 IsolasidyeklorofilSpirulina sp...29
4.2 Karakterisasi Optik dan KarakterisasiI-V Dye ...30
4.2.1 Karakteristik OptikDyeklorofilSpirulina sp...30
x
4.2.3 KarakterisasiI-VLarutan KlorofilSpirulina sp... 33
4.3 Pengukuran Sifat Listrik Fraksi Klorofil Spirulina Sp dengan struktur DSSC ... 36
BAB V KESIMPULAN DAN SARAN... 42
5.1 Kesimpulan... 42
5.2 Saran ... 42
DAFTAR PUSTAKA... 43
LAMPIRAN... 46
xi
DAFTAR TABEL
Halaman
Tabel 4.1. Nilai puncak absorbansi larutan klorofil ... 31
Table 4.2. Kandungan klorofil masing masing sampelSpirulina sp...32
Tabel 4.3. Tabel konduktivitasdyeklorofilSpirulina sp...35
Tabel 4.4. Nilai Responsivitas DSSC ... 41
xii
DAFTAR GAMBAR
Halaman
Gambar 2.1. Struktur dan komponen DSSC ... 5
Gambar 2.2. Prinsip kerja dari DSSC ... 6
Gambar 2.3. Struktur anatase (a) dan rutile (b) pada TiO2... 7
Gambar 2.4. Struktur molekuler klorofil ... 8
Gambar 2.5. Spektrum absorbs cahaya tampak klorofil a dan klorofil b ... 9
Gambar 2.6. Skema Hukum Lambert-Beer... 11
Gambar 2.7. StrukturIodine... 14
Gambar 3.1. Diagram penelitian... 20
Gambar 3.2. BubukSpirulina sp... 21
Gambar 3.3. Ekstraksi klorofilSpirulina sp... 22
Gambar 3.4. Kolom kromatografi dan statif ... 23
Gambar 3.5.UV-Vis Spectrophotometer Lambda 25... 24
Gambar 3.6.Elkahfi 100 I-V Meter ...26
Gambar 3.7. Larutan elektrolit ... 27
Gambar 3.8. Perangkaian DSSC dengan struktur berlapis (sandwich) ... 28
Gambar 3.9.Solar Power Meter 1333RdanKeithley 2602A... 28
Gambar 4.1. Larutan hasil ekstraksi ... 29
Gambar 4.2. Perbedaan warna hasil kromatografi ... 30
Gambar 4.3. Grafik absorbansi larutan klorofil Sp1, Sp2, dan Sp3... 30
Gambar 4.4. Grafik karakterisasiI-V pada Sp1, Sp2, dan Sp3kondisi terang... 34
Gambar 4.5. Grafik karakterisasiI-Vpada Sp1, Sp2, dan Sp3kondisi gelap ... 35
Gambar 4.6. Pengukuran DSSC pada kondisi terang ... 36
Gambar 4.7. Grafik karakterisasiI-VDSSC dengandyeSp1... 37
Gambar 4.8. Grafik karakterisasiI-VDSSC dengandyeSp2... 37
Gambar 4.9. Grafik karakterisasiI-VDSSC dengandyeSp3... 38
xiii
Gambar 4.10. Grafik perbandingan DSSC tanpa elektrolit dan DSSC dengan
elektrolit pada kondisi terang ... 40
Gambar 4.11. Grafik perbandingan DSSC tanpa elektrolit dan DSSC dengan
elektrolit pada kondisi gelap ... 40
xiv
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Perhitungan kandungan klorofil untuk masing masing fraksi ... 46
Lampiran 2 Perhitungan konduktivitas larutan klorofilSpirulina sp... 47
Lampiran 3 Perhitungan nilai Responsivitas (Re) ... 48
Lampiran 4 Struktur rutile TiO2hasilXRD... 49
1 BAB I
PENDAHULUAN
1.1. Latar Belakang Masalah
Perkembangan paling berarti dalam penelitian sel surya adalah penemuan
sel surya yang menggunakan pewarna tersensitasi atau Dye Sensitized Solar Cell
(DSSC) oleh Michael Grätzel pada 1991. Dye Sensitizer berasal dari dua kata
yaitu,dye dansensitization.Dye merupakan molekul pigmen atau senyawa kimia
yang dapat menyerap cahaya, sensitization merupakan proses yang membuat sel
surya menjadi peka terhadap cahaya. Sel surya ini disebut juga dengan sel Grätzel,
yaitu jenis sel surya yang melibatkan proses absorbsi optis dan proses pemisahan
muatan karena keberadaan sensitizer sebagai materi penyerap cahaya dengan
semikonduktor berpita lebar yang memiliki struktur morfologi nanokristalin.
Pada DSSC terjadi proses injeksi yaitu proses transfer elektron dari molekul
dye ke daerah pita konduksi semikonduktor yang terjadi karena adanya absorbsi
cahaya (Agot et.al; 2001). Lapisan dye berfungsi sebagai absorber sinar matahari
yang utama sehingga menghasilkan aliran elektron. Proses penyerapan cahaya
matahari oleh sel surya nanokristal titanium dioksida (TiO2) tersensitasi dye
menyerupai mekanisme fotosintesis pada daun tumbuhan dengan klorofil sebagai
dye-nya.Dyeyang digunakan sebagaisensitizerdapat berupadye sintesis maupun
dye alami. DSSC komersial dengan dye sintesis jenis ruthenium complex telah
mencapai efisiensi 10% (Gratzel, 2003). Namun karena jumlahnya yang terbatas
dan harganya yang relatif mahal. Maka perlu adanya alternatif lain sebagai
penggantidyejenis ini yaitudyealami.
Salah satu penelitian terbaru menyatakan bahwa larutan klorofil dari
Spirulina sptelah memenuhi karakteristik sebagai dye pada DSSC (Sumaryanti,
2010). Syarat agardyemampu berfungsi sebagai sensitizeradalah bahan tersebut
mampu menjadi medium transfer pembawa muatan listrik sebagai akibat foton
yang diserap (Supriyanto dkk, 2009). Maka dari itu dalam penelitian ini
menggunakan dye alami dari klorofil Spirulina sp yang di ekstrak menggunakan
metode kromatografi.
1.2. Perumusan Masalah
Berdasarkan latar belakang masalah yang telah dikemukakan, maka dapat
dirumuskan beberapa masalah sebagai berikut :
1. Bagaimana kemampuan absorbansi dari fraksi klorofil Spirulina sp yang
akan digunakan sebagaidye?
2. Bagaimana karakteristik I-V dari fraksi klorofil Spirulina sp yang akan
digunakan sebagaidye?
3. Bagaimana pengaruh fraksi klorofil Spirulina sp terhadap sifat listrik
dengan struktur DSSC?
1.3. Batasan Masalah
Beberapa batasan perlu diberikan agar permasalahan yang akan dibahas
menjadi terarah. Batasan tersebut adalah sebagai berikut :
1. Dyepada penelitian ini merupakan fraksi klorofil dari ekstrakSpirulina sp
hasil pemisahan kromatografi sebanyak 3 fraksi, yaitu Sp1 untuk warna
hijau pekat, Sp2untuk warna hijau tidak pekat, dan Sp3untuk warna hijau
kekuning-kuningan.
2. Karakteristik optik meliputi absorbansi menggunakan UV-Vis
Spectrometer Lambda 25 dan karakterisasi listrikI-V denganElkahfi 100
I-Vmeter.
3. Deposisi TiO2pada kaca Fluorine doped Tin Oxide (FTO) menggunakan
metodeslipcasting.
4. Karakteristik I-V fraksi klorofil Spirulina sp dengan struktur DSSC
denganKeithley 2602A .
1.4.Tujuan Penelitian
Adapun tujuan penelitian yang ingin dicapai dalam penyusunan tugas akhir
ini adalah:
1. Mengetahui kemampuan absorbansi dari fraksi klorofil Spirulina sp yang
akan digunakan sebagaidye.
2. Mengetahui karakteristik I-V dari fraksi klorofil Spirulina sp yang akan
digunakan sebagaidye.
3. Mengetahui pengaruh fraksi klorofil Spirulina sp terhadap sifat listrik
dengan struktur DSSC.
1.5. Manfaat Penelitian
Dari penelitian yang dilakukan, dapat diperoleh manfaat sebagai berikut :
1. Mengkaji pembuatan DSSC sebagai sarana alternatif energi terbarukan.
2. Mengetahui prinsip kerja sel surya tersensitasi zat warna.
3. Teknologi pembuatan DSSC yang dikembangkan pada penelitian ini dapat
menjadi studi awal untuk penelitian lebih lanjut sehingga menghasilkan sel
surya yang mempunyai kinerja lebih baik.
4 BAB II
LANDASAN TEORI
2.1. DSSC (Dye-Sensitized Solar Cell)
Dye Sensitized Solar Cell (DSSC), pertama kali ditemukan oleh Michael
Gratzel pada tahun 1991, kemudian menjadi salah satu topik penelitian yang
dilakukan intensif oleh peneliti di dunia. DSSC disebut juga terobosan pertama
dalam teknologi sel surya sejak sel surya silikon. Penemuan Gratzel tersebut
berhubungan dengan penerapan prinsip efisiensi kompleks ruthenium untuk
mengaktifkan semikonduktor oksida, yang sangat sensitif di daerah cahaya
tampak (visible region). DSSC terdiri dari sebuah elektroda kerja, sebuah
elektroda lawan dan sebuah elektrolit. Zat warna dari ruthenium complexs
melekat pada pori nanokristal dari film semikonduktor, misalnya TiO2 yang
merupakan elektroda kerja. Selain itu digunakan kaca konduktif platina sebagai
elektroda lawan dan larutanI3-/I-sebagai elektrolit (Halme, 2002). DSSC atau Sel
Gratzel ini sangat menjanjikan karena pembuatannya tidak membutuhkan
peralatan yang rumit. Efisiensi DSSC dengan dye ruthenium (II) polypyridyl
complexmencapai 10% (Gratzel, 2003)
2.1.1. Prinsip Kerja DSSC
Prinsip kerja sel surya jenis DSSC pada dasarnya melibatkan tiga komponen
utama, yaitu elektroda kerja yang berfungsi untuk menyerap foton dan
membangkitkan elektron bebas, elektroda lawan, dan elektrolit yang berfungsi
sebagai penghubung kedua jenis elektroda tersebut. Elektroda kerja merupakan
lapis tipis TiO2 pada substrat kaca transparan. Energi cahaya yang diterima oleh
DSSC mengakibatkan tereksitasinya elektron dari pita HOMO (High Occupied
Molecular Orbital) ke pita LUMO (Low Unoccupied Molecular Orbital) karena
adanya perbedaan tingkat energi dari pita konduksi semikonduktor TiO2 yang
lebih rendah dibandingkan dengan orbital LUMO pada dye, maka akan
menyebabkan terjadinya perpindahan elektron dari orbital LUMO dye ke pita
konduksi dari semikonduktor dan selanjutnya ke kaca konduktif (Natalita, 2011)
Gambar 2.1. Struktur dan Komponen DSSC (Gratzel, 2003)
Absorbsi cahaya dari DSSC dilakukan oleh molekul dye dan separasi
muatan oleh injeksi elektron dari dye pada TiO2 di permukaan elektrolit
semikonduktor. Dengan struktur pori yang nano maka permukaan dari TiO2
menjadi luas sehingga memperbanyak dye yang terabsorbsi dan akan
meningkatkan efisiensi (O’Regan dan Gratzel, 1991). Saat penyusunannya,
molekul dye menjadi sebuah lapisan dye yang tebal. Lapisan tersebut mampu
meningkatkan kemampuan optik DSSC. Kontak langsung antara molekul dye
dengan permukaan elektroda semikonduktor dapat memisahkan muatan dan
berkontribusi pada pembangkit arus.
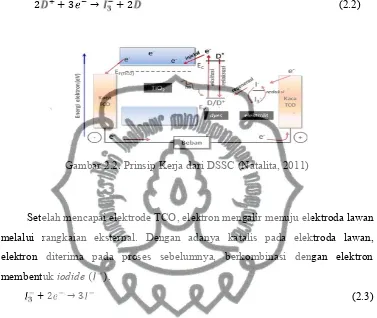
Prinsip kerja DSSC digambarkan dengan Gambar 2.2. Pada dasarnya prinsip
kerja dari DSSC merupakan reaksi dari transfer elektron. Proses pertama dimulai
dengan terjadinya eksitasi elektron pada molekul dye akibat absorbsi foton.
Elektron tereksitasi dariground state(D) keexcited state(D*).
+ → ∗ (2.1)
Elektron dari exited state kemudian langsung terinjeksi menuju conduction
band (ECB) titania sehingga molekul dye teroksidasi (D+). Dengan adanya donor
elektron oleh elektrolit ( ) maka molekul dye kembali ke keadaan awalnya
(ground state) dan mencegah penangkapan kembali elektrondyeyang teroksidasi.
2 + 3 → + 2 (2.2)
Gambar 2.2. Prinsip Kerja dari DSSC (Natalita, 2011)
Setelah mencapai elektrode TCO, elektron mengalir menuju elektroda lawan
melalui rangkaian eksternal. Dengan adanya katalis pada elektroda lawan,
elektron diterima pada proses sebelumnya, berkombinasi dengan elektron
membentukiodide( ).
+ 2 → 3 (2.3)
Iodideini digunakan untuk mendonor elektron kepadadyeyang teroksidasi,
sehingga terbentuk suatu siklus transport elektron. Dengan siklus ini terjadi
konversi langsung dari cahaya matahari menjadi listrik.
2.2. Material DSSC
2.2.1. Substrat
Substrat yang digunakan dalam DSSC pada umumnya yaitu jenis TCO
(Transparent Conductive Oxide) yang merupakan kaca transparan konduktif.
Material Substrat pada DSSC memiliki fungsi sebagai badan dari sel surya, dan
lapisan konduktifnya berfungsi tempat mengalirnya muatan. Material yang sering
digunakan adalahFluorine doped Tin Oxide( FTO ) danIndium Tin Oxide(ITO),
hal ini dikarenakan pada proses pelapisan material pada substrat diperlukan proses
sintering pada suhu 400-500°C dan material tersebut merupakan pilihan tepat
karena tidak mengalamidefectpada rentang temperatur tersebut.
2.2.2. Semikonduktor TiO2
TiO2 merupakan material semikonduktor tipe-n yang mempunyai ukuran
partikel antara 10-50 nm. TiO2 memiliki peran penting dalam pemanfaatan
fotoenergi karena memiliki daya oksidatif dan stabilitas yang tinggi terhadap
fotokorosi, selain itu harganya relatif murah , mudah didapat, dan tidak beracun
(Gratzel, 2003). TiO2 mempunyai kemampuan untuk menyerapdyelebih banyak
karena didalamnya terdapat rongga dan ukurannya dalam nano, sehingga disebut
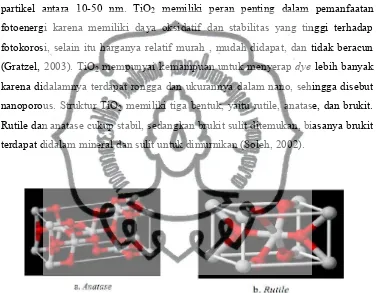
nanoporous. Struktur TiO2memiliki tiga bentuk, yaitu rutile, anatase, dan brukit.
Rutile dan anatase cukup stabil, sedangkan brukit sulit ditemukan, biasanya brukit
terdapat didalam mineral dan sulit untuk dimurnikan (Soleh, 2002).
Gambar 2.3. Struktur Anatase (a) dan Rutile (b) (Soleh, 2002)
2.2.3.Dye
Molekul dye berfungsi melakukan absorbsi cahaya pada permukaan TiO2.
Sejauh ini dye yang digunakan dapat berupa dye sintesis maupun dye alami.
DSSC komersial dengan penggunaan dye sintesis jenis ruthenium complexs
memiliki efisiensi sebesar 10% (Gratzel, 2003), namun karena jumlahnya yang
terbatas dan harganya yang mahal membuat adanya alternatif penggunaan dye
alami yang dapat di ekstrak dari bagian tumbuhan seperti daun, bunga, atau buah
(Maddu dkk, 2007). Zat warna yang dihasilkan oleh tumbuhan tersebut telah
terbukti mampu memberikan efek fotovoltaik walaupun efisiensi yang dihasilkan
masih sangat kecil dibanding zat warna sintesis, namun demikian zat warna dari
bahan organik sangat kompetitif untuk dijadikan fotosensitizer karena biaya
produksi yang murah dan proses isolasi yang mudah (Anggraini, 2009).
2.2.3.1. Klorofil sebagaiDye
Ekstrak atau pigmen tumbuhan yang digunakan sebagai fotosensitizerpada
daerah visible dapat berupa ekstrak klorofil (Amoa, 2003). Klorofil merupakan
pigmen utama tumbuhan yang berfungsi untuk menyerap cahaya dan
mengubahnya menjadi energi kimia yang dibutuhkan dalam mereduksi
karbondioksida menjadi karbohidrat dalam proses fotosintesis. Zat ini terdapat
pada kloroplas dalam jumlah yang banyak serta mudah untuk di ekstraksi kedalam
pelarut aseton (Harbone, 1996). Klorofil memiliki struktur seperti pada gambar
berikut
Gambar 2.4. Struktur Molekuler Klorofil (Shakhashiri, 2010)
Secara kimia semua klorofil mengandung satu inti porfirin (tetrapinol)
dengan satu atom magnesium yang terikat kuat ditengahnya dan satu rantai
samping dihidrokarbon panjang (fitil) tergabung melalui gugus asam karboksilat.
Didalam tumbuhan sekurang-kurangnya terdapat lima jenis klorofil. Semua
memiliki struktur dasar yang sama, tetapi memiliki sifat sesuai dengan rantai
samping yang terikat pada sebelah kanan atas inti porfirin yang
macam. Klorofil a memiliki rantai samping dengan gugus metal dan klorofil b
memiliki rantai samping dengan gugus aldehid. Klorofil a dan b terdapat pada
tumbuhan tingkat tinggi seperti lumut dan paku-pakuan, sedangkan klorofil c, d,
dan e hanya ditemukan dalam alga.
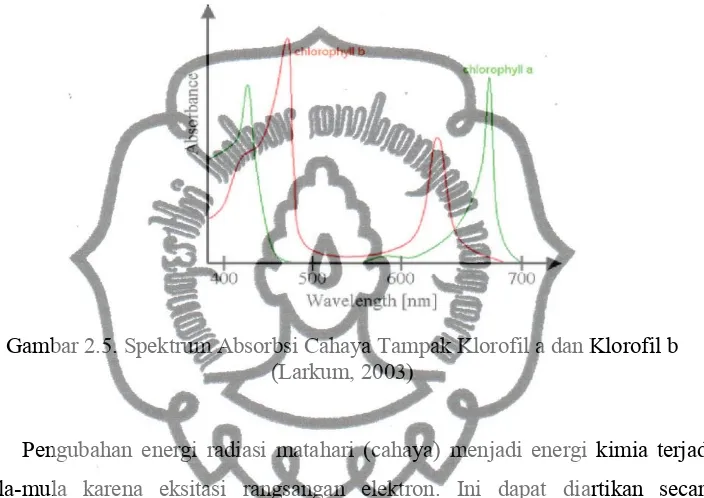
Gambar 2.5. Spektrum Absorbsi Cahaya Tampak Klorofil a dan Klorofil b (Larkum, 2003)
Pengubahan energi radiasi matahari (cahaya) menjadi energi kimia terjadi
mula-mula karena eksitasi rangsangan elektron. Ini dapat diartikan secara
sederhana dengan pemindah elektron dari orbit dasar (paling dekat dengan inti) ke
orbit 1 atau 2 yang menjadi inti. Atom berada pada keadaan paling stabil bila
elektron menempati garis orbit yang paling dekat dengan inti (keadaan energi
paling kecil atau posisi dasar elektron). Karena garis orbit tempat mengorbitnya
sangat definit, hanya gelombang cahaya dengan kandungan energi (kuanta atau
foton) tertentu yang dapat menghasilkan transisi elektron. Kuanta cahaya yang
memiliki energi yang lebih besar atau lebih rendah tidak efektif. Cahaya biru dan
merah dari sinar matahari merupakan yang paling efektif menghasilkan transisi
elektron. Hanya gelombang cahaya tertentu yang aktif dalam proses fotosintesis.
Bagian radiasi yang aktif dalam fotosintesis yang dikenal dengan istilah
photosynthetic active radiation (PAR) adalah cahaya nampak yang terletak pada
panjang gelombang 400-700 nm.
2.2.3.2. Spirulina sp
Spirulina spadalah sejenis tumbuhan air yang hanya memiliki satu sel dan
tumbuh didalam air yang beralkali. Air yang beralkali memiliki Ph lebih dari 8.
KlasifikasiSpirulina spmenurut Bold & Wyne (1978) adalah sebagai berikut :
Kingdom :Protista
Divisi :Cyanophyta
Kelas :Cyanophyceae
Ordo : Nostocales
Famili :Oscilatoriaceae
Genus :Spirulina
Spesies :Spirulina sp
Spirulina spmengandung beberapa pigmen fotosintesis, yaitu klorofil a dan
b, xantofil, beta karoten, echinenone, mixoksantofil, zeaxanthin, canthaxanthin,
diatoxantin, trihidroksi echinenone, beta-cryptoxantin, oscillaxanthin,
diatoxanthin, phycobiliprotein c-phycocyanin dan allophycocyanin. Pigmen
fotosintesis yang mendominasi Spirulina sp adalah klorofil a, klorofil b dan beta
karoten. Klorofil a memiliki spektrum absorbsi yang stabil. Hal ini dikarenakan
adanya konjugasi diantara ikatan rangkapnya (Lehninger, 1982). Spirulina sp
memiliki kandungan klorofil lebih tinggi dibandingkan alfalfa yaitu sejenis
legume yang paling kaya dengan klorofil, sekurang-kurangnya 4 kali lebih tinggi
daripada sayur-sayuran biasa (Fikri, 2007). Bentuk tubuh Spirulina sp yang
menyerupai benang merupakan rangkaian sel yang berbentuk silindris dengan
dinding sel yang tipis, berdiameter 1-12 mm.
2.2.3.3. Kandungan Klorofil
Pengukuran klorofil a dan klorofil b dapat dilakukan dengan menentukan
serapan langsung pada berbagai panjang gelombang. Nilai serapan larutan pada
tiap panjang gelombang dapat diukur memakaiUV- Vis Spektrofotometer Lambda
25. Adapun untuk mengetahui kandungan konsentrasi klorofil menggunakan
persamaan (Porra et.al; 1989 )
Chl-a =12.25 × A , − 2.55 × A ,
Chl-b=20.31 × A , − 4.91 × A , (2.4)
2.2.3.4. Karakterisasi Sifat Optik dan Listrik
2.2.3.4.1. Karakterisasi Sifat Optik
Berkas cahaya yang dikenakan pada sebuah materi seperti yang ditunjukkan
pada Gambar 2.6 akan mengalami tiga hal yaitu absorbsi, refleksi, dan transmisi.
Gambar 2.6. Skema Hukum Lambert-Beer (Ingle, 1988)
Hukum Lambert menyatakan bahwa berkas cahaya datang yang diabsorbsi
oleh suatu materi tidak bergantung pada intensitasnya. Hukum Lambert ini hanya
berlaku jika di dalam material tidak ada reaksi kimia ataupun proses fisis yang
dapat dipicu oleh berkas cahaya datang tersebut. Intensitas cahaya yang di
absorbsi oleh material tersebut dapat dituliskan dalam persamaan (2.5) (Ingle,
1988).
0 I T
I (2.5)
Hukum Beer menyatakan bahwa absorbansi cahaya berbanding lurus dengan
konsentrasi dan ketebalan media yang dinyatakan dalam Persamaan (2.6) (Ingle,
1988).
lc T Log I
I
Alog( ) ( ) 0
(2.6)
Sehingga diperoleh Persamaan (2.7) (Ingle, 1988).
lc
Koefisien absorbsi α dapat diperoleh menggunakan Persamaan (2.8) (Ingle, 1988).
)
adalah koefisien absorbansi (cm-1)
Tadalah transmitansi
Ioadalah daya cahaya datang (W.m-2)
Iadalah daya cahaya keluar (W.m-2)
cadalah konsentrasi molar (mol. l-1)
ladalah tebal media (cm)
Absorbsi cahaya oleh suatu molekul merupakan suatu bentuk interaksi
antara gelombang cahaya atau foton dan atom atau molekul. Energi cahaya
diserap oleh atom atau molekul dan digunakan oleh elektron di dalam atom atau
molekul tersebut untuk bertransisi ke tingkat energi yang lebih tinggi. Persamaan
(2.9) (Beiser, 1999) menyatakan bahwa absorbsi hanya terjadi jika selisih kedua
tingkat energi elektronik tersebut ΔE =E2– E1bersesuaian dengan energi cahaya
atau foton yang datang.
ΔE=Efoton
(2.9)
Probabilitas absorbsi bergantung pada kerapatan elektron pada tingkat
energi pita konduksi dan pita valensi serta tingkat energi cahaya yang datang.
Jika energi cahaya yang datang lebih besar dari celah pita energi, maka koefisien
absorbsi akan makin besar pula. Koefisien absorbsi berguna dalam penentuan
besarnya pembangkitan pasangan elektron danholeakibat adanya penyinaran.
2.2.3.4.2. Karakterisasi Sifat Listrik
Besarnya resistansi dari suatu larutan dapat diukur menggunakan metode
two point probedengan menggunakan alatElkahfi 100 I-V Meter . Pada metode
ini terdapat dua probe, yaitu satu probe arus dan satu probe tegangan. Probe
pertama berfungsi untuk mengalirkan arus listrik dan probe yang lain untuk
mengukur tegangan listrik ketika probe-probe tersebut dikenakan pada sampel.
Dari variasi perubahan tegangan yang diberikan, akan diperoleh perubahan arus
yang diukur sehingga besarnya resistansi berdasarkan nilai tegangan dan arusnya.
Nilai resistansi sangat dipengaruhi oleh elektroda. Resistansi yang terukur
merupakan resistansi total antara resistansi larutan klorofil dan resistansi
elektroda. Bahan konduktor yang baik mempunyai nilai konduktivitas tinggi,
sedangkan untuk bahan isolator, konduktivitasnya rendah karena tingginya
resistivitas. Besarnya resistivitas berbanding terbalik dengan konduktivitas, dan
hubungannya ditunjukkan dengan Persamaan (2.10) (Tipler, 2001).
1 (2.10)
merupakan konduktivitas (Ωm)-1danadalah resistivitas (Ωm).
Medan listrik Edan rapat arus J akan dihasilkan pada suatu konduktor
apabila konduktor tersebut dialiri arus, dimana besarnya rapat arus sebanding
dengan kuat medan listrik dalam konduktor dan secara matematik dirumuskan
oleh Persamaan (2.11) (Tipler, 2001).
E
J (2.11)
J adalah rapat arus yang menunjukkan besarnya aliran muatan (I) pada suatu
konduktor persatuan luas (A), dan dinyatakan dengan Persamaan (2.12) (Tipler,
2001).
A I
J (2.12)
Persamaan (2.11) digunakan untuk menentukan nilai medan listrik E pada
konduktor tersebut apabila diberi teganganV(Tipler, 2001).
L V
E (2.13)
Lmerupakan panjang penampang dalam satuan meter.
Mengacu pada Persamaan (2.11), (2.12), dan (2.13) diperoleh Persamaan
(2.14).
Nilai tahanan R dari suatu konduktor dirumuskan oleh Persamaan (2.10) (Tipler,
2001).
I V
R (2.15)
Berdasarkan Persamaan ( 2.14) dan ( 2.15) dapat diperoleh Persamaan (2.16).
A L I V .
(2.16)
Sehingga resistansi dapat juga dinyatakan sesuai Persamaan (2.17).
A L
R. (2.17)
Nilai resistansi berbanding lurus terhadap resistivitas bahan dan panjang
resistor dan berbanding terbalik dengan luas penampang yang tegak lurus arah
aliran arus. Persamaan (2.10) menunjukkan bahwa resistivitas berbanding terbalik
dengan konduktivitas. Dengan konduktivitas kecil maka larutan itu lebih bersifat
resistan (penghambat listrik) dan sebaliknya bila konduktivitas suatu bahan itu
besar maka resistansi bahan tersebut akan kecil.
2.2.4. Elektrolit
Larutan elektrolit yang digunakan pada sistem DSSC berfungsi untuk
menggantikan kehilangan elektron pada pita HOMO dari dye akibat eksitasi
elektron dari pita HOMO (High Occupied Molecular Orbital) ke pita LUMO
(Low Unoccupied Molecular Orbital) karena penyerapan cahaya tampak olehdye.
Elektrolit juga dapat menerima elektron pada sisi elektroda lawan. Pada umumnya
pembuatan sel DSSC menggunakan pasangan elektrolit I- dan I3- sebagai
elektrolit, karena sifatnya yang stabil dan mempunyai reversibilitas yang baik
(Wang et.al; 2005).
Gambar 2.7. StrukturIodine(Wang et.al; 2005).
2.2.5. Elektroda lawan
Katalis dibutuhkan untuk mempercepat kinetika reaksi proses reduksi
triiodidepada TCO (Transparant Conductive Oxide). Platina merupakan material
yang umum digunakan sebagai katalis pada berbagai aplikasi, dan juga sangat
efisien dalam aplikasinya pada DSSC. Walaupun platina memiliki kemampuan
katalistik yang tinggi, namun platina merupakan material yang mahal, maka
sebagai alternatif dikembangkan elektroda lawan berupa karbon sebagai lapisan
katalis. Karena luas permukaannya yang tinggi elektroda lawan karbon
mempunyai keaktifan reduksitriiodideyang menyerupai elektroda platina.
2.3. Responsivitas Fotodioda
Responsivitas merupakan sebuah ukuran dari sensitivitas yang
memperhitungkan daerah aktif dari fotodioda. Salah satu metode standar yang
digunakan untuk menentukan responsivitas dari fotodioda adalah dengan
membagi arusshort circuit(ISC) dengan intensitas cahaya dari sumber lampu yang
digunakan. Arus short circuit (ISC) merupakan arus pada saat tegangan nol.
Sedangkan intensitas cahaya dari suatu sumber cahaya dapat diukur dengan
menggunakanSolar Power Meter.
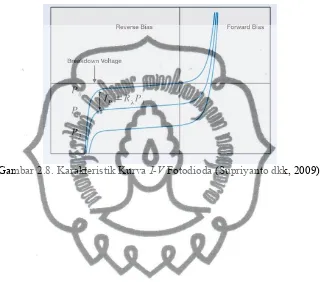
Nilai responsivitas sendiri diperoleh dari kurvaI-Vseperti Gambar 2.8. Pada
saat diberikan tegangan, maka akan menghasilkan arus tertentu. Persamaan untuk
menghitung nilai responsivitas sendiri adalah
= (2.18)
Keterangan :Re adalah Responsivitas (A/[Watt/m2])
ISCadalah Arusshort circuit(Ampere)
Eeadalah Intensitas cahaya (Watt m-2)
Gambar 2.8. Karakteristik KurvaI-VFotodioda (Supriyanto dkk, 2009)
17 BAB III
METODE PENELITIAN
3.1. Tempat dan Waktu Penelitian
Metode Penelitian yang digunakan adalah metode eksperimen. Penelitian ini
dilakukan di Laboratorium Material Jurusan Fisika FMIPA UNS untuk tahap
ekstraksi serta preparasi dan pengujian sifat listrik DSSC, Laboratorium Jurusan
Kimia FMIPA UNS untuk tahap kromatografi, Laboratorium MIPA Terpadu
FMIPA UNS untuk karakterisasi XRD TiO2. Penelitian dilaksanakan dari bulan
Juni – November 2011.
3.2. Alat dan Bahan
3.2.1. Alat Penelitian
Alat yang digunakan dalam penelitian ini adalah:
1. IsolasidyeklorofilSpirulina sp
a. Ekstraksi
Tabung erlenmeyer 250 ml digunakan pada proses ekstraksi sebagai
wadah, Neraca analitik Metler Toledo digunakan untuk menimbang
bahan yang akan di ekstrak (Spirulina sp),Magnetic stirerdigunakan
untuk mengaduk larutan dalam tabung reaksi, Gelas ukur 250 ml
digunakan untuk mengukur aseton, corong digunakan untuk
mempermudah menuangkan larutan pada wadah lain, pipet tetes
digunakan untuk mengambil larutan dari dalam botol.
b. Kromatografi
Satu set kolom kromatografi, digunakan untuk memisahkan klorofil
Spirulina sp dari pigmen fotosintesis yang ikut larut pada proses
ekstraksi, gelas beker digunakan untuk menampung larutan hasil
kromatografi yang terpisah menjadi beberapa fraksi, kompresor udara
mini digunakan untuk memampatkan tekanan udara pada kolom agar
proses turunnya larutan lebih cepat.
2. Alat uji karakterisasi fraksiSpirulina sp
UV-Visible Spectrophotometer Lambda 25, untuk mengukur absorbansi
pada masing - masing fraksi hasil kromatografi,Elkahfi 100 I-VMeter,
untuk mengetahui karakteristik arus dan tegangan larutan klorofil.
3. Alat uji karakterisasi XRD
X-Ray Diffraction Bruker D8 Advance (XRD), untuk mengidentifikasi
struktur kristal TiO2.
4. Alat preparasi DSSC
Hot Plate IKAR C-MAG HS7 untuk pengaduk larutan dan pemanas,
supaya larutan tercampur rata digunakanmagnetic stirrer, spatula untuk
mengambil bubuk dan mendeposisi TiO2pada kaca FTO
5. Pengujian sifat listrik DSSC
Lampu OHP (Over Head Projector) untuk lampu iluminasi, Keithley
2602A System Source Meter untuk mengetahui karakteristik I-V, Solar
Power Meter 1333R untuk mengukur intensitas cahaya.
3.2.2. Bahan Penelitian
Bahan yang digunakan dalam penelitian adalah:
1. IsolasidyeklorofilSpirulina sp
a. Ekstraksi
Bubuk Spirulina sp, sebagai bahan ekstrak, aseton sebagai pelarut
pigmen klorofil, kertas saring Whatman no.42 untuk menyaring
larutan ekstrak, alumunium foil untuk melindungi larutan agar tidak
terjadi kontak langsung dengan cahaya matahari, tissue secukupnya
sebagai bahan pembersih.
b. Kromatografi
N-Heksan,silica gel
2. Uji karakterisasi absorbansi
Fraksi hasil kromatografi, yaitu Sp1, Sp2,dan Sp3.
3. Uji fabrikasi X-Ray Diffraction(XRD)
Bubuk TiO2
4. Preparasi komponen- komponen DSSC
a. Pembuatan elektroda kerja
Kaca FTO, bubuk TiO2dan etanol untuk membersihkan kaca
b. Pembuatan elektroda lawan
Kaca FTO, grafit dari pensil kayu
c. Larutan elektrolitIodine
3.3. Diagram Penelitian
Secara umum alur penelitian ditunjukkan seperti gambar di bawah ini
Gambar 3.1. Diagram Alur Penelitian Persiapan
Alat dan Bahan
Isolasi klorofilSpirulina sp 1. Ekstraksi
2. Kromatografi
Karakteristik Dasar : 1.UV-Vis
2.I-V
Preparasi elektroda kerja 1.Pembuatan suspensi TiO2
2. Deposisi TiO2pada FTO
3. Pemanasan
Preparasi larutan elektrolit
Preparasi elektroda lawan
Pengujian sifat listrik DSSC Perangkaian DSSC TiO2/dye/elektrolit/karbon/TiO2
Analisa
Kesimpulan
3.3.1. Persiapan
Tahap persiapan ini meliputi mempersiapkan dan membersihkan semua alat
yang akan digunakan mengetahui pengaruh fraksi klorofil Spirulina sp terhadap
sifat listrik dengan struktur DSSC.
3.3.2. IsolasiDyeKlorofil
3.3.2.1. EkstraksiSpirulina sp
Proses isolasi terdiri dari ekstraksi klorofil Spirulina sp, kemudian
dilakukan proses kromatografi. Spirulina sp yang digunakan berupa bubuk
sebanyak 50 gram. Pada pembuatan larutan ekstraksiSpirulina spyang digunakan
sebagai pelarut adalah aseton sebanyak 250 ml. Aseton digunakan karena
memiliki sifat polar, yaitu tidak dapat bereaksi dengan komponen-komponen
lainnya yang diisolasi. Selain itu aseton juga memiliki sifat – sifat yang spesifik
seperti hanya mengisolasi atau melarutkan zat-zat yang diinginkan, mempunyai
titik didih rendah dan dapat dihilangkan dengan teknik pemanasan yang
sederhana.
Bubuk klorofil yang telah dicampur pelarut diaduk menggunakanHot Plate
IKAR C-MAG HS7 dengan kecepatan putar 100 rpm selama 30 menit dan
menggunakan magnetic stirrer. Pengadukan ini bertujuan untuk memisahkan
larutan dengan endapan bubuk klorofil. Kemudian hasilnya disaring menggunakan
kertasWhatman no. 42. Ukuran porikertasWhatmanno. 42 sebesar 450 nm akan
menahan komponen terlarut yang lebih besar dari ukuran pori kertas, sehingga
diperoleh larutan klorofil dengan ukuran komponen terlarut yang homogen.
Tahap ekstraksi seperti pada gambar 3.3 dengan langkah-langkah sebagai berikut:
1. BubukSpirulina spditimbang menggunakan neraca digitalMetler Toledo.
2. Aseton diambil dengan gelas ukur sebanyak 250ml.
3. Bubuk Spirulina sp yang sudah ditimbang di larutkan dengan aseton ke
dalam tabung erlenmeyer.
4. Larutan tersebut diaduk menggunakan magnetic stirrer dengan kecepatan
100 rpm selama 30 menit sampai semua bubukSpirulina splarut.
5. Larutan disaring dengan kertas saring whatman no. 42 supaya sisa bubuk
Spirulina sptertinggal.
6. Hasil ekstraksi klorofil Spirulina sp disimpan dalam botol yang tertutup
rapat dan dilapisi aluminium foil agar tidak terjadi kontak dengan cahaya
matahari.
Gambar 3.3. Ekstraksi KlorofilSpirulina sp
3.3.2.2. Kromatografi
Larutan hasil ekstraksi kemudian dikromatografi untuk memisahkan fraksi
warna larutan klorofil. Selain itu, proses kromatografi bertujuan untuk
menghasilkan larutan klorofil yang bersih dari endapan bubuk klorofil. Sebelum
proses kromatografi dilakukan, larutan hasil ekstraksi diuapkan menggunakan
evaporator untuk mengurangi kadar pelarut. Proses evaporasi dilakukan pada
tekanan kamar dan suhu 60oC. Evaporasi menghasilkan larutan klorofil yang lebih
kental dan pekat. Proses kromatografi ditunjukkan pada Gambar 3.4. Langkah
langkah pada tahap kromatografi adalah sebagai berikut :
1. Kolom kromatografi dan kompresor mini dipasang pada statif.
2. Silica gel dimasukkan ke dalam kolom kromatografi sampai batas yang
ditentukan (3/4 dari tinggi labu kolom Erlenmeyer).
3. N-Heksana dituangkan ke dalam kolom kromatografi.
4. Pompa udara dinyalakan sampai tidak ada gelembung dalam campuran
silica geldan N-Heksana.
5. Pompa udara kemudian dimatikan dan larutan hasil ekstraksi klorofil
Spirulina spdimasukkan di atas campuransilica geldan N-Heksana dalam
kolom kromatografi.
6. Pompa udara dinyalakan kembali sampai klorofil yang dalam penelitian ini
berwarna hijau turun sampai ujung kolom dan terpisah dalam 3 warna
yang berbeda.
7. Masing – masing klorofil hasil kromatografi ditampung sesuai perbedaan
warna.
8. Klorofil hasil kromatografi atau disebut fraksi 1 ditandai dengan Sp1yang
merupakan larutan dengan warna hijau pekat yang turun pertama kali, Sp2
(fraksi 2) merupakan cairan berikutnya berwarna hijau tetapi tidak pekat,
dan Sp3 (fraksi 3) untuk cairan berikutnya yang memiliki warna hijau
kekuning-kuningan.
Gambar 3.4. Kolom Kromatografi dan Statif
3.3.3. Karakterisasi OptikDye Spirulina sp
Karakterisasi optik dye klorofil ini diperoleh dengan menguji nilai
absorbansi dye klorofil tersebut, menggunakan UV-Visible Spectrophotometer
Lambda 25 dengan variasi masing – masing fraksi klorofil hasil kromatografi.
Pengujian larutan klorofil dilakukan untuk mengetahui fraksi klorofil hasil
kromatografi mana yang mempunyai kemampuan absorbansi lebih tinggi. Semua
sampel diuji untuk mengetahui spektrum masing-masing sampel. Larutan
dimasukkan pada kuvet hingga kuvet terisi minimal tiga per empat tinggi kuvet
(5ml). Pembanding sampel adalah aseton, itu dikarenakan aseton adalah pelarut
yang digunakan pada saat ekstraksi.
LarutanSpirulina sp diuji absorbansinya dengan SpektrometerUV-Visible
Spectrophotometer Lambda 25. Langkah awal melakukan UV-Vis yaitu
menghidupkan mesin UV-Visible Spectrophotometer Lambda 25 dan komputer
dengan menyalakan tombol on. Pada program dipilih parameterabs yang artinya
absorbansi. Sebelum melakukan proses pengukuran absorbansi dilakukanbaseline
terlebih dahulu. Baseline saat pengukuran larutan dilakukan dengan meletakkan
kuvet berisi aseton. Baseline dilakukan pada panjang gelombang 400 – 800 nm.
Pada rentang panjang gelombang tersebut, klorofil secara alami efektif menyerap
cahaya pada panjang gelombang saat berlangsungnya proses fotosintesis.
Gambar 3.5.UV-Visible Spectrophotometer Lambda 25
3.3.4 KarakterisasiI-VLarutan Klorofil
KarakterisasiI-VLarutan klorofil dilakukan dengan metodetwo point probe
menggunakan alat Elkahfi 100 I-V Meter. Sampel larutan klorofil Sp1, Sp2, dan
Sp3diukur dalam kondisi gelap dan terang untuk mendapatkan data respon sampel
terhadap cahaya. Tahapan pengukuran yang dilakukan adalah sebagai berikut :
a. Elkahfi 100 I-V Meterdinyalakan dengan menghubungkan kontak daya
alat padastavoltyang sudah terhubung dengan sumber tegangan.
b. Elkahfi 100 I-V Meterdihubungkan dengan PC melalui sambungan kabel
USB ke Serial RS232.
c. AplikasiElkahfi 100 I-V Meterdijalankan pada komputer.
d. Kabel untuk mengukur sampel disambung pada port current in dan
voltage outyang ada pada panel antarmuka alat.
e. Kabel dari port current in dan voltage out dihubungkan. Kabel merah
dihubungkan ke kedua elektroda sampel, sedangkan kabel hitam saling
dihubungkan.
f. Program pengukuran pada aplikasi alat yang sudah dijalankan di komputer
dijalankan dengan memilih setting untuk menentukan port yang
digunakan, memilih view kemudian I-V Characteristic dan pilih I-V
Measurement.
g. Data hasil pengukuran disimpan dengan memilihsave as.
h. Langkah a sampai f diulangi dengan perlakuan sampel diberi cahaya dan
pada kondisi gelap.
Gambar 3.6.Elkahfi 100 I-V Meter
3.3.5 Preparasi Elektroda Kerja
Elektroda kerja dibuat pada kaca konduktif FTO yang di atasnya
dideposisikan semikonduktor anorganik TiO2rutile. Semikonduktor tersebut akan
diendapkan di atas kaca konduktif FTO dengan metode slipcasting. Sebelumnya
terlebih dahulu dibuat pasta TiO2. Dalam pembuatan pasta TiO2 dibutuhkan
bubuk TiO2 sebanyak 3,5gr dan etanol 95% sebanyak 14ml lalu di aduk dengan
Hot Plate IKAR C-MAG HS7 dengan kecepatan 300 rpm selama 30 menit dan
menggunakan magnetic stirrer. Setelah pasta TiO2 siap, dilakukan langkah –
langkah sebagai berikut :
1. Pada kaca FTO, sebelum dilakukan deposisi TiO2 terlebih dahulu dicari
bagian yang bersifat konduktif.
2. Pada kaca konduktif FTO ukuran 2cm x 5cm dibentuk area pendeposisi
TiO2dengan ukuran 1cm x 2cm. Sisi FTO ditempel dengan selotip sebagai
pembatas.
3. Pasta TiO2yang telah disiapkan sebelumnya, diletakkan di atas permukaan
kaca FTO yang tidak berselotip, kemudian pasta tersebut diratakan secara
halus dengan spatula. Ketebalan lapisan TiO2 yang dideposisi sesuai
dengan tebal selotip yang digunakan.
4. Setelah deposisi, selotip diangkat secara perlahan dan lapisan dibiarkan
pada suhu ruang agar mengering. Agar deposisi TiO2 menjadi lebih baik,
elektroda ini di sintering pada temperatur 150°C selama 10 menit dengan
Hot Plate IKARC-MAG HS7. Kemudian didinginkan hingga mencapai suhu
kamar. Elektroda yang dibuat sebanyak 3 sampel, masing – masing untuk
variasidyeSp1, Sp2, dan Sp3.
3.3.6 Preparasi Larutan Elektrolit
Larutan Elektrolit yang digunakan dalam penelitian ini adalah pasangan
redoksIodinedanTriiodide.
Gambar 3.7. Larutan Elektrolit
3.3.7 Preparasi Elektroda Lawan
Elektroda lawan untuk DSSC dapat dibuat dari kaca konduktif yang
diatasnya dilapisi karbon (C) karena mudah dan biayanya yang murah. Fungsi
karbon sebagai katalis untuk mempercepat reaksi pada DSSC. Karbon yang
digunakan berasal dari grafit pensil kayu. Sama seperti pada pembuatan elektroda
kerja, pada pembuatan elektroda lawan, terlebih dahulu mencari bagian kaca FTO
yang konduktif, lalu dibuat ukuran 1 cm x 2 cm, setelah itu dibuat lapisan karbon
dengan pensil grafit kayu.
3.3.8 Perangkaian DSSC
Setelah semua komponen siap, kemudian dilakukan perangkaian DSSC
yaitu elektroda kerja yang sudah disiapkan direndam dalam ekstrak dye klorofil
Spirulina sp masing – masing pada Sp1, Sp2, dan Sp3 selama 24 jam. Setelah
elektroda kerja siap, kemudian ditetesi elektrolit. Selanjutnya elektroda lawan
diletakkan di atas elektroda kerja dengan struktur berlapis (sandwich) lalu dijepit
dengan binder klip setelah itu DSSC siap untuk diuji.
Gambar 3.8. Perangkaian DSSC dengan Struktur Berlapis (sandwich)
3.3.9 Pengujian KarakteristikI-VDSSC
Pengujian karakteristikI-V fraksi klorofil dengan struktur DSSC dilakukan
saat kondisi gelap dan terang. Hal ini akan menunjukkan ada tidaknya sifat
fotokonduktivitas DSSC. Pada kondisi terang menggunakan pencahayaan dari
lampu OHP (Over Head Projector) dengan intensitas sebesar 1235 Watt/m2,
sedangkan untuk kondisi gelap ditutup dengan kotak penutup. Pengukuran
intensitas cahaya dilakukan dengan Solar Power Meter 1333R dan pengujian
dilakukan dengan menggunakan Keithley 2602Ayang ditunjukkan pada Gambar
3.9.
Gambar 3.9.Solar Power Meter 1333RdanKeithley 2602A
29
BAB IV
HASIL DAN PEMBAHASAN
Penelitian terhadap pengaruh fraksi klorofil Spirulina sp terhadap sifat listrik
dengan struktur DSSC telah dilakukan. Penelitian ini meliputi isolasi dye klorofil
dari ekstrakSpirulina sp, pengujian karakteristik sifat optik dan sifat listrik pada dye
klorofil hasil kromatografi, pembuatan elektroda kerja dengan deposisi TiO2 di atas
kaca FTO dengan metode slipcasting dan tahap pemanasan dengan hot plate serta
pengujian karakteristik dari TiO2, pembuatan elektroda lawan dengan menggosokkan
grafit pensil kayu, perangkaian DSSC, dan pengukuran sifat listrik DSSC.
4.1. IsolasiDyeKlorofil
Proses ekstraksi padaSpirulina sp menunjukkan hasil ekstraksi berupa larutan
berwarna hijau pekat ditunjukkan pada Gambar 4.1. Warna hijau pekat hasil
ekstraksi memenuhi syarat bahwa Spirulina sp mampu menjadi zat pewarna (dye)
klorofil.
Gambar 4.1. Larutan Hasil Ekstraksi
Selanjutnya untuk hasil kromatografi dari penelitian ini didapatkan 3 larutan
dye ditunjukkan pada Gambar 4.2. Larutan klorofil yang keluar lebih dulu dan
berwarna hijau pekat ditandai dengan label Sp1. Larutan dengan warna hijau yang
lebih cerah ditandai dengan label Sp2 dan larutan yang keluar setelahnya ditandai
dengan label Sp3dengan warna hijau kekuning – kuningan.
Sp1 Sp2 Sp3
Gambar 4.2. Perbedaan Warna Hasil Kromatografi
4.2. Karakterisasi Optik dan Karakteristik I-V Dye Spirulina sp
4.2.1. Karakteristik Optik
Hasil absorbansi ketiga sampel klorofil Sp1, Sp2, dan Sp3 dari hasil isolasi
Spirulina sp ditunjukkan pada Gambar 4.3
4 0 0 4 5 0 5 0 0 5 5 0 6 0 0 6 5 0 7 0 0 7 5 0 8 0 0
Gambar 4.3. Grafik absorbansi larutan klorofilSpirulina spuntuk Sp1, Sp2, Sp3
Gambar 4.3 memperlihatkan grafik absorbansi larutan Spirulina sp pada ketiga
sampel Sp1, Sp2, dan Sp3 sebagai fungsi dari panjang gelombang (nm) yang diukur
dari panjang gelombang 400 nm hingga 800 nm. Hasil pengujian tersebut
memperlihatkan bahwa puncak absorbsi Sp1, Sp2, dan Sp3terjadi pada interval λ yang
sama yaitu 400-450nm yang merupakan puncak klorofil a. Puncak kedua muncul
pada interval 600-625nm, karakteristik absorbansi yang ditunjukkan pada puncak
kedua merupakan klorofil b. Selanjutnya pada rentang panjang gelombang
650-700nm muncul puncak yang merupakan karakteristik puncak klorofil a. Karakteristik
puncak - puncak hasil eksperimen menunjukkan konsistensi terhadap spektrum
absorbansi klorofil sesuai referensi pada Gambar 2.5
Tabel 4.1. Nilai Puncak Absorbansi Larutan Klorofil
Sampel Warna Panjang
Gelombang
(nm)
Absorbansi
SP1 Hijau pekat 664 1,26958
647 0,34449
SP2 Hijau muda 664 1,16946
667 0,20771
SP3 Hijau
kekuning-kuningan
664 0,72854
667 0,11497
Pada Gambar 4.3 dan Tabel 4.1 dapat diamati dengan jelas puncak absorbansi
yang terbentuk. Sp1 diserap pada panjang gelombang λ= 664 nm dengan nilai
absorbansi sebesar 1,26958 dan pada panjang gelombang λ= 647 nm dengan nilai
absorbansi sebesar 0,34449, untuk Sp2diserap pada panjang gelombang λ= 664 nm
dengan nilai absorbansi sebesar 1,16946 dan pada panjang gelombang λ= 667 nm
dengan nilai absorbansi sebesar 0,20771 dan Sp3 pada panjang gelombang λ= 664
nm dengan nilai absorbansi sebesar 1,26958 dan pada panjang gelombang λ= 667
nm dengan nilai absorbansi sebesar 0,11497. Keseluruhan tipe puncak absorbansi
sampel tersebut melemah dari Sp1hingga Sp3.
Pada Sp3 terjadi puncak absorbansi lebih rendah dari pada Sp1 dan Sp2. Pada
sampel ini menunjukkan kemampuan absorbansi yang lebih rendah dibanding Sp1
dan Sp2. Penurunan kemampuan absorbansi pada sampel ini dikarenakan kadar
klorofil Sp3 lebih rendah dibanding Sp1 dan Sp2. Meskipun kemampuan
mengabsorbsinya rendah namun pada sampel ini muncul konsistensi yakni dua
puncak pada spektrum absorbansinya. Sedangkan pada Sp2 dan Sp3 terjadi puncak
absorbansi dengan selisih yang sangat kecil, ini berarti kemampuan Sp1 dan Sp2
dalam mengabsorbsi juga memiliki selisih yang kecil.
4.2.2. Kandungan Klorofil Spirulina sp
Dari perhitungan menggunakan rumus dari Persamaan (2.4) serta hasil kurva
absorbansi maka diperoleh nilai kandungan klorofil masing-masing sampel secara
kuantitatif dapat dihitung pada Tabel 4.2
Tabel 4.2 Kandungan Klorofil masing-masing FraksiSpirulina sp.
Sampel Klorofil a (mg/L) Klorofil b (mg/L)
Sp1 15,545 0,756
Sp2 13,793 0,671
Sp3 8,62 0,419
Tinggi puncak absorbansi berhubungan dengan kandungan klorofil yang
terlarut. Dari Tabel, untuk Sp1 diperoleh klorofil a sebesar 15,545 mg/L dan klorofil
b=0,756mg/L, sedangkan Sp2 diperoleh klorofil a sebesar 13,793mg/L dan klorofil
b=0,671mg/L, dan Sp3 kandungan klorofil a yg diperoleh sebesar 8,62 mg/L dan
klorofil b=0,419 mg/L.
Nilai absorbansi molekul klorofil akan mempengaruhi jumlah kandungan
klorofil masing-masing sampel. Dari Tabel 4.2 di atas dapat diketahui bahwa Sp1
memiliki kandungan klorofil yang paling banyak sehingga Sp1memiliki kemampuan
menyerap energi foton lebih baik daripada Sp2 dan Sp3. Sampel yang memiliki
kandungan klorofil optimum berarti memiliki jumlah molekul penyerap foton
maksimal. Energi foton tersebut dapat dikonversi menjadi energi listrik pada aplikasi
sel surya. Kandungan klorofil a dan b pada Sp1 tidak begitu jauh dengan kandungan
klorofil a dan b pada Sp2, hal ini dikarenakan pada Sp1 dan Sp2 tersebut memiliki
tinggi puncak absorbansi dengan selisih yang kecil juga sperti dibahas pada Tabel
4.1.
4.2.3. KarakterisasiI-VLarutan KlorofilSpirulina Sp
Perbedaan kemampuan larutan klorofil dalam mengabsorbsi cahaya
mempengaruhi kemampuannya dalam mengalirkan elektron. Hal ini ditunjukkan pada
hasil pengujian I-V larutan. Pada pengukuran sifat listrik larutan klorofil untuk Sp1,
Sp2, dan Sp3 diperolah hasil seperti pada Gambar 4.4 pada kondisi terang.
Kemampuan absorbansi paling tinggi yang dimiliki sampel Sp1, menunjukkan hal
yang sama pada kemampuan Sp1 dalam menghasilkan arus. Perbandingan antar
sampel menunjukkan kemampuan sampel dalam mengalirkan arus. Dari hasil kurva
menunjukkan Sp1 menghasilkan arus yang paling tinggi dari pada sampel yang lain.
Hal ini menunjukkan bahwa fraksi klorofil terlarut menentukan konduktivitas larutan.
Pada saat diberi cahaya arus meningkat perlahan. Perbandingan antara pengujian
setiap sampel adalah pada Sp3 kurva cenderung linier dan menghasilkan arus yang
kecil dibanding sampel lainnya. Pengujian sifat listrik larutan ketiga sampel
menunjukkan bahwa pada kondisi gelap arus naik secara perlahan namun cenderung
konstan yakni pada saat tegangan 0 - 9V.
0 1 2 3 4 5 6 7 8 9 10 0.00E+000
5.00E-009 1.00E-008 1.50E-008 2.00E-008 2.50E-008
Sp 1 Sp2 Sp
3
A
rus
(A
m
per
e)
Tegangan(Volt)
Gambar 4.4. Grafik karakterisasiI-V dyeSp1, Sp2, dan Sp3pada kondisi terang
Selanjutnya hasil pengukuran pada kondisi gelap ditunjukkan pada Gambar 4.5.
Gambar 4.5 merupakan perbandingan setiap sampel pada kondisi gelap. Teramati
dengan jelas karakteristik peningkatan arus secara linier dilanjutkan eksponensial
ketika tegangan dinaikkan. Arus yang muncul pada kondisi gelap pada sampel Sp3
lebih kecil dibandingkan dengan sampel Sp2 dan Sp3. Hasil ini mengidentifikasikan
bahwa klorofil berperan sebagai fotosensitizersehingga terdapat arus. Pengujian sifat
listrik larutan ketiga sampel menunjukkan bahwa pada kondisi gelap arus naik secara
perlahan namun cenderung konstan yakni pada saat tegangan 0-9V.
0 1 2 3 4 5 6 7 8 9 10
Gambar 4.5. Grafik karakterisasiI-Vpada Sp1, Sp2, dan Sp3pada kondisi gelap
Perbedaan kemampuan larutan klorofil dalam mengabsorbsi cahaya pada
kondisi gelap dan terang mempengaruhi kemampuannya dalam mengalirkan
elektron. Hal ini ditunjukkan pada hasil pengujian I-V larutan. Pada Gambar 4.4. dan
Gambar 4.5 menunjukkan karakteristik tegangan dan arus yang lebih tinggi pada
keadaan terang dibandingkan dalam keadaan gelap.
Pengukuran sifat listrik menunjukkan hasil yang berbeda saat di ukur pada
keadaan gelap dan terang. Karakteristik ini menunjukkan sifat fotosensitizer klorofil
sebagaidyepada DSSC (Sumaryanti, 2011)
Tabel 4.3 menunjukkan peningkatan nilai konduktivitas larutan klorofil dari mulai
Sp3, Sp2, dan Sp1. Semakin pekat suatu larutan klorofil mengindikasikan semakin
banyak jumlah klorofil terdeposit. Jumlah klorofil terdeposit sebanding dengan
peningkatan kemampuan absorbsi larutan klorofil. Kemampuan absorbsi klorofil
yang semakin meningkat menyebabkan banyaknya pembawa muatan tereksitasi.
Eksitasi terjadi karena pembawa muatan memperoleh tambahan energi dari cahaya.
4.3. Pengukuran Sifat Listrik Fraksi Klorofil Spirulina sp dengan Struktur
DSSC
Hasil perangkaian DSSC dengan sistem struktur berlapis (sandwich) dengan
susunan FTO/TiO2/dye/elektrolit/FTO. TiO2 yang dipakai pada rangkaian DSSC
berstruktur rutile sesuai dengan hasil XRDyang terdapat pada lampiran 3.Dye yang
digunakan merupakan variasi dari ketiga fraksi klorofil yaitu Sp1, Sp2, dan Sp3.
Sehingga menghasilkan 3 buah DSSC, selanjutnya pada ketiga DSSC yang dibuat
dilakukan uji karakterisasiI-Vpada kondisi gelap dan terang dengan Keithley 2602A.
Pada kondisi gelap yaitu dengan cara DSSC ditutup dengan kotak penutup,
sedangkan pada kondisi terang dilakukan dengan penyinaran OHP dengan intensitas
1235 Watt/m2seperti pada Gambar 4.6.
Gambar 4.6. Pengukuran DSSC pada Kondisi Terang
Pada Gambar 4.7, 4.8, dan 4.9 ditunjukkan hasil pengukuran arus yang diberi
tegangan antara 0-2Volt. Kemampuan menghasilkan arus pada kondisi terang
menunjukkan peningkatan dibanding arus yang dihasilkan pada keadaan gelap.
Gambar 4.7 Grafik Karakterisasi I-VDSSC denganDyeSp1
Gambar 4.8 Grafik Karakterisasi I-VDSSC denganDyeSp2 -1.00E-04
tegangan antara 0-2Volt. Kemampuan menghasilkan arus pada kondisi terang
menunjukkan peningkatan dibanding arus yang dihasilkan pada keadaan gelap.
Gambar 4.7 Grafik Karakterisasi I-VDSSC denganDyeSp1
Gambar 4.8 Grafik Karakterisasi I-VDSSC denganDyeSp2 -1.00E-04
tegangan antara 0-2Volt. Kemampuan menghasilkan arus pada kondisi terang
menunjukkan peningkatan dibanding arus yang dihasilkan pada keadaan gelap.
Gambar 4.7 Grafik Karakterisasi I-VDSSC denganDyeSp1
Gambar 4.8 Grafik Karakterisasi I-VDSSC denganDyeSp2