Konstruksi Diagram Potensial-pH untuk Baja Karbon dalam Buffer
Asetat secara Potensiodinamik Eksperimental
Bunbun Bundjali, N.M. Surdia, Oei Ban Liang, Bambang Ariwahjoedi
Departemen Kimia-FMIPA ITB
Diterima Maret 2004, disetujui untuk dipublikasikan Nopember 2004
Abstrak
Diagram Potensial-pH, atau diagram Pourbaix, sistem Fe-H2O pada umumnya dikonstruksi dari hasil perhitungan
berdasarkan data termodinamika. Pada pekerjaan ini diagram tersebut dikonstruksi berdasarkan hasil pengukuran potensiodinamik pada sistem baja karbon dalam larutan buffer asam asetat-ion asetat pada rentang suhu 25-85 0C. Walaupun diagram yang diperoleh tidak selebar cakupan pH berdasarkan data termodinamika, karena terbatasi oleh trayek pH larutan buffer asetat, namun lebih dapat dipergunakan untuk pembahasan korosi baja karbon dalam lingkungan asam asetat-ion asetat pada rentang suhu tersebut. Selain itu dapat diperoleh pula persamaan-persamaan yang mengkaitkan pengaruh pH dan suhu terhadap nilai potensial pasif primer (Epp) dan potensial
Fladge (EF).
Kata kunci: diagram potensial-pH, potensiodinamik, potensial pasif primer, potensial Fladge. Abstract
The pH-potential, or the so called Pourbaix, diagram for the system Fe - H2O is normally been constructed by using
thermodynamic data. In this work the diagram was constructed experimentally based on potentiodynamic measurements of carbon steel in acetic acid - acetate ion buffer solutions at a temperature range of 25-85 0C. Due to the limited pH trajectory of buffer acetate solutions the resulted diagrams were not as wide pH as those of thermodynamic Pourbaix diagrams, but they are more useful for analysing carbon steel corrosion in acetate environment systems at that temperature range. In Addition the effects of pH and temperature on the primary passive potential (Epp) and Fladge potential (EF) relationship could also be obtained.
Keywords: potential-pH diagram, potentiodynamic, primary passive potential, Fladge potential. 1. Pendahuluan
Diagram potensial-pH atau diagram Pourbaix1) memetakan fasa-fasa stabil logam dan senyawanya dalam larutan dengan pelarut air, yang berada dalam kesetimbangan termodinamika, sebagai fungsi dari potensial elektroda dan pH larutan. Dalam diagram potensial pH untuk besi terdapat zona korosi, yaitu daerah reaksi pelarutan besi yang terletak dalam daerah asam dan di daerah
sempit pada kondisi sangat basa; zona pasif, yaitu daerah terbentuknya selaput tak larut di permukaan logam yang menghalangi proses korosi lebih lanjut; dan zona kebal, yaitu daerah yang secara termodinamika keadaan sebagai logam adalah fasa paling stabil. Gambar 1 memperlihatkan diagram Pourbaix sederhana untuk besi pada keadaan standar pada suhu 25 0C. Korosi Pasifasi Kebal Korosi pH -1 0 1 2 E ( V )
Gambar 1. Diagram Pourbaix sederhana untuk besi dengan batas-batas pada keaktifan 10-6 ekivalen L-1
10 102 103 104 -0,6 -0,4 -0,2 0,0 0,2 0,4 0,6 0,8 1,0 1,2 1,4
Rapat arus (µA/cm2)
Po te ns ia l (Vo lt v s SCE )
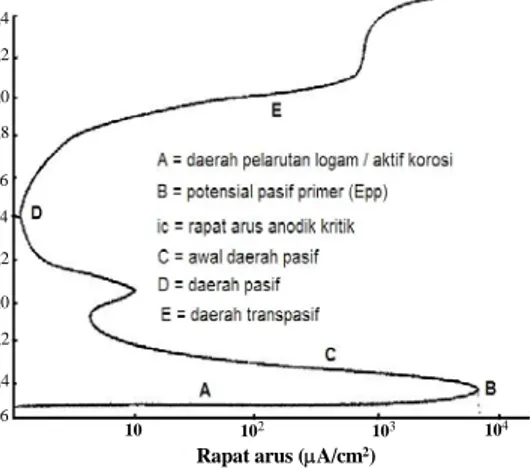
Gambar 2. Kurva tipikal polarisasi anodik potensio-dinamik dari suatu baja nirkarat.
Kegunaan diagram Pourbaix2,3,4) terutama adalah untuk memperkirakan arah reaksi spontan; komposisi produk korosi; dan perubahan lingkungan yang akan mencegah atau menurunkan laju serangan korosi. Dengan menggunakan data termodinamika terpilih yang sesuai dan pemodelan yang tepat, diagram potensial pH untuk sistem Fe-H2O masih
terus direvisi5) dan sudah dibuat sampai suhu 300 0C. Walaupun sudah ada usaha membuat diagram potensial pH untuk sistem aliasi logam Zn-larutan 3% NaCl (tidak pada keadaan standar) secara eksperimen polarisasi terapan6), namun belum ada yang mengkonstruksi diagram potensial pH untuk sistem Fe-H2O berdasarkan hasil eksperimen
potensiodinamik. Proses korosi dalam larutan dengan pelarut air adalah proses elektrokimia, karenanya dapat diikuti dengan pengukuran polarisasi potensiodinamik, yaitu salah satu teknik mengkarakterisasi kelakuan korosi suatu sampel logam dari kaitan antara arus dengan potensial di bawah kondisi terkontrol. Karakteristik polarisasi sampel logam diukur dengan mengalurkan respons arus sebagai fungsi dari potensial terapan.
Gambar 2 memperlihatkan kurva tipikal polarisasi anodik potensiodinamik dari suatu baja nirkarat7). Pada gambar tersebut daerah A adalah daerah aktif korosi, yaitu daerah potensial pH yang menyebabkan logam mengalami korosi, dengan meningkatnya potensial terapan ke arah positif. Pada titik B laju korosi seolah-olah berhenti, rapat arus anodik tidak bertambah dengan naiknya potensial terapan, yang diartikan mulai terbentuknya pasifasi. Pasifasi dapat didefinisikan sebagai hilangnya kereaktifan kimiawi logam di bawah suatu kondisi lingkungan tertentu, akibat terbentuknya suatu selaput pelindung. Titik B dicirikan oleh dua nilai koordinat, potensial pasif primer (Epp ) dan rapat arus
kritis (ic). Pada daerah C, rapat arus berkurang
dengan cepat sejalan dengan meningkatnya perlindungan selaput pasifasi. Di daerah D terdapat kondisi dengan rapat arus pertukaran minimum terhadap kenaikan potensial. Dalam daerah E terjadi perusakan selaput pasif akibat penerapan potensial yang sangat positif, ditunjukkan oleh peningkatan kembali laju korosi, daerah ini dikenal sebagai daerah transpasif.
Potensial awal terjadinya peralihan dari keadaan pasif kembali ke aktif korosi dikenal sebagai potensial Fladge (EF). Baik potensial pasif primer
maupun potensial Fladge, keduanya dipengaruhi oleh pH larutan, yang diungkapkan oleh persamaan berikut8,9) : Epp = - 0,059 pH 1) 0 pp
E
dan EF = 0 FE
- 0,059 pH 2) dengan dan , berturut-turut, menyatakan potensial pasif primer dan potensial Fladge pada pH = 0.0 pp
E EF0
Untuk mengkaji korosi baja karbon dalam lingkungan asam asetat-ion asetat, pada pekerjaan ini diagram potensial-pH baja karbon (besi)-larutan buffer asam asetat-ion asetat disusun berdasarkan data potensiodinamik secara eksperimen. Kelebihan dari pemetaan ini adalah dapat diperoleh gambaran eksperimental mengenai karakteristik elektrokimiawi suatu baja karbon dalam lingkungan larutan asam asetat-ion asetat. Peta ini memberikan informasi penting dalam membahas kelakuan korosi dan terjadinya pasifasi pada sistem terkait, karena proses korosi seringkali terjadi dalam keadaan tidak setimbang dan pada kondisi tidak standar. Namun pada pemetaan ini, diagram potensial-pH tidak dapat mencakup seluruh daerah pH, karena terbatasi oleh trayek rentang pH sistem buffer. Walaupun demikian, rentang pH 3,22-9,03 adalah salah satu daerah pH penting dalam kajian korosi baja karbon, karena daerah itu meliput sebagian besar daerah peralihan korosi aktif ke keadaan pasif.
2. Cara Kerja
Bahan dan larutan uji
Baja karbon SC 38 (komposisi kimia rata-rata dalam % berat selain Fe adalah C 0,38; Si 0,27; S 0,25; P 0,02 dan Mn 0,76) sebagai elektroda kerja dengan luas permukaan 0,95 cm2. Pada saat akan digunakan untuk pengukuran elektrokimia permukaan, elektroda kerja dipoles basah dengan ampelas silicon karbida (SiC) 800 grit, dicuci dengan aqua DM dan aseton. Larutan uji dibuat dengan melarutkan-padatan kristal natrium asetat (p.a), dan asam asetat dari cairan asam asetat pekat 98 % (p.a) - dalam aqua DM yang telah dimurnikan melalui alat pemurnian air buatan Barnstead (air hasil pemurnian berdaya hantar ~ 1,5 µS/cm dan pH = 5,80 + 0,20). Larutan uji berupa larutan buffer asam asetat-ion asetat pada rentang pH 3,22 s/d 8,52-dibuat dengan memvariasikan perbandingan [HAc]/[NaAc]-dalam [NaAc] tetap 0,2 M, dan larutan 0,2 M natrium asetat (pH 9,03) agar berdaya hantar sama, sekitar 12 mS/cm.
Pengukuran elektrokimia
Semua pengukuran potensiodinamik ini dilakukan dalam sel elektrokimia tiga elektroda, menggunakan Potensiostat/Galvanostat VoltaLab 40, PGZ 402 Radiometer dengan perangkat lunak Volta Master 4. Elektroda kerja dibuat dari batang baja karbon berbentuk silinder yang disekat dengan politetrafluoroetilen dan perekat Araldite sehingga memiliki luas permukaan kontak dengan larutan uji sebesar 0,95 cm2. Elektroda kalomel jenuh (SCE) digunakan sebagai elektroda referensi dan elektroda platina digunakan sebagai elektroda bantu (luas permukaan kontak 0,78 dan 1,43 cm2). Daerah permukaan sentuh elektroda/larutan dari elektroda kerja dan elektroda bantu disusun saling berhadapan berjarak 3 mm satu sama lain. Sebanyak 100 mL larutan uji ditempatkan dalam sel elektrokimia yang
terbuat dari gelas berdinding rangkap dan berfungsi sebagai ruang mantel aliran air pengatur suhu larutan, diaduk dengan batang pengaduk magnetik. Pengukuran dilakukan pada suhu-suhu larutan uji 25, 45, 65, dan 85 ± 1 o
C. Pemindaian (scanning) secara potensiodinamik dilakukan dengan teknik Linear
Potential V, pada rentang potensial dari 1200 mV
sampai dengan 1800 mV dan laju sapuan potensial 2 mV s-1.
3. Hasil dan pembahasan
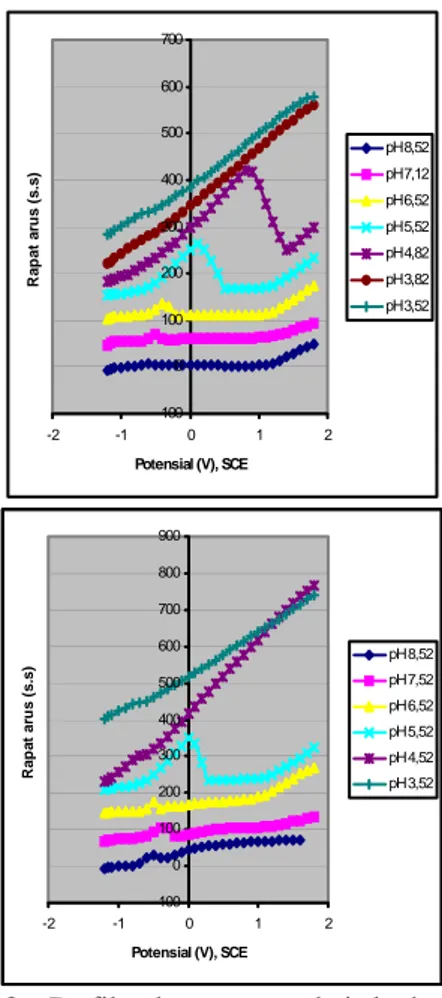
Profil Voltammogram baja karbon dalam larutan buffer asam asetat-ion asetat pada berbagai pH pada suhu 25, 45, 65 dan 85 0C, yang diperoleh secara potensiodinamik ditampilkan berturut-turut pada Gambar 3 (a), (b), (c) dan (d). Dari gambar tersebut tampak bahwa larutan buffer yang lebih asam lebih sukar membentuk lapisan selaput pasif. Pembentukan selaput pasif dipermudah dan diperlebar rentang potensialnya dengan kenaikan pH. Peningkatan suhu menyebabkan awal terbentuknya selaput pasif bergeser ke pH yang lebih tinggi. Voltammogram potensiodinamik baja karbon dalam setiap pH larutan buffer, dianalisis untuk menentukan masing-masing nilai potensial pasif primer (Epp),
potensial Fladge (EF), potensial transpasif (Etp), dan
potensial korosi, Ecorr
-50 0 50 100 150 200 250 300 -2 -1 0 1 2 Potensial (V), SCE R a pa t a rus ( s .s ) pH 8,52 pH 7,52 pH 6,52 pH 5,52 pH 4,52 pH 3,82 (a) -50 0 50 100 150 200 250 300 350 -2 -1 0 1 2 Potensial (V), SCE R a pa t a rus (s .s ) pH 8,52 pH 7,82 pH 6,82 pH 5,52 pH 4,82 pH 3,82 (b) -100 0 100 200 300 400 500 600 700 -2 -1 0 1 2 Potensial (V), SCE R a pa t a rus (s .s ) pH 8,52 pH 7,12 pH 6,52 pH 5,52 pH 4,82 pH 3,82 pH 3,52 (c) -100 0 100 200 300 400 500 600 700 800 900 -2 -1 0 1 2 Potensial (V), SCE R a pa t a rus (s .s ) pH 8,52 pH 7,52 pH 6,52 pH 5,52 pH 4,52 pH 3,52 (d)
Gambar 3. Profil voltammogram baja karbon pada berbagai pH larutan buffer asetat, pada (a) 25oC, (b) 45oC, (c) 65oC, dan (d) 85oC. Skala pada ordinat hanya untuk pembandingan, bukan nilai sebenarnya.
-20 0 20 40 60 80 100 120 140 -1.6 -0.8 0 0.8 1.6 Potensial (V), SCE R a pa t a rus ( m A /c m 2) 25 C 45 C 65 C 85 C Ecorr Epp EF Etp
Gambar 4. Pembandingan voltammogram baja
karbon dalam buffer asam asetat pH 5,52 pada suhu 25, 45, 65, dan 85oC.
Gambar 4 merupakan voltammogram baja karbon dalam larutan buffer asetat pH 5,52 pada suhu 25, 45, 65 dan 85 0C, dan ditunjukkan titik posisi Ecorr, Epp, EF, dan Etp untuk voltammogram pada suhu
850C. Diagram potential-pH pada masing-masing suhu di atas, dikonstruksi dengan mengalurkan pH v/s. potential. Selanjutnya ditarik garis yang menghubungkan nilai-nilai Ecorr, garis yang
menghubungkan nilai-nilai EF dan garis yang
menghubungkan nilai-nilai Etp, kemudian garis-garis
itu diproyeksikan pada bidang dengan kerapatan arus anodik nol. Penentuan zona kebal, zona aktif korosi, dan zona pasif pada diagram tersebut, berturut-turut, adalah daerah voltammogram dengan rapat arus anodik bernilai negatif, daerah antara Ecorr dan Epp,
dan daerah yang berada di antara EF dan Etp. Dengan
cara ini, diagram potensial-pH pada suhu 25, 45, 65, dan 850C dapat dikonstruksi seperti terlukiskan pada Gambar 4 (a) s/d (d). Zona pasif pada diagram tersebut, lebih merepresentasikan daerah potensial- pH dengan laju korosi lambat akibat terbentuknya selaput pelindung pada permukaan logam. Potensial Fladge (EF) adalah nilai potensial pada daerah pasif
dengan laju korosi minimum, yaitu kondisi yang memberikan perlindungan selaput pasif maksimum.
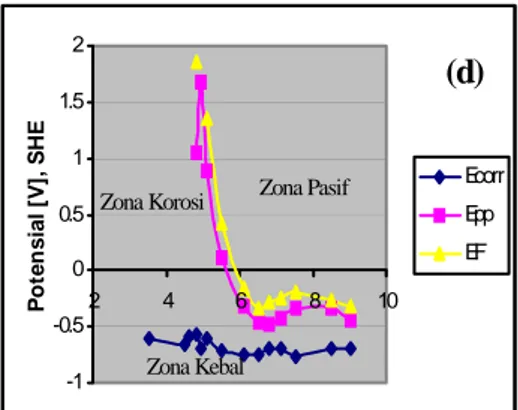
-1 -0.5 0 0.5 1 1.5 2 2 4 6 8 10 pH P o te n s ia l [ V ], S H E Ecorr Epp EF Etp Zona Kebal Zona Korosi Zona Pasif (a) -1 -0.5 0 0.5 1 1.5 2 2 4 6 8 10 pH P o te n s ia l [V ], S H E Ecorr Epp EF Etp Zona Kebal Zona korosi Zona Pasif (b) -1 -0.5 0 0.5 1 1.5 2 2.5 2 4 6 8 10 pH P o te n s ia l ( V ), S H E Ecorr Epp EF Etp Zona Kebal Zona Korosi Zona Pasif (c) -1 -0.5 0 0.5 1 1.5 2 2 4 6 8 10 pH P o te ns ia l [V ], S H E Ecorr Epp EF Zona Kebal
Zona Korosi Zona Pasif
(d)
Gambar 5. Diagram potensial-pH baja karbon dalam larutan buffer asam asetat – natrium asetat pada suhu (a) 250C, (b) 450C, (c) 650C dan (d) 85oC.
Gambar 5 memperlihatkan diagram potensial-pH yang dihasilkan dari eksperimen potensiodinamik ini. EHS (supaya dapat dibandingkan dengan diagram Pourbaix). Skala potensial disesuaikan menjadi potensial terhadap elektroda standar hidrogen. Diagram potensial-pH pada Gambar 5 (a) dengan Gambar 1, pada daerah pH dan suhu yang sama, mempunyai kemiripan bentuk kurva. Suhu berpengaruh terhadap profil kurva diagram potensial-pH, terutama pada 65 0C dan 85 0C pada pH > 6,52. Baik pada garis kurva Epp
maupun pada EF terdapat kecenderungan titik belok
yang melengkung ke potensial yang lebih tinggi, karenanya pada suhu tersebut, persamaan garis linier hanya dapat ditarik sampai pH 6,52. Pengaruh pH larutan terhadap sebaran nilai Epp dan EF pada
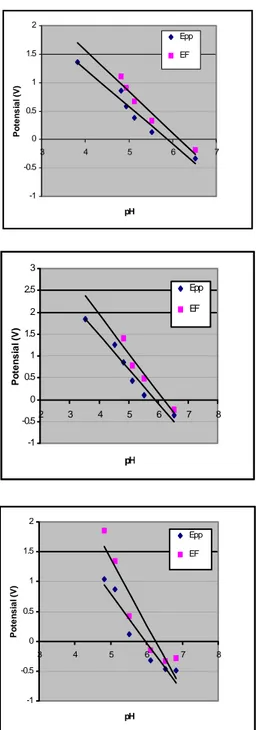
rentang suhu 25 s/d 850C, untuk pH < 7, diperoleh dengan penarikan garis regresi sebagai dilukiskan pada Gambar 6, menghasilkan ungkapan Epp dan EF
terhadap pH, yang dirangkumkan pada Tabel 1.
-0.6 -0.4 -0.2 0 0.2 0.4 0.6 0.8 1 1.2 1.4 1.6 3 4 5 6 7 8 pH Po te n s ia l ( V ) Epp EF (a)
-1 -0.5 0 0.5 1 1.5 2 3 4 5 6 7 pH P o te n s ia l ( V ) Epp EF (b) -1 -0.5 0 0.5 1 1.5 2 2.5 3 2 3 4 5 6 7 8 pH P o te ns ia l ( V ) Epp EF (c) -1 -0.5 0 0.5 1 1.5 2 3 4 5 6 7 8 pH Po te n s ia l (V ) Epp EF
(d)
Gambar 6. Pengaruh pH larutan buffer asam asetat – natrium asetat terhadap Epp dan EF pada suhu (a)
250C, (b) 450C, (c) 650C dan (d) 85oC.
Tabel 1. Ungkapan pengaruh pH terhadap Epp dan EF
pada 25, 45, 65 and 85oC
Suhu
(oC) Kaitan E (V, SCE) pp dengan pH Kaitan E (V, SCE) F dengan pH
25 45 65 85 Epp = 2,242-0,397 pH Epp = 3,181-0,517 pH Epp = 4,61-0,783 pH Epp = 4,904-0,821 pH EF = 2,993-0,506 pH EF = 4,466-0,724 pH EF = 5,527-0,895 pH EF = 6,908-1,105 pH
Persamaan di atas menyatakan bahwa baik
Epp maupun EF, bertambah dengan naiknya suhu dan
berkurang dengan naiknya pH. Hal ini memberi petunjuk bahwa proses pembentukan selaput pasif baja karbon dalam lingkungan asam asetat – ion asetat bersifat eksoterm, dan lebih mudah terbentuk pada pH yang lebih tinggi. Pengaruh suhu (τ0
C), terhadap potensial
E
0pp danE
F0, potensial pasif primer dan potensial Fladge pada pH = 0 (ekstrapolasi hipotetik), ditunjukkan pada Gambar 7, dapat diungkapkan dengan persamaan sebagai berikut:0
pp
E
= 1,143 + 0,0471 τ 3) danE
F0 = 1,452 + 0,064 τ 4)Perbedaan yang tampak antara persamaan (1) dan (2) dengan ungkapan yang diperoleh pada Tabel 1, kemungkinan besar bersumber dari perbedaan jenis selaput pasif yang terbentuk, dan keaktifan ion-ion yang terlibat dalam sistem ini dengan yang diandaikan pada penurunan persamaan secara teoritik tersebut.
0 1 2 3 4 5 6 7 8 0 20 40 60 80 100 Suhu (0 C) Po te n s ia l ( V ) Epp EF
Gambar 7. Pengaruh suhu terhadap Epp dan EF baja
karbon dalam buffer asam asetat-ion asetat pada pH = 0 (hipotetik)
4. Kesimpulan
Hasil pengukuran potensiodinamik dapat digunakan untuk mengkonstruksi diagram potensial-pH. Pemetaan dengan cara ini terutama akan sangat membantu dalam pembahasan korosi logam atau paduan logam yang memperlihatkan kelakuan aktif/pasif korosi. Hal yang dapat menjadi pembatas penggunaan cara ini adalah ketersediaan elektroda referensi yang stabil pada suhu tinggi, dan rentang cakupan pH yang terbatasi oleh trayek pH sistem larutan buffer tertentu. Karenanya cara ini hanya dapat dipergunakan untuk kondisi spesifik, tergantung keperluan, terutama pada suhu di bawah 100 0C.
Daftar Pustaka
1. Pourbaix, M., ”Atlas of Electrochemical Equilibria in Aqueous Solutions”, Pergamon Press (1966).
2. Townsend, H.E., ”Potential-pH Diagram at Elevated Temperature for the System Fe-H2O”,
Corros. Sci., 10, 343 (1970).
3. Ueda, M., ”Potential-pH Diagram at Elevated Temperature for Metal-CO2/H2-Water System
and the Application for Corrosion of Pure Iron”,
Corros. Eng.,44, 3,159 (1995).
4. Inoue, H., ”How to Use Potential-pH Equilibrium Diagram”, Corros. Eng., 45, 12, 811 (1996).
5. Beverskog, B., & Puigdomenech, I., ”Revised Pourbaix Diagram for Iron at 25-300 0C”,
Corros. Sci., 38, 12, 2121 (1996).
6. Kurov, O.V., ”Plotting Alloy Corrosion State Diagrams”, Corrosion, 57, 6, 502 (2001). 7. Sastri, V.S., Corrosion Inhibitors Principles and
Applications, John Wiley & Sons Ltd, 74-79 (1998).
8. Scully, J.C., The fundamental of Corrosion, 3rd. ed, Pergamon Press, 107-120 (1990).
9. Shreir, L.L., (editor), Corrosion, Volume 1, Metal/Environment Reactions, Newnes-Butterworths, London, 1: 103-1: 110 (1978).