BAB I BAB I
PENDAHULUAN PENDAHULUAN
A.
A. Latar BelakangLatar Belakang
Laju reaksi dipengaruhi oleh konsentrasi pereaksi bukan konsentrasi hasil Laju reaksi dipengaruhi oleh konsentrasi pereaksi bukan konsentrasi hasil reaksi. Seperti yang dikemukakan oleh Gulberg dan Wooge dalam hukum Aksi Massa reaksi. Seperti yang dikemukakan oleh Gulberg dan Wooge dalam hukum Aksi Massa berikut
berikut “Laju “Laju reaksi reaksi dalam dalam suatu suatu sistem sistem pada pada suatu suatu temperatur temperatur tertentu berbandingtertentu berbanding lurus dengan konsentrasi dipangkatkan dengan koefisiennya dalam persamaan yang lurus dengan konsentrasi dipangkatkan dengan koefisiennya dalam persamaan yang bersangkutan.” Misalnya pada reaksi:
bersangkutan.” Misalnya pada reaksi: mA + nB
mA + nB pC + qDpC + qD
Secara teoritis hukum laju reaksi dirumuskan dengan persamaan berikut: Secara teoritis hukum laju reaksi dirumuskan dengan persamaan berikut:
v = k [A] v = k [A]mm[B][B]nn Keterangan: Keterangan: v = laju reaksi (m/dt) v = laju reaksi (m/dt)
k = konstanta atau tetapan konsentrasi laju reaksi [L/mol.dt] k = konstanta atau tetapan konsentrasi laju reaksi [L/mol.dt] [A] = konsentrasi zat A (mol/L)
[A] = konsentrasi zat A (mol/L) [B] = konsentrasi zat B (mol/L) [B] = konsentrasi zat B (mol/L)
Sukrosa yaitu gula biasa. Sukrosa terjadi pada semua tanaman yang Sukrosa yaitu gula biasa. Sukrosa terjadi pada semua tanaman yang mengalami fotosintesis, yang fungsinya adalah sebagai sumber energi. Gula ini mengalami fotosintesis, yang fungsinya adalah sebagai sumber energi. Gula ini diperoleh dari tanaman tebu yang menyusun sebanyak 14-20% dari cairannya. diperoleh dari tanaman tebu yang menyusun sebanyak 14-20% dari cairannya. Hidrolisis sukrosa menghasilkan D-Glukosa dan gula keto D-fruktosa dalam jumlah Hidrolisis sukrosa menghasilkan D-Glukosa dan gula keto D-fruktosa dalam jumlah yang sama. Sukrosa tak dapat bermutarotasi karena tak ada lagi gugus aldehida yang yang sama. Sukrosa tak dapat bermutarotasi karena tak ada lagi gugus aldehida yang bebas, sukrosa tak
bebas, sukrosa tak dapat mereduksi ladapat mereduksi lagi mereduksi pereaksigi mereduksi pereaksi -pereaksi Tollens, -pereaksi Tollens, FehlingFehling dan Benedict, karena itu sukrosa dinamakan gula non pereduksi.
dan Benedict, karena itu sukrosa dinamakan gula non pereduksi. Sukrosa mempunyai putaran optik [α] = +66
Sukrosa mempunyai putaran optik [α] = +66oo. Jika sukrosa dihidrolisis. Jika sukrosa dihidrolisis terdapat campuran D-Glukosa dan D-Fruktosa dalam jumlah yang sama, dan rotasi terdapat campuran D-Glukosa dan D-Fruktosa dalam jumlah yang sama, dan rotasi optiknya berubah tanda menjadi [α] =
optiknya berubah tanda menjadi [α] = -20-20oo. Hal ini disebabkan oleh campuran. Hal ini disebabkan oleh campuran kesetimbangan anomer
D-kesetimbangan anomer D-glikosa (α dan β ) mempunyai rotasi +52glikosa (α dan β ) mempunyai rotasi +52oo, tetapi anomer , tetapi anomer fruktosa mempunyai rotasi negatif yang ku
sukrosa menukar (=invert) tanda rotasi optik, enzim yang melakukan hidrolisisnya sukrosa menukar (=invert) tanda rotasi optik, enzim yang melakukan hidrolisisnya adalah invertase, dan hasilnya berupa campuran sebanding glukosa dan fruktosa adalah invertase, dan hasilnya berupa campuran sebanding glukosa dan fruktosa dinamakan gula invert.
dinamakan gula invert.
Enantiomer yang memutar cahaya terpolarisasi tekanan diberi tanda (+) atau d Enantiomer yang memutar cahaya terpolarisasi tekanan diberi tanda (+) atau d (dextro), sedangkan yang memutar ke kiri diberi tanda (-) atau l (levo). Besarnya (dextro), sedangkan yang memutar ke kiri diberi tanda (-) atau l (levo). Besarnya sudut putar / sudut rotasi (θ) tergantung pada jenis senyawa, suhu, cahaya terpolarisasi sudut putar / sudut rotasi (θ) tergantung pada jenis senyawa, suhu, cahaya terpolarisasi dan banyaknya molekul pada jalan yang dilalui cahaya rotasi spesifik ialah putaran / dan banyaknya molekul pada jalan yang dilalui cahaya rotasi spesifik ialah putaran / rotasio yang dihasilkan oleh 1 gram senyawa dalam mol larutan dalam 1 sel sepanjang rotasio yang dihasilkan oleh 1 gram senyawa dalam mol larutan dalam 1 sel sepanjang 1 dm. 1 dm. Dimana, Dimana,
A = sudut rotasi yang diamati A = sudut rotasi yang diamati e = panjang (dm)
e = panjang (dm)
Gula inversi adalah campuran D-glukosa dan D-fruktosa yang diperoleh Gula inversi adalah campuran D-glukosa dan D-fruktosa yang diperoleh dengan hidrolisis asam dari sukrosa. Berdasarkan teori bahwa mayoritas gula adalah dengan hidrolisis asam dari sukrosa. Berdasarkan teori bahwa mayoritas gula adalah fruktosa dan fruktosa membelokkan cahaya ke kiri. Gula yang terdiri dari Sukrosa fruktosa dan fruktosa membelokkan cahaya ke kiri. Gula yang terdiri dari Sukrosa maupun Glukosa memutar cahaya ke kanan. Sukrosa memiliki rotasi+66,5 (positif) maupun Glukosa memutar cahaya ke kanan. Sukrosa memiliki rotasi+66,5 (positif) produk
produk yang dihasilkan yang dihasilkan glukosa[α]= +52,7 glukosa[α]= +52,7 dan dan fruktosa fruktosa [α] [α] == -92-92oo (negatif). Dengan(negatif). Dengan mengetahui pembelokan cahaya yang dihasilkan oleh larutan gula, dapat di analisa mengetahui pembelokan cahaya yang dihasilkan oleh larutan gula, dapat di analisa jenis / komposisi gula yang ada dalam larutan tersebut.
jenis / komposisi gula yang ada dalam larutan tersebut.
Orde reaksi dari inverse gula merupakan orde ke satu. Pada reaksi ini laju Orde reaksi dari inverse gula merupakan orde ke satu. Pada reaksi ini laju reaksi hanya tergantung pada satu kosentrasi saja yaitu [C
reaksi hanya tergantung pada satu kosentrasi saja yaitu [C1212HH2222OO1111] sedangkan H] sedangkan H22OO tidak berpengaruh dalam reaksi tersebut. Pada percobaan ini akan ditentukan orde tidak berpengaruh dalam reaksi tersebut. Pada percobaan ini akan ditentukan orde reaksi dari reaksi inversi
reaksi dari reaksi inversi gula menggunakan polarimeter.gula menggunakan polarimeter.
B.
B. Rumusan MasalahRumusan Masalah
Berapa orde reaksi dari reaksi inversi gula menggunakan polarimeter ? Berapa orde reaksi dari reaksi inversi gula menggunakan polarimeter ? C.
C. TujuanTujuan
Menentukan orde reaksi dari reaksi inversi gula menggunakan polarimeter. Menentukan orde reaksi dari reaksi inversi gula menggunakan polarimeter.
BAB II BAB II KAJIAN TEORI KAJIAN TEORI
Istilah laju atau kecepatan sering dibicarakan dalam pelajaran fisika. Istilah laju atau kecepatan sering dibicarakan dalam pelajaran fisika. Pengertian laju dalam reaksi sebenarnya sama dengan laju pada kendaraan yang Pengertian laju dalam reaksi sebenarnya sama dengan laju pada kendaraan yang bergerak.
bergerak. Reaksi Reaksi kimia kimia menyangkut perubahan menyangkut perubahan dari dari suatu suatu pereaksi pereaksi (reaktan) (reaktan) menjadimenjadi hasil reaksi (produk), yang dinyatakan dalam persamaan reaksi. Pereaksi (reaktan) hasil reaksi (produk), yang dinyatakan dalam persamaan reaksi. Pereaksi (reaktan) Hasil reaksi (produk). Persamaan laju reaksi pertama kali dikemukakan oleh Gulberg Hasil reaksi (produk). Persamaan laju reaksi pertama kali dikemukakan oleh Gulberg dan Wooge dalam hukum Aksi Massa. Mereka menyebutkan laju reaksi pada suatu dan Wooge dalam hukum Aksi Massa. Mereka menyebutkan laju reaksi pada suatu sistem pada temperatur tertentu berbanding lurus dengan konsentrasi zat yang sistem pada temperatur tertentu berbanding lurus dengan konsentrasi zat yang bereaksi
bereaksi setelah setelah tiaptiap – – tiap konsentrasi dipangkatkan dengan koefisien dalamtiap konsentrasi dipangkatkan dengan koefisien dalam persamaan yang bersangkutan.
persamaan yang bersangkutan.
Dengan cara fisis penentuan konsentrasi dilakukan secara langsung, yaitu Dengan cara fisis penentuan konsentrasi dilakukan secara langsung, yaitu berdasar
berdasar sifatsifat – – sifat fisis campuran yang dipengaruhi oleh konsentrasi campuran,sifat fisis campuran yang dipengaruhi oleh konsentrasi campuran, misalnya daya hantar listrik, tekanan, adsorbsi cahaya, dan sebagainya. Penentuan misalnya daya hantar listrik, tekanan, adsorbsi cahaya, dan sebagainya. Penentuan secara kimia dilakukan dengan menghentikan reakis secara tiba
secara kimia dilakukan dengan menghentikan reakis secara tiba – – tiba (reaksitiba (reaksi dibekukan) setelah selang waktu tertentu, kemudian konsentrasinya dihitung dengan dibekukan) setelah selang waktu tertentu, kemudian konsentrasinya dihitung dengan analisis kimia. Laju reaksi akan menurun dengan bertambahnya waktu. Hal ini analisis kimia. Laju reaksi akan menurun dengan bertambahnya waktu. Hal ini menunjukkan adanya hubungan antara konsentrasi zat yang tersisa saat itu dengan menunjukkan adanya hubungan antara konsentrasi zat yang tersisa saat itu dengan laju reaksi sehingga dapat dikatakan umumnya laju reaksi tergantung pada konsentrasi laju reaksi sehingga dapat dikatakan umumnya laju reaksi tergantung pada konsentrasi awal dari zat
awal dari zat – – zat pereaksi, pernyataan ini dikenal sebagai Hukum Laju Reaksizat pereaksi, pernyataan ini dikenal sebagai Hukum Laju Reaksi atauatau Persamaan Laju
Persamaan Laju ReaksiReaksi
m A + n B o C + p D m A + n B o C + p D
Dalam persamaan laju reaksi dapat dituliskan Dalam persamaan laju reaksi dapat dituliskan
v
v== k k [A]m [B]n[A]m [B]n
dimana,
dimana, vv= laju reaksi (m/detik)= laju reaksi (m/detik)
k
k = konstanta tetapan laju reaksi (L/mol.detik)= konstanta tetapan laju reaksi (L/mol.detik)
[A] = konsentrasi zat A (mol/L) [A] = konsentrasi zat A (mol/L)
[B] = konsentrasi zat B (mol/L) [B] = konsentrasi zat B (mol/L)
m = tingkat reaksi (orde reaksi) terhadap A m = tingkat reaksi (orde reaksi) terhadap A n = tingkat reaksi (orde reaksi) terhadap n = tingkat reaksi (orde reaksi) terhadap BB
Tingkat reaksi total adalah jumlah total dari tingkat reaksi semua pereaksi. Tingkat reaksi total adalah jumlah total dari tingkat reaksi semua pereaksi. Tingkat reaksi nol (0) berarti laju reaksi tersebut tidak terpengaruh oleh konsentrasi Tingkat reaksi nol (0) berarti laju reaksi tersebut tidak terpengaruh oleh konsentrasi pereaksi,
pereaksi, tetapi tetapi hanya hanya bergantung bergantung pada pada harga harga tetapan tetapan laju laju reaksi reaksi ((k k ). Harga). Harga k k tergantung pada suhu, jika suhunya tetap harga
tergantung pada suhu, jika suhunya tetap harga k k juga juga tetap. tetap. Untuk Untuk mengetahuimengetahui hubungan pereaksi dengan reaktan, digunakan orde reaksi yang diperoleh dari hubungan pereaksi dengan reaktan, digunakan orde reaksi yang diperoleh dari perhitungan
perhitungan konsentrasi konsentrasi sehingga sehingga grafik grafik yang yang diperoleh diperoleh berbentuk berbentuk grafik grafik perpangkatan. Harga
perpangkatan. Hargak k tergantung pada tingkat (orde) reaksi totalnya.tergantung pada tingkat (orde) reaksi totalnya. ●
●Orde reaksi nol,Orde reaksi nol,
Reaksi yang memiliki kecepatan reaksi tetap dan tidak dipengaruhi konsentrasi Reaksi yang memiliki kecepatan reaksi tetap dan tidak dipengaruhi konsentrasi reaktan. Kecepatan reaksi dipengaruhi / ditentukan oleh intensitas
reaktan. Kecepatan reaksi dipengaruhi / ditentukan oleh intensitas katalis.katalis. Persamaannya orde 0:
Persamaannya orde 0: v = k
v = k [x]0 =[x]0 = k k Orde reaksi satu, Orde reaksi satu, Persamaannya : Persamaannya :
v
v ==k k [x]1 =[x]1 =k k [x][x] Orde Reaksi dua,
Orde Reaksi dua, Persamaannya : Persamaannya : v v ==k k [x]2[x]2 Polarimeter Polarimeter
Polarimetri adalah suatu cara analisa yang didasarkan pada pengukuran sudut Polarimetri adalah suatu cara analisa yang didasarkan pada pengukuran sudut putaran
putaran (optical (optical rotation) rotation) cahaya cahaya terpolarisir terpolarisir oleh oleh senyawa senyawa yang transparan yang transparan dandan optisoptis aktif apabila senyawa tersebut dilewati sinar monokromatis yang terpolarisir tersebut. aktif apabila senyawa tersebut dilewati sinar monokromatis yang terpolarisir tersebut. Senyawa optis aktif adalah senyawa yang dapat memutar bidang getar sinar Senyawa optis aktif adalah senyawa yang dapat memutar bidang getar sinar terpolarisir. Zat yang optis ditandai dengan adanya atom karbon asimetris atau atom C terpolarisir. Zat yang optis ditandai dengan adanya atom karbon asimetris atau atom C kiral dalam senyawa organik, contoh : kuarsa ( SiO2 ), fruktosa. Cahaya kiral dalam senyawa organik, contoh : kuarsa ( SiO2 ), fruktosa. Cahaya monokromatik pada dasarnya mempunyai bidang getar yang banyak sekali. Bila monokromatik pada dasarnya mempunyai bidang getar yang banyak sekali. Bila dikhayalkan maka bidang getar tersebut akan tegak lurus pada bidang datar. Bidang dikhayalkan maka bidang getar tersebut akan tegak lurus pada bidang datar. Bidang getar yang banyak sekali ini secara mekanik dapat dipisahkan menjadi dua bidang getar yang banyak sekali ini secara mekanik dapat dipisahkan menjadi dua bidang
getar yang saling tegak lurus. Yang dimaksud dengan cahaya terpolarisasi adalah getar yang saling tegak lurus. Yang dimaksud dengan cahaya terpolarisasi adalah senyawa yang mempunyai satu arah getar dan arah getar tersebut tegak lurus terhadap senyawa yang mempunyai satu arah getar dan arah getar tersebut tegak lurus terhadap arah rambatnya. Prinsip dasar polarimetris ini adalah pengukuran daya putar optis arah rambatnya. Prinsip dasar polarimetris ini adalah pengukuran daya putar optis suatu zat yang menimbulkan terjadinya putaran bidang getar sinar terpolarisir. suatu zat yang menimbulkan terjadinya putaran bidang getar sinar terpolarisir. Pemutaran bidang getar sinar terpolarisir oleh s
Pemutaran bidang getar sinar terpolarisir oleh senyawa optis aktif ada 2 macam :enyawa optis aktif ada 2 macam : 1.
1. Dexro rotary (+), jika arah putarnya ke kanan atau sesuai putaran jarum jam.Dexro rotary (+), jika arah putarnya ke kanan atau sesuai putaran jarum jam. 2.
2. Levo rotary (-), jika arah putarnya ke kiri atau berlawanan dengan putaran jarumLevo rotary (-), jika arah putarnya ke kiri atau berlawanan dengan putaran jarum jam.
jam.
Inversi Gula Inversi Gula
Karbohidrat merupakan senyawa karbon, hidrogen dan oksigen yang terdapat Karbohidrat merupakan senyawa karbon, hidrogen dan oksigen yang terdapat dalam alam. Karbohidrat sangat beranekaragam sifatnya. Misalnya, sukrosa (gula dalam alam. Karbohidrat sangat beranekaragam sifatnya. Misalnya, sukrosa (gula pasir)
pasir) dan dan kapas, kapas, keduanya keduanya adalah adalah karbohidrat. karbohidrat. Salah Salah satu satu perbedaan perbedaan utama utama antaraantara pelbagai
pelbagai tipe tipe karbohidrat karbohidrat ialah ialah ukuran ukuran molekulnya. molekulnya. Gula Gula merupakan merupakan zat zat optis optis aktif.aktif. Bila cahaya terpolarisasi linier jatuh pada bahan optis aktif, maka cahaya yang keluar Bila cahaya terpolarisasi linier jatuh pada bahan optis aktif, maka cahaya yang keluar bahan
bahan akan akan tetap tetap terpolarisasi terpolarisasi linier linier dengan dengan arah arah bidang bidang getar getar terputar terputar terhadap terhadap araharah bidang
bidang getar getar semula. semula. Sifat Sifat optis optis aktif aktif zat zat dispesifikasikan dispesifikasikan dengan dengan sudut sudut putar putar jenis.Sudut
jenis.Sudut putar putar bidang bidang polarisasi polarisasi sebanding sebanding dengan dengan sudut sudut putar putar jenis jenis dandan konsentrasi bila sudut putar jenis diketahui dan sudut putar bidang polarisasi dapat konsentrasi bila sudut putar jenis diketahui dan sudut putar bidang polarisasi dapat diukur, maka konsentrasi (kadar) zat optis aktif dapat ditentukan (hal ini merupakan diukur, maka konsentrasi (kadar) zat optis aktif dapat ditentukan (hal ini merupakan prinsip
prinsip yang yang digunakan digunakan untuk untuk menentukan menentukan kadar kadar zat zat optis. optis. Gula Gula inversi inversi adalahadalah campuran D-glukosa dan D- fruktosa yang diperoleh dengan hidrolisis asam atau campuran D-glukosa dan D- fruktosa yang diperoleh dengan hidrolisis asam atau enzimatik dari sukrosa. Enzim yang mengkatalis hidrolisis sukrosa disebut enzimatik dari sukrosa. Enzim yang mengkatalis hidrolisis sukrosa disebut
invertase
invertase,bersifat spesifik untuk ikatan,bersifat spesifik untuk ikatan ββ-Dfruktofuranosida dan terdapat dalam ragi-Dfruktofuranosida dan terdapat dalam ragi
dan lebah (madu terutama terdiri dari gula inversi). Berdasarkan teori bahwa dan lebah (madu terutama terdiri dari gula inversi). Berdasarkan teori bahwa mayoritas gula adalah fruktosa dan fruktosa membelokkan cahaya ke kiri. Gula yang mayoritas gula adalah fruktosa dan fruktosa membelokkan cahaya ke kiri. Gula yang terdiri dari Sukrosa maupun Glukosa memutar cahaya ke kanan. Sukrosa memiliki terdiri dari Sukrosa maupun Glukosa memutar cahaya ke kanan. Sukrosa memiliki rotasi +66,5° (positif) produk yang dihasilkan glukosa[
rotasi +66,5° (positif) produk yang dihasilkan glukosa[αα]= +52,7° dan fruktosa []= +52,7° dan fruktosa [αα] = -] = -92,4o
92,4o mempunyai mempunyai rotasi netto rotasi netto negatif. negatif. Dengan mengetahui Dengan mengetahui pembelokan cahaypembelokan cahaya yanga yang dihasilkan oleh larutan gula, dapat di analisa jenis/komposisi gula yang ada dalam dihasilkan oleh larutan gula, dapat di analisa jenis/komposisi gula yang ada dalam larutan tersebut.
Sudut putar jenis jenis dapat dihitung : Sudut putar jenis jenis dapat dihitung :
[[]]
(()) ( ( ))
Kinetika reaksi inversi gula merupakan reaksi orde satu terhadap sukrosa. Kinetika reaksi inversi gula merupakan reaksi orde satu terhadap sukrosa. Dalam larutan gula yang netral (pH=5) reaksi hidrolisa gula mempunyai waktu paruh Dalam larutan gula yang netral (pH=5) reaksi hidrolisa gula mempunyai waktu paruh 10 minggu. Sedangkan didalam larutan asam, dengan adanya katalis ion H+, waktu 10 minggu. Sedangkan didalam larutan asam, dengan adanya katalis ion H+, waktu paruh
paruh tersebut tersebut lebih lebih pendek. pendek. Hukum Hukum laju laju reaksi reaksi inversi inversi gula gula tersebut tersebut dapatdapat diungkapkan sebagai berikut:
diungkapkan sebagai berikut:
R = - d (gula) / dt = k (H+)(H2O)(gula) R = - d (gula) / dt = k (H+)(H2O)(gula)
Reaksi hidrolisis dari percobaan: Reaksi hidrolisis dari percobaan:
C
C1111HH2222OO1111 + H+ H22OO CC66HH1212OO66+ C+ C66HH1212OO66 6
6
Cara Penggunaan Polarimeter Cara Penggunaan Polarimeter
Cara penggunaan berikut adalah cara pada Zeiss Polarimeter, tetapi secara Cara penggunaan berikut adalah cara pada Zeiss Polarimeter, tetapi secara umum cara penggunaan polarimeter manapun adalah sama. Untuk memulai umum cara penggunaan polarimeter manapun adalah sama. Untuk memulai penggunaan polarimeter pasti
penggunaan polarimeter pastikan tombol power kan tombol power pada posisi pada posisi on dan biaon dan biarkan selama rkan selama 5- 5-10 menit agar lampu natriumnya siap digunakan. Selalu mulai dengan menentukan 10 menit agar lampu natriumnya siap digunakan. Selalu mulai dengan menentukan keadaan nol (zero point) dengan mengisi tabung sampel dengan pelarut saja. Keadaan keadaan nol (zero point) dengan mengisi tabung sampel dengan pelarut saja. Keadaan nol ini perlu untuk mengkoreksi pembacaan atau pengamatan rotasi optik. Tabung nol ini perlu untuk mengkoreksi pembacaan atau pengamatan rotasi optik. Tabung sampel harus dibersihkan sebelum digunakan agar larutan yang diisikan tidak sampel harus dibersihkan sebelum digunakan agar larutan yang diisikan tidak terkontaminasi zat lain. Pembacaan/pengamatan bergantung kepada tabung sampel terkontaminasi zat lain. Pembacaan/pengamatan bergantung kepada tabung sampel yang berisi larutan/pelarut dengan penuh. Perhatikan saat menutup tabung sampel, yang berisi larutan/pelarut dengan penuh. Perhatikan saat menutup tabung sampel, harus dilakukan hati-hati agar di dalam tabung tidak terdapat gelembung udara. Bila harus dilakukan hati-hati agar di dalam tabung tidak terdapat gelembung udara. Bila sebelum tabung diisi larutan didapat keadaan terang, maka setelah tabung diisi larutan sebelum tabung diisi larutan didapat keadaan terang, maka setelah tabung diisi larutan putarlah
putarlah analisator analisator sampai sampai didapat didapat keadaan keadaan terang terang kembali. kembali. Sebaliknya Sebaliknya bila bila awalnyaawalnya keadaan gelap harus kembali kekeadaan gelap. Catat besarnya rotasi optik yang dapat keadaan gelap harus kembali kekeadaan gelap. Catat besarnya rotasi optik yang dapat terbaca pada skala. Tetapi jangan hanya besar rotasi optiknya, arah rotasinya juga terbaca pada skala. Tetapi jangan hanya besar rotasi optiknya, arah rotasinya juga harus dicatat searah jarum jam atau berlawanan arah jarum jam. Lakukan pembacaan harus dicatat searah jarum jam atau berlawanan arah jarum jam. Lakukan pembacaan berkali-kali sampai diperoleh nilai yang dapat dirata-ratakan.
BAB III BAB III PEMBAHASAN PEMBAHASAN
Pada percobaan yang bertujuan untuk menentukan orde reaksi dari reaksi Pada percobaan yang bertujuan untuk menentukan orde reaksi dari reaksi inversi gula dengan menggunakan alat polarimeter ini, langkah pertama yaitu menimbang inversi gula dengan menggunakan alat polarimeter ini, langkah pertama yaitu menimbang sebanyak 2,5 gram gula pasir yaitu sukrosa,
sebanyak 2,5 gram gula pasir yaitu sukrosa, kemudian dimasukkan ke dalam labu ukur 25 ml.kemudian dimasukkan ke dalam labu ukur 25 ml. Ditambahkan sedikit air ke dalam labu ukur berisi sukrosa kemudian dikocok hingga larut, Ditambahkan sedikit air ke dalam labu ukur berisi sukrosa kemudian dikocok hingga larut, setelah itu ditambah lagi air hingga mencapai tanda batas. Dalam hal ini akan dihasilkan setelah itu ditambah lagi air hingga mencapai tanda batas. Dalam hal ini akan dihasilkan sampel berupa 10% larutan sukrosa (gula pasir).
sampel berupa 10% larutan sukrosa (gula pasir). Selanjutnya terdiri dari beberapa tahap, antara l
Selanjutnya terdiri dari beberapa tahap, antara lain adalah sebagai berikut :ain adalah sebagai berikut :
a.
a. Mempersiapkan apparatus polarimeter.Mempersiapkan apparatus polarimeter.
Dalam mempersiapkan apparatus polarimeter, yang pertama kali dilakukan Dalam mempersiapkan apparatus polarimeter, yang pertama kali dilakukan adalah mengeluarkan kuvet dari polarimeter kemudian dicuci dengan aquades sebersih adalah mengeluarkan kuvet dari polarimeter kemudian dicuci dengan aquades sebersih mungkin dan dikeringkan. Untuk memperkecil kemungkinan kesalahan terjadi dalam mungkin dan dikeringkan. Untuk memperkecil kemungkinan kesalahan terjadi dalam pengamatan
pengamatan maka maka lebih lebih baik baik tabung tabung (kuvet) (kuvet) dibilas dibilas dengan dengan pelarut pelarut yang yang akan akan dipakaidipakai sebagai pelarut zat optis aktif yang akan dianalisis. Setelah bersih dan dikeringkan, kuvet sebagai pelarut zat optis aktif yang akan dianalisis. Setelah bersih dan dikeringkan, kuvet siap dipakai.
siap dipakai.
b.
b. MenentuMenentukan titik kan titik nolnol
Dalam menentukan titik nol pelarut, dalam percobaan ini adalah air, yang Dalam menentukan titik nol pelarut, dalam percobaan ini adalah air, yang pertama k
pertama kali ali dilakukan adilakukan adalah dalah mengisi mengisi kuvet dengan kuvet dengan air air dengan menggunakan dengan menggunakan pipet pipet dandan diusahakan tidak ada gelembung udara dalam kuvet yang berisi air tersebut, agar hasil diusahakan tidak ada gelembung udara dalam kuvet yang berisi air tersebut, agar hasil pengamatan
pengamatan yang yang diperoleh diperoleh lebih lebih akurat. akurat. Kuvet Kuvet yang yang berisi berisi air air dimasukkan dimasukkan kedalamkedalam polarimeter, lalu mencari
polarimeter, lalu mencari cahaya gelap terang yang ditunjukkan pada polarimeter. Setelcahaya gelap terang yang ditunjukkan pada polarimeter. Setel ahah ditemukan cahaya gelap terang, kemudian melihat skala yang ditunjukkan pada ditemukan cahaya gelap terang, kemudian melihat skala yang ditunjukkan pada polarimeter. Pada pengamatan ini diketahui putaran yang
polarimeter. Pada pengamatan ini diketahui putaran yang diamati adalah 0diamati adalah 0oo..
c.
c. Menentukan sudut putar jenis sampelMenentukan sudut putar jenis sampel
Pada penentuan sudut putar jenis sampel, pertama mengeluarkan kuvet yang Pada penentuan sudut putar jenis sampel, pertama mengeluarkan kuvet yang berisi air kemudian dikosongkan dan diisi lagi deng
berisi air kemudian dikosongkan dan diisi lagi dengan larutan gula 10%. Kuvet yang telahan larutan gula 10%. Kuvet yang telah berisi larutan gula 10%, dimasukkan kedalam polarimeter kemudian diamati cahaya gelap berisi larutan gula 10%, dimasukkan kedalam polarimeter kemudian diamati cahaya gelap terangnya dan dilihat skalanya. Dari pengamatan ini diketahui putaran yang diamati. terangnya dan dilihat skalanya. Dari pengamatan ini diketahui putaran yang diamati.
Kemudian menghitung sudut putar jenis sampel (α), yang diperoleh dari perbedaan skala Kemudian menghitung sudut putar jenis sampel (α), yang diperoleh dari perbedaan skala
pengukuran titik nol air dan sud
7,9
7,9oo – – 00oo= 7,9= 7,9oo Dengan menggunakan rumus : Dengan menggunakan rumus :
[α] =
[α] = panjang panjang tabung tabung dalamdalamdmdm kadar kadar (( gram gram per per mol mol )) diamati diamati yang yang putaran putaran = = 11,,1313 00,,11 9 9 ,, 7 7 = 69,91 = 69,91
Dari perhitungan tersebut diketahui bahwa sudut putar sukrosa sebesar 69,91
Dari perhitungan tersebut diketahui bahwa sudut putar sukrosa sebesar 69,91oo, sudut putar , sudut putar yang kami peroleh berbeda dengan sudut putar sukrosa sesuai teori yaitu sebesar 66,5 yang kami peroleh berbeda dengan sudut putar sukrosa sesuai teori yaitu sebesar 66,5oo..
d.
d. MenentukMenentukan sudut putar sampel dari an sudut putar sampel dari waktu ke waktuwaktu ke waktu
Dalam menentukan sudut putar sampel dari waktu ke waktu, pertama adalah Dalam menentukan sudut putar sampel dari waktu ke waktu, pertama adalah mengosongkan kuvet kemudian mengisi dengan larutan yang dibuat dengan cara mengosongkan kuvet kemudian mengisi dengan larutan yang dibuat dengan cara mencampurkan 25 ml larutan gula 10% dengan 10 ml larutan HCl 2N. Penambahan HCl mencampurkan 25 ml larutan gula 10% dengan 10 ml larutan HCl 2N. Penambahan HCl adalah sebagai katalis yang dapat mempercepat reaksi terurainya sukrosa menjadi glukosa adalah sebagai katalis yang dapat mempercepat reaksi terurainya sukrosa menjadi glukosa dan fruktosa, dimana pada akhir reaksi akan terbentuk kembali. Kemudian kuvet yang dan fruktosa, dimana pada akhir reaksi akan terbentuk kembali. Kemudian kuvet yang berisi
berisi campuran campuran larutan larutan gula gula dan dan HCl HCl dimasukkan dimasukkan kedalam kedalam polarimeter polarimeter dan dan melakukanmelakukan pengamatan sudut putar dari
pengamatan sudut putar dari waktu ke waktu waktu ke waktu yaitu pada waktu : yaitu pada waktu : 5, 10, 15, 20, 5, 10, 15, 20, 25, 30, 35,25, 30, 35, 40, 45, 50, 55 dan 60 menit.
40, 45, 50, 55 dan 60 menit.
Selanjutnya disiapkan apparatus polarimeter. Kuvet dikeluarkan dari dalam Selanjutnya disiapkan apparatus polarimeter. Kuvet dikeluarkan dari dalam bak
bak polarimeter polarimeter untuk untuk dilakukan dilakukan pencucian pencucian hingga hingga bersih bersih serta serta dikeringkan. dikeringkan. Untuk Untuk menghindari kemungkinan terjadinya kesalahan, maka lebih baik kuvet dibilas dengan menghindari kemungkinan terjadinya kesalahan, maka lebih baik kuvet dibilas dengan pelarut yang akan dipakai sebagai pelarut zat optis aktif yang ak
pelarut yang akan dipakai sebagai pelarut zat optis aktif yang akan dianalisis.an dianalisis.
Agar mendapat hasil yang akurat, kuvet diisi hingga tidak ada gelembung Agar mendapat hasil yang akurat, kuvet diisi hingga tidak ada gelembung udara di dalamnya. Kuvet diisi larutan sampai tanda batas bawah, alat polarimeter juga udara di dalamnya. Kuvet diisi larutan sampai tanda batas bawah, alat polarimeter juga diarahkan pada sumber cahaya yang terang agar pada alat polarimeter dapat terlihat batas diarahkan pada sumber cahaya yang terang agar pada alat polarimeter dapat terlihat batas terang dan gelap. Selanjutnya adalah menentukan titik nol pelarut air yang pasti akan terang dan gelap. Selanjutnya adalah menentukan titik nol pelarut air yang pasti akan didapatkan putaran optik sama dengan nol. Kemudian dilakukan pengukuran sudut didapatkan putaran optik sama dengan nol. Kemudian dilakukan pengukuran sudut sampel yaitu larutan gula 10%, tetapi sebelumnya kuvet dibilas terlebih dahulu dengan sampel yaitu larutan gula 10%, tetapi sebelumnya kuvet dibilas terlebih dahulu dengan larutan gula 10% dan akan didapat skala. Nilai skala yang didapat dapat digunakan untuk larutan gula 10% dan akan didapat skala. Nilai skala yang didapat dapat digunakan untuk menghitung nilai
menghitung nilai dengan menggunakan rumus berikut :dengan menggunakan rumus berikut :
//
putaran yang
putaran yang diamatidiamati panjang
panjang tabung dalamtabung dalam dm dm kadar kadar gr gr mLmL
Misalnya, diketahui panjang tabung 1,1 dm ; kadar 0,1 gr/ml; se
Misalnya, diketahui panjang tabung 1,1 dm ; kadar 0,1 gr/ml; se rta nilai skala rta nilai skala larutan gulalarutan gula yang didapat sebesar 6,6
yang didapat sebesar 6,6..
Sehingga dapat dihitung nilai
Sehingga dapat dihitung nilai dari larutan gula 10% (0 menit) sebagai berikut:dari larutan gula 10% (0 menit) sebagai berikut:
111100,,99 1 1 ,, 0 0 1 1 ,, 1 1 2 2 ,, 12 12 x x Maka didapat [α] sebesar
Maka didapat [α] sebesar 110,9110,9oo..
Selanjutnya yaitu dilakukan pengukuran sudut putar dari waktu ke waktu Selanjutnya yaitu dilakukan pengukuran sudut putar dari waktu ke waktu dengan membuat campuran 25 ml larutan sukrosa dengan 10 ml larutan HCl 2N. Tujuan dengan membuat campuran 25 ml larutan sukrosa dengan 10 ml larutan HCl 2N. Tujuan dari hal ini ialah untuk mengetahui reaksi hidrolisis yang terjadi pada gula dengan dari hal ini ialah untuk mengetahui reaksi hidrolisis yang terjadi pada gula dengan menggunakan suatu asam (HCl) sebagai katalis.
menggunakan suatu asam (HCl) sebagai katalis.
Setelah itu, putaran optik diukur menggunakan polarimeter dengan cara yang Setelah itu, putaran optik diukur menggunakan polarimeter dengan cara yang sama dengan sebelumnya ketika mengukur putaran optik larutan blanko. Pengamatan sama dengan sebelumnya ketika mengukur putaran optik larutan blanko. Pengamatan sudut putar dilakukan dari waktu ke waktu yaitu 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, sudut putar dilakukan dari waktu ke waktu yaitu 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60 menit dan setelah 24 jam. Terjadinya reaksi hidrolisis sukrosa menjadi glukosa dan 60 menit dan setelah 24 jam. Terjadinya reaksi hidrolisis sukrosa menjadi glukosa dan fruktosa ditandai dengan semakin turun nilai putaran optik dari waktu ke waktu. Pada fruktosa ditandai dengan semakin turun nilai putaran optik dari waktu ke waktu. Pada sukrosa yang memiliki putaran optik +66
sukrosa yang memiliki putaran optik +66oo jika jika terhidrolisisterhidrolisis akan terdapat campuran D-akan terdapat campuran D-Glukosa dan D-Fruktosa dalam jumlah yang sama, dan rotasi optiknya berubah tanda Glukosa dan D-Fruktosa dalam jumlah yang sama, dan rotasi optiknya berubah tanda menjadi [
menjadi [ ] = -20] = -20oo. Hal ini disebabkan oleh campuran kesetimbangan anomer D-glukosa. Hal ini disebabkan oleh campuran kesetimbangan anomer D-glukosa
(( dandan ) mempunyai rotasi +52) mempunyai rotasi +52oo, tetapi anomer fruktosa mempunyai rotasi negatif yang, tetapi anomer fruktosa mempunyai rotasi negatif yang
kuat yaitu [
kuat yaitu [ ] = -92] = -92oo, karena hidrolisis sukrosa menukar (=invert) tanda rotasi optik., karena hidrolisis sukrosa menukar (=invert) tanda rotasi optik. Reaksi inversi gula :
Reaksi inversi gula : C
C1212HH2222OO1111 + + HH22OO C6C6HH1212OO66 + + CC66HH1212OO66 Reaksi ini disebut juga orde reaksi satu pseudo.
Reaksi ini disebut juga orde reaksi satu pseudo.
Orde reaksi dari inversi gula merupakan orde ke satu. Pada reaksi ini laju Orde reaksi dari inversi gula merupakan orde ke satu. Pada reaksi ini laju reaksi hanya tergantung pada satu kosentrasi saja yaitu [C
reaksi hanya tergantung pada satu kosentrasi saja yaitu [C1212HH2222OO1111] sedangkan H] sedangkan H22O tidak O tidak berpengaruh dalam reaksi tersebut.
berpengaruh dalam reaksi tersebut.
Jika hasil dari percobaan sesuai dengan teori menghasilkan data
Jika hasil dari percobaan sesuai dengan teori menghasilkan data sebagai berikut:sebagai berikut: Waktu
Waktu (menit) (menit) skalaskala αα 0
0 +12,2+12,2 110,90110,90
5
10 10 +9,5+9,5 86,3786,37 15 15 +8,4+8,4 76,2276,22 20 20 +7,4+7,4 67,2767,27 25 25 +6,5+6,5 59,3659,36 30 30 +5,8+5,8 52,3952,39 35 35 +5,1+5,1 46,2346,23 40 40 +4,5+4,5 40,8040,80 45 45 +3,9+3,9 36,0136,01 50 50 +4,0+4,0 31,7731,77 55 55 +3,1+3,1 28,0428,04 60 60 +2,7+2,7 24,7424,74 setelah 24 jam setelah 24 jam + 1,1+ 1,1 1010 t
t a a (a-x) (a-x) (a-x)(a-x)22 ln(a-x) ln(a-x) 1/(a-x)1/(a-x)
0 110,9 0 110,9 5 5 110,9 110,9 97,87 97,87 9578,5369 9578,5369 4,58364,5836 0,0102176360,010217636 10 10 110,9 110,9 86,37 86,37 7459,7769 7459,7769 4,45864,4586 0,0115780940,011578094 15 15 110,9 110,9 76,22 76,22 5809,4884 5809,4884 4,33364,3336 0,0131199160,013119916 20 20 110,9 110,9 67,27 67,27 4525,2529 4525,2529 4,20874,2087 0,0148654680,014865468 25 25 110,9 110,9 59,36 59,36 3523,6096 3523,6096 4,08364,0836 0,0168463610,016846361 30 30 110,9 110,9 52,39 52,39 2744,7121 2744,7121 3,95873,9587 0,0190876120,019087612 35 35 110,9 110,9 46,23 46,23 2137,2129 2137,2129 3,83363,8336 0,0216309760,021630976 40 110,9 40 110,9 40,8 40,8 1664,64 1664,64 3,708683,70868 0,0245098040,024509804 45 45 110,9 110,9 36,01 36,01 1296,7201 1296,7201 3,58383,5838 0,0277700640,027770064 50 50 110,9 110,9 31,77 31,77 1009,3329 1009,3329 3,45853,4585 0,0314762350,031476235 55 55 110,9 110,9 28,04 28,04 786,2416 786,2416 3,33363,3336 0,0356633380,035663338 60 60 110,9 110,9 24,74 24,74 612,0676 612,0676 3,20843,2084 0,0404203720,040420372
Data tersebut dapat digunakan untuk mencari nilai k dengan integral metode grafik Data tersebut dapat digunakan untuk mencari nilai k dengan integral metode grafik maupun non grafik sebagai berikut.
maupun non grafik sebagai berikut.
1.
1. METODE INTEGRAL GRAFIK METODE INTEGRAL GRAFIK
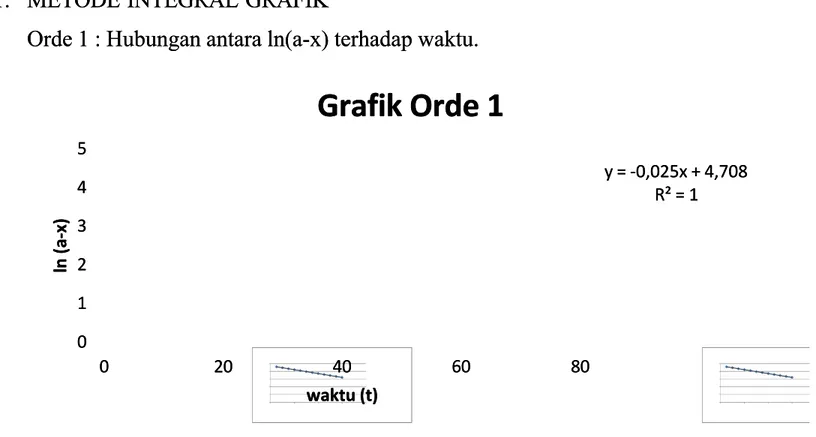
Orde 1 : Hubungan antara ln(a-x) terhadap waktu. Orde 1 : Hubungan antara ln(a-x) terhadap waktu.
Orde 2: Hubungan antara 1/(a-x) terhadap waktu. Orde 2: Hubungan antara 1/(a-x) terhadap waktu.
Dari kedua grafik diatas, diketahui bahwa yang paling memenuhi syarat ialah Dari kedua grafik diatas, diketahui bahwa yang paling memenuhi syarat ialah grafik pada orde 1 ditinjau dari nilai gradien(m) menunjukkan nilai k serta nilai R
grafik pada orde 1 ditinjau dari nilai gradien(m) menunjukkan nilai k serta nilai R 22 adalahadalah y = -0,025x + 4,708 y = -0,025x + 4,708 R² = 1 R² = 1 0 0 1 1 2 2 3 3 4 4 5 5 0 0 2200 4400 6600 8800 l l n n ( ( a a - x x ) ) waktu (t) waktu (t)
Grafik Orde 1
Grafik Orde 1
y = 0.0005x + 0.0048 y = 0.0005x + 0.0048 R² = 0.9653 R² = 0.9653 0 0 0.005 0.005 0.01 0.01 0.015 0.015 0.02 0.02 0.025 0.025 0.03 0.03 0.035 0.035 0.04 0.04 0.045 0.045 0 0 1100 2200 3300 4040 5500 6600 7700 1 1 / / ( ( a a - x x ) ) Waktu (t) Waktu (t)Grafik Orde 2
Grafik Orde 2
sama dengan 1. Sehingga dalam hal ini diketahui dari grafik didapatkan harga
sama dengan 1. Sehingga dalam hal ini diketahui dari grafik didapatkan harga k k sebesar sebesar
0,025 dan orde reaksinya adalah satu. Sehingga persamaan laju inversi gula ini adalah: 0,025 dan orde reaksinya adalah satu. Sehingga persamaan laju inversi gula ini adalah:
ln (a-x) = 1
ln (a-x) = 1 – – 0,025t 0,025t dan dan v v = = 0,025 0,025 [x][x]
Dengan menggunakan formula differensial untuk Dengan menggunakan formula differensial untuk
Maka didapat rumus tetapan laju
Maka didapat rumus tetapan laju k k bagi inversi gula, yaitu:bagi inversi gula, yaitu:
Dimana,
Dimana, k k = = tetapan tetapan konsentrasi konsentrasi laju laju reaksireaksi a
a = = konsentrasi konsentrasi mula-mulamula-mula (a-x)
(a-x) = = konsentrasi konsentrasi setiap setiap reaksireaksi t
t = = waktuwaktu
Sehingga dapat dihitung konstanta atau tetapan konsentrasi laju reaksi gula tiap 5 menit. Sehingga dapat dihitung konstanta atau tetapan konsentrasi laju reaksi gula tiap 5 menit.
2.
2. METODE INTEGRAL NONMETODE INTEGRAL NON – – GRAFIK GRAFIK
Orde 1. Untuk mencari harga k dapat digunakan rumus : Orde 1. Untuk mencari harga k dapat digunakan rumus :
ln ln ln ln a a kt kt a a xx a a a a xx k k t t t = 5 menit t = 5 menit 025 025 ,, 0 0 5 5 1331 1331 ,, 1 1 5 5 87 87 ,, 97 97 9 9 ,, 110 110 ln ln 1 1 1 1 k k k k t = 10 menit t = 10 menit 025 025 ,, 0 0 5 5 2840 2840 ,, 1 1 5 5 37 37 ,, 86 86 9 9 ,, 110 110 ln ln 1 1 1 1 k k k k t = 15 menit t = 15 menit 025 025 ,, 0 0 5 5 45499 45499 ,, 1 1 5 5 22 22 ,, 76 76 9 9 ,, 110 110 ln ln 1 1 1 1 k k k k tt = = 20 20 menit menit t t =25 =25 menit menit t t =30 =30 menitmenit
dx dx k k a a xx dt dt
ln ln aa a a xx k k t t 025 025 ,, 0 0 5 5 6487 6487 ,, 1 1 5 5 22 22 ,, 76 76 9 9 ,, 110 110 ln ln 1 1 1 1 k k k k 025 025 ,, 0 0 5 5 8682 8682 ,, 1 1 5 5 36 36 ,, 59 59 9 9 ,, 110 110 ln ln 1 1 1 1 k k k k 025 025 ,, 0 0 5 5 1170 1170 ,, 2 2 5 5 39 39 ,, 52 52 9 9 ,, 110 110 ln ln 1 1 1 1 k k k k t =35 menit t =35 menit 025 025 ,, 0 0 5 5 3988 3988 ,, 2 2 5 5 23 23 ,, 46 46 9 9 ,, 110 110 ln ln 1 1 1 1 k k k k t =40 menit t =40 menit 025 025 ,, 0 0 5 5 7182 7182 ,, 2 2 5 5 8 8 ,, 40 40 9 9 ,, 110 110 ln ln 1 1 1 1 k k k k t =45 menit t =45 menit 025 025 ,, 0 0 5 5 0802 0802 ,, 3 3 5 5 01 01 ,, 36 36 9 9 ,, 110 110 ln ln 1 1 1 1 k k k k t =50 menit t =50 menit 025 025 ,, 0 0 5 5 49 49 ,, 3 3 5 5 77 77 ,, 31 31 9 9 ,, 110 110 ln ln 1 1 1 1 k k k k t =55 menit t =55 menit 025 025 ,, 0 0 5 5 955 955 ,, 3 3 5 5 04 04 ,, 28 28 9 9 ,, 110 110 ln ln 1 1 1 1 k k k k t =60 menit t =60 menit 025 025 ,, 0 0 5 5 4816 4816 ,, 4 4 5 5 74 74 ,, 24 24 9 9 ,, 110 110 llnn 1 1 1 1 k k k k
Dari perhitungan menggunakan rumus orde 1 tersebut dihasilkan nilai k yang sama atau Dari perhitungan menggunakan rumus orde 1 tersebut dihasilkan nilai k yang sama atau konstan. Hal ini membuktikan bahwa orde reaksi inversi gula adalah berorde 1.
BAB IV BAB IV KESIMPULAN KESIMPULAN
Kesimpulan yang dapat diperoleh dari percobaan ini adalah : Kesimpulan yang dapat diperoleh dari percobaan ini adalah :
1.
1. Pada percobaan ini terjadi hidrolisis gula menjadi glukosa dan fruktosa ditandai denganPada percobaan ini terjadi hidrolisis gula menjadi glukosa dan fruktosa ditandai dengan sudut putar dari waktu ke waktu menurun secara berturut turut.
sudut putar dari waktu ke waktu menurun secara berturut turut. 2.
2. Pada percobaan ini orde reaksi yang terjadi adalah orde reaksi satu (pseudo) karena lajuPada percobaan ini orde reaksi yang terjadi adalah orde reaksi satu (pseudo) karena laju reaksi hanya tergantung pada satu kosentrasi saja yaitu [C
reaksi hanya tergantung pada satu kosentrasi saja yaitu [C1212HH2222OO1111] sedangkan H] sedangkan H22OO
tidak berpengaruh dalam reaksi tersebut. tidak berpengaruh dalam reaksi tersebut.
DAFTAR PUSTAKA DAFTAR PUSTAKA
Lailatul. 2011.
Lailatul. 2011. PAPER LAPORAN PRAKTIKUM KIMIA FISIKA II PAPER LAPORAN PRAKTIKUM KIMIA FISIKA II I INVERSI GULAI INVERSI GULA..
http://www.scribd.com/doc/73241057/Paper-Inversi-Gula-2003
http://www.scribd.com/doc/73241057/Paper-Inversi-Gula-2003 (27 Oktober (27 Oktober 2012)
2012) Sonny. 2011.
Sonny. 2011. LAJU INVERSI LAJU INVERSI GULAGULA.. http://www.scribd.chttp://www.scribd.com/doc/69515637om/doc/69515637/Laporan-KF-
/Laporan-KF-03
03(27 Oktober 2012)(27 Oktober 2012) Reski Wahyudi, Udin.2011.
Reski Wahyudi, Udin.2011. Polarimeter Polarimeter . http://www.wahyudi.blogspot.com (27. http://www.wahyudi.blogspot.com (27
Oktober 2012) Oktober 2012) Tim. 2012.
Tim. 2012. PANDUAN PRAKTIKUM PANDUAN PRAKTIKUM KIMIA FISIKA III KIMIA FISIKA III . Surabaya : Unesa Press. Surabaya : Unesa Press
Yanuarin. 2011.
Yanuarin. 2011. MAKALAH MAKALAH KF KF REV REV .. http://www.scribd.com/doc/87036221/Makalah-
http://www.scribd.com/doc/87036221/Makalah-KF-Rev#download