FITOAKUMULASI ION LOGAM TEMBAGA(II) OLEH TANAMAN LIDAH MERTUA (Sansevieria trifasciata Prain)
Ayu Ika Pratiwi1*, Asmawati, Syarifuddin Liong
1Laboratorium Analitik, Jurusan Kimia, Fakultas MIPA, Universitas Hasanuddin
2Jurusan Kimia, Fakultas MIPA, Universitas Hasanuddin, Jl. Perintis Kemerdekaan KM 10, Tamalanrea Makassar, Indonesia 90245
*E-mail :
[email protected]
ABSTRAK
Limbah Cu yang bersumber dari aktivitas industri memiliki sifat toksik bagi makhluk hidup. Pengolahan limbah Cu dapat dilakukan dengan teknik fitoremediasi yaitu teknik pembersihan lingkungan yang tercemar dengan memanfaatkan tanaman hiperakumulator dan telah dikembangkan menjadi metode yang murah dan ramah lingkungan. Pada penelitian ini digunakan tanaman lidah mertua (Sansevieria trifasciata Prain) untuk menarik ion logam berat Cu(II) dari tanah dengan variasi waktu sehingga dapat diketahui pengaruh waktu terhadap penyerapan ion Cu2+ serta
variasi konsentrasi untuk mengetahui konsentrasi terbesar yang dapat ditarik oleh tanaman tersebut. Konsentrasi ion logam Cu(II) yang telah ditarik dapat diketahui dengan menggunakan Spektrofotometer Serapan Atom (SSA). Hasil penelitian menunjukkan bahwa pada pekan kedua dengan variasi konsentrasi 400ppm sebesar 256,2748mg/kg berat kering. Ion logam Cu(II) yang terserap terdistribusi paling besar pada bagian akar. Dapat disimpulkan bahwa tanaman ini tidak hiperakumulator terhadap logam Cu.
Kata kunci: Fitoremediasi, Hiperakumulator, Lidah Mertua, Tembaga.
ABSTRACT
The waste of Cu source from industrial activities have toxic properties in for living things. The waste treatment Cu can be done with phytoremediation technique which is a technique of cleaning a polluted environment by utilizing hiperakumulator plants and has developed into a method that is cheap and environmentally friendly. In this experiment, the plants Sansevieria trifasciata Prain to attract heavy metal ions Cu(II) on the ground with the variation of time so that it can be seen the influence of time on the absorption of Cu2+ ions and varying concentrations to determine the
concentration of the largest that can be drawn by the plant. The concentration of metal ions Cu(II) which has been drawn can be determined using Atomic Absorption Spectrophotometer (AAS). The results showed that in the second week with a variation of 400 ppm of 256.2748 mg / kg dry weight. Metal ions Cu(II), which absorbed most distributed in the roots. It can be concluded that the plant is not hiperakumulator against Cu.
PENDAHULUAN
Logam berat banyak digunakan dalam berbagai bidang industri maupun rumah tangga. Hal ini menyebabkan konsentrasi logam berat terus meningkat pada strata lingkungan air, udara, dan tanah. Akibat peningkatan logam berat ini memberikan dampak negatif bagi makhluk hidup, baik dari sifat toksik maupun karsinogeniknya (Hardiani, 2009).
Beberapa logam berat yang berbahaya dan sering mencemari lingkungan adalah merkuri (Hg), timbal (Pb), arsen (As), kobal (Co), tembaga (Cu), kadmium (Cd), krom (Cr), dan nikel (Ni). Logam berat dapat masuk kedalam tubuh organisme melalui makanan dan minuman serta pernafasan dan kulit. Logam berat tersebut tetap tinggal dalam tubuh dalam jangka waktu yang lama sebagai racun (Fardiaz, 2008). Logam berat terbagi atas logam esensial dan non-esensial. Logam berat esensial adalah jenis logam berat yang dibutuhkan oleh tubuh dalam konsentrasi kecil dan berbahaya bila melewati ambang batas (Sembel, 2015), sedangkan logam berat non-esensial adalah jenis logam berat yang tidak diketahui manfaatnya bagi tubuh dan cenderung menimbulkan gangguan bagi kelangsungan hidup organisme walaupun dalam jumlah yang kecil (Sumardjo, 2008).
Tembaga (Cu) merupakan salah satu jenis logam berat yang bersifat esensial (Hamzah dan Setiawan, 2010). Logam Cu sangat berguna untuk perumbuhan jaringan tumbuhan terutama jaringan daun tempat terjadinya proses fotosintesis (Kamaruzzaman dkk., 2009). Menurut Rosmarkam dan Yuwono (2002), apabila ketersediaan logam Cu di dalam tanah telah mencapai 100mg/kg maka akan mencemari tanah tersebut.
Beberapa penelitian telah dilakukan dalam upaya mengatasi pencemaran logam berat, diantaranya menggunakan metode presipitasi (pengendapan), osmosis, metode pertukaran ion, resin pengkhelat, membran pemisah, oksidasi reduksi, filtrasi dan adsorpsi menggunakan karbon. Namun metode ini lebih mahal dan tidak efisien (Aiyen, 2004).
Salah satu cara untuk memulihkan lingkungan tanah dari suatu kontaminan logam berat adalah dengan menggunakan tanaman, yaitu dengan cara menanam jenis-jenis tanaman yang mampu menyerap logam berat dari dalam tanah. Metode ini dikenal dengan nama fitoremediasi (Raskin dkk., 1997). Fitoremediasi juga sering disebut sebagai bioremediasi botani (Chaney dkk., 1997). Fitoremediasi merupakan sebuah teknologi baru alami dan ramah lingkungan yang dapat dipertimbangkan untuk remediasi tanah yang terkontaminasi karena keuntungan estetika dan penerapan jangka panjang (Huang dkk., 2004). Teknologi ini juga sangat efisien digunakan karena mudah dan biaya yang digunakan relatif murah, serta telah diterima dengan baik oleh masyarakat luas (Singh dkk., 2009; Turan dan Esringu, 2007; Revathi dkk., 2011; Luqman dkk., 2013).
Penelitian yang dilakukan oleh Ogunkunle dkk. (2013) mengenai fitoremediasi logam Cu dengan menggunakan tanaman tomat (Lycopersicones culentum) dan tanaman bayam duri (Amaranthus hybridus) mampu
mengakumulasi masing-masing 171,1mg/kg dan
144,1mg/kg. Menurut Ariyakanon dan Winaipanich (2006) pada tanaman sawi india (Brassica juncea L.) dan tanaman ketul (Bidens alba) dapat mengakumulasi konsentrasi sebesar 3.771mg/kg dan 879mg/kg.
Sedangkan, menurut Syaputra (2005) tanaman eceng gondok (Eichhornia Crassipes (Mart.) Solms) dapat mengakumulasi sebesar 442,895µg/g.
Setiap tanaman memiliki kemampuan
mengakumulasi berbagai jenis logam berat yang berbeda-beda. Untuk menentukan kemampuan tanaman dalam mengakumulasi logam tertentu maka digunakan faktor biokonsentrasi (BCF) dan faktor translokasi (FT) (Siahaan dkk., 2013). Faktor biokonsentrasi merupakan parameter yang berguna untuk mengevaluasi potensi biota untuk mengakumulasi logam dan nilai ini dihitung berdasarkan berat kering (Wardani dkk., 2014). Sedangkan faktor translokasi digunakan untuk mengetahui potensi tanaman untuk fitoremediasi (Yoon dkk., 2006).
Tanaman lidah mertua (Sansevieria trifasciata P.) merupakan salah satu spesies dari 60 spesies tanaman Sansevieria yang tersebar diseluruh dunia terutama di daerah kering dan gersang seperti Afrika yang menjadi pusat keanekaragaman tanaman ini (Lu dan Morden, 2014). Di Afrika Selatan dan Amerika, tanaman ini digunakan untuk pengobatan pada peradangan dan dijual sebagai obat mentah di pasar untuk mengobati korban gigitan ular (Antunes dkk., 2003) dan sebelumnya telah banyak dimanfaatkan sebagai absorben polutan (Tchegnitegni dkk., 2015). Tanaman ini mampu mengakumulasi polutan logam berat karena mengandung senyawa-senyawa kimia seperti β-sitosterol (Gonzalez dkk., 1972), steroidal saponin (Said dkk., 2015; Mimaki dkk., 1996) dan memiliki gugus sulfidril (-SH) serta gugus karbonil (-CO) yang berpotensi untuk mengikat logam berat.
Permasalahan mengenai pencemaran logam berat serta adanya teknik fitoremediasi yang sangat menunjang, maka perlu dikembangkan penelitian mengenai jenis tanaman yang mampu mengakumulasi logam berat dan berpotensi untuk dijadikan sebagai tanaman hiperakumulator. Pada penelitian ini, digunakan tanaman lidah mertua untuk mengakumulasi logam Cu2+, pada tanah tercemar.
METODOLOGI Bahan
Bahan-bahan yang digunakan pada penelitian ini adalah CuSO4.5H2O, tanah, bibit tanaman lidah mertua
(Sansevieria trifasciata Prain), H2O2 30%, HNO3 6M,
akuades, akuabides, kertas pH universal, kertas saring Whatman No. 42.
Alat
Alat-alat yang digunakan pada penelitian ini adalah baskom, pot bunga, neraca analitik, oven, desikator, hot plate, cawan petri, lumpang, sendok tanduk, peralatan pembuatan limbah buatan, alat gelas
yang umum digunakan di laboratorium, dan
Spektrofotometer Serapan Atom (SSA) Back Scientific model 205 VGP.
Prosedur Kerja
A. Penyiapan Media Tanah
Tanah yang digunakan dalam penelitian ini diambil dari perkebunan sayur-sayuran. Tanah tersebut dibersihkan dari batuan dan akar-akaran yang ada. Kandungan Nitrogen, Phosfat, Kalium, Tembaga (Cu),
Kapasitas Tukar Kation (KTK) dan bahan organik dalam tanah dianalisis di Laboratorium.Tanah kemudian dibiarkan selama dua minggu sambil diaduk dan diangin-anginkan.
B. Penyiapan Media Tanam
Beberapa pot bersih diisi dengan 1 kg tanah yang telah dicampur dengan ion Cu(II). Tanah kemudian ditaburi dengan pupuk kompos, lalu disiram dengan akuades. Kontrol dilakukan dengan menggunakan pot yang berukuran sama dan jumlah tanah yang sama tetapi tanah yang digunakan tidak mengandung ion-ion tersebut.
C. Pembuatan Tanah Terkontaminasi Ion Cu(II)
Pembuatan tanah yang terkontaminasi dengan ion Cu(II), konsentrasi yang diinginkan dalam penelitian ini terlebih dahulu ditentukan. Konsentrasi ion Cu(II) yang digunakan adalah 100 ppm (100mg/kg), 200 ppm, 400 ppm, dan 800 ppm.
D. Penanaman Tanaman Lidah Mertua
Tanaman Lidah Mertua yang berumur ± 1bulan ditanam di pot yang telah disediakan. Setiap hari, benih disiram dengan akuades. Panen dilakukan setiap minggu selama empat minggu. Lidah mertua yang telahdipanen dicuci dengan air bebas mineral hingga bersih dari tanah dan benda-benda lainnya. Akar dan tungkai daun yang telah bersih dipisahkan kemudian disimpan dalam kantong plastik dan siap dianalisis secara kimia.
E. Analisis kadar ion Cu(II) pada Akar dan tangkai daun
Metode analisis jumlah ion-ion Cu(II) mengacu kepada prosedur kerja yang telah digunakan oleh Hummer (2002), Pioterowesk-Cyplik dan Csamekai (2005), Nouairi dkk (2005), Aiyen (2004), Dancavee dkk (2000). Pada umumnya peniliti-peneliti tersebut mengatakan bahwa untuk analisis ion logam yang terkandung dalam bahan organik, cara basah lebih baik digunakan daripada cara organik.
Akar dan tangkai daun yang telah bersih diangin-anginkan beberapa jam. Kemudian, ditimbang dengan teliti pada Petridish yang telah diketahui berat kosongnya. Bagian tanaman tersebut dipanasakan dalam oven selama 24jam pada suhu 80oC, kemudian
didinginkan dalam desikator. Bagian tanaman yang kering ditimbang kembali sehingga diketahui berat yang hilang sebagai jumlah air yang terkandung dalam akar dan tangkai daun. Sampel kering ini digerus pada lumpang porselen. Contoh yang telah digerus ditimbang kira-kira 0,5g dengan neraca analitik. Contoh tersebut dilarutkan dalam 5ml HNO3 6M dan 5ml H2O2 30%,
dipanaskan sampai semua materi larut sempurna. Larutan didinginkan, ditambahkan akuades, dipanaskan dan disaring dalam keadaan panas kedalam labu ukur 50ml. Larutan sampel ini diatur pHnya dengan HNO3 dan NaOH hingga pH-nya sekitar 2-3. Larutan diimpitkan hingga tanda batas dengan aquades dan dikocok hingga homogen. Larutan siap diukur dengan Spektrofotometer Serapan Atom (SSA).
F. Penentuan Waktu Optimum Akumulasi Cu(II)
Penentuan waktu optimum penyerapan ion Cu(II) oleh lidah mertua, panen dilakukan setelah
tanaman berumur satu minggu. Panen selanjutnya dilakukan tiap minggu selama 4 minggu. Setiap selesai panen, lidah mertua dibersihkan dari tanah dan kotoran-kotoran lainnya kemudian akar dan tangkai daun dipisahkan dan dianalisis seperti prosedur E. Waktu optimum merupakan waktu dimana penyerapan ion Cu(II) maksimum yang dapat diperoleh dari kurva antara konsentrasi versus waktu penyerapan.
G. Pengaruh Konsentrasi Terhadap Jumlah Ion yang terakumulasi dalam tanaman lidah mertua
Penentuan konsentrasi ion Cu(II) dalam media tumbuh terhadap jumlah ion yang terkamulasi tanah, terkontaminasi ion Cu(II) dengan variasi konsentrasi 100ppm, 200ppm, 400ppm dan 800ppm. Kemudian tanah-tanah yang terkontaminasi ini ditanami lidah mertua sesuai dengan prosedur D. panen dilakukan pada minggu ke-3 sesuai dengan waktu optimum yang diperoleh pada prosedur F. Selanjutnya kandungan ion Cu(II) pada akar dan tangkai daun lidah mertua dianalisis sesuai dengan prosedur E.
H. Mekanisme akumulasi Cu(II) pada lidah mertua
Penentuan mekanisme akumulasi logam berat pada tanaman dilakukan sesuai dengan prosedur Gosh dan Singh (2005) dengan menghitung faktor biokonsentrasi (BCF) dan factor translokasi (TF) dengan rumus berikut: BK) (mg/kg tanah dalam ke n ditambahka yang [M] BK) (mg/kg an akar tanam bagian pada [M] rasi biokonsent Faktor BK) (mg/kg akar dalam [M] BK) (mg/kg daun dalam [M] nslokasi Faktor tra
HASIL DAN PEMBAHASAN A. Analisis Pendahuluan
Analisis pendahuluan dilakukan dengan menganalisis sifat fisik dan kimia tanah yang akan dijadikan sebagai media tanam karena sifat-sifat tersebut sangat penting untuk diketahui sebelum melakukan proses penanaman. Adapun parameter uji yang dianalisis yaitu N, P, K, pH, KTK (Kapasitas Tukar Kation) dan kandungan bahan organik untuk mengetahui tingkat kesuburan tanah tersebut. Hasil analisis menunjukkan bahwa tanah tersebut merupakan tanah dengan tekstur yang sesuai dengan pertumbuhan tanaman lidah mertua.Tanah ini termasuk jenis lempung liat berpasir atau lebih dikenal sebagai tanah alluvial. Tekstur tanah sangat penting untuk penentuan karakteristik tanah, air yang tersimpan, ukuran pori, kesuburan tanah serta pH tanah yang digunakan yaitu 5,1.
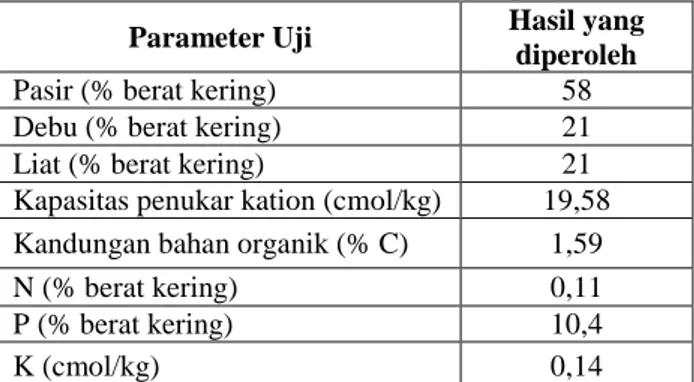
Tabel 1. Sifat fisik dan kimia tanah yang digunakan
Parameter Uji Hasil yang
diperoleh
Pasir (% berat kering) 58
Debu (% berat kering) 21
Liat (% berat kering) 21
Kapasitas penukar kation (cmol/kg) 19,58
Kandungan bahan organik (% C) 1,59
N (% berat kering) 0,11
P (% berat kering) 10,4
Kapasitas Tukar Kation (KTK) yaitu kemampuan absorpsi kation (logam berat) dan kemampuan penukaran kation antara kation yang ada dalam tanah dan larutan.Nilai kapasitas tukar kation pada tanah yang digunakan adalah 19,58cmol/kg dan termasuk dalam daerah sedang (17-24cmol/kg).
Kandungan bahan organik dapat mempengaruhi kandungan mineral tanah sifat fisik dan kimia tanah. Berdasarkan hasil analisis pendahuluan terhadap tanah yang digunakan terdapat C sebesar 1,59% dan N sebesar 0,11% yang menurut FAO (1986) termasuk dalam kategori rendah (1-1,9%).
Selain itu, dilakukan pula analisis kandungan logam berat Cu yang ada didalam tanah dan pupuk sebelum digunakan pada proses penanaman lidah mertua. Tabel 2 menunjukkan kandungan Cu dari tanah tersebut.
Tabel 2. Kandungan Cu dalam tanah dan pupuk
Bahan Uji Cu (mg/kg)
Tanah 6,41
Pupuk Kompos 0,5607
Pupuk Pertanian TT
Hasil analisis pendahuluan menunjukkan bahwa tanah yang digunakan dalam penelitian ini telah mengandung logam berat Cu tetapi tidak memberikan efek negatif bagi tanaman yang tumbuh di tempat tersebut. Hasil analisis sifat fisika dan kimia tanah juga menunjukkan bahwa beberapa parameter uji dianggap telah memenuhi syarat untuk penanaman lidah mertua walaupun kandungan nitrogen, kalium dan fosfat masih rendah, namun penggunaan pupuk urea, NPK dan KCl tidak dianjurkan karena pada tanaman lidah mertua tidak terlalu baik jika menggunakan pupuk tersebut sehingga pupuk yang dianjurkan untuk digunakan yaitu pupuk kompos.
B. Analisis Kandungan Kadar Air pada Tanaman Lidah Mertua
Kadar air rata-rata yang diserap oleh tanaman lidah mertua dapat dilihat pada Tabel 3.
Tabel 3. Kadar Air tanaman lidah mertua
Sampel Morfologi Kadar Air (%)
I II III IV Kontrol Akar 2,81 19,15 16,99 10,01 Daun 12,00 14,26 16,39 14,93 Total 14,81 33,41 33,38 24,94 100ppm Akar 15,64 9,40 15,39 14,76 Daun 23,22 13,41 11,56 16,32 Total 38,86 22,81 26,95 31,08 200ppm Akar 5,87 13,07 10,55 13,37 Daun 12,34 34,38 0,04 14,76 Total 18,21 47,45 10,59 28,13 400ppm Akar 5,76 3,61 4,65 13,03 Daun 13,48 12,09 10,49 15,97 Total 19,24 15,70 15,14 19,00 800ppm Akar 12,48 10,52 12,24 12,20 Daun 14,43 12,25 16,30 37,06 Total 26,91 22,77 28,54 49,26 Rata-Rata 23,61 28,43 22,92 30,48
Berdasarkan tabel diatas menunjukkan nilai rata-rata kadar air dari tanaman lidah mertua cukup baik yaitu
30,48%. Hal ini menunjukkan adanya distribusi logam yang terjadi dalam jaringan dari akar menuju tungkai daun karena adanya penyerapan air yang membantu proses distribusi logam.
C. Analisis Kandungan Ion Cu(II) Setelah Akumulasi
Jumlah ion Cu(II) yang terakumulasi pada tanaman lidah mertua sebagai fungsi waktu panen serta sebagai fungsi konsentrasi ion yang ditambahkan dalam media tanam ditunjukkan pada Gambar 5.
Tabel 5. Jumlah Ion Cu(II) yang diakumulasi oleh tanaman lidah mertua
Sampel
Penyerapan di minggu ke- (mg/kg)
I II III IV Kontrol 25.2296 15.8057 19.435 33.7757 100 ppm 21.8949 24.1103 116.8553 21.2428 200 ppm 26.6449 29.4308 33.3104 11.4279 400 ppm 23.1758 256.2748 30.9848 21.7089 800 ppm 26.3104 23.6339 20.0373 36.6278
Hasil analisis menunjukkan pada masing-masing konsentrasi terjadi perbedaan penambahan jumlah akumulasi logam. Terlihat pada minggu pertama jumlah akumulasi terbanyak yaitu 26,6449mg/kg pada konsentrasi ion Cu(II) 200ppm dalam tanah sedangkan pada minggu kedua maksimum akumulasi terjadi pada
konsentrasi Cu(II) 400ppm yaitu sebanyak
256,2748mg/kg.
Akumulasi tertinggi di minggu ketiga terdapat
pada konsentrasi Cu(II) 100ppm sebanyak
116,8553mg/kg. Hasil yang berbeda ditunjukkan di minggu keempat, pada minggu tersebut jumlah akumulasi ion Cu(II) cenderung rendah dibandingkan dengan minggu-minggu sebelumnya serta jumlah yang diakumulasi juga jauh lebih rendah dibandingkan dengan kontrol.
Perbedaan penyerapan dari masing-masing tanaman sangat jelas berbeda, hal ini dapat dipengaruhi oleh beberapa faktor yaitu diantaranya jumlah akar tanaman yang tidak merata serta ukuran akar yang berbeda-beda sehingga mengakibatkan perbedaan jumlah ion Cu(II) yang dapat masuk kedalam tanaman.
Menurunnya jumlah akumulasi ion Cu(II) di minggu keempat ini juga dimungkinkan oleh kemampuan tanaman dalam mengakumulasi logam sudah berkurang atau telah melewati titik maksimum penyerapannya.
D. Penentuan Mekanisme Penyerapan dari Tanaman Lidah Mertua
Tanaman hiperakumulator adalah tanaman yang mampu untuk mengkonsentrasikan logam di dalam biomassanya dalam kadar yang luar biasa tinggi (Baker dkk., 2000). Defenisi lain yaitu spesies tanaman yang mampu mentranslokasikan polutan atau logam pencemar
ke bagian pucuk tanaman lebih banyak tanpa mengalami gejala toksisitas (Lasat, 2000). Tanaman yang dapat dikatakan hiperakumulator terhadap logam Cu jika dapat menyerap ion logam Cu(II) sebanyak 1000mg/kg berat kering (Watanabe, 1997).
Tanaman lidah mertua merupakan salah satu jenis tanaman hiperakumulator karena karena mengandung protein yang memiliki gugus amina (-NH2),
gugus karboksil (-COOH), juga gugus sulfidril (-SH) yang mampu mengikat logam berat.
HS H2 C HC C HN C H H2 C H2 C C NH C HC CH2 HS H N C H2 C NH2 O O OH O C O OH O + Cu 2+ HS H2 C HC C HN C H H2 C H2 C C NH C HC CH2 HS H N C H2 C NH2 O O O H O C O OH O SH H2 C H C C H N C H H2 C H2 C C NH C CH H2C SH H N C H2 C H2N O O HO O C O HO O Cu2+
Gambar 4. Mekanisme Pengikatan Logam dalam Tanaman
Hasil analisis yang diperoleh menunjukkan bahwa tanaman lidah mertua tidak hiperakumulator terhadap logam Cu karena secara keseluruhan penyerapan tanaman ini terhadap ion logam Cu tidak ada yang mencapai 1.000mg/kg dan penyeran tertinggi sebanyak 256,2748mg/kg berat kering.
Kemampuan tanaman dalam mentranslokasikan logam dapat diukur dari nilai faktor biokonsentrasi (BCF) dan faktor translokasi (FT) (Yoon dkk., 2006). BCF didefinisikan sebagai rasio konsentrasi logam dalam akar dengan konsentrasinya dalam tanah.Sedangkan, TF didefinisikan sebagai rasio konsentrasi logam dalam
pucuk terhadap konsnetrasinya dalam akar
(Fitz dan Wenzel, 2002).Nilai BCF dan TF dapat dilihat pada Tabel 6.
Tabel 6. Nilai BCF dan TF tanaman lidah mertua
Waktu Sampel Nilai BCF Nilai TF
I 100ppm 0,0162 0,9535 200ppm 0,0210 0,4849 400ppm 0,0145 0,5212 800ppm 0,0094 0,9310 II 100ppm 0,0232 0,3759 200ppm 0,0244 0,4148 400ppm 0,2265 0,0734 800ppm 0,0091 0,7857 III 100ppm 0,0227 0,5778 200ppm 0,0227 5,8271 400ppm 0,0248 0,7155 800ppm 0,0080 0,1874 IV 100ppm 0,0148 0,9004 200ppm 0,0052 1,5968 400ppm 0,0086 1,3889 800ppm 0,0182 0,3845
Pada tabel,terlihat bahwa nilai BCF rendah (>1) dan nilai TF cukup rendah, walaupun terdapat sampel yang memiliki nilai TF yang lebih tinggi (<1). Nilai BCF yang tinggi menunjukkan kemampuan yang besar dalam menarik logam dari dalam tanah sedangkan kemampuan untuk mentranslokasikan ke tungkai daun rendah terlihat dari nilai TF yang rendah.
Berdasarkan data yang diperoleh, kemampuan tanaman lidah mertua dalam mentranslokasikan logam tidak termasuk dalam kategori fitoekstraksi ataupun fitostabilisasi.Hal ini disebabkan oleh data nilai BCF maupun TF dari tanaman lidah mertua tidak sesuai dengan teori. Berdasarkan teori, tanaman yang cocok untuk fitoekstraksi jika memiliki nilai BCF <1 dan TF >1, sedangkan untuk fitostabilisasi apabila nilai BCF >1 dan TF <1 (Liong dkk., 2010). Namun, dari data keseluruhan menunjukkan jumlah ion logam Cu(II) terbanyak terdapat di akar sehingga dapat disimpulkan bahwa mekanisme akumulasi yang terjadi pada tanaman lidah mertua yaitu rhizofiltrasi.
Proses rhizofiltrasi adalah metode fitoremediasi dimana akar tumbuhan dapat mengabsorpsi dan mengendapkan zat kontaminan sehingga jumlah ion logam diakar akan lebih banyak terdapat diakar dbandingkan dibagian tanaman lainnya (Etim, 2012).
Kemampuan tanaman yang rendah dalam mentranslokasikan logam dapat dipengaruhi oleh faktor genetika yaitu tanaman cenderung menyimpan logam di akar daripada mengirimnya ke bagian atas tanaman.
E. Distribusi ion Cu(II) pada tanaman lidah mertua
Tabel 7 menunjukkan bahwa secara keseluruhan distribusi ion logam Cu(II) pada tanaman lidah mertua paling banyak ada di akar. Pada umumnya tanaman akan menunjukkan gejala tersebut terkecuali pada tanaman yang mekanismenya fitoekstraksi.
Tabel 7. Distribusi ion Cu(II) pada tanaman lidah mertua
Sampel Morfo logi
Penyerapan di minggu ke- (mg/kg)
I II III IV Kontrol Akar 13,7839 8,7977 12,3176 26,1876 Daun 11,4457 7,0080 7,1174 7,5881 100 ppm Akar 11,2082 17,5229 17,1164 11,1778 Daun 10,6867 6,5874 99,7389 10,0650 200 ppm Akar 17,9445 20,8024 19,4175 4,4008 Daun 8,7004 8,6284 13,8929 7,0271 400 ppm Akar 15,2348 238,7449 26,0943 9,1042 Daun 7,9410 17,5299 4,8905 12,6447 800 ppm Akar 13,6250 13,2353 11,6624 26,4564 Daun 12,6854 10,3986 8,3749 10,1714
Distribusi logam dipengaruhi oleh beberapa faktor yaitu kemampuan tanaman itu sendiri dalam mentranslokasikan logam ke daun. Jika tanaman mempunyai kemampuan yang rendah dalam mengirim logam ke bagian atas tanaman, maka logam akan lebih banyak diendapkan di vakuola sel akar daripada mengirimnya ke pembuluh angkut. Logam dapat mencapai daun jika melalui pembuluh angkut yaitu xylem, dan logam pada tanaman akan mengendap di akar ketika kemampuan mengirim logam ke pembuluh angkut berkurang. Hal ini kemungkinan disebabkan hanya sedikit sistem pengangkut logam yang dapat menembus pembuluh angkut karena tergantung dari genetika tumbuhan (Barcelo dan Poschenrieder, 2003).
Penyebab lain menumpuknya logam berat Cu diakar dikarenakan jumlah zat khelat yang lebih banyak terdapat pada akar serta akar yang dimiliki tanaman lidah mertua termasuk dalam akar serabut berupa rambut-rambut halus yang memungkinkan banyaknya logam berat yang dapat terjerap kedalam akar.
Kesimpulan
Berdasarkan pembahasan atas penelitian yang telah dilakukan, dapat disimpulkan sebagai berikut: 1. tanaman lidah mertua tidak berpotensi sebagai
tanaman hiperakumulator terhadap logam Cu. 2. akumulasi ion logam Cu(II) pada tanaman lidah
mertua terbesar pada minggu kedua dan pada konsentrasi 400ppm sebesar 256,2748mg/kg berat kering.
3. jenis mekanisme fitoremediasi yang terjadi pada tanaman lidah mertua yaitu rhizofiltrasi.
Saran
Untuk penelitian selanjutnya diharapkan dapat menggunakan variasi konsentrasi serta variasi waktu panen yang lebih lama. Pengujian juga dapat dilakukan pada tanah yang benar-benar telah tercemar oleh logam berat.
DAFTAR PUSTAKA
Aiyen, 2004, Importance of Root Growth Paramterers to Cd and Zn Aequistion by Non-hyperaccumulator and Hyperaccumulator Plants, Dissertation University of Hohenheim, Institute of Plant Nutrition, VerlagGraner-Meuren-Stutgard. Antunes, A.D.S., Silva, B.P.D., Parente, J.P., dan
Valente, A.P., 2003, A New Bioactive Steroidal Saponin from Sansevieria cylindrical, Phytotherapy Research, 17(2): 179-182.
Ariyakanon, N., danWinaipanich, B., 2006,
Phytoremediation of Copper Contaminated Soil by Brassica juncea (L.) Czern and Bidens alba(L.) DC. var. radiate, J. Sci. Res. Chula. Univ, 31(1): 49-56.
Baker, A.J.M., McGrath, S.P., Reeves, R.D., danSmitch, J.A.C., 2000, Metal Hyperaccumulator Plants: A review of The Ecology and Physiology of A Biological Resource for Phytoremediation of
Metal-Polluted Soils, University of Oxford, Inggris.
Chaney, R.L., Malik, M., Li, Y.M., Brown, S.L., Brewer, E.P., Angle J.S., dan Baker, A.J.M., 1997, Phytoremediation of Soil Metals, Current Opinion in Biotechnology, 8(3): 279-284. Etim, E.E., 2012, Phytoremediation and Its Mechanisms:
A Review, International Journal of Environment and Bioenergy, 2(3): 120-136.
Fardiaz, S., 2008, Polusi Air dan Udara, Kanisius, Yogjakarta.
Fitz, W.J., dan Wenzel, W.W., 2002, Arsenic Transformations In The Soil/Rhizosphere/Plant System:Fundamentals And Potential Application To Phytoremediation, Journal of Biotechnology,
99(3): 259-278.
Gonzalez, A.G., Freire, R., Garcia-Estrada, M.G., Salazar, J.A., dan Suarez, E., 1972, New Sources Of Steroid Sapogenins-XIV 25S-Ruscogenin and Sansevierigenin, Two New Spirostan Sapogenins From Sansevieria trifasciata, Tetrahedron, 28: 1289-1297.
Hamzah, F., dan Setiawan A., 2010, Akumulasi Logam Berat Pb, Cu, dan Zn di Hutan Mangrove Muara Angke Jakarta Utara, Jurnal Ilmu dan Teknologi Kelautan Tropis, 2(2): 41-52.
Hardiani, H., 2009, Potensi Tanaman Dalam Mengakumulasi Logam Cu Pada Media Tanah Terkontaminasi Limbah Padat Industri Kertas, Biosains, 44(1): 27-40.
Huang, X.D., El-Alawi, Y., Penrose, D.M., Glick, B.R., Greenberg, B.M., 2004, A Multi-process Phytoremediation System For Removal of Polycyclic Aromatic Hydrocarbons From Contaminated Soils, Environmental Pollution,
130(3): 465-476.
Kamaruzzaman, B.Y., Ong, M.C., Jalal, K.C.A., Sahbudin, S., dan Nor O.M., 2009, Accumulation of Lead and Copper In Rhizoporaapiculata From Setiu Mangrove Forest, Terengganu, Malaysia, Journal of Environmental Biology, 30(5): 821-824.
Lasat, M.M., 2000, Phytoextraction Of Metals From
Contaminated Soil: A Review Of
Plant/Soil/MetalInteraction And Assessment Of Pertinent Agronomic Issues, Journal of Hazardous Substance Research, 2(5): 1-25. Liong, S., Noor, A., Taba, P., dan Abdullah, A., 2010,
Studi Fitoakumulasi Pb dalam Kangkung Darat
(Ipomoea reptans Poir), (Online),
(http://www.pustaka.ac.id), diakses pada tanggal 14 Maret 2016 pukul 21.35 WITA.
Lu, P-L., danMorden, C.W., 2014, Phylogenetic Relationships Among Dracenoid Genera (Asparagaceae: Nolinoideae) Inferred From Chloroplast DNA Loci, Systematic Botany,
39(1): 90-104.
Luqman M., Butt, T.M., Tanvir, A., Atiq, M., Hussan, M.Z.Y., danYaseen, M., 2013, Phytoremediation of Polluted Water By Trees: A Review, African Journal of Agricultural Research, 8(17): 1591-1595.
Mimaki Y., Inoue, T., Kuroda, M., danSashida, Y., 1996, Steroidal Saponins From Sansevieria trifasciata, Elsevier Science Ltd., 43(6): 1325-1331.
Ogunkunle, C.O., Fatoba, P.O., Awotoye, O.O., dan Olorunmaiye, K.S., 2013, Root-Shoot Partitioning of Copper, Chromium and Zinc in Lycopersicones culentum and Amaranthus hybridus Grown in Cement-Polluted Soil, Environmental and Experimental Biology, 11: 131-136.
Raskin, I., dan Ensley, B.D., 1999, Phytoremediation Of Metals: Using Plants to Clean Up The Environment, Environmental Pollution And Green Plants, ISSN: 978-0-471-19254-1. Raskin, I., Smith, R.D., dan Salt, D.E., 1997,
Phytoremediation Of Metals: Using Plants to Remove Pollutants From The Environment, Current Opinion in Biotechnology, 8(2): 221-226.
Revathi, K., Haribabu, T.E., danSudha, P.N., 2011, Phytoremediation of Chromium Contaminated Soil Using Sorghum Plant, International journal of Environmental Sciences, 2(2): 429-440. Rosmarkam, A., danYuwono, N.W., 2002, Ilmu
Kesuburan Tanah, Kanisius, Yogyakarta. Said, A., Aboutabl, E.A., Melek, F.R., Jaleel, G.A.R.A.,
danRaslan, M., 2015, Steroidal Saponins and Homoisoflavanone From The Aerial Parts Of Sansevieria cylindria Bojer ex Hook, Phytochemistry Letters, 12: 113-118.
Sembel, D.T., 2015, Toksikologi Lingkungan: Dampak Pencemaran dari Berbagai Bahan Kimia dalam Kehidupan Sehari-hari, Andi Offset, Yogyakarta.
Siahaan, M.T.A., Ambariyanto, danYulianto, B., 2013, Pengaruh Pemberian Timbal (Pb) dengan Konsentrasi Berbeda Terhadap Klorofil, Kandungan Timbal Pada Akar dan Daun, Serta Struktur Histologi Jaringan Akar Anakan Mangrove Rhizophora mucronata, Journal of Marine Research, 2(2): 111-119.
Singh, K., Eapen S., danFulekar, M.H., 2009, Potential of Medicago sativa for Uptake of Cadmium From
Contaminated Environment, Romanian
Biotechnological Letters, 14(1): 4164-4169. Syaputra, R., 2005, Fitoremediasi Logam Cu dan Zn
dengan Tanaman Eceng Gondok (Eichhornia Crassipes (Mart.) Solms), LOGIKA, 2(2): 57-67. Tchegnitegni, B.T., Teponno, R.B., Tanaka, C., Gabriel, A.F., Tapondjou L.A., dan Miyamoto, T., 2015, Sappanin-type Homoisoflavonoids From Sansevieria trifasciata Prain, Phytochemistry Letters, 12: 262-266.
Turan, M., danEsringu, A., 2007, Phytoremediation Based On Canola (Brassica napusL.) and Indian Mustard (Brassica junceaL.) Planted On Spiked Soil By Aliquot Amount of Cd, Cu, Pb, and Zn, Plant Soil Environ.,53(1): 7-15.
Wardani, D.A.K., Dewi, N.M., dan Utami, N.R., 2014, Akumulasi Logam Berat Timbal (Pb) Pada Daging Kerang Hijau (Pernaviridis) di Muara Sungai Banjir Kanal Barat Semarang, Unnes Journal of Life Science, 3(1): 1-8.
Watanabe, M.E., 1997, Phytoremediation On The Brink of Commercialization, Environmental Science & Technology, 31(4): 182-186.
Yoon, J., Cao, X., Zhou, Q., dan Ma, L.Q., 2006, Accumulation of Pb, Cu, and Zn in Native Plants Growing on A Contaminated Florida Site, Science of The Total Environment, 368(2): 456-464.