DEFISIENSI BESI DENGAN PARAMETER sTfR SEBAGAI
FAKTOR RISIKO BANGKITAN KEJANG DEMAM
IRON DEFICIENCY WITH sTfR PARAMETER AS A RISK FACTOR
OF FEBRILE SEIZURES
Tesis
Untuk memenuhi sebagian persyaratan mencapai derajat Sarjana S-2
dan memperoleh keahlian dalam bidang Ilmu Kesehatan Anak
Abdul Khanis
PROGRAM PASCASARJANA
MAGISTER ILMU BIOMEDIK
DAN
PROGRAM PENDIDIKAN DOKTER SPESIALIS I
ILMU KESEHATAN ANAK
UNIVERSITAS DIPONEGORO
SEMARANG
PERNYATAAN
Dengan ini saya menyatakan bahwa:
• Tesis ini adalah hasil pekerjaan saya sendiri dan didalamnya tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi dan lembaga pendidikan lainnya. Pengetahuan yang diperoleh dari hasil penerbitan maupun yang belum/tidak diterbitkan, sumbernya dijelaskan di dalam tulisan dan daftar pustaka.
• Hasil penelitian ini selanjutnya menjadi milik Bagian Ilmu Kesehatan Anak Fakultas Kedokteran Universitas Diponegoro/RSUP. Dr. Kariadi Semarang dan karenanya untuk kepentingan publikasi keluar harus seizin Ketua Bagian Ilmu Kesehatan Anak Fakultas Kedokteran Universitas Diponegoro/RSUP. Dr. Kariadi Semarang.
Demikian pernyataan ini saya buat dengan sebenarnya.
Semarang, Mei 2010
RIWAYAT HIDUP
A. Identitas
Nama : Abdul Khanis
Tempat dan Tanggal Lahir : Brebes, 27 Juni 1976
Agama : Islam
Jenis Kelamin : Laki-laki
Status : Menikah
Alamat : Puri Anjasmoro Blok K 4 / No. 23
Semarang, Jawa Tengah
B. Riwayat Pendidikan
1. Sekolah Dasar Negeri 1, Pangebatan, lulus tahun 1989
2. Sekolah Menengah Pertama Negeri 1, Bumiayu, lulus tahun 1992 3. Sekolah Menengah Atas Negeri 2, Purwokerto, lulus tahun 1995
4. Fakultas Kedokteran Universitas Diponegoro, Semarang, lulus tahun 2001 5. PPDS-I Ilmu Kesehatan Anak Fakultas Kedokteran Universitas Diponegoro,
Juli 2004 – sekarang
6. Magister Ilmu Biomedik Program Pascasarjana Universitas Diponegoro, Juli 2004 – sekarang
C. Riwayat Pekerjaan
• Dokter di RSI Sukapura, Jakarta Utara, 2002-2004
• Dokter di Indonesian Holistic Medical Centre, Purwakarta, 2003-2004
KATA PENGANTAR
Puji syukur saya panjatkan ke hadirat Allah SWT, karena berkat karunia-Nya, Laporan Penelitian yang berjudul “Defisiensi besi dengan parameter sTfR sebagai faktor risiko bangkitan kejang demam“ dapat saya selesaikan, guna memenuhi sebagian persyaratan dalam mencapai derajat S-2 dan memperoleh keahlian dalam bidang Ilmu Kesehatan Anak Fakultas Kedokteran Universitas Diponegoro.
Saya menyadari bahwa tulisan ini masih jauh dari sempurna karena keterbatasan yang saya miliki. Namun karena dorongan keluarga, bimbingan guru-guru kami dan teman-teman maka tulisan ini dapat terwujud.
Banyak sekali pihak yang telah berkenan membantu saya dalam menyelesaikan penulisan ini, sehingga kiranya tidaklah berlebihan apabila pada kesempatan ini saya menghaturkan rasa terima kasih dan penghormatan yang setinggi-tingginya kepada:
1. Rektor Universitas Diponegoro Semarang, Prof. Dr. dr. Susilo Wibowo, MS.
Med, Sp.And dan mantan Rektor Prof. Ir. Eko Budiardjo, M.Sc dan beserta
jajarannya yang telah memberikan ijin bagi saya untuk menempuh PPDS-1 Ilmu Kesehatan Anak Fakultas Kedokteran Universitas Diponegoro Semarang. 2. Direktur Program Pascasarjana Universitas Diponegoro, Prof. Drs. Y.
Warella, MPA, Ph.D yang telah memberikan ijin bagi penulis untuk
3. Ketua Program Studi Magister Ilmu Biomedik Program Pascasarjana Universitas Diponegoro Dr. dr. Winarto, SpMK, SpM(K), yang telah memberikan ijin bagi saya untuk menempuh Program Studi Magister Ilmu Biomedik Program Pascasarjana Universitas Diponegoro Semarang.
4. Dekan Fakultas Kedokteran Universitas Diponegoro, dr. Soejoto, PAK,
Sp.KK(K) dan mantan Dekan Prof. dr. Kabulrahman, Sp.KK, beserta
jajarannya yang telah memberikan kesempatan kepada penulis untuk mengikuti PPDS-1 Ilmu Kesehatan Anak Fakultas Kedokteran Universitas Diponegoro. 5. Direktur Utama Rumah Sakit Dr. Kariadi Semarang, dr. Hendriani Selina,
Sp.A(K), MARS, dan mantan Direktur Utama Rumah Sakit Dr. Kariadi
Semarang dr. Budi Riyanto, Sp.PD, M.Sc beserta jajaran Direksi yang telah memberikan ijin bagi penulis untuk meneliti dan menempuh PPDS-1 di Bagian Ilmu Kesehatan Anak/SMF Kesehatan Anak di RSUP Dr. Kariadi Semarang. 6. Ketua Bagian Ilmu Kesehatan Anak Fakultas Kedokteran Universitas
Diponegoro/ SMF Kesehatan Anak RSUP Dr. Kariadi Semarang, dr. Dwi
Wastoro Dadiyanto, Sp.A(K) serta dr. Budi Santosa, SpA(K) selaku mantan
Ketua Bagian Ilmu Kesehatan Anak Fakultas Kedokteran Universitas Diponegoro/SMF Kesehatan Anak yang telah memberikan kesempatan kepada penulis untuk mengikuti PPDS-1 dan atas segala ketulusannya dalam memberikan motivasi, bimbingan, wawasan dan arahan untuk menyelesaikan studi.
7. Ketua Program Studi PPDS-1 Ilmu Kesehatan Anak Fakultas Kedokteran Universitas Diponegoro, dr. Alifiani Hikmah P, SpA(K) saya sampaikan
ucapan terima kasih dan penghargaan setinggi-tingginya atas kesabaran, pengertian dalam memberikan arahan, dorongan dan motivasi terus-menerus dalam menyelesaikan penelitian ini.
8. Penghargaan setinggi-tingginya dan rasa terima kasih saya haturkan kepada
Dr. dr. Tjipta Bahtera, SpA(K), sebagai pembimbing utama penelitian ini
atas segala kesabaran dan ketulusannya dalam memberikan bimbingan, motivasi, wawasan, arahan sehingga penulis dapat menyelesaikan penelitian ini.
9. dr. Noor Wijayahadi, M.Kes, PhD, SpFK sebagai pembimbing kedua
penelitian ini saya ucapkan terima kasih yang sebesar-besarnya atas segala kesabaran dan ketulusannya dalam memberikan bimbingan, untuk perbaikan Tesis ini.
10.Prof. dr. Lisyani B Suromo, Sp.PK (K), Prof. Dr. dr. H. Tjahjono, Sp.PA(K), FIAC, dr. Pudjadi, SU, dr. Niken Puruhita, MMed.Sc, SpGK,
dan Dr. dr. Andrew Johan, M.Si, saya ucapkan terima kasih yang sebesar-besarnya atas kesediaannya sebagai tim penguji Proposal dan Tesis serta segala bimbingannya untuk perbaikan dan penyelesaian Tesis ini.
11. dr. Anggoro DB Sachro, Sp.A(K), DTM&H, saya ucapkan terima kasih yang sebesar-besarnya selaku dosen wali yang telah berkenan memberikan dorongan, motivasi dan arahan yang tidak putus-putusnya untuk dapat menyelesaikan studi dan penyusunan laporan penelitian ini.
12. Para guru besar dan guru-guru kami staf pengajar di Bagian IKA Fakultas Kedokteran Universitas Diponegoro / RS. Dr. Kariadi Semarang : Prof. dr.
Moeljono S. Trastotenojo, Sp.A(K), Prof. Dr. dr. Ag. Soemantri, Sp.A(K), Ssi (Stat), Prof. Dr. dr. I. Sudigbia, Sp.A(K), Prof. Dr. dr. Lydia Kristanti K, Sp.A(K), Prof. Dr. dr. Harsoyo N, Sp.A(K), DTM&H, Prof. dr. Sidhartani Zain, MSc, SpA(K), Dr. dr. Tatty Ermin S, Sp.A(K), P.hD, dr. H. R. Rochmanadji Widajat, Sp.A(K), MARS, dr. Kamilah Budhi R, SpA(K), Dr. dr. Tjipta Bachtera, Sp.A(K), dr. Budi Santosa, SpA(K), dr. HM Sholeh Kosim, SpA(K), dr. Moedrik Tamam, Sp.A(K), dr. Rudy Susanto, Sp.A(K), dr. I. Hartantyo, Sp.A(K), dr. Hendriani Selina, Sp.A(K), MARS, dr. JC Susanto, Sp.A(K), dr. Agus Priyatno, Sp.A(K), dr. Asri Purwanti, Sp.A(K), MPd, dr. Bambang Sudarmanto, Sp.A(K), dr. MM DEAH Hapsari, Sp.A(K), dr. Alifiani Hikmah P, SpA(K), dr. Mexitalia Setiawati, Sp.A(K), dr. M. Herumuryawan, Sp.A, dr. Gatot Irawan Sarosa, Sp.A(K), dr. Anindita S, Sp.A, dr. Wistiani, Sp.A, dr. Moh. Supriyatna, SpA, dr. Fitri Hartanto Sp.A, dr. Omega Melyana, SpA, dr. dr. Yetty Movieta Nancy, SpA, dr. Ninung Rose D, MsiMed, SpA dan dr. Nahwa A, MsiMed, SpA, dr. Yusrina Istanti, MsiMed, SpA
yang telah berperan besar dalam proses pendidikan saya, hanya Allah SWT yang dapat membalasnya dengan yang lebih baik.
13. dr. HM Sholeh Kosim, SpA(K) yang telah meluangkan waktu untuk memberi masukan yang mencerahkan penulisan proposal penelitian dan dr.
Hardian yang dengan cerdas, sabar, teliti dan senang hati membantu peneliti
dalam penyusunan laporan penelitian ini, semoga Allah SWT membalas beliau dengan yang lebih baik.
14. Teman-teman seangkatan Juli 2004 ( dr. Novita W, dr. Zuhriah H, dr. Tun Paksi S) yang telah berbagi suka dan duka, saling memotivasi dan saling membantu selama menempuh pendidikan. Semoga sukses selalu dan yang terbaik untuk kalian.
15. Seluruh teman sejawat peserta PPDS-I, atas kerjasama yang baik, saling membantu dan memotivasi. Juga tak lupa rasa terima kasih dan penghargaan kepada rekan-rekan paramedis, petugas laboratorium khususnya Ibu Farida dan Pak Agus serta Tata Usaha bagian Ilmu Kesehatan Anak atas kerjasama dan bantuannya selama penulis menimba ilmu.
16. Semua pasien dan keluarganya yang telah turut berpartisipasi secara ikhlas dalam penelitian ini, saya sampaikan terima kasih serta penghargaan setinggi-tingginya. Semoga anak-anak kelak dapat menjadi generasi yang lebih baik dan sehat. Untuk mereka semua penelitian ini saya persembahkan.
17. Terima kasih kepada kedua orangtuaku tercinta Ibunda Hj Muriyah dan Ayahanda HM Husen yang dengan penuh kasih sayang dan pengorbanan telah mengasuh, membesarkan, mendidik dan menanamkan kemandirian dan tanggung jawab serta memberikan dorongan semangat, bantuan moril maupun material, semoga Allah Ar-Rahim menyayangi mereka sebagaimana mereka menyayangiku di waktu kecil, memberikan kesehatan, umur panjang yang barokah dan keselamatan dunia akhirat, amin. Saudara-saudaraku tersayang, Muksin, Hasanudin, Syamsul Anam atas bantuan, perhatian, dukungan, nasehat dan doa tulus yang penulis rasakan hingga sekarang. Semoga kita selalu kompak dalam kebaikan dan bisa istiqomah.
18. Isteriku tercinta Widyastuti, SE. dan buah hati kami tersayang, Avisena Duta W dan Nasywa Sausan Khanis yang begitu luar biasa dengan setia dan tabah mendampingi dalam suka dan duka, memberikan dukungan, semangat, pengorbanan, kesabaran, dan senyuman yang menyejukkan selama menjalani pendidikan. Mertuaku yang saya hormati HM Yusuf Sudiono dan Hj Khusnul Khotimah yang dengan penuh kasih sayang dan perhatian memberikan dorongan semangat, dukungan moril dan material, Semoga Allah SWT. Membalas beliau berdua dengan yang lebih baik dan berkenan memberikan kebahagiaan dunia dan akhirat.
Tiada gading yang tak retak, saya memohon kepada semua pihak untuk memberikan masukan dan sumbang saran atas penelitian ini sehingga dapat meningkatkan kualitas penelitian ini dan memberikan bekal bagi saya untuk penelitian ilmiah di masa yang akan datang.
Akhirnya dari lubuk hati yang paling dalam, penulis juga menyampaikan permintaan maaf kepada semua pihak yang mungkin telah mengalami hal yang kurang berkenan dalam berinteraksi dengan penulis selama kegiatan penelitian ini. Semoga Allah Yang Maha Rahman-Rahim senantiasa melimpahkan berkah dan karunia-Nya kepada kita semua, Amin.
Semarang, Mei 2010
DAFTAR ISI
halaman Halaman judul ... i Lembar pengesahan ... Pernyataan ... Riwayat hidup ... Kata pengantar ... Daftar isi ... Daftar gambar ... Daftar tabel ... Daftar lampiran ... Daftar singkatan ... Abstract ... ii iii iv v xi xiv xv xvi xvii xviii Abstrak ... BAB 1. PENDAHULUAN ... 1.1. Latar belakang ... 1.2. Perumusan masalah ... 1.3. Tujuan penelitian ... 1.4. Manfaat penelitian ... 1.5. Orisinalitas penelitian ... xix 1 1 3 4 4 5BAB 2. TINJAUAN PUSTAKA ... 2.1. Defisiensi besi ………... 2.1.1. Definisi ………... 2.1.2. Parameter dan tahap defisiensi besi ... 2.1.3. Patogenesis ... 2.1.4. Absorbsi besi di otak ...………. 2.2. Serum transferrin receptor (sTfR) ………... 2.3. Kejang demam ……….. 7 7 7 8 10 12 13 15
2.3.1. Definisi ……….. 2.3.2. Patofisiologi ……….. 2.3.3. Faktor risiko ……….. 2.3.3.1. Umur ………. 2.3.3.2. Demam ……….. 2.3.3.3. Faktor genetik ………... 2.3.3.4. Riwayat kehamilan dan persalinan …………... 2.3.3.5. Infeksi berulang ………. 2.3.3.6. Status besi ………. 2.4. Hubungan antara defisiensi besi dengan bangkitan kejang demam .. 2.5. Kerangka teori ………... 2.6. Kerangka Konsep ………. 2.7. Hipotesis ……… 15 16 20 20 20 22 23 25 25 27 31 32 32
BAB 3. METODA PENELITIAN ... 3. 1. Ruang lingkup penelitian ... 3. 2. Tempat dan waktu penelitian ... 3. 3. Jenis dan rancangan penelitian ... 3. 4. Populasi dan sampel ... 3.4.1. Populasi target ... 3.4.2. Populasi terjangkau ... 3.4.3. Sampel penelitian ... 3.4.4. Besar sampel ………... 3.4.5. Metode sampling ... 3. 5. Variabel penelitian ………... 3.5.1. Variabel terikat ... 3.5.2. Variabel bebas ... 3.5.3. Variabel perancu ... 3.6. Definisi operasional ………... 3.7. Alur penelitian ……… 3.8. Cara pengumpulan data. ………. 3.9. Analisis data ……… 33 33 33 33 33 33 34 34 35 36 36 36 36 36 37 38 38 39
3.10. Etika penelitian ……….……….. 40
BAB 4. HASIL PENELITIAN ..………. 4.1. Karakteristik umum subyek penelitian ………. 4.2. Karakteristik Faktor-faktor yang berpengaruh terhadap bangkitan kejang demam pada kelompok kasus dan kontrol ……….. 4.2.1. Umur ………..……….. 4.2.2. Demam ……….………. 4.2.3. Riwayat kejang demam dalam keluarga …..……… 4.2.4. Riwayat kehamilan maupun persalinan ………….………... 4.2.5. Status infeksi ……….………. 4.3. Karakteristik parameter laboratorium defisiensi besi pada kelompok kasus dan kontrol ………. 4.3.1. Parameter laboratorium secara umum ……… 4.3.2. Parameter laboratorium secara khusus …………..……..…. 4.4. Kadar sTfR sebagai indikator bangkitan kejang demam …………. 4.5. Hasil analisis multivariat ……….…………. 41 41 42 42 43 43 45 46 48 48 49 50 52 BAB 5. PEMBAHASAN ………..……..……..………….……….. 54
BAB 6. SIMPULAN DAN SARAN ……… 65
DAFTAR PUSTAKA ……….. 67
DAFTAR GAMBAR
Gambar Judul Halaman
1. Proses absorbsi besi di otak 13
2. Mekanisme skematik ambilan besi oleh sel 14
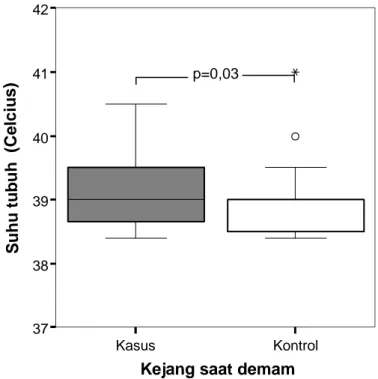
3. Suhu tubuh pada kelompok kasus dan kontrol 43
4. Distribusi kejadian anemia pada kelompok kasus dan
kontrol
49
5. Analisis ROC kadar sTfR sebagai indikator bangkitan
kejang demam
DAFTAR TABEL
Tabel Judul Halaman
1. Penelitian-penelitian tentang hubungan defisensi besi dengan bangkitan kejang demam pada anak
5
2. Cutt off level anemia menurut WHO / UNICEF tahun
1997
7
3. Perubahan parameter laboratorium pada setiap tahapan
defisiensi besi
9
4. Karakteristik umum subyek penelitian pada kelompok
kasus dan kontrol
41
5. Karakteristik umur pada kelompok kasus dan kontrol 42
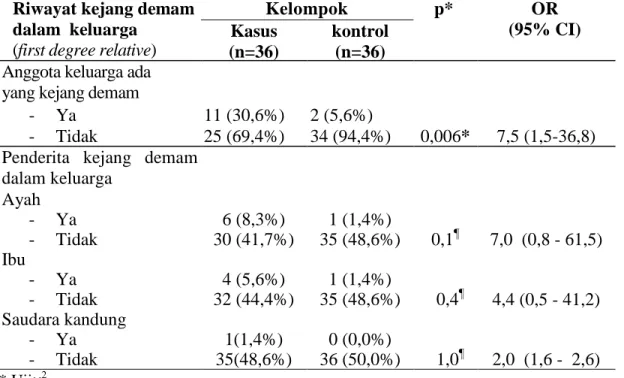
6. Riwayat kejang demam dalam keluarga (first degree
relative)
44
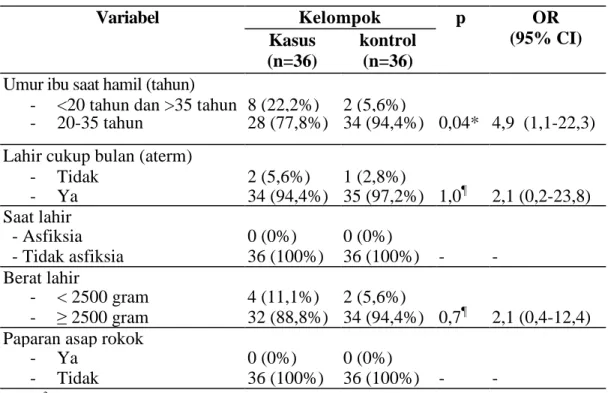
7. Riwayat kehamilan maupun persalinan anak pada
kelompok kasus dan kontrol
45
8. Status infeksi pada kelompok kasus dan kontrol 47
9. Parameter laboratorium secara umum 48
10. Kadar sTfR serum pada kelompok kasus dan kontrol 49
11. Kategori kadar sTfR serum pada kelompok kasus dan
kontrol
50
12. Kategori kadar sTfR berdasarkan cut-off point analisis ROC
51 13. Analisis multivariat regresi logistik untuk faktor-faktor
yang berpengaruh terhadap kejadian kejang demam
DAFTAR LAMPIRAN
Lampiran 1 Ethical Clearance
Lampiran 2 Izin penelitian dari RSUP Dr. Kariadi Semarang
Lampiran 3 Persetujuan setelah penjelasa (Informed Consent )
Lampiran 4 Lembar pengisian data penelitian
Lampiran 5 Hasil pemeriksaan sTfR
Lampiran 6 Data penelitian
DAFTAR SINGKATAN
1 FS + : Febrile seizures plus 2. GABA : Gamma aminobutyric acid 3. SCNIA : Subunit channel natrium alfa I 4. SCNIB : Subunit channel natrium beta I
5. sTfR : Serum transferrin receptor
6. Hb : Hemoglobin
7. Ht : Hematokrit
8. MCV : Mean corpuscular volume
9. DMT 1 : Divalent metal transporter 1
10. NMDA : N methyl D aspartate
11. AMPA : Amino 3 hydroxy 5 methyl 4 isoxazole proprionic acid. 12. CRH : Corticotropin releasing hormon
13. ATP : Adenosin tri pospat
14. Na+ : Ion natrium
15. K + : Ion kalium
16. Ca2+ : Ion calsium
ABSTRACT
Background. Febrile seizures is the most often neurologic disorder in children,
2%-5% children under 5 years old have experienced febrile seizures. Prognosis of febrile seizures is good, but worrying their parents. Iron deficiency as a risk factor of febrile seizures is still controversial.
Objective. Analyze iron deficiency with serum transferrin receptor (sTfR)
parameter as a risk factor of febrile seizures in children.
Method. Study design was case control with subjects 72 children aged 3 months –
5 years in Dr.Kariadi hospital on August 2009 – January 2010, 36 children with febrile seizures as case group and 36 children with febrile with no seizure as control group. Clinical data and blood sampling were recorded from study subjects for sTfR level measurement. Risk factors were analyzed with odds ratio (95% confidence interval) and multivariate logistic regression.
Results. Mean sTfR level was 6.2 µg/mL (2.6-6.8) in case group and 2.0 µg/mL (1.8-2.3) in control group. Multivariate analysis showed iron deficiency with sTfR parameter was significantly as a risk factor for febrile seizures (p<0.001 ; OR=25.1 ; 95%CI 5.1-122.6). sTfR level could be used as febrile seizures indicator with sTfR level cut-off point was 2.55 µg/ml.
Conclusion. Iron deficiency with sTfR parameter is a risk factor for febrile
seizures.
ABSTRAK
Latar belakang. Kejang demam merupakan kelainan saraf tersering pada anak dimana 2%-5% anak dibawah umur 5 tahun pernah mengalami kejang demam. Prognosis kejang demam baik, namun cukup mengkhawatirkan bagi orang tuanya. Defisiensi besi sebagai faktor risiko bangkitan kejang demam masih kontroversial.
Tujuan. Menganalisis defisiensi besi dengan parameter serum transferrin receptor (sTfR) sebagai faktor risiko bangkitan kejang demam pada anak.
Metode. Rancangan penelitian adalah kasus kontrol dengan subyek penelitian 72
anak berumur 3 bulan sampai 5 tahun di RS Dr. Kariadi pada Agustus 2009 – Januari 2010, 36 anak kelompok kasus dengan bangkitan kejang demam dan 36 anak kelompok kontrol dengan demam tanpa kejang. Subyek penelitian dicatat data klinis dan pengambilan darah untuk diperiksa kadar sTfR. Faktor risiko dianalisis dengan ratio odds (95% interval kepercayaan) dan multivariat regresi logistik.
Hasil. Rerata kadar sTfR pada kelompok kasus 6,2 µg/mL (2,6-6,8) dan kelompok kontrol 2,0 µg/mL (1,8-2,3). Analisis multivariat menunjukkan defisiensi besi dengan parameter sTfR secara bermakna merupakan faktor risiko bangkitan kejang demam (p<0,001 ; OR=25,1 ; 95%CI 5,1-122,6). Kadar sTfR dapat dipergunakan sebagai indikator bangkitan kejang demam dengan cut-off
point kadar sTfR adalah 2,55 µg/mL.
Simpulan. Defisiensi besi dengan parameter sTfR merupakan faktor risiko
bangkitan kejang demam.
BAB 1 PENDAHULUAN
1.1. Latar belakang
Kejang demam adalah kejang yang terkait dengan demam dan umur, serta tidak didapatkan infeksi intrakranial ataupun kelainan lain di otak. Demam adalah kenaikan suhu tubuh di atas 380 C rektal atau di atas 37,80 C aksila. Para ahli berbeda pendapat tentang umur penderita saat terjadi bangkitan kejang demam. Pendapat terbanyak para ahli kejang demam terjadi pada waktu anak berumur antara 3 bulan sampai dengan 5 tahun, dengan insiden bangkitan kejang tertinggi terjadi pada umur 18 bulan.1-41,2,3,4
Kejang demam merupakan kelainan saraf tersering pada anak dimana 2%-5% anak dibawah umur 5 tahun pernah mengalami bangkitan kejang demam. Insiden kejang demam di Amerika Serikat dan Eropa berkisar 2-5%. Insiden kejang demam di Asia meningkat dua kali lipat bila dibandingkan di Eropa dan Amerika Serikat, di Jepang berkisar 8,3%-9,9%, India 10,1%, bahkan di Guam insiden kejang demam mencapai 14%.5 Prognosis kejang demam baik, namun cukup mengkhawatirkan bagi orang tuanya. Angka kematian berkisar 0,64-0,75%. Sebagian besar penderita kejang demam sembuh tanpa cacat, sebagian kecil berkembang menjadi epilepsi dan sangat jarang akan meninggalkan gejala sisa berupa cacat neurologis atau gangguan perkembangan mental.1
Faktor-faktor risiko timbulnya bangkitan kejang demam adalah 1) umur 2) demam 3) faktor riwayat kejang demam pada keluarga 4) faktor penyulit dalam kehamilan maupun persalinan 5) infeksi berulang 6) ketidakseimbangan neurotransmiter inhibitor dan eksitator.6,7
Defisiensi besi sebagai faktor risiko bangkitan kejang demam masih kontroversial. Penelitian Pisacane dkk menyatakan bahwa anemia defisiensi besi merupakan faktor risiko bangkitan kejang demam pada anak berumur di bawah 2 tahun (OR=3,3),8 sedangkan penelitian Kobrinsky dkk sebaliknya menyatakan bahwa defisiensi besi menurunkan risiko atau faktor protektif terhadap bangkitan kejang demam pada anak berumur di bawah 3 tahun (OR=0,13). Menurut kobrinsky dkk bahwa lemak peroksidase yang terinduksi besi memainkan peranan penting dalam perkembangan kejang non traumatik, termasuk didalamnya bangkitan kejang demam.9
Defisiensi besi adalah kelainan yang umum dijumpai di seluruh dunia, khususnya pada kelompok umur anak. Prevalensi defisiensi besi tinggi pada bayi, hal yang sama juga dijumpai pada anak usia sekolah dan anak praremaja. Angka kejadian anemia defisiensi besi pada anak usia sekolah (5-8 tahun) di daerah perkotaan sekitar 5,5%, anak praremaja 2,6% dan gadis remaja yang hamil 26%. Angka kejadian di Amerika Serikat pada tahun 2001 tercatat sekitar 6% anak berumur 1-2 tahun diketahui defisiensi besi, 3% menderita anemia. Gadis remaja di Amerika Serikat kurang lebih 9% menderita defisiensi besi dan 2% menderita anemia, sedangkan pada anak laki-laki sekitar 50% cadangan besinya berkurang saat pubertas. Berdasarkan penelitian yang pernah dilakukan di Indonesia prevalensi anemia defisiensi besi pada anak balita sekitar 25-35%.10,11
Otak merupakan organ yang cukup sensitif terhadap defisiensi besi.12 Peran zat besi pada neurotransmiter berpusat pada proses sintesis dan degradasinya. Penelitian Mittal dkk melaporkan bahwa defisiensi besi fase awal pada hewan coba telah menunjukkan penurunan bermakna pada kadar GABA di
otak. Defisiensi besi menyebabkan enzim yang bertanggung jawab untuk sintesis GABA yaitu Glutamic acid decarboxylase (GAD) berkurang secara signifikan. Penelitian Agarwal melaporkan defisiensi besi fase awal menunjukkan peningkatan secara bermakna kadar asam glutamat di otak. Ketidakseimbangan antara neurotransmiter eksitator asam glutamat dan inhibitor GABA13berperan
penting14dalam menimbulkan15bangkitan kejang demam.13-15 Namun GABA
tidak termasuk parameter defisiensi besi sehingga tidak diteliti pada penelitian ini. Salah satu indikator ketersediaan besi dalam tubuh adalah serum
transferrin receptor (sTfR), dimana peningkatan kadar sTfR terdeteksi pada
defisiensi besi tahap kedua dan ketiga. STfR merupakan petanda klinis dari aktivitas eritropoietik. STfR merupakan indeks ketersediaan besi jaringan dan sensitif terhadap perubahan status besi serum. Pada keadaan defisiensi besi kadar sTfR akan meningkat secara progresif.16,17
Penggunaan sTfR sebagai indikator ketersediaan besi dalam tubuh mempunyai beberapa keuntungan, antara lain tidak dipengaruhi oleh adanya inflamasi dan infeksi, dapat memberikan informasi ketersediaan besi tubuh seperti yang diperoleh dengan pemeriksan aspirasi sumsum tulang dan hanya membutuhkan sampel serum yang sedikit sehingga lebih sesuai untuk anak. Sedangkan parameter selain sTfR seperti feritin tidak stabil dalam keadaan inflamasi dan infeksi.16-18 16,17,18
1.2. Rumusan masalah
Apakah defisiensi besi dengan parameter sTfR merupakan faktor risiko bangkitan kejang demam ?
1.3. Tujuan penelitian 1.3.1. Tujuan umum
Membuktikan defisiensi besi dengan parameter sTfR merupakan faktor risiko bangkitan kejang demam.
1.3.2. Tujuan khusus
1. Menganalisis perbedaan antara kadar sTfR pada kelompok anak umur 3 bulan-5 tahun dengan bangkitan kejang demam dan tanpa bangkitan kejang demam.
2. Menganalisis hubungan defisiensi besi dengan parameter sTfR terhadap bangkitan kejang demam.
3. Menganalisis besarnya risiko defisiensi besi dengan parameter sTfR terhadap bangkitan kejang demam.
4. Menentukan kadar sTfR yang dapat dipergunakan sebagai indikator bangkitan kejang demam.
1.4. Manfaat penelitian
1.4.1. Manfaat Pendidikan/Keilmuan
Memberikan pemahaman yang lebih baik tentang pengaruh defisiensi besi terhadap bangkitan kejang demam.
1.4.2. Manfaat Pelayanan Kesehatan
Apabila terbukti dapat menjadi dasar ilmiah untuk melakukan upaya promotif dan preventif dengan pemberian preparat besi kepada anak umur 3 bulan-5 tahun untuk menurunkan risiko bangkitan kejang demam.
1.4.3. Manfaat Penelitian
Sebagai titik tolak penelitian lebih lanjut tentang peranan besi terhadap bangkitan kejang demam.
1.5. Orisinalitas penelitian
Penelitian-penelitian tentang hubungan defisensi besi dengan bangkitan kejang demam pada anak. Penelitian terdahulu :
No. Peneliti, judul, nama
jurnal Metode Hasil
1. Kobrinsky NL, et al. Does iron deficiency raise the seizure threshold ?. The J Child Neurol 1995; 10: 105 – 9.
Kohort prospektif Subyek :
51 anak umur 6-24 bulan dengan kejang demam. 25 anak dengan kejang demam, 26 anak tanpa kejang demam.
Pemeriksaan : FEP, Hb, Ht, MCV, MCH, trombosit, feritin serum.
Defisiensi besi bersifat protektif terhadap bangkitan kejang demam. Defisiensi besi
menurunkan risiko kejadian bangkitan kejang demam 7,8x (OR=0,13).9
2. Pisacane A, et al. Iron deficiency anemia and febrile convulsion. BMJ 1996;313:343.
Kasus kontrol Subyek:
156 anak umur 6-36 bulan dengan kejang demam yang dirawat di rumah sakit. Kontrol ada 2 kelompok:
- Kelompok anak yang dirawat dengan infeksi saluran nafas dan saluran cerna (n=146). - Kelompok anak sehat pada
populasi (n=147).
Pemeriksaan : SI, Hb, MCV
Anemia defisiensi besi yang dirawat di rumah sakit merupakan faktor risiko bangkitan kejang demam (OR = 2,6x; 95%CI 1,4 – 4,8)
Sedangkan faktor risiko pada populasi OR 3,3x 95% CI 1,7- 6,5.8
3. Daoud AS, et al. Iron Status: A Possible Risk Factor for the First Febrile Seizure. Epilepsia 2002, 43(7):740–743.
Kasus kontrol
150 anak umur 3 bulan -6 tahun. - Kasus: 75 anak kejang demam
pertama kali
- Kontrol: 75 anak demam tanpa kejang
Penyesuaian umur dan jenis kelamin.
Pemeriksaan : Hb, MCV, MCH, feritin serum.
Defisiensi besi merupakan faktor yang berpengaruh terhadap bangkitan kejang demam. OR tidak disebutkan.4
4. Hartfield DS, et al. The Association Between Iron
Deficiency and Febrile Seizures in Childhood. Clin Pediatrics, Feb 2009.
kasus kontrol.
Kasus anak yang dirujuk ke UGD oleh karena kejang demam (n = 361). Kontrol anak dengan demam tanpa kejang (n=390). Pemeriksaan : Hb, MCV, RDW
Anak dengan defisiensi besi mempunyai risiko 2 kali lebih besar untuk terjadi bangkitan kejang demam (OR=1,84). 12
Penelitian yang akan dilakukan oleh peneliti :
Peneliti, judul Metode Hasil
Abdul Khanis. Defisiensi besi dengan parameter sTfR sebagai faktor risiko bangkitan kejang demam.
Kasus kontrol, 72 anak umur 3 bulan-5 tahun. -Kasus : 36 anak dengan kejang demam -Kontrol : 36 anak demam tanpa kejang pemeriksaan : sTfR.
-
Penelitian ini adalah penelitian kasus kontrol pada anak dengan umur 3 bulan-5 tahun dengan kejang demam di RS Dr. Kariadi Semarang. Penentuan status besi berdasarkan kadar sTfR. Dilakukan analisis kadar sTfR terhadap hubungan dan besarnya risiko terhadap bangkitan kejang demam. Penelitian seperti ini belum pernah dilakukan sebelumnya.
BAB 2
TINJAUAN PUSTAKA
2.1. Defisiensi besi 2.1.1. Definisi
Anemia secara umum diartikan sebagai menurunnya massa sel darah merah dibandingkan nilai normal pada umur tertentu pada suatu populasi. Pengukuran massa sel darah merah selain memerlukan waktu lama juga biaya yang mahal karena dibutuhkan transfusi eritrosit yang berlabel radioaktif. Pemeriksaan praktis digunakan pengukuran jumlah sel darah merah yang dicerminkan sebagai angka hemoglobin dan hematokrit. Secara sederhana anemia diartikan sebagai turunnya kadar hemoglobin atau hematokrit dibawah nilai normal pada umur tertentu pada suatu populasi.19,20
Tabel 2. Cut off level anemia menurut WHO / UNICEF tahun 1997.
Hemoglobin (g/dl) Hematokrit (%) 6 bulan – 5 tahun < 11 < 33 6 – 11 tahun < 11,5 < 34 <12 – 13 tahun < 12 < 36 Perempuan dewasa < 12 < 36 Wanita hamil < 11 < 33 Laki-laki dewasa < 13 < 39
Sumber : Wu AC, Lesperance L, Bernstein L.19
Defisiensi besi pada bayi dan anak sebagian besar disebabkan oleh faktor nutrisi. Pada periode kehidupan kelompok ini, defisiensi besi terjadi antara lain karena 1) penurunan cadangan besi saat lahir (bayi prematur, gemelli, perdarahan perinatal, dan pengekleman umbilikus terlalu dini (early clamping) 2) suplai besi yang tidak adekuat (penurunan masukan besi dan/atau rendahnya ketersediaan
besi dalam makanan 3) meningkatnya kebutuhan besi karena proses tumbuh kembang dan 4) meningkatnya kehilangan besi (akibat diare, perdarahan gastrointestinal).21
2.1.2. Parameter dan tahap defisiensi besi
Kebutuhan besi pada bayi umumnya tidak tercukupi jika hanya dari diet normal, yang utamanya adalah ASI. Masalah ini semakin berat pada anak yang mendapat susu sapi yang kandungan besinya sulit diabsorpsi. Absorbsi besi dari ASI dapat mencapai sampai 50%, sedangkan pada susu formula baik yang berasal dari susu sapi maupun kedelai absorbsi hanya sekitar 4%-10%. Risiko terjadinya anemia defisiensi besi meningkat pada bayi yang diberi susu sapi sejak dini atau bayi yang mendapat susu yang tidak mengandung besi.21,22
Apabila kebutuhan besi tubuh tidak terpenuhi melalui makanan yang dikonsumsi maka cadangan besi dalam tubuh akan berkurang (iron depletion), yang ditandai dengan rendahnya serum ferritin menjadi di bawah 12 mg/l. Jika keseimbangan negatif ini berlangsung lama maka ketersediaan besi dalam tubuh akan dikompensasi sehingga terjadi eritropoiesis defisiensi besi. Pada fase ini maka akan terjadi peningkatan awal konsentrasi sTfR secara progresif disertai dengan peningkatan free erythrocyte porphyrin (FEP), serta penurunan saturasi transferin (Sat) sehingga terjadi penurunan kadar Hb. Jika defisiensi besi ini berlanjut akan berakhir sebagai anemia defisiensi besi.11,21
Ada 3 tahap defisiensi besi :
1. Stadium Prelaten, stadium ini juga sering disebut iron depletion atau storage
iron deficiency. Pada stadium ini terjadi penurunan cadangan besi tetapi besi
pemeriksaan pewarnaan besi pada aspirat sumsum tulang dan pengukuran kadar feritin serum.
2. Stadium Laten atau iron deficient erythropoiesis. pada stadium ini terjadi penurunan cadangan besi maupun besi di plasma tetapi di eritrosit masih normal. Keadaan ini dapat diketahui melalui penurunan kadar serum iron (SI) dan saturasi transferin sedangkan total iron binding capacity (TIBC), free
erytrhrocyte porphyrin (FEP) dan sTfR meningkat.
3. Stadium anemia defisiensi besi. Pada stadium ini terjadi penurunan zat besi, baik dalam cadangan, di plasma maupun di eritrosit sehingga menyebabkan penurunan kadar Hb dan Ht. Dari gambaran darah tepi didapatkan mikrositik hipokromik.11,20,21
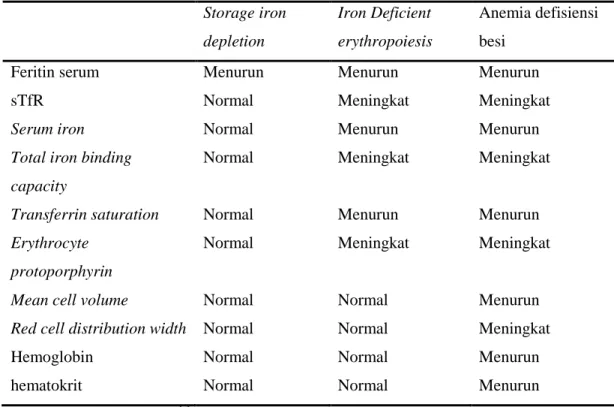
Perubahan parameter laboratorium setiap tahapan defisiensi besi ditampilkan sebagai berikut :
Tabel 3. Perubahan parameter laboratorium pada setiap tahapan defisiensi besi.
Storage iron depletion Iron Deficient erythropoiesis Anemia defisiensi besi
Feritin serum Menurun Menurun Menurun
sTfR Normal Meningkat Meningkat
Serum iron Normal Menurun Menurun
Total iron binding capacity
Normal Meningkat Meningkat
Transferrin saturation Normal Menurun Menurun
Erythrocyte protoporphyrin
Normal Meningkat Meningkat
Mean cell volume Normal Normal Menurun
Red cell distribution width Normal Normal Meningkat
Hemoglobin Normal Normal Menurun
hematokrit Normal Normal Menurun
2.1.3. Patogenesis
Besi yang terdapat dalam jumlah kecil pada semua sel di tubuh, melaksanakan beberapa fungsi yang penting, termasuk transpor oksigen. Sebagian besar besi tubuh digunakan untuk membuat kelompok heme di dalam molekul pembawa oksigen hemoglobin dan mioglobin. Besi juga penting untuk fungsi biologis sitokrom dan enzim-enzim lain yang terlibat dalam respirasi selular.19
Besi diserap dari saluran cerna dan ditransportasikan ke darah berikatan dengan transferin. Kelebihan besi disimpan terutama di dalam hati, sumsum tulang, dan lien dalam bentuk feritin.23
Fetus yang sedang berkembang membentuk penyimpanan besi dari suplai maternal. Bayi aterm yang lahir memiliki simpanan besi yang cukup selama setidaknya 4 sampai 6 bulan pertumbuhan postnatal, kecuali pada kondisi defisiensi besi maternal yang berat. Selama bulan-bulan pertama kehidupan, bayi baru lahir menggunakan besi dengan kecepatan tinggi untuk pertumbuhan yang cepat dan penambahan volume darah. Pada umur 4 bulan, simpanan besi bayi telah menurun sebasar 50%, sedangkan berat bayi biasanya dua kali lipat berat lahirnya. Bayi preterm memiliki lebih sedikit waktu untuk mengumpulkan besi selama dalam kandungan sehingga lahir dengan simpanan besi yang lebih sedikit. Bayi preterm memiliki kecepatan pertumbuhan postnatal yang tampak lebih cepat daripada bayi aterm dan mungkin mengurangi simpanan besinya dalam waktu 2 sampai 3 bulan.23,24
Besi harus tersedia dengan adekuat untuk memenuhi kebutuhan ini. Walaupun sebagian besar besi dalam tubuh disimpan dan digunakan kembali, beberapa hilang melalui saluran cerna, kulit, dan urin. Selama tahun pertama
kehidupan, bayi normal perlu menyerap kira-kira 0,8 mg/hari besi dalam diet (0,6 mg untuk pertumbuhan, 0,2 mg untuk menggantikan kehilangan besi).19
Mendekati akhir tahun kedua kehidupan, kecepatan pertumbuhan yang cepat ini mulai melambat, sehingga diet rutin biasanya menyertakan cukup makanan kaya besi untuk memenuhi kebutuhan. Kebutuhan besi meningkat kembali selama masa remaja karena pertumbuhan yang cepat, remaja wanita memerlukan besi tambahan untuk menggantikan kehilangan dari menstruasi.19
Terdapat dua tipe besi dalam diet yaitu heme dan non heme. Besi heme sudah tergabung dalam molekul hemoglobin dan mioglobulin dan diabsorbsi dengan baik oleh tubuh. Kira-kira 10% besi dalam diet adalah heme yang berasal dari daging, unggas dan ikan. Sebagian besar besi dalam diet adalah non heme, dalam bentuk garam besi. Bioavailibilitas besi non heme adalah sangat bervariasi dan dipengaruhi oleh beberapa faktor, termasuk diet saat ini, dan jumlah besi yang sudah ada dalam tubuh. Sekam padi, serat diet, kalsium, tannin (pada teh dan kopi), dan oksalat, phytate, dan polifenol (pada makanan dengan dasar tanaman tertentu) menghambat absorbsi besi. Absorbsi, ditingkatkan dengan mereduksi zat-zat seperti asam hidroklorik dan asam askorbik. Konsumsi besi heme, bahkan dalam jumlah kecil, meningkatkan absorbsi besi non heme. Absorbsi besi juga meningkat ketika simpanan tubuh total menurun atau ketika kebutuhan besi meningkat, seperti selama pertumbuhan yang cepat pada masa remaja.19,25,26
Susu matur manusia dan sapi mengandung jumlah besi yang sama, kira-kira 0,5 mg/L, susu formula mengandung 10 sampai 13 mg/L. Namun, kira-kira-kira-kira 50% besi dari susu manusia yang terserap dibandingkan dengan hanya 10% dari susu sapi dan kurang dari 5% pada susu formula. Alasan-alasan peningkatan
bioavailibilitas besi dari susu manusia tidak dipahami dengan baik, tetapi hal tersebut termasuk konsentrasi kalsium yang lebih rendah dan konsentrasi asam askorbik yang lebih tinggi pada susu manusia.19
2.1.4. Absorbsi besi di otak
Otak menyerap besi melalui transferin dan transferin reseptor yang terdapat pada sel endotel pembuluh darah otak. Sel-sel astrosit terdekat memiliki fungsi regulasi terhadap pengambilan besi melewati sawar darah otak. Sawar darah otak juga merupakan titik regulasi efektif terhadap pergerakan besi dari plasma ke cairan serebrospinal. Selain itu pleksus khoroidalis juga merupakan sumber pergerakan besi kedalam dan keluar otak. Bagian otak yang kaya besi adalah ganglia basalis, substansia nigra dan nuklei serebellar profunda. MRI telah digunakan untuk memetakan distribusi besi di otak anak dan remaja. Konsentrasi besi yang tertinggi didapatkan pada globus pallidus, nukleus kaudatus, putamen dan substansia nigra. Konsentrasi besi paling tinggi di otak saat lahir, berkurang pada masa penyapihan, dan kemudian mulai naik kembali bersamaan dengan awitan mielinisasi dan peningkatan ekspresi mRNA Tf. Absorbsi besi oleh otak akan meningkat bila terjadi defisiensi dan menurun bila kadar besi meningkat. Proses ini berlangsung sangat selektif dan tidak mencerminkan permeabilitas sawar darah otak secara keseluruhan. Kehilangan dan pengambilan besi berlangsung secara heterogen di seluruh area otak. Hal ini berdasarkan adanya perbedaan pengaturan pengambilan serta distribusi besi regional yang tergantung pada jumlah reseptor transferin, protein transfer logam endosomal (divalent metal
Masing-masing area otak memiliki jumlah tersendiri tergantung fungsi yang dilakukan.14,27
2.2. Serum transferrin receptor (sTfR)
Transferrin receptor (TfR) merupakan membran glikoprotein yang bekerja
sebagai pintu gerbang bagi sirkulasi transferin yang berikatan dengan besi untuk masuk ke dalam seluruh badan sel, terdiri dari dua rantai polipeptida 95 kDa identik. TfR diekspresikan pada seluruh badan sel yang membutuhkan besi, oleh karena itu konsentrasi tertingginya terdapat dalam sel organ dengan kebutuhan besi yang tinggi, seperti eritroid sumsum tulang dan plasenta. Reseptor ini mengikat transferin yang membawa besi dan memediasi ambilan besi melalui proses endositosis oleh kompleks reseptor-transferin. Ketika berada di dalam sitoplasma, besi dilepaskan dan digunakan untuk kebutuhan sel, sedangkan transferin dan reseptornya dilepaskan kembali ke membran plasma.16,28
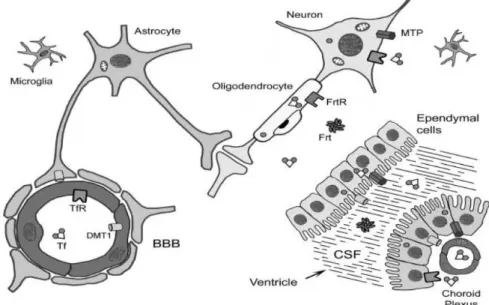
Gambar 1. Proses absorbsi besi di otak, memperlihatkan peranan sawar darah otak dan protein-protein transporter besi dalam pergerakan besi kedalam otak. Tf : transferrin, TfR : transferrin receptor, Frt : ferritin, FrtR : ferritin receptor, BBB : blood brain barrier. Sumber : Beard J.14
Sebagai suatu protein membran, reseptor transferin tidak dapat larut dalam air. Namun, sebagian daripada reseptor transferrin ini terdeteksi di dalam plasma dalam bentuk larut air (soluble), yang terbentuk akibat pelepasan sebagian segmen rantai polipeptida asli pada saat reseptor menempati membran plasma. Konsentrasi sTfR plasma atau serum secara akurat menggambarkan reseptor transferin seluler dari massa tubuh secara keseluruhan.17,28
STfR merupakan petanda klinis dari aktivitas eritropoietik dimana mekanismenya berlangsung sampai 120 hari. STfR merupakan indeks ketersediaan besi jaringan yang sensitif terhadap perubahan status besi serum. Pada keadaan defisiensi besi kadar sTfR akan meningkat secara progresif. Perubahan konsentrasi sTfR ini masuk pada tahap kedua defisiensi besi dan berhubungan secara terbalik dengan kecukupan besi sebab tubuh bereaksi terhadap kekurangan besi dengan meningkatkan jumlah sTfR pada membran plasma sel tersebut. Beberapa keuntungan dari pemeriksaan sTfR untuk menentukan kadar besi dibanding pemeriksaan laboratorium konvensional yang lain yaitu 1) pemeriksaan ini membutuhkan jumlah serum yang sangat sedikit (10 µl), oleh karena itu pemeriksaan reseptor ini juga cocok untuk pasien anak, 2) pemeriksaan ini memberikan informasi yang sama mengenai kandungan besi
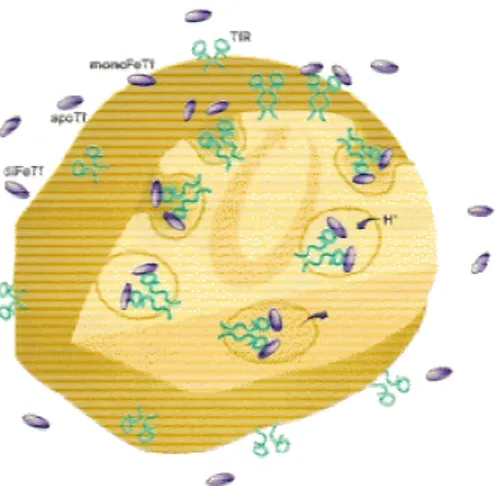
Gambar 2. Mekanisme skematik ambilan besi oleh sel. Sumber : Testa U.28
seperti yang didapat dari pemeriksaan aspirasi sumsum tulang, hanya saja tidak invasif, 3) tidak terpengaruh oleh inflamasi, infeksi akut maupun kronis dan penyakit kronik 4) memiliki sensitifitas dan spesifisitas yang tinggi.16-1816,17,18
Human sTfR ELISA RD 194011100 merupakan immunoassay dengan
menggunakan antibodi monoklonal ganda untuk pengukuran kuantitatif, konsentrasi sTfR normal adalah sekitar 1,0-2,9 µg/ml untuk dewasa, bila menggunakan assay ini, keadaan defisiensi besi dapat meningkatkan nilai tersebut hingga 20 kali lipat. Nilai batas kadar sTfR pada anak yang sehat untuk mengindikasikan adanya tanda permulaan defisiensi besi intraseluler adalah bila kadar sTfR >2,5 µg/ml.16,17
2.3. Kejang demam 2.3.1. Definisi
Ada dua definisi kerja yang telah dipublikasikan tentang kejang demam. Definisi kejang demam menurut National Institutes of Health Consensus
Conference adalah kejadian kejang pada bayi dan anak, yang biasanya terjadi
antara umur 3 bulan sampai 5 tahun, berkaitan dengan demam tanpa adanya bukti-bukti infeksi atau sebab yang jelas di intrakranial. Kejang yang disertai demam pada anak yang sebelumnya menderita kejang tanpa demam atau epilepsi tidak termasuk dalam kategori ini. Sedangkan definisi menurut International League
Against Epilepsy Commision on Epidemiology and Prognosis adalah kejang yang
terjadi pada anak-anak setelah umur 1 bulan, berkaitan dengan demam dan penyakit yang tidak disebabkan karena infeksi pada susunan saraf pusat, gangguan metabolik dan elektrolit, epilepsi atau kejang tanpa provokasi sebelumnya. Kejang
demam kebanyakan disertai infeksi virus dibandingkan bakteri, umumnya terjadi pada 24 jam pertama sakit dan berhubungan dengan infeksi saluran nafas akut, seperti faringitis dan otitis media, pneumonia, infeksi saluran kemih, serta gangguan gastroenteritis.29-3129,30,31
Kejang demam dikelompokkan menjadi dua, yaitu kejang demam sederhana dan kejang demam kompleks. Yang termasuk kejang demam sederhana apabila :
1. Kejang bersifat umum
2. Lama bangkitan kejang berlangsung kurang dari 15 menit
3. Dalam waktu 24 jam atau selama periode demam tidak ada bengkitan kejang berulang
Sedangkan yang termasuk kejang demam kompleks apabila : 1. Lama bangkitan kejang berlangsung lebih dari 15 menit 2. Manifestasi kejang bersifat fokal
3. Didapatkan bangkitan kejang berulang dalam kurun waktu 24 jam 4. Didapatkan abnormalitas status neurologi
5. Didapatkan riwayat kejang tanpa demam pada orangtua atau saudaranya Sebagian besar kejang demam (63%) berupa kejang demam sederhana dan 35% berupa kejang demam kompleks.32-3432,33,34
2.3.2. Patofisiologi
Energi yang didapat dari metabolisme diperlukan untuk mempertahankan kelangsungan hidup sel atau organ otak. Energi tersebut diperoleh dari oksidasi glukosa menjadi CO2 dan H2O. Sel dikelilingi oleh suatu membran yang terdiri dari permukaan dalam adalah lipoid dan permukaan luar adalah ionik. Dalam keadaan normal membran sel neuron dapat dilalui dengan mudah oleh ion K+ dan
sangat sulit dilalui oleh ion Na+ dan elektrolit-elektrolit lain kecuali ion Cl-, akibatnya konsentrasi K+ dalam sel neuron tinggi dan konsentrasi Na+ rendah, sedangkan diluar sel neuron keadaan sebaliknya. Perbedaan jenis dan konsentrasi ion didalam dan diluar sel mengakibatkan perbedaan potensial yang disebut potensial membran dari sel neuron. Konsentrasi ion K+ dan Na + intrasel dan ekstrasel selalu dipertahankan tetap oleh Na+- K+ATPase. Perubahan keseimbangan potensial membran bisa terjadi karena adanya :
1. perubahan konsentrasi ion intraseluler dan ekstraseluler.
2. Rangsangan yang datangnya mendadak misalnya mekanis, kimiawi atau aliran listrik dari sekitarnya.
3. Perubahan fisiologi dari membran sendiri karena penyakit atau kelainan genetik.35
Potensial aksi adalah aktivitas listrik mendadak sel neuron. Potensial aksi terjadi akibat perubahan potensial membran. Perubahan permeabilitas membran sel mengakibatkan terjadi difusi ion melewati membran sel sehingga terjadi perubahan konsentrasi ion intra dan ekstra sel. Adanya potensial aksi berpengaruh terhadap pintu-voltase kanal ion (voltage-gated ion channel) pada membran sel. Ion-ion natrium sekarang dapat mengadakan difusi masuk ke dalam sel neuron atau akson. Masuknya ion-ion natrium yang bermuatan listrik positif ke dalam sel neuron atau akson menyebabkan membran tersebut menjadi positif di dalam dan negatif di luar, sehingga dengan demikian terjadi suatu keadaan yang sebaliknya dari keadaan istirahat dan peristiwa ini disebut depolarisasi. Depolarisasi yang berlebihan ini dapat disebabkan karena gangguan produksi energi yang diperlukan untuk mempertahankan potensial membran (misalnya kondisi hipoksemia,
iskemia, hipoglikemia), ketidakseimbangan neurotransmiter eksitator dan inhibitor, serta interaksi antara kalsium dan magnesium dengan membran saraf yang menyebabkan hambatan pergerakan natrium sehingga terjadi peningkatan ion natrium yang masuk ke dalam sel dan depolarisasi.36,37 Potensial aksi yang terjadi akan dihantarkan sampai ke ujung akson. Adanya potensial aksi pada ujung akson mengakibatkan visikel di ujung akson pecah dan terlepas neurotrasmiter keluar ke celah sinaps. Neurotrasmiter di celah sinaps ditangkap oleh reseptor yang sesuai, terletak pada membran sel post sinapsis.36
Neurotransmiter merupakan zat kimia yang disintesis dalam neuron dan disimpan dalam gelembung sinaptik pada ujung akson. Zat kimia ini dilepaskan dari akson terminal melalui eksositosis dan juga direabsorbsi untuk daur ulang. Neurotransmiter merupakan cara komunikasi antar neuron. Setiap neuron melepaskan satu transmiter. Zat-zat kimia ini menyebabkan perubahan permeabilitas sel neuron, sehingga neuron menjadi lebih atau kurang dapat menyalurkan impuls, tergantung dari jenis neurotransmiter tersebut.38 Terdapat 50 jenis neurotransmiter yang telah ditemukan. Neurotransmiter di dalam susunan saraf pusat meliputi monoamin (noradrenalin, dopamin, dan serotonin), asetilkolin, γ-aminobutyric acid (GABA), neuropeptida (vasipresin, oksitosin),
dan berbagai ”releasing factors” yang dikeluarkan oleh hipotalamus, enkefalin, endorfin, dan zat P. Pada umumnya prostaglandin tidak dimasukkan kelompok neurotransmiter tetapi dipandang sebagai mediator sinaptik. Berdasarkan fungsinya dibagi 2, yaitu eksitator (asam glutamat, asetilkolin, serotonin) dan inhibitor (GABA, glisin). Pengaturan fungsi neurotransmiter berperan penting dalam menimbulkan kejang dan pencegahan bangkitan kejang.7,39
Asam glutamat merupakan neurotransmiter eksitator utama dalam otak. Asam glutamat dapat berperan sebagai reseptor ionotropik dan metabotropik. Rangsangan asam glutamat terespon oleh reseptor ionotropik (NMDA, AMPA,
Kainate) mengakibatkan pintu-voltase kanal ion Na+ dan Ca2+ terbuka sehingga
mengakibatkan ion Na+ dan Ca2+ influx, hal ini mengakibatkan depolarisasi post
sinapsis. Perubahan potensial membran tersebut apabila melewati nilai ambang
letup akan mengakibatkan potensial aksi di neuron post sinapsis. Pengarug asam glutamat yang terespon oleh reseptor metabotropik mengaktifkan fosfolipase C di plasma membran, sehingga terjadi pemecahan fosfatidil inositol difosfat (PIP2) menjadi inositol trifosfat (IP3) dan diacyl glyserol. Inositol trifosfat akan meenyebabkan mobilisasi ion Ca2+ didalam retikulum endoplasma keluar ke plasma intrasel. Rangsangan pada sel neuron post sinapsis dapat mengalami
sumasi, fasilitasi, oklusi dan reverberating.36,39
GABA merupakan neurotransmiter inhibitor yang mengaktifkan reseptor GABA-A dan GABA-B sehingga permeabilitas membran sel terhadap ion Cl- dan K+ meningkat. Peningkatan permeabilitas ion Cl- dan K+ mengakibatkan hiperpolarisasi post sinapsis. Keadaan hiperpolarisasi mengakibatkan hambatan terhadap timbulnya potensial aksi di post sinapsis. 7,39
Apabila neurotransmiter eksitator lebih dominan daripada inhibitor maka akan terjadi depolarisasi post sinapsis. Adanya peristiwa sumasi dan fasilitasi mengakibatkan keadaan depolarisasi diperbesar dan apabila mencapai nilai ambang letup akan terjadi potensial aksi pada neuron post sinapsis. Apabila potensial aksi meluas dan terjadi sinkronisasi akan menimbulkan bangkitan kejang demam.7,39
2.3.3. Faktor risiko
Kejang demam dapat terjadi karena adanya pengaruh beberapa hal, yaitu:
2.3.3.1. Umur
Umur terjadinya kejang demam berkisar antara 6 bulan-5 tahun. Insiden bangkitan kejang demam tertinggi terjadi pada umur 18 bulan. Umur tersebut terkait dengan fase perkembangan otak yaitu masa developmental window. Masa
developmental window merupakan masa perkembangan otak fase organisasi yaitu
pada waktu anak berumur kurang dari 2 tahun. Pada masa perkembangan otak (developmental window) keadaan otak belum matang, reseptor untuk asam glutamat baik ionotropik meliputi N methyl D aspartate (NMDA) dan Amino 3 hydroxy 5 methyl 4 isoxazole proprionic acid (AMPA) maupun metabotropik sebagai reseptor eksitator padat dan aktif, sebaliknya reseptor GABA sebagai inhibitor kurang aktif, sehingga mekanisme eksitasi lebih dominan dibanding inhibisi. Eksitabilitas membrane sel, pengangkut dan reseptor neurotransmiter, reseptor neuropeptid, neuromudulator peptid, pintu kanal ion dan mekanisme homeostasis ion selalu berubah selama perkembangan otak dan sejalan dengan pertambahan umur. Pada otak yang belum matang regulasi ion Na+, K+, dan Ca++ belum sempurna, sehingga mengakibatkan gangguan repolarisasi pasca depolarisasi dan meningkatkan eksitabilitas neuron. Sehingga pada masa
developmental window merupakan masa yang rawan terjadinya kejang
demam.7,40,41
2.3.3.2. Demam
Demam tersering disebabkan oleh infeksi terutama virus (80%). Pada infeksi terjadi karena reaksi dari lipopolisakarida bakteri, serpihan protein dari lekosit dan degenerasi jaringan terhadap thermostat hipothalamus. Interleukin-1
dan prostagladin sebagai pirogen endogen berperan terhadap kenaikan suhu di otak dan eksitabilitas neuron serta nilai ambang kejang. Perubahan kenaikan temperatur tubuh berpengaruh terhadap nilai ambang kejang dan eksitabilitas neural, karena kenaikan suhu tubuh berpengaruh pada kanal ion dan metabolisme seluler serta produksi ATP. Setiap kenaikan suhu tubuh satu derajat Celsius akan meningkatkan metabolisme karbohidrat 10-15%, sehingga dengan adanya peningkatan suhu akan mengakibatkan peningkatan kebutuhan glukosa dan oksigen.36,40
Demam tinggi akan dapat mengakibatkan hipoksi jaringan termasuk jaringan otak. Pada keadaan metabolisme di siklus Kreb normal, satu molukul glukose akan menghasilkan 38 ATP, sedangkan pada keadaan hipoksi jaringan metabolisme berjalan anaerob, satu molukul glukosa hanya akan menghasilkan 2 ATP, sehingga pada keadaan hipoksi akan kekurangan energi, hal ini akan menggangu fungsi normal pompa Na+ dan reuptake asam glutamat oleh sel g1ia. Ke dua hal tersebut mengakibatkan masuknya ion Na+ ke dalam sel meningkat dan timbunan asam glutamat ekstrasel. Timbunan asam glutamat ekstrasel akan mengakibatkan peningkatan permeabilitas membran sel terhadap ion Na+ sehingga semakin meningkatkan masuknya ion Na+ ke dalam sel. Masuknya ion Na+ ke dalam sel dipermudah dengan adanya demam, sebab demam akan meningkatkan mobilitas dan benturan ion terhadap membran sel. Perubahan konsentrasi ion Na+ intrasel dan ekstrasel tersebut akan mengakibatkan perubahan potensial memban sel neuron sehingga membran sel dalam keadaan depolarisasi. Disamping itu demam dapat merusak neuron GABA-ergik sehingga fungsi inhibisi terganggu.36,42
Bangkitan kejang demam terbanyak terjadi pada kenaikan suhu tubuh berkisar 38,9o C – 39,9oC ( 40-56%). Bangkitan kejang terjadi pada suhu tubuh 37 o C – 38,9 o C sebanyak 11% penderita dan sebanyak 20 % penderita kejang demam terjadi pada suhu tubuh di atas 40 o C.43
2.3.3.3. Faktor genetik
Cara pewarisan sifat genetik terkait dengan kejang demam belum dapat dipastikan, Tetapi nampaknya pewarisan gen secara autosomal dominan paling banyak ditemukan. Penetrasi autosomal dominan diperkirakan sekitar 60% - 80% dengan mutasi gen pada kromosom 19p dan 8q13-21.44,45
Apabila salah satu orang tua penderita dengan riwayat pernah menderita kejang demam mempunyai risiko untuk terjadi bangkitan kejang demam sebesar 20 % - 22%. Dan apabila ke dua orang tua penderita tersebut mempunyai riwayat pernah menderita kejang demam maka risiko untuk terjadi bangkitan kejang demam meningkat menjadi 59-64%, tetapi sebaliknya apabila kedua orangtuanya tidak mempunyai riwayat pernah menderita kejang demam maka risiko terjadi kejang demam hanya 9%. Pewarisan kejang demam lebih banyak oleh ibu dibandingkan ayah, yaitu 27% berbanding 7%. Pada anak dengan kejang demam yang pertama, risiko untuk terjadi kejang demam pada saudara kandungnya berkisar 10%-45%.36,44
Menurut penelitian yang dilakukan oleh Bahtera T terhadap 148 anak yang menderita kejang demam, didapatkan adanya hubungan mutasi gen pintu-voltase kanal ion natrium (channelopathy) dengan umur, suhu, jarak waktu antara mulai demam sampai timbul bangkitan kejang, jenis kejang demam saat bangkitan
kejang demam pertama, riwayat keluarga (first degree relative) pernah menderita kejang demam. Mutasi gen pintu-voltase kanal ion natrium subunit α (SCNIA) mengakibatkan terjadi pergantian asam amino argenin bersifat polar oleh asam amino alanin yang bersifat non polar dan terjadi kodon stop. Adanya kodon stop mengakibatkan deretan asam amino penyusun pintu-voltase kanal ion natrium (voltage-gated Na+ channel) lebih pendek. Pergantian asam amino argenin bersifat polar oleh asam amino alanin bersifat non polar dan kodon stop mengakibatkan fungsi pintu-voltase kanal ion natrium (voltage-gated Na+
channel) terganggu. Mutasi gen pintu-voltase kanal ion natrium subunit α
(SCNIA) mempunyai risiko 3,5 kali terjadi kejang demam berulang sedangkan mutasi gen pintu-voltase kanal ion natrium subunit β (SCNIB) mempunyai risiko 2,8 kali terjadi kejang demam berulang.36
2.3.3.4. Riwayat penyulit dalam kehamilan maupun persalinan
Faktor-faktor pre natal yang berpengaruh terhadap terjadinya kejang demam antara lain umur ibu saat hamil, kehamilan dengan eklampsia dan hipertensi, kehamilan primipara atau multipara, paparan asap rokok saat kehamilan.46
Umur ibu pada saat hamil sangat menentukan status kesehatan bayi yang akan dilahirkan. Umur ibu kurang dari 20 tahun atau lebih dari 35 tahun dapat mengakibatkan berbagai komplikasi kehamilan dan persalinan. Komplikasi kehamilan di antaranya adalah hipertensi dan eklamsia, sedangkan gangguan pada persalinan di antaranya adalah trauma persalinan. Komplikasi kehamilan dan persalinan dapat menyebabkan prematuritas, lahir dengan berat badan kurang, penyulit persalinan dan partus lama. Keadaan tersebut dapat mengakibatkan janin
dengan asfiksia. Pada asfiksia akan terjadi hipoksia dan iskemia. Hipoksia dapat mengakibatkan rusaknya faktor inhibisi dan atau meningkatnya fungsi neuron eksitasi, sehingga mudah timbul kejang bila ada rangsangan yang memadai.46
Merokok dapat mempengaruhi kehamilan dan perkembangan janin, bukti ilmiah menunjukkan bahwa merokok selama kehamilan meningkatkan risiko kerusakan janin. Dampak lain dari merokok pada saat hamil adalah terjadinya placenta previa. Placenta previa dapat menyebabkan perdarahan berat pada kehamilan atau persalinan dan bayi sungsang sehingga diperlukan seksio sesaria. Keadaan ini dapat menyebabkan trauma lahir yang berakibat teriadinya kejang. Penelitian Cassano dan Vestergaard menunjukkan bahwa konsumsi rokok dan alkohol pada masa kehamilan termasuk faktor risiko terjadinya kejang demam sederhana maupun kejang demam kompleks. Sebaliknya, pengurangan atau pembatasan komsumsi rokok dan alkohol selama masa kehamilan merupakan usaha yang efektif untuk mencegah kejang demam pada anak.47
Faktor natal yang menjadi faktor risiko untuk terjadinya kejang demam antara lain adalah prematuritas, asfiksia, bayi berat lahir rendah, dan partus lama. Pada asfiksia perinatal akan terjadi hipoksia dan iskemia di jaringan otak. Hipoksia dan iskemia akan menyebabkan peningkatan cairan dan natrium intraseluler sehingga terjadi edema otak. Daerah yang sensitif terhadap hipoksia adalah inti-inti pada batang otak, thalamus, dan kolikulus inferior, sedangkan daerah yang sensitif terhadap iskemia adalah ”watershead area” yaitu daerah parasagital hemisfer yang mendapat vaskularisasi paling sedikit. Hipoksia dapat mengakibatkan rusaknya faktor inhibisi dan atau meningkatnya fungsi neuron eksitator sehingga mudah timbul kejang bila ada rangsangan yang memadai.48
Bayi prematur perkembangan alat-alat tubuhnya kurang sempurna sehingga belum berfungsi dengan baik. Hal ini menyebabkan bayi sering mengalami apneu, asfiksia berat, dan sindrom gangguan nafas sehingga bayi mengalami hipoksia. Semakin lama terjadi hipoksia, semakin berat kerusakan otak yang terjadi dan semakin besar kemungkinan terjadi kejang. Daerah yang rentan terhadap kerusakan antara lain adalah hipokampus. Serangan kejang yang berulang akan menyebabkan kerusakan otak juga semakin luas. Pada masa pasca natal, infeksi susunan saraf, trauma kepala dan gangguan toksik metabolik dapat menjadi faktor risiko terjadinya kejang demam di kemudian hari.46
2.3.3.5. Infeksi berulang
Infeksi berulang merupakan faktor risiko untuk terjadi kejang demam.
Penderita pengunjung day care atau dititipkan pada penitipan anak lebih sering terkena infeksi dibandingkan anak yang tinggal dirumah. Kejang demam sebagian besar (80%) disebabkan infeksi virus, sedangkan karena bakteri jarang. Beberapa peneliti melaporkan infeksi virus yang ditemukan pada penderita kejang demam seperti Human Herpes Virus 6, enterovirus dan virus Influenza A Sydney variant (H3N2). Peneliti lain menemukan bangkitan kejang demam karena penyakit-penyakit Shigellosis 19,7%, Faringitis 38%, Otitis media 23%, Pneumonia 15%, Gastroenteritis 7%, Roseola infantum 5%, penyakit bukan karena infeksi 12% (pasca imunisasi MMR dan DPT).49
2.3.3.6. Status besi
Otak cukup sensitif terhadap defisiensi besi dalam makanan. Terdapat banyak mekanisme untuk mengatur arus zat besi secara homeostatik. Besi dibutuhkan untuk mielinisasi medula spinalis dan substansia alba pada girus-girus
serebelar di otak dan merupakan kofakor bagi sejumlah enzim yang terlibat dalam sintesis neurotransmiter. Selain itu, defisiensi besi menyebabkan perubahan pada berbagai proses metabolik yang dapat mengganggu fungsi otak, di antaranya termasuk metabolisme neurotransmiter, sintesis protein, organogenesis, dan lain-lain. Bukti peranan besi pada metabolisme neurotransmiter telah diselidiki oleh para peneliti. Besi sangat penting untuk beberapa enzim yang terlibat dalam sintesis neurotransmiter, termasuk triptofan hidroksilase (serotonin) dan tirosin hidroksilase (norepinefrin/NE dan dopamin). Selain itu, besi adalah kofaktor untuk ribonukleotida reduktase dan sangat penting untuk fungsi sejumlah reaksi transfer elektron yang berhubungan dengan metabolisme lipid maupun metabolisme energi otak. Besi berhubungan dengan aktivitas monoamin oksidase, suatu enzim yang sangat penting untuk laju degradasi normal dari neurotransmiter-neurotransmiter.13,14
Metabolisme serotonin maupun norepinefrin akan berubah pada defisiensi besi di otak. Kepadatan transporter serotonin lebih rendah secara bermakna pada mencit-mencit yang mengalami defisiensi besi, sedangkan mikrodialisis in vivo pada tikus memberikan bukti penurunan laju pengambilan norepinefrin. Penelitian Beard J tentang toleransi dingin dan termoregulasi menunjukkan bahwa wanita dan tikus kekurangan zat besi akan mengalami peningkatan kadar norepinefrin plasma. Hal ini sesuai dengan penguraian norepinefrin yang lebih cepat dari cadangan di sistem saraf tepi dan menunjukkan efek dari defisiensi besi terhadap mekanisme pengambilan monoamin. Penting untuk diketahui bahwa transporter serotonin, norepinefrin dan dopamin semuanya termasuk golongan kotransporter
Na+ yang sama dan menunjukkan karakteristik regulasi dan translokasi yang sama.14
Penelitian Mittal dkk melaporkan bahwa defisiensi besi fase awal pada hewan coba telah menunjukkan penurunan bermakna pada kadar GABA di otak. Enzim yang bertanggung jawab untuk sintesis GABA yaitu Glutamic acid
decarboxylase (GAD) berkurang secara signifikan. Penelitian Agarwal
melaporkan defisiensi besi fase awal menunjukkan peningkatan secara bermakna kadar asam glutamat di otak. Ketidakseimbangan antara neurotransmiter eksitator asam glutamat dan inhibitor GABA berperan penting dalam menimbulkan bangkitan kejang demam.15
2.4. Hubungan antara defisiensi besi dengan bangkitan kejang demam
Besi merupakan komponen esensial pada pertumbuhan otak dan fungsi sistem saraf pusat. Pertumbuhan otak sangat sensitif terhadap perubahan status besi karena pertumbuhan dan perkembangan otak yang cepat serta terjadi pada jeda waktu yang singkat sehingga defisiensi besi dapat mengakibatkan gangguan fungsi otak. Terdapat 3 proses di otak bila terjadi defisiensi besi yang masing-masing proses umumnya berjalan secara hampir bersamaan, yaitu :14,27
a. Gangguan pembentukan mielin
b. Gangguan metabolisme neurotransmiter c. Gangguan metabolisme energi sel
Gangguan pembentukan mielin
Tipe sel predominan yang mengandung besi dalam otak adalah oligodendrosit. Sel ini berperan dalam proses mielinisasi sehingga gangguan
fungsi dari sel ini menyebabkan hipomielinisasi. Oligodendrosit berperan dalam pembentukan asam lemak dan kholesterol yang berperan dalam proses mielinisasi dimana sintesa keduanya memerlukan besi. Sebagai contoh, gangguan maturasi oligodendrosit, seperti yang terlihat sebagai akibat mutasi gen, akumulasi besi hanya 50% dari normal. Pada defisiensi besi, oligodendrosit tampak imatur akibat kurangnya besi terutama pada periode perkembangan otak dini. Tidak ada data kuantitatif yang menunjukkan defisiensi besi menyebabkan jumlah sel oligodendrosit berkurang, namun gangguan proses mielinisasi dibuktikan pada studi Shankar serta Algarin yang menunjukkan transmisi susunan saraf pada defisiensi besi cenderung lebih lambat. Temuan ini memiliki hubungan dengan tingkat keparahan defisiensi besi, semakin berat defisiensi besi maka transmisi saraf semakin lambat.27
Gangguan metabolisme neurotransmiter
Peranan besi pada neurotransmiter berpusat pada proses sintesa dan degradasinya. Dalam proses sintesa, besi sangat esensial pada berbagai enzim yang berperan pada sintesa neurotransmiter termasuk triptofan hidroksilase (serotonin) dan tirosin hidroksilase (norepinefrin dan dopamin). Selain itu, besi berhubungan dengan aktivitas enzim monoamin oksidase yang berperan dalam proses degradasi berbagai neurotransmiter.50
Pada percobaan binatang, efek besi pada fungsi saraf berhubungan dengan kadar besi dalam otak. Defisiensi besi pada tikus menghasilkan penurunan kepadatan reseptor dopamin, peningkatan kadar dopamin ekstraseluler, dan penurunan re uptake dopamin. Akibat dari berbagai proses tersebut mengakibatkan gangguan kognitif dan perilaku seperti iritabilitas, cenderung lebih
tidak aktif, dan terlihat lebih “takut” dibandingkan dengan kontrol. Efek perubahan neurotransmiter ini paling mengganggu fungsi hipokampus yang merupakan area sentral pengenalan kembali memori. Penelitian Mittal dkk melaporkan bahwa defisiensi besi fase awal pada hewan coba telah menunjukkan penurunan bermakna pada kadar GABA di otak. Enzim yang bertanggung jawab untuk sintesis GABA yaitu Glutamic acid decarboxylase (GAD) berkurang secara signifikan. Penelitian Agarwal melaporkan defisiensi besi fase awal menunjukkan peningkatan secara bermakna kadar asam glutamat di otak. 15,50,51
Gangguan metabolisme energi sel
Gangguan metabolisme pada sel otak yang mengakibatkan gangguan fungsi kognitif diperkirakan terdapat pada peranan zat besi pada aktivitas enzim sitokrom C oksidase. Enzim sitokrom C oksidase berperan pada tahap akhir proses oksidasi fosforilasi dan berperan penting pada pembentukan ATP sehingga enzim ini sangat berperan pada aktivitas metabolisme sel saraf. Dalam studi pada binatang oleh De Ungria menunjukkan penurunan kadar besi dalam otak hingga 75% akan menurunkan kadar enzim sitokrom C oksidase hingga 42%, serta area yang paling banyak terpengaruh adalah area dengan fungsi kognitif tinggi seperti hipokampus, korteks piriformis, nukleus thalamus dorsomedial, dan korteks singularis. Gangguan metabolisme pada berbagai area yang berperan dalam fungsi kognitif tinggi ini merupakan salah satu teori mengapa defisiensi besi menyebabkan gangguan fungsi kognitif.27,50
Selain ketiga proses di atas, peranan besi pada aktivitas enzim ribonukleotida reduktase sangat penting untuk fungsi sejumlah reaksi transfer elektron yang berhubungan dengan metabolisme lipid maupun metabolisme
energi otak dan berperan dalam regulasi pertumbuhan otak serta ikut mengatur terjadinya gangguan fungsi kognitif.51
Neurotransmiter yang berperan pada bangkitan kejang demam adalah neurotransmiter eksitator asam glutamat dan neurotransmiter inhibitor GABA.50
2.5. Kerangka teori - Perdarahan - Infeksi - BBLR - prematuritas Laktoferin
Diet Defisiensi besi Proses tumbuh kembang
(sTfR)
Transmisi saraf
Kadar neurotransmiter asam glutamat dan GABA
Eksitator > inhibitor
Kadar enzim sitokrom C oksidase
Perilaku dan kognitif Perilaku dan kognitif
Kadar transferin serum
Faktor penyulit dalam kehamilan maupun
persalinan Status infeksi
Riwayat kejang demam pada keluarga
Demam Umur
Nilai ambang kejang
Terminal presinap akson sel neuron Na+-K+ pump ATP ase