MAKALAH
Korosi celah (crevice corrosion) &Korosi sumuran (pitting corrosion)
disusun untuk memenuhi tugas mata kuliah PBKTK
Oleh:
1. Avrillia Ika Swastikadewi
( 21030113060054 )
2013 A
2. Lyonita Clarasmara Dafitri ( 21030113060055 )
2013 A
3. Deanda Hary Rahadianti
( 21030113060056 )
2013 A
4. Surya Indra Pratama
( 21030113060057)
2013 A
PROGRAM STUDI DIPLOMA III TEKNIK KIMIA
FAKULTAS TEKNIK
UNIVERSITAS DIPONEGORO
SEMARANG
KATA PENGANTAR
Puji dan Syukur Penulis Panjatkan ke Hadirat Tuhan Yang Maha Esa karena berkat limpahan Rahmat dan Karunia-Nya sehingga penulis dapat menyusun makalah dengan judul Korosi celah (crevice corrosion) &Korosi sumuran (pitting corrosion).
Dalam penyusunan makalah ini, penulis banyak mendapat tantangan dan hambatan akan tetapi dengan bantuan dari berbagai pihak tantangan itu bisa teratasi. Olehnya itu, penulis mengucapkan terima kasih yang sebesar-besarnya kepada semua pihak yang telah membantu dalam penyusunan makalah ini, semoga bantuannya mendapat balasan yang setimpal dari Tuhan Yang Maha Esa.
Penulis menyadari bahwa makalah ini masih jauh dari kesempurnaan baik dari bentuk penyusunan maupun materinya. Kritik konstruktif dari pembaca sangat penulis harapkan untuk penyempurnaan makalah selanjutnya.
Akhir kata semoga makalah ini dapat memberikan manfaat kepada kita sekalian.
Semarang,Mei 2014
Penulis
ii
PENDAHULUAN
1.1. Latar Belakang
Dalam kehidupan sehari-hari, korosi dapat kita jumpai terjadi pada berbagai jenis logam. Bangunan-bangunan maupun peralatan elektronik yang memakai komponen logam seperti seng, tembaga, besi baja, dan sebagainya semuanya dapat terserang oleh korosi ini. Selain pada perkakas logam ukuran besar, korosi ternyata juga mampu menyerang logam pada komponen-komponen renik peralatan elektronik, mulai dari jam digital hingga komputer serta peralatan canggih lainnya yang digunakan dalam berbagai aktivitas umat manusia, baik dalam kegiatan industri maupun di dalam rumah tangga.
Kerugian yang dapat ditimbulkan oleh korosi tidak hanya biaya langsung seperti pergantian peralatan industri, perawatan jembatan, konstruksi dan sebagainya, tetapi juga biaya tidak langsung seperti terganggunya proses produksi dalam industri serta kelancaran transportasi yang umumnya lebih besar dibandingkan biaya langsung.
1.2. Rumusan Masalah
Berdasarkan latar belakang masalah yang dikemukakan di atas, maka kami merumuskan permasalahan sebagai berikut :
1. Apa yang dimaksud dengan korosi dan faktor apa yang mempengaruhi korosi?
2. Apa yang dimaksud dengan korosi celah dan korosi sumuran?
3. Bagaimana dampak korosi dan pencegahan korosi?
1.3. Tujuan
Dapat memahami tentang korosi
Dapat memahami dampak- dampak dari korosi
Dapat memahami upaya pencegahan korosi
Dapat memahami tentang korosi celah dan korosi sumuran
BAB II ISI 2.1 Pengertian Korosi
Korosi berasal dari bahasa latin ”Corrodere” yang artinya perusakan logam atau berkarat akibat lingkungannya. Korosi merupakan proses elektrokimia yang terjadi pada logam, atau proses perusakan material karena bereaksi dengan lingkungannya. Selain itu, korosi juga diartikan sebagai kerusakan yang terjadi pada material akibat adanya reaksi kimia. Tetapi dimasyarakat korosi lebih identik dengan istilah ”karat” yang merupakan korosi khusus pada besi, hal ini terjadi karena besi merupakan logam yang paling banyak digunakan oleh masyarakat.
2.2 Proses Terjadinya Korosi
Korosi adalah penurunan mutu logam akibat reaksi elektro kimia dengan lingkungannya. Korosi atau pengkaratan merupakan fenomena kimia pada bahan – bahan logam yang pada dasarnya merupakan reaksi logam menjadi ion pada permukaan logam yang kontak langsung dengan lingkungan berair dan oksigen. Contoh yang paling umum, yaitu kerusakan logam besi dengan terbentuknya karat oksida. Dengan demikian, korosi menimbulkan banyak kerugian. (Kennet dan Chamberlain, 1991)
2.3 Penyebab Korosi
Faktor yang berpengaruh terhadap korosi dapat dibedakan menjadi dua, yaitu yang berasal dari bahan itu sendiri dan dari lingkungan. Faktor dari bahan meliputi kemurnian bahan, struktur bahan, bentuk kristal, unsur-unsur kelumit yang ada dalam bahan, teknik pencampuran bahan dan sebagainya. Faktor dari lingkungan meliputi tingkat pencemaran udara, suhu, kelembaban, keberadaan zat-zat kimia yang bersifat korosif dan sebagainya. Bahan-bahan korosif (yang dapat menyebabkan korosi) terdiri atas asam, basa serta garam, baik dalam bentuk senyawa an-organik maupun organik. (Kennet dan Chamberlain, 1991)
2.4. Faktor yang mempengaruhi Korosi
Korosi pada permukaan suatu logam dapat dipercepat oleh beberapa faktor, antara lain:
1. Kontak Langsung logam dengan H2O dan O2
Korosi pada permukaan logam merupakan proses yang mengandung reaksi redoks. Reaksi yang terjadi ini merupakan sel Volta mini. sebagai contoh, korosi besi terjadi apabila ada oksigen (O2) dan air (H2O). Logam besi tidaklah murni, melainkan mengandung
campuran karbon yang menyebar secara tidak merata dalam logam tersebut. Akibatnya menimbulkan perbedaan potensial listrik antara atom logam dengan atom karbon (C). Atom
logam besi (Fe) bertindak sebagai anode dan atom C sebagai katode. Oksigen dari udara yang larut dalam air akan tereduksi, sedangkan air sendiri berfungsi sebagai media tempat berlangsungnya reaksi redoks pada peristiwa korosi. Semakin banyak jumlah O2 dan H2O
yang mengalami kontak denan permukaan logam, maka semakin cepat berlangsungnya korosi pada permukaan logam tersebut.
2. Keberadaan Zat Pengotor
Zat Pengotor di permukaan logam dapat menyebabkan terjadinya reaksi reduksi tambahan sehingga lebih banyak atom logam yang teroksidasi. Sebagai contoh, adanya tumpukan debu karbon dari hasil pembakaran BBM pada permukaan logam mampu mempercepat reaksi reduksi gas oksigen pada permukaan logam. Dengan demikian peristiwa korosi semakin dipercepat pengotor yang mempercepat korosi pada permukaan logam.
3. Kontak dengan Elektrolit
Keberadaan elektrolit, seperti garam dalam air laut dapat mempercepat laju korosi dengan menambah terjadinya reaksi tambahan. Sedangkan konsentrasi elektrolit yang besar dapat melakukan laju aliran elektron sehingga korosi meningkat. Bangkai kapal di dasar laut yang telah terkorosi oleh kandungan garam yang tinggi.
4. Temperatur
Temperatur mempengaruhi kecepatan reaksi redoks pada peristiwa korosi. Secara umum, semakin tinggi temperatur maka semakin cepat terjadinya korosi. Hal ini disebabkan dengan meningkatnya temperatur maka meningkat pula energi kinetik partikel sehingga kemungkinan terjadinya tumbukan efektif pada reaksi redoks semakin besar. Dengan demikian laju korosi pada logam semakin meningkat. Efek korosi yang disebabkan oleh pengaruh temperatur dapat dilihat pada perkakas-perkakas atau mesin-mesin yang dalam pemakaiannya menimbulkan panas akibat gesekan (seperti cutting tools ) atau dikenai panas secara langsung (seperti mesin kendaraan bermotor). Knalpot kendaraan bermotor yang mudah terkorosi akibat temperatur tinggi.
5. pH
Peristiwa korosi pada kondisi asam, yakni pada kondisi pH < 7 semakin besar, karena adanya reaksi reduksi tambahan yang berlangsung pada katode yaitu: 2H+
(aq) + 2e- → H2
menyebabkan lebih banyak atom logam yang teroksidasi sehingga laju korosi pada permukaan logam semakin besar.
6. Mikroba
Adanya koloni mikroba pada permukaan logam dapat menyebabkan peningkatan korosi pada logam. Hal ini disebabkan karena mikroba tersebut mampu mendegradasi logam melalui reaksi redoks untuk memperoleh energi bagi keberlangsungan hidupnya. Mikroba yang mampu menyebabkan korosi, antara lain: protozoa, bakteri besi mangan oksida, bakteri reduksi sulfat, dan bakteri oksidasi sulfur-sulfida. Thiobacillus thiooxidans Thiobacillus ferroxidans. Koloni bakteri Thiobacillus ferrooxidans pada permukaan logam besi yang terkorosi. Koloni bakteri Thiobacillus thiooxidans yang dapat menyebabkan korosi pada logam. (Supardi, 1997)
2.5. Bakteri Penyebab Korosi
Fenomena korosi yang terjadi dapat disebabkan adanya keberadaan dari bakteri. Jenis-jenis bakteri yang berkembang yaitu :
1. Bakteri reduksi sulfat
Bakteri ini merupakan bakteri jenis anaerob membutuhkan lingkungan bebas oksigen atau lingkungan reduksi, bakteri ini bersirkulasi di dalam air aerasi termasuk larutan klorin dan oksidiser lainnya, hingga mencapai kondisi ideal untuk mendukung metabolisme. Bakteri ini tumbuh pada oksigen rendah. Bakteri ini tumbuh pada daerah-daerah kanal, pelabuhan, daerah air tenang tergantung pada lingkungannya.
Bakteri ini mereduksi sulfat menjadi sulfit, biasanya terlihat dari meningkatnya kadar H2S atau Besi sulfida.Tidak adanya sulfat, beberapa turunan dapat berfungsi sebagai fermenter menggunakan campuran organik seperti pyruvnate untuk memproduksi asetat, hidrogen dan CO2, banyak bakteri jenis ini berisi enzim hidrogenase yang mengkonsumsi hidrogen.
2. Bakteri oksidasi sulfur-sulfida
Bakteri jenis ini merupakan bakteri aerob yang mendapatkan energi dari oksidasi sulfit atau sulfur. Bebarapa tipe bakteri aerob dapat teroksidasi sulfur menjadi asam sulfurik dan nilai pH menjadi 1. bakteriThiobaccilus umumnya ditemukan di deposit mineral dan menyebabkan drainase tambang menjadi asam.
3. Bakteri besi mangan oksida
Bakteri memperoleh energi dari osidasi Fe2+ Fe3+ dimana deposit berhubungan dengan bakteri korosi. Bakteri ini hampir selalu ditemukan di Tubercle (gundukan Hemispherikal berlainan ) di atas lubang pit pada permukaan baja. Umumnya oksidaser besi ditemukan di lingkungan dengan filamen yang panjang. (Supardi, 1997)
2.6 Korosi celah / Crevice Corrosion
Gambar korosi celah pada sambungan pipa
Sumber : Ismanto Alpha (2009)
Korosi celah mengacu pada serangan lokal pada permukaan logam pada, atau berbatasan langsung dengan, kesenjangan atau celah antara dua permukaan bergabung. Kesenjangan atau celah dapat terbentuk antara dua logam atau logam dan bahan non-logam. Di luar kesenjangan atau tanpa celah, kedua logam yang tahan terhadap korosi. Kerusakan yang disebabkan oleh korosi celah biasanya dibatasi pada satu logam di wilayah lokal dalam atau dekat dengan permukaan yang bergabung.
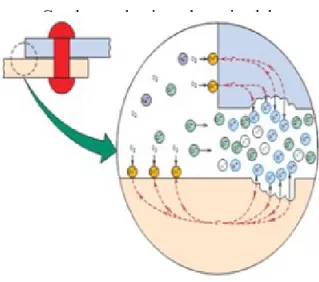
Mekanisme Crevice Corrosion : dimulai oleh perbedaan konsentrasi beberapa kandungan kimia, biasanya oksigen, yang membentuk konsentrasi sel elektrokimia (perbedaan sel aerasi dalam kasus oksigen). Di luar dari celah (katoda), kandungan oksigen dan pH lebih tinggi -tetapi klorida lebih rendah.
Gambar mekanisme korosi celah
Cara pengendalian korosi celah adalah sebagai berikut:
Hindari pemakaian sambungan paku keeling atau baut, gunakan sambungan las.
Gunakan gasket non absorbing.
Usahakan menghindari daerah dengan aliran udara.
( Ismanto Alpha ,2009 )
Gambar korosi sumuran pada westafle
Gambar 6. Korosi Sumuran Sumber : Ismanto Alpha (2009)
Korosi sumuran adalah korosi lokal dari permukaan logam yang dibatasi pada satu titik atau area kecil, dan membentukn bentuk rongga. Korosi sumuran adalah salah satu bentuk yang paling merusak dari korosi.
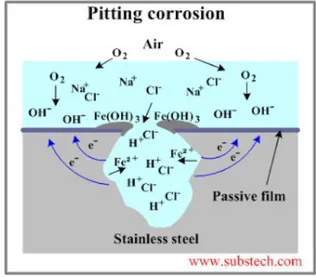
Mekanisme Pitting Corrosion : Untuk material bebas cacat, korosi sumuran disebabkan oleh lingkungan kimia yang mungkin berisi spesies unsur kimia agresif seperti klorida. Klorida sangat merusak lapisan pasif (oksida) sehingga pitting dapat terjadi pada dudukan oksida. Lingkungan juga dapat mengatur perbedaan sel aerasi (tetesan air pada permukaan baja, misalnya) dan pitting dapat dimulai di lokasi anodik (pusat tetesan air).
Gambar mekanisme pitting corrosion
Cara pengendalian korosi sumuran adalah sebagai berikut:
Hindari permukaan logam dari goresan.
Perhalus permukaan logam.
Menghindari komposisi material dari berbagai jenis logam.
( Ismanto Alpha ,2009 )
2.8. Akibat dan dampak korosi dalam kehidupan
Kerugian yang ditimbulkan oleh korosi diantaranya adalah: 1. Adanya kerugian teknis dan depresiasi
2. menurunnya efisiensi
3. menurunnya kekuatan konstruksi 4. Apperance yang buruk
5.karat merupakan polusi dan menambah biaya maintenance
Kerugian Akibat Korosi
Ditinjau dari segi kerugian akibat korosi dapat digolongkan menjadi tiga jenis yaitu kerugian dari segi biaya korosi itu sangat tinggi atau mahal, kerugain dari segi pemborosan sumber daya mineral yang sangat tinggi dan kerugian dari segi keselamatan jiwa manusia juga sangat membahayakan.
Kerugian Ekonomi
Menurut sumber dari biro Klasifikasi indonesia pada tahun 1997 mengatakan bahwa pada umumnya biaya pengendalian korosi di Indonesia berkisar antara 2 hingga 3,5 % dari GNP ( Growth National Produk ). Biaya pengendalian korosi adalah semua
biaya yang timbul untuk menanggulangi korosi mulai dari desain sampai dengan proses pemeliharaan.
Pemborosan Sumber Daya Alam
Pada dasarnya proses korosi dapat juga didefinisikan sebagai proses kembalinya logam teknis ke bentuk asalnya di alam. Bentuk asalnya logam di alam adalah senyawa-senyawa mineral yang abadi di perut bumi. Pada umumnya senyawa-senyawa-senyawa-senyawa mineral logam tersebut merupakan ikatan kimia antara unsur logam dengan unsur logam dengan unsur halogen misalnya oksigen dan belerang. Dengan adanya proses korosi pada struktur bangunan di tempat-tempat yang tersebar di seluruh dunia, mengakibatkan sumber daya mineral yang semula berbentuk logam teknis telah berubah menjadi produk korosi yang tersebar tanpa bisa didaur ulang untuk dijadikan logam teknis kembali.
Korosi dapat membahayakan jiwa manusia
Korosi dapat menimbulkan kecelakaan yang menelan puluhan korban bahkan ratusan korban jiwa atau mencederai manusia disebabkan karena kegagalan dari konstruksi bangunan akibat korosi. Di dunia pelayaran, korban manusia yang meninggal akibat kapal tenggalam jumlahnya sudah sangat banyak.
Estetika menurun
Korosi dapat menurunkan nilai estetika suatu material. Hal ini karena korosi dapat merusak lapisan permukaan material.
(Supardi, 1997)
2.9. Pencegahan korosi
Pencegahan korosi didasarkan pada prinsip berikut :
1. Mencegah kontak dengan oksigen dan/atau air
Korosi besi memerlukan oksigen dan air. Bila salah satu tidak ada, maka peristiwa korosi tidak dapat terjadi. Korosi dapat dicegah dengan melapisi besi dengan cat, oli, logam lain yang tahan korosi (logam yang lebih aktif seperti seg dan krom). Penggunaan logam lain yang kurang aktif (timah dan tembaga) sebagai pelapis pada kaleng bertujuan agar kaleng cepat hancur di tanah. Timah atau tembaga bersifat mampercepat proses korosi.
Besi yang dilapisi atau dihubugkan dengan logam lain yang lebih aktif akan membentuk sel elektrokimia dengan besi sebagai katoda. Di sini, besi berfungsi hanya sebagai tempat terjadinya reduksi oksigen. Logam lain berperan sebagai anoda, dan mengalami reaksi oksidasi. Dalam hal ini besi, sebagai katoda, terlindungi oleh logam lain (sebagai anoda, dikorbankan). Besi akan aman terlindungi selama logam pelindungnya masih ada / belum habis. Untuk perlindungan katoda pada sistem jaringan pipa bawah tanah lazim digunakan logam magnesium, Mg. Logam ini secara berkala harus dikontrol dan diganti.
3. Membuat alloy atau paduan logam yang bersifat tahan karat, misalnya besi dicampur dengan logam Ni dan Cr menjadi baja stainless (72% Fe, 19%Cr, 9%Ni). (Supardi, 1997)
2.10 Aplikasi korosi a. Korosi celah
Contoh : Sebuah logam stainless steel di masukkan ke dalam air laut dalam waktu yang cukup lama sehingga pada permukaan logam yang semularata dan bersih tidak ada karat akan menjadi bergelombang pada permukaannyadan berkarat, hal itu mencerminkan bahwa terjadi perbedaan konsentrasi zat asam antara logam dan air laut.
b. Korosi sumuran
Contoh : terjadinya korosi sumuran yaitu pada selembar baja lunak yang bersih di biarkan kehujanan dalam beberapa hari akan terkorosi dengan cepat dan ”karat” yang terbentuk akan berupa endapan keras, tonjolan-tonjolan bundar, pada bagian tertentu di mana titik-titik air menggenang lebih lama. Apabila “karat” kita sikat dengan sikat kawat maka akan terlihat lubang-lubang di tempat yang sama.
Contoh nyata korosi lainnya adalah keroposnya jembatan, body mobil, pintu pagar dari besi atau pun berbagai konstruksi dari besi lainnya yang sangat mudah berkarat. (Supardi, 1997)
PENUTUP
3.1 Kesimpulan
Berdasarkan hasil diskusi kami, maka dapat disimpulkan bahwa
Korosi merupakan proses elektrokimia yang terjadi pada logam, atau proses perusakan material karena bereaksi dengan lingkungannya. Selain itu, korosi juga diartikan sebagai kerusakan yang terjadi pada material akibat adanya reaksi kimia.
Faktor yang mempengaruhi Korosi
1. Kontak Langsung logam dengan H2O dan O2
2. Keberadaan Zat Pengotor 3. Kontak dengan Elektrolit 4. Temperatur.
5. pH 6. Mikroba.
Korosi celah mengacu pada serangan lokal pada permukaan logam pada, atau berbatasan langsung dengan, kesenjangan atau celah antara dua permukaan bergabung.
Korosi sumuran adalah korosi lokal dari permukaan logam yang dibatasi pada satu titik atau area kecil, dan membentukn bentuk rongga. Korosi sumuran adalah salah satu bentuk yang paling merusak dari korosi.
Akibat dan dampak korosi dalam kehidupan
Kerugian yang ditimbulkan oleh korosi diantaranya adalah: 1. Adanya kerugian teknis dan depresiasi
2. menurunnya efisiensi
3. menurunnya kekuatan konstruksi 4. Apperance yang buruk
5. Karat merupakan polusi dan menambah biaya maintenance
Kerugian Akibat Korosi
Kerugian Ekonomi
Pemborosan Sumber Daya Alam
Korosi dapat membahayakan jiwa manusia
Estetika menurun
Pencegahan korosi
Pencegahan korosi didasarkan pada prinsip berikut :
2. Perlindungan katoda (pengorbanan anoda)
3 Membuat alloy atau paduan logam yang bersifat tahan karat, misalnya besi dicampur dengan logam Ni dan Cr menjadi baja stainless (72% Fe, 19%Cr, 9%Ni).
Aplikasi korosi a. Korosi celah
Contoh : Sebuah logam stainless steel di masukkan ke dalam air laut dalam waktu yang cukup
b. Korosi sumuran
Contoh : terjadinya korosi sumuran yaitu pada selembar baja lunak yang bersih di biarkan kehujanan dalam beberapa hari akan terkorosi dengan cepat.
Contoh nyata korosi lainnya adalah keroposnya jembatan, body mobil, pintu pagar dari besi atau pun berbagai konstruksi dari besi lainnya yang sangat mudah berkarat.
DAFTAR PUSTAKA
Anonim.http://m10mechanicalengineering.blogspot.com/2013/11/macam-macam-bentuk-korosi.html (Diakses pada tanggal 20 Mei 2014 pukul 21:10 )
Anonim
.http://material-sciences.blogspot.com/2011/05/korosi-celah-cresive-corrosion.html(Diakses pada tanggal 20 Mei 2014 pukul 21:10 )
Anonim
/http://www.angelfire.com/ak5/process_control/korosi__celah.html(Di
Anonim.(http://fitransyah.wordpress.com/2013/07/25/korosi-celah-dan-korosi-sumuran-sel-sel-konsentrasi/) (Diakses pada tanggal 15 Maret 2014 pukul 15:36 )