Enzim siklooksigenase merupakan enzim yang berperan dalam terjadinya peradangan yang merupakan gejala dari beberapa penyakit. Penemuan pengembangan senyawa obat yang dapat menghambat enzim siklooksigenase dapat digunakan untuk mengatasi nyeri, peradangan, rheumatoid arthritis dan osteoarthritis serta termasuk dalam kelompok obat anti inflamasi non steroid (OAINS). Perkembangan senyawa NSAID terus berkembang, terutama senyawa obat yang secara selektif hanya menghambat enzim siklooksigenase 2 (COX-2) untuk menghindari efek samping obat.
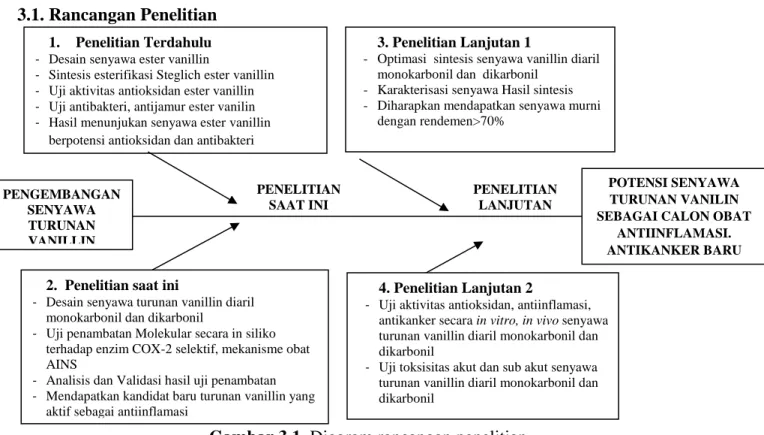
Penelitian dimulai dengan merancang senyawa monokarbonil dan dikarbonil vanillin kemudian dilakukan docking molekuler menggunakan software PLANTS 1.2 dengan parameter keluaran ChemPLP. Hasil yang diperoleh dengan melihat skor chemPLP yang lebih rendah, interaksi ikatan hidrogen, interaksi sterik, sifat hidrofobik dan interaksi elektrostatik, ligan B5 menunjukkan interaksi ligan (senyawa pengembang) yang lebih stabil dengan makromolekul (enzim COX-2) dibandingkan dengan Celecoxib.
PENDAHULUAN
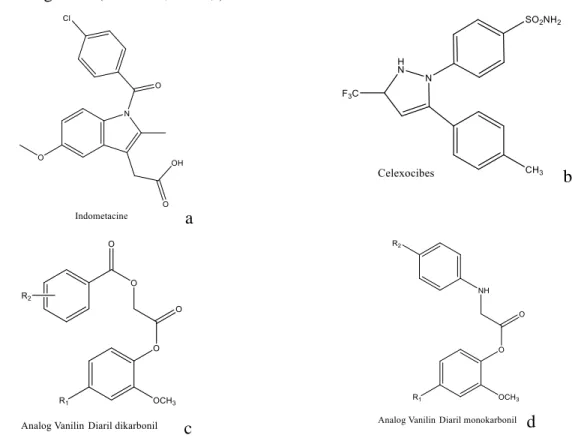
Mekanisme kerja kurkumin sebagai anti inflamasi adalah dengan menghambat produksi prostaglandin yang dapat dimediasi dengan menghambat aktivitas enzim siklooksigenase (Yu et al., 2015; Beberapa struktur senyawa inhibitor selektif COX-2 merupakan turunan dari senyawa kurkumin, yaitu analog monokarbonil dari kurkumin, yang mirip dengan turunan monokarbonil dari vanilin. bertindak sebagai inhibitor COX-2, oleh karena itu, dalam penelitian ini, senyawa-senyawa ini diuji secara praktis menggunakan metode penambatan molekuler.
Untuk mendapatkan kandidat senyawa turunan vanilin diaril-karbonil (DVK) yang baru dan mengetahui mekanisme kerja senyawa ini dalam penghambatan selektif enzim siklooksigenase-2 (COX-2) yang lebih baik. Penelitian dan pengembangan obat NSAID telah dilakukan selama lebih dari satu abad, namun hingga saat ini obat NSAID yang ideal belum ditemukan. NSAID klasik sering menyebabkan efek yang tidak diinginkan seperti pendarahan lambung dan kerusakan ginjal.
Kelas obat NSAID baru dari inhibitor COX-2 selektif ("coxib") memiliki toksisitas gastrointestinal dan ginjal yang lebih rendah, tetapi selektivitas yang berlebihan dapat meningkatkan risiko kejadian kardiovaskular (Segev & Katz, 2004; Coruzzi, Venturi & Spaggiari, 2007; Funk & FitzGerald, 2007). Keadaan di atas menunjukkan bahwa masih sangat diperlukan penemuan NSAID atau inhibitor COX-2 baru yang memiliki efek terapeutik dan tolerabilitas yang lebih baik.
TINJAUAN PUSTAKA
Situs aktif COX, yang melakukan reaksi pertama dalam sintesis PG, tertutup dalam kantong yang terkubur di dalam protein, yang dapat diakses melalui saluran berbentuk corong terbuka yang mengarahkan asam arakidonat keluar dari membran dan masuk ke situs aktif enzim. Situs aktif peroksidase pada permukaan atas enzim, yang mengubah peroksida dalam molekul PGG2 menjadi gugus hidroksi, menggunakan gugus heme untuk memulai reaksi kimia (Goodsell, 2001; Blobaum dan Marnett, 2007). Situs aktif COX adalah saluran yang diikat oleh residu hidrofobik dan diproyeksikan ke pusat domain globular utama enzim.
Awalnya, baik alkil peroksida maupun peroksinitrit, yang berasal dari kondensasi nitrat oksida (NO) dan superoksida, mengoksidasi gugus heme di situs aktif peroksidase. Molecular docking adalah teknik yang digunakan untuk mempelajari interaksi yang terjadi dari suatu molekul kompleks. Informasi tentang orientasi ini dapat digunakan untuk memprediksi kekuatan ikatan atau afinitas pengikatan antara dua molekul menggunakan mis. fungsi penilaian.
Docking sering digunakan untuk memprediksi orientasi pengikatan kandidat obat molekul kecil ke target proteinnya untuk memprediksi afinitas dan aktivitas molekul kecil. Keuntungan dari metode pemodelan molekul dengan docking molekul adalah dapat digunakan untuk memprediksi aktivitas suatu senyawa sebelum sintesis, sehingga mengurangi penggunaan pelarut dan bahan kimia yang dapat mencemari lingkungan. Dalam penambatan protein-ligan, koloni semut buatan digunakan untuk menemukan konformasi energi minimum ligan di tempat pengikatan.
Semut ini digunakan untuk meniru perilaku semut asli dan menandai ligan konformasi berenergi rendah dengan jejak feromon. PLP digunakan untuk memodelkan komplementaritas sterik antara ligan dan protein, sedangkan CHEMPLP memiliki penambahan sudut dan jarak ikatan hidrogen. Meskipun kekuatan ikatan hidrogen tidak sebesar ikatan kovalen, namun keberadaannya dalam suatu molekul dapat memberikan kontribusi pada struktur dan karakteristik molekul tersebut.
Selain mempengaruhi sifat suatu senyawa, misalnya dalam meningkatkan titik didih, titik lebur, kelarutan dan viskositas, ikatan hidrogen penting dalam bidang farmasi dan kedokteran, terutama dalam mempelajari rancangan dan interaksi molekuler antara obat dan sistem metabolisme tubuh. Bahkan secara alami, ikatan hidrogen secara aktif terlibat dalam menghubungkan asam amino yang membentuk protein dan basa yang membentuk DNA. Selain itu, ikatan hidrogen dalam suatu senyawa juga dapat mempengaruhi struktur molekul dalam fasa padat, baik senyawa organik maupun anorganik, yang selanjutnya juga mempengaruhi sistem kristal, parameter sel dan sifat keseluruhan senyawa tersebut.
Dalam konteks sintesis dan desain arsitektur senyawa supramolekul dan polimer koordinasi, ikatan hidrogen merupakan salah satu faktor utama karena kekuatannya (dibandingkan dengan interaksi non-kovalen lainnya) dan kemampuan pengarahan yang baik. Ikatan hidrogen memiliki kemampuan untuk menghubungkan satu molekul senyawa koordinasi dengan molekul lainnya sehingga dapat membentuk struktur yang lebih kompleks (Jeffrey, 1997).
![Gambar 2.1. Representasi struktural dimer murine PGHS (COX-2) [Kurumbail et al., 1996]](https://thumb-ap.123doks.com/thumbv2/123dok/9989763.0/13.918.365.587.107.306/gambar-representasi-struktural-dimer-murine-pghs-cox-kurumbail.webp)
METODE PENELITIAN
Pemisahan makromolekul dari molekul yang tidak diperlukan dilakukan dengan menggunakan program YASARA (edit > hapus > residu). Buang airnya (Edit > Hapus > Air) dan tambahkan hidrogen ke struktur (Edit > Tambahkan > .hidrogen ke semua). Protonasi dimodifikasi pada pH 7,4 menggunakan Marvin Sketch (Calculation > Protonation > .Major Microspecies), data yang diperoleh disimpan dalam format .mrv.
Buka file yang disimpan dalam format .mrv dan lakukan pencarian konformasi dengan software yang sama, lalu simpan dalam format .mol2 (Calculation > Conformation > Conformer). Validasi menggunakan program YASARA (Analyze > RMSD > Molekul) dengan memasukkan ligan dan reseptor spesifik pada format.mol2. Kemudian pindahkan semua data dan aplikasi PLANTS ke desktop Buka terminal di linux, masukkan root (sudo -s).
Ketik perintah “cp /home/desktop/PLANTS1.2 PLANTS” lalu ketikkan perintah “chmod u+x PLANTS” untuk mengaktifkan aplikasi PLANTS. Download hasil preparat ligan dan reseptor dalam format .mol2 ke root dengan perintah “cp /home/desktop/*.mol2. Pada langkah selanjutnya, Anda dapat menemukan situs pengikatan dengan perintah "./PLANTS --mode bind ref_ligand.mol2 5 protein.mol2".
Untuk mengetahui apakah setting PLANTS sudah benar, anda bisa melihat dengan perintah "kwrite plantsconfig". Setelah pengaturan sudah benar, masukkan perintah "./PLANTS --mode screen plantsconfig" dan tunggu proses koneksi selesai. Konformasi kompleks merapat ditentukan dengan memilih konformasi yang memiliki energi ikat terendah. Hasil docking divisualisasikan menggunakan software Molegro Molecular Viewer 2.5 untuk melihat interaksi dengan residu asam amino dan jarak ikatan hidrogen, interaksi sterik, sifat hidrofobisitas, dan interaksi elektrostatik.
HASIL DAN PEMBAHASAN
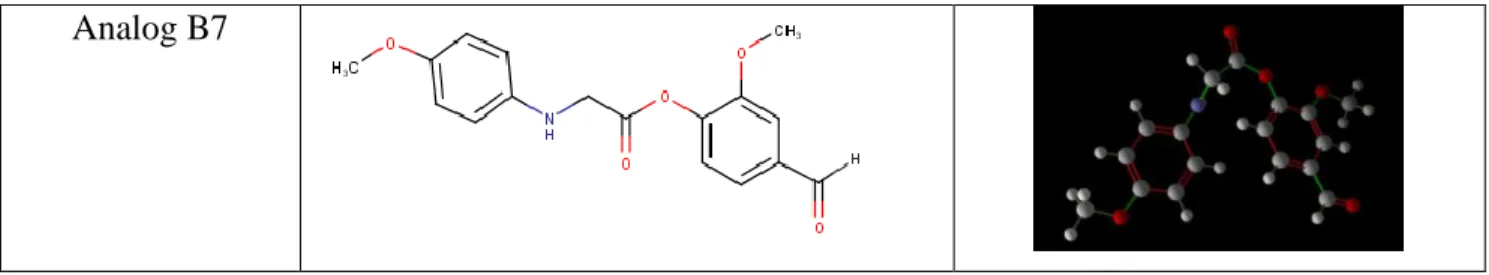
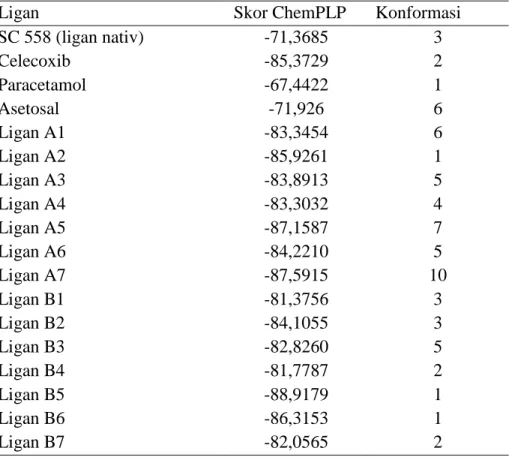
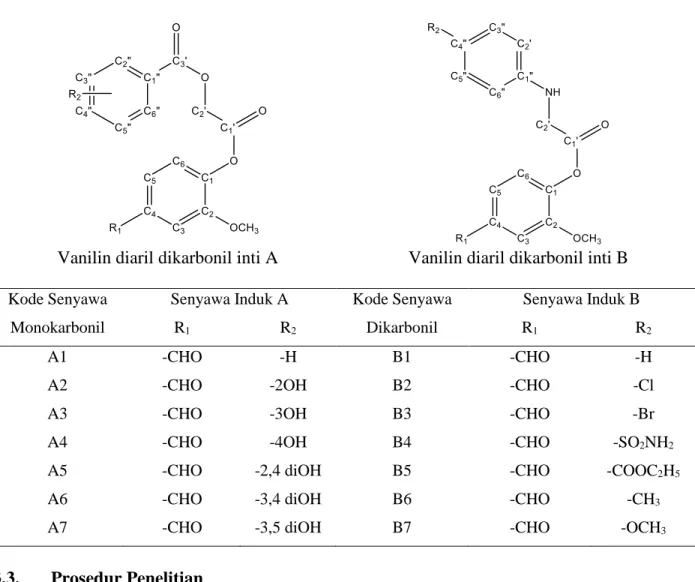
Hasil pengikatan 14 ligan uji turunan karbonil diaril vanilin dan senyawa pembanding menunjukkan bahwa ligan A2, A5, A7, B5 dan B6 memiliki skor ChemPLP yang lebih rendah dibandingkan dengan ligan pembanding (Tabel 3). Tidak seperti ligan B5, ia memiliki skor ChemPLP terendah dibandingkan dengan pembanding dan ligan uji lainnya yang relatif lebih tinggi. Sehingga ligan B5 memiliki interaksi yang paling stabil dan memiliki kemampuan inhibisi enzim COX-2 yang paling baik dibandingkan dengan ligan lainnya.
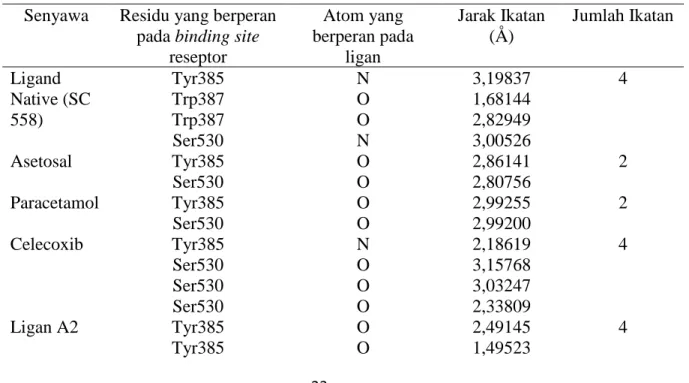
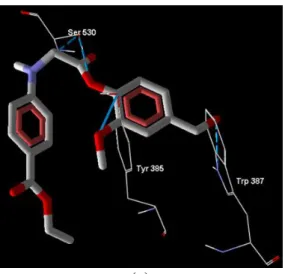
Interaksi dengan residu asam amino pada tempat pengikatan ligan berperan penting dalam penghambatan enzim COX-2. Residu asam amino yang berperan dalam binding site enzim COX-2 adalah Serine530 dan Tyrosine385 yaitu. Hasil visualisasi pada ligan B5 yang memiliki skor ChemPLP terendah menunjukkan bahwa ligan B5 memiliki ikatan hidrogen yang paling stabil dan memiliki kemampuan terbaik untuk menghambat enzim COX-2 (Gambar 4).
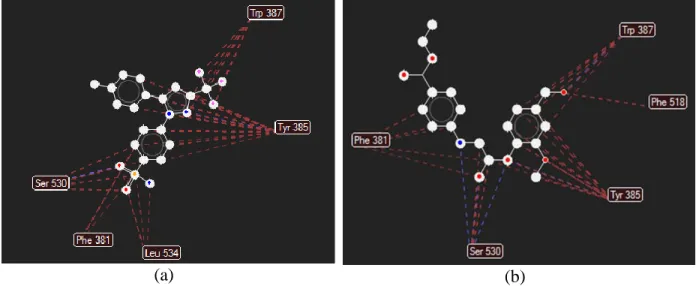
Keenam ikatan hidrogen yang terbentuk dengan residu asam amino Serin530, Tyrosine385 dan Tryptophan387 pada ligan B5 terdiri dari 2 atom, yaitu nitrogen pada gugus amida dan oksigen pada gugus aldehida dan karbonil (Tabel 4). Gugus aldehida dapat berperan sebagai akseptor ikatan hidrogen karena aldehida bersifat reaktif secara kimiawi dan mudah teroksidasi menjadi asam karboksilat (Patrick, 2001). Interaksi ikatan hidrogen ini lebih unggul dibandingkan ligan pembanding celecoxib dan ligan native SC-558 yang hanya dapat membentuk empat ikatan hidrogen pada residu tempat pengikatan asam amino COX-2, yaitu residu asam amino Serin530 dan Tyrosine385 dengan celecoxib dan Serin530, Tyrosine385 dan Tryptophan387 dengan SC-558 (Gambar 3).
Semakin banyak interaksi ikatan hidrogen pada ligan B5 berkontribusi terhadap stabilitas ikatan ligan. Selain itu, jarak pengikatan mempengaruhi stabilitas interaksi antara ligan B5 dengan reseptor 6COX yang rendah di bawah 3,5 Å, sehingga afinitas pengikatan juga semakin ditingkatkan. Selain interaksi ikatan hidrogen yang berperan dalam interaksi obat-reseptor, terdapat interaksi sterik, hidrofobisitas, dan interaksi elektrostatik.
Berdasarkan interaksi sterik pada Gambar 5, celecoxib dan ligan B5 memiliki interaksi sterik yang besar dengan residu situs pengikatan Ser530 dan Tyr385. Interaksi ikatan hidrogen (----) dan interaksi sterik (----) antara ligan dan residu asam amino. Titik putih adalah titik merah non-polar. Gambar 6 menunjukkan hidrofobisitas permukaan residu asam amino, dimana warna biru pada permukaan menunjukkan bahwa residu bersifat hidrofobik sedangkan warna merah menunjukkan bahwa residu bersifat hidrofilik.
Berdasarkan penentuan skor ChemPLP hasil docking, ikatan hidrogen, interaksi sterik, hidrofobisitas dan sifat elektrostatik dibandingkan dengan inhibitor COX-2 yaitu celecoxib, dapat disimpulkan bahwa ligan diarilkarbonil B5 turunan vanilin merupakan ligan terbaik untuk reseptor enzim COX-2. Senyawa ligan B5 memiliki potensi antiinflamasi terbaik terhadap reseptor enzim COX-2 sehingga dapat disintesis dan uji antiinflamasi in vitro dan in vivo dapat dilakukan.
KESIMPULAN DAN SARAN