KARAKTERISASI SIMPLISIA
DAN SKRINING FITOKIMIA SERTA ISOLASI
STEROID/TRITERPENOID DARI EKSTRAK
ETANOL PUCUK LABU SIAM
(Sechium edule (Jacq.) Sw.)
SKRIPSI
OLEH:
TARZIAH
NIM 101524036
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KARAKTERISASI SIMPLISIA
DAN SKRINING FITOKIMIA SERTA ISOLASI
STEROID/TRITERPENOID DARI EKSTRAK
ETANOL PUCUK LABU SIAM
(Sechium edule (Jacq.) Sw.)
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
TARZIAH
NIM 101524036
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
KARAKTERISASI SIMPLISIA
DAN SKRINING FITOKIMIA SERTA ISOLASI
STEROID/TRITERPENOID DARI EKSTRAK
ETANOL PUCUK LABU SIAM
(Sechium edule (Jacq.) Sw.)
OLEH: TARZIAH NIM 101524036
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: Juli 2012
Pembimbing I, Panitia Penguji,
Dra. Herawaty Ginting, M.Si., Apt. Dr. Marline Nainggolan, M.S., Apt. NIP 195112231980032002 NIP 195709091985112001
Pembimbing II, Dra. Herawaty Ginting, M.Si., Apt. NIP 195112231980032002
Dr. M. Pandapotan Nasution, MPS., Apt. Drs. Panal Sitorus, M.Si., Apt. NIP 194908111976031001 NIP 195310301980031002
Dra. Aswita Hafni Lubis, M.Si., Apt. NIP 195304031983032001
Medan, Juli 2012 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji dan syukur kehadirat Allah SWT, karena limpahan rahmat dan karuniaNya, sehingga penulis dapat menyelesaikan penelitian dan penulisan skripsi yang berjudul ”Karakterisasi Simplisia dan Skrining Fitokimia serta Isolasi Steroid/Triterpenoid dari Ekstrak Etanol Pucuk Labu Siam (Sechium edule (Jacq.) Sw.)”, yang merupakan salah satu syarat memperoleh gelar sarjana Farmasi di Fakultas Farmasi Universitas Sumatra Utara
Penulis juga ingin mempersembahan terimakasih yang tak terhingga dan rasa cinta yang mendalam kepada kedua orangtua, ayahanda Armoza dan ibunda Syamsiar, untuk nasehat dan motivasinya dalam menyelesaikan pendidikan ini.
Penulis menyadari bahwa skripsi ini masih banyak kekurangannya, oleh karena itu sangat diharapkan kritik dan saran yang bersifat membangun dari semua pihak guna perbaikan skripsi ini. Akhir kata penulis berharap semoga skripsi ini bermanfaat bagi ilmu pengetahuan khususnya bidang Farmasi.
Medan, Juli 2012 Penulis,
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA SERTA ISOLASI STEROID/TRITERPENOID DARI EKSTRAK ETANOL
PUCUK LABU SIAM (Sechium edule (Jacq.) Sw.)
ABSTRAK
Salah satu suku Cucurbitaceae yaitu labu siam (Sechium edule (Jacq.) Sw.), dapat digunakan untuk mengobati penyakit batu ginjal, arteriosklerosis dan tekanan darah tinggi. Labu siam mengandung saponin, flavonoid, polifenol, dan steroid/triterpenoid. Karakterisasi simplisia serta kandungan senyawa kimia yang terkandung dalam pucuk labu siam belum tercantum di buku Materia Medika Indonesia. Tujuan penelitian ini adalah untuk mengetahui karakterisasi simplisia, skrining fitokimia untuk senyawa yang terkandung di dalam pucuk labu siam dan mengisolasi senyawa steroid/triterpenoid.
Penelitian ini meliputi karakterisasi simplisia, skrining fitokimia, ekstraksi dilakukan secara maserasi dengan etanol, kemudian ekstrak yang diperoleh dilakukan ekstraksi cair-cair dengan n-heksan dan kromatografi cair vakum (KCV), isolasi dengan kromatografi kolom (KK) dan dikromatografi lapis tipis (KLT), isolasi triterpenoid dilakukan dengan menggunakan kromatografi lapis tipis (KLT) preparatif, uji kemurnian dengan kromatografi lapis tipis (KLT) dua arah dan isolat yang diperoleh dikarakterisasi secara spektrofotometri ultraviolet (UV) dan spektrofotometri inframerah (IR).
Hasil karakterisasi simplisia pucuk labu siam meliputi kadar air 3,99%, kadar sari yang larut air 33,45%, kadar sari yang larut dalam etanol 9,96%, kadar abu total 4,13% dan kadar abu tidak larut asam 0,96%. Hasil skrining fitokimia pucuk daun labu siam mengandung flavonoid, steroid/triterpenoid, tanin, glikosida, dan saponin. Hasil analisis isolat menunjukkan bahwa isolat yang diperoleh adalah senyawa golongan steroid/triterpenoid dengan harga Rf 0,35 dengan penampak bercak Liebermann-Burchard berwarna merah ungu dan isolat yang diperoleh dianalisis secara spektrofotometri UV memberikan absorbansi maksimum pada panjang gelombang (λ) 207,5 nm menunjukkan adanya gugus kromofor dan hasil spektrofotometri IR diketahui adanya gugus –OH, C-H alifatis, C=O, C=C, -CH2, –CH3 dan C-O.
SIMPLEX CHARACTERIZATION AND PHYTOCHEMICAL
SCREENING AND ISOLATION OF STEROID/TRITERPENOID
n-HEXANE FRACTION ETHANOL EXTRACT OF CHAYOTE SHOOTS
(Sechium edule (Jacq.) Sw.)
ABSTRACT
One of the Cucurbitaceou plans is chayote (Sechium edule (Jacq.) Sw.). used to treat kidney stone disease, arteriosclerosis and high blood pressure that contains saponin, flavonoid, polyphenol, and steroid/triterpenoid. Simplex characterization and chemical content contained in chayote shoots are not listed in the book Materia Medika Indonesia. The purpose of this study was to determine the simplex characterization, phytochemical screening for compounds that contained in chayote shoots and isolating the compound of steroid/triterpenoid.
This research included the simplex characterization, phytochemical screening, extraction accomplished by maceration with ethanol, the extract with liquid extraction, isolated with Vacuum Liquid Chromatography, isolated with Coloumn Chromatography and the fraction with Thin Layer Chromatography , the steroidal isolation was accomplished by using the preparative Thin Layer Chromatography, the purity test by two-dimensional Thin Layer Chromatography, and the resulting isolate was identified by ultraviolet spectrophotometry and infrared spectophotometry.
The result of simplex characterization included the water content 3.99%, water-soluble extract content 33.45%, ethanol-soluble extract content 9.96%, total ash content 4.13%, acid-insoluble ash content 0.96%. The result of phytochemical screening of chayote shoots contain flavonoid, steroid/triterpenoid, tannin, glikosida, and saponin. The result of isolate analysis indicated that the isolate was steroid/triterpenoid Rf 0.35 red purple with Liebermann-Burchard reagent, and the resulting isolat was then analyzed by UV spectrophotometry that have maximum absorbtion at wavelength 207.5 nm to indicate the presence of chromophor and the result of IR spectrophotometry indicated the presence of –OH and C-H , C=O, C=C, CH2, CH3, C-O functional groups.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
LEMBAR PENGESAHAN SKRIPSI ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... xiv
DAFTAR LAMPIRAN ... xv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 2
1.3 Hipotesis ... 3
1.4 Tujuan ... 3
1.5 Manfaat ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Tumbuhan ... 5
2.1.1 Daerah tumbuh ... 5
2.1.2 Nama daerah ... 5
2.1.3 Nama asing ... 6
2.1.5 Morfologi tumbuhan ... 6
2.1.6 Kandungan kimia ... 7
2.1.7 Kegunaan labu siam ... 7
2.2 Uraian Kandungan Kimia Tumbuhan ... 10
2.2.1 Alkaloida ... 10
2.2.2 Flavonoida ... 11
2.2.3 Saponin ... 11
2.2.4 Tanin ... 12
2.2.5 Glikosida ... 13
2.2.6 Glikosida antrakuinon ... 13
2.2.7 Steroid/Triterpenoid ... 14
2.3 Metode Ekstraksi ... 15
2.4 Kromatografi ... 17
2.4.1 Kromatografi lapis tipis ... 17
2.4.2 Kromatografi cair vakum ... 20
2.4.3 Kromatografi kolom ... 21
2.4.4 Kromatografi lapis tipis preparatif ... 21
2.4.5 Kromatografi lapis tipis dua arah ... 22
2.5 Spektrofotometri ... 23
2.5.1 Spektrofotometri sinar ultraviolet ... 23
2.5.2 Spektrofotometri sinar inframerah ... 23
BAB III METODE PENELITIAN ... 25
3.1 Alat-alat ... 25
3.3 Pembuatan Pereaksi ... 26
3.3.1 Pereaksi Bouchardat ... 26
3.3.2 Pereaksi Mayer ... 26
3.3.3 Pereaksi Dragendorff ... 26
3.3.4 Pereaksi Molish ... 27
3.3.5 Larutan Asam Klorida 2 N ... 27
3.3.6. Larutan Asam Sulfat 2 N ... 27
3.3.7 Larutan Asam Nitrat 0,5 N ... 27
3.3.8 Larutan Timbal (II) Asetat 0,4 M ... 27
3.3.9 Larutan Besi (III) Klorida 1% b/v ... 27
3.3.10 Larutan Pereaksi Kloralhidrat ... 27
3.3.11 Larutan Pereaksi Lieberman-Burchard ... 27
3.3.12 Larutan Floroglusin HCl ... 28
3.4 Pengumpulan Bahan Tumbuhan, Identifikasi Tumbuhan Dan Pembuatan Simplisia ... 28
3.4.1 Pengumpulan bahan tumbuhan ... 28
3.4.2 Identifikasi tumbuhan ... 28
3.4.3 Pembuatan simplisia ... 28
3.5 Pemeriksaan Karakteristik Simplisia ... 29
3.5.1 Pemeriksaan makroskopik... 29
3.5.2 Pemeriksaan mikroskopik ... 29
3.5.3 Penetapan kadar air ... 29
3.5.4 Penetapan kadar sari yang larut dalam air ... 30
3.5.5 Penetapan kadar sari yang larut dalam etanol ... 31
3.5.7 Penetapan kadar abu yang tidak larut dalam asam ... 31
3.6 Skrining Fitokimia ... 32
3.6.1 Pemeriksaan alkaloida ... 32
3.6.2 Pemeriksaan flavonoid ... 32
3.6.3 Pemeriksaan tanin ... 32
3.6.4 Pemeriksaan glikosida ... 33
3.6.5 Pemeriksaan saponin ... 33
3.6.6 Pemeriksaan steroida/triterpenoida ... 33
3.6.7 Pemeriksaan glikosida antrakuinon ... 34
3.7 Pembuatan Ekstrak Etanol Dan Ekstraksi Cair-Cair Ekstrak Etanol ... 34
3.7.1 Pembuatan ekstrak etanol ... 34
3.7.2 Ekstraksi cair-cair ekstrak etanol ... 35
3.8 Analisis Fraksi n-Heksan Secara KLT ... 35
3.9 Pemisahan Ekstrak n-Heksan Dengan KCV ... 36
3.10 Pemisahan Ekstrak n-Heksan Dengan Kromatografi Kolom .. 37
3.11 Isolasi Senyawa Steroid/Triterpenoid Hasil Kromatografi Kolom ... 38
3.12 Uji Kemurnian Terhadap Kristal Hasil Isolasi ... 39
3.13 Karakterisasi Isolat ... 39
3.13.1 Karakterisasi isolat dengan spektrofotometri UV ... 39
3.13.2 Karakterisasi isolat dengan spektrofotometri IR ... 40
BAB IV HASIL DAN PEMBAHASAN ... 41
4.1 Hasil Identifikasi Sampel ... 41
4.3 Hasil Skrining Fitokimia ... 43
4.4 Hasil Ekstraksi Dan Fraksinasi Cair-Cair Senyawa Aktif Dari Ekstrak Etanol Dan Isolasi Senyawa Aktif ... 45
BAB V KESIMPULAN DAN SARAN ... 48
5.1 Kesimpulan ... 48
5.2 Saran ... 48
DAFTAR PUSTAKA ... 49
DAFTAR TABEL
Tabel Halaman
2.1 Komposisi gizi per 100 gram labu siam ... 9
4.1 Hasil karakteristik simplisia dari pucuk labu siam ... 42
4.2 Hasil skrining fitokimia dari simplisia pucuk labu siam ... 44
DAFTAR GAMBAR
DAFTAR LAMPIRAN
Lampiran Halaman
1. Identifikasi tumbuhan ... 52
2. Bagan kerja penelitian ... 53
3. Bagian makroskopik tumbuhan dari pucuk labu siam (Sechium edule (Jacq.) Sw. ... 54
4. Bagian mikroskopik dari pucuk labu siam (Sechium edule (Jacq.) Sw. ... 56
5. Bagan skrining fitokimia dan karakterisasi serbuk simplisia ... 59
6. Bagan pembuatan ekstrak etanol pucuk labu siam (Sechium edule (Jacq.) Sw.) ... 60
7. Bagan ekstraksi cair-cair ekstrak etanol ... 61
8. Isolasi steroid/triterpenoid dari fraksi n-heksan pucuk labu siam (Sechium edule (Jacq.) Sw.) ... 62
9. Kromatogram dan harga Rf dari fraksi n-heksan pucuk labu siam (Sechium edule (Jacq.) Sw.) ... 64
10. Kromatogram cair vakum I ... 65
11. Kromatogram cair vakum II ... 66
12. Kromatogram kolom ... 67
13. KLT preparatif ... 68
14. KLT dua arah dan harga Rf ... 69
15. Panjang gelombang isolat pucuk labu siam (Sechium edule (Jacq.) Sw.) ... 70
16. Spektrum isolat ... 71
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA SERTA ISOLASI STEROID/TRITERPENOID DARI EKSTRAK ETANOL
PUCUK LABU SIAM (Sechium edule (Jacq.) Sw.)
ABSTRAK
Salah satu suku Cucurbitaceae yaitu labu siam (Sechium edule (Jacq.) Sw.), dapat digunakan untuk mengobati penyakit batu ginjal, arteriosklerosis dan tekanan darah tinggi. Labu siam mengandung saponin, flavonoid, polifenol, dan steroid/triterpenoid. Karakterisasi simplisia serta kandungan senyawa kimia yang terkandung dalam pucuk labu siam belum tercantum di buku Materia Medika Indonesia. Tujuan penelitian ini adalah untuk mengetahui karakterisasi simplisia, skrining fitokimia untuk senyawa yang terkandung di dalam pucuk labu siam dan mengisolasi senyawa steroid/triterpenoid.
Penelitian ini meliputi karakterisasi simplisia, skrining fitokimia, ekstraksi dilakukan secara maserasi dengan etanol, kemudian ekstrak yang diperoleh dilakukan ekstraksi cair-cair dengan n-heksan dan kromatografi cair vakum (KCV), isolasi dengan kromatografi kolom (KK) dan dikromatografi lapis tipis (KLT), isolasi triterpenoid dilakukan dengan menggunakan kromatografi lapis tipis (KLT) preparatif, uji kemurnian dengan kromatografi lapis tipis (KLT) dua arah dan isolat yang diperoleh dikarakterisasi secara spektrofotometri ultraviolet (UV) dan spektrofotometri inframerah (IR).
Hasil karakterisasi simplisia pucuk labu siam meliputi kadar air 3,99%, kadar sari yang larut air 33,45%, kadar sari yang larut dalam etanol 9,96%, kadar abu total 4,13% dan kadar abu tidak larut asam 0,96%. Hasil skrining fitokimia pucuk daun labu siam mengandung flavonoid, steroid/triterpenoid, tanin, glikosida, dan saponin. Hasil analisis isolat menunjukkan bahwa isolat yang diperoleh adalah senyawa golongan steroid/triterpenoid dengan harga Rf 0,35 dengan penampak bercak Liebermann-Burchard berwarna merah ungu dan isolat yang diperoleh dianalisis secara spektrofotometri UV memberikan absorbansi maksimum pada panjang gelombang (λ) 207,5 nm menunjukkan adanya gugus kromofor dan hasil spektrofotometri IR diketahui adanya gugus –OH, C-H alifatis, C=O, C=C, -CH2, –CH3 dan C-O.
SIMPLEX CHARACTERIZATION AND PHYTOCHEMICAL
SCREENING AND ISOLATION OF STEROID/TRITERPENOID
n-HEXANE FRACTION ETHANOL EXTRACT OF CHAYOTE SHOOTS
(Sechium edule (Jacq.) Sw.)
ABSTRACT
One of the Cucurbitaceou plans is chayote (Sechium edule (Jacq.) Sw.). used to treat kidney stone disease, arteriosclerosis and high blood pressure that contains saponin, flavonoid, polyphenol, and steroid/triterpenoid. Simplex characterization and chemical content contained in chayote shoots are not listed in the book Materia Medika Indonesia. The purpose of this study was to determine the simplex characterization, phytochemical screening for compounds that contained in chayote shoots and isolating the compound of steroid/triterpenoid.
This research included the simplex characterization, phytochemical screening, extraction accomplished by maceration with ethanol, the extract with liquid extraction, isolated with Vacuum Liquid Chromatography, isolated with Coloumn Chromatography and the fraction with Thin Layer Chromatography , the steroidal isolation was accomplished by using the preparative Thin Layer Chromatography, the purity test by two-dimensional Thin Layer Chromatography, and the resulting isolate was identified by ultraviolet spectrophotometry and infrared spectophotometry.
The result of simplex characterization included the water content 3.99%, water-soluble extract content 33.45%, ethanol-soluble extract content 9.96%, total ash content 4.13%, acid-insoluble ash content 0.96%. The result of phytochemical screening of chayote shoots contain flavonoid, steroid/triterpenoid, tannin, glikosida, and saponin. The result of isolate analysis indicated that the isolate was steroid/triterpenoid Rf 0.35 red purple with Liebermann-Burchard reagent, and the resulting isolat was then analyzed by UV spectrophotometry that have maximum absorbtion at wavelength 207.5 nm to indicate the presence of chromophor and the result of IR spectrophotometry indicated the presence of –OH and C-H , C=O, C=C, CH2, CH3, C-O functional groups.
BAB I
PENDAHULUAN
1.1Latar Belakang
Obat tradisional adalah bahan atau ramuan bahan yang berupa tumbuhan, hewan, mineral, sediaan galenik, atau campuran dari bahan tersebut yang secara turun temurun telah digunakan untuk pengobatan berdasarkan pengalaman. Sejalan dengan tren back to nature yang berkembang pada masyarakat saat ini, penggunaan berbagai tumbuhan serta bahan alam lainnya sebagai obat terus berkembang semakin besar, baik untuk pengobatan suatu penyakit maupun pemeliharaan kesehatan (Wasito, 2011).
Suku Cucurbitaceae merupakan salah satu kelompok tanaman yang banyak terdapat di Indonesia. Suku ini mencakup lebih dari 750 jenis yang terbagi dalam 100 marga dan mempunyai potensi sebagai obat beberapa penyakit, mengandung beberapa senyawa seperti saponin yang berguna sebagai antitumor pada paru-paru dan rahim, senyawa β-sitosterol sebagai antioksidan dan mencegah kanker payudara serta senyawa spinasterol dan stigmasterol berguna sebagai pencegah radang tenggorokan dan obat pereda nyeri (Marliana, 2005).
ular, gangguan kulit, kerusakan hati dan malaria (Robinson, 1995). Pucuk, batang dan buah labu siam (Sechium edule (Jacq.) Sw.) yang dibudidayakan relatif rendah serat, protein dan vitamin, namun demikian memiliki kandungan karbohidrat yang tinggi (Supriatno dan Sulaiman, 2011).
Menurut literatur bahwa senyawa metabolit sekunder yang terdapat dalam tumbuhan biasanya tersebar merata keseluruh bagian tumbuhan tetapi dalam kadar yang berbeda-beda (Markham, 1988). Uji pendahuluan metabolit sekunder pada pucuk labu siam ditemukan senyawa triterpenoid/steroid serta didukung oleh hasil penelitian dalam ekstrak n-heksan telah ditemukan senyawa golongan triterpenoid/steroid yang aktif sebagai antiradikal bebas dengan nilai IC50 sebesar 156,14 µg/ml (Pratiwi, 2011). Karakteristik simplisia serta golongan senyawa kimia yang terkandung dalam pucuk labu siam belum tercantum di buku Materia Medika Indonesia.
Berdasarkan alasan di atas penulis tertarik untuk melakukan penelitian tentang karakterisasi simplisia dan skrining fitokimia serta isolasi triterpenoid/steroid dari ekstrak etanol pucuk labu siam (Sechium edule (Jacq.) Sw.).
1.2 Perumusan Masalah
a. Apakah golongan senyawa kimia dari simplisia pucuk labu siam (Sechii
edulei herba) dapat ditentukan.
c. Apakah senyawa steroid/triterpenoid yang diperoleh dari fraksi n-heksan pucuk labu siam (Sechium edule (Jacq.) Sw.) dapat diisolasi dan dikarakterisasi.
1.3Hipotesis
a. Golongan senyawa kimia dari serbuk simplisia pucuk labu siam (Sechii
edulei herba) dapat ditentukan dengan menggunakan prosedur skrining
fitokimia pada Materia Medika Indonesia dan Farnsworth.
b. Karakteristik simplisia pucuk labu siam (Sechii edulei herba) dapat ditentukan dengan menggunakan prosedur karakterisasi simplisia pada Materia Medika Indonesia dan World Health Organization (WHO).
c. Senyawa steroid/triterpenoid dapat diisolasi dari fraksi n-heksan pucuk labu siam (Sechium edule (Jacq.) Sw) yang diperoleh, dapat dikarakterisasi dengan spektrofotometri ultraviolet (UV) dan spektrofotometri infrared (IR).
1.4Tujuan
a. Untuk mengetahui golongan senyawa kimia dari simplisia pucuk labu siam (Sechii adulei herba).
b. Untuk mengetahui karakteristik simplisia pucuk labu siam (Shecii edulei herba) yang diteliti.
1.5Manfaat
a. Mengetahui golongan senyawa kimia dari pucuk labu siam (Sechium edule (Jacq.) Sw.).
b. Mengetahui karakteristik pucuk labu siam (Sechium edule (Jacq.) Sw.). c. Mengetahui karakteristik senyawa steroid/triterpenoid yang terdapat dalam
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi daerah tumbuh (habitat), nama daerah, nama asing, sistematika tumbuhan, morfologi tumbuhan, kandungan kimia dan kegunaan dari tumbuhan.
2.1.1 Daerah tumbuh
Labu siam merupakan tumbuhan yang mudah ditemukan di hutan-hutan jati, hutan campuran, tepi-tepi jalan, atau sawah dan kebun. Tanaman ini dapat tumbuh pada ketinggian 50 meter sampai 500 meter di atas permukaan laut (Prahasta, 2009).
2.1.2 Nama daerah
Tanaman labu siam memiliki nama daerah sebagai berikut (Prahasta, 2009): Sumatera : Labu siam (Melayu)
Aceh : Labu jipang
Karo : Ropah
Jawa (Sunda) : Gambas, waluh siam
Jawa Tengah : Waluh jipang, labu jipang Jawa Timur : Manisah
2.1.3 Nama asing
Sayuran ini dikenal dengan nama asing chayote (Prahasta, 2009).
2.1.4 Sistematika tumbuhan
Tumbuhan labu siam (Sechium edule (Jacq.) Sw.) diklasifikasikan sebagai berikut (Prahasta, 2009).
Kerajaan : Plantae
Divisio : Spermatophyta Subdivisio : Angiospermae Kelas : Dicotyledonae Bangsa : Cucurbitales Suku : Cucurbitaceae Marga : Sechium
Jenis : Sechium edule ( Jacq.) Sw.
2.1.5 Morfologi tumbuhan
Tumbuhan labu siam memiliki morfologi sebagai berikut (Prahasta, 2009). Batang : Lunak, beralur, cabang banyak, serta memiliki sulur batang untuk membelit pada benda lain. Permukaan umumnya kasap atau agak kasar, berwarna hijau, dan berbulu. Berbentuk segi lima dan melilit, dengan panjang batang 50-2.500 cm dan memiliki tunas yang keluar dari ketiak daun.
Bunga : Majemuk yang keluar dari ketiak daun, dengan kelopak bertajuk lima, mahkota beralur, lima benang sari, kepala sari jingga, satu putik yang berwarna kuning. Benang sari dan kepala sari berlekatan.
Buah : Menggantung ditangkai, dengan permukaan berlekuk berwarna hijau ketika muda dengan larik-larik putih kekunigan, semakin matang warna bagian luar buah berubah menjadi hijau pucat sampai putih, bentuk lonjong, dengan ukuran ujung berbeda.
Biji : Pipih, berkeping dua, berwarna putih.
Akar : Berwarna putih kecoklatan, tunggang, bercabang banyak, berbentuk bulat sampai agak persegi, dan berbatang lemah, akar menyebar tetapi dangkal, akar-akar cabang, rambut-rambut akar terdapat dekat permukaan tanah karena hanya dapat menembus tanah 30-40 cm.
2.1.6 Kandungan kimia
Buah Sechium edule (Jacq.) Sw., mengandung saponin, alkaloid dan tanin sedangkan daunnya mengandung saponin, flavonoid dan polifenol (Pratiwi, 2011).
2.1.7 Kegunaan labu siam
1. Diuretik: kandungan air pada labu siam memiliki efek diuretik yang baik sehingga melancarkan buang air kecil
sehingga tekanan darah menurun. Kandungan alkaloidnya berfungsi sebagai vasodilator maka labu siam bisa menurunkan darah tinggi.
3. Buah tanaman ini baik untuk menyembuhkan gangguan sariawan, panas dalam serta menurunkan demam pada anak-anak karena mengandung banyak air
4. Gangguan asam urat
5. Penderita diabetes mellitus juga cocok mengkonsumsi labu siam yang telah dikukus. Kandungan patinya mengenyangkan sehingga perderita diabetes mellitus tidak lagi mengosumsi makanan pokok secara berlebihan (Pratiwi, 2011).
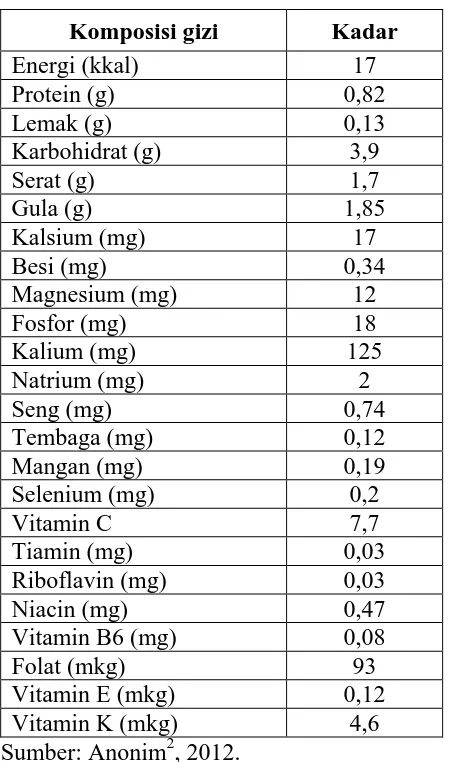
Labu siam memiliki kadar vitamin C yang tinggi, rendah kalori, rendah sodium, tidak mengandung kolesterol, dan merupakan sumber serat yang baik. Berbagai kandungan gizi labu siam dan manfaat kesehatannya antara lain sebagai berikut (Anonim2, 2012).
1. Asam folat: labu siam adalah sumber folat, vitamin B ya
2. Vitamin C: vitamin C adalah salah sat
melindungi sel dari kerusakan oleh radikal bebas
3. Mineral: mineral dalam labu siam membantu tubuh mengubah protein
dan lemak menjadi energi
4. Serat: membantu mencegah sembelit dan melancarkan pencernaan
5. Tembaga: membantu iodium dalam menjaga kesehatan tiroid
6. Zinc: membantu menyehatkan kulit
Buah labu siam memiliki kadar serat yang cukup baik, yaitu 1,7 g per 100 g. Konsumsi serat dalam jumlah yang cukup, sangat baik untuk mengatasi sembelit dan aman untuk lambung yang sensitif atau radang usus. Serat pangan dapat mengurangi risiko penyakit kanker yang disebabkan sistem pencernaan yang tidak sempurna (Anonim2, 2012).
Tabel 2.1 Komposisi gizi per 100 gram labu siam
Komposisi gizi Kadar
Energi (kkal) 17
Protein (g) 0,82
Lemak (g) 0,13
Karbohidrat (g) 3,9
Serat (g) 1,7
Gula (g) 1,85
Kalsium (mg) 17
Besi (mg) 0,34
Magnesium (mg) 12
Fosfor (mg) 18
Kalium (mg) 125
Natrium (mg) 2
Seng (mg) 0,74
Tembaga (mg) 0,12
Mangan (mg) 0,19
Selenium (mg) 0,2
Vitamin C 7,7
Tiamin (mg) 0,03
Riboflavin (mg) 0,03
Niacin (mg) 0,47
Vitamin B6 (mg) 0,08
Folat (mkg) 93
Vitamin E (mkg) 0,12
Vitamin K (mkg) 4,6
Sumber: Anonim2, 2012.
karsinogenik bermukim dalam tubuh juga makin pendek, sehingga peluang terjadinya kanker menjadi sangat kecil (Anonim2, 2012).
2.2Uraian Kandungan Kimia Tumbuhan
2.2.1 Alkaloida
Alkaloida merupakan golongan zat tumbuhan sekunder yang terbesar. Alkaloida mencakup senyawa bersifat basa yang mengandung satu atau lebih atom nitrogen, biasanya sebagai bagian dari sistem siklik. Alkaloida mempunyai aktivitas fisiologi yang menonjol sehingga banyak yang diantaranya digunakan secara luas dalam bidang pengobatan (Harborne, 1987).
Ada tiga pereaksi yang sering digunakan dalam skrining fitokimia untuk mendeteksi alkaloida sebagai pereaksi pengendapan yaitu pereaksi Mayer, pereaksi Bouchardat, dan pereaksi Dragendorff (Farnsworth, 1966).
Kegunaan alkaloida pada tanaman (Anonim4, 2011):
1. Sebagai racun untuk melindungi tanaman dari serangga dan binatang pemakan serangga
2. Sebagai hasil akhir dari reaksi detoksifikasi yang merupakan hasil metabolit akhir dari komponen-komponen yang membahayakan bagi bagi tanaman 3. Sebagai faktor pertumbuhan tanaman
2.2.2 Flavonoida
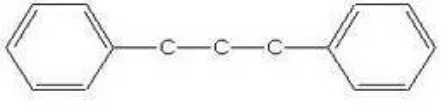
Golongan flavonoida dapat digambarkan sebagai deretan senyawa C6-C 3-C6, artinya kerangka karbonya terdiri atas dua gugus C6 (cincin benzena tersubstitusi) disambungkan oleh rantai alifatik tiga karbon (Robinson, 1995).
Gambar 2.1 Kerangka dasar flavonoid
Flavonoida mencangkup banyak pigmen yang banyak terdapat pada tumbuhan mulai dari jamur sampai angiospermae. Pada tumbuhan tinggi, flavonoida terdapat baik dalam bagian vegetatif maupun dalam bunga. Fungsi flavonoida pada tumbuhan adalah dapat menarik burung dan serangga yang membantu proses penyerbukan, pengatur tumbuh, pengatur fotosintesis, kerja antimikroba dan antivirus (Robinson, 1995).
Sedangkan fungsi flavonoid pada manusia dalam dosis kecil adalah flavon bekerja sebagai stimulan pada jantung, hisperidin mempengaruhi pembuluh darah kapiler, flavon terhidroksilasi bekerja sebagai diuretik dan sebagai antioksidan pada lemak (Sirait, 2007).
2.2.3 Saponin
dingin, dan tumbuhan yang mengandung saponin telah digunakan sebagai racun ikan selama beratus-ratus tahun (Robinson, 1995; Gunawan, et al., 2004).
Saponin dibedakan menjadi dua golongan berdasarkan struktur kimia dari aglikonnya (Sirait, 2007):
1. Saponin netral dengan inti steroid
2. Saponin asam dengan struktur triterpenoid
2.2.4 Tanin
Tanin merupakan salah satu senyawa yang termasuk ke dalam golongan polifenol yang terdapat dalam tumbuhan, mempunyai rasa sepat dan memiliki kemampuan menyamak kulit. Tanin terdapat luas dalam tumbuhan berpembuluh, dalam angiospermae terdapat khusus dalam jaringan kayu (Harborne, 1987).
Salah satu fungsi tanin dalam tumbuhan adalah sebagai penolak herbivora karena rasanya yang pahit (Harborne, 1987).
Sifat-sifat tanin (Anonim3, 2011):
1. Dalam air membentuk larutan koloidal yang bereaksi asam dan sepat 2. Mengendapkan larutan gelatin dan larutan alkaloid
3. Tidak dapat mengkristal
4. Larutan alkali mampu mengoksidasi oksigen
5. Mengendapkan protein dari larutannya dan bersenyawa dengan protein tersebut sehingga tidak dipengaruhi oleh enzim protiolitik.
Tanin dapat dibagi menjadi 2 kelompok (Anonim3, 2011):
2. Tanin terhidrolisis (pirogalol) berwarna biru dengan FeCl3 dan mempunyai tiga gugus fenol.
2.2.5 Glikosida
Glikosida adalah suatu golongan senyawa bila dihidrolisis akan terurai menjadi gula (glikon) dan senyawa lain (aglikon atau genin). Umumnya glikosida mudah terhidrolisis oleh asam mineral atau enzim. Hidrolisis oleh asam memerlukan panas, sedangkan hidrolisis oleh enzim tidak memerlukan panas (Sirait, 2007).
Berdasarkan ikatan antara glikon dan aglikon, glikosida dapat dibedakan menjadi (Sirait, 2007):
a. Tipe O-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan O
b. Tipe S-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan S. Contoh: sinigrin
c. Tipe N-glikosida, ikatan antara bagian dari glikon dengan aglikon melalui jembatan N. Contoh: nikleosidin, krotonosidin
d. Tipe C-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan C. Contoh: aloin, viteksin.
2.2.6 Glikosida antrakuinon
Keluarga tumbuhan yang kaya akan senyawa jenis ini adalah Rubiaceae, Rhamnaceae, Polygonaceae, Caesalpiniaceae dan Liliaceae. Antrakuinon biasanya berupa senyawa kristal bertitik leleh tinggi, aglikonnya larut dalam pelarut organik, senyawa ini berwarna merah, kuning atau coklat, dalam larutan basa membentuk warna violet merah (Robinson, 1995).
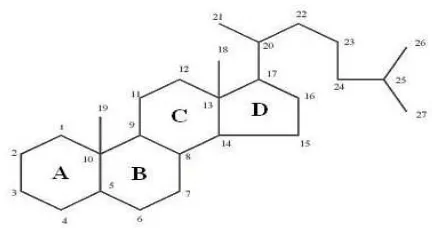
2.2.7 Steroid/triterpenoid
Triterpenoid adalah senyawa yang kerangka karbonnya berasal dari enam satuan isoprena dan secara biosintesis diturunkan dari hidrokarbon C30 asiklik, yaitu skualen. Senyawa tersebut mempunyai struktur siklik yang relatif kompleks, kebanyakan merupakan suatu alkohol, aldehid atau asam karboksilat. Triterpenoid adalah senyawa tanpa warna, berbentuk kristal, sering kali bertitik leleh tinggi dan aktif optik, dapat dibagi atas 4 kelompok senyawa yaitu triterpen sebenarnya, steroid, saponin dan glikosida jantung. Uji kualitatif yang banyak digunakan ialah reaksi Liebermann-Burchard (asam asetat anhidrida-H2SO4 pekat) yang kebanyakan triterpena dan steroida memberikan warna hijau biru (Harborne, 1987).
[image:31.595.204.420.607.728.2]Dahulu steroida dianggap sebagai senyawa yang hanya terdapat pada hewan tetapi sekarang ini makin banyak senyawa steroida yang ditemukan dalam tumbuhan (fitosterol). Fitosterol merupakan senyawa steroida yang berasal dari tumbuhan. Senyawa fitosterol yang biasa terdapat pada tumbuhan tinggi yaitu sitosterol, stigmasterol dan kampesterol (Harborne, 1987).
2.3Metode Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair (Depkes, 2000). Ekstraksi dengan menggunakan pelarut dapat dilakukan dengan beberapa cara yaitu:
Cara dingin
a. Maserasi
Maserasi adalah proses ekstraksi simplisia dengan perendaman menggunakan pelarut yang sesuai dengan sesekali pengadukan pada temperatur ruangan (Depkes, 2000). Hasilnya disebut maserat, maserat diuapkan pelarutnya sebagian atau seluruhnya menjadi ekstrak.
b. Perkolasi
Cara panas
a. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik. Umumnya dilakukan pengulangan proses pada residu pertama sampai 3-5 kali sehingga dapat termasuk proses ekstraksi sempurna (Depkes, 2000).
b. Sokletasi
Sokletasi adalah ekstraksi menggunakan pelarut yang umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinu dengan jumlah pelarut relatif konstan dengan adanya pendingin balik (Depkes, 2000).
c. Digestasi
Digestasi adalah maserasi dengan pengadukan kontinu pada temperatur yang lebih tinggi dari temperatur ruangan, yaitu secara umum dilakukan pada temperatur 40-50℃ (Depkes, 2000).
d. Infustasi
Infustasi adalah sediaan cair yang dibuat dengan menyari simplisia nabati dengan air pada suhu 90℃selama 15 menit (Depkes, 1979).
e. Dekoktasi
2.4Kromatografi
Kromatografi adalah suatu metode pemisahan berdasarkan perbedaan perpindahan dari komponen-komponen senyawa diantara dua fase yaitu fase diam (dapat berupa zat cair atau zat padat) dan fase gerak (dapat berupa gas atau zat cair) (Depkes, 1995). Fase diam berupa zat padat maka cara tersebut dikenal sebagai kromatografi serapan, jika zat cair dikenal sebagai kromatografi partisi. Karena fase gerak dapat berupa zat cair dan gas maka ada empat macam sistem kromatografi (Sastrohamidjojo, 1985):
1. Fase gerak zat cair–fase diam padat: - Kromatografi lapis tipis
- Kromatografi penukar ion 2. Fase gerak gas–fase diam padat:
- Kromatografi gas padat
3. Fase gerak zat cair–fase diam zat cair: - Kromatografi cair kinerja tinggi 4. Fase gerak gas–fase diam zat cair:
- Kromatografi gas cair - Kromatografi kolom kapiler
Pemisahan dan pemurnian kandungan tumbuhan dilakukan dengan menggunakan salah satu atau gabungan dari beberapa teknik tersebut dan dapat digunakan pada skala mikro maupun makro (Harborne, 1987).
2.4.1 Kromatografi lapis tipis
berupa plat gelas, logam atau lapisan yang cocok. Campuran yang akan dipisah berupa larutan yang ditotolkan baik berupa bercak ataupun pita, setelah plat atau lapisan dimasukkan ke dalam bejana tertutup rapat yang berisi larutan pengembang yang cocok (fase gerak), pemisahan terjadi selama perambatan kapiler (pengembangan), selanjutnya senyawa yang tidak berwarna harus ditampakkan (Stahl, 1985).
Pendeteksian bercak hasil pemisahan dapat dilakukan dengan beberapa cara. Untuk senyawa tak berwarna cara yang paling sederhana adalah dilakukan pengamatan dengan sinar ultraviolet. Beberapa senyawa organik bersinar atau berfluorosensi jika disinari dengan sinar ultraviolet gelombang pendek (254 nm) atau gelombang panjang (366 nm), jika dengan cara itu senyawa tidak dapat dideteksi maka harus dicoba disemprot dengan pereaksi yang membuat bercak tersebut tampak yaitu pertama tanpa pemanasan, kemudian bila perlu dengan pemanasan (Gritter, et al., 1991; Stahl, 1985).
a. Fase diam (lapisan penjerap)
Kromatografi lapis tipis, fase diam berupa lapisan tipis yang terdiri atas bahan padat yang dilapiskan pada permukaan penyangga datar yang biasanya terbuat dari kaca, dapat pula terbuat dari plat polimer atau logam. Lapisan melekat pada permukaan dengan bantuan bahan pengikat, biasanya kalsium sulfat atau amilum. Penjerap yang umum dipakai untuk kromatografi lapis tipis adalah silika gel, alumina, kieselgur dan selulosa (Gritter, et al., 1991).
yang butirannya sangat kasar tidak akan memberikan hasil yang memuaskan dan salah satu cara untuk memperbaiki hasil pemisahan adalah dengan menggunakan fase diam yang butirannya lebih halus. Butiran yang halus memberikan aliran pelarut yang lebih lambat dan resolusi yang lebih baik (Sastrohamidjojo, 1985).
b. Fase gerak (pelarut pengembang)
Fase gerak ialah medium angkut yang terdiri atas satu atau beberapa pelarut, jika diperlukan sistem pelarut multi komponen, harus berupa suatu campuran sesederhana mungkin yang terdiri atas maksimum tiga komponen (Stahl, 1985).
Pemisahan senyawa organik selalu menggunakan pelarut campur. Tujuan menggunakan pelarut campur adalah untuk memperoleh pemisahan senyawa yang baik. Kombinasi pelarut adalah berdasarkan atas polaritas masing-masing pelarut, sehingga dengan demikian akan diperoleh sistem pengembang yang cocok. Pelarut pengembang yang digunakan dalam kromatografi lapis tipis antara lain:
n-heksan, karbontetraklorida, benzen, kloroform, eter, etilasetat, piridian, aseton,
etanol, metanol dan air (Gritter, et al., 1991).
c. Harga Rf
Mengidentifikasi noda-noda dalam kromatografi lapis tipis sangat lazim menggunakan harga Rf (Retordation Factor) yang didefinisikan sebagai:
Jarak titik pusat bercak dari titik awal Rf =
Jarak garis depan pelarut dari titik awal
Harga Rf beragam mulai dari 0 sampai 1. Faktor-faktor yang mempengaruhi harga Rf (Sastrohamidjojo, 1985):
b. Sifat penjerap
c. Tebal dan kerataan dari lapisan penjerap d. Pelarut dan derajat kemurniannya
e. Derajat kejenuhan uap pengembang dalam bejana f. Teknik percobaan
g. Jumlah cuplikan yang digunakan h. Suhu
i. Kesetimbangan.
2.4.2 Kromatografi cair vakum
Cara ini pertama kali dipublikasikan oleh Coll dkk., pada tahun 1977 dengan menggunakan corong Buchner kaca masir atau kolom pendek untuk mengisolasi diterpena sembrenoida dari terumbu karang Australia. Kolom kromatografi dikemas kering dalam keadaan vakum agar diperoleh kerapatan kemasan maksimum. Vakum dihentikan, pelarut yang kepolarannya rendah dituangkan ke permukaan penjerap lalu divakumkan lagi. Kolom dihisap sampai kering dan sekarang siap dipakai (Hostettmann, et al., 1995).
2.4.3 Kromatografi kolom
Kromatografi cair yang dilakukan di dalam kolom besar merupakan metode kromatografi terbaik untuk pemisahan campuran dalam jumlah besar (lebih dari 1 g), kadang-kadang cara ini disebut kromatografi cair preparatif (KCP = PLC). Pada kromatografi kolom, campuran yang akan dipisahkan diletakkan berupa pita pada bagian atas kolom penjerap yang berada pada tabung kaca, tabung logam, atau tabung plastik. Pelarut (fase gerak) dibiarkan mengalir melalui kolom, karena aliran yang disebabkan oleh gaya berat atau didorong dengan tekanan. Pita senyawa bergerak melalui melalui kolom dengan laju yang berbeda, memisah dan dikumpulkan berupa fraksi ketika keluar dari alas kolom (Sastrohamidjojo, 1985).
2.4.4 Kromatografi lapis tipis preparatif
Kromatografi lapis tipis (KLT) preparatif merupakan salah satu metode pemisahan dengan menggunakan peralatan sederhana. Ketebalan penjerap yang sering dipakai adalah 0,5-2 mm, ukuran plat kromatografi biasanya 20x20 cm. Pembatasan ketebalan lapisan dan ukuran plat sudah tentu mengurangi jumlah bahan yang dapat dipisahkan dengan KLT preparatif. Penjerap yang paling umum digunakan adalah silika gel (Hostettmann, et al., 1995).
jenuh dengan pelarut pengembang dengan bantuan kertas saring yang diletakkan berdiri disekeliling permukaan bagian dalam bejana (Hostettmann, et al., 1995).
Kebanyakan penjerap KLT preparatif mengandung indikator fluorosensi yang membantu mendeteksi letak pita yang terpisah pada senyawa yang menyerap sinar ultraviolet. Untuk mendeteksi senyawa yang tidak menyerap sinar ultraviolet yaitu dengan cara menutup plat dengan sepotong kaca lalu menyemprot kedua sisi dengan penyemprot (Hostettmann, et al., 1995).
Pita ditampakkan dengan cara yang tidak merusak maka senyawa yang tidak berwarna dengan penjerap dikerok dari plat kaca. Cara ini berguna untuk memisahkan campuran beberapa senyawa sehingga diperoleh senyawa murni (Gritter, et al., 1991).
2.4.5 Kromatografi lapis tipis dua arah (two-dimensional TLC)
KLT dua arah atau KLT dua dimensi ini bertujuan untuk meningkatkan resolusi sampel ketika komponen-komponen solut mempunyai karakteristik kimia yang hampir sama, karena nilai Rf juga hampir sama, selain itu dua sistem fase gerak yang sangat berbeda dapat digunakan secara berurutan pada suatu campuran tertentu sehingga memungkinkan untuk melakukan pemisahan analit yang mempunyai tingkat polaritas yang hampir sama (Rohman, 2009).
tergantung pada kemampuan untuk memodifikasi selektifitas eluen kedua dibandingkan dengan selektifitas eluen pertama (Rohman, 2009).
2.5 Spektrofotometri
Spektrofotometri adalah metode pengukuran dimana sumber energinya berupa sinar/cahaya dan sistem detektornya menggunakan sel fotolistrik (Noerdin, 1985).
2.5.1 Spektrofotometri sinar ultraviolet
Spektrum ultraviolet adalah suatu gambaran yang menyatakan hubungan antara panjang gelombang atau frekuensi serapan terhadap intensitas serapan (transmitansi atau adsorbansi) (Sastrohamidjojo, 1985). Apabila suatu molekul menyerap radiasi ultraviolet, di dalam molekul tersebut terjadi perpindahan tingkat energi elektron-elektron ikatan pada orbital molekul paling luar dari tingkat energi yang lebih rendah ke tingkat energi yang lebih tinggi (Noerdin, 1985).
Pelarut yang banyak digunakan untuk spektrofotometri sinar UV adalah etanol 95% karena kebanyakan golongan senyawa larut dalam pelarut tersebut. Alkohol absolut komersial harus dihindari karena mengandung benzena yang dapat menyerap di daerah sinar UV pendek. Pelarut yang sering digunakan ialah air, etanol, metanol, n-heksana, eter minyak bumi dan eter (Harborne, 1987).
2.5.2 Spektrofotometri sinar inframerah
diserap. Daerah inframerah terletak antara spektrum elektromagnetik cahaya tampak dan spektrum radio, yakni antara 4000-400 cm-1 (Noerdin, 1985).
Daerah pada spektrum inframerah di atas bilangan gelombang 1200 cm-1 menunjukkan pita spektrum atau puncak yang disebabkan oleh getaran ikatan kimia atau gugus fungsi dalam molekul yang ditelaah. Daerah di bawah 1200 cm-1 menunjukkan pita yang disebabkan oleh getaran seluruh molekul, dan karena kerumitannya dikenal sebagai daerah sidik jari. Intensitas berbagai pita direkam secara subjektif pada skala sederhana (Noerdin, 1985).
BAB III
METODE PENELITIAN
Metode yang digunakan adalah metode eksperimental meliputi pengumpulan bahan tumbuhan, identifikasi tumbuhan, pembuatan simplisia, pemeriksaan karakterisasi simplisia, skrining fitokimia simplisia, pembuatan ekstrak etanol, ekstraksi cair-cair, kromatografi lapis tipis, kromatografi cair vakum, kromatografi kolom, KLT preparatif, KLT dua arah, uji kemurnian isolat dan karakterisasi isolat secara spektrofotometri UV dan spektrofotometri IR. Penelitian dilakukan di Laboratorium Farmakognosi dan Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara.
5.1 Alat-alat
Alat-alat yang digunakan pada penelitian ini adalah alat-alat gelas laboratorium, cawan penguap, spatula, blender (Panasonic), eksikator, seperangkat alat destilasi, seperangkat alat kromatografi cair vakum, seperangkat alat kromatografi kolom, chamber, plat KLT dan plat kaca KLT preparatif, pipet kapiler, spray kromatografi, oven listrik (Stork), tanur, elektromantel (EM 2000),
hair dryer (Maspion), neraca analitik (Vibra AJ), neraca kasar (Saherand),
5.2 Bahan-bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah pucuk labu siam (Sechium edule (Jacq.) Sw). Semua bahan yang digunakan kecuali dinyatakan lain adalah berkualitas proanalisa yaitu n-heksan proanalisis (Merk), metanol (Merk), benzen, etilasetat, etanol, toluen, asam asetat anhidrida, asam sulfat pekat, asam klorida pekat, kalium bromida, plat pra lapis silika gel GF254, silika gel 60H, metanol, n-heksan hasil destilasi dan air suling.
3.3 Pembuatan Pereaksi
3.3.1 Pereaksi Bouchardat
Sebanyak 4 g kalium iodida P dilarutkan dalam air secukupnya, lalu ditambahkan 2 g iodium P kemudian ditambahkan air hingga 100 ml (Depkes, 1995).
3.3.2 Pereaksi Mayer
Larutan raksa (II) klorida P 2,266% b/v sebanyak 60 ml dicampur dengan 10 ml larutan kalium iodida P 50% b/v, kemudian ditambahkan air secukupnya hingga 100 ml (Depkes, 1995).
3.3.3 Pereaksi Dragendorff
3.3.4 Pereaksi Molish
Sebanyak 3 g α-naftol P, dilarutkan dalam asam nitrat 0,5 N hingga diperoleh larutan 100 ml (Depkes, 1995).
3.3.5 Larutan Asam Klorida 2 N
Larutan asam klorida pekat sebanyak 17 ml ditambahkan air suling sampai 100 ml (Depkes, 1995).
3.3.6 Larutan Asam Sulfat 2 N
Larutan asam sulfat pekat sebanyak 9,8 ml ditambahkan air suling sampai 100 ml (Depkes, 1995).
3.3.7 Larutan Asam Nitrat 0,5 N
Sebanyak 3,4 ml asam nitrat pekat diencerkan dengan air suling hingga volume 100 ml (Depkes, 1995).
3.3.8 Larutan Timbal (II) Asetat 0,4 M
Sebanyak 15,17 g timbal (II) asetat P dilarutkan dalam air bebas karbon dioksida hingga 100 ml (Depkes, 1995).
3.3.9 Larutan Besi (III) Klorida 1% b/v
Sebanyak 1 g besi (III) klorida dilarutkan dalam air secukupnya hingga 100 ml (Depkes, 1995).
3.3.10 Larutan Pereaksi Kloralhidrat
Sebanyak 50 g kristal kloralhidrat ditimbang lalu dilarutkan dalam 71,43 ml air suling (Depkes, 1995).
3.3.10.1Larutan Pereaksi Liebermann-Burchard
Asam sulfat pekat sebanyak 5 ml dicampurkan dalam 50 ml etanol 96%,
3.3.11 Larutan Floroglusin HCl
Larutan floroglusin P 1% b/v dalam etanol (90%), kemudian ditambahkan 3 ml HCl pekat (Depkes, 1995).
3.4 Pengumpulan Bahan Tumbuhan, Identifikasi Tumbuhan dan
Pembuatan Simplisia
3.4.1 Pengumpulan bahan tumbuhan
Metode pengumpulan bahan tumbuhan dilakukan secara purposif yaitu tanpa membandingkan dengan bahan tumbuhan yang sama dari daerah lain. Bahan yang digunakan adalah pucuk labu siam segar yang diambil dari Pasar Sore Jalan Jamin Ginting, Medan, Provinsi Sumatera Utara.
3.4.2 Identifikasi tumbuhan
Identifikasi tumbuhan dilakukan di Herbarium Bogoriense, Bidang Botani, Pusat Penelitian Biologi, Lembaga Ilmu Pengetahuan Indonesia (LIPI) Bogor, Jl. Raya Jakarta-Bogor. Provinsi Jawa Barat. Identifikasi tumbuhan pucuk labu siam (Sechium edule (Jacq.) Sw.) dapat dilihat pada Lampiran 1, halaman 52.
3.4.3 Pembuatan simplisia
3.5 Pemeriksaan Karakteristik Simplisia
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik, pemeriksaan mikroskopik, penetapan kadar air, penetapan kadar sari yang larut dalam air, penetapan kadar sari yang larut dalam etanol, penetapan kadar abu total dan penetapan kadar abu yang tidak larut dalam asam (Depkes, 1989).
3.5.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk, bau, rasa dan warna dari herba serta serbuk simplisia pucuk labu siam (Sechium edule (Jacq.) Sw.). Pemeriksaan makroskopik pucuk labu siam (Sechium edule (Jacq.) Sw.) dapat dilihat pada Lampiran 3, halaman 54 sampai 55.
3.5.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik terhadap serbuk simplisia dan daun segar pucuk labu siam dilakukan dengan cara sampel diletakkan di atas kaca objek yang telah diteteskan dengan larutan kloralhidrat dan ditutup dengan kaca penutup kemudian diamati dibawah mikroskop. Batang segar dari pucuk labu siam dilakukan dengan cara sampel diletakkan pada kaca objek kemudian ditetesi dengan larutan flurogusinol HCl dan diamati dibawah mikroskop. Pemeriksaan mikroskopik pucuk labu siam (Sechium edule (Jacq.) Sw.) dapat dilihat pada Lampiran 4, halaman 56 sampai 58.
3.5.3 Penetapan kadar air
1. Penjenuhan toluen
Sebanyak 200 ml toluen dan 2 ml air suling dimasukkan ke dalam labu alas bulat, didestilasi selama 2 jam, kemudiaan toluen didinginkan selama 30 menit dan volume air pada tabung penerima dibaca dengan ketelitian 0,05 ml (WHO, 1992).
2. Penetapan kadar air simplisia
Sebanyak 5 g simplisia yang telah ditimbang seksama dimasukkan kedalam labu alas bulat berisi toluen tersebut, lalu dipanaskan hati-hati selama 15 menit, setelah toluen mendidih kecepatan tetesan diatur lebih kurang 2 tetes perdetik sampai bagian air terdestilasi, bagian dalam pendingin dibilas dengan toluen. Destilasi dilanjutkan selama 5 menit kemudian tabung penerima dibiarkan dingin sampai suhu kamar, setelah air dan toluen memisah sempurna volume air dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa. Kadar air yang dihitung dalam persen (WHO, 1992). Perhitungan penetapan kadar air dari simplisia pucuk labu siam (Sechii edulei herba) dapat dilihat pada Lampiran 17, halaman 72.
3.5.4 Penetapan kadar sari yang larut dalam air
Pehitungan hasil penetapan kadar sari yang larut dalam air dapat dilihat pada Lampiran 17, halaman 72 sampai 73.
3.5.5 Penetapan kadar sari yang larut dalam etanol
Sebanyak 5 g simplisia dimaserasi selama 24 jam dalam 100 ml etanol 96% dalam labu tersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam, kemudian disaring cepat untuk menghindari penguapan etanol, 20 ml filtrat diuapkan sampai kering dalam cawan dangkal berdasar rata yang telah ditara dan dipanaskan pada suhu 105℃ sampai bobot tetap. Kadar sari larut dalam etanol dihitung terhadap bahan yang telah dikeringkan (Depkes RI, 1989). Pehitungan hasil penetapan kadar sari yang larut dalam etanol dapat dilihat pada Lampiran 17, halaman 74.
3.5.6 Penetapan kadar abu total
Sebanyak 2 g simplisia yang telah digerus dan ditimbang seksama dimasukkan dalam krus porselin yang telah dipijar dan ditara, kemudian diratakan dan dipijarkan pada suhu 600℃ sampai arang habis, kemudian didinginkan dan ditimbang sampai diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan (WHO, 1992). Perhitungan hasil penetapan kadar abu total dapat dilihat pada Lampiran 17, halaman 75.
3.5.7 Penetapan kadar abu yang tidak larut dalam asam
asam dihitung terhadap bahan yang dikeringkan (WHO, 1992). Pehitungan hasil penetapan kadar abu yang tidak larut dalam asam dapat dilihat pada Lampiran 17, halaman 75 sampai 76.
3.6 Skrining Fitokimia
3.6.1 Pemeriksaan alkaloida
Serbuk simplisia ditimbang sebanyak 0,5 g kemudian ditambahkan 1 ml asam klorida 2 N dan 9 ml air suling, dipanaskan di atas penangas air selama 2 menit, didinginkan lalu disaring. Filtrat dipakai untuk percobaan berikut :
a. Diambil 3 tetes filtrat, lalu ditambahkan 2 tetes pereaksi Mayer b. Diambil 3 tetes filtrat, lalu ditambahkan 2 tetes pereaksi Bouchardat c. Diambil 3 tetes filtrat, lalu ditambahkan 2 tetes pereaksi Dragendrof Alkaloida dianggap positif jika terjadi endapan atau paling sedikit dua atau tiga dari percobaan di atas (Depkes, 1995).
3.6.2 Pemeriksaan flavonoid
Sebanyak 10 g serbuk simplisia kemudian ditambahkan 100 ml air panas, dididihkan selama 5 menit dan disaring dalam keadaan panas. Filtrat yang diperoleh kemudian diambil 5 ml lalu ditambahkan 0,1 g serbuk Mg dan 1 ml HCl pekat dan 2 ml amil alkohol, dikocok dan dibiarkan memisah. Flavonoid positif jika terjadi warna merah, kuning, jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.6.3 Pemeriksaan tanin
larutan lalu ditambahkan 1 sampai 2 tetes pereaksi besi (III) klorida. Terjadi warna biru atau hijau kehitaman menunjukkan adanya tanin (Farnsworth, 1966).
3.6.4 Pemeriksaan glikosida
Serbuk simplisia ditimbang sebanyak 3 g kemudian disari dengan 30 ml campuran 7 bagian volume etanol 96% dan 3 bagian volume air suling (7:3), direfluk selama 10 menit didinginkan dan disaring, pada 20 ml filtrat tambahkan 25 ml air dan 25 ml timbal (II) asetat 0,4 M, dikocok, diamkan selama 5 menit lalu disaring. Filtrat disari sebanyak 3 kali, setiap kali dengan 20 ml campuran 3 bagian volume kloroform P dan 2 bagian volume isopropanolol P, pada sari yang dikumpukan tambahkan natrium sulfat anhidrida P, disaring dan uapkan pada suhu tidak lebih dari 50℃. Larutkan sisa dengan 2 ml metanol P, dimasukkan 0,1 ml larutan dalam tabung reaksi, uapkan di atas penangas air, pada sisa tambahkan 2 ml air dan 5 tetes Molish, ditambahkan hati-hati 2 ml asam sulfat P, bila terbentuk cincin berwarna ungu pada batas cairan, menunjukkan adanya ikatan gula (reaksi Molish) (Depkes, 1995).
3.6.5 Pemeriksaan saponin
Sebanyak 0,5 g sampel dimasukan ke dalam tabung reaksi dan ditambahkan 10 ml air suling panas, didinginkan kemudian dikocok kuat-kuat selama 10 detik, terbentuk buih atau busa tidak kurang dari 10 menit setinggi 1-10 cm, pada penambahan 1 tetes larutan asam klorida 2 N apabila buih tidak hilang menunjukkan adanya saponin (Depkes, 1995).
3.6.6 Pemeriksaan steroid/triterpenoid
asam asetat anhidrida dan 1 tetes asam sulfat pekat, apabila timbul warna ungu atau merah kemudian berubah menjadi hijau biru menunjukkan adanya steroid/triterpenoid (Harbone, 1987).
3.6.7 Pemeriksaan glikosida antrakuinon
Sebanyak 0,2 g serbuk simplisia dicampur dengan 5 ml asam sulfat 2 N, didihkan sebentar, setelah dingin ditambahkan 10 ml benzen, dikocok dan didiamkan. Lapisan benzen dipisahkan dan disaring. Lapisan benzen dikocok dengan 2 ml NaOH 2 N, didiamkan. Lapisan air berwarna merah menunjukan adanya glikosida antrakuinon (Depkes, 1979).
3.7 Pembuatan Ekstrak Etanol dan Ekstraksi Cair-cair Ekstrak Etanol
3.7.1 Pembuatan ekstrak etanol
Pembuatan ekstrak dilakukan secara maserasi dengan pelarut etanol 96%. Cara kerja:
3.7.2 Ekstraksi cair-cair ekstrak etanol
Ekstraksi cair-cair ekstak etanol dengan pelarut n-heksan. Cara kerja:
Ekstrak etanol ditambahkan 40 ml etanol, lalu dilarutkan dengan air panas sebanyak 100 ml, lalu dimasukkan ke dalam corong pisah, difraksinasi dengan
n-heksan sebanyak 100 ml, dilakukan tiga kali, diperoleh fraksi n-heksan dan
fraksi air. Fraksi n-heksan dipekatkan. Bagan ekstraksi cair-cair ekstrak etanol dapat dilihat pada Lampiran 7, halaman 61.
3.8 Analisis Fraksi n-Heksan Secara KLT
Analisis dengan kromatografi lapis tipis (KLT) berguna untuk mendapatkan fase gerak yang terbaik. Fase gerak yang terbaik adalah fase gerak yang dapat menghasilkan bercak paling banyak yang digunakan untuk fase gerak pada kromatografi kolom.
Terhadap fraksi n-heksan dilakukan analisis secara KLT menggunakan fase diam silika gel GF254 dan fase gerak campuran n-heksan:etilasetat dengan perbandingan (100:0), (90:10), (80:20), (70:30), dan (60:40), sebagai penampak bercak digunakan pereaksi Liebermann-Burchard.
Cara kerja:
dan dihitung harga Rf pada semua bercak. Fase gerak yang menghasilkan noda (bercak) paling banyak adalah fase gerak yang terbaik. Kromatogram dan harga Rf dari fraksi n-heksan pucuk labu siam (Sechium edule (Jacq.) Sw.) dapat dilihat pada Lampiran 9, halaman 64.
3.9 Pemisahan Ekstrak n-Heksan Dengan KCV
Kromatografi cair vakum (KCV) merupakan kromatografi yang dilakukan untuk memisahkan golongan senyawa metabolit sekunder secara kasar dengan menggunakan silika gel sebagai adsorben dan berbagai perbandingan pelarut
n-heksan:etilasetat (elusi gradien) dan menggunakan pompa vakum untuk
memudahkan penarikan eluen (Hostettmann, et al, 1995).
Ekstrak n-heksan difraksinasi secara KCV menggunakan pelarut landaian
n-heksan:etilasetat dengan perbandingan (100:0), (95:5), (90:10), (85:15), (80:20),
(75:25), (70:30), (65:35), (60:40), (55:45), (50:50) dan (100:0), (90:10), (80:20), (70:30), (60:40), (50:50), (40:60), (30:70), (20:80), (10:90), (0:100).
Cara kerja:
dan kolom dihisap sampai kering pada setiap pengumpulan fraksi (Hostettmann,
et al, 1995). Kromatogram KLT hasil KCV dapat dilihat pada Lampiran 10 dan
11, halaman 65 sampai 66.
3.10 Pemisahan Ekstrak n-Heksan Dengan Kromatografi Kolom
Kromatografi kolom dipakai untuk memperoleh komponen campuran dalam jumlah yang memadai (mg sampai g) dalam keadaan murni sehingga komponen itu dapat dicirikan lebih lengkap atau dipakai pada reaksi berikutnya (Gritter, 1991).
Kandungan kimia yang terdapat dalam ekstrak n-heksan dipisahkan secara kromatografi kolom menggunakan pelarut isokratik n-heksan:etilasetat (80:20). Fase diam silika gel 60 H ukuran partikel 0,063-0,200 mm (mesh 70-230 ASTM). Cara kerja:
perlahan-lahan sambil fase gerak terus ditambah. Eluat yang keluar ditampung dalam vial, masing-masing sebanyak 5 ml. Hal ini dilakukan sampai eluat memberikan hasil negatif terhadap pereaksi Liebermann-Burchard. Hasil dipantau dengan kromatografi lapis tipis menggunakan fase gerak n-heksan:etilasetat (80:20), penampang bercak Liebermann-Burchard. Untuk eluat yang mempunyai pola kromatogram yang sama digabung menjadi satu. Kromatogram KLT hasil kromatografi kolom dapat lihat pada Lampiran 12, halaman 67.
3.11 Isolasi Senyawa Steroid/Triterpenoid Hasil Kromatografi Kolom
Terhadap fraksi hasil kromatografi kolom yang memberikan bercak sama berwarna merah ungu dilakukan isolasi secara KLT preparatif, sebagai penampak bercak digunakan pereaksi Liebermann-Burchard dan sebagai fase gerak digunakan n-heksan:etilasetat (80:20) dan fase diam silika gel GF254.
Cara kerja:
terhadap isolat yang diperoleh. Kromatogram KLT preparatif dapat dilihat pada Lampiran 13, halaman 68.
3.12 Uji Kemurnian Terhadap Kristal Hasil Isolasi
Terhadap isolat hasil isolasi dilakukan KLT 2 arah menggunakan fase gerak n-heksan:etilasetat (80:20) dan toluen:etilasetat (90:10).
Cara kerja:
Isolat ditotolkan pada plat pra lapis silika gel GF254 ukuran 10x10 lalu dielusi memakai fase gerak I yaitu n-heksan:etilasetat (80:20) hingga mencapai batas pengembangan, kemudian plat dikeluarkan dari dalam bejana dan dikeringkan, setelah plat kering dielusi kembali dengan arah yang berbeda 90℃ memakai fase gerak II yaitu toluen:etilasetat (90:10), disemprot dengan memakai penampak bercak Liebermann-Burchard, setelah itu plat dipanaskan pada suhu 105℃ selama 10 menit lalu diamati warna yang terbentuk. Hasil KLT dua arah dan harga Rf dapat dilihat pada Lampiran 14, halaman 69.
3.13 Karakterisasi Isolat
Karakterisasi isolat dengan spektrofotometri ultraviolet dan spektrofotometri inframerah dilakukan di Laboratorium Penelitian Fakultas Farmasi USU Medan.
3.13.1 Karakterisasi isolat dengan spektrofotometri UV
Cara kerja:
absorbansi larutan sampel diukur pada panjang gelombang 200-400 nm. Panjang gelombang hasil spektrofometri sinar UV dapat dilihat pada Lampiran 15, halaman 70.
3.13.2 Karakterisasi isolat dengan spektrofotometri IR
Cara kerja:
Karakterisasi isolat dengan spektrofotometri IR dilakukan dengan cara mencampurkan 1 mg isolat dengan 100 mg kalium bromida menggunakan alat
mixture vibrator kemudian dicetak menjadi pelet pada tekanan 11,5 ton dan
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Sampel
Hasil identifikasi tumbuhan yang dilakukan di Herbarium Bogoriense Bidang Botani Pusat Penelitian Biologi-LIPI Bogor menunjukkan bahwa tumbuhan yang diteliti termasuk suku Cucurbitaceae spesies Sechium edule (Jacq.) Sw.
4.2 Hasil Karakteristik Serbuk Simplisia
Hasil makroskopik dari serbuk simplisia pucuk labu siam adalah bentuk
serbuk kasar, berwarna hijau kekuningan, tidak mempunyai bau dan rasa yang khas. Hasil pemeriksaan makroskopik dilakukan terhadap daun muda segar pucuk labu siam yaitu bentuk jantung, ujung meruncing, panjang 3-8 cm, lebar 2-10 cm, berwarna hijau, tidak mempunyai bau dan rasa yang khas. Makroskopik batang segar dari pucuk labu siam yaitu bentuk bulat memanjang, panjang 18-28 cm, lebar 0,5-1 cm, berwarna hijau, tidak mempunyai bau dan rasa yang khas.
Hasil pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia
kolenkim, sklerenkim, parenkim, floem luar, xilem, floem dalam, parenkim penghubung, dan kambium.
Menurut Depkes (2000), standarisasi suatu simplisia merupakan pemenuhan terhadap persyaratan sebagai bahan obat dan menjadi penetapan nilai untuk berbagai parameter produk. Simplisia sebagai bahan baku obat dari pucuk labu siam belum ada tercantum dalam monografi terbitan resmi Departemen Kesehatan (Materia Medika Indonesia) sehingga digunakan prosedur karakterisasi tumbuhan dari monografi ini untuk menentukan karakteristik simplisia dari pucuk labu siam. Beberapa karakterisasi yang dilakukan masing-masing memberikan tujuan sehingga diharapkan memenuhi persyaratan simplisia sebagai bahan baku
obat.
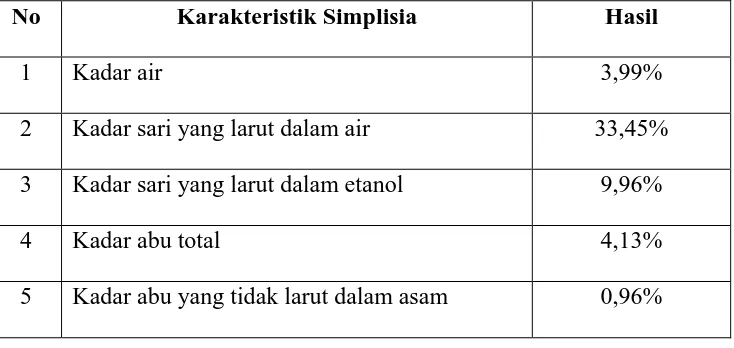
[image:59.595.118.485.471.645.2]Hasil pemeriksaan karakteristik simplisia pucuk labu siam dapat dilihat pada Tabel 4.1.
Tabel 4.1. Hasil karakteristik simplisia dari pucuk labu siam
No Karakteristik Simplisia Hasil
1 Kadar air 3,99%
2 Kadar sari yang larut dalam air 33,45% 3 Kadar sari yang larut dalam etanol 9,96%
4 Kadar abu total 4,13%
5 Kadar abu yang tidak larut dalam asam 0,96%
Perubahan senyawa kimia berkhasiat dan aktivitas enzim karena enzim tertentu dalam sel masih dapat bekerja dalam menguraikan senyawa aktif setelah sel mati dan selama bahan simplisia masih mengandung jumlah air tertentu (Depkes, 1999). Penetapan kadar sari larut air untuk mengetahui kadar senyawa kimia bersifat polar yang terkandung di dalam simplisia pucuk daun labu siam yang hasilnya diperoleh 33,45%, sedangkan kadar sari larut dalam etanol dilakukan untuk mengetahui kadar senyawa larut dalam etanol, baik senyawa polar maupun non polar hasilnya adalah 9,96%. Hasil penetapan kadar sari larut air dan etanol tidak dapat dibandingkan dengan kadar yang tertera pada monografi, karena belum terdapat monografi. Kandungan sari larut air lebih tinggi daripada kadar sari larut etanol, ini berarti senyawa kimia yang larut di dalam air lebih banyak dibandingkan larut etanol. Penetapan kadar abu total dilakukan untuk mengetahui kadar senyawa anorganik dalam simplisia, misalnya logam K, Ca, Na, Pb, Hg, silika, sedangkan penetapan kadar abu tidak larut dalam asam dilakukan untuk mengetahui kadar senyawa yang tidak larut dalam asam, misalnya silikat. Perhitungan hasil penetapan kadar dapat dilihat pada Lampiran 17, halaman 72 sampai 76.
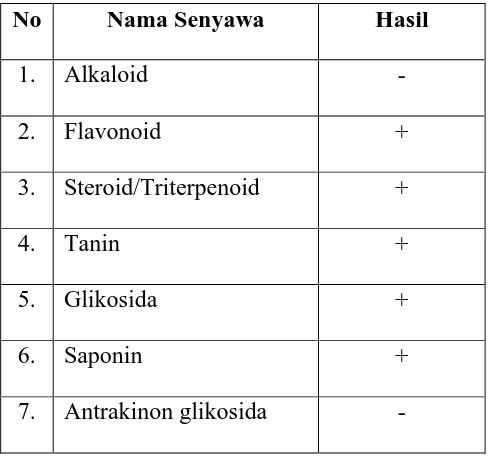
4.3 Hasil Skrining Fitokimia
Tabel 4.2. Hasil skrining fitokimia dari simplisia pucuk labu siam
No Nama Senyawa Hasil
1. Alkaloid -
2. Flavonoid +
3. Steroid/Triterpenoid +
4. Tanin +
5. Glikosida +
6. Saponin +
7. Antrakinon glikosida -
Penentuan golongan senyawa kimia terhadap simplisia pucuk labu siam dilakukan untuk mendapatkan informasi golongan senyawa metabolit sekunder yang terdapat di dalamnya. Serbuk simplisia pucuk labu siam yang ditambah dengan pereaksi Dragendorff memberikan endapan warna jingga kecoklatan, dengan pereaksi Bouchardat tidak memberikan endapan warna kuning kecoklatan, dan dengan pereaksi Mayer tidak terbentuk endapan putih dan kekeruhan, ini menunjukkan simplisia tidak mengandung alkaloid. Alkaloid dianggap positif jika terjadi endapan atau paling sedikit dua atau tiga dari pereaksi yang ditambahkan (Depkes, 1995). Skrining fitokimia terhadap flavonoid yakni dengan penambahan serbuk Mg, HCl p dan amil alkohol memberikan warna kuning pada lapisan amil alkohol. Ini dianggap bahwa flavonoid positif pada pucuk labu siam (Farnsworth, 1966).
sedangkan skrining pada tanin dengan penambahan FeCl3 memberikan warna biru kehitaman menunjukan adanya tanin (Farnsworth, 1966).
Skrining glikosida ditunjukkan dengan penambahan pereaksi Molish dan asam sulfat pekat dimana terbentuk cincin berwarna ungu. Pereaksi Molish merupakan pereaksi umum yang digunakan untuk identifikasi karbohidrat, dalam hal ini adalah gula (Depkes, 1995).
Skrining saponin menghasilkan busa yang stabil dengan tinggi busa 3 cm dan tidak hilang dengan penambahan HCl 2 N, sifat busa saponin disebabkan adanya struktur amfifilik saponin mengakibatkan sifat fisika saponin sebagai surfaktan yang sifat ini sama seperti sabun dan deterjen, penambahan HCl 2 N mengakibatkan kestabilan busa semakin lama sesuai dengan sifat sabun (Depkes, 1995).
4.4 Hasil Ekstraksi Dan Fraksinasi Cair-Cair Senyawa Aktif Dari Ekstrak Etanol Dan Isolasi Senyawa Aktif
Hasil maserasi 300 g serbuk simplisia dengan 3000 ml etanol diperoleh 40,53 g ekstrak etanol, kemudian 20 g diekstraksi cair-cair dengan n-heksan diperoleh fraksi n-heksan 6 g. KLT dengan fase gerak n-heksan:etilasetat perbandingan 80:20 merupakan fase gerak yang terbaik yaitu fase gerak dengan noda yang lebih banyak digunakan untuk menentukan fase gerak pada kromatografi kolom. Kandungan kimia fraksi n-heksan 6 g dipisahkan secara kromatografi cair vakum dengan menggunakan fase gerak secara landaian yaitu
n-heksan:etilasetat dengan perbandingan 100:0, 95:5, 90:10, 85:15, 80:20, 75:25,
kromatografi kolom secara isokratik dengan fase gerak n-heksan:etilasetat (80:20) sehingga diperoleh 85 vial. Masing-masing fraksi dikromatografi lapis tipis dengan fase gerak n-heksan:etilasetat (80:20) dengan penampak bercak Lieberman-Burchard. Kromatogram yang baik terdapat pada fraksi 10-14.
Pada fraksi 10-14 dilakukan kromatografi lapis tipis preparatif, dengan fase gerak n-heksan:etilasetat (80:20), fase diam silika gel GF 254 dan penampak bercak Liebermann-Burchard. Hasil kromatografi lapis tipis preparatif yang berwarna merah ungu ada 2 pita, masing-masing dikerok dan direndam selama satu malam dalam metanol kemudian disaring dan diuapkan, selanjutnya dicuci dengan metanol dingin sehingga diperoleh kristal yang berwarna putih yang berupa isolat
murni. Terhadap isolat dilakukan KLT dua arah dengan fase gerak I
n-heksan:etilasetat (80:20) dan fase gerak II toluen:etilasetat (90:10). Isolat
menunjukkan satu noda warna merah ungu harga Rf 0,35 dengan fase gerak II bukti bahwa adanya triterpenoid.
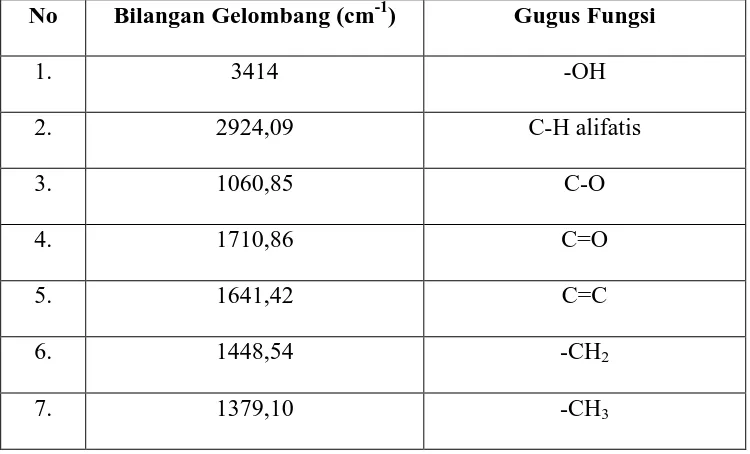
(CH3). Adanya puncak tajam pada bilangan gelombang 1710,86 cm-1 menunjukkan adanya gugus C=O yang diduga berasal dari senyawa ester karena diperkuat oleh puncak pada bilangan gelombang 1060,85 cm-1 menunjukkan ikatan C-O, pada bilangan gelombang 1641,42 cm-1 menunjukkan adanya gugus C=C, dicocokkan dengan melihat CH-alifatis pada bilangan gelombang 2924,09 cm-1 yang berada di sebelah kanan dari bilangan gelombang 3000 cm-1, dapat dilihat pada Tabel 4.3.
Tabel 4.3 Hasil spektrofotometer infrared
No Bilangan Gelombang (cm-1) Gugus Fungsi
1. 3414 -OH
2. 2924,09 C-H alifatis
3. 1060,85 C-O
4. 1710,86 C=O
5. 1641,42 C=C
6. 1448,54 -CH2
BAB V
KESIMPULAN DAN SARAN
5.1Kesimpulan
a. Golongan senyawa kimia simplisia pucuk labu siam (Sechii edulei herba) adalah flavonoid, steroid/triterpenoid, tanin, glikosida, dan saponin.
b. Hasil karakterisasi simplisia pucuk labu siam (Sechii edulei herba) diperoleh kadar air 3,99%, kadar sari yang larut dalam air 33,45%, kadar sari yang larut dalam etanol 10,09%, kadar abu total 4,13% dan kadar abu yang tidak larut dalam asam 0,96%.
c. Hasil spektrofotometer sinar ultraviolet isolat memberikan panjang gelombang maksimum 207,5 nm. Hasil spektrofotometer sinar infrared menunjukkan adanya gugus –OH, C-H alifatis, C=O, C=C, -CH2, -CH3 dan C-O menunjukkan adanya senyawa triterpenoid.
5.2 Saran
DAFTAR PUSTAKA
Anonim1. (2010). Khasiat/Manfaat Jipang atau Labu Siam (Sechium edule). Theodoradessy.Blogdetik.com/index.php/2010/11/khasiat–manfaat- jipang-atau-labu-siem-sechium-edule. Diakses tanggal 14 Mei 2012. Anonim2. (2012). Manfaat Labu Siam.
Diakses tanggal 15 Juli 2012.
Anonim3. (2011). Tanin. www.nadjeeb.wordpress.com. Diakses tanggal 26 Juli 2012.
Anonim4. (2011). Alkaloid.
http://asia-musfikah.blogspot.com/2011/10/alkaloid.html. Diakses tanggal 26 Juli 2012.
Depkes. (1999). Cara Pengelolaan Simplisia yang Baik. Jakarta: Direktorat Jenderal Pengawasan Obat dan Makanan. Hal. 3-4.
Depkes. (1979). Materia Medika Indonesia. Jilid III. Jakarta: Direktorat Jenderal Pengawasan Obat dan Makanan. Hal. 134-135, 141.
Depkes. (1986). Sediaan Galenik. Jakarta: Departemen Kesehatan RI. Hal. 10, 19, 21.
Depkes. (1989). Materia Medika Indonesia. Jilid V. Jakarta: Direktorat Jenderal Pengawasan Obat dan Makanan. Hal. 41-45.
Depkes. (1995). Materia Medika Indonesia. Jilid VI. Jakarta: Departemen Kesehatan RI. Hal. 300-304, 306.
Depkes. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Departemen Kesehatan RI. Hal. 1-11.
Farnsworth, N.R. (1966). Biological and