PEMANFAATAN ARANG SEKAM PADI SEBAGAI ADSORBEN
UNTUK MENURUNKAN KADAR BESI DALAM AIR SUMUR
SKRIPSI
CRISMASLY SITANGGANG
070822002
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PEMANFAATAN ARANG SEKAM PADI SEBAGAI ADSORBEN UNTUK MENURUNKAN KADAR BESI DALAM AIR SUMUR
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
CRISMASLY SITANGGANG 070822002
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PEMANFAATAN ARANG SEKAM PADI SEBAGAI ADSORBEN UNTUK MENURUNKAN KADAR BESI DALAM AIR SUMUR
Kategori : SKRIPSI
Nama : CRISMASLY SITANGGANG
Nomor Induk Mahasiswa : 070822002
Program Studi : SARJANA (S1) KIMIA EKSTENSI Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Agustus 2010
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Drs. Chairuddin, M.Sc Drs. Saut Nainggolan
NIP : 195912311987011001 NIP : 194701251974031001
Diketahui/Disetujui oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PEMANFAATAN ARANG SEKAM PADI SEBAGAI ADSORBEN UNTUK MENURUNKAN KADAR BESI DALAM AIR SUMUR
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Agustus 2010
PENGHARGAAN
Segala puji, hormat serta syukur penulis ucapkan kepada Tuhan Yesus Kristus, atas kasih karuniaNYA dalam setiap pimpinanNYA dalam setiap detik kehidupan penulis. Sesungguhnya kesanggupan penulis dalam menyelesaikan penelitian dan penyusunan skripsi ini hanya karena campur tangan Tuhan sehingga penulis dapat mengerjakan apa yang menjadi tugas dan tanggung jawab penulis dalam mencapai gelar Sarjana Sains.
Ucapan terima kasih saya sampaikan kepada Bapak Drs.Saut Nainggolan selaku Pembimbing 1 dan Bapak Drs.Chairuddin selaku Pembimbing 2 yang telah meluangkan waktunya untuk memberikan bimbingan dan saran kepada penulis selama melakukan penelitian dan penyusunan skripsi ini dan kepada Bapak Prof Harlem Marpaung selaku Kepala Laboratorium bidang Kimia Analitik FMIPA USU yang telah memberikan saran-saran kepada penulis. Ucapan terima kasih juga ditujukan kepada Ketua dan Sekretaris Departemen KIMIA FMIPA USU, Ibu Dr. Rumondang Bulan Nst,M.Sc dan Bapak Drs.Firman Sebayang,MS. Kepada semua Dosen Departemen Kimia FMIPA USU yang telah membimbing penulis selama mengikuti perkuliahan di FMIPA USU Medan. Kepada laboran Seri Mawarni dan Sri Pratiwi Aritonang, seluruh asisten Laboratorium Kimia Analitik, teman- teman stambuk 2007, seluruh elemen KMKS, KTB Manna, KPA Rajawali dan teman-teman satu kost. Akhirnya penulis mengucapkan terima kasih kepada orang tua yang terkasih Bapak Drs. Dj Sitanggang, Mama R. Sipayung, Keluarga Bang Juni dan Kak Yani, Ade Olive, Kak Ister dan Bang Moan untuk dukungan doa, materi dan motivasi kepada penulis.
Penulis menyadari bahwa skripsi ini masih banyak kekurangan, karena keterbatasan penulis baik dalam literatur maupun pengetahuan. Oleh karena itu, Penulis mengharapkan kritik dan saran yang membangun demi kesempurnaan skripsi ini, semoga skripsi ini bermanfaat bagi kita semua.
Medan, Agustus 2010
ABSTRAK
The Application Of Rice Husk Charcoal As Adsorbent For Reducing
Iron Contents Of Well Water
ABSTRACT
DAFTAR ISI
Halaman
PERSETUJUAN ii
PERNYATAAN iii
PENGHARGAAN iv
ABSTRAK v
ABSTRACT vi
DAFTAR ISI vii
DAFTAR TABEL ix
DAFTAR GAMBAR x BAB 1 PENDAHULUAN 1
1.1Latar Belakang 1 1.2Permasalahan 2 1.3Pembatasan Masalah 3 1.4Tujuan Penelitian 3
1.5Manfaat Penelitian 3
1.6Lokasi Penelitian 3
1.7Metodologi Penelitian 4 BAB 2 TINJAUAN PUSTAKA 5 2.1 Padi 5 2.2 Sekam Padi 6 2.2.1 Komposisi Sekam Padi dan Abu Sekam Padi 7 2.2.2 Pemanfaatan Sekam Padi di Bidang Industri 7 2.3 Persyaratan Kualitas Air 8 2.3.1 Persyaratan Fisika 8 2.3.2 Persyaratan Kimia 9
2.4 Air Tanah 10
2.5 Senyawa Besi dalam Air 11
2.6 Arang Aktif 12
2.7 Adsorpsi 14
2.7.1 Adsorpsi Zat Terlarut oleh Zat Padat 14
2.7.2 Jenis-Jenis Adsorpsi 15
2.7.3 Faktor-Faktor yang Mempengaruhi Adsorpsi 15
2.8 Spektrofotometri 16
BAB 3 BAHAN DAN METODE PENELITIAN 18
3.1 Alat – Alat 18
3.2 Bahan – Bahan 18
3.3 Prosedur Penelitian 19
3.3.1 Pembuatan Pereaksi dan Larutan Standar untuk Penentuan Besi 19
3.3.3 Penentuan Panjang Gelombang Maksimum 20
3.3.4 Pembuatan Kurva Kalibrasi 20
3.3.5 Pembuatan Arang Aktif 21
3.3.6 Penentuan Besi (Fe) dari Sampel secara Spektrofotometri 21
3.3.7 Penentuan Besi (Fe) dari Sampel setelah Dilewatkan Adsorben 22
3.4 Bagan Penelitian 23
3.4.1 Pembuatan Arang Aktif 23
3.4.2 Penentuan Besi (Fe) dari Air Sumur 24
3.4.3 Penentuan Besi (Fe) dari Air Sumur setelah Dilewatkan Adsorben25 BAB 4 HASIL DAN PEMBAHASAN 26
4.1 Hasil Penelitian 26
4.2 Pengolahan Data 26
4.2.1 Penurunan Persamaan Garis Regresi dengan Metode Kurva Kalibrasi 26
4.2.2 Penurunan Persamaan Garis Regresi 27
4.2.3 Koefisien Korelasi 28
4.2.4 Penentuan Batas Deteksi 30
4.2.5 Penentuan Kadar Besi dari Sampel 31
4.2.6 Penentuan Deviasi Standar 34
4.2.7 Penentuan Persen Penurunan Kadar Besi dari Sampel 35
4.3 Pembahasan 37
BAB 5 KESIMPULAN DAN SARAN 41
5.1 Kesimpulan 41
5.2 Saran 41
DAFTAR PUSTAKA 42
DAFTAR TABEL
Halaman
Tabel 1 Hasil Penentuan Kadar Besi dari Sampel Air Sumur Gali dan Air Sumur Bor sebelum dan setelah Dilewatkan Adsorben dan Penentuan
Kadar Besi 26
Tabel 2 Hasil Pengukuran % Transmitansi/Absorbansi Logam Besi sebelum
Dilewatkan Adsorben 31 Tabel 3 Hasil Pengukuran % Transmitansi/Absorbansi Logam Besi setelah
Dilewatkan Adsorben 32 Tabel 4 Kadar Besi dari Air Sumur Bor sebelum dan setelah Dilewatkan
Adsorben 36
Tabel 5 Kadar Besi dari Air Sumur Gali sebelum dan setelah Dilewatkan
Adsorben 36
Tabel 6 Penentuan Panjang gelombang Maksimum dari Larutan Standar
DAFTAR GAMBAR
Halaman
Gambar 1 Penentuan Panjang Gelombang Maksimum dari Larutan
ABSTRAK
The Application Of Rice Husk Charcoal As Adsorbent For Reducing
Iron Contents Of Well Water
ABSTRACT
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Hingga saat ini padi masih merupakan produk utama pertanian dinegara agraris
termasuk Indonesia, hal ini disebabkan oleh kenyataan bahwa beras merupakan bahan
makanan pokok. Sekam padi merupakan salah satu produk samping dari proses
penggilingan padi, selama ini hanya menjadi limbah dan belum dimanfaatkan secara
optimal. Sekam padi merupakan lapisan keras yang terdiri dari dua bentuk daun, yaitu
sekam kelopak dan sekam mahkota. Saat proses penggilingan padi, sekam akan
terpisah dari butiran beras dan menjadi bahan sisa/limbah dari penggilingan padi.
Dari penggilingan padi akan menghasilkan sekitar 25% sekam, 8% dedak, 2% bekatul
& 65% beras. (Haryadi. 2006)
Ditinjau dari komposisi kimia, sekam padi mengandung beberapa unsur kimia
penting yaitu kadar air (9,02%), protein kasar (3,03%), lemak (1,18%), serat kasar
(35,68%), abu (17,17%) dan karbohidrat (33,71%). (Houston.1972)
Hasil pembakaran sekam padi dapat menghasilkan arang yang dinamakan
arang sekam padi, dapat dimanfaatkan untuk berbagai keperluan diantaranya sebagai
bahan baku untuk industri kimia, bahan bangunan, sebagai adsorben logam-logam
berat seperti Pb, Cd, Cr, Fe dalam air.
(http://Penggunaan-arang-sekam-padi.htmL.aditbayore.blogspot.com)
Besi merupakan salah satu elemen kimia yang dapat ditemui hampir disetiap
tempat dibumi/semua lapisan geologis. Umumnya besi yang terdapat dalam air dapat
bersifat terlarut sebagai Fe2+dan Fe3+, sebagai butiran koloidal dalam bentuk senyawa
Fe(OH)3, Fe2O3, FeO dan bergabung dengan zat anorganik seperti tanah liat.
(lumpur dan pasir halus) maupun bahan organik yang berupa plankton dan
mikroorganisme lain. Salah satu masalah dari air sumur yaitu tingginya kandungan
besi, jika air sumur tersebut didiamkan dalam bak penampungan maka secara perlahan
akan berubah warnanya menjadi kuning atau kelihatan keruh karena Fe2+ teroksidasi
oleh udara menjadi Fe2O3. (Alaerts.1984)
Berbagai macam bahan baku dapat digunakan untuk menghasilkan arang aktif
yaitu bahan yang mengandung karbon, antara lain berbagai jenis kayu, serbuk gergaji,
kulit atau biji buah-buahan, batu bara, tongkol jagung, tempurung kelapa, sekam padi
dan lain-lain. Dari semua bahan baku ini ada kalanya dapat langsung diproses sebagai
arang aktif dan ada pula yang melalui proses aktivasi. Cara mengaktifkan yaitu dngan
memakai gas pengoksidasi seperti udara atau karbondioksida dan karbonasi bahan
baku dengan memakai pelarut kimia seperti seng klorida atau asam fosfat.
(Kusnaedi, 2010)
Dari hasil penelitian terdahulu, telah dilakukan pembuatan arang aktif dari
sekam kayu dengan menggunakan asam fosfat sebagai aktivator. Peneliti terdahulu
juga telah melakukan penelitian tentang pemakaian berbagai aktivator dalam
pembuatan arang aktif dan diperoleh bahwa asam fosfat merupakan aktivator yang
baik karena lebih efektif untuk menghasilkan arang aktif dengan daya serap yang
tinggi, bila dibandingkan dengan aktivator lain seperti H2SO4, NaOH, senyawa
khlorida dan lain-lain. (Silalahi.1996)
Berdasarkan hasil penelitian tersebut, peneliti tertarik untuk memanfaatkan
sekam padi sebagai adsorben dengan menggunakan aktivator asam fosfat dan
diaplikasikan untuk menurunkan kadar besi dalam air sumur.
1.2 Permasalahan
Berapa besar kemampuan arang aktif dari sekam padi untuk menurunkan logam Besi
1.3 Pembatasan Masalah
Dalam penelitian ini, penulis memberikan batasan masalah sebagai berikut :
1. Bahan baku yang digunakan dalam pembuatan arang aktif yaitu dari sekam
padi.
2. Parameter yang dianalisis yaitu menurunkan kadar besi secara
spektrofotometri.
3. Perlakuan sampel dilakukan sebelum dan setelah dilewatkan dari kolom,
dalam hal ini fase diam adalah arang aktif dari sekam padi dan fase geraknya
adalah sampel. Sampel yang akan dianalisis yaitu air sumur bor dan air sumur
gali.
1.4 Tujuan
Penelitian ini bertujuan untuk menentukan persen penurunan kadar Besi dari sampel
dengan memanfaatkan sekam padi sebagai adsorben.
1.5 Manfaat
Dari hasil penelitian yang dilakukan dapat memberikan informasi tentang
pemanfaatan sekam padi bagi masyarakat sehingga tidak hanya sekedar limbah yang
akan dijadikan sebagai pupuk untuk tanaman, namun dapat bermanfaat sebagai
adsorben yaitu untuk menurunkan kadar Besi dalam air sumur.
1.6 Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Analitik Fakultas Matematika dan
1.7 Metodologi Penelitian
Penelitian ini merupakan eksperimen laboratorium, dilakukan dengan cara :
1. Penyediaan Bahan Baku sebagai Adsorben
Sekam padi diambil dari pabrik kilang padi di daerah Setia Budi, pemanfaatan sekam
padi sebagai adsorben dengan menggunakan aktivator asam fosfat. Dilakukan
perendaman selama 24 jam, dilakukan pengarangan didalam tanur pada suhu 500°C
selama 4 jam. Sekam padi yang diolah lebih lanjut menjadi arang aktif di ayak dengan
ukuran partikel 80 mesh. Penurunan kadar Besi dari air sumur yaitu dengan
melewatkan air sumur melalui kolom yang berisi arang aktif dari sekam padi dan
dibiarkan selama 1 jam (arang aktif sebagai fase diam dan air sumur sebagai fase
gerak ). Penentuan kadar Besi (Fe) dilakukan dengan metode spektrofotometri.
2. Pengambilan Sampel
Sampel air sumur bor dan air sumur gali diambil dari perumahan penduduk di jalan
Sempurna pasar 7 Tembung – Bandar Kalippa. Kedalaman sumur bor 30 m dan sumur
gali 9 m. Pengambilan sampel air sumur bor dan air sumur gali masing-masing
dilakukan dari 3 titik pengambilan. Pengambilan sampel air sumur bor diambil
langsung dari kran/mulut pompa, ditampung kira-kira lima menit setelah air mulai
dibuang (dikeluarkan), pengambilan dilakukan berdasarkan variasi waktu yaitu
dengan selang waktu 1 jam untuk setiap pengambilan. Pengambilan air sumur gali
yaitu secara sembarang sebanyak 3 kali pengambilan. Masing-masing sampel air
sumur bor dan air sumur gali yang telah diambil dari 3 titik pengambilan dicampur
BAB 2
TINJAUAN PUSTAKA
2.1 Padi
Padi merupakan produk utama pertanian dinegara agraris termasuk Indonesia, hal ini
disebabkan oleh kenyataan bahwa beras merupakan hasil olahan dari padi yang
merupakan bahan makanan pokok. Tumbuhan padi adalah tumbuhan yang tergolong
tanaman air, namun sebagai tanaman air bukan berarti tanaman padi itu hanya bisa
tumbuh di tanah yang terus - menerus digenangi air, baik penggenangan itu terjadi
secara alamiah, ditanah rawa-rawa, maupun penggenangan itu disengaja pada
tanah-tanah sawah. Tanaman padi juga dapat tumbuh ditanah-tanah daratan atau tanah-tanah kering
asalkan curah hujan mencukupi kebutuhan tanaman akan air. (Siregar.1981)
Klasifikasi Ilmiah Kingdom Plantae
Ordo Poales
Famili Poaceae
Genus Oryza
Spisies O. sativa
Nama Binomial
2.2 Sekam Padi
Sekam padi adalah bagian terluar dari butir padi yang merupakan hasil samping saat
proses penggilingan padi dilakukan. Sekitar 20% dari bobot padi adalah sekam padi
dan kurang lebih 15% dari komposisi sekam padi adalah abu sekam yang selalu
dihasilkan setiap kali sekam dibakar. (Hara. 1986)
Sekam padi merupakan lapisan keras yang meliputi kariopsis yang terdiri dari
dua bentuk daun yaitu sekam kelopak dan sekam mahkota, dimana pada proses
penggilingan padi, sekam akan terpisah dari butir beras dan menjadi bahan sisa atau
limbah penggilingan. Dari penggilingan padi akan menghasilkan sekitar 25% sekam,
8% dedak, 2% bekatul dan 65% beras. Sekam tersusun dari jaringan serat-serat
selulosa yang mengandung banyak silika dalam bentuk serabut-serabut yang sangat
keras. Pada keadaan normal, sekam berperan penting melindungi biji beras dari
kerusakan yang disebabkan oleh serangan jamur secara tidak langsung, melindungi
biji dan juga menjadi penghalang terhadap penyusupan jamur. Selain itu sekam juga
dapat mencegah reaksi ketengikan karena dapat melindungi lapisan tipis yang kaya
minyak terhadap kerusakan mekanis selama pemanenan, penggilingan dan
pengangkutan. ( Haryadi. 2006 )
Sekam padi menduduki 7% dari produksi total padi yang biasanya hanya
ditimbun dekat penggilingan padi sebagai limbah sehingga mencemari lingkungan,
kadang-kadang juga dibakar. Sekam padi juga dapat digunakan sebagai pupuk, bahan
tambahan untuk media tumbuh tanaman sayuran secara hidroponik. Penumpukan
sekam padi ditanah dapat membantu mempercepat proses dalam peningkatan hasil
tanaman. Hasil analisis sekam padi adalah sebagai berikut:
Pemanfaatan sekam padi secara tidak langsung dapat memperbaiki sifat fisik
tanah karena dapat mempengaruhi sifat fisika, kimia dan biologi tanah. Pengaruh
utama terhadap struktur tanah yaitu berhubungan dengan pemadatan, aerasi dan
perkembangan akar. Apabila persentase kandungan sekam padi berkurang/menurun
maka konsekuensinya terjadi penurunan aerasi yang akan menghambat perkembangan
akar, menurunkan kemampuan akar untuk menyerap dan menghambat aktivitas
mikroorganisme. (Sutanto.2002)
2.2.1 Komposisi Sekam Padi dan Abu Sekam Padi
(Luh.1991)
2.2.2 Pemanfaatan Sekam Padi di Bidang Industri
a. Sumber Silika
Sekitar 20% silika dalam sekam padi merupakan suatu sumber silika yang cukup
tinggi, silika dari sekam merupakan saingan dari sumber silika lain seperti pasir,
bentonit dan tanah diatomae tetapi biasanya silika dari sekam padi mempunyai
keuntungan karena jumlah elemen lain (pengotor) yang tidak diinginkan adalah sangat
Komposisi Kulit Padi
Air, % 7,6 – 10,2 Protein Kasar, % 1,9 – 3,7 Lemak Kasar, % 0,3 – 0,8 Serat Kasar, % 35,0 – 46,0 Karbohidrat, % 26,5 – 29,8 Abu, % 13,2 – 21,0 Silika, % 18,0 – 22,3 Kalsium, mg/g 0,6 – 1,3 Fosfor, mg/g 0,3 – 0,7 Serat murni pencuci, % 66,0 – 74,0 Serat asam pencuci, % 58,0 – 62,0 Lignin, % 9,0 – 20,0 Selulosa, % 28,0 – 36,0 Pentosa, % 21,0 – 22,0 Hemiselulosa, % 12,0
sedikit dibandingkan jumlah silikanya. Silika diperoleh dari pembakaran sekam untuk
menghasilkan abu atau secara ekstraksi sebagai natrium – silikat dengan larutan alkali.
b. Pemurnian Air
Pemanfaatan sekam antara lain sebagai sumber energi, abu gosok yaitu untuk
keperluan rumah tangga, bahan pencampur untuk pembuatan semen portland dalam
bidang industri, selain itu untuk menjernihkan air. Pemanfaatan sekam padi untuk
menjernihkan air yaitu melalui proses filtrasi/penyaringan partikel, koagulasi dan
adsorpsi. Akan tetapi karbon yang terkandung didalam sekam padi berfungsi sebagai
koagulan pembantu dengan menyerap atau menurunkan logam – logam pada air yang
tercemar.
c. Bahan Bakar
Pembakaran merupakan satu metode yang umum dan sering digunakan dalam proses
akhir pengolahan sekam padi. Sekam padi yang dibakar secara langsung untuk
meneruskan aliran uapnya atau digunakan didalam generator untuk menghasilkan
tenaga penguat dengan minyak ter yang memiliki nilai bahan bakar.
d. Bahan Bangunan
Manfaat sekam padi sebagai bahan bangunan berhubungan dengan pengerasan balok,
batu bata, ubin, batu tulis dan sifat lunak. (Luh.1991)
2.3 Persyaratan Kualitas Air
2.3.1 Persyaratan Fisika
Air yang berkualitas harus memenuhi persyaratan fisika sebagai berikut:
a. Jernih atau Tidak Keruh
Air yang keruh disebabkan oleh adanya butiran-butiran koloid dari tanah liat, semakin
b. Tidak Berwarna
Air untuk keperluan rumah tangga harus jernih, air yang berwarna berarti
mengandung bahan-bahan lain yang berbahaya bagi kesehatan.
c. Rasanya Tawar
Secara fisika, air bisa dirasakan oleh lidah, air yang terasa asam, manis, pahit atau asin
menunjukkan air tersebut tidak baik. Rasa asin disebabkan adanya garam-garam
tertentu yang larut dalam air sedangkan rasa asam diakibatkan adanya asam organik
maupun asam anorganik.
d. Tidak Berbau
Air yang baik memiliki ciri tidak berbau bila dicium dari jauh maupun dari dekat. Air
yang berbau busuk mengandung bahan organik yang sedang mengalami dekomposisi
(penguraian) oleh mikroorganisme air.
e. Temperaturnya Normal
Air yang baik harus memiliki temperatur sama dengan temperatur udara
(20-26°C). Air yang sudah tercemar mempunyai temperatur di atas atau di bawah
temperatur udara. (Kusnaedi.2010)
2.3.2 Persyaratan Kimia
Kualitas air tergolong baik bila memenuhi persyaratan kimia sebagai berikut :
a. pH Netral
Derajat keasaman air minum harus netral, tidak boleh bersifat asam atau basa. Air
murni mempunyai pH=7 apabila pH<7 berarti air bersifat asam sedangkan pH>7
b. Tidak Mengandung Zat Kimia Beracun
Air yang berkualitas baik tidak mengandung bahan kimia beracun seperti sianida,
sulfida dan fenolik.
c. Tidak Mengandung Garam atau Ion-Ion Logam
Air yang berkualitas baik tidak mengandung garam atau ion logam seperti Fe, Mg, Ca,
K, Hg, Zn, Mn, Cl dan Cr.
d. Kesadahan Rendah
Tingginya kesadahan berhubungan dengan garam-garam yang terlarut di dalam air
terutama Ca dan Mg.
e. Tidak Mengandung Bahan Organik
Kandungan bahan organik dalam air dapat terurai menjadi zat-zat yang berbahaya
bagi kesehatan. Bahan-bahan organik itu seperti NH4, H2S, SO42- dan NO3.
(Kusnaedi.2010)
2.4 Air Tanah
Air tanah merupakan air yang berada di bawah permukaan tanah, pergerakan air tanah
sangat lambat dengan kecepatan arus berkisar antara 10ˉ 10-10ˉ3m/detik dan
dipengaruhi oleh porositas, permeabilitas dari lapisan tanah. Pada dasarnya air tanah
dapat berasal dari air hujan baik melalui proses infiltrasi secara langsung ataupun
tidak langsung dari air sungai, danau, rawa dan genangan air lainnya. Kemampuan
tanah dan batuan untuk menahan air tergantung pada sifat porositas dan permeabilitas
tanah. Air tanah biasanya memiliki kandungan besi relatif tinggi, jika air tanah
mengalami kontak dengan udara dan mengalami oksigenasi, ion ferri pada ferri
hidroksida yang banyak terdapat dalam air tanah akan teroksidasi menjadi ion ferro
dan akan mengalami presipitasi (pengendapan) serta membentuk warna kemerahan
pada air. Oleh karena itu sebelum digunakan untuk berbagai peruntukkan, sebaiknya
mengendapkan besi. Perlakuan ini bertujuan untuk menurunkan kadar karbondioksida
dan menaikkan kadar oksigen terlarut. (Hefni.2003)
Adapun keadaan/sifat dari air sumur gali, dengan ketinggian air bebas
umumnya sekitar 1-3 m dari dasar sumur yaitu tergantung dari jumlah air yang
diambil dan musim. Rasa dan warna air tergantung jenis tanah yang ada, tanah sawah
airnya kekuning-kuningan, tanah berpasir airnya jernih dan rasanya sejuk, tanah liat
airnya terasa sedikit sepat. Air sumur gali mudah tercemar oleh karena kelalaian
dalam menutup mulut sumur dan mengandung bakteri cukup banyak. Keadaan/sifat
air sumur bor yaitu airnya jernih dan rasanya sejuk, jumlah bakteri jauh lebih kecil
dari pada air sumur gali. Tanah berpasir biasanya memiliki kedalaman 30-40 m sudah
memperoleh air dan biasanya airnya naik sampai 5-7 m dari permukaan tanah
sedangkan tanah liat dengan kedalaman 40-60 m akan diperoleh air yang baik dan
airnya naik mencapai 7 m dari permukaan tanah. (Gabriel.1987)
2.5 Senyawa Besi dalam Air
Perairan yang mengandung besi tidak diinginkan untuk keperluan rumah tangga,
karena dapat menyebabkan bekas karat pada pakaian, porselin dan alat-alat lainnya
serta menimbulkan rasa yang tidak enak untuk air minum. Adapun sifat kimia perairan
antara lain sifat redoks, pembentukan kompleks, metabolisme oleh mikroorganisme.
Besi (II) sebagai ion berhidrat dapat larut, merupakan jenis besi yang terdapat dalam
air tanah, karena air tanah tidak berhubungan dengan oksigen dari atmosfer, konsumsi
oksigen bahan organik dalam media mikroorganisme akan menghasilkan keadaan
reduksi dalam air tanah. Oleh karena itu, besi dengan bilangan oksidasi rendah yaitu
Fe(II) umumnya ditemukan dalam air tanah dibandingkan Fe(III). Secara umum Fe(II)
terdapat dalam air tanah berkisar antara 1,0-10 mg/L, dalam kondisi tidak ada oksigen
air tanah mengandung Fe(II) jernih tetapi saat mengalami oksidasi oleh oksigen yang
berasal dari atmosfer ion ferro akan berubah menjadi ion ferri dengan reaksi sebagai
berikut :
dan air menjadi keruh, pada pembentukan Fe(III) oksidasi terhidrat yang tidak larut
akan menyebabkan air berubah menjadi abu-abu. (Achmad.2004 )
Kadar besi pada perairan yang mendapat cukup aerasi (aerob) hampir tidak
pernah lebih dari 0,3 mg/liter, kadar besi pada perairan alami berkisar
0,05-0,2 mg/liter. Pada air tanah dengan kadar oksigen yang rendah, kadar besi dapat
mencapai 10-100 mg/liter. Kadar besi >1,0 mg/liter dianggap membahayakan
kehidupan organisme akuatik. Air yang diperuntukkan untuk air minum sebaiknya
memiliki kadar besi kurang dari 0,3 mg/L. (Hefni.2003)
Besi dan mangan sering menjadi masalah dalam penyediaan air untuk
kebutuhan rumah tangga terutama kalau sumbernya adalah air tanah. Dalam tanah, Fe
terdapat sebagai Fe2O3 atau sebagai FeS2 yang sifatnya sukar larut dan adakalanya
terdapat sebagai FeCO3 yang juga sukar larut. Kekeruhan dan warna kuning yang
terdapat di air terbentuk karena oksidasi Fe (II) menjadi Fe (III) berupa endapan
koloid berwarna kuning. Dalam kisaran pH 6–9 kelarutan Fe (II) dipengaruhi oleh
kelarutan senyawa karbonatnya, bukan oleh senyawa hidratnya. Senyawa Fe(III)
terdapat dalam air sebagai Fe(OH)3, FeOOH. Konstanta pembentukan
senyawa-senyawa Fe(III) yang larut dalam air seperti FeOH2+, Fe(OH)2+, Fe2(OH)24+ dan
Fe(OH)4-. (Fair.1968)
2.6 Arang Aktif
Arang aktif adalah karbon amorf yang telah mendapat perlakuan dengan uap dan
panas sampai mempunyai afinitas yang kuat untuk menyerap berbagai bahan. Arang
aktif mempunyai luas permukaan yang sangat besar, berkisar 300 sampai 2500 m2/g
dan dapat digunakan untuk menyerap hampir semua jenis pelarut organik pada suhu
sekitar 35°C. Berbagai bahan berkarbon seperti kokas migas (petroleum), serbuk
gergaji, lignit batu bara, gambut, kayu, arang batok dan biji-bijian buah dapat
digunakan untuk membuat arang aktif. Sifat-sifat bahan tidak hanya bergantung pada
memecahkan ikatan hidrokarbon atau mengoksidasi molekul-molekul permukaan
sehingga arang mengalami perubahan sifat, baik fisika maupun kimia yaitu luas
permukaan bertambah besar dan berpengaruh terhadap daya adsorpsi. Bahan baku
yang digunakan di rendam dengan bahan kimia, lalu dikeringkan dan dikarbonisasi
pada suhu sampai 850°C. Aktivator yang digunakan antara lain hidroksida logam
alkali, garam-garam karbonat, klorida, sulfat dan khususnya ZnCl2, asam-asam
anorganik seperti H2SO4 dan H3PO4. (Austin.1996)
Arang aktif adalah sejenis adsorben (penyerap) yang berwarna hitam dan
berbentuk granula, bulat, pelet atau bubuk. Arang aktif dipakai dalam proses
pemurnian udara, gas, larutan atau cairan, penyerap rasa dan bau dari air,
menghilangkan senyawa-senyawa organik dalam air. Hanya dengan 1 g arang aktif
akan didapatkan suatu material yang memiliki luas permukaan sekitar 500 m2. Dengan
luas permukaan yang sangat besar, arang aktif memiliki kemampuan menyerap zat-zat
yang terkandung dalam air dan sangat efektif dalam menyerap zat terlarut dalam air
baik organik maupun anorganik. (Kusnaedi.2010)
Daya serap ditentukan oleh luas permukaan partikel dan kemampuan ini dapat
menjadi lebih tinggi jika terhadap arang dilakukan aktivasi dengan bahan-bahan kimia
atau dengan pemanasan pada suhu tinggi sehingga akan mengalami perubahan
sifat-sifat fisik dan kimia. Beberapa keuntungan arang aktif dibandingkan dengan
adsorben – adsorben lain yaitu:
a. Penyerapan yang dilakukan untuk proses pemisahan dan pemurnian umumnya
tanpa terlebih dahulu melakukan penghilangan kelembapan.
b. Karena luasnya untuk mencapai permukaan bagian dalam dapat menyerap dengan
banyak molekul non polar dan menyerap dengan lemah molekul-molekul polar
organik.
c. Panas adsorpsi atau kekuatan ikatan, pada arang aktif lebih rendah dibandingkan
penyerap yang lain karena kekuatan Vander Waals merupakan kekuatan utama
mudah dan membutuhkan energi yang lebih rendah untuk regenerasi arang aktif.
(Ralph. 2003)
2.7 Adsorpsi
Adsorpsi adalah peristiwa penyerapan suatu zat, ion atau molekul yang melekat pada
permukaan, dimana molekul dari suatu materi terkumpul pada bahan pengadsorpsi
atau adsorben. Sifat adsorpsi partikel koloid banyak dimanfaatkan dalam proses
penjernihan air atau pemurnian suatu bahan yang masih mengandung pengotor,
partikel koloid mempunyai permukaan luas sehingga mempunyai daya serap adsorpsi
yang besar. Terjadinya adsorpsi pada permukaan larutan disebabkan karena adanya
kekuatan atau gaya tarik – menarik antara atom atau molekul pada permukaan larutan.
Peristiwa penyerapan suatu zat pada permukaan zat lain disebut adsorpsi, zat yang
diserap disebut fase terserap sedangkan zat yang menyerap disebut adsorben.
Peristiwa adsorpsi disebabkan oleh gaya tarik molekul dipermukaan adsorben.
(Estein.2005)
2.7.1 Adsorpsi Zat Terlarut oleh Zat Padat
Arang merupakan adsorben yang paling banyak dipakai untuk menyerap zat-zat dalam
larutan, biasanya dipakai di pabrik untuk menghilangkan warna dari larutan.
Penyerapan zat dari larutan mirip dengan penyerapan gas oleh zat padat, penyerapan
bersifat selektif yang diserap hanya zat terlarut atau pelarut. Bila dalam larutan ada
dua zat atau lebih, zat yang satu akan diserap lebih kuat dari yang lain. Jumlah zat
yang diserap setiap berat adsorben, tergantung konsentrasi dan zat terlarut sehingga
bila adsorben sudah jenuh maka konsentrasi tidak lagi berpengaruh. Zat-zat terlarut
dapat diadsorpsi oleh zat padat, misalnya CH3COOH oleh arang aktif, NH3 oleh arang
2.7.2 Jenis Adsorpsi
Adsorpsi ada dua jenis yaitu adsorpsi fisika dan adsorpsi kimia, adsorpsi fisika
disebabkan oleh gaya Vander Waals pada permukaan adsorben, panas adsorpsi fisika
biasanya rendah dan lapisan yang terjadi pada permukaan adsorben lebih dari satu
molekul. Kesetimbangan adsorpsi reversibel dan cepat. Adsorpsi kimia atau adsorpsi
aktivasi terjadi reaksi antara zat yang diserap dan adsorben, lapisan molekul pada
permukaan adsorben hanya satu lapis dan panas adsorpsinya tinggi, pada adsorpsi ini
terjadi pembentukan senyawa kimia sehingga ikatannya lebih kuat.. Perbedaan antara
adsorpsi kimia dengan adsorpsi fisika kadang-kadang tidak jelas dan bayak
prinsip-prinsip adsorpsi fisika berlaku pada adsorpsi kimia. (Sukardjo.1984)
2.7.3 Faktor – Faktor yang Mempengaruhi Adsorpsi
Adapun faktor – faktor yang mempengaruhi adsorpsi antara lain :
a. Suhu dan Konsentrasi Zat Terlarut
Dengan bertambahnya suhu maka adsorpsi dari larutan akan berkurang, untuk
senyawa yang mudah menguap adsorpsi dilakukan pada suhu kamar dan jika
memungkinkan dengan suhu yang lebih rendah.
b. Jumlah Adsorben
Suatu adsorben yang mempunyai ukuran partikel yang seragam yaitu mempunyai luas
permukaan per satuan luas yang tetap sehingga banyaknya adsorbat yang diadsorpsi
sebanding dengan berat adsorben.
c. Kelarutan Adsorbat
Adsorpsi akan terjadi jika molekul dipisahkan dari pelarut dan diikat pada permukaan
karbon, dimana senyawa yang dapat larut yaitu yang mempunyai afinitas yang kuat
d. Pengadukan
Kecepatan adsorpsi tergantung pada jumlah pengadukan dalam sistem, pengadukan
dilakukan untuk memberi kesempatan pada partikel arang aktif untuk bersinggungan
dengan senyawa serapan.
e. Sifat Adsorben dan Luas Permukaan
Banyak senyawa yang dapat diadsorpsi oleh arang aktif namun kemampuan untuk
mengadsorpsi berbeda untuk masing-masing senyawa. Adsorpsi akan bertambah besar
sesuai dengan bertambahnya ukuran molekul serapan dari struktur yang sama. Makin
besar pori–pori adsorben maka adsorpsi molekul dari larutan akan terjadi dengan baik,
semakin luas permukaan adsorben maka semakin banyak molekul yang terserap.
(Alberty.1983 )
2.8 Spektrofotometri
Pengukuran kuantitatif dengan menggunakan spektrofotometer UV–Vis terdiri dari
beberapa tahap :
a. Pengukuran λ maks
Pengukuran ini ditentukan melalui pengukuran absorbansi atau transmitansi, hasil pengukuran ini jika di plotkan dalam kurva yaitu absorbansi Vs λ dan akan dihasilkan kurva absorpsi atau spektrum absorpsi dari zat tersebut. Sensitivitas pengukuran konsentrasi pada λ maks ditentukan pada kisaran T = 20 % s/d 80 %.
b. Penentuan Operating Time
Ditunjukkan pada saat mana larutan berwarna mencapai transmitansi minimum dan
absorbansi maksimum, hal ini dilakukan karena umumnya intensitas warna larutan
c. Pengukuran Transmitansi/Absorbansi untuk Satu Larutan Seri Standar yaitu untuk
Kurva Kalibrasi
Metoda ini mencakup pengukuran absorbansi/transmitansi dari satu larutan seri
standar dengan konsentrasi yang diperkirakan sedemikian sehingga konsentrasi analit
di dalam sampel berada pada range konentrasi larutan standar yang akan diukur.
Pengukuran ini dilakukan pada λ maks dan operating time yang telah ditentukan
sehingga persamaan untuk kurva kalibrasi yaitu plot absorbansi Vs konsentrasi.
d. Pengukuran Transmitansi/Absorbansi dari Larutan Sampel
Pengukuran terhadap sampel dilakukan dibawah kondisi yang sama seperti larutan
standar.
Jika transmitansi absorbansi dari sampel berada diluar range dari pada
transmitansi/absorbansi standar, maka ada dua hal yang diperhatikan yaitu :
a. Transmitansi sampel lebih besar (Absorbansi lebih kecil) dari pada larutan standar
yang konsentrasinya terkecil. Hal ini berarti konsentrasi analit dalam sampel
terlalu kecil (larutan ini terlalu encer, perlu dipekatkan terlebih dahulu).
b. Transmitansi sampel lebih kecil (Asbsorbansi lebih besar) dari pada larutan
standar yang konsentrasinya besar (larutan ini terlalu pekat, perlu diencerkan
terlebih dahulu). (Kenner.1979)
Spektrofotometer dikembangkan beberapa puluh tahun yang lalu untuk
keperluan para fisikawan dan kimiawan dalam mempelajari struktur molekul dan
mengembangkan teori molekul. Spektrofotometer absorbsi adalah suatu instrumen
untuk mengukur absorbsi/penyerapan cahaya dengan energi (panjang gelombang)
tertentu oleh suatu molekul/atom. Spektrofotometer juga banyak digunakan untuk
berbagai kegiatan seperti studi bahan lingkungan ataupun dapat juga digunakan untuk
mengontrol suatu proses kimiawi dalam perindustrian. Spektrofotometer dapat
digunakan untuk penentuan terhadap sampel yang berupa larutan dan uap.
BAB 3
BAHAN DAN METODE PENELITIAN
3.1. Alat-Alat
Alat – alat yang digunakan dalam penelitian ini adalah :
Nama Alat Merek 1. Spektrofotometer Spektronik 20 Milton Roy
2. Neraca analitis Mettler PM 400
3. Oven Fisher
4. Tanur Fisher
5. Hot plate stirer PMC
6. Alat-alat gelas Pyrex
7. Kolom Pyrex
8. Cawan penguap
9. Kertas saring Whatman 42
10. Statif
11. Klem
3.2. Bahan-Bahan
Bahan – bahan yang digunakan dalam penelitian ini adalah :
Nama Bahan Merek 1. Sekam padi
2. KMnO4 0,1 N p.a(E.Merck)
5. 1,10-Fenantrolin p.a(E.Merck)
6. NH2OH.HCl p.a(E.Merck)
7. HCl (p) p.a(E.Merck)
8. CH3COOH glasial p.a(E.Merck)
9. CH3COONH4 p.a(E.Merck)
3.3 Prosedur Penelitian
3.3.1 Pembuatan Pereaksi dan Larutan Standar untuk Penentuan Besi (Fe)
a. Larutan Standar Fe 1000 mg/L
Ditimbang 7,0161 g Fe(NH4)2(SO4)2.6H2O dimasukkan ke dalam labu takar 1000 mL,
dilarutkan dengan 50 mL akuades, ditambahkan secara perlahan-lahan 20 mL
H2SO4(p) ditambah setetes demi setetes KMnO4 0,1 N sampai terbentuk warna merah
muda pucat dan diencerkan sampai garis tanda dan dihomogenkan.
b. Larutan Hidroksilamin
Ditimbang 10 g NH2OH.HCl dan diencerkan dalam labu takar 100 mL sampai garis
tanda dan dihomogenkan.
c. Larutan 1,10 Fenantrolin
Ditimbang 0,1 g 1,10 fenantrolin monohidrat (C12H8N2.H2O) dilarutkan dalam
100 mL akuades, kemudian dipanaskan sampai 80º C (tidak sampai mendidih).
d. Larutan Buffer Amonium Asetat
Ditimbang 25 g NH4.C2H3O2 dilarutkan dengan 15 mL akuades dan ditambah 70 mL
asam asetat glasial, kemudian diencerkan di dalam labu takar 100 mL sampai garis
3.3.2 Pembuatan Larutan Seri Standar Fe 0,2 ; 0,4 ; 0,6 ; 0,8 dan 1,0 mg/L
Dipipet 10 mL larutan standar Fe 1000 mg/l, dimasukkan kedalam labu takar 100 mL
dan diencerkan sampai garis tanda dan dihomogenkan sehingga diperoleh larutan
standar 100 mg/l. Dipipet 10 ml larutan standar Fe 100 mg/l, dimasukkan kedalam
labu takar 100 mL dan diencerkan sampai garis tanda dan dihomogenkan, sehingga
diperoleh larutan standar 10 mg/l. Dipipet sebanyak 1, 2, 3, 4 dan 5 mL dari larutan
standar 10 mg/l dan dimasukkan ke dalam masing-masing labu takar 50 mL,
kemudian diencerkan dengan akuades sampai garis tanda dan dihomogenkan.
3.3.3 Penentuan Panjang Gelombang Maksimum ( λ maks )
Dipipet 3 mL larutan standar Fe 10 mg/L, diencerkan dalam labu takar 50 mL sampai
garis tanda dan dihomogenkan. Dimasukkan kedalam erlenmeyer 150 mL ditambah 2
mL HCl (p) , ditambah 1 mL NH2OH.HCl , di didihkan diatas hotplate sampai
volumenya ½ dari volume awal, didinginkan dan ditambah 10 mL buffer amonium
asetat dan 2 mL 1,10-Fenantrolin , sehingga diperoleh larutan berwarna merah orange.
Didiamkan selama 10 menit dan selanjutnya diukur absorbansi larutan dengan
spektrofotometer spektronik 20 dari panjang gelombang 480, 490, 500, 510, 520, 530
dan 540 nm.
3.3.4 Pembuatan Kurva Kalibrasi
Dipipet 1 mL larutan standar Fe 10 mg/L diencerkan dalam labu takar 50 mL sampai
garis tanda dan dihomogenkan (Larutan ini mengandung 0,2 mg/L Fe). Dimasukkan
kedalam erlenmeyer 150 mL, ditambah 2 mL HCl(p) , ditambah 1 mL NH2OH.HCl , di
didihkan diatas hotplate sampai volumenya ½ dari volume awal, didinginkan dan
ditambah 10 mL buffer amonium asetat dan 2 mL 1,10-Fenantrolin , sehingga
λ maks 510 nm. (Perlakuan yang sama dilakukan sebanyak 3 kali dan dilakukan hal yang sama untuk larutan seri standar Fe 0,4 ; 0,6 ; 0,8 ; 1,0 mg/L).
3.3.5 Pembuatan Arang Aktif
Dikeringkan 100 g sekam padi kedalam oven pada suhu ± 110ºC, direndam dengan
H3PO4 30% selama 24 jam, disaring dan residu yang diperoleh dimasukkan ke dalam
cawan penguap dan dikeringkan dalam oven pada suhu ± 110ºC, diarangkan dalam
tanur pada suhu 500 ºC selama 4 jam, dibilas dengan akuades, dikeringkan dalam
oven pada suhu ± 110º C selanjutnya digiling atau dihaluskan dan diayak dengan
ukuran partikel 80 mesh.
3.3.6 Penentuan Fe dari Air Sumur secara Spektrofotometri
Dipipet 5 mL air sumur dan diencerkan dalam labu takar 50 mL sampai garis tanda
dan dihomogenkan, dimasukkan kedalam erlenmeyer 250 mL, ditambah 2 mL HCl
(p), ditambah 1 mL NH2OH.HCl , di didihka n diatas hotplate sampai volumenya
½ dari volume awal, didinginkan, selanjutnya ditambah 10 mL buffer amonium asetat
dan 2 mL 1,10-fenantrolin , sehingga diperoleh larutan berwarna merah orange.
Didiamkan selama 10 menit dan diukur absorbansi larutan dengan spektrofotometer
3.3.7 Penentuan Fe dari Air Sumur setelah Dilewatkan Adsorben
Dirangkai alat kolom, dimasukkan 10 g arang aktif dari sekam padi kedalam kolom,
dipipet 5 mL air sumur dan diencerkan dalam labu takar 50 mL. Dimasukkan sampel
yang telah diencerkan ke dalam kolom, didiamkan selama ± 1 jam selanjutnya dibuka
kran kolom dan ditampung filtrat larutan sampel yang telah dilewatkan dari kolom.
Ditambah 2 mL HCl(p) dan 1 mL NH2OH.HCl , di didihkan diatas hotplate sampai
volumenya ½ dari volume awal, didinginkan, selanjutnya ditambah 10 mL buffer
amonium asetat dan 2 mL 1,10-fenantrolin , sehingga diperoleh larutan berwarna
merah orange. Didiamkan selama 10 menit dan diukur absorbansi larutan dengan
3.4. Bagan Penelitian
3.4.1 Pembuatan Arang Aktif
Dikeringkan dalam oven pada
suhu ± 110°C
Direndam dengan H3PO4 30%
selama 24 jam
Disaring
Dimasukkan kedalam cawan penguap
Dikeringkan dalam oven pada suhu ± 110ºC
Diarangkan dalam tanur pada suhu 500ºC selama 4 jam
Dibilas dengan akuades
Dikeringkan dalam oven pada suhu ± 110ºC
Digiling/dihaluskan
Diayak dengan ukuran partikel 80 mesh 100 g sekam padi
Sampel kering
Residu Filtrat
Arang
3.4.2 Penentuan Logam Fe dari Air Sumur
Dipipet 5 mL dan diencerkan dalam labu takar 50 mL
Dimasukkan dalam erlenmeyer
Ditambah 2 mL HCl(p) dan 1 mL NH2OH.HCl
Di didihkan diatas hotplate hingga ½ volume awal
Didinginkan
Ditambah 10 mL buffer amonium asetat
Ditambah 2 mL 1,10-fenantrolin sehingga
diperoleh larutan merah orange
Didiamkan selama 10 menit
Diukur absorbansi larutan dengan Spektrofotometer
spekronik 20 pada λ 510 nm
Catatan : Perlakuan yang sama dilakukan untuk sampel air sumur gali
Hasil air sumur bor
3.4.3 Penentuan Logam Fe dari Air Sumur setelah Dilewatkan Adsorben
Dipipet 5 mL dan diencerkan dalam labu takar 50 mL
Dimasukkan kedalam kolom yang berisi 10 g arang aktif
Dibiarkan selama ± 1 jam
Dibuka kran kolom dan ditampung filtrat yang telah dilewatkan
dari kolom
Ditambah 2 mL HCl(p) dan 1 mL NH2OH.HCl
Di didihkan diatas hotplate, hingga ½ volume awal
Didinginkan
Ditambah 10 mL buffer amonium asetat
Ditambah 2 mL 1,10-fenantrolin sehingga diperoleh larutan
merah orange
Didiamkan selama 10 menit
Diukur absorbansi larutan dengan Spektrofotometer spektronik
20 pada λ 510 nm
Catatan : Perlakuan yang sama dilakukan untuk sampel air sumur gali Hasil
air sumur bor
Filtrat
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
Dari hasil penelitian ini diperoleh data hasil penentuan kadar besi dari sampel air
sumur bor dan air sumur gali sebelum dan setelah dilewatkan adsorben adalah sebagai
[image:39.595.109.526.367.474.2]berikut :
Tabel 1. Hasil Penentuan Kadar Besi dari Sampel Air Sumur Gali dan Air Sumur Bor sebelum dan setelah Dilewatkan Adsorben dan Penurunan Kadar Besi
NO Sampel Kadar Fe
(mg/L)
Penurunan Kadar Besi
(%) 1. Air sumur Bor sebelum dilewatkan Adsorben 1,2424
72,99 2. Air sumur Bor setelah dilewatkan Adsorben 0,3351
3. Air sumur Gali sebelum dilewatkan Adsorben 1,0905
77,24 4. Air sumur Gali setelah dilewatkan Adsorben 0,2479
4.2 Pengolahan Data
4.2.1 Penurunan Persamaan Garis Regresi Besi (Fe) dengan Metode Kurva Kalibrasi
Hasil pengukuran transmitansi dari suatu larutan seri standar yang digunakan, terlebih
dahulu dikonversikan menjadi absorbansi dengan menggunakan rumus:
A = 2 – Log %T
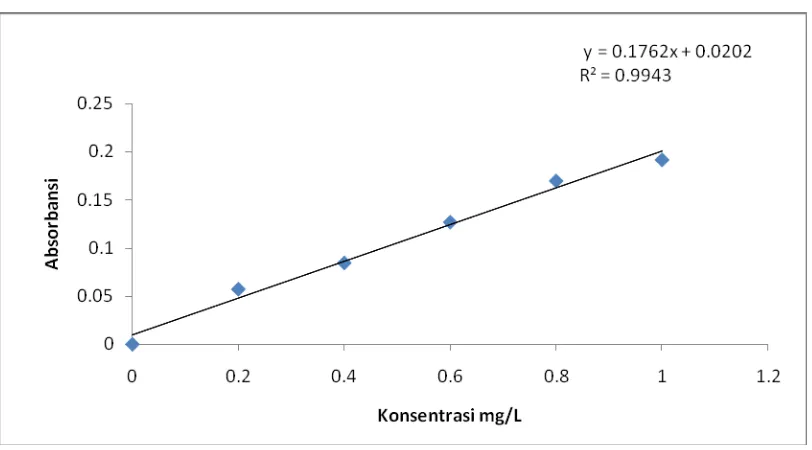
Selanjutnya absorbansi diplotkan terhadap konsentrasi larutan standar sehingga
diperoleh suatu kurva kalibrasi berupa garis linier dapat dilihat pada gambar 2 pada
Persamaan garis regresi untuk kurva kalibrasi ini dapat diturunkan dengan metode
Least Square sebagai berikut :
No Xi Yi Xi -X (Xi )2 ( Yi –Y ) ( Yi -Y )2
(Xi-X )(Yi- Y ) 1 0,2 0,0572 - 0,4 0,16 - 0,0687 0,0047 0,0274
2 0,4 0,0845 - 0,2 0,04 0,0414 0,0017 0,0082
3 0,6 0,1269 0 0 0,0010 0 0
4 0,8 0,1697 0,2 0,04 0,0438 0,0019 0,0087
5 1,0 0,1916 0,4 0,16 0,0657 0,0043 0,0262 ∑ 3,0 0,6299 0 0,40 0,0004 0,0126 0,0705
Dari tabel diatas diperoleh X rata-rata :
X = n Xi ∑ = 5 0 , 3
= 0,6
Dan harga Y rata – rata :
Y = n Yi ∑ = 5 6299 , 0 = 0,1259
4.2.2 Penurunan Persamaan Garis Regresi
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan garis :
Y = aX + b
Dimana : a = slope
b = intersept
Harga slope ( a) dapat ditentukan dengan persamaan sebagai berikut :
a =
(
)( )
(
)
∑
∑
− − − 2 X Xi Y Yi X XiSehingga diperoleh harga (a) :
a = 40 , 0 0705 , 0
Sedangkan harga intersept (b) dapat diperoleh melalui substitusi harga (a) ke
persamaan berikut :
Y = aX + b
b = Y – aX
= 0,1259 – ( 0,1762 x 0,6 )
= 0,0202
Maka persamaan garis regresi yang diperoleh adalah :
Y = 0,1762 X + 0,0202
4.2.3 Koefisien Korelasi
Koefisien korelasi (r) dapat ditentukan dengan menggunakan persamaan sebagai
berikut :
r =
(
) (
)
∑
∑
− − − − 2 2 ) )( ( Y Yi X Xi Y Yi X Xir =
0126 , 0 40 , 0 0705 , 0 x
= 0,9943
Dengan mensubstitusikan harga konsentrasi larutan standar (Xi) ke persamaan garis
regresi maka diperoleh harga Y yang baru (Y ) seperti yang tercantum dalam tabel : NO Xi Yi Xi2 Y | Yi - Y | (Yi - Y )2
1 0,2 0,057 0,04 0,0554 0,0018 0,03X10-4
2 0,4 0,0845 0,16 0,0906 0,0061 0,37x10-4
3 0,6 0,1269 0,36 0,1259 0,0010 0,01x10-4
4 0,8 0,1697 0,64 0,1611 0,0086 0,73x10-4
Dari perhitungan pada tabel diatas maka dapat ditentukan deviasi standar untuk
intersept (Sb) yaitu dengan persamaan :
Sb =
(
)
2 12
∑
Xi − Xx Sy
Dimana,
x
Sy =
(
)
2 1 2
2
−
−
∑
n
Y
Yi
= 2 1 42
5
10
37
,
1
−
−x
= 0,6757 x 10-2
Sehingga diperoleh,
Sb =
(
)
12 2 40 , 0 10 6757 ,0 x −
= 1,0600 x 10-2
Harga Sb dihitung untuk menentukan batas kepercayaan nilai intersept yaitu
b ± t (Sb), dimana t diperoleh dari tabel t-distribusi dengan derajat kepercayaan 95%
dan derajat kebebasan (n-2) = 5–2 = 3 diperoleh p = 0,05 dan t = 3,18 sehingga batas
kepercayaan untuk nilai intersept adalah :
0,0202 ± ( 3,18) ( 1,0600 x 10-2)
0,0202 ± ( 3,3708 x 10-2)
Deviasi slope dari standar dapat dihitung dengan persamaan :
Sa = x Sy =
(
)
2 1 2 2 −∑
∑
Xi Xn
Xi
= 0,6757 x 10-2
40 , 0 3 2 , 2 x
= 0,9148 x 10-2
Sesuai dengan cara untuk menentukan batas kepercayaan nilai intersept maka
kepercayaan nilai slope adalah a ± t ( Sa)
0,1762 ± 3,18 ( 0,9148 x 10-2 )
0,1762 ± 2,9090 x 10-2
0,1762 ± 0,0290
4.2.4 Penentuan Batas Deteksi
Batas deteksi dapat dihitung dengan persamaan :
3 Sb = Y - Yb
atau, Y = 3 Sb + Yb
Dimana : Y = signal pada batas kadar deteksi
Sb = standar deviasi
Yb = intersep kurva kalibrasi
Persamaan Kurva kalibrasi, Y = 0,1762 X + 0,0202
Dimana, Yb = 0,0202
Sb = x
Maka dengan mensubstitusikan harga (Yb) dan (Sb) pada persamaan Y = 3 Sb + Yb
dapat diperoleh harga untuk batas deteksi :
Y = 3 Sb + Yb
= 3 ( 0,6757 x 10-2) + 0,0202
= 0,0202 + 0,0202
= 0,0404
Dengan mensubstitusikan nilai (Y) terhadap persamaan :
Y = 0,1762 X + 0,0202
0,0404 = 0,1762 X + 0,0202
X = 0,1146 mg/L
Jadi, batas deteksi pengukuran besi untuk penelitian ini adalah 0,1146 mg/L.
4.2.5 Penentuan Kadar Besi (Fe) dalam Sampel
Kadar Besi (Fe) dapat ditentukan dengan menggunakan metode kurva kalibrasi
dengan mensubstitusikan nilai Y (absorbansi) yang diperoleh dari hasil pengukuran
terhadap persamaan garis regresi dari kurva kalibrasi.
[image:44.595.159.430.535.644.2]a. Penentuan Kadar Besi dari Sampel sebelum Dilewatkan Adsorben
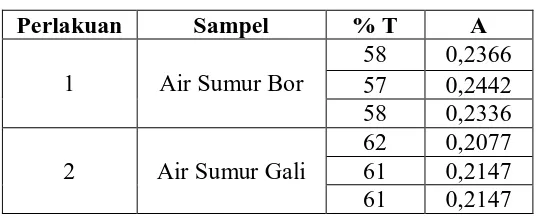
Tabel 2. Hasil Pengukuran % Transmitansi/Absorbansi Logam Besi sebelum Dilewatkan Adsorben
Perlakuan Sampel % T A
1 Air Sumur Bor
58 0,2366 57 0,2442 58 0,2336
2 Air Sumur Gali
62 0,2077 61 0,2147 61 0,2147
Dengan mensubstitusikan nilai Y (Absorbansi) dari tabel 2 ke persamaan garis regresi,
maka dapat dihitung kadar Besi (Fe) dalam sampel.
Kadar Besi dalam Air Sumur Bor
Y = 0,1762 X + 0,0202
1762 , 0 0202 , 0 2366 , 0 − = X
= 1,2281 mg/L
Sehingga diperoleh,
X1 = 1,2281 mg/L
X2 = 1,2712 mg/L
X3 = 1,2281 mg/L
X = n
Xi
∑
= 1,2424 mg/LKadar Besi dari Air Sumur Gali
Y = 0,1762 X + 0,0202
0,2077 = 0,1762 X + 0,0202
1762 , 0 0202 , 0 2077 , 0 − = X = 1,0641mg/L Sehingga diperoleh,
X1 = 1,0641 mg/L
X2 = 1,1038 mg/L
X3 = 1,1038 mg/L
X = n
Xi
∑
= 1,0905 mg/Lb. Penentuan Kadar Besi dari Sampel setelah Dilewatkan Adsorben
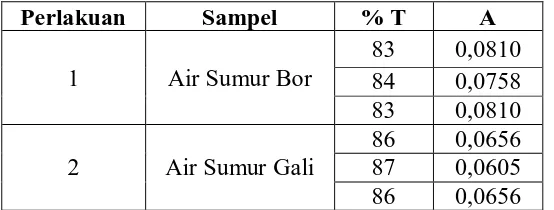
Tabel 3. Hasil Pengukuran % Transmitansi/Absorbansi Logam Besi setelah Dilewatkan Adsorben
Perlakuan Sampel % T A
1 Air Sumur Bor
83 0,0810 84 0,0758 83 0,0810
2 Air Sumur Gali
86 0,0656 87 0,0605 86 0,0656
[image:45.595.161.438.616.721.2]Kadar Besi dari Air Sumur Bor
Y = 0,1762 X + 0,0202
0,0810 = 0,1762 X + 0,0202
1762 , 0 0202 , 0 0810 , 0 − = X
= 0,3450 mg/L
Sehingga diperoleh,
X1 = 0,3450 mg/L
X2 = 0,3155 mg/L
X3 = 0,3450 mg/L
X = n
Xi
∑
= 0,3351 mg/LKadar Besi dari Air Sumur Gali
Y = 0,1762 X + 0,0202
0,0656 = 0,1762 X + 0,0202
1762 , 0 0202 , 0 0656 , 0 − = X
= 0,2576 mg/L
Sehingga diperoleh,
X1 = 0,2576 mg/L
X2 = 0,2287 mg/L
X3 = 0,2576 mg/L
X = n
Xi
4.2.6 Penentuan Deviasi Standar
a. Kadar Besi dari Air Sumur Bor
Kemudian dihitung deviasi standar sebagai berikut :
(
)
2(
)
2 41 0,3450 0,3551 0,9801 10
− =
− =
−X x
X
(
)
2(
)
2 43−X = 0,3450−0,3551 =0,9801x10−
X
(
)
∑
− 2X
Xi 4
10 8018 ,
5 x −
Maka, S =
(
)
1 3 10 8018 , 5 1 4 2 − = − − −
∑
x n X Xi= 1,7032x10−2 = 01700,
Didapat harga 0,0098 3 0170 , 0 = = = n S Sx
b. Kadar Besi dari Air Sumur Gali Dihitung deviasi standar sebagai berikut :
(
)
2(
)
2 41 0,2576 0,2479 0,9409 10
− =
− =
−X x
X
(
)
2(
)
2 42 0,2287 0,2479 3,6864 10
− =
− =
−X x
X
(
)
2(
)
2 41 0,2576 0,2479 0,9409 10
− =
− =
−X x
X
(
)
∑
− 2X
Xi 5,5682x10−4
Maka, S =
(
)
1 3 10 5682 , 5 1 4 2 − = − − −
∑
x n X Xi= 1,6685x10−2 = 01660,
Didapat harga Sx= S = 0,0166 =0,0095
(
)
(
)
2 42
2− X = 0,3155−0,3551 =3,8416x10−
Dari data hasil distribusi t student untuk n = 3, derajat kebebasan (dk) = n – 1 = 2
Untuk derajat kepercayaan 95% ( p = 0,05 ), t = 4,30
Maka, d = t ( 0,05 x n – 1) Sx
Untuk Air Sumur Bor
d = 4,30 x 0,1 x 0,0098
d = 0,0042
Dari data hasil pengukuran kadar besi pada air sumur bor adalah sebesar :
0,3351 ± 0,0042 mg/L
Untuk Air Sumur Gali
d = 4,30 x 0,1 x 0,0095
d = 0,0040
Dari data hasil pengukuran kadar besi pada air sumur gali adalah sebesar :
0,2479 ± 0,0040 mg/L
4.2.7 Penentuan Persen Penurunan Kadar Besi dalam Sampel
Data hasil percobaan yang diperoleh, dapat dilihat pada tabel 3 pada lampiran. Persen
penurunan kadar diperoleh dari hasil perhitungan dengan rumus sebagai berikut :
(
) (
)
(
)
x
100
%
adsorben dilewatkan
sebelum
adsorben dilewatkan
setelah adsorben
dilewatkan sebelum
Fe
Fe
Fe
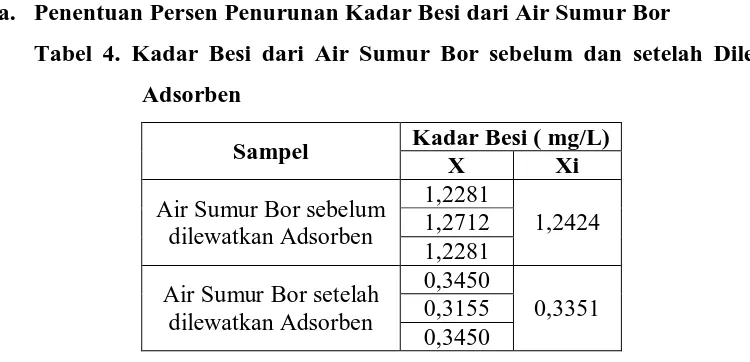
a. Penentuan Persen Penurunan Kadar Besi dari Air Sumur Bor
Tabel 4. Kadar Besi dari Air Sumur Bor sebelum dan setelah Dilewatkan Adsorben
Sampel Kadar Besi ( mg/L)
X Xi
Air Sumur Bor sebelum dilewatkan Adsorben
1,2281
1,2424 1,2712
1,2281
Air Sumur Bor setelah dilewatkan Adsorben
0,3450
0,3351 0,3155
0,3450
Maka diperoleh, persen penurunan kadar besi dalam air sumur Bor
% 100 2281 , 1 3450 , 0 2281 , 1
%= − x
= 71,90 %
Sehingga diperoleh,
% 1 = 71,90 %
% 2 = 75,18 %
% 3 = 71,90 %
% = n
i
∑
%= 72,99 %
[image:49.595.160.422.558.677.2]b. Penentuan Persen Penurunan Kadar besi dari Air Sumur Gali
Tabel 5. Kadar Besi dari Air Sumur Gali sebelum dan setelah Dilewatkan Adsorben
Sampel Kadar Besi (mg/L)
X Xi
Air Sumur Gali sebelum dilewatkan Adsorben
1,0641
1,0905 1,1038
1,1038
Air Sumur Gali setelah dilewatkan Adsorben
0,2576
02479 0,2287
Maka diperoleh, persen penurunan kadar besi dari air sumur Gali
% 100 0641
, 1
2576 , 0 0641 , 1
%= − x
= 75,79 %
Sehingga diperoleh,
% 1 = 75,79 %
% 2 = 79,28 %
% 3 = 76,66 %
% = n
i
∑
%= 77,24 %
4.3 Pembahasan
Dari hasil penelitian yang telah dilakukan diperoleh panjang gelombang maksimum
(λ maks) dari pembentukan warna kompleks merah orange dari larutan standar besi
0,6 mg/L sebesar 510 nm. Kurva kalibrasi larutan standar besi dibuat dengan
memvariasikan konsentrasi larutan standar besi dengan menggunakan persamaan
Least-Square sehingga diperoleh persamaan garis Linier : Y = 0,1762 X + 0,0202. Hal
ini dapat dilihat pada grafik 2 di lampiran. Dalam penentuan apakah suatu penelitian
memiliki titik yang sejajar pada kurva kalibrasi dengan harga slope positif dapat
dilihat dari perhitungan koefisien korelasi (r), diperoleh harga koefisien korelasi
sebesar 0,9943. Hal ini menunjukkan ada hubungan antara konsentrasi dengan
absorbansi. Pada penelitian analitik, grafik kurva kalibrasi yang baik ditunjukkan pada
harga (r) lebih besar atau sama dengan 0,99. (Miller.1991)
Karbon amorf dapat diaktivasi, sehingga mempunyai kapasitas absorpsi yang
besar dan dapat menyerap fase gas maupun fase cair secara selektif. Luas permukaan
spesifiknya berkisar 300 sampai 2500 m2/g, kuantitas bahan yang diserap oleh karbon
aktif sangat besar. Adsorpsi merupakan suatu fenomena fisika yang sangat bergantung
pada luas permukaan dan volume pori. Struktur pori itu menyebabkan ukuran molekul
yang dapat diadsorpsi itu terbatas sedangkan ukuran partikelnya tidak menjadi
Sifat-sifat bahan tidak hanya bergantung pada bahan baku yang digunakan tetapi juga pada
cara aktivasi. Aktivasi adalah suatu perlakuan terhadap arang yang bertujuan untuk
memperbesar pori yaitu dengan cara memecahkan ikatan hidrokarbon atau
mengoksidasi molekul-molekul permukaan sehingga arang mengalami perubahan
sifat, baik fisika maupun kimia yaitu luas permukaannya bertambah besar dan
berpengaruh terhadap daya adsorpsi. Proses aktivasi merupakan hal yang penting
dalam pembuatan arang aktif, cara yang paling umum digunakan adalah perlakuan
bahan berkarbon dengan gas pengoksidasi seperti udara, uap atau karbon dioksida dan
karbonisasi bahan baku dengan bahan kimia seperti seng klorida dan asam fosfat.
Bahan hasil karbonisasi itu mengalami aksi gas oksidasi, biasanya uap atau karbon
dioksida, di dalam tanur pada suhu 800 – 980°C. (Austin.1996)
Pembuatan arang aktif dari sekam padi dilakukan dalam 3 tahap yaitu
dehidrasi (penghilangan kadar air), karbonisasi dan aktivasi. Dilakukan perendaman
dengan asam fosfat 30% selama 24 jam dan diarangkan dalam tanur pada
suhu 500o C selama 4 jam. Pada penelitian ini, dilakukan metode aktivasi kimia yaitu
merupakan proses pemutusan rantai karbon dari senyawa organik dengan pemakaian
bahan kimia yaitu asam fosfat yang merupakan aktivator yang lebih efektif
dibandingkan aktivator lain karena mampu menghasilkan arang aktif dengan daya
serap yang tinggi, dengan pemanasan yang tinggi didalam furnace. Arang aktif yang
diperoleh digunakan untuk menurunkan kadar besi dalam air sumur bor dan air sumur
gali. Penurunan kadar besi dalam sampel diketahui setelah sampel dilewatkan ke
dalam kolom yang berisi arang aktif. Dengan menggunakan kolom sebagai alat untuk
memisahkan komponen-komponen dalam campuran atau menurunkan kadar besi
dalam sampel. Kolom yang digunakan berupa pipa gelas yang dilengkapi dengan
suatu kran dibagian bawah kolom untuk mengendalikan aliran zat cair dan dapat juga
digunakan buret atau corong pisah. Ukuran kolom tergantung pada banyaknya zat
yang akan dipisahkan, untuk menahan penyerapan (adsorben) dalam kolom digunakan
gelas wool/kapas dengan tinggi kolom 20 cm dan diameter 3 cm.
Pencemaran air tanah adalah suatu keadaan dimana air tesebut telah
sebagai bahan buangan organik yang berupa limbah yang membusuk/terdegradasi
oleh mikroorganisme sehingga mengakibatkan semakin berkembangnya
mikroorganisme. Bahan buangan anorganik berupa limbah yang tidak dapat
membusuk dan sulit didegradasi oleh mikroorganisme, apabila bahan buangan
anorganik masuk ke air lingkungan maka akan terjadi peningkatan jumlah logam di
dalam air. Air tanah biasanya memiliki kandungan besi yang relatif tinggi, jika air
tanah kontak dengan udara akan mengalami oksigenasi dimana ion ferri pada ferri
hidroksida yang banyak terdapat dalam air tanah akan teroksidasi menjadi ion ferro
yang akan mengalami pengendapan serta membentuk warna kemerahan pada air.
Kekeruhan pada air menggambarkan sifat optik air yang ditentukan berdasarkan
banyaknya cahaya yang diserap dan dipancarkan oleh bahan-bahan yang terdapat di
dalam air. Hal ini juga disebabkan adanya bahan organik dan anorganik yang berupa
plankton dan mikroorganisme lain. (Hefni.2003)
Selain itu bau dan warna pada air yang berubah disebabkan oleh buangan
bahan organik dan bahan anorganik, bahan organik yang mengalami pembusukan
sehingga melepaskan gas yang terlarut dalam air sedangkan bahan anorganik misalnya
kadar Fe dan Cu yang terlalu banyak dalam air akan memberi bau metal, klorida bebas
akan memberi bau khlor dan juga keberadaan plankton, humus dan ion-ion logam (Fe
dan Mn) dan bahan lainnya. (Achmad.2004)
Faktor lain yang menyebabkan tingginya kadar besi dalam air yaitu pH air
yang berpengaruh terhadap kesadahan kadar besi dalam air, pH yang rendah akan
berakibat terjadinya proses korosif, besi yang ada dalam air akan mengendap dan
tidak larut dalam air sehingga menyebabkan air menjadi berwarna, berbau dan berasa.
Secara biologis tingginya kadar besi terlarut dipengaruhi oleh bakteri besi yaitu
bakteri yang dalam hidupnya membutuhkan makanan dengna mengoksidasi besi
sehingga larut, antara lain jenis bakteri besi yaitu Crenotrik, Leptotrik, Calltonella,
yang mempertahankan hidupnya dengan membutuhkan oksigen dan besi.
(Kusnaedi.2010)
Dari hasil analisis yang dilakukan terhadap sampel air sumur bor dan air sumur
kadar besi dari sampel air sumur. Kadar besi dalam sampel air sumur sebelum
dilewatkan adsorben yaitu pada air sumur bor 1,2424 mg/L dan pada air sumur gali
sebesar 1,0905 mg/L, setelah dilewatkan adsorben maka kadar besi dalam sampel air
sumur berkurang/menurun yaitu pada air sumur bor 0,3351 mg/L dan air sumur gali
sebesar 0,2479 mg/L. Dengan demikian persen penurunan kadar besi (Fe) pada air
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari hasil penelitian ini diperoleh persen penurunan kadar besi dari air sumur bor
sebesar 72,99 % dan persen penurunan kadar besi dari air sumur gali sebesar 77,24 %.
5.2 Saran
Perlu adanya penelitian lebih lanjut tentang pemanfaatan dari berbagai bahan baku
lain yang mengandung karbon sebagai adsorben dengan menggunakan berbagai
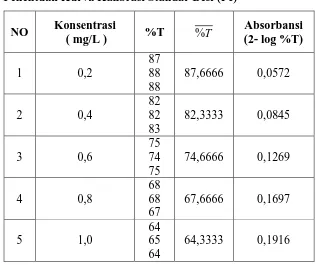
Tabel 6. Penentuaan Panjang Gelombang Maksimum dari Larutan Standar Besi (Fe) 0,6 mg/L
Tabel 7. Penentuan Kurva Kalibrasi Standar Besi (Fe) NO Konsentrasi
( mg/L ) %T % T
Absorbansi (2- log %T) 1 0,2
87 88 88
87,6666 0,0572
2 0,4
82 82 83
82,3333 0,0845
3 0,6
75 74 75
74,6666 0,1269
4 0,8
68 68 67
67,6666 0,1697
5 1,0
64 65 64
64,3333 0,1916
NO λ ( nm) %T A ( 2 – Log %T )
[image:56.595.149.465.343.608.2]Tabel 8. Data Perubahan Hasil Analisis Besi (Fe) setelah Dilewatkan Adsorben Sampel Perulangan Konsentrasi
(mg/L)
Kadar Fe (mg/L) (c ± d)
Penurunan Kadar Besi (%) Air
sumur Bor
I 0,3450
0,3351± 0,0042 72,79 II 0,3155
III 0,3450
Air sumur
Gali
I 0,2576
0,2479 ± 0,0040 77,24 II 0,2287
III 0,2576 Catatan : n = 3
Tabel 9. Daftar Harga Distribusi t-student Derajat Kebebasan
(n-1)
Tingkat Probabilitas
90% 95% 98% 99%
Gambar 1. Penentuan Panjang Gelombang Maksimum dari Larutan Standar Besi (Fe) 0,6 mg/L
[image:58.595.109.515.443.668.2]