PENGARUH pH DAN PENAMBAHAN ASAM TERHADAP
PENENTUAN KADAR UNSUR KROM DENGAN MENGGUNAKAN
METODE SPEKTROFOTOMETRI SERAPAN ATOM
Zul Alfian
Departemen Kimia FMIPA Universitas Sumatera Utara
Jl. Bioteknologi No. 1 Kampus USU Medan
Abstrak
Penelitian mengenai pengaruh pH dan penambahan asam terhadap kadar unsur Krom telah dilakukan. Dalam penelitian ini pelarut asam yang digunakan adalah HNO3, HCl, Aqua Regia dengan variasi pH 2.0, 2.5, 3.0, dan 3.5.Kadar Krom diukur dengan metode Spektrofotometri Serapan Atom (SSA) setelah penambahan pelarut asam dan memvariasikan pH larutan. Hasil penelitian menunjukkan bahwa konsentrasi maksimum dari Krom dengan menggunakan Aqua Regia dan pH optimum adalah 3. Dari hasil penelitian ini diketahui bahwa pH dan penambahan asam sangat berpengaruh terhadap pengukuran konsentrasi Krom dengan menggunakan metode Spektrofotometri Serapan Atom (SSA).
Kata kunci: pH, Unsur Krom, dan Spektrofotometer Serapan Atom
PENDAHULUAN
Pada spektrofotometer serapan atom nyala, sampel harus dalam bentuk larutan. Sampel dan standar dilarutkan dalam pelarut yang sama dan dibuat sesegar mungkin untuk menghindarkan efek penyimpanan. Bila sampel bukan dalam bentuk larutan maka sampel harus dilarutkan lebih dahulu. Pelarut yang digunakan adalah menggunakan asam. Asam Nitrat dan Asam Klorida merupakan pelarut yang sangat baik dan umum digunakan untuk melarutkan unsur logam yang akan dianalisis dengan metode SSA.
Dengan menggunakan Asam Klorida otoionisasinya sedikit tetapi banyak senyawaan organik dan beberapa senyawaan anorganik melarut. Sedangkan Asam Nitrat bereaksi hampir dengan semua logam kecuali Au, Pt, Rh, dan Ir serta beberapa logam lain yang cepat menjadi pasif (tertutup oleh lapisan oksida yang merintangi) seperti Al, Fe, dan Cu.(Cotton, 1984)
Dengan Asam Nitrat dan Aqua Regia serta Asam Sulfat pekat dingin logam Kromium menjadi pasif (tertutup oleh lapisan oksida yang merintangi). Sedangkan kromium dapat larut dengan asam klorida baik encer maupun pekat. (Vogel, 1984)
Penggunaan asam yang terlalu pekat dapat pula menyebabkan gangguan dalam analisis dengan SSA. Di mana kepekatan terlalu asam akan menyebabkan nilai absorbansi menjadi lebih rendah dari pada yang semestinya dan akan mengakibatkan konsentrasi sampel (bahan) yang dianalisis akan berkurang nilai serapannya dari nilai yang sebenarnya. (Tambunan, 1998)
perbandingan volume pelarut serta bentuk organik logamnya. (Vivianti, 2003)
Efek kronis dari jenis kromium (trivalen dan hekasavalen) dilaporkan meliputi kulit, iritasi membran selaput lender dan efek sistemik termasuk pada anak-anak, hati, kanker paru-paru pada pekerja pada industri pewarna yang menggunakan kromium. (John, D.H, 1969)
Berdasarkan uraian di atas penulis ingin melakukan penelitian tentang sejauh mana pengaruh pH dan pelarut asam terhadap pengukuran konsentrasi dan menentukan pH optimum dan pelarut yang sesuai untuk logam Krom dengan menggunakan SSA.
BAHAN DAN METODA
Alat
Neraca Analitis, pH meter, Spektrofotometer Serapan Atom, Botol Akuades, dan alat-alat gelas yang ada di Laboratorium Kimia.
Bahan
Bahan-bahan yang dipakai dalam penelitian ini adalah HNO3, HCl, Akuaregia, K2CrO4, Akuades dan NaOH.
Pembuatan Larutan Standar Cr 1000 ppm 3,7348 g K2CrO4 dimasukkan ke dalam labu takar 1000 ml, kemudian dicukupkan dengan aquades, sehingga diperoleh larutan standar Cr 1000 ppm.
Pembuatan Kurva Kalibrasi
− Dari larutan standar Cr 1000 ppm dipipet sebanyak 10 ml lalu dimasukkan ke dalam labu takar 100 ml, kemudian dicukupkan dengan aquades sampai garis batas, sehingga diperoleh larutan Cr100 ppm. − Kemudian dari larutan standar 100 ppm
dipipet sebanyak 10 ml lalu dimasukkan ke dalam labu takar 100 ml, kemudian
batas, sehingga diperoleh larutan Cr 10 ppm.
− Selanjutnya dari larutan 10 ppm dipipet masing-masing 2; 4; 8; 10 dan 20 ml lalu dimasukkan kedalam labu takar 100 ml dan diencerkan dengan aquades sampai garis batas, sehingga diperoleh larutan standar 0,2000; 0,4000; 0,8000; 1,0000; 2,0000 ppm.
Pembuatan Sampel Larutan Cr dengan Penambahan Pelarut HNO3 (p)
− Dari larutan standar Cr 1000 ppm dipipet sebanyak 1 ml dan dimasukkan ke dalam labu takar 1000 ml kemudian ditambah aqudes sampai garis batas untuk memperoleh larutan Cr 1,00 ppm
− Dari larutan Krom 1,00 ppm diatur pH 2, 2.5, 3, dan 3,5 dengan pH meter dengan penambahan HNO3(p) dan NaOH kemudian diukur nilai absorbansinya dengan AAS pada panjang gelombang 357,9 nm.
Pembuatan Sampel Larutan Cr dengan Penambahan Pelarut HCl (p)
− Dari larutan Standar Cr 1000 ppm dipipet sebanyak 1 ml dan dimasukkan ke dalam labu takar 1000 ml kemudian ditambah aqudes sampai garis batas untuk memperoleh larutan Cr 1,00 ppm.
− Dari larutan Krom 1,00 ppm diatur pH 2, 2.5, 3, dan 3,5 dengan pH meter dengan penambahan HCl(p) dan NaOH kemudian diukur nilai absorbansinya dengan AAS pada panjang gelombang 357,9 nm.
Pembuatan Sampel Larutan Cr dengan Penambahan Aqua Regia
− Dari larutan Krom 1,00 ppm diatur pH 2, 2.5, 3, dan 3,5 dengan pH meter dengan penambahan Aqua Regia dan NaOH kemudian diukur nilai absorbansinya dengan AAS pada panjang gelombang 357,9 nm.
HASIL DAN PEMBAHASAN
Data hasil pengukuran kadar Krom yang diperoleh dapat dilihat seperti pada tabel sebagai berikut:
Tabel 1. Data Hasil Pengukuran Absorbansi Larutan Standar Krom dengan Sepktrofotometer Serapan Atom
No. Kadar (ppm) Absorbansi (A)
1 0.0000 0.0002
2 0.2000 0.0074
3 0.4000 0.0142
4 0.8000 0.0279
5 1.0000 0.0339
6 2.0000 0.0693
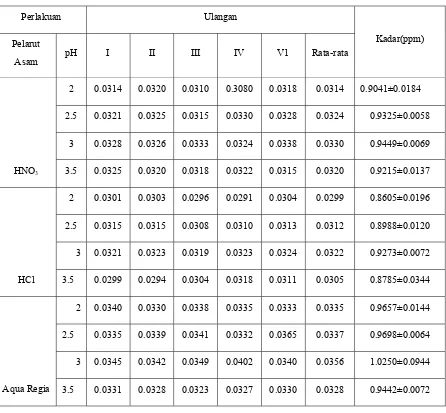
Tabel 2. Data Hasil Pengukuran Kadar Krom dalam Sampel
Perlakuan Ulangan Pelarut
Asam pH I II III IV V1 Rata-rata
Kadar(ppm)
2 0.0314 0.0320 0.0310 0.3080 0.0318 0.0314 0.9041±0.0184 2.5 0.0321 0.0325 0.0315 0.0330 0.0328 0.0324 0.9325±0.0058
3 0.0328 0.0326 0.0333 0.0324 0.0338 0.0330 0.9449±0.0069 HNO3 3.5 0.0325 0.0320 0.0318 0.0322 0.0315 0.0320 0.9215±0.0137
2 0.0301 0.0303 0.0296 0.0291 0.0304 0.0299 0.8605±0.0196 2.5 0.0315 0.0315 0.0308 0.0310 0.0313 0.0312 0.8988±0.0120 3 0.0321 0.0323 0.0319 0.0323 0.0324 0.0322 0.9273±0.0072 HCl 3.5 0.0299 0.0294 0.0304 0.0318 0.0311 0.0305 0.8785±0.0344
Pembahasan
Dari data pada Tabel 2 dapat dilihat bahwa pH optimum untuk logam Krom adalah 3, karena pada pH ini nilai absorbansi yang diperoleh lebih besar. Ini menunjukkan bahwa bahwa pada pH ini (pH=3) tereksitasinya logam Krom lebih sempurna. Pada pH 3 atom- atom Cr dapat tereksitasi oleh energi thermal dari nyala dan menyerap sinar dengan panjang gelombang 357,9 nm dari lampu katoda (sumber radiasi) dimana intensitas sinar yang diserap oleh atom-atom logam akan sebanding dengan kandungan logam-logam dalam larutan tersebut. Sedang pada pH 2, dan pH 2.5 terlihat nilai absorbansinya lebih rendah dari absorbansi pada pH 3 yang dikarenakan pada pH ini terlalu asam(pekat) dimana terlalu asam akan menyebabkan suhu nyala berkurang dari semestinya sehingga tidak dapat secara optimum mengeksitasikan logam Krom tersebut akibatnya bacaan serapan atom menjadi lebih rendah dibanding dengan menggunakan larutan pH 3. Pada pH 3.5 nilai absorbansi menurun, disebabkan pada batas pH tersebut telah mulai terbentuk endapan sehingga pada saat eksitasi terjadi tidak keseluruhan logam Cr tersebut dapat dieksitasikan, dengan ini akan mengurangi nilai bacaan serapan atomnya.
Dari data pada Tabel 2 dapat dilihat bahwa pelarut asam yang sesuai untuk logam Krom adalah Aqua Regia, karena dengan penambahan pelarut ini nilai absorbansinya lebih besar. Hal ini disebabkan karena
kemampuan Aqua Regia untuk mendekomposisikan logam Krom lebih sempurna, sehingga penentuan kadar abunya lebih baik. Sedangkan dengan pelarut HNO3 dan HCl terlihat nilai absorbansinya lebih kecil. Hal ini disebabkan karena kemampuan perombakan terhadap logam Krom kurang sempurna.
Rancangan Acak Lengkap untuk kadar Cr dapat dilihat pada Tabel 3 dengan variasi pH dan pelarut asam.
Untuk taraf faktor pelarut asam terhadap kadar Cr Fhitung > F0,05 Fhitung sebesar 52,707 adalah lebih besar dari nilai F0,05 sebesar 2,21, berarti hipotesa nol (Ho) ditolak dan hipotesa alternatif (Ha) diterima. Hal ini menunjukkan bahwa pelarut asam mempunyai pengaruh yang nyata terhadap kadar Krom.
Untuk taraf faktor pH larutan terhadap kadar Cr Fhitung > F0,05
Fhitung sebesar 14,763 adalah lebih besar dari F0,05 sebesar 2,82, berarti hipotesa nol (Ho) ditolak dan hipotesa alternatif (Ha) diterima. Hal ini menunjukkan bahwa pH larutan mempunyai pengaruh yang nyata terhadap kadar Krom.
Untuk taraf faktor interaksi terhadap kadar Cr Fhitung < F 0,05, Fhitung sebesar 1,2544 adalah lebih kecil dari F0,05 sebesar 2,31, berarti bahwa hipotesa nol (Ho) diterima dan hipotesa alternatif ditolak. Hal ini menunjukkan bahwa interaksi antara pelarut asam dengan pH larutan terhadap kadar Krom tidak berbeda nyata.
Tabel 3. Rancangan Acak Lengkap untuk Kadar Cr dengan Variasi pH dan Pelarut Asam Sumber
Keragaman
KESIMPULAN DAN SARAN
Kesimpulan
Dari hasil penelitian yang dilakukan diketahui bahwa pelarut asam dan pH larutan sangat berpengaruh terhadap pengukuran kadar logam Krom dengan menggunakan Spektrofotometer Serapan Atom. Pelarut yang sesuai untuk penentuan kadar unsur Krom adalah Aqua Regia pada pH 3.
Saran
Dalam menganalisa kadar logam Krom hendaknya dengan menggunakan pelarut asam Aqua Regia pada pH 3.
DAFTAR PUSTAKA
Cotton, F. A., Wilkinson. G., 1984, “Kimia
Anorganik Dasar”, (terjemahan), Penerbit
UI-Press, Jakarta
John, D. H., 1969, “Practical Statistic For Chemical
Research”, Meuthuen and co. Ltd and Sciences
Paper back, London
Tambunan, Hotmian Dame. B. M., 1998, “Studi Pengaruh pH Terhadap Penentuan Logam-Logam Cd, Pb, Cu, Co dan Ni dengan Menggunakan Metode Spektrofotometri
Serapan Atom (SSA)”, Skripsi Jurusan Kimia
FMIPA-USU
Vivianti., 2003, “Studi Perbandingan Dekstruksi Logam Krom Total Menggunakan Metode Destruksi Basah dan Kering dengan Pelarut
HNO3(p) dan HCl (p) dari Limbah Padat
Industri Pelapisan Logam”, Skripsi Jurusan
Kimia FMIPA USU
Vogel, A. I., 1984, “Buku Teks Analisis Anorganik
Kualitatif Makro dan Semimikro”, Edisi
Kelima, PT. Kalman Media Pustaka, Jakarta Walsh, A., 1955, “Aplication of Atomic Absorption
Spectra to Chemical Analysis