FERMENTABILITAS DAN KECERNAAN
in vitro
RANSUM
BERBASIS JERAMI PADI DAN KONSENTRAT
YANG DISUPLEMENTASI DENGAN
PROBIOTIK PADAT ATAU CAIR
MUHAMMAD ICHSAN ALMAI
DEPARTEMEN ILMU NUTRISI DAN TEKNOLOGI PAKAN FAKULTAS PETERNAKAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Fermentabilitas dan Kecernaan in vitro Ransum Berbasis Jerami Padi dan Konsentrat yang Disuplementasi dengan Probiotik Padat atau Cair adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, November 2013
ABSTRAK
MUHAMMAD ICHSAN ALMAI. Fermentabilitas dan Kecernaan in vitro Ransum Berbasis Jerami Padi dan Konsentrat yang Disuplementasi dengan Probiotik Padat atau Cair. Dibimbing oleh ANITA S. TJAKRADIDJAJA dan JAJAT JACHJA.
Tujuan penelitian ini adalah untuk melihat efek optimalisasi ransum berbasis jerami padi dan konsentrat peternak yang diberi suplemen probiotik padat atau cair terhadap fermentasi dan kecernaan in vitro. Penelitian ini terdiri atas dua faktor, yaitu Faktor A : pemberian ransum dengan rasio 60:40% antara jerami padi (JP) dan konsentrat (isokalori, TDN 60%); A1 = JP + konsentrat kontrol (10% PK), A2 = JP + konsentrat optimal (12% PK), A3 = JP + konsentrat suboptimal (14% PK). Faktor B : perlakuan probiotik; B1 = tanpa probiotik (0%), B2 = probiotik padat (0.25% b/b), B3 = probiotik cair (0.10% v/b). Rancangan percobaan menggunakan rancangan acak kelompok (RAK) pola faktorial 3 x 3 (4 ulangan). Konsentrasi amonia dan VFA total serta kecernaan dipengaruhi oleh suplementasi probiotik; sedangkan populasi bakteri dipengaruhi oleh perlakuan pakan dan suplementasi probiotik, namun perlakuan ini tidak menghasilkan efek signifikan terhadap populasi protozoa dan sintesis protein mikroba. Ransum A3 merupakan perlakuan pakan yang terbaik. Hasil uji ortogonal kontras menunjukkan bahwa pemberian probiotik cair (B3) adalah perlakuan yang optimal.
Kata kunci: in vitro, konsentrat, probiotik cair, probiotik padat, taraf protein
ABSTRACT
MUHAMMAD ICHSAN ALMAI. In vitro Fermentability and Digestibility of Rice Straw Based Diet and Concentrate Supplemented with Solid or Liquid Probiotics. Supervised by ANITA S. TJAKRADIDJAJA and JAJAT JACHJA.
This study was aimed at examining effects of rice straw-based feed and concentrate supplemented with solid or liquid probiotic on in vitro fermentation and digestibility. This study consisted of two factors; Factor A : feed treatment with a ratio 60:40% of a mixture of rice straw (RS) and concentrate; A1 = RS + control concentrate (10% CP), A2 = RS + optimal concentrate (12% CP), A3 = RS + suboptimal concentrate (14% CP). Factor B : probiotic treatment; B1 = without probiotic (0%), B2 = solid probiotic (0.25% b/b), B3 = liquid probiotic (0.10% v/b). A factorial randomized block design (RBD) 3 x 3 (4 replications) was applied. The result showed that ammonia and total VFA concentrations and digestibility were influenced by probiotic supplementation whereas bacterial populations were affected by feed treatments and probiotic supplementation; however, these treatments did not significantly affect protozoal populations and microbial protein synthesis. A3 is the best feed treatment that can be used, and liquid probitic supplementation (B3) is the optimal treatment.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Peternakan
pada
Departemen Ilmu Nutrisi dan Teknologi Pakan
FERMENTABILITAS DAN KECERNAAN
in vitro
RANSUM
BERBASIS JERAMI PADI DAN KONSENTRAT
YANG DISUPLEMENTASI DENGAN
PROBIOTIK PADAT ATAU CAIR
MUHAMMAD ICHSAN ALMAI
DEPARTEMEN ILMU NUTRISI DAN TEKNOLOGI PAKAN FAKULTAS PETERNAKAN
INSTITUT PERTANIAN BOGOR BOGOR
Judul Skripsi : Fermentabilitas dan Kecernaan in vitro Ransum Berbasis Jerami Padi dan Konsentrat yang Disuplementasi dengan Probiotik Padat atau Cair
Nama : Muhammad Ichsan Almai NIM : D24090133
Disetujui oleh
Ir Anita S Tjakradidjaja, MRurSc Pembimbing I
Dr Ir Jajat Jachja, MAgrSc Pembimbing II
Diketahui oleh
Prof Dr Ir Panca Dewi MHKS, MSi Ketua Departemen
PRAKATA
Segala puji dan syukur penulis panjatkan kehadirat Allah SWT atas rahmat dan karunia-Nya sehingga skripsi ini berhasil diselesaikan. Penulis menyusun skripsi yang berjudul Fermentabilitas dan Kecernaan in vitro Ransum Berbasis Jerami Padi dan Konsentrat yang Disuplementasi dengan Probiotik Padat atau Cair berdasarkan hasil penelitian yang dilakukan sejak Januari sampai dengan Agustus 2013.
Peternakan sapi di Indonesia mempunyai banyak permasalahan dari segi nutrisi pakan, seperti defisiensi dan ketidakseimbangan nutrien pada ransum. Hal ini yang mendasari penulis untuk melakukan penelitian tentang probiotik sebagai salah satu alternatif guna memperbaiki nutrisi dan kecernaan pakan. Penelitian ini bertujuan untuk melihat efek optimalisasi ransum berbasis jerami padi dan konsentrat peternak yang diberi suplemen probiotik padat atau cair terhadap fermentasi dan kecernaan in vitro.
Penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan, oleh karena itu kritik dan saran yang membangun sangat diharapkan demi perbaikan di masa mendatang. Penulis juga berharap semoga skripsi ini dapat memberikan informasi, wawasan maupun sesuatu yang bermanfaat bagi pihak-pihak yang membutuhkan dan semoga kekurangan yang terdapat pada tulisan ini dapat diperbaiki dalam tulisan selanjutnya.
DAFTAR ISI
DAFTAR TABEL x
DAFTAR LAMPIRAN x
PENDAHULUAN 10
METODE PENELITIAN 2
Alat 2
Bahan 2
Waktu dan Lokasi Penelitian 2
Prosedur Penelitian 2
Pengambilan cairan rumen 2
Pembuatan larutan McDougall 3
Pencernaan fermentatif 3
Pengukuran NH3 3
Pengukuran volatile fatty acid (VFA) 3
Perhitungan populasi bakteri total 4
Perhitungan populasi protozoa 4
Pengukuran sintesis protein mikroba 5
Pengukuran koefisien cerna bahan kering dan bahan organik 5
Peubah yang diamati 6
Analisis Data 6
HASIL DAN PEMBAHASAN 6
Karakteristik Probiotik 6
Komposisi Ransum 7
Konsentrasi NH3 9
Konsentrasi Volatile Fatty Acid (VFA) Total 10
Bakteri Total 11
Populasi Protozoa Total 12
Sintesis Protein Mikroba 13
Kecernaan 13
SIMPULAN DAN SARAN 15
Simpulan 15
Saran 15
DAFTAR PUSTAKA 15
RIWAYAT HIDUP 22
DAFTAR TABEL
1 Jenis dan jumlah mikroba dalam probiotik padat dan cair 7
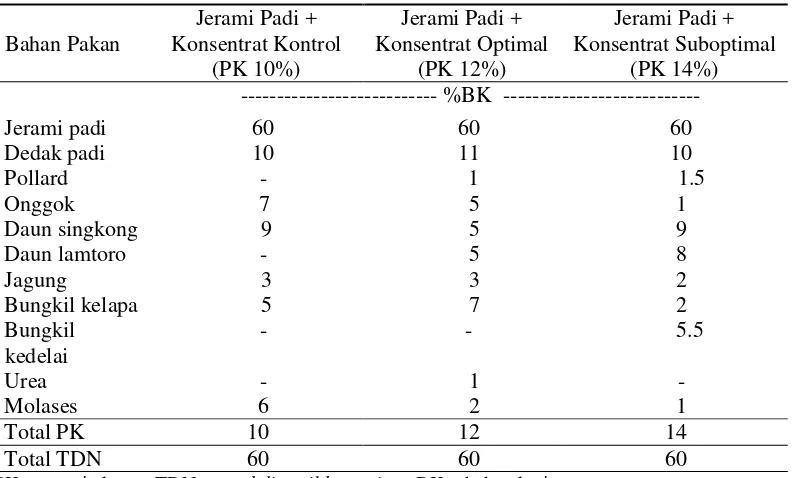
2 Presentase penggunaan bahan pakan 8
3 Analisis proksimat ransum yang digunakan 8
4 Pengaruh perlakuan terhadap konsentrasi NH3 9
5 Pengaruh perlakuan terhadap rataan VFA total 11 6 Pengaruh perlakuan terhadap rataan populasi bakteri total 11 7 Pengaruh perlakuan terhadap rataan populasi protozoa total 12 8 Pengaruh perlakuan terhadap rataan sintesis protein mikroba 13
9 Rataan kecernaan bahan kering 14
10 Rataan kecernaan bahan organik 14
DAFTAR LAMPIRAN
1 Analisis ragam (ANOVA) terhadap konsentrasi amonia 18
2 Uji ortogonal kontras perlakuan probiotik 18
3 Analisis ragam (ANOVA) terhadap konsentrasi VFA total 18
4 Uji ortogonal kontras perlakuan probiotik 18
5 Analisis ragam (ANOVA) terhadap populasi protozoa total 19 6 Analisis ragam (ANOVA) terhadap populasi bakteri total 19
7 Uji ortogonal kontras perlakuan pakan 19
8 Uji ortogonal kontras perlakuan probiotik 19
9 Analisis ragam (ANOVA) perlakuan terhadap sintesis protein
mikroba 20
10 Analisis ragam (ANOVA) perlakuan terhadap koefisien bahan kering 20
11 Uji ortogonal kontras perlakuan probiotik 20
12 Analisis ragam (ANOVA) perlakuan terhadap koefisien bahan
organik 21
PENDAHULUAN
Konsumsi daging sapi di Indonesia semakin meningkat setiap tahunnya. Konsumsi daging sapi per kapita bangsa Indonesia mencapai 0.365 kg (Kementerian Pertanian Republik Indonesia 2010). Indonesia dengan jumlah penduduk 237 641 300 jiwa setidaknya memerlukan 86 740 ton daging sapi per tahun (Badan Pusat Statistik 2010). Akan tetapi, laju peningkatan populasi sapi potong belum mampu untuk memenuhi kebutuhan daging dalam negeri. Hal ini merupakan faktor utama terjadinya impor sapi di Indonesia. Oleh karena itu, diperlukan upaya dalam meningkatkan kualitas dan kuantitas daging dalam bentuk sapi potong maupun karkas di Indonesia.
Permasalahan umum yang sering terjadi adalah ketersediaan dan kualitas pakan dengan kontinuitas rendah, di lain sisi limbah pertanian seperti jerami padi merupakan salah satu limbah pertanian yang potensial sebagai sumber energi yang dapat dimanfaatkan oleh ternak ruminansia karena ketersediaannya yang melimpah. Ketersediaan pakan yang harus selalu ada menjadi suatu pertimbangan tersendiri dalam pemenuhan kebutuhan ternak baik dalam segi nutrien maupun efektivitas pakan. Pemberian pakan hijauan pada ternak sapi potong saja tidak memenuhi kebutuhan nutrien ternak sehingga diperlukan penambahan konsentrat. Menurut Tillman et al. (1997), konsentrat merupakan suatu bahan makanan yang digunakan bersama bahan makanan lain untuk meningkatkan keserasian gizi dari keseluruhan makanan dan dimaksudkan untuk disatukan dan dicampur sebagai pelengkap. Akan tetapi, kondisi konsentrat sapi potong di peternakan rakyat belum memenuhi standar nutrisi untuk pertambahan bobot badan yang optimal.
Salah satu upaya perbaikan yang dapat dilakukan yaitu dengan penggunaan probiotik. Probiotik merupakan feed additive (imbuhan pakan) yang mengandung mikroorganisme hidup yang menguntungkan induk semang, dengan memperbaiki keseimbangan mikroorganisme di dalam saluran pencernaan. Manfaat lain dari probiotik yaitu mampu memperbaiki ekosistem rumen, meningkatkan efisiensi pakan akibat meningkatnya populasi bakteri rumen selulolitik dan meningkatkan status kesehatan ternak dengan terhambatnya bakteri patogen (FAO/WHO 2000). Penggunaan probiotik juga merupakan upaya alternatif yang dilakukan karena beberapa negara telah melakukan pelarangan penggunaan antibiotika sebagai growth promotor dan kecenderungan terjadinya resistensi bakteri-bakteri patogen terhadap antibiotik tertentu.
2
meneliti mekanisme fermentasi mikroba, dan mempelajari aksi terhadap faktor antinutrisi, suplemen pakan, dan aditif.
Penelitian ini bertujuan untuk melihat efek optimalisasi ransum berbasis jerami padi dan konsentrat peternak yang diberi suplemen probiotik padat atau cair terhadap fermentasi dan kecernaan in vitro.
METODE PENELITIAN
Alat
Peralatan yang digunakan adalah seperangkat alat-alat percobaan fermentasi dan kecernaan in vitro seperti timbangan digital, tabung fermentor, tutup karet berventilasi, shaker waterbath, tabung gas CO2, cawan porselen, oven 105 oC,
tanur listrik 600 oC, kertas saring Whatman No 41, cawan Conway, labu
Erlenmeyer, alat-alat destilasi, alat-alat titrasi, plastik kemasan, label, counting chamber, tabung Hungate, autoclave, sentrifuge.
Bahan
Bahan yang digunakan adalah cairan rumen segar sapi potong yang berasal dari rumah potong hewan (RPH) di Bubulak, probiotik padat, probiotik cair, larutan McDougall dengan pH 6.5 sampai 6.9, larutan pepsin HCl 0.2%, aquadest, larutan HgCl2 jenuh, larutan Na2CO3 jenuh, larutan H2SO4 0.005 N, asam borat
berindikator merah metil dan hijau bromo kresol, larutan HCl 0.5N, larutan H2SO4
15%, larutan NaOH 0.5 N, larutan indikator Phenolphtalein 0.1% (PP), larutan garam formalin (formal saline), media brain heart infusion (BHI), gas CO2,
trichloro acetic acid (TCA), dan sulfo salicylic acid (SSA).
Waktu dan Lokasi Penelitian
Penelitian dimulai dari bulan Januari 2013 hingga Agustus 2013. Penelitian dilaksanakan di Laboratorium Biokimia, Fisiologi dan Mikrobiologi, dan di Laboratorium Nutrisi Ternak Perah, Departemen Ilmu Nutrisi dan Teknologi Pakan, Fakultas Peternakan, Institut Pertanian Bogor, Bogor.
Prosedur Penelitian Pengambilan cairan rumen
3
Pembuatan larutan McDougall
Sejumlah 1 liter air destilasi dimasukkan ke dalam labu takar dan dimasukkan bahan-bahan sebagai berikut : NaHCO3 sebesar 9.8 g;
Na2HPO4.7H2O sebesar 4.6325 g; KCl sebesar 0.57 g; NaCl sebesar 0.47 g;
MgSO4.7H2O sebesar 0.12 g; CaCl2.2H2O sebesar 0.04 g. CaCl2.2H2O
ditambahkan paling akhir setelah bahan lainnya larut sempurna. Leher labu dicuci dengan air destilasi hingga permukaan air mencapai tanda tera untuk volume 1 liter. Selanjutnya campuran dikocok dengan gas CO2 perlahan-lahan dengan
melewatkannya untuk menurunkan pH hingga mencapai pH 6.8.
Pencernaan fermentatif
Percobaan fermentasi in vitro dilakukan dengan menggunakan metode Tilley and Terry (1963) yang dimodifikasi oleh Sutardi (1979). Metode Sutardi (1979) menggunakan fermentor berupa tabung polyetilen berkapasitas 50 ml yang kemudian diisi dengan 1 g sampel, 12 ml larutan McDougall dan 8 ml cairan rumen segar. Tabung lalu dialiri CO2 selama 30 detik dan ditutup dengan karet
berventilasi. Tabung kemudian dimasukkan ke dalam shaker waterbath pada suhu 390C untuk menciptakan suasana yang hampir sama dengan kondisi di dalam
rumen dan diinkubasi selama 4 jam. Sampel untuk pengamatan populasi bakteri total dan populasi protozoa diambil sebelum penambahan larutan HgCl2 jenuh.
Proses fermentasi dihentikan dengan meneteskan larutan HgCl2 jenuh sebanyak 2
tetes. Tabung fermentor disentrifuse pada kecepatan 3000 rpm selama 15 menit. Supernatan diambil untuk analisis konsentrasi NH3 dan Volatile fatty acid (VFA).
Pengukuran NH3
Konsentrasi NH3 diukur dengan menggunakan metode Mikrodifusi Conway
(General Laboratory Procedure, Department of Dairy Science University of Wisconsin 1969). Bibir dan tutup cawan Conway diolesi dengan vaselin. Sebanyak 1 ml supernatan diambil dan ditempatkan di salah satu ujung alur cawan Conway. Setelah itu 1 ml larutan Na2CO3 jenuh ditempatkan pada ujung lain
cawan Conway yang bersebelahan dengan supernatan (tidak boleh bercampur). Larutan asam borat berindikator merah metil dan hijau bromo kresol sebanyak 1 ml larutan ditempatkan dalam cawan kecil yang terletak di tengah cawan Conway. Cawan Conway lalu ditutup rapat hingga kedap udara, larutan Na2CO3 dicampur
dengan supernatan hingga merata dengan cara menggoyangkan dan memiringkan cawan tersebut. Setelah itu cawan dibiarkan dalam suhu kamar. Setelah 24 jam, tutup cawan dibuka, asam borat berindikator dititrasi dengan larutan H2SO4 0.005
N sampai terjadi perubahan warna dari biru menjadi merah. Konsentrasi NH3
dihitung berdasarkan rumus berikut:
Pengukuran volatile fatty acid (VFA)
4
Wisconsin 1969). Supernatan diambil sebanyak 5 ml dan dimasukkan ke dalam tabung destilasi. Larutan H2SO4 15% ditambahkan 1 ml, kemudian segera ditutup
dan dihubungkan labu pendingin. Segera setelah ditambahkan larutan H2SO4 ke
dalam supernatan, tabung destilasi dimasukkan ke dalam labu penyulingan yang berisi air mendidih (dipanaskan terus selama destilasi). Uap air panas akan mendesak VFA yang akan terkondensasi dalam pendingin. Cairan yang terbentuk ditampung dalam labu Erlenmeyer yang berisi 5 ml NaOH 0.5 N sampai mencapai 250 ml. Indikator PP ditambahkan sebanyak 2 tetes dan dititrasi dengan HCl 0.5 N sampai warna titrat berubah dari merah jambu menjadi tidak berwarna. Rumus berikut digunakan untuk menghitung konsentrasi VFA :
Keterangan:
a = volume titran blangko b = volume titran contoh
Perhitungan populasi bakteri total
Perhitungan populasi bakteri total dilakukan menggunakan metode Ogimoto and Imai (1981). Medium tumbuh BHI digunakan untuk menghitung populasi bakteri total. Medium BHI dibuat dengan cara mencampur BHI dengan bahan sumber nutrien mikroba lainnya, kemudian dimasukkan ke dalam botol Schott yang telah disterilkan dengan autoclave. Campuran tersebut dipanaskan sampai terjadi perubahan warna dari coklat menjadi merah dan menjadi coklat muda, lalu didinginkan sambil dialiri CO2. Selanjutnya media dimasukkan ke dalam tabung
Hungate masing-masing sebanyak 5 ml yang sebelumnya telah diisi agar Bacto sebanyak 0.15 g, kemudian media disterilkan dalam autoclave (suhu 121 ºC, 15 menit, tekanan 1,2 Kgf cm-3). Medium yang siap digunakan untuk pembiakan
bakteri, dimasukkan ke dalam penangas air (suhu 47 ºC) dan diinokulasi dengan sampel yang telah diencerkan. Populasi bakteri dapat dihitung dengan rumus :
Populasi bakteri (CFUml-1) = n x 10x 0.05 x 0.1
Keterangan :
n = jumlah koloni yang terdapat pada tabung seri pengenceran ke-x
Perhitungan populasi protozoa
Perhitungan populasi protozoa dilaksanakan dengan menggunakan metode Ogimoto and Imai (1981). Perhitungan populasi protozoa dilakukan dengan meneteskan sampel (2 tetes) yang telah dicampur dengan larutan garam formalin (TFBS) dengan rasio 1:1 pada counting chamber (haemacytometer). Larutan TFBS dibuat dari campuran formalin 4% ditambah larutan garam NaCl fisiologis 0.9% dalam 100 ml larutan. Protozoa yang dihitung adalah total dari protozoa yang terdapat dalam counting chamber dengan ketebalan 0.1 mm, luas kotak terkecil 0.0625 mm2 yang terdapat 16 kotak dan jumlah kotak yang dibaca
5
Protozoa ml-1 cairan rumen = 1000 x FP x C
0.1 x 0.0625 x 16 x 5
Keterangan
C = Jumlah protozoa terhitung FP = Faktor pengenceran
Pengukuran sintesis protein mikroba
Sintesis protein mikroba diukur dengan metode Shultz and Shultz (1969). Sintesis protein yang berupa non protein nitrogen (NPN) diukur dengan menggunakan TCA dan SSA. Larutan yang akan digunakan dibuat dengan mencampurkan larutan TCA 20% dan larutan SSA 2% dengan proporsi 50:50. Sebanyak 1 ml cairan sampel hasil inkubasi dicampur dengan 9 ml larutan TCA dan SSA, kemudian larutan ini dihomogenkan dengan vortex selama 2 menit. Larutan tersebut lalu disentrifuse dengan kecepatan 3000 rpm selama 15 menit. Supernatan dibuang dan endapan ditambah dengan 3 ml aquadest, kemudian ditambahkan 6 ml campuran TCA-SSA. Campuran ini dihomogenkan lagi dengan vortex selama 2 menit, kemudian disentrifuse pada kecepatan 3000 rpm selama 15 menit. Supernatannya dibuang dan endapannya dianalisis dengan metode Kjehldal mikro.
Pengukuran koefisien cerna bahan kering dan bahan organik
Koefisien Cerna Bahan Kering (KCBK) dan Bahan Organik (KCBO) diukur dengan metode Tilley and Terry (1963) yang dimodifikasi oleh Sutardi (1979). Proses fermentasi yang dilakukan untuk pengukuran KCBK dan KCBO sama seperti dalam proses fermentasi untuk mengukur fermentabilitas, hanya proses inkubasi dilakukan selama 24 jam. Setelah 24 jam proses fermentasi dihentikan dengan menambah larutan HgCl2 jenuh (2 tetes). Tabung fermentor lalu
disentrifuse (kecepatan 3000 rpm, 15 menit), supernatan lalu dibuang. Residu yang didapat lalu ditambahkan 20 ml larutan pepsin-HCl 0.2%. Campuran ini diinkubasi lagi selama 24 jam (39 oC), sisa pencernaan disaring dengan kertas
6
Peubah yang diamati
Peubah yang diamati yaitu konsentrasi NH3, konsentrasi VFA total, populasi
protozoa, populasi bakteri total, sintesis protein mikroba, KCBK, dan KCBO.
Analisis Data
Data yang diperoleh dianalisis dengan menggunakan sidik ragam (ANOVA) dan untuk mengetahui perbedaan antara perlakuan diuji dengan ortogonal kontras (Steel and Torrie 1993).
Penelitian ini terdiri atas dua faktor, yaitu Faktor A adalah pemberian ransum dengan rasio 60:40% antara jerami padi dan konsentrat: A1 = jerami padi + konsentrat kontrol (yang biasa digunakan oleh peternak), A2 = jerami padi + konsentrat optimal (berdasarkan NRC), A3 = jerami padi + konsentrat suboptimal. Faktor B merupakan perlakuan probiotik yaitu: B1 = tanpa probiotik (0%), B2 = probiotik padat (0.25% b/b), B3 = probiotik cair (0.10% v/b).
Model matematika yang digunakan adalah:
ßk = pengaruh perlakuan penambahan probiotik ke-k
αjßk = pengaruh interaksi antar peubah
εijk = galat percobaan untuk kelompok ke-i, pengaruh pakan ke-j
dan pengaruh perlakuan penambahan probiotik ke-k
HASIL DAN PEMBAHASAN
Karakteristik Probiotik
7
Tabel 1 Jenis dan jumlah mikroba dalam probiotik padat dan cair
Jenis Hasil Pengujian Probiotik
Padat (CFU g-1) Cair (CFU ml-1)
Total plate count 3.9 x 108 1.5 x 1010
Lactobacillus acidophilus 7.2 x 109 1.1 x 1010
Bifidobacterium sp. 4.9 x 109 7.0 x 105
Streptococcus thermophilus 5.6 x 107 1.0 x 1010
Bacillus sp. 4.0 x 105 -
Sumber: Suryahadi dan Tjakradidjaja (2012)
Bifidobacterium sp., Lactobacillus sp. termasuk dalam kategori Bakteri Asam Laktat (BAL). Bakteri asam laktat memiliki kemampuan sebagai antimikroba dengan cara memproduksi asam laktat, asam format, dan asam asetat; oleh karena itu pemberian probiotik yang mengandung BAL dapat meningkatkan kecernaan pada tubuh ternak (Jenie et al. 2001). Cho (2010) menjelaskan bahwa Streptococcus thermophilus memiliki sifat homofermentatif yang dapat memproduksi asam laktat, asam piruvat, dan juga dapat memproduksi asam folat yang tinggi yang berfungsi sebagai senyawa penting dalam memperbaiki sifat DNA. penambahan Bacillus sp. dalam ransum dapat memperbaiki produksi ternak dan efisiensi penggunaan pakan (Supriyati 2008).
Tabel 1 menunjukkan bahwa jumlah sel hidup lebih dari 107 sampai 109
CFU ml-1 sehingga produk probiotik yang digunakan pada penelitian ini memenuhi syarat sebagai probiotik. Jenis bakteri pada probiotik padat maupun cair tidak banyak perbedaan, hanya terdapat perbedaan jumlah. Adapun pemberian probiotik padat yaitu 0.25% (b/b), sedangkan pemberian probiotik cair yaitu 0.10% (v/b) sehingga jumlah sel hidup pada probiotik padat sebesar 0.975 × 108cfu g-1dan pada probiotik cair yaitu 1.5 × 108cfu ml-1. Perbedaan pemberian probiotik padat dan cair tersebut dimaksudkan agar jumlah bakteri yang diberikan seimbang antara probiotik padat dan cair.
Komposisi Ransum
Ransum yang digunakan yaitu campuran antara jerami padi dan konsentrat dengan rasio 60:40%. Tabel 2 menunjukkan presentase penggunaan bahan pakan. Rasio pemberian hijauan dan konsentrat bergantung kepada kualitas hijauan, perbandingan 60:40% (dalam bahan kering ransum) adalah pemberian yang baik; jika hijauan yang diberikan berkualitas rendah maka rasio pemberian pakan menjadi 55:45%; rasio dapat ditingkatkan menjadi 65:35% jika kualitas hijauan tinggi (Siregar 2008). Berdasarkan tabel NRC (2000), kebutuhan PK sapi potong dalam fase growing dan finishing dengan bobot 300 sampai 400 kg sebesar 7.4 sampai 14.4% dan kebutuhan TDN sebesar 50 sampai 80%.
8
jumlah produksi N mikroba dalam rumen. Arora (1995) menyatakan bahwa protein didalam pakan akan dihidrolisis oleh mikroba rumen menjadi asam amino, kemudian amonia yang dibebaskan akan digunakan untuk produksi N mikroba bersama energi dari VFA.
Tabel 2 Persentase penggunaan bahan pakan Bahan Pakan
PK = protein kasar; TDN = total digestible nutrient; BK = bahan kering.
Tabel 3 Analisis proksimat ransum yang digunakan Kandungan
1Hasil analisis Labolatorium Pengetahuan Bahan Makan Ternak, Fakultas Peternakan, Institut Pertanian
Bogor (2013); 2Perhitungan nilai TDN (SK>18% dan PK<20%): TDN = 70.6+0.259PK+1.10LK–
0.760SK+0.991BETN (Sutardi 2001 dalam Irawan 2002); BK = bahan kering; PK = protein kasar; SK = serat kasar; LK = lemak kasar; Beta-N = bahan ekstrak tanpa nitrogen; TDN = total digestible nutrient.
9
keliru akan menyebabkan tumbuhnya jamur, kapang, dan mikroorganisme lainnya sehingga dapat menurunkan kualitas ransum. Kerusakan selama penyimpanan meliputi kerusakan fisik, biologi, dan kimia (McDonald et al. 2002). Selain itu, penggunaan data proksimat bahan pakan berupa data sekunder memiliki kondisi yang tidak sama dengan bahan pakan yang digunakan pada saat formulasi ransum yang digunakan dalam penelitian. Ransum A2 dan A3 memiliki kadar PK yang sama. Namun, kandungan energi atau TDN dari ketiga ransum hampir sama dengan yang diharapkan.
Konsentrasi NH3
Berdasarkan hasil sidik ragam didapatkan bahwa perlakuan pakan tidak menunjukkan pengaruh yang nyata terhadap konsentrasi amonia. Hal ini menunjukkan bahwa pakan kontrol atau yang biasa digunakan peternak, pakan optimal yang sesuai dengan NRC tahun 2000 serta pakan suboptimal tidak berpengaruh pada konsentrasi amonia atau belum menunjukkan adanya perbedaan konsentrasi yang nyata di dalam rumen. Hal ini diduga karena kandungan nutrien khususnya protein kasar dari masing-masing ransum mempunyai taraf yang hampir sama (Tabel 3), sehingga protein yang dimanfaatkan untuk pembentukan amonia tidak jauh berbeda.
Konsentrasi amonia dipengaruhi oleh perlakuan probiotik (P<0.05). Uji ortogonal kontras menunjukkan bahwa suplementasi probiotik dapat meningkatkan konsentrasi amonia (P<0.01). Penggunaan probiotik cair 0.10% lebih baik untuk menstimulasi aktivitas mikroba rumen sehingga konsentrasi amonia lebih tinggi. Hal ini diduga karena probiotik cair yang ditambahkan dapat langsung dimanfaatkan di dalam rumen dibandingkan probiotik padat. Bentuk cairan akan memudahkan adaptasi bakteri probiotik untuk beraktivitas di dalam cairan rumen daripada bentuk padatan, karena bakteri dari probiotik padat harus melepaskan diri terlebih dahulu dari bahan penyalut dan beradaptasi dalam kondisi rumen.
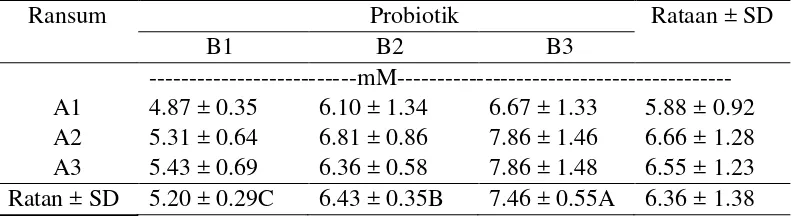
Tabel 4 Pengaruh perlakuan terhadap konsentrasi NH3
Ransum Probiotik Rataan ± SD
Angka-angka yang diikuti oleh huruf besar yang berbeda pada baris yang sama berbeda nyata pada taraf uji 1% (Uji Ortogonal Kontras), A1 = Pakan PK10%, A2 = pakan PK 12%, A3 = pakan PK 14%, B1 = tanpa probiotik; B2 = Probiotik padat (0.25%); B3 = Probiotik cair (0.1%).
Hau et al. (2005) mengemukakan bahwa pemberian probiotik dapat meningkatkan konsentrasi N-NH3. Konsentrasi N-NH3 meningkat diperkirakan
10
ikatan serat bahan pakan akan terlepas dan dicerna secara optimal. Lee and Salminen (2009) juga menyatakan bahwa untuk mendapatkan hasil yang optimal, standar probiotik padat yang ditambahkan sebesar 1011 CFU g-1. Jumlah tersebut merupakan penambahan probiotik cair pada kisaran 0.01 sampai 0.1% (b/b). Tabel 4 menunjukkan bahwa konsentrasi amonia berdasarkan hasil penelitian berkisar antara 5.20 sampai 7.46 mM. Konsentrasi ini sesuai untuk pembentukan protein mikroba menurut Sutardi (1979) yaitu 4 sampai 12 mM.
Konsentrasi Volatile Fatty Acid (VFA) Total
VFA merupakan sumber energi bagi ruminansia yang diproduksi bila ransum mengalami fermentasi dalam rumen. Menurut Hartati (1998), konsentrasi VFA total dalam cairan rumen dapat digunakan sebagai tolok ukur fermentabilitas pakan dan sangat erat kaitannya dengan aktivitas dan populasi mikroba rumen. Hasil sidik ragam menunjukkan bahwa konsentrasi VFA total tidak dipengaruhi oleh perlakuan ransum (faktor A) dan interaksi antara kedua faktor, namun konsentrasi VFA total dipengaruhi oleh perlakuan probiotik (P<0.01) dan uji ortogonal kontras memperlihatkan adanya perbedaan antara perlakuan tersebut. Perlakuan ransum yang tidak berpengaruh terhadap konsentrasi VFA diduga karena kandungan nutrien dalam masing-masing ransum relatif sama, sehingga pola fermentasi dalam rumen sama dan menghasilkan VFA total yang tidak jauh berbeda.
Konsentrasi VFA total tertinggi terdapat pada perlakuan ransum yang ditambah probiotik cair, sangat berbeda nyata (P<0.01) dengan perlakuan lainnya. Probiotik cair lebih cepat menstimulasi pertumbuhan mikroba sehingga dapat meningkatkan konsentrasi VFA total. Bakteri probiotik yang digunakan adalah bakteri asam laktat yang dapat menghasilkan asam laktat di dalam rumen sehingga pH rumen menurun dan menyebabkan bakteri patogen tidak berkembang bahkan mati. Menurut McDonald et al. (2002), asam laktat merupakan prekursor pembentukan asam propionat sehingga produk asam propionat meningkat. Propionat merupakan salah satu produk VFA, oleh karena itu VFA juga meningkat.
Selain menghasilkan asam laktat, bakteri asam laktat juga menghasilkan zat antimikroba yang dapat menghambat pertumbuhan dan membunuh bakteri patogen. Menurunnya bakteri patogen akan menyebabkan bakteri-bakteri menguntungkan di dalam rumen menjadi lebih optimal untuk beraktivitas dalam mencerna zat makanan. Hal ini sesuai dengan pendapat Lee and Salminen (2009) bahwa bakteri asam laktat menghasilkan zat antimikroba seperti asam organik, hidrogen peroksida, dan bakteriosin.
11
Konsentrasi ini termasuk ke dalam kisaran normal VFA yang dinyatakan oleh McDonald et al. (2002) dan France and Dijkstra (2005).
Konsentrasi VFA pada penelitian ini termasuk optimum untuk mikroba rumen. Kandungan VFA merupakan hasil aktivitas bakteri pada waktu melakukan fermentasi di dalam rumen, sehingga jika bakteri semakin banyak akan menghasilkan VFA yang semakin banyak pula. Hal ini sejalan dengan penelitian ini karena populasi bakteri total paling tinggi terdapat pada perlakuan probiotik cair dan konsentrasi VFA tertinggi juga terdapat pada perlakuan probiotik cair.
Tabel 5 Pengaruh perlakuan terhadap rataan VFA total
Ransum Probiotik Rataan ± SD
Angka-angka yang diikuti oleh huruf besar yang berbeda pada baris yang sama berbeda nyata pada taraf uji 1% (Uji Ortogonal Kontras), A1 = Pakan PK 10%, A2 = pakan PK 12%, A3 = pakan PK 14%, B1 = tanpa probiotik; B2 = Probiotik padat (0.25%); B3 = Probiotik cair (0.1%)
Bakteri Total
Populasi bakteri dalam cairan rumen yaitu 109 sampai 1010 ml-1 (Theodorou
and France 2005). Bakteri mempunyai fungsi dan produk yang bermacam-macam. Bakteri total yang terdapat dalam cairan rumen berdasarkan jenis bahan yang difermentasi dan hasil akhirnya terdiri dari: bakteri pemanfaat selulosa, bakteri pemanfaat hemiselulosa, bakteri pemanfaat pati, bakteri penghasil metan, bakteri pemanfaat gula, bakteri pemanfaat asam, bakteri pemanfaat asam, dan bakteri pemanfaat lipid (Dehority and Burk 2003). Pengaruh perlakuan terhadap rataan populasi bakteri total disajikan pada Tabel 6.
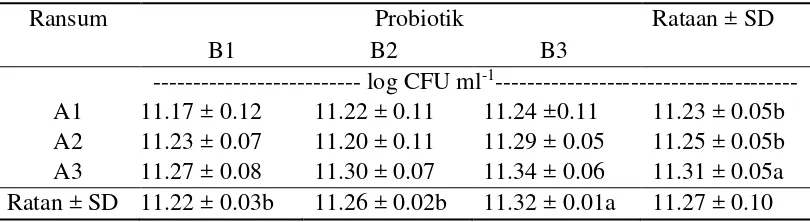
Tabel 6 Pengaruh perlakuan terhadap rataan populasi bakteri total
Ransum Probiotik Rataan ± SD
Angka-angka yang diikuti oleh huruf kecil yang berbeda pada baris yang sama berbeda nyata pada taraf uji 5% (Uji Ortogonal Kontras), A1 = Pakan PK10%, A2 = pakan PK 12%, A3 = pakan PK 14%, B1 = tanpa probiotik; B2 = Probiotik padat (0.25%); B3 = Probiotik cair (0.1%)
12
juga perlakuan pakan (P<0.05). Perlakuan pakan A3 memiliki pertumbuhan bakteri total yang paling baik. Perlakuan probiotik cair lebih baik dalam meningkatkan bakteri total dibandingkan probiotik padat dan ransum kontrol (tanpa perlakuan probiotik). Kenaikan dari bakteri total ini juga memicu naiknya konsentrasi NH3, konsentrasi VFA total, KCBK, dan KCBO.
Hal ini disebabkan bakteri patogen terhambat pertumbuhannya sehingga bakteri-bakteri menguntungkan di dalam rumen dapat tumbuh dan beraktivitas lebih optimal dalam mendegradasi bahan pakan dan dapat dimanfaatkan oleh tubuh ternak. Selain NH3, peningkatan VFA juga dapat dipengaruhi oleh
peningkatan populasi bakteri (Lee and Salminen 2009). Peningkatan populasi bakteri mengakibatkan peningkatan kecernaan bahan kering maupun organik.
Populasi Protozoa Total
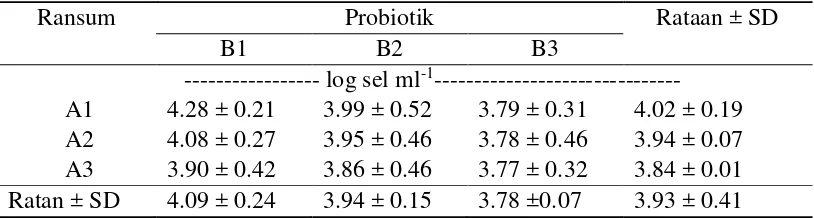
Protozoa rumen merupakan protista eukariotik yang membantu pencernaan karbohidrat yang mudah tercerna seperti pati dan sebagian serat. Protozoa dibagi berdasarkan fungsinya menjadi pengguna gula terlarut, pendegradasi pati, dan penghidrolisis ligno-selulosa (Kamra 2005). Mikroorganisme dalam rumen didominasi oleh populasi bakteri, protozoa dan fungi. Populasi protozoa antara 105 sampai 106 sel ml-1 (Theodorou and France 2005). Kisaran normal rataan populasi protozoa pada ternak ruminansia adalah 104 sampai 106 sel ml-1 cairan rumen (Kamra 2005). Jumlah populasi dalam penelitian ini sesuai dengan kisaran menurut Kamra (2005) yaitu 4 log sel ml-1 cairan rumen atau 104 sel ml-1 cairan rumen.
Tabel 7 Pengaruh perlakuan terhadap rataan populasi protozoa total
Ransum Probiotik Rataan ± SD
13
Pemberian probiotik tidak meningkatkan populasi protozoa atau menghambat pertumbuhan protozoa sehingga memberi kesempatan bakteri untuk hidup dan tumbuh lebih baik. Terdapat beberapa dampak positif dengan pengurangan jumlah protozoa di dalam cairan rumen, diantaranya adanya penurunan aktivitas proteolisis, metanogenesis berkurang, peningkatan jumlah bakteri kemungkinan untuk mengambil alih fungsi protozoa, dan adanya peningkatan efisiensi konversi pakan terutama ransum yang mengandung serat yang tinggi (Kamra 2005).
Sintesis Protein Mikroba
Sintesis protein mikroba penting untuk diketahui karena sel mikroba dan protein makanan yang lolos dari degradasi dalam rumen adalah sumber utama protein dan asam amino yang dibutuhkan ternak ruminansia. Menurut Fellner (2005), protein mikroba menyumbang sejumlah besar protein yang masuk ke dalam usus halus karena protein mikroba dapat mensuplai 50% lebih dari kebutuhan sapi. Leng and Kanjanapruthipong (1998) mengemukakan bahwa faktor utama yang mempengaruhi sintesis protein mikroba dalam rumen adalah penghancuran atau perusakan bakteri oleh protozoa sebagai predator, ketersediaan dan konsentrasi dari prekusor seperti asam nukleat, asam amino, glukosa, NH3,
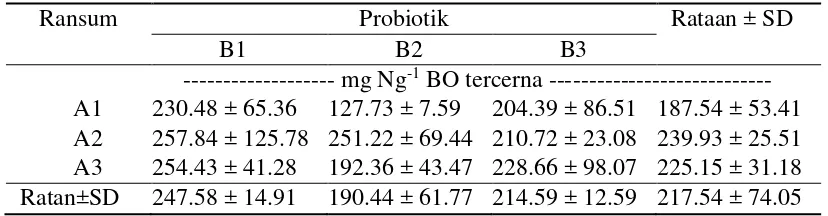
mineral dalam cairan rumen, dan kebutuhan hidup pokok mikroba rumen. Tabel 8 Pengaruh perlakuan terhadap rataan sintesis protein mikroba
Ransum Probiotik Rataan ± SD
B1 B2 B3
--- mg Ng-1 BO tercerna --- A1 230.48 ± 65.36 127.73 ± 7.59 204.39 ± 86.51 187.54 ± 53.41 A2 257.84 ± 125.78 251.22 ± 69.44 210.72 ± 23.08 239.93 ± 25.51 A3 254.43 ± 41.28 192.36 ± 43.47 228.66 ± 98.07 225.15 ± 31.18 Ratan±SD 247.58 ± 14.91 190.44 ± 61.77 214.59 ± 12.59 217.54 ± 74.05 A1 = Pakan PK10%, A2 = pakan PK 12%, A3 = pakan PK 14%, B1 = tanpa probiotik; B2 = Probiotik padat (0.25%); B3 = Probiotik cair (0.1%)
Hasil sidik ragam menunjukkan bahwa perlakuan pakan, suplementasi probiotik maupun interaksi antara perlakuan pakan dengan suplementasi probiotik tidak memiliki pengaruh terhadap sintesis protein mikroba. Hal ini dapat disimpulkan bahwa dengan suplementasi probiotik padat dan cair maupun perlakuan pakan belum mampu meningkatkan sintesis protein mikroba.
Kecernaan
14
dalam menentukan kualitas suatu bahan pakan. Rataan KCBK dan KCBO terdapat pada Tabel 9 dan Tabel 10.
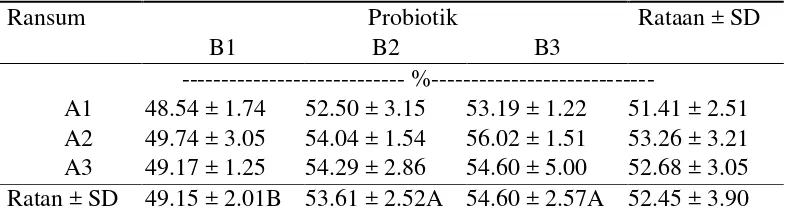
Tabel 9 Rataan kecernaan bahan kering
Ransum Probiotik Rataan ± SD Angka-angka yang diikuti oleh huruf besar yang berbeda pada baris yang sama berbeda nyata pada taraf uji 1% (Uji Ortogonal Kontras); A1 = Pakan PK 10%, A2 = pakan PK 12%, A3 = pakan PK 14%, B1 = tanpa probiotik; B2 = Probiotik padat (0.25%); B3 = Probiotik cair (0.1%)
Tabel 10 Rataan kecernaan bahan organik
Ransum Probiotik Rataan ± SD Angka-angka yang diikuti oleh huruf besar yang berbeda pada baris yang sama berbeda nyata pada taraf uji 1% (Uji Ortogonal Kontras); A1 = Pakan PK 10%, A2 = pakan PK 12%, A3 = pakan PK 14%, B1 = tanpa probiotik; B2 = Probiotik padat (0.25%); B3 = Probiotik cair (0.1%)
Berdasarkan hasil sidik ragam, perlakuan pakan dan interaksi antar kedua faktor tidak memberikan pengaruh yang nyata, namun perlakuan probiotik berpengaruh sangat nyata terhadap KCBK dan KCBO (P<0.01). Hal ini sesuai dengan pernyataan Hau et al. (2005), bahwa perlakuan probiotik nyata berpengaruh terhadap kecernaan zat-zat makanan. Perlakuan ransum yang diberi probiotik cair memiliki rataan KCBK dan KCBO tertinggi (P<0.01) sebesar 54.28% dan 54.60%. Hogan and Leche (1981) melaporkan bahwa komponen jerami padi tanpa perlakuan tambahan yang dapat dicerna secara in vitro sebesar 45% sampai 50%. Hal ini sejalan dengan ransum penelitian yaitu jerami padi dan konsentrat (60:40%) dan diperoleh KCBK di atas 45% sampai 50%, yaitu berkisar antara 51.51% sampai 54.28%.
15
Sebagai mikroorganisme alami, Lactobacillus sp. memberi pengaruh yang menguntungkan melalui produksi asam organik sehingga menghambat kerja bakteri patogen (Surung 2008). Harjanto (2005) menjelaskan bahwa semakin banyak mikroba yang terdapat dalam rumen maka jumlah pakan tercerna akan semakin tinggi pula. Sejalan dengan penelitian Harjanto (2005) bahwa didalam penelitian ini bakteri patogen aktivitasnya menurun di dalam rumen sehingga meningkatkan perkembangan dan aktivitas mikroba rumen. Peningkatan jumlah mikroba rumen dapat meningkatkan aktivitas mikroba rumen dalam memfermentasi bahan organik pakan menjadi senyawa sederhana yang mudah larut, dampaknya terjadi peningkatan dalam pencernaan dan penyerapan zat-zat organik.
SIMPULAN DAN SARAN
Simpulan
Perlakuan ransum A3 pada tingkatan PK 14% dan TDN 60% paling baik dalam meningkatkan populasi bakteri total. Penambahan probiotik cair (B3) ke dalam perlakuan pakan lebih efisien dalam meningkatkan konsentrasi NH3¸
konsentrasi VFA total, populasi bakteri, KCBK, dan KCBO.
Saran
Hasil penelitian menunjukkan perlu dilakukan penelitian lebih lanjut dengan penambahan taraf probiotik baik cair maupun padat untuk mendapatkan taraf yang paling optimal. Selain itu aplikasi percobaan in vivo perlu dilakukan untuk mengetahui seberapa jauh manfaatnya secara langsung pada ternak.
DAFTAR PUSTAKA
Arora SP. 1995. Pencernaan Mikroba pada Ruminansia.Murwani R, penerjemah; Srigandono B. Editor. Ed ke-2. Terjemahan dari: Microbial Digestion in Ruminant. Yogyakarta (ID): Gajah Mada Univ Pr.
[BPS] Badan Pusat Statistik. 2010. Penduduk Indonesia menurut Provinsi 1971, 1980, 1990, 1995, 2000 dan 2010.[diunduh 2013 April 20]; http://www.bps.go.id/tab_sub/view.php?kat=1&tabel=1&daftar=1&id_sub yek=12¬ab=1.
Cho SS, Finocchiaro ET. 2010. Handbook of Probiotics and Probiotics Ingredients: Health Benefits and Food Applications. New York (US): CRC Pr.
Dehority BA, Burk A. 2003. Rumen microbiology. Nottingham (UK): Nottingham Univ Pr.
16
Despal. 1993. Evaluasi nutrisi daun kembang sepatu (Hibiscus ross-sinensis LINN.) menggunakan teknik in sacco dan in vitro dengan pembanding beberapa legum pohon [skripsi]. Bogor (ID): Institut Pertanian Bogor. [FAO/WHO] Food and Agriculture Organization/World Health Organization.
2002. Guidelines for the Evaluation of Probiotics in Food. London, Ontario, Canada: FAO/WHO.
Fellner V. 2005. Rumen microbes and nutrient management. North Carolina State Univ, Animal Science Departemental Report.
France J, Dijkstra J. 2005.Volatille Fatty Acid Production. In: J Dijkstra, JM Forbes and J France (Eds). Quantitative Aspect for Ruminant Digestion and Metabolism. 2nd Ed. London (UK): CABI.
Harjanto K. 2005. Pengaruh penambanhan probiotik bio H+ terhadap kecernaan bahan kering dan bahan organik ransum sapi PFH jantan [skripsi]. Surakarta (ID): UNS.
Hartati E. 1998. Suplementasi minyak lemuru dan seng ke dalam ransum yang mengandung silase POD kakao dan urea untuk memacu pertumbuhan sapi Holstein jantan [disertasi]. Program Pascasarjana Institut Pertanian Bogor. Bogor.
Hau DK, Nenobasis M, Nulik J, Katipana NGF. 2005. Pengaruh probiotik terhadap kemampuan cerna mikroba rumen sapi bali. Seminar Nasional Teknologi Peternakan dan Veteriner. [Waktu dan tempat pertemuan tidak diketahui]. Kupang (ID): Universitas Nusa Cendana.
Hogan JP, Leche TF. 1981. Types of fibrous residues and their characteristic. In: The Utilization of Fibrous Agricultural Residues GR Pearce, editor. Canberra (AUS): Australian Government Publishing Service.
Hobson PN, Stewart CS. 1997. The Rumen Microbial Ecosystem. London (UK): Blackie Academic and Professional.
Irawan B. 2002. Suplemen Zn dan Cu organik pada ransum berbasis agroindustri untuk memacu pertumbuhan domba [tesis]. Bogor (ID): Institut Pertanian Bogor.
Jenie B, Atifah N, Suliantri. 2001. Peningkatan keamanan dan mutu pindang ikan kembung (Rastellinger sp.) dengan aplikasi kombinasi natrium asetat, bakteri asam laktat dan pengemasan vakum. J.Ilmu dan Teknologi Pangan 12(1) : 21-27.
Kamra DN. 2005. Rumen microbial ecosystem. Indian Veterinary Research Institute 89(1): 124–135.
[Kementan] Kementerian Pertanian Republik Indonesia.2013.Konsumsi Rata-rata per Kapita Setahun Beberapa Bahan Makanan di Indonesia Tahun 2007-2011.[diunduh 2013 April 20]. http://www.deptan.go.id/Indikator/tabe-15b-konsumsi-rata.pdf.
Lee YK, Salminen S. 2009. Handbook of Probiotics and Prebiotics. 2nd ed. New
Jersey (USA): John Wiley and Sons.
Leng RA, Kanjanapruthipong J. 1998. The effects of dietary urea on microbial populations in the rumen of sheep. Asian-Aust. J Anim Sci 11: 661-672. Lopez J. 2000. Probiotic in animal nutrition. J Anim Sci. 13 : 12-26.
17
[NRC] National Research Council. 2000. Nutrient Requirement of Beef Cattle. 8th
Ed. New York (US): National Academy Pr.
Ogimoto K, Imai S. 1981. Atlas of Rumen Microbiology. Tokyo (JPN): Japan Scientific Soc Pr.
Selly. 1994. Peningkatan kualitas pakan serat bermutu rendah dengan amoniasi dan inokulasi digesta rumen [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Shultz TA, Shultz E. 1969. Estimation of rumen microbial nitrogen by three analytical methods. J Dairy Sci. 53:781-784.
Siregar SB. 2008. Penggemukan Sapi. Jakarta (ID): Penebar Swadaya.
Steel RGD, Torrie JH. 1993. Prinsip dan Prosedur Statistika: Suatu Pendekatan Biometrik.Ed ke-3. M Syah, penerjemah. Jakarta (ID): PT Gramedia Pustaka Utama.
Supriyati. 2008. Pengaruh suplementasi probiotik dalam peningkatan produksi dan kualitas susu sapi perah di tingkat peternak. Semiloka Nasional Prospek Industri Sapi Perah Menuju Perdagangan Bebas – 2020. [Waktu dan tempat pertemuan tidak diketahui]. Bogor (ID): Balai penelitian Ternak. hlm 206-212.
Surung MY. 2008. Pengaruh dosis EM4 (effective microorganisms-4) dalam air minum terhadap berat badan ayam buras. J Agrisitem 4(2).
Surono IS.2004. Probiotik Susu Fermentasi dan Kesehatan. PT. Tri Cipta Karya. Jakarta.
Suryahadi, Tjakradidjaja AS. 2012. Pengujian Mutu dan Efikasi Probiotik Biofeed dan Turrimavita. Bogor (ID): Laporan Penelitian Kerjasama Centras LPPM IPB dengan CV Sinar Aras.
Sutardi T. 1979. Ketahanan Protein Bahan Makanan terhadap Degradasi oleh Mikroba Rumen dan Manfaatnya Bagi Produktivitas Ternak.Proceeding Seminar dan Penunjang Peternakan. Bogor (ID): Lembaga Penelitian Peternakan.
Sutardi T. 1980. Sapi Perah dan Pemberian Makanannya. Departemen Ilmu Nutrisi dan Makanan Ternak. Fakultas Peternakan. Bogor (ID): Institut Pertanian Bogor.
Theodorou MK, France J. 2005.Rumen Microorganism and their Interactions.In : J. Dijkstra, J. M. Forbes and J. France (Eds). Quantitative Aspect for Ruminant Digestion and Metabolism. 2nd ed. London (UK): CABI.
Tilley JMA, Terry RA. 1963. A two-stage tehnique for the in-vitro digestion of forage crops. J Grassland Soc.18:104-111.
Tillman AD, Reksohadiprodjo S,Hartadi H. 1997. Tabel Komposisi Pakan untuk Indonesia.Cetakan keempat. Yogyakarta [ID]: Gadjah Mada Univ Pr. Verschuere L, Rombaut G, Sorgeloos P, Verstraete W. 2000. Probiotic Bacteria
18
Lampiran 1 Analisis ragam (ANOVA) terhadap konsentrasi amonia SK db JK KT Fhit F0.05 F0.01
Total 35 66.258
Kelompok 3 11.746 3.915 5.152 3.009 4.718 ** Perlakuan 8 36.273 4.534 5.966 2.355 3.363 ** Faktor A 2 4.272 2.136 2.811 3.403 5.614 ns Faktor B 2 30.780 15.390 20.251 3.403 5.614 ** 1 vs 2 3 1 24.297 24.297 31.972 4.260 7.823 ** 2 vs 3 1 6.483 6.483 8.530 4.260 7.823 ** A*B 4 1.221 0.305 0.402 2.776 4.218 ns Galat 24 18.239 0.760
** sangat berbeda nyata (P<0.01); * berbeda nyata P(0.05); nstidak signifikan; SK: sumber
keragaman, db: derajat bebas, JK: jumlah kuadrat, KT: kuadrat tengah, Fhit: nilai F.
Lampiran 2 Uji ortogonal kontras perlakuan probiotik
B1 B2 B3
62.43 77.10 89.58 C Q JK
1 vs 2 3 2.00 -1.00 -1.00 -41.83 6.00 24.30 2 vs 3 0.00 1.00 -1.00 -12.47 2.00 6.48
JK Total 30.78
B1 = Tanpa probiotik; B2 = Probiotik padat (0.25%); B3 = Probiotik cair (0.1%)
Lampiran 3 Analisis ragam (ANOVA) terhadap konsentrasi VFA total SK db JK KT Fhit F0.05 F0.01
Total 35 17069.117 Kelompok 3 123.424 41.14125 0.201 3.0088 4.7181 ns Perlakuan 8 12032.661 1504.083 7.347 2.3551 3.3629 ** Faktor A 2 1134.014 567.0072 2.770 3.4028 5.6136 ns Faktor B 2 10630.028 5315.014 25.964 3.4028 5.6136 ** 1 vs 2 3 1 8056.786 8056.786 39.357 4.2597 7.8229 ** 2 vs 3 1 2573.242 2573.242 12.570 4.2597 7.8229 ** A*B 4 268.619 67.15474 0.328 2.7763 4.2184 ns Galat 24 4913.032 204.7096
** sangat berbeda nyata (P<0.01); * berbeda nyata P(0.05); ns tidak signifikan; SK: sumber
keragaman, db: derajat bebas, JK: jumlah kuadrat, KT: kuadrat tengah, Fhit: nilai F.
Lampiran 4 Uji ortogonal kontras perlakuan probiotik
B1 B2 B3
1057.62 1314.18 1562.69 c Q JK
1 vs 2 3 2.00 -1.00 -1.00 -761.64 6.00 8056.79 2 vs 3 0.00 1.00 -1.00 -248.51 2.00 2573.242 JK Total 10630.03
19
Lampiran 5 Analisis ragam (ANOVA) terhadap populasi protozoa total
SK db JK KT Fhit F0.05 F0.01
Total 35 5.89
Kelompok 3 3.03 1.01 12.288 3.01 4.72 **
Perlakuan 8 0.88 0.11 1.338 2.36 3.36 ns
Faktor A 2 0.55 0.28 3.357 3.40 5.61 ns
Faktor B 2 0.19 0.10 1.170 3.40 5.61 ns
A*B 4 0.14 0.03 0.413 2.78 4.22 ns
Galat 24 1.976 0.08
** sangat berbeda nyata (P<0.01); * berbeda nyata P(0.05); ns tidak signifikan; SK: sumber
keragaman, db: derajat bebas, JK: jumlah kuadrat, KT: kuadrat tengah, Fhit: nilai F.
Lampiran 6 Analisis ragam (ANOVA) terhadap populasi bakteri total
SK db JK KT Fhit F0.01 F0.05
Total 35 0.36
Kelompok 3 0.09 0.03 4.766 4.72 3.01 **
Perlakuan 8 0.11 0.01 2.087 3.36 2.36 ns
Faktor A 2 0.05 0.02 3.510 5.61 3.40 *
1 2 VS 3 1 0.04 0.04 6.180 7.82 4.26 * 1 VS 2 1 0.004 0.00 0.618 7.82 4.26 ns
Faktor B 2 0.06 0.03 4.269 5.61 3.40 *
1 2 VS 3 1 0.05 0.05 7.725 7.82 4.26 * 1 VS 2 1 0.007 0.01 1.081 7.82 4.26 ns
A*B 4 0.01 0.002 0.284 4.22 2.78 ns
Galat 24 0.155 0.01
** sangat berbeda nyata (P<0.01); * berbeda nyata P(0.05); ns tidak signifikan; SK: sumber
keragaman, db: derajat bebas, JK: jumlah kuadrat, KT: kuadrat tengah, Fhit: nilai F.
Lampiran 7 Uji ortogonal kontras perlakuan pakan
A1 A2 A3
134.75 135.05 135.77 C Q JK 1 2 VS 3 -1.00 -1.00 2.00 1.73 6.00 0.04 1 VS 2 -1.00 1.00 0.00 0.30 2.00 0.004
JK Total 0.05
A1 = Ransum kontrol; A2 = Ransum optimal; A3 = Ransum suboptimal
Lampiran 8 Uji ortogonal kontras perlakuan probiotik
B1 B2 B3
134.67 135.08 135.81 C Q JK 1 2 VS 3 -1.00 -1.00 2.00 1.86 6.00 0.05 1 VS 2 -1.00 1.00 0.00 0.41 2.00 0.007
JK Total 0.06
20
Lampiran 9 Analisis ragam (ANOVA)perlakuan terhadap sintesis protein mikroba
SK db JK KT Fhit F0.05 F0.01
Total 35 191919.180
Kelompok 2 648.293 324.15 0.059 3.39 5.57 ns
Perlakuan 8 53317.488 6664.69 1.208 2.34 3.32 ns
Faktor A 2 17512.959 8756.48 1.587 3.39 5.57 ns
Faktor B 2 19748.977 9874.49 1.789 3.39 5.57 ns 12 vs 3 1 18693.870 18693.87 3.388 4.24 7.77 ns 1 vs 2 1 6147.356 6147.36 1.114 4.24 7.77 ns
A*B 4 16055.552 4013.89 0.727 2.76 4.18 ns
Galat 25 137953.399 5518.14
** sangat berbeda nyata (P<0.01); * berbeda nyata P(0.05); ns tidak signifikan; SK: sumber
keragaman, db: derajat bebas, JK: jumlah kuadrat, KT: kuadrat tengah, Fhit: nilai F.
Lampiran 10 Analisis ragam (ANOVA)perlakuan terhadap koefisien bahan kering SK db JK KT Fhit F0.01 F0.05
Total 35 741.292 21.180
Kelompok 2 69.431 34.716 5.529 5.568 3.385 * Perlakuan 8 514.894 64.362 10.251 3.324 2.337 ** A 2 27.630 13.815 2.200 5.568 3.385 ns B 2 472.667 236.333 37.640 5.568 3.385 ** 1 2 VS 3 1 365.073 365.073 58.145 7.770 4.242 ** 1 VS 2 1 107.594 107.594 17.136 7.770 4.242 ** AB 4 14.597 3.649 0.581 4.177 2.759 ns Galat 25 156.968 6.279
** sangat berbeda nyata (P<0.01); * berbeda nyata P(0.05); ns tidak signifikan; SK: sumber
keragaman, db: derajat bebas, JK: jumlah kuadrat, KT: kuadrat tengah, Fhit: nilai F.
Lampiran 11 Uji ortogonal kontras perlakuan probiotik
B1 B2 B3
611.76 662.57 718.23 C Q JK 1 2 VS 3 -1.00 -1.00 2.00 162.13 6.00 365.07 1 VS 2 -1.00 1.00 0.00 50.82 2.00 107.594 JK Total 472.67
21
Lampiran 12 Analisis ragam (ANOVA) perlakuan terhadap koefisien bahan organik
SK db JK KT Fhit F0.01 F0.05
Total 26 531.656 20.448
Perlakuan 8 320.335 40.042 3.323 3.890 2.591 * A 2 23.854 11.927 0.990 6.226 3.634 Ns B 2 290.726 145.363 12.063 6.226 3.634 ** 1 VS 2 3 1 240.497 240.497 19.958 8.531 4.494 ** 2 VS 3 1 50.229 50.229 4.168 8.531 4.494 Ns AB 4 5.756 1.439 0.119 4.773 3.007 Ns Kelompok 2 18.519 9.260 0.768 6.226 3.634 Ns Galat 16 192.801 12.050
** sangat berbeda nyata (P<0.01); * berbeda nyata P(0.05); ns tidak signifikan; SK: sumber
keragaman, db: derajat bebas, JK: jumlah kuadrat, KT: kuadrat tengah, Fhit: nilai F.
Lampiran 13 Uji ortogonal kontras perlakuan probiotik
B1 B2 B3
589.35 637.79 672.51 C Q JK 1 VS 2 3 2.00 -1.00 -1.00 -131.59 6.00 240.50 2 VS 3 0.00 1.00 -1.00 -34.72 2.00 50.229
JKTotal 290.73
22
RIWAYAT HIDUP
Penulis dilahirkan di Bandar Lampung,Lampung pada tanggal 21 Maret 1990. Penulis merupakan anak keempat dari lima bersaudara dari pasangan Bapak Ir. H. Dancik Ibrahim dan Ibu Hj. Ten Aswaliah SPd. Penulis menempuh pendidikan dasar di SD Kartika II-5 pada tahun 1996-2002. Pendidikan dilanjutkan di SMP Negeri 2 Bandar Lampung hingga tahun 2003 dan dilanjutkan kembali di MTs Al-Zaytun hingga tahun 2007. Pendidikan lanjutan menengah atas diselesaikan pada tahun 2009 di SMA Negeri 5 Kota Bogor.
Penulis diterima di IPB pada tahun 2009 melalui jalur
Seleksi Nasional Masuk Perguruan Tinggi Negeri (SNMPTN).Selama kuliah, penulis pernah menjadi Ketua Departemen Budaya Olahraga dan Seni BEM Fakultas Peternakan IPB periode 2012/2013. Penulis juga aktif dalam kegiatan ekstra dan intra kampus lainnya. Prestasi yang dicapai penulis yaitu menerima dana penelitian untuk program kreatifitas mahasiswa (PKM-P) pada tahun 2011 serta mendapat juara 1 Band lomba cipta lagu dalam IPB Art Contest tahun 2012 mewakili Fakultas Peternakan.Penulis juga pernah menjadi asisten praktikum mata kuliah Formulasi Ransum pada tahun ajaran 2012/2013.
UCAPAN TERIMA KASIH
Alhamdulillahirabbil’alamin, puji dan syukur penulis panjatkan kehadirat