Bonardo Tigor Sagala. Seleksi dan Uji Aktivitas Fiksasi Nitrogen (N2) Bakteri Metanotrof Asal
Sawah pada Konsentrasi Oksigen (O2) Berbeda. Dibimbing oleh IMAN RUSMANA dan ALINA
AKHDIYA.
Bakteri metanotrof merupakan bakteri pengoksidasi CH4. Enzim spesifik pengoksidasi
metan pada bakteri ini adalah metan monooksigenase (MMO) yang mampu menambahkan satu atom oksigen ke molekul CH4untuk membentuk senyawa metanol. Selain itu, bakteri metanotrof
juga dapat memfiksasi nitrogen. Bakteri metanotrof type II dan type X dapat memfiksasi nitrogen menggunakan enzim nitrogenase. Enzim nitrogenase sangat peka oksigen. Sebanyak 19 isolat bakteri metanotrof berhasil diremajakan dan diuji aktivitas fiksasi N24nya pada konsentrasi oksigen
yang berbeda. Aktivitas fiksasi N2ditentukan berdasarkan akumulasi amonium pada media NMS
bebas nitrogen. Akumulasi amonium yang tinggi ditemukan pada kultur isolat BGM 1, BGM 3, BGM 5, dan BGM 9. Akumulasi amonium tertinggi dimiliki oleh kultur isolat BGM 9 pada konsentrasi oksigen 30% yaitu 88,816 <M. Kerapatan sel tertinggi dimiliki oleh isolat BGM 5 dengan OD 0,103 pada konsentrasi oksigen 80%.
Kata kunci: Metan, bakteri metanotrof, fiksasi nitrogen, Nitrogenase
Bonardo Tigor Sagala. Selection and Nitrogen Fixing (N2) Activity Test of Methanotrophic
Bacteria from Rice Field Under Different Concentration of Oxygen. Under supervision of IMAN RUSMANA and ALINA AKHDIYA.
Methanotrophic bacteria is methane oxydizing bacteria. This bacteria has a specific enzyme known as methane monooksigenase (MMO) catalizing reaction of CH4 and O2 to methanol.
Methanotrophic bacteria also have ability to fix nitrogen. Methanotrophic bacteria type II and type X could fix nitrogen using nitrogenase enzyme. This enzyme is very sensitive to oxygen. As many as 19 isolates of methanotrophic bacteria was recultured and determined their nitrogen fixation activity at different oxygen concentration. Nitrogen fixation activity was determined by measuring ammonium accumulation in NMS free nitrogen medium. High ammonium accumulation was found at cultures of BGM 1, BGM 3, BGM 5, dan BGM 9 isolates. The highest ammonium accumulation (88,816 <M) was showed by BGM 9 isolate on 30% oxygen concentration and the highest cell density was showed by BGM 5 isolate (OD 0,103) on 80% oxygen concentration.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Judul
: Seleksi dan Uji Aktivitas Fiksasi Nitrogen (N
2) Bakteri
Metanotrof Asal Sawah pada Konsentrasi Oksigen (O
2) Berbeda.
Nama
: Bonardo Tigor Sagala
NIM
: G34051698
Disetujui:
Pembimbing I,
Pembimbing II,
(Dr. Ir. Iman Rusmana M.Si)
(Alina Akhdiya M.Si)
NIP 196507201991031002
NIP 196812082001122001
Diketahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Dr. Drh. Hasim, DEA
NIP 196103281986011002
Puji syukur penulis panjatkan kepada Tuhan YME yang telah memberi rahmat dan kemudahan dalam menyelesaikan karya ilmiah ini. Tema penelitian penulis yaitu tentang reduksi emisi gas rumah kaca dari lahan sawah, dengan judul Seleksi dan Uji Aktivitas Fiksasi Nitrogen (N2) Bakteri Metanotrof Asal Sawah pada Konsentrasi Oksigen (O2) Berbeda. Penelitian ini
dilaksanakan mulai bulan April sampai Agustus 2009 di Laboratorium Mikrobiologi Departemen Biologi, Institut Pertanian Bogor.
Penulis mengucapkan terima kasih kepada Bapak Dr. Ir. Iman Rusmana, M.Si. dan Ibu Alina Akhdiya, M.Si. selaku pembimbing atas saran dan bimbingannya dalam pelaksanaan penelitian dan penyusunan karya ilmiah ini. Terima kasih juga kepada Papah, Mamah (alm), Mamah, Mba Dian, Bang Haris, Inang Uda Lina atas doa, dukungan, dan segala cintanya. Terima kasih kepada Yohanna, Bu Ratna, Mba Rika, Ade, Tika, Lia, Dina, Puji, Bram, Una, Meli, Yurin, Nida, Ason, Bu Maysaroh, Pak Hadi, Ka Fina, keluarga besar laboratorium mikrobiologi FMIPA IPB, keluarga besar laboratorium Fisologi Tumbuhan FMIPA IPB, alumni dan adik4adik di SMAN 1 Depok, serta sahabat4sahabatku tercinta di Biologi 42 atas segala bantuan yang telah diberikan.
Semoga karya ilmiah ini dapat bermanfaat.
Penulis dilahirkan di Bandar Lampung pada tanggal 01 Desember 1986 dari ayah Robert Bulthon Sagala dan ibu Sri Banundari (alm). Penulis merupakan anak kedua dari dua bersaudara. Tahun 2005 penulis lulus dari SMU Negeri 1 Depok dan lolos seleksi masuk IPB melalui jalur Seleksi Penerimaan Mahasiswa Baru IPB (SPMB) pada Departemen Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, penulis aktif sebagai staf Bioworld Himpunan Mahasiswa Biologi (Himabio) pada tahun 200742008, staf Komisi Kesenian Persekutuan Mahasiswa Kristen IPB (PMK) pada tahun 200842009. Penulis juga aktif dalam beberapa kegiatan yang diadakan oleh kampus IPB.
!
DAFTAR TABEL...vi
DAFTAR GAMBAR ...vi
DAFTAR LAMPIRAN ...vi
PENDAHULUAN ...1
Latar Belakang ...1
Tujuan...1
Waktu dan Tempat ...1
BAHAN DAN METODE...1
Bahan...1
Metode ...2
HASIL DAN PEMBAHASAN ...3
Hasil...3
Peremajaan Isolat ...3
Aktivitas Fiksasi N
2Bakteri Metanotrof...3
Aktivitas Fiksasi N
2Isolat Terpilih pada Konsentrasi O
2Berbeda...4
Pembahasan ...4
SIMPULAN...5
SARAN ...5
DAFTAR PUSTAKA ...5
vi
!
1 Kerapatan sel (OD
620) dan akumulasi amonium pada kultur bakteri metanotrof
pada media agar NMS dengan masa inkubasi 14 hari pada suhu 27429
oC ……. 3
!
1 Morfologi koloni isolat BGM 1 pada media agar NMS dengan masa inkubasi
lima hari pada suhu 27429
oC ………...…….………...… 3
2 Kerapatan sel kultur
BGM 1,
BGM 3,
BGM 5,
BGM 9
pada beberapa konsentrasi oksigen menggunakan media agar NMS
dengan masa inkubasi 14 hari pada suhu 27429
oC.……..…... 4
3 Konsentrasi amonium dalam kultur
BGM 1,
BGM 3,
BGM 5,
BGM 9 pada beberapa konsentrasi oksigen menggunakan media agar NMS
dengan masa inkubasi 14 hari pada suhu 27429
oC………...………... 4
!
1 Kerapatan sel kultur isolat terpilih pada beberapa konsentrasi oksigen... 8
2 Akumulasi amonium dalam kultur metanotrof pada beberapa konsentrasi
1
" # $ % !&
Metan (CH4) merupakan salah satu gas
rumah kaca utama yang dapat menyerap radiasi infra merah sehingga berkontribusi
terhadap pemanasan global.
,
IPCC (1992) menyatakan bahwa metan
menempati urutan ketiga dalam hal
pemanasan global setelah CO2 dan
(CFC). Salah satu sumber emisi metan berasal dari tanah sawah, oleh karena itu perlu upaya untuk menurunkan laju emisi tersebut tanpa mengorbankan sistem pertanian lahan sawah dan produksi beras Indonesia. Secara alami metan diproduksi di lingkungan anaerob oleh bakteri metanogen, sebesar 43% emisi metan ke atmosfer berasal dari lahan basah dan sawah (Wild 1995). Jumlah metan yang berada di atmosfer 20% berasal dari
sawah dan 20% dari lahan rawa
(Notohadiprawiro 2006).
Konsentrasi metan di atmosfer pada tahun
1990 adalah 1,72 ppm dengan laju
peningkatan 1% per tahun, sedangkan untuk karbon dioksida pada tahun yang sama sebesar 354 ppm dengan laju peningkatan
0,5% per tahun (Lelieveld . 1993).
Kontribusi peningkatan konsentrasi tersebut terhadap pemanasan global selama seratus tahun terakhir diperkirakan sebesar 19% metan dan 50% untuk CO2 (Bouwman &
Sombroek 1990). Bahkan menurut Lelieveld (1993) dan Hanson & Hanson (1996) kontribusi CH4 dalam perubahan iklim
mencapai 26 kali dari CO2. Hal ini disebabkan
karena CH4 lebih efektif menyerap radiasi
pada panjang gelombang 4 4 100 nm (irradiasi sinar infra merah) dibandingkan dengan CO2.
Laju peningkatan konsentrasi metan di atmosfer dua kali lipat dibandingkan dengan CO2, oleh karena itu perlu diantisipasi
pengaruhnya terhadap perubahan iklim global di masa mendatang.
Proses oksidasi metan dilakukan oleh bakteri metanotrof pada kondisi aerobik yang terdapat pada lapisan permukaan sedimen sawah (Conrad & Rothfus 1991). Bakteri metanotrof memanfaatkan metan sebagai donor elektron untuk menghasilkan energi dan sebagai sumber karbonnya. Oksidasi CH4
menjadi CO2oleh bakteri metanotrof di lahan
sawah dapat mencapai 80 % dari CH4 yang
diproduksi oleh bakteri metanogen (Conrad & Rothfus 1991). Proses oksidasi metan tersebut dapat dilakukan oleh berbagai macam bakteri
metanotrof seperti ,
, (Rao 1979).
Bakteri metanotrof dikelompokkan
menjadi tiga, yaitu metanotrof tipe I, tipe II, dan tipe X. Pengelompokkan ini berdasarkan atas perbedaan internal membran, lintasan asimilasi formaldehid, dan siklus asam sitratnya. Contoh bakteri metanotrof tipe I
adalah dan ,
contoh tipe II adalah dan
, dan contoh tipe X adalah (Hanson & Hanson, 1996).
Bakteri metanotrof tipe II and tipe X memiliki kemampuan untuk memfiksasi N2
(Hanson & Hanson, 1996). Fiksasi nitrogen adalah proses penambatan nitrogen bebas yang diubah menjadi amonium sehingga dapat dimanfaatkan sebagai sumber nitrogen oleh
tanaman. Proses fiksasi nitrogen
membutuhkan kondisi yang bebas oksigen, karena keberadaan oksigen akan menghambat
ekspresi gen yang menyandikan enzim
nitrogenase yang mengkatalisis proses fiksasi nitrogen.
'(' !
Penelitian ini bertujuan mengetahui aktivitas fiksasi nitrogen (N2) bakteri
metanotrof asal sawah wilayah Bogor dan Sukabumi pada konsentrasi oksigen (O2) yang
berbeda.
%"' ) ! $ * "
Penelitian dilakukan pada bulan April
hingga Agustus 2009 di Laboratorium
Mikrobiologi Departemen Biologi FMIPA IPB.
+ !
Bahan yang digunakan adalah media
selektif (MgSO4.7H2O
1.0 g/L, CaCl2.6H2O 0.2 g/L, KNO31.0 g/L,
KH2PO40.272 g/L, Na2HPO4.12 H2O 0.717
g/L, NH4Cl 4.0 mg/L, Na2EDTA 0.5 g/L,
FeSO4. 7H2O 0.2 g/L, H3BO3 0.03 g/L,
CoCl2.6H2O 0.02 g/L, ZnSO4.7H2O 0.01 g/L,
MnCl2. 4H2O 3.0 mg/L, Na2MoO4.2H2O 3.0
mg/L, NiCl2.6H2O 2.0 mg/L, CaCl2.2H2O 1.0
mg/L, dan Bacto agar 20 g/L),larutangaram fisiologis, larutan NH4Cl 100 ppm, Milli4Q
water, larutan fenol4alkohol (C6H5OH) 10% ,
larutan Natrium Dihidro Nitroprusid
(Na2[Fe(CN)NO]2. H2O) 0,5 %, dan larutan
2
(C6H5Na3O7.2H2O) 20% dan Natrium
Hipoklorit (NaOCl2) 5,25 %.
$",)$
$#$ ( ! -, ".
Isolat4isolat bakteri metanotrof asal sawah BGM 1, BGM 2, BGM 3, BGM 4, BGM 5, BGM 6, BGM 9, BGM 12, SKM 1, SKM 2, SKM 4, SKM 5, SKM 7, SKM 9, SKM 10, SKM 14, SKM 15, SKM 16, SKM 18 (Hapsari 2008) diremajakan pada medium
agar (NMS) + 1%
metanol dan diinkubasi pada suhu ruang selama 547 hari.
$ $%-. %"$#. $" !,"#,/ $ /.%- -. 0
Sebanyak 142 lup isolat bakteri metanotrof dari media agar miring NMS diinokulasikan ke dalam tabung eppendorf steril yang berisi 1 ml larutan garam fisiologis steril selanjutnya
eppendorf divortex hingga homogen.
Sebanyak 500 <l biakan dari eppendorf diinokulasikan ke dalam botol serum 76 ml
yang ditutup berisi 10 ml
media cair NMS steril tanpa mengandung unsur N. Inkubasi dilakukan pada suhu ruang menggunakan alat ! selama dua minggu.
Kerapatan selnya diukur menggunakan
spektrofotometer " 20 Perancis λ 20041000 nm pada OD620 dengan blanko
medium NMS cair.
$!&'%'# ! ' + ,!.' 1 !&
. %' ' -. ) . % !0
Sebanyak 1 ml sampel kultur diencerkan dengan 4 ml Milli4Q water dalam botol serum bertutup karet. Sampel ditambah dengan 0.2 ml fenol4alkohol 10% selanjutnya divortex
hingga homogen. Setelah itu sampel
ditambahkan dengan 0,2 ml Na4nitroprusid 0.5% kemudian divortex kembali hingga homogen. Selanjutnya sampel ditambahkan 0.5 ml campuran Na4sitrat : Na4hipoklorit (1:4). Selanjutnya sampel didiamkan selama satu jam sampai berubah menjadi warna biru (Cleseri . 1989). Setelah semua sampel
berwarna biru kemudian diukur kadar
amoniumnya menggunakan spetrofotometer
(640 nm) dan blanko Milli4Q water.
Selanjutnya dipilih empat isolat terbaik dari hasil pengukuran amonium yang diakumulasi tersebut, yaitu: BGM 1, BGM 3, BGM 5, dan BGM 9.
(. $ *' ! .%- -. -, " $#*. .+ * ) ,!-$!"# -. $#2$) 0
Pengukuran aktivitas fiksasi N2 pada
konsentrasi oksigen berbeda dilakukan pada
botol serum steril 76 ml yang ditutup dengan . Botol serum steril volume 76 ml diisi dengan 10 ml medium NMS cair tanpa unsur nitrogen. Kemudian udara saturasi pada masing4masing botol dikondisikan menjadi 10%, 30%, 50%, 80%, dan 100%. Pada botol serum yang ditutup saturasi udara 10% dan
30%, komposisi gas di botol
serum dibuat kondisi anaerobik dengan cara menghilangkan oksigen yang berada di botol serum. Sebelum gas dimasukkan, terlebih dahulu gas disaring dengan filter steril diameter 47 mm dengan pori 0.45 <m. Pengkondisian udara saturasi dilakukan dengan memperhitungkan volume
botol serum. Udara saturasi dimasukkan pada masing4masing botol serum yang telah diberi perlakuan pembebasan oksigen sebanyak 6.6 ml dan 19.8 ml, sedangkan pada saturasi udara 50% dan 80% dibuat dengan cara udara saturasi dimasukkan pada masing4masing botol serum sebanyak 33 ml dan 13.2 ml, sedangkan untuk udara saturasi 100% tidak diberi perlakuan gas nitrogen murni pada botol serum.
Sebanyak 142 lup isolat bakteri metanotrof dari media agar miring NMS diinokulasikan ke dalam tabung eppendorf steril yang berisi 1 ml garam fisiologis steril lalu eppendorf divortex sampai homogen. Kemudian biakan dalam eppendorf diinokulasikan sebanyak 500
<l dengan cara menyuntikkannya
menggunakan steril 3 ml dari
eppendorf tersebut ke dalam botol serum 76 ml berisi 10 ml media cair NMS steril tanpa unsur nitrogen.
Sampel diambil dengan menggunakan steril sebanyak 2.5 ml untuk diukur OD sel dengan panjang gelombang OD620
menggunakan spektrofotometer sebelum kultur diinkubasi. Selanjutnya kultur diinkubasi selama dua minggu di atas mesin
! pada suhu ruang. Pengukuran jumlah amonium yang diakumulasi dalam kultur dilakukan menggunakan spektrofotometer dengan panjang gelombang 640 nm dan
pengukuran OD sel dengan panjang
gelombang OD620pada akhir inkubasi. Jumlah
amonium yang diakumulasi dihitung dengan cara:
Keterangan:
a & b = konstanta pada persamaan linier kurva standar NH4Cl
y = OD amonium sampel
F.P = faktor pengenceran (4)
[amonium] = y – b – OD amonium awala x F.P
3
-.
$#$ ( ! -, "
Sebanyak 19 isolat bakteri metanotrof berhasil diremajakan dari 40 isolat metanotrof yang telah diisolasi dari tanah sawah asal Bogor dan Sukabumi (Hapsari 2008). Isolat tersebut terdiri atas: BGM 1, BGM 2, BGM 3, BGM 4, BGM 5, BGM 6, BGM 9, BGM 12, SKM 1, SKM 2, SKM 4, SKM 5, SKM 7, SKM 9, SKM 10, SKM 14, SKM 15, SKM 16, SKM 18.
Gambar 1 Morfologi koloni isolat BGM 1 pada media agar NMS dengan masa inkubasi lima hari pada suhu 27429oC
Isolat4isolat tersebut menunjukkan warna
koloni yang berbeda, yaitu putih
(tipis/bening), putih krem (Gambar 1), pink, pink oranye, kuning terang, dan oranye (Hapsari 2008). Kecepatan pertumbuhan koloni tiap isolat pada media agar NMS bervariasi, yaitu mencapai ukuran ± 2 mm dalam waktu 3 4 14 hari.
%".3." - .%- -. %"$#. $" !,"#,/
Seleksi uji aktivitas fiksasi nitrogen pada 19 isolat yang berhasil diremajakan pada medium NMS tanpa mengandung unsur N menunjukkan bahwa isolat BGM 1, BGM 3, BGM 5, dan BGM 9 merupakan isolat terpilih karena akumulasi amonium dalam media pertumbuhannya lebih tinggi dibandingkan dengan isolat yang lainnya. Kerapatan sel bakteri tertinggi dari isolat asal sawah Sukabumi (SKM) ditunjukkan oleh isolat SKM 5 dengan nilai OD620 sebesar 0.049,
sedangkan isolat asal sawah Bogor (BGM)
ditunjukkan oleh BGM 12 dengan nilai OD620
sebesar 0.040 (Tabel 1).
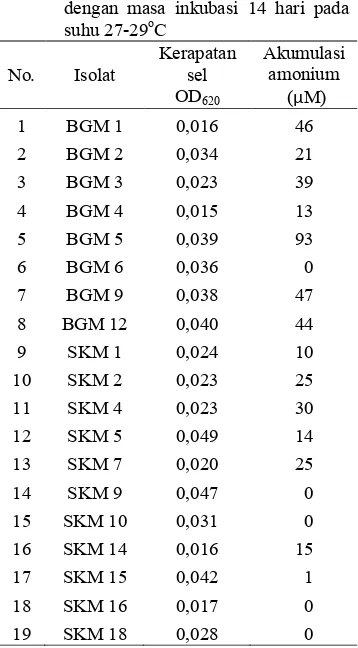
Tabel 1 Kerapatan sel (OD620) dan akumulasi
amonium pada kultur bakteri
metanotrof pada media agar NMS dengan masa inkubasi 14 hari pada suhu 27429oC
No. Isolat Kerapatan sel OD620 Akumulasi amonium (µM)
1 BGM 1 0,016 46
2 BGM 2 0,034 21
3 BGM 3 0,023 39
4 BGM 4 0,015 13
5 BGM 5 0,039 93
6 BGM 6 0,036 0
7 BGM 9 0,038 47
8 BGM 12 0,040 44
9 SKM 1 0,024 10
10 SKM 2 0,023 25
11 SKM 4 0,023 30
12 SKM 5 0,049 14
13 SKM 7 0,020 25
14 SKM 9 0,047 0
15 SKM 10 0,031 0
16 SKM 14 0,016 15
17 SKM 15 0,042 1
18 SKM 16 0,017 0
19 SKM 18 0,028 0
Keterangan: BGM= Bogor metanotrof SKM= Sukabumi metanotrof
Meskipun secara umum isolat SKM
memiliki nilai OD sel yang lebih tinggi namun
berdasarkan jumlah amonium yang
diakumulasi isolat BGM secara umum
[image:11.612.331.510.146.470.2] [image:11.612.132.305.229.404.2]4
%".3." - .%- -. -, " $#*. .+ * ) ,!-$!"# -. $#2$)
Setelah inkubasi selama 14 hari isolat terpilih menunjukkan kerapatan sel berbeda4 beda pada konsentrasi oksigen berbeda (Gambar 2). Secara umum kerapatan sel empat isolat rendah pada saturasi udara 100% yaitu antara OD 0.003 dan 0.088 (OD620).
Kerapatan sel tertinggi pada saturasi udara 100% dimiliki oleh isolat BGM 5 dengan OD 0.088. Kerapatan sel secara umum tinggi pada saturasi udara 10% yaitu antara OD 0.01 dan 0.097 (OD620). Kerapatan sel tertinggi pada
saturasi udara 10% dimiliki oleh isolat BGM 5 dengan OD 0.097 (OD620).
Gambar 2 Kerapatan sel kultur BGM 1,
BGM 3, BGM 5, BGM 9
pada beberapa konsentrasi oksigen menggunakan media agar NMS dengan masa inkubasi 14 hari pada suhu 27429oC.
Hasil uji fiksasi N2terhadap isolat BGM 1,
BGM 3, BGM 5, dan BGM 9 pada
konsentrasi O2berbeda yaitu 10%, 30%, 50%,
80%, dan 100% menunjukkan jumlah
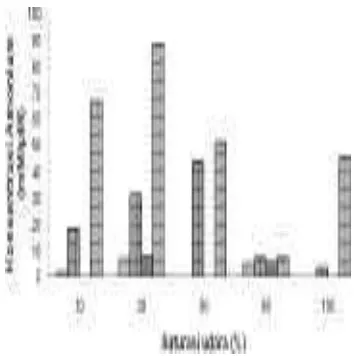
amonium yang diakumulasi berbeda tiap isolatnya (Gambar 3). Secara umum jumlah amonium yang diakumulasi rendah pada saturasi udara 100% yaitu antara 0 dan 46.027 <M. Jumlah amonium yang diakumulasi tertinggi pada saturasi udara 100% dimiliki oleh isolat BGM 9 yaitu 46.027 <M. Jumlah amonium yang diakumulasi secara umum tinggi pada saturasi udara 30%, jumlah yang tertinggi pada saturasi udara 30% dimiliki oleh isolat BGM 9 yaitu 88.816 <M.
Gambar 3 Konsentrasi amonium dalam kultur
BGM 1, BGM 3, BGM 5,
BGM 9 pada beberapa
konsentrasi oksigen menggunakan
media agar NMS dengan masa
inkubasi 14 hari pada suhu 274 29oC.
$ 2 + - !
Bakteri metanotrof merupakan bakteri pengoksidasi metan pada kondisi aerob menggunakan sistem enzim spesifik yaitu metan monooksigenase (MMO) (Madigan
2000). Isolat BGM 1, BGM 3, BGM 5, dan BGM 9 merupakan isolat terpilih karena dapat
mengakumulasi amonium lebih tinggi
dibandingkan dengan isolat lainnya.
Amonium yang diakumulasi isolat BGM 12 memang cukup tinggi bila dibandingkan dengan isolat BGM 3, namun pemilihan isolat BGM 3 dikarenakan isolat tersebut termasuk dalam empat isolat terbaik pengoksidasi metan (Hapsari 2008). Perbedaan amonium
yang diakumulasi dipengaruhi faktor
pertumbuhan bakteri metanotrof dan aktivitas enzim nitrogenase.
Pada uji aktivitas fiksasi nitrogen
menggunakan medium bebas N dengan
konsentrasi udara yang berbeda (10%, 30%, 50%, 80%, dan 100%), pertumbuhan bakteri berbeda yang ditunjukkan oleh nilai kerapatan sel yang berbeda pada tiap isolatnya. Secara umum kerapatan sel keempat isolat rendah pada saturasi udara 100% dan tinggi pada saturasi udara 10%. Hal ini diduga bakteri menggunakan sumber N dari udara untuk
pertumbuhannya. Tingkat pertumbuhan
tertinggi bakteri metanotrof tipe I dan II terdapat pada medium tanpa unsur N terdapat pada konsentrasi oksigen yang rendah
[image:12.612.332.509.82.260.2] [image:12.612.131.307.249.441.2]5
Pengamatan yang dilakukan terhadap kerapatan sel kultur cair isolat metanotrof terpilih menunjukkan kerapatan sel yang kecil. Kecilnya peningkatan kerapatan menunjukkan bahwa pertumbuhan isolat sangat lambat. Bakteri metanotrof merupakan bakteri yang tumbuh lambat (Begonja & Hrsák 1998), bahkan pada media agar NMS koloni bakteri ini baru tumbuh optimal pada umur 14 hari inkubasi.
Akumulasi amonium terendah dihasilkan oleh isolat BGM 1 dan BGM 5, sedangkan akumulasi amonium tertinggi dihasilkan oleh
isolat BGM 9 (Gambar 3). Aktivitas
nitrogenase akan terhambat apabila terdapat oksigen, namun oksigen juga dibutuhkan dalam respirasi aerob bakteri metanotrof untuk menghasilkan ATP yang mendukung aktivitas nitrogenase. Bakteri metanotrof tipe
II umumnya hanya mampu memfiksasi
nitrogen pada kondisi mikroaerofil (Murrel & Dalton 1983).
Proses fiksasi N2 menggunakan enzim
nitrogenase. Enzim tersebut sangat peka terhadap keberadaan oksigen yang tinggi. Hal
ini karena oksigen yang tinggi akan
menghambat ekspresi gen D dan H yang menyandikan enzim nitrogenase (Auman
, 2001). Oleh karena itu, oksigen dibutuhkan dalam jumlah sedikit untuk kecepatan fiksasi N2 maksimum (James & Olivares, 1997).
Hasil penelitian yang telah dilakukan menunjukkan bahwa jumlah amonium yang diakumulasi rendah pada konsentrasi oksigen 100%.
Ketersediaan sumber energi (C4organik) di lingkungan rizosfer merupakan faktor utama yang menentukan banyaknya nitrogen yang dihasilkan (Alexander 1977; Zuberer & Silver 1998). Proses fiksasi satu molekul nitrogen
membutuhkan 16 molekul ATP untuk
selanjutnya diubah menjadi dua molekul amonia yang dalam proses ini dikatalisis oleh enzim nitrogenase.
Sebanyak empat isolat bakteri metanotrof memiliki aktivitas fiksasi nitrogen yang tinggi yaitu isolat BGM 1, BGM 3, BGM 5, dan
BGM 9. Kerapatan sel tertinggi yang
ditumbuhkan pada konsentrasi oksigen berbeda dimiliki oleh isolat BGM 5 dengan OD 0.103 (OD620) pada saturasi udara 80%.
Jumlah amonium yang diakumulasi tertinggi dimiliki oleh isolat BGM 9 yaitu 88.816 <M pada saturasi udara 30%.
Karakterisasi bakteri terbaik dalam memfiksasi nitrogen dan uji potensi untuk efektivitasnya di laboratorium dan di lapang perlu dilakukan.
Alexander M. 1977.
. Ed ke42. New York : John Wiley and Sons.
Auman AJ, Speake CC, Lidstrom ME. 2001. nif#sequences and nitrogen fixation in type I and type II Methanotrophs.$
% 45: 400944016.
Begonja A, Hrsák D. 1998. Growth
characteristics and metabolic activities of the methanotrophic4heterotrophic groundwater community. & $
67: 4484456.
Bouwman AF, Sombroek WG. 1990. Inputs to climate change by soil and agriculture
related activities. Di dalam:
Scharpenseel HW, Scomaker M,
Ayoup A. (eds.) '
% % . Amsterdam: hlm. 154
30.
Cleseri LS, Greenberg AE and Trussel RR.
1989. (
%) * *
* . Port City Press. Baltimore.
Conrad R, Rothfus F. 1991. Methane
oxidation in the soil surface layer of a flooded rice field and the effect of
ammonium. ( 8 : 28432.
Hanson R, Hanson TE. 1996. Methanotrophic
Bacteria.& + ' 4 : 4394
471.
Hapsari W. 2008. Isolasi dan karakterisasi bakteri metanotrof asal sawah di Bogor dan Sukabumi [skripsi]. Bogor:
Fakultas Matematika dan Ilmu
Pengetahuan Alam, Institut Pertanian Bogor.
[IPCC] Intergovernmental Panel on Climate Change. 1992.
+ . Hougton
JT, Callendar BA, Varney SK, editor. Cambridge: Cambridge University Press.
6
Lelieveld J, Crutzen PJ, Bruhl C. 1993. Climate effects of atmospheric
methane. 4: 739–768.
Madigan MT, Martinko JM, Parker J. 2000.
! Ed
ke49. New Jersey : Prentice Hall. Murrell JC, Dalton H. 1983. Nitrogen Fixation
in Obligate Methanotrophs. & " 8 : 348143486. Notohadiprawiro T. 2006. '
" , . Yogyakarta: UGM Press.
Rao NSS. 1979. Recent Advances in
Biological Nitrogen Fixation. New Delhi: Oxford and IBH Publishing Co.
Wild A. 1995. % - $
Cambridge: Cambridge University Press.
Zuberer DA, Silver WS. 1998. Biological dinitrogen fixation (Acetylene reduction) associated with florida
mangrove.$ % 97:
8
Lampiran 1 Kerapatan sel kultur isolat terpilih pada beberapa konsentrasi oksigen
Isolat Saturasi
udara (%) Ulangan OD620 Rata4rata st. error
BGM 1
10 1 0,009 0,011 0,002
2 0,012
30 1 0,009 0,018 0,012
2 0,026
50 1 0,003 0,006 0,004
2 0,009
80 1 0,020 0,020 0,001
2 0,019
100 1 0,004 0,004 0,000
2 0,004
BGM 3
10 1 0,052 0,090 0,053
2 0,127
30 1 0,030 0,037 0,010
2 0,044
50 1 0,006 0,010 0,006
2 0,014
80 1 0,004 0,008 0,006
2 0,012
100 1 0,005 0,003 0,003
2 0,001
BGM 5
10 1 0,103 0,097 0,008
2 0,091
30 1 0,111 0,077 0,049
2 0,042
50 1 0,093 0,098 0,006
2 0,102
80 1 0,108 0,103 0,007
2 0,098
100 1 0,089 0,089 0,001
2 0,088
BGM 9
10 1 0,079 0,077 0,003
2 0,075
30 1 0,046 0,034 0,017
2 0,022
50 1 0,009 0,031 0,031
2 0,053
80 1 0,027 0,019 0,012
2 0,01
100 1 0,005 0,008 0,004
9
Lampiran 2 Akumulasi amonium dalam kultur metanotrof pada beberapa konsentrasi oksigen
Isolat
Saturasi udara (%)
[Amonium] <M
BGM 1
10 1,798
30 6,832
50 0,360
80 5,034
100 0
BGM 3
10 18,339
30 31,643
50 44,229
80 7,551
100 3,596
BGM 5
10 0
30 7,911
50 0
80 5,394
100 0
BGM 9
10 66,882
30 88,817
50 51,420
80 7,551
100 46,027