40
41
42 Lampiran 3.Bagan kerja penelitian
Batang Patah tulang
Dibersihkan dengan air mengalir Ditiriskan
Dipotong
Dikeringkan dilemari pengering Diserbuk
43 Lampiran 3. Lanjutan
Serbuk simplisia
dimasukkan ke dalam wadah
dimasukkan n-heksan sampai serbuk terendam sempurna
dibiarkan selama 5 hari terlindung dari cahaya, sambil sesekali diaduk
disaring
Maserat Ampas
dimaserasi kembali dengan pelarut n-heksan
dienap tuang
Maserat Ampas
44 Lampiran 3. Lanjutan
Ekstrak n-heksan kental
Kromatogram
Isolat murni
Spektrum Di KLT:
- fase gerak : n-heksana-etilasetat (90:10), (80:20), (70:30)
- fase diam = plat lapis tipis
Di KLT preparatif:
- fase gerak : n-heksana-etilasetat (80:20)
- fase diam : silikagel 60 F254
Kromatogram
Isolat-isolat
Diisolasi secara KLT
preparatif kemudian di KLT satu arah dan dua arah Isolat
Dikarakterisasi dengan spektrofotometri UV dan IR Noda (ungu) dikerok
45
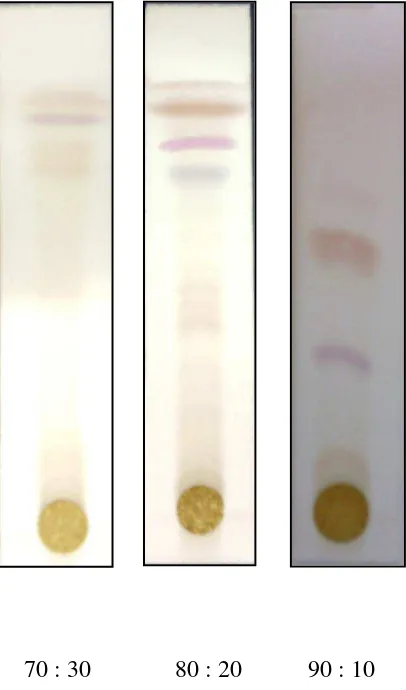
Lampiran 4. Gambar kromatogram ekstrak n-heksana batang patah tulang
70 : 30 80 : 20 90 : 10
Keterangan : Fase gerak n-heksanaetilasetatdanfasediam plat lapis tipis, jarak rambat 8 cm, TP = 1 cm, BP= 1 cm.
TP = titik penotolan, BP = batas penotolan
46
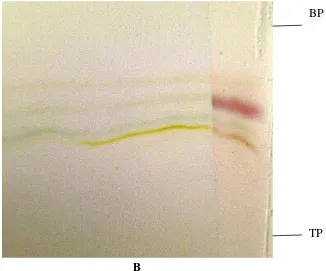
Lampiran 5.Gambar kromatogram dari ekstrak n-heksan
B
Keterangan: TP = titikpenotolan, BP = bataspenotolan
Dilihatsetelahpenyemprotandengan Liebermann-bourchard Gambar 3:Gambar kromatogram dari ekstrak n-heksan
BP
47
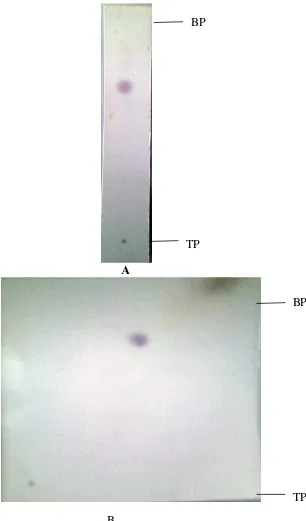
Lampiran 6.Gambar kromatogram KLT satuarahdanduaarah
A
B
Keterangan : TP = titik penotolan, BP = batas penotolan
A. KLT satu arah n-heksana:etilasetat = 8 ml:2 ml(Rf 0,78) B. KLT dua arah n-heksana:etil asetat = 8 ml : 2 ml (Rf 0,78) Toluen : etil asetat = 9 ml : 1 ml
Gambar 4:Gambar kromatogram KLT satuarahdanduaarah TP
BP
BP
48
Lampiran 7.Gambar alat spektrofotometer yang digunakan analisis isolat murni
A
B
Keterangan : A. Spektrofotometer ultraviolet B. Spektrofotometer inframerah
49
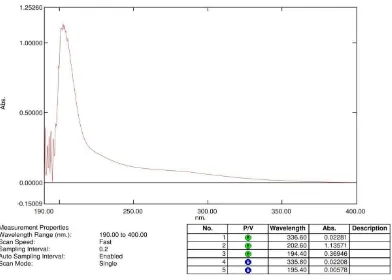
Lampiran 8. Gambar spektrum senyawa triterpenoid hasil isolasi dengan spektrofotometer ultraviolet.
50
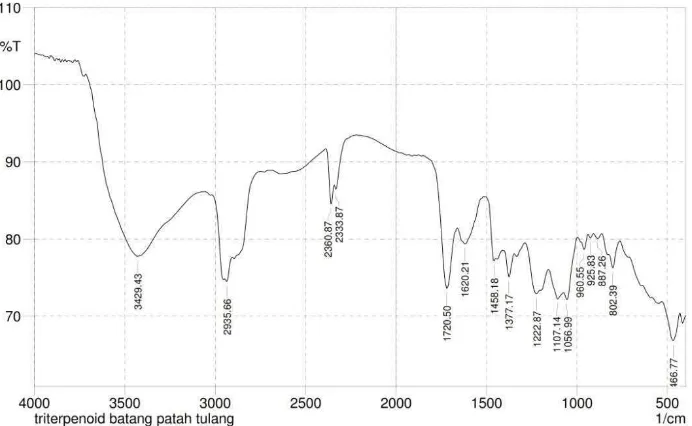
Lampiran 9. Gambar spektrum senyawa triterpenoid hasil isolasi dengan spektrofotometer inframerah isolat
Tabel hasil analisis spektrum inframerah dengan isolat murni triterpen No. Bilangan gelombang (cm-1) Ikatan kimia / gugus fungsi
1 1720,50 C=O
2 2935,66 -CHalifatik
3 1377,17 -CH3
4 1107,14 C-H
5 3429,43 -OH
51 Lampiran 10.Perhitungan hasil penetapan kadar a. Perhitungan hasil penetapan kadar air
No. Berat sempel Volume air
1 5,012 g 0,3 ml
2 5,013 g 0,3 ml
3 5,034 g 0,3 ml
Kadar air =volume air (ml)
berat sampel (g)
�
100%
1. Kadar air = 0,3
5,012
x100%
= 5,98 %v b�2.
Kadar air = 0,35,013
x100%
= 5,98 %v b�3. Kadar air = 0,3
5,034
x100%
= 5,95 %v b�Kadar air rata – rata = 5,98%+5,98%+5,95%
3 = 6,64%v b�
b. Perhitungan hasil penetapan kadar sari yang larut dalam air
No. Berat sampel Berat sari
1 5,004 g 0,166 g
2 5,025 g 0,195 g
3 5,053 g 0,163 g
Kadar sari larut air = berat sari berat sampel x
100
20 x 100%
1. Kadar sari larut air = 0,166
5,004 x
100
20 x 100% = 16,59%
2. Kadar sari larut air = 0,195
5,025 x
100
20 x 100% = 19,40%
3. Kadar sari larut air = 0,163
5,053 x
100
20 x 100% = 16,12%
Kadar sari larut air rata – rata = 16,59%+19,40%+16,12%
52
c. Perhitungan hasil penetapan kadar sari yang larut dalam etanol
No. Berat sempel Berat sari
1 5,004 g 0,142 g
2 5,020 g 0,104 g
3 5,001 g 0,124 g
1. Kadar sari larut etanol
=
0,1425,004
x
100
20
x100%
= 13,94%
2. Kadar sari larut etanol
=
0.1045,020
x
100
20
x100%
= 10.35%
3. Kadar sari larut etanol
=
0,1245,001
x
100
20
x 100%
= 12.39%Kadar sari larut etanol rata-rata
=
13,94%+10,35%+12,39%3 = 12,22% d. Perhitungan hasilpenetapankadarabu total
No. Berat sampel Berat abu
1 2,0010 g 0,0649 g
2 2,0015 g 0,0660 g
3 2,0010 g 0,0662 g
1. Kadar abu total
=
0,06492,0010
x100%
=3,24%2. Kadar abu total
=
0,06602,0015
x100%
= 3,29%3. Kadar abu total
=
0,06622,0010
x 100%
= 3,21%Kadarabu total rata-rata
=
3,24%+3,29%+3,21%3 =3,21%
e. Perhitungan Hasil Penetapan Kadar Abu Tidak Larut Dalam Asam
No. Berat sempel Berat abu
1 2,0010 g 0,0172 g
2 2,0015 g 0,0155 g
3 2,0012 g 0,0143 g
Kadar sari larut etanol
=
berat sari berat sempelx
100
20
x
100%Kadar abu total
=
berat abu53 1. Kadar abu tidak larut asam
=
0,01722,0010
x 100%
= 0,86%2. Kadar abu tidak larut asam
=
0,01552,0015
x 100%
= 0,77%3.Kadar abu tidak larut asam
=
0,01432,0012
x 100%
= 0,71%Kadarabu tidak larut asam rata-rata
=
0,84%+0.77%+0,71%3 = 0,78%
Kadar abu tidak larut dalam asam
=
berat abu36
DAFTAR PUSTAKA
Aksara, R.,Musa W., J.,A., La Alio. (2013). Identifikasi Senyawa Alkaloid dari Ekstrak Metanol Kulit Mangga (Mangifera indica L.). Gorontalo: Universitas Negeri Gorontalo. Halaman 4.
Aldhani, E. (2014). Penapisan Kandungan Fitokimia pada Buah Labu Kuning.
Bogor. Institut Pertanian Bogor. Halaman 4.
Dachriyanus.(2004). Analisis Struktur Senyawa Organik Secara Spektroskopi. Padang: Andalas University Press. Halaman 1-18, 21-37.
Dalimartha, S. (2003).Atlas tanaman obat Indonesia. Jilid I. Jakarta: Trubus Agriwidya.Halaman 130-132.
Dalimartha, S. (2007).Atlas tanaman obat Indonesia. Puspa swara. Jakarta.Hal 149.
Depkes RI. (1995). Materia Medika Indonesia. Jilid VI. Jakarta: Departemen Kesehatan RI. Halaman 300-304, 306.
Depkes RI. (1986).Cara Pengelolaan Simplisia yang Baik. Jakarta: Direktorat Jenderal Pengawas Obat dan Makanan. Halaman 3-4.
Depkes RI. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Departemen Kesehatan RI. Halaman 1-11.
Farnsworth, N. R. (1966). Biological and Phytochemical Screening of Plant.Journal of Pharmaceutical Sciences.55(3). Halaman 262-263.
Gritter, R.J., Bobbit, J.M., dan Schwarting, A.E. (1985).Introduction to Cromatography. Penerjemah: Kokasih Padmawinata (1991) .Pengantar Kromatografi.Edisi 2. Bandung: ITB. Hal.107-146.
37
Harborne, J.,B. (1984). Phytochemical Methods .Penerjemah: Padmawinata,K., danSooediro, I. (1987).Metode Fitokimia Penuntun Cara Modern Menganalisis Tumbuhan.Edisi 2. Bandung: ITB. Halaman 102-103, 147-149, 234.
Lata, N., dan Dubey, V. (2010). Preliminary Phytochemical Screening of Eichhornia crassipes: The World’s Worst Aquatic Weed. Journal of Pharmacy Research3(6).
Mwine, J., Van Damme, P., Hastilestari, B.R., Papenbrock, J. (1999). The Miracle Tree: Curent Status of Knowledge.Uganda: Uganda Martyrs University. Halaman 4-6.
Robinson, T.(1991).The Organic Constituents of Higher Plant. Penerjemah: Padmawinata, K. (1995) .Kandungan Organik Tumbuhan Tinggi.
Bandung: ITB. Halaman 123-157, 191.
Rohman, A. (2009). Kromatografi Untuk Analisis Obat. Yogyakarta: Graha Ilmu. Halaman 51.
Roslizawaty., Ramadani, N.Y., Fakhrurrazi., dan Herialfian. (2013). Aktivitas antibakteri ekstrak etanol dan rebusan sarang semut (Myrenecodia sp.) terhadap bakteri Escherichia coli.Jurnal medika veterinaria 7(2): 91-93. Saifudin, A., Rahayu, V., dan Teruna, H.Y. (2011). Standarisasi Bahan Obat
Alam. Yogyakarta: Graha Ilmu. Halaman 1-2.
Sastrohamidjojo, H. (1985). Spektroskopi. Yogyakarta: Penerbit Liberty. Halaman 11-12, 22-23.
Sastrohamidjojo,H. (1991). Kromatografi. Yogyakarta: Penerbit Liberty. Halaman 22-36.
Sarker, S.D., Zahid L., dan Alexander, I.G. (2006).Natural Products Isolation.Edisi Kedua.New Jersey: Humana Press Inc. Halaman 332.
Setiorini, M. S., Soegihardjo C.,J , Atmojo K. (2014). Potensi Antimikroba Krim Ekstrak Ranting Patah Tulang(Euphorbia Tirucalli Linn.) terhadap Propionibacterium Acnes ATCC 11827 dan Candica Albicans ATCC 24433. Yogyakarta: Universitas Atma Jaya Yogyakarta. Halaman 2-7. Sirait, M. (2007).Penuntun Fitokimia Dalam Farmasi. Bandung: ITB. Halaman
158.
38
Supriyanto dan Luviana, L.A.I. (2010). Pengaruh Pemberian Getah Tanaman Patah Tulang Secara Topikal terhadap Gambaran Histopatologis dan Ketebalan Lapisan Keratin Kulit.Semarang: Universitas Negeri Semarang. Halaman1.
.
Wagner, H., Bladt, s., dan Zyainski, E., M. (1984).Plant Drug Analysis a Thin Layer Chromatography Atlas.Translated by Th. A. Scott. New York: Springer Verlay. Halaman 301.
18
jauh (400-10 cm-1) (Gandjar dan Rohman, 2012).Daerah IR tengah merupakan daerah yang digunakan untuk penentuan gugus fungsi (Dachriyanus, 2004).
BAB III
METODE PENELITIAN
Metode penelitian ini dilakukan secara eksperimental meliputi pengumpulan dan pengolahan sampel, karakterisasi simplisia, skrining fitokimia, pembuatan ekstrak, analisis fraksi n-heksan yang dilanjutkan dengan isolasi senyawa triterpenoid/steroid mengunakan KLT preparatif.Isolat yang diperoleh diuji kemurniannya dengan KLT satu arah dan dua arah, karakterisasi isolat dengan spektrofotometri UV dan IR.
3.1. Alat-alat dan Bahan
3.1.1 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah: alat-alat gelas (Iwaki Pyrex), blender (Philips), mikroskop (Olympus), neraca analitik (Vibra AJ), neraca kasar (Homeline), oven listrik (Memmert), penangas air, penguap vakum putar (Stuart), seperangkat alat kromatografi lapis tipis, seperangkat alat penentu kadar air (Pyrex), spektrofotometer inframerah (Shimadzu), spektrofotometer ultraviolet (Shimadzu) dan tanur (Nabertherm).
19
Sampel yang digunakan adalah ranting tanaman patah tulang (Euphorbia tirucalli L.). Bahan kimia yang digunakan kecuali dinyatakan lain adalah berkualitas proanalisa yaitu: amil alkohol, ammonia pekat, asam asetat anhidrida, asam klorida, asam nitrat, asam sulfat, benzena,besi (III) klorida,bismuth (III) nitrat, etanol, etilasetat, iodium, kalium iodida, kloroform, methanol, n-heksana, pra lapis silika gel F254, raksa (II) klorida, serbuk magnesium, silika gel 60F254, timbal (II) asetat, toluen serta air suling.
3.2 Pembuatan Larutan Pereaksi 3.2.1 Pereaksi Liebermann-Burchard
Sebanyak 5 ml asam asetat anhidrida dicampurkan perlahan-lahan dengan 5 ml asam sulfat pekat tambahkan etanol hingga 50 ml (Wagner dkk., 1984). 3.2.2 Pereaksi Dragendorff
Sebanyak 20 ml larutan bismut nitrat P 40% b/v dalam asam nitrat P dicampur dengan 50 ml kalium iodida P 54,4% b/v, didiamkan sampai memisah sempurna. Lalu diambil lapisan jernih dan diencerkan dengan air secukupnya hingga 100 ml (Depkes RI., 1995).
3.2.3 Pereaksi asam sulfat 2 N
Sebanyak 5,5 ml asam sulfat pekat diencerkan dengan air suling hingga volume 100 ml (Depkes RI., 1995).
3.2.4 Pereaksi Molish
Sebanyak 3 gram α-naftol ditimbang, dilarutkan dalam asam nitrat 0,5 N hingga diperoleh larutan 100 ml (Depkes RI., 1995).
20
Sebanyak 1,359 gram raksa (II) klorida dilarutkan dalam air suling hingga 60 ml. Pada wadah lain sebanyak 5 gram kalium iodida dilarutkan dalam 10 ml airsuling, kemudian keduanya campur dan ditambahkan air suling hingga 100 ml (Depkes RI., 1995).
3.2.6 Pereaksi besi (III) klorida 10%
Sebanyak 10 gram besi (III) klorida ditimbang, dilarutkan dalam air suling sehingga diperoleh larutan 100 ml (Depkes RI., 1995).
3.2.7 Pereaksi Bouchardat
Sebanyak 4 gram kalium iodida dilarutkan dalam air suling dan sebanyak 2 gram iodium dilarutkan dalam larutan kalium iodida dan dicukupkan dengan air suling hingga 100 ml (Depkes RI., 1995).
3.2.8 Pereaksi natrium hidroksida 2 N
Sebanyak 8,001 gram kristal natrium hidroksida ditimbang, dilarutkan dalam air suling sehingga diperoleh larutan 100 ml (Depkes RI., 1995).
3.2.9 Pereaksi asam nitrat 0,5 N
Sebanyak 3,4 ml asam nitrat pekat diencerkan dengan air suling hingga 100 ml (Depkes RI., 1995).
3.2.10 Pereaksi timbal (II) asetat 0,4 M
Sebanyak 15,17 g timbal (II) asetat dilarutkan dalam air suling bebas CO2 hingga 100 ml (Depkes RI., 1995).
21
Pengambilan sampel dilakukan secara purposif tanpa membandingkan dengan tumbuhan yang sama dari daerah lain. Sampel yang digunakan dalam penelitian ini adalah batang tanaman patah tulang yang masih segar, yang diambil dari daerah Padang Bulan, Kotamadya Medan, Sumatera Utara.
3.3.2 Identifikasi tumbuhan
Identifikasi tanaman patah tulang dilakukan oleh bagian Herbarium Medanense (MEDA) Universitas Sumatera Utara.
3.3.3 Pengolahan sampel
Batang tanaman patah tulang terlebih dahulu di potong menjadi ukuran ukuran yang lebih kecil, dibersihkan dari pengotoran, dicuci bersih dengan air mengalir, ditiriskan, kemudian dikeringkan di udara terbuka dan terlindung dari cahaya matahari. Selanjutnya dikeringkan di lemari pengering pada suhu 50˚C.Sampel yang telah kering diserbuk kemudian disimpan dalam wadah bersih.
3.4 Karakterisasi Simplisia
Karakterisasi simplisia meliputi penetapan kadar air,penetapan kadar sari yang larut dalam air,penetapan kadar sari yang larut dalam etanol,penetapan kadar abu total, dan penetapan kadar abu tidak larut dalam asam.
3.4.1 Penetapan kadar air
22
ditimbang seksama, labu dipanaskan hati-hati selama 15 menit. Setelah toluen mendidih, kecepatan tetesan diatur lebih kurang 2 tetes tiap detik sampai sebagian besar air terdestilasi, kemudian kecepatan tetesan dinaikkan hingga 4 tetes tiap detik.Setelah semua air terdestilasi, bagian dalam pendingin dibilas dengan toluen.Destilasi dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan mendingin pada suhu kamar. Setelah air dan toluen memisah sempurna, volume air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air yang dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa. Kadar air dihitung dalam persen (World Health Organization, 1992).
3.4.2 Penetapan kadar sari yang larut dalam air
Sebanyak 5 gram serbuk simplisia dimaserasi selama 24 jam dengan 100 ml air-kloroform (2,5 ml kloroform dalam air sampai 1 liter) menggunakan labu bersumbat sambil berkali-kali dikocok selama 6 jam pertama, kemudian dibiarkan selama 18 jam dan disaring. Sejumlah 20 ml filtrat diuapkan sampai kering dalam cawan dangkal berdasarkan rata yang telah ditara.Sisa dipanaskan sampai kering pada suhu 105oC hingga bobot tetap.Kadar sari yang larut dalam air dihitung dalam persen terhadap bahan yang telah dikeringkan di udara (Depkes RI., 1995). 3.4.3 Penetapan kadar sari larut dalam etanol
23
etanol dihitung dalam persen terhadap bahan yang telah dikeringkan di udara (Depkes RI., 1995)
3.4.4 Penetapan kadar abu
Sebanyak 2 gram serbuk simplisia yang telah digerus ditimbang seksama, dimasukkan ke dalam krus porselen yang telah terlebih dahulu dipijar dan ditara, kemudian diratakan.Lalu krus dipijarkan perlahan-lahan sampai bobot tetap.Kadar abu dihitung terhadap bahan yang telah dikeringkan di udara (Depkes.,RI1995). 3.4.5 Penetapan kadar abu yang tidak larut dalam asam
Abu yang diperoleh pada penetapan kadar abu dididihkan dengan 25 ml asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam dikumpulkan, disaring melalui kertas saring bebas abu, dicuci dengan air panas. Residu dan kertas saring dipijar sampai bobot tetap.Kadar abu yangtidak larut dalam asam dihitung terhadap bahan yang telah dikeringkan di udara (Depkes RI., 1995).
3.5 Skrining Fitokimia
Skrining fitokimiaserbuk simplisia meliputi pemeriksaan senyawa alkaloida, flavonoida, glikosida, antrakinonglikosida, saponin, tanin, dan triterpenoida/steroida.
3.5.1 Pemeriksaan glikosida
24
asetat 0,4 M dikocok dan didiamkam selama 5 menit, lalu disaring. Filtrat diekstraksi dengan 20 ml campuran 3 bagian kloroform dan 2 bagian isopropanol, ini dilakukan sebanyak tiga kali. Kumpulan sari diuapkan pada temperatur tidak lebih dari 50oC.sisanya dilarutkan dalam 2 ml metanol. Larutan ini digunakan untuk percobaan berikut: larutan sisa dimasukkan ke dalam tabung reaksi, diuapkan di atas penangas air, sisanya ditambahkan 2 ml air dan 5 tetes pereaksi Molish kemudian ditambahkan hati-hati 2 ml asam sulfat pekat melalui dinding tabung. Jika terbentuk cincin ungu pada batas kedua cairan menunjukkan adanya gula (Depkes RI., 1995).
3.5.2 Pemeriksaan alkaloida
Sebanyak 0,5 gram serbuk simplisia ditimbang, kemudian ditambahkan 1 ml asam klorida 2 N dan 9 ml air suling, dipanaskan di atas penangas air selama 2 menit, didinginkan dan disaring. Filtrat dipakai untuk percobaan berikut:
− Diambil 3 tetes filtrat, lalu ditambahkan 2 tetes pereaksi Mayer
− Diambil 3 tetes filtrat, lalu ditambahkan 2 tetes pereaksi Bouchardat
− Diambil 3 tetes filtrat, lalu ditambahkan 2 tetes pereaksi Dragendorff
Alkaloida positif jika terjadi endapan atau kekeruhan paling sedikit dua dari tiga percobaan di atas (Depkes RI., 1995).
3.5.3 Pemeriksaan triterpenoid/steroid
25 3.5.4 Pemeriksaan saponin
Sebanyak 0,5 gram serbuk simplisia ditimbang, dimasukkan dalam tabung reaksi lalu ditambahkan 10 ml air panas, didinginkan kemudian dikocok kuat-kuat selama 10 detik, jika terbentuk buih yang stabil selama tidak kurang dari 10 menit setinggi 1-10 cm dan dengan penambahan 1 tetes asam klorida 2 N buih tidak hilang menunjukkan adanya saponin (Depkes RI., 1995).
3.5.5 Pemeriksaan flavonoida
Sebanyak 10 g serbuk simplisia ditambahkan 10 ml air panas, dididihkan selama 5 menit dan disaring dalam keadaan panas, kedalam 5 ml filtrat ditambahkan 0,1 g serbuk magnesium dan 1ml asam klorida pekat dan 2 ml amil alkohol, dikocok dan dibiarkan memisah. Flavonoida positif jika terjadi warna merah atau kuning atau jingga pada lapisan amil alkohol (Farnsworth, 1966). 3.5.6 Pemeriksaan tanin
Sebanyak 0,5 gram serbuk simplisia ditimbang, disari dengan 10 ml air suling selama 15 menit lalu disaring. Filtratnya diencerkan dengan air suling sampai tidak berwarna.Larutan diambil sebanyak 2 ml dan ditambahkan 1-2 tetes larutan pereaksi besi (III) klorida 10 %.Apabila terjadi warna biru atau hijau kehitaman menunjukkan adanya tanin (Farnsworth, 1966).
3.5.7 Pemeriksaan glikosida antrakinon
26
berwarna merah intensif dan lapisan benzena tidak berwarna menunjukkan adanya glikosida antrakinon (Depkes RI., 1995).
3.6 Pembuatan Ekstrak n-heksan Batang Tanaman Patah Tulang
Pembuatan ekstrak n-heksan batang tanaman patah tulang dilakukan dengan cara maserasi menggunakan pelarut n-heksan.Sebanyak 500 g serbuk simplisia batang tanaman patah tulang dimasukkan ke dalam wadah gelas berwarna gelap dan ditambahkan pelarut n-heksansampai serbuk terendam sempurna, ditutup dan dibiarkan selama 2 hari terlindung dari cahaya sambil sering diaduk.Disaring diperoleh maserat I dan ampas.Ampas dimaserasi kembali dengan n-heksan sampai terendam sempurna dan dibiarkan selama 2 hari. Perlakuan dilakukan sampai diperoleh filtrat yang jernih dan negatif dengan pereaksi Liebermann-Burchard.Seluruh maserat digabungkan dan diuapkan menggunakan rotary evaporator pada temperatur ± 40oC sampai diperoleh ekstrak kental.
3.7 Analisis Ekstrakn-Heksan Secara Kromatografi Lapis Tipis (KLT)
Ekstrak n-heksan batang tanaman patah tulang dianalisis secara KLT menggunakan plat pra lapis tipis silika gel 60 F254 dan fase gerak n heksan-etil asetat dengan perbandingan (90:10), (80:20), (70:30), sebagai penampak bercak digunakan pereaksi Liebermann-Burchard.
27
Ekstrak n-heksan batangtanaman patah tulang ditotolkan pada plat pra lapis silikal gel F254 yang sebelumnya telah diaktifkan, kemudian dimasukkan ke dalam chamber yang telah jenuh dengan uap pengembang dan ditutup rapat. Sesudah elusi selesai, plat dikeluarkan dan dikeringkan di udara, plat disemprot dengan larutan penampak bercak pereaksi Lieberman-Burchard. Warna bercak yang terjadi diamati dan dihitung harga Rf-nya.
3.8 Isolasi Senyawa Tritepenoid Secara KLT Preparatif
Isolasi senyawa tritepenoid dilakukan secara KLT preparatif, sebagai fase gerak digunakan n-heksan-etilasetat (80:20) perbandingan yang memberikan pemisahan terbaik dan sebagai penampak bercak digunakan pereaksi Liebermann-Burchard.
Cara kerja:
28
dengan pelarut metanol, diuapkan dan kristal yang terbentuk direkristalisasi dengan metanol dingin.
3.9 Uji Kemurnian Isolat
3.9.1 Uji kemurnian isolat dengan KLT satu arah
Terhadap isolat dilakukan uji kemurnian dengan KLT satu arah menggunakan fase diam plat pra lapis silika gel 60 F254, fase gerak n-heksan-etilasetat (80:20) perbandingan yang memberikan pemisahan terbaik dan sebagai penampak bercak digunakan pereaksi LB.
Cara kerja:
Isolat ditotolkan pada plat pra lapis silika gel 60 F254 yang sebelumnya telah diaktifkan, kemudian dimasukkan ke dalam bejana kromatografi yang telah jenuh dengan uap pengembang dan ditutup rapat. Sesudah elusi selesai plat dikeluarkan dari bejana kromatografi dan dikeringkan di udara, kemudian plat disemprot dengan larutan penampak bercak LB. Warna bercak yang terjadi diamati dan dihitung harga Rf-nya..
3.9.2 Uji kemurnian isolat dengan KLT dua arah
Terhadap isolat dilakukan uji kemurnian dengan KLT dua arah menggunakan fase diam plat pra lapis silika gel 60 F254, fase gerak pertama n -heksan-etilasetat (80:20), fase gerak kedua toluen-etilasetat (90:10), dan sebagai penampak bercak digunakan pereaksi LB.
29
Isolat ditotolkan pada plat pra lapis silika gel 60 F254 yang sebelumnya telah diaktifkan, kemudian dimasukkan ke dalam bejana kromatografi yang telah jenuh uap pengembang pertama dan ditutup rapat. Sesudah elusi selesai plat dikeluarkan dari bejana kromatografi, lalu diputar 90o dimasukkan ke dalam bejana kromatografi yang telah jenuh uap pengembang kedua dan ditutup rapat. Setelah selesai elusi plat dikeluarkan dan dikeringkan di udara, kemudian plat disemprot dengan penampak bercak pereaksi LB. Warna bercak yang terjadi diamati dan dihitung harga Rf-nya.
3.10 Karakterisasi Isolat
Karakterisasi senyawa triterpenoid hasil isolasi dilakukan dengan spektrofotometri ultraviolet (UV) dan spektrofotometri inframerah (IR).
3.10.1 Karakterisasi isolat dengan spektrofotometri ultraviolet
Karakterisasi isolat dengan spektrofotometri ultraviolet dilakukan dengan cara melarutkan senyawa hasil isolasi dengan metanol kemudian diukur absorbansinya pada panjang gelombang 200-400 nm.
3.10.2 Karakterisasi isolat dengan spektrofotometri inframerah
30 BAB IV
HASIL DAN PEMBAHASAN
4.1Hasil Identifikasi Tumbuhan Patah Tulang
Identifikasi sampel dilakukan oleh bagian Herbarium Medanense (MEDA) Universitas Sumatera Utara terhadap tanaman patah tulang adalah Euphorbia tirucalli L. suku Euphorbiaceae. Hasil identifikasi sampel dapat dilihat pada Lampiran 1.
4.2 Hasil ekstraksi serbuk simplisia
Ekstraksi serbuk simplisia dilakukan secara maserasi menggunakan pelarut n-heksan, dari 500 g serbuk simplisia setelah diuapkan dengan alat rotary evaporator((± 40°C)diperoleh ekstrak kental 40 g.
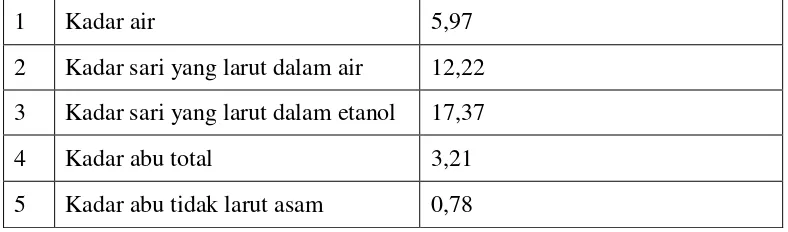
4.3 Hasil Karakterisasi Simplisia
Hasil pemeriksaan karakterisasi serbuk simplisia ranting tanaman patah tulang dapat dilihat pada Tabel 4.1 berikut dan perhitungannya dapat dilihat pada Lampiran 10.
Tabel 4.1Hasil pemeriksaan karakterisasi serbuk simplisia.
31
Penetapan kadar air dilakukan untuk ,mengetahui apakah simplisia sudah memenuhi pesyaratan, karena air merupakan media pertumbuhan yang baik bagi jamur sehingga dapat mempengaruhi mutu simplisia ternyata hasilnya memenuhi syarat yaitu 6%.Menurut persyaratan umum MMI simplisia memenuhi syarat jika kadar air dibawah 10%. Penetapan kadar sari yang larut dalam air dilakukan untuk mengetahui kadar senyawa yang bersifat polar sedangkanpenetapan kadar sari yang larut dalam etanol dilakukan untuk mengetahui kadar senyawa yang polar maupun nonpolar. Kadar sari larut dalam etanol harus selalu lebih besar daripada kadar sari larut dalam air. Penetapan kadar abu dilakukan untuk mendestruksi serta menguapkan senyawa organik dan turunannya sehingga yang tersisa senyawa anorganik, misalnya logam K, Ca, Na, Pb, dan silika sedangkan kadar abu tidak larut asam untuk mengetahui kadar senyawa anorganik yang tidak larut dalam asam misalnya silika.
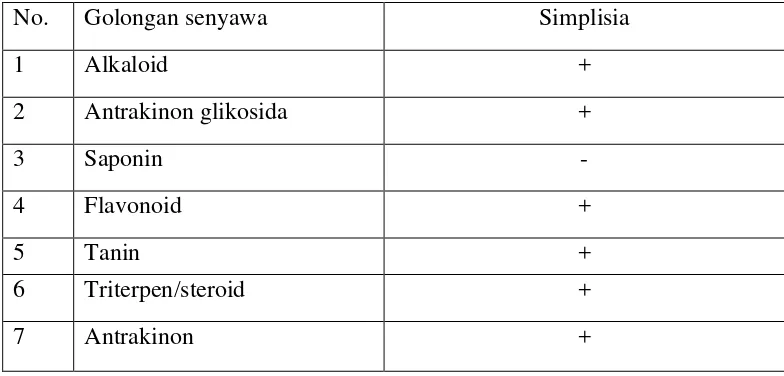
4.4 Hasil Skrining Fitokimia
[image:31.595.113.507.86.202.2]Hasil skrining fitokimia terhadap simplisia ranting tanaman patah tulang didapat hasil bahwa pada simplisia tersebut terdapat metabolit sekunder alkaloid, antrakinon glikosida, flavonoid, tannin dan triterpenoid/steroid. Hasil skrining dapat dilihat pada Tabel 4.2.
Tabel 4.2 Hasil skrining fitokimia dari ekstrak n-heksan ranting tanaman patah tulang (Euphorbia tirucalli L.)
1 Kadar air 5,97
2 Kadar sari yang larut dalam air 12,22 3 Kadar sari yang larut dalam etanol 17,37
4 Kadar abu total 3,21
32
No. Golongan senyawa Simplisia
1 Alkaloid +
2 Antrakinon glikosida +
3 Saponin -
4 Flavonoid +
5 Tanin +
6 Triterpen/steroid +
7 Antrakinon +
Keterangan:
+ = mengandung golongan senyawa, – = tidak mengandung golongan senyawa
4.5 Hasil Analisis Ekstrak n-heksan Secara KLT
[image:32.595.112.504.84.272.2]Analisis senyawa triterpenoid digunakan KLT dengan fase diam plat lapis tipis dan fase gerak n-heksan : etilasetat perbandingan (90:10), (80:20), (70:30), sebagai penampak noda LB. Hasil KLT n-heksan : etilasetat dengan perbandingan (80:20) memberikan bercak senyawa triterpenoid berwarna merah ungu yang lebih dominan. Harga Rf dari masing-masing perbandingan fase gerak dapat dilihat pada Tabel 4.3 dan pola kromatogram pada Lampiran 4.
Tabel 4.3 Harga Rf ekstrak n-heksanranting tanaman patah tulang (Euphorbia tirucalli L.) denganbeberapa perbandingan fase gerak.
NO
Harga Rf
Fase gerak n-heksan: etilasetat, fase diam plat lapis tipis silica gel F254
70 : 30 80 : 20 90 : 10
1 0,86 0,78 0,35
33
menggunakan fase diam silika gel 60 F254 dan penampak bercak pereaksi LB. Hasil KLT yang dikerok adalah Rf 0,78, setelah dikerok silika dielusi dengan metanol dingin.
4.6Hasil Uji Kemurnian Isolat
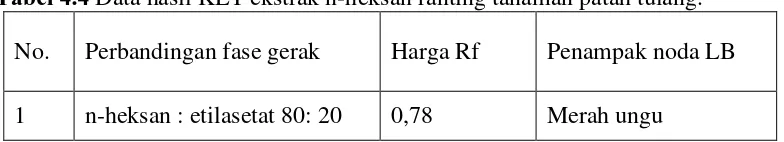
[image:33.595.116.508.369.440.2]Hasil uji kemurnian isolat dengan KLT menggunakan fase gerak n-heksan-etilasetat dengan perbandingan (80:20) dan toluen : etilasetat (90:10) dan penampak bercak adalah pereaksi LB, memberikan bercak tunggal berwarna merah ungu pada Rf 0,78, hasilnya dapat dilihat pada Tabel 4.4 dan pola kromatogramnya dapat dilihat pada Lampiran 6.
Tabel 4.4 Data hasil KLT ekstrak n-heksan ranting tanaman patah tulang. No. Perbandingan fase gerak Harga Rf Penampak noda LB 1 n-heksan : etilasetat 80: 20 0,78 Merah ungu
Pemeriksaan uji kemurnian KLT dua arah dengan fase gerak pertama n-heksan-etilasetat (80:20), dan fase gerak kedua toluen-etilasetat (90:10) dengan penampak bercak pereaksi LB, hasilnya tetap memberikan satu bercak warna merah ungu dengan harga Rf 0,78. Ini menunjukkan bahwa triterpenoid yang dihasilkan dari KLT preparatif telah murni.
4.7Hasil Karakterisasi Isolat Dengan Spektrofotometri Ultraviolet Dan Inframerah
34
35 BAB V
KESIMPULAN DAN SARAN
5.1Kesimpulan
a. Hasil karakterisasi simplisia batang tanaman patah tulang diperoleh kadar air 5,97%, kadar sari yang larut dalam air 12,22%, kadar sari yang larut dalam etanol 17,37%, kadar abu total 3,21% dan kadar abu yang tidak larut asam 0,78%.
b. Golongan senyawa kimia simplisia batang tanaman patah tulang adalah, alkaloid, flavonoid, tanin dan triterpen/steroid.
c. Hasil pengukuran spektrum secara spektrofotometri UV isolat memberikan absorbsi maksimum pada panjang gelombang 202,60 nm. Hasil pengukuran spektrofotometri inframerah menunjukkan adanya gugus C-O, C=O, -CH2,-CH3, C-H alifatis dan -OH.
5.2Saran
4 BAB II
TINJAUAN PUSTAKA
2.1Uraian Tumbuhan 2.1.1 Habitat
Tanaman patah tulang merupakan salah satu dari 8000 tumbuhan yang berasal dari suku Euphorbiaceae.Tanaman patah tulang merupakan tanaman yang hidup di daerah tropis, menyukai tempat terbuka dan banyak sinar matahari langsung.Tanaman patah tulang di Indonesia biasanya banyak ditanam di halaman rumah, di pot atau sebagai tanaman pagar (Setiorini dkk., 2014).
2.1.2 Morfologi tumbuhan
Tanaman patah tulang berbentuk perdu yang tumbuh tegak, mempunyai tinggi 2-6 meter dengan pangkal berkayu, bercabang bayak, dan bergetah seperti susu yang bersifat toksik terhadap kulit, mata, dan beberapa serangga. Patah tulang mempunyai ranting yang bulat silindris berbentuk pensil, beralur halus membujur dan berwarna hijau. Ranting patah tulang setelah tumbuh sekitar satu jengkal akan segera bercabang dua yang letaknya melintang demikian seterusnya, sehingga tampak seperti percabangan yang terpatah-patah (Dalimartha, 2007).
5 2.1.3 Sistematika tumbuhan
Menurut Herbanium Medanense Universitas Sumatera Utara (2014), tanaman patah tulang diklasifikasikan sebagai berikut:
Kingdom : Plantae
Divisio : Spermatophyta Kelas : Dicotyledoneae Ordo : Euphorbiales Famili : Euphorbiaceae Genus : Euphorbia
Spesies : Euphorbia tirucalli L. 2.1.4 Nama daerah
Patah tulang memiliki nama daerah kayu urip di Jawa, kayu tabar dalam bahasa Madura, susuru dalam bahasa Sunda, dan di luar negeri seperti Tiongkok disebut sebagai Lu San Hu (Dalimartha, 2007).
2.1.5 Kandungan kimia
6
yaitu alkaloid, tannin, steroid, flavonoid, triterpenoid, dan hidroquinon.Dengan pelarut etanol metabolit sekunder yang terdapat pada ranting tanaman patah tulang adalah alkaloid, steroid, flavonoid, triterpenoid, saponin dan hidroquinon (Setiorini dkk., 2014).
2.2 Uraian Kimia
2.2.1 Triterpenoid/steroid
Triterpenoid adalah senyawa yang kerangka karbonnya berasal dari enam satuan isoprena dan secara biosintesis diturunkan dari hidrokarbon C30 asiklik, yaitu skualen.Senyawa tersebut mempunyai struktur siklik yang relatif kompleks, kebanyakan merupakan suatu alkohol, aldehid atau asam karboksilat. Triterpenoid adalah senyawa tanpa warna, berbentuk kristal, sering kali bertitik leleh tinggi dan aktif optik, dapat dibagi atas 4 kelompok senyawa yaitu triterpen sebenarnya, steroid, saponin dan glikosida jantung (Harborne, 1987). Struktur kimia isopren dapat dilihat pada gambar.
Struktur kimia isopren
Pembagian triterpenoid berdasarkan jumlah cincin yang terdapat pada struktur molekulnya (Robinson, 1995), antara lain:
7
b. Triterpenoid trisiklik, yaitu triterpenoid yang mempunyai tiga cincin tertutup dalam cincin molekulnya, contohnya ambrein.
c. Triterpenoid tetrasiklik, yaitu triterpenoid yang mempunyai empat cincin tertutup dalam cincin molekulnya, contohnya lanosterol.
d. Triterpenoid pentasiklik, yaitu triterpenoid yang mempunyai lima cincin tertutup dalam cincin molekulnya, contohnya α-amirin. Contoh struktur kimia triterpenoid dapat dilihat pada gambar
struktur dasar triterpen
skualen ` ambrein
lanosterol α-amirin
Contoh struktur kimia triterpenoid
Steroid adalah triterpen yang kerangka dasarnya sistem cincin siklopentana perhidrofenanten (Harborne, 1987).
OH
H
OH
8 Struktur dasar steroid dan sistem penomorannya
Senyawa steroid dahulu dianggap sebagai senyawa yang hanya terdapat pada hewan tetapi sekarang ini makin banyak senyawa steroid yang ditemukan dalam tumbuhan (fitosterol).Fitosterol merupakan senyawa steroid yang berasal dari tumbuhan.Senyawa fitosterol yang biasa terdapat pada tumbuhan tinggi yaitu sitosterol, stigmasterol dan kampesterol (Harborne, 1987).
2.2.2 Alkaloid
Menurut Harborne, alkaloid adalah senyawa bersifat basa yang mengandung satu atau lebih atom nitrogen yang terletak dalam sistem siklik. Alkaloid mempunyai aktivitas fisiologi yang menonjol sehingga digunakan secara luas dalam bidang pengobatan.
Ada tiga pereaksi yang sering digunakan dalam skrining fitokimia untuk mendeteksi golongan senyawa alkaloid sebagai pereaksi pengendapan yaitu pereaksi Mayer, Bouchardat dan Dragendroff (Farnsworth, 1966).
Manfaat alkaloid dalam bidang kesehatan antara lain adalah memicu sistem saraf, menaikkan atau menurunkan tekanan darah, dan melawan infeksi mikroba (Aldhani, E., 2014).
8 9 5 6 7 10
A
B
C
D
4 1 2 3 12 11 1914 15
16 13 17 18 20 21 22 23
24 25
26
9 2.2.3 Glikosida
Glikosida adalah senyawa organik yang bila dihidrolisis menghasilkan satu atau lebih gula yang disebut glikon dan bagian bukan gula disebut aglikon.Gula yang paling sering dijumpai dalam glikosida adalah glukosa.Sacara kimia dan fisiologi, glikosida alam cenderung dibedakan berdasarkan bagian aglikonnya (Robinson, 1995).
Berdasarkan ikatan antara glikon dan aglikon (Sirait, 2007), glikosida dapat dibedakan menjadi :
a. Tipe O-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan O. Contoh: Kuersetin
b. Tipe S-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan S. Contoh: sinigrin
Gambar 2.5 Sinigrin
[image:41.595.193.383.421.513.2]10
d. Tipe C-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan C. Contoh: aloin.
2.2.4 Flavonoid
Golongan flavonoid dapat digambarkan sebagai deretan senyawa C6-C3-C6, artinya kerangka karbonya terdiri atas dua gugus C6 (cincin benzena tersubstitusi) disambungkan oleh rantai alifatik tiga karbon (Robinson, 1995).Flavonoid mencangkup banyak pigmen yang banyak terdapat pada tumbuhan mulai dari jamur sampai angiospermae.Pada tumbuhan tinggi, flavonoid terdapat baik dalam bagian vegetatif maupun dalam bunga. Fungsi flavonoid pada tumbuhan adalah dapat menarik burung dan serangga yang membantu proses penyerbukan, pengatur tumbuh, pengatur fotosintesis, kerja antimikroba dan antivirus (Robinson, 1995).
Senyawa flavonoida memiliki aktifitas antioksidan, antibiotik (Roslizawatydkk., 2013) antikoagulan, antimikrobadan antiinflamasi(Lata dan Dubey, 2010). Makanan yang kaya flavonoid digunakan untuk mengobati penyakit-penyakit seperti kanker dan penyakit jantung (Robinson,1995).
11
Saponin adalah sekelompok senyawa dengan struktur triterpenoid yang mengikat satu atau lebih gula sehingga memiliki sisi hidrofil dan lipofil dengan penggocokan akan menimbulkan buih (Saifudin dkk., 2011). Saponin merupakan senyawa aktif permukaan yang kuat, dapat menimbulkan busa jika dikocok dalam air, pada konsentrasi rendah sering menyebabkan hemolisis sel darah merah (Robinson, 1995). Uji saponin sederhana adalah dengan mengocok ekstrak alkohol air dari tumbuhan dalam tabung reaksi, maka akan terbentuk busa yang bertahan lama pada permukaan cairan (Harborne, 1987).
2.2.6 Tanin
Tanin merupakan salah satu senyawa metabolitme sekunder yang termasuk kedalam golongan polifenol yang terdapat dalam tumbuhan, yang mempunyai rasa sepat dan memiliki kemampuan menyamakan kulit.Tanin terdapat luas dalam tumbuhan berpembuluh, dalam angiospermae terdapat khusus dalam jaringan kayu (Harborne, 1987).
2.3 Metode Ekstraksi
Ekstraksi adalah proses penarikan zat aktif yang terdapat dalam tumbuhan dengan pelarut yang sesuai. Metode ekstraksi terdiri dari maserasi, perkolasi, Soxhlet, refluks, dan destilasi uap. Maserasi dan perkolasi merupakan metode yang paling sederhana dan ekonomis (Sarker dkk., 2006).
12
pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnnya dilakukan pada suhu kamar (Depkes RI., 2000).
2.4 Kromatografi
International Union Of Pure and Applied Chemistry (IUPAC) (1993) mendefinisikan kromatografi adalah metode pemisahan secara fisika yang mana komponen-komponen yang akan dipisahkan terbagi diantara dua fase, yang satu fase diam sementara yang lain adalah fase gerak yang bergerak kearah tertentu (Gandjar dan Rohman, 2012).
Cara-cara kromatografi dapat digolongkan sesuai dengan sifat-sifat dari fase diam, yang berupa zat padat atau cair.Jika fase diam berupa zat padat disebut kromatografi serapan, jika berupa zat cair disebut kromatografi partisi. Karena fase gerak berupa zat cair atau gas maka terdapat 4 macam sistem kromatografi, yaitu:
1. Fase gerak zat cair - fase diam padat (kromatografi serapan): - Kromatografi lapis tipis
- Kromatografi kolom
2. Fase gerak gas - fase diam padat - Kromatografi gas - padat
3. Fase gerak zat cair - fase diam zat cair (kromatografi partisi) - Kromatografi kertas
13 - Kromatografi kolom kapiler
Pemisahan dengan kromatografi tergantung pada kenyataan bahwa senyawa-senyawa yang dipisahkan terdistribusi diantara fase gerak dan fase diam dalam perbandingan yang sangat berbeda-beda dari satu senyawa terhadap senyawa yang lain (Sastrohamidjojo, 1991).
2.4.1 Kromatografi lapis tipis
Kromatografi lapis tipis (KLT) adalah metode pemisahan fisikokimia.Lapisan yang memisahkan, yang terdiri atas bahan berbutir-butir (fase diam), ditempatkan pada penyangga berupa pelat gelas, logam, atau lapisan yang cocok. Campuran yang akan dipisahkan, berupa larutan, ditotolkan berupa bercak atau pita. Setelah plat atau lapisan diletakkan dalam bejana tertutup rapat yang berisi larutan pengembang yang cocok (fase gerak), pemisahan terjadi selama perambatan kapiler.Senyawa yang tidak berwarna harus ditampakkan (Stahl,1985).
Pendeteksian bercak hasil pemisahan dapat dilakukan dengan beberapa cara, untuk senyawa tak berwarna cara yang paling sederhana adalah dilakukan pengamatan dengan sinar ultraviolet. Beberapa senyawa organik bersinar atau berfluorosensi jika disinari dengan sinar ultraviolet gelombang pendek (254 nm) atau gelombang panjang (366 nm), jika dengan cara itu senyawa tidak dapat dideteksi maka harus dicoba disemprot dengan pereaksi yang membuat bercak tersebut tampak yaitu pertama tanpa pemanasan, kemudian bila perlu dengan pemanasan (Gritter dkk., 1991; Stahl, 1985).
14
Kromatografi lapis tipis, fase diam berupa lapisan tipis yang terdiri atas bahan padat yang dilapiskan pada permukaan penyangga datar yang biasanya terbuat dari kaca, plat polimer atau logam. Lapisan melekat pada permukaan dengan bantuan bahan pengikat, biasanya kalsium sulfat atau amilum. Penyerap yang umum dipakai untuk kromatografi lapis tipis adalah silika gel, alumina, kieselgur dan selulosa (Gritter dkk., 1991).
Dua sifat yang penting dari fase diam adalah ukuran partikel dan homogenitasnya, karena adesi terhadap penyokong sangat tergantung pada kedua sifat tersebut.Ukuran partikel yang biasa digunakan adalah 1-25 mikron. Partikelyang butirannya sangat kasar tidak akan memberikan hasil yang memuaskan dan salah satu cara untuk memperbaiki hasil pemisahan adalah dengan menggunakan fase diam yang butirannya lebih halus. Butiran yang halus memberikan aliran pelarut yang lebih lambat dan resolusi yang lebih baik (Sastrohamidjojo, 1985).
b. Fase gerak (pelarut pengembang)
Fase gerak ialah medium angkut yang terdiri atas satu atau beberapa pelarut, jika diperlukan sistem pelarut multi komponen, harus berupa suatu campuran sesederhana mungkin yang terdiri atas maksimum tiga komponen (Stahl, 1985).
15
karbontetraklorida, benzen, kloroform, eter, etilasetat, piridian, aseton, etanol, metanol dan air (Gritter dkk., 1991).
c. Harga Rf
Mengidentifikasi noda-noda dalam kromatografi lapis tipis sangat lazim menggunakan harga Rf (Retordation Factor) mulai dari 0 sampai 1.
�� = Jarak titik pusat bercak dari titik awal Jarak garis depan pelarut dari titik awal
Faktor-faktor yang mempengaruhi harga Rf yaitu struktur kimia dari senyawa yang dipisahkan, sifat penjerap, tebal dan kerataan dari lapisan penjerap, pelarut dan derajat kemurniannya, derajat kejenuhan uap pengembang dalam bejana, teknik percobaan, jumlah cuplikan yang digunakan, suhu dan kesetimbangan (Sastrohamidjojo, 1985).
2.4.2 Kromatografi lapis tipis preparatif
Kromatografi lapis tipis (KLT) preparatif merupakan salah satu metode pemisahan dengan menggunakan peralatan sederhana. Ketebalan penjerap yang sering dipakai adalah 0,5-2 mm, ukuran plat kromatografi biasanya 20 x 20 cm. Pembatasan ketebalan lapisan dan ukuran plat sudah tentu mengurangi jumlah bahan yang dapat dipisahkan dengan KLT preparatif. Penjerap yang paling umum digunakan adalah silika gel (Gritter dkk., 1991).
16
cuplikan adalah pelarut yang atsiri. Pengembangan plat KLT preparatif dilakukan dalam bejana kaca yang dapat menampung beberapa plat. Bejana dijaga tetapjenuh dengan pelarut pengembang dengan bantuan kertas saring yang diletakkan berdiri disekeliling permukaan bagian dalam bejana. Pita ditampakkan dengan cara yang tidak merusak maka senyawa yang tidak berwarna dengan penjerap dikerok dari plat kaca. Cara ini berguna untuk memisahkan campuran beberapa senyawa sehingga diperoleh senyawa murni (Gritter dkk., 1991).
2.4.3 Kromatografi lapis tipis dua arah
KLT dua arah atau KLT dua dimensi ini bertujuan untuk meningkatkan resolusi sampel ketika komponen-komponen solut mempunyai karakteristik kimia yang hampir sama, karena nilai Rf juga hampir sama, selain itu dua sistem fase gerak yang sangat berbeda dapat digunakan secara berurutan pada suatu campuran tertentu sehingga memungkinkan untuk melakukan pemisahan analit yang mempunyai tingkat polaritas yang hampir sama (Rohman, 2009).
KLT dua arah dilakukan dengan melakukan penotolan sampel disalah satu sudut lapisan lempeng tipis dan mengembangkannya sebagaimana biasa dengan eluen pertama.Lempeng kromatografi selanjutnya dipindahkan dari chamber yang menggunakan eluen kedua sehingga pengembangan dapat terjadi pada arah kedua yang tegak lurus dengan arah pengembangan yang pertama.Suksesnya pemisahantergantung pada kemampuan untuk memodifikasi selektifitas eluen kedua dibandingkan dengan selektifitas eluen pertama (Rohman, 2009).
17
Spektrofototmetri Ultra Violet merupakan suatu analisis berdasarkan atas pengukuran serapan radiasi monokromatis oleh molekul zat terlarut dalam suatu larutan.Penyerapan sinar ultra violet sering dikenal sebagai spektroskopi elektronik (Aksara dkk., 2013).
Spektrofotometer UV pada umumnya digunakan untuk menentukan jenis kromofor, ikatan rangkap yang terkonjugasi dan auksokrom dari suatu senyawa organik, menjelaskan informasi dari struktur berdasarkan panjang gelombang maksimum suatu senyawa dan mampu menganalisis senyawa organik secara kuantitatif dengan menggunakan hukum Lambert-Beer (Dachriyanus, 2004).
Elektron yang terlibat dalam beberapa molekul organik pada penyerapan sinar UV adalah electron sigma (δ), elektro phi (π) dan non bonding electron (n).Elektron δ merupakan electron yang membentuk ikatan tunggal dan electron π
terdapat ikatan rangkap (Gandjar dan Rohman, 2012).
2.6Spektrofotometri Infra Merah
Spektra infra merah mengandung banyak serapan yang dihubungkan dengan sistem vibrasi yang berinteraksi dalam molekul, dan karena mempunyai karakteristik yang unik untuk setiap molekul maka dalam spektrum memberikan pita-pita serapan yang karakteristik juga (Sastrohamidjojo, 1985).
1 BAB I PENDAHULUAN
1.1LatarBelakang
Tanaman patah tulang (Euphorbia tirucalli L.) berasal dari Afrika, namun secara luas ditanam dan mengalami penyebaran di seluruh daerah tropis dan subtropis.Tanaman ini di Indonesia tumbuh dengan baik dan dikenal sebagai salah satu jenis tanaman yang biasa digunakan masyarakat sebagai obat tradisional. Tanaman patah tulang memiliki getah yang putih seperti susu, getah yang berasal dari potongan dahan dan ranting tanaman ini mengandung triterpen (Supriyanto dan Luviana, 2010).
Menurut Van Damme penggunaan tanaman ini secara tradisional berbeda-beda di setiap negara, di Afrika digunakan untuk pengobatan impoten, epilepsi, kutil, sakit gigi, wasir, dan gigitan ular.Di Brazil digunakan untuk pengobatan kanker, tumor dan kutil sedangkan di Indonesia digunakan untuk pengobatan patah tulang, wasir, bisul, dan kapalen (Mwine dkk., 1999).
Ada beberapapenggolonganmetabolitsekunder, yaitu alkaloid, flavonoid, steroid/ triterpenoid, tanin, glikosidadanantrakuinon.(Harbone, 1987).Senyawa triterpenoid/steroidmenunjukkan berbagai macam aktifitas fisiologi yang telah digunakan untuk antifungi, insektisida, antibakteri atau antivirus (Robinson, 1995).
Berdasarkanuraian diatas, peneliti merasa tertarik untukmelakukanpenelitiantentangkarakterisasisimplisia,
2
carakromatografi lapis tipis (KLT) dan dipisahkan dengan KLT preparatif. Isolat yang diperoleh diidentifikasi dengan spektrofotometer UV dan IR.
1.2 PerumusanMasalah
Berdasarkan latar belakang di atas, peneliti membuat rumusan masalah sebagai berikut:
1. Apakah simplisia batang tanaman patah tulang dapat ditentukan karakteristiknya?
2. Apakah senyawa triterpenoid dari ekstrak n-heksan batang tanaman patah tulang dapat diisolasi dengan KLT preparatif?
3. Apakah senyawa triterpenoid hasil isolasi dapat diidentifikasi secara spektrofotometri UV dan spektrofotometri IR?
1.3 Hipotesis
Adapun perumusan masalah yang dibuat peneliti adalah:
1. Karakteristiksimplisiabatangtanaman patah tulang
dapatditentukandenganmenggunakanprosedurkarakterisasi.
2. Senyawa triterpenoid dari ekstrak n-heksan batang tanaman patah tulang dapat diisolasi dengan KLT preparatif.
3 1.4 TujuanPenelitian
Tujuan penelitian ini adalah untuk :
1. Mengetahui karakteristik simplisiabatangtanaman patah tulang.
2. Mengisolasisenyawatriterpenoid yang terdapatdalam ekstrak n-heksan batang tanaman patah tulang.
3. Mengidentifikasi senyawa
triterpenoidhasilisolasisecaraspektrofotometri UV danspektrofotometri IR.
1.5ManfaatPenelitian
vi
ISOLASI DAN KARAKTERISASI TRITERPENOID DARI TANAMAN PATAH TULANG (Euphorbia tirucalli L.)
ABSTRAK
Tanaman patah tulang merupakan tanaman yang dapat tumbuh subur di daerah tropis dan subtropis.Tanaman yang berasal dari Afrika ini diketahui banyak digunakan untuk pengobatan tradisional untuk pengobatan tulang yang patah, sebagai insektisida, pengobatan bisul, antibakteri, antiinflamasi, anelgesik, dan gigitan ular.Senyawa triterpenoid mempunyai aktivitas fisiologis untuk pengobatan diabetes, gangguan menstruasi, patukan ular, gangguan kulit, kerusakan hati, antimalaria, antifungi, insektisida, antibakteri dan antivirus. Tujuan penelitian ini adalah untuk mengetahui karakterisasi simplisia dan skrining fitokimia serta isolasi triterpenoid dari ekstrak n-heksan tanaman secara spektrofotometri ultraviolet (UV) dan spektrofotometri inframerah (IR).
Terhadap serbuk simplisia ranting tanaman patah tulang dilakukan karakterisasi dan skrining fitokimia, selanjutnya dimaserasi dengan pelarut n-heksan selama 24 jam sambil sesekali diaduk dan ampas dimaserasi kembali sampai diperoleh maserat yang jernih. Maserat digabung dan dipekatkan dengan
rotary evaporator ((± 40°C). Selanjutnya dianalisa secara kromatografi lapis tipis (KLT) dengan fase gerak n-heksan : etilasetat dengan beberapa perbandingan, sebagai penampak bercak digunakan pereaksi LiebermanBurchard. Ekstrak n-heksan dipisahkan dengan KLT preparatif menggunakan fase gerak n-n-heksan : etilasetat, kemudian diuji kemurniannya secara KLT satu arah dan KLT dua arah. Isolat murni yang diperoleh diidentifikasi dengan spektrofotometer UV dan IR.
Hasil karakterisasi serbuk simplisia diperoleh kadar air 5,79%; kadar sari larut dalam air 12,22%; kadar sari larut dalam etanol 17,37%; kadar abu total 3,21%; kadar abu tidak larut asam 0,78%. Hasil skrining fitokimia diperoleh golongan alkaloid, antrakuinon glikosida, flavonoid, tannin, dan triterpenoid. Ekstrak n-heksan tanaman patah tulang dianalisis secara KLT menggunakan plat pra lapis tipis silika gel F254dan fase gerak n-heksan-etilasetat dengan perbandingan (90:10), (80:20), (70:30). Hasil KLT ekstrak n-heksan diperoleh fase gerak n-heksan : etilasetat (80:20) yang memberikan pemisahan yang terbaik, hasil KLT preparatif diperoleh isolat murni pada Rf 0,78 berwarna merah ungu dengan LB. Isolat memberikan absorbansi maksimum pada panjang gelombang 202,60 nm dengan spektrofotometer UV dan hasil spektrofotometer IR menunjukkan adanya gugus OH, -CH, -CH2, -C=O, -C-O.
Kata kunci: Tanaman patah tulang, karakterisasi, skrining fitokimia, isolasi
vii
ISOLATION AND CHARACTERISTICS OF PATAH TULANG PLANTS (Euphorbia tirucalli L.)
ABSTRACT
Patah tulang plant is a plant that can thrive in the tropics and subtropics. Plants from Afrika is known to many people that use for trditional medicine for broken bones treatment, as insectiside, ulcers treatment, antibacterial, anti inflammatory, analgesic, and snakebite. Triterpenoid compounds have physiological activity for diabetic treatment, menstrual disorders, pecks snake, skin disorders, liver damage, malaria, antifungal, insecticidal, antibacterial or antiviral. The purpose of this research was determine to the characteristics of the simplisia and phytochemicals screening and triterpenoids isolation of n-hexane extracs of patah tulang plants by ultraviolet (UV) spectrophotometry and infrared spectrophotometry (IR).
About the simplisia powder of the patah tulang stem plants characterization and phytochemical screening, then macerated with with n-hexane solvent for 24 hours while stirring occasionally and macerated the pulp again until obtained the clear macerat. Macerat combined and concentrated by rotary evaporator (± 40°C). Then analyzed by Thin Layer Chromatography (TLC) with a n-hexane mobile phase : ethyl acetate with some comparisons, as visible spotting Lieberman Burchard reagent. N-hexane extracts were separated by preparative TLC using the n-hexane mobile phase : ethylacetate, and get tested for purity by one-way TLC and two-way TLC. Pure isolates were identified by UV and IR means.
Simplicia powder characterization results obtained 5.97% water contained, water soluble extract content 12.22% :soluble extract content in ethanol 17.37% : total ash content 3.21% and acid insoluble ash content 0.78%. Phytochemical screening results obtained alkaloids, anthraquinone glycosides, flavonoids, tannins and triterpenoids/steroids. N-hexan extract of patah tulang plant analyze TLC using thin layer silica gel F254and n-hexana mobile phase : ethyl acetate with comparison (90:10), (80:20), (70:30). TLC results hexane extract obtained n-hexane mobile phase : ethyl acetate (80:20) that gave the best separation, the results obtained by TLC preparative pure isolates at Rf 0.78 scarlet with LB. Isolates provides maximum absorbance at a wavelength of 202.60 nm with UV spectrophotometry and IR spectrophotometry result indicate a clusterOH, CH, -CH2, -C=O, -C-O.
ISOLASI DAN KARAKTERISASI TRITERPENOID DARI
TANAMAN PATAH TULANG (Euphorbia tirucalli L.)
SKRIPSI
OLEH: Kriston Nababan
NIM 091501107
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
ISOLASI DAN KARAKTERISASI TRITERPENOID DARI
TANAMAN PATAH TULANG (Euphorbia tirucalli L.)
SKRIPSI
OLEH:
KRISTON NABABAN NIM 091501107
Diajukan untuk melengkapi salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
iv
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa yang telah melimpahkan rahmat dan anugerah-Nya sehingga penulis menyelesaikan skripsi ini yang berjudul “Isolasi dan Karakterisasi Triterpenoid dari Tanaman Patah Tulang (Euphorbia tirucalli L.)”. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
Penulis mengucapkan terimakasih yang sebesar-besarnya kepada IbuDr. Masfria, M.S., Apt.selaku PejabatDekan Fakultas Farmasi Universitas Sumatera Utara yang telah memberikan bantuan dan fasilitas selama masa pendidikan. IbuDra. Masria Lasma Tambunan, M.Si., Apt.,danBapakDrs. Nahitma Ginting, M.Si., Apt., selaku pembimbing yang telah memberikan waktu, bimbingan, dan nasehat selama penelitian dan penulisan skripsi ini berlangsung. Bapak Prof. Dr. Ginda Haro, M.Sc., Apt., bapak Drs. Fathur Rahman Harun, M.Si., Apt., dan ibu Dra. Siti Nurbaya, M.Si., Apt., selaku dosen penguji yang memberikan masukan, kritikan, arahan, dan saran dalam penyusunan skripsi ini.Ibu Dra. Aswita Hafni Lubis, M.Si., Apt. selaku Kepala Laboratorium Fitokimia Fakultas Farmasi Universitas Sumatera Utara yang telah memberikan fasilitas, petunjuk dan membantu selama penelitian. Ibu Dra. Masria Lasma Tambunan, M.Si., Apt., selaku pembimbing akademis, serta Bapak dan Ibu staf pengajar Fakultas Farmasi Universitas Sumatera Utara yang telah membimbing penulis selama masa pendidikan.
v
Bosfer Taripar Rikardo Nababan S. H., M. Hum., kakak Ester Dermina Nababan S.kep., adik Reymon Erikson Nababan dan Teresia Rut Junita Nababan. Terima kasih atas doa, dorongan dan pengorbanan baik moril maupun materil dalam penyelesaian skripsi ini.
Penulis menyadari skripsi ini masih belum sempurna, oleh karena itudiharapkan kritik dan saran yang membangun untuk penyempurnaannya. Harapan saya semoga skripsi ini dapat bermanfaat bagi ilmu pengetahuan kefarmasian.
.
Medan, Oktober2015 Penulis,
vi
ISOLASI DAN KARAKTERISASI TRITERPENOID DARI TANAMAN PATAH TULANG (Euphorbia tirucalli L.)
ABSTRAK
Tanaman patah tulang merupakan tanaman yang dapat tumbuh subur di daerah tropis dan subtropis.Tanaman yang berasal dari Afrika ini diketahui banyak digunakan untuk pengobatan tradisional untuk pengobatan tulang yang patah, sebagai insektisida, pengobatan bisul, antibakteri, antiinflamasi, anelgesik, dan gigitan ular.Senyawa triterpenoid mempunyai aktivitas fisiologis untuk pengobatan diabetes, gangguan menstruasi, patukan ular, gangguan kulit, kerusakan hati, antimalaria, antifungi, insektisida, antibakteri dan antivirus. Tujuan penelitian ini adalah untuk mengetahui karakterisasi simplisia dan skrining fitokimia serta isolasi triterpenoid dari ekstrak n-heksan tanaman secara spektrofotometri ultraviolet (UV) dan spektrofotometri inframerah (IR).
Terhadap serbuk simplisia ranting tanaman patah tulang dilakukan karakterisasi dan skrining fitokimia, selanjutnya dimaserasi dengan pelarut n-heksan selama 24 jam sambil sesekali diaduk dan ampas dimaserasi kembali sampai diperoleh maserat yang jernih. Maserat digabung dan dipekatkan dengan
rotary evaporator ((± 40°C). Selanjutnya dianalisa secara kromatografi lapis tipis (KLT) dengan fase gerak n-heksan : etilasetat dengan beberapa perbandingan, sebagai penampak bercak digunakan pereaksi LiebermanBurchard. Ekstrak n-heksan dipisahkan dengan KLT preparatif menggunakan fase gerak n-n-heksan : etilasetat, kemudian diuji kemurniannya secara KLT satu arah dan KLT dua arah. Isolat murni yang diperoleh diidentifikasi dengan spektrofotometer UV dan IR.
Hasil karakterisasi serbuk simplisia diperoleh kadar air 5,79%; kadar sari larut dalam air 12,22%; kadar sari larut dalam etanol 17,37%; kadar abu total 3,21%; kadar abu tidak larut asam 0,78%. Hasil skrining fitokimia diperoleh golongan alkaloid, antrakuinon glikosida, flavonoid, tannin, dan triterpenoid. Ekstrak n-heksan tanaman patah tulang dianalisis secara KLT menggunakan plat pra lapis tipis silika gel F254dan fase gerak n-heksan-etilasetat dengan perbandingan (90:10), (80:20), (70:30). Hasil KLT ekstrak n-heksan diperoleh fase gerak n-heksan : etilasetat (80:20) yang memberikan pemisahan yang terbaik, hasil KLT preparatif diperoleh isolat murni pada Rf 0,78 berwarna merah ungu dengan LB. Isolat memberikan absorbansi maksimum pada panjang gelombang 202,60 nm dengan spektrofotometer UV dan hasil spektrofotometer IR menunjukkan adanya gugus OH, -CH, -CH2, -C=O, -C-O.
Kata kunci: Tanaman patah tulang, karakterisasi, skrining fitokimia, isolasi
vii
ISOLATION AND CHARACTERISTICS OF PATAH TULANG PLANTS (Euphorbia tirucalli L.)
ABSTRACT
Patah tulang plant is a plant that can thrive in the tropics and subtropics. Plants from Afrika is known to many people that use for trditional medicine for broken bones treatment, as insectiside, ulcers treatment, antibacterial, anti inflammatory, analgesic, and snakebite. Triterpenoid compounds have physiological activity for diabetic treatment, menstrual disorders, pecks snake, skin disorders, liver damage, malaria, antifungal, insecticidal, antibacterial or antiviral. The purpose of this research was determine to the characteristics of the simplisia and phytochemicals screening and triterpenoids isolation of n-hexane extracs of patah tulang plants by ultraviolet (UV) spectrophotometry and infrared spectrophotometry (IR).
About the simplisia powder of the patah tulang stem plants characterization and phytochemical screening, then macerated with with n-hexane solvent for 24 hours while stirring occasionally and macerated the pulp again until obtained the clear macerat. Macerat combined and concentrated by rotary evaporator (± 40°C). Then analyzed by Thin Layer Chromatography (TLC) with a n-hexane mobile phase : ethyl acetate with some comparisons, as visible spotting Lieberman Burchard reagent. N-hexane extracts were separated by preparative TLC using the n-hexane mobile phase : ethylacetate, and get tested for purity by one-way TLC and two-way TLC. Pure isolates were identified by UV and IR means.
Simplicia powder characterization results obtained 5.97% water contained, water soluble extract content 12.22% :soluble extract content in ethanol 17.37% : total ash content 3.21% and acid insoluble ash content 0.78%. Phytochemical screening results obtained alkaloids, anthraquinone glycosides, flavonoids, tannins and triterpenoids/steroids. N-hexan extract of patah tulang plant analyze TLC using thin layer silica gel F254and n-hexana mobile phase : ethyl acetate with comparison (90:10), (80:20), (70:30). TLC results hexane extract obtained n-hexane mobile phase : ethyl acetate (80:20) that gave the best separation, the results obtained by TLC preparative pure isolates at Rf 0.78 scarlet with LB. Isolates provides maximum absorbance at a wavelength of 202.60 nm with UV spectrophotometry and IR spectrophotometry result indicate a clusterOH, CH, -CH2, -C=O, -C-O.
viii DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
PENGESAHAN SKRIPSI ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... viii
DAFTAR LAMPIRAN ... ix
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Rumusan Masalah ... 2
1.3 Hipotesis ... 2
1.4 Tujuan Penelitian ... 2
1.5 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Uraian Tumbuhan ... 4
2.1.1 Habitat ... 4
2.1.2 Morfologi Tumbuhan ... 4
2.1.3 Sistematika Tumbuhan ... 5
2.1.4 Nama Daerah ... 5
ix
2.2 Uraian Kimia ... 6
2.2.1 Triterpenoid/steroid ... 6
2.2.2 Alkaloid ... 8
2.2.3 Glikosida ... 8
2.2.4 Flavonoid ... 9
2.2.5 Saponin ... 10
2.2.6 Tanin ... 10
2.3 Metode Ekstraksi ... 10
2.4 Kromatografi ... 11
2.4.1 Kromatografi lapis tipis ... 12
2.4.2 Kromatografi lapis tipis preparatif ... 15
2.4.3 Kromatografi lapis tipisdua arah ... 15
2.5 Spektrofotometri Ultraviolet ... 16
2.6 Spektrofotometri Infrared ... 17
BAB III METODE PENELITIAN ... 18
3.1 Alat dan Bahan ... 18
3.1.1Alat ... 18
3.1.2 Bahan ... 18
3.2 Pembuatan Larutan Pereaksi ... 19
3.2.1 Pereaksi Liebermann-Burchard ... 19
3.2.2 Pereaksi asam sulfat 2 N ... 19
3.2.3 Pereaksi Molisch ... 19
3.2.4 Pereaksi Meyer ... 19
x
3.2.6 Pereaksi Dragendorff ... 20
3.2.7 Pereaksi Bouchardat ... 20
3.2.8 Pereaksi natrium hidroksida 2 N ... 20
3.2.9 Pereaksi asam nitrat 0,5 N ... 20
3.2.10 Pereaksi timbal (II) asetat 0,4 M ... 20
3.3 Pengambilan dan Pengolahan Sampel ... 20
3.3.1 Pengambilan sampel... 20
3.3.2 Identifikasi tumbuhan... 21
3.3.3 Pembuatan simplisia ... 21
3.4 Karakterisasi Simplisia ... 21
3.4.1 Penetapan kadar air ... 21
3.4.2 Penetapan kadar abu total... 22
3.4.3 Penetapan kadar abu yang tidak larut dalam asam ... 22
3.4.5 Penetapan kadar sari yang larut dalam air... 22
3.4.6 Penetapan kadarsari yang larut dalam etanol ... 22
3.5 Skrining Fitokimia ... 23
3.5.1 Pemeriksaan triterpenoid/steroid ... 23
3.5.2 Pemeriksaan alkaloid ... 24
3.5.3 Pemeriksaan glikosida ... 24
3.5.4 Pemeriksaan glikosida antrakinon... 25
3.5.5 Pemeriksaan flavonoid ... 25
3.5.6 Pemeriksaan saponin ... 25
3.5.7 Pemeriksaan tanin ... 25
xi
3.7Analisis Ekstrak n-Heksana Secara KLT ... 26
3.8 Isolasi Senyawa Triterpenoid Secara KLT Preparatif ... 27
3.9 Uji Kemurnian Isolat ... 28
3.9.1 Uji kemurnian isolat dengan KLT satu arah ... 28
3.9.2 Uji kemurnian isolat dengan KLT dua arah ... 28
3.10 Karakterisasi Isolat ... 29
3.10.1 Karakterisasi isolat dengan spektrofotometri UV ... 29
3.10.2 Karakterisasi isolat dengan spektrofotometri IR ... 29
BAB IV HASIL DAN PEMBAHASAN ... 30
4.1 Hasil Identifikasi Tumbuhan ... 30
4.2 Hasil Ekstrasi Serbuk Simplisia ... 30
4.3 Hasil Karakterisasi Simplisia ... 30
4.4 Hasil Skrining Fitokimia ... 31
4.5 Hasil Analisis Ekstrak n-heksan Secara KLT ... 32
4.6 Hasil Uji Kemurnian Isolat ... 33
4.7 Hasil Karakterisasi Isolat dengan Spektrofotomerti ultraviolet dan inframerah ... 33
BAB V KESIMPULAN DAN SARAN ... 35
5.1 Kesimpulan ... 35
5.2 Saran ... 35
DAFTAR PUSTAKA ... 36
xii
DAFTAR TABEL
Tabel Halaman 4.1 Hasil pemeriksaan karakterisasi serbuk simplisia ranting
tanaman patah tulang ... 30 4.2 Hasil skrining fitokimia dari ranting patah tulang ... 31 4.3 Harga Rf ekstrak n-heksan ranting tanaman patah tulang
denganbeberapa perbandingan fase gerak ... 32 4.4 Data hasil analisis KLT ekstrak n-heksan ranting tanaman
xiii
DAFTAR LAMPIRAN
Lampiran Halaman 1. Identifikasi Tumbuhan ... 38 2. Makroskopik Tumbuhan Patah Tulang ... 39 3. Bagan Kerja Penelitian ... 40 4. Gambar Kromatogram Ekstrak n-Heksan Ranting Tanaman
Patah Tulang ... 43 5. Gambar Kromatogram Preparatif dari Ekstrak n-Heksan
RantingTanaman Patah Tulang ... 44 6. Gambar Kromatogram KLT Satu Arah dan Dua Arah ... 45 7. Gambar Alat Spektrofotometer ... 46 8. Gambar Spektrum Senyawa Triterpenoid dengan
Spektrofotometer ultraviolet ... 47 9. Gambar Spektrum Senyawa Triterpenoid dengan
[image:67.595.146.505.95.462.2]